Myrey %0.05 Burun Spreyi Kısa Ürün BilgisiSolunum Sistemi » Burunla İlgili İlaçlar » Topikal Dekonjestanlar ve Diğer Nazal İlaçlar » Kortikosteroidler » MometazonNazal 1. BEŞERİ TIBBİ ÜRÜNÜN ADIMYREY %0.05 bunın spreyi 2. KALİTATİF VE KANTİTATİF BİLEŞİM Etkin madde; Her püskürtme 50.00 mcg mometazon furoata eşdeğer 51.75 mcg mometazon fııroat monohidrat içerir. Yardımcı maddeler: Benzalkonyum klorür (% 50 çözelti) 0.40 mg/g Yardımcı maddeler için, bkz. 6.1. 3. FARMASÖTİK FORM Burun spreyi. Beyaz- beyazımsı, homojen görünümlü kollaidal süspansiyon. 4. KLİNİK ÖZELLİKLER 4.1. Terapötik endikasyonlar MYREY, erişkinler, adolesanlar ve 6-11 yaş arasındaki çocuklarda mevsimsel ve yıl boyu süren alerjik rinit semptomlarının tedavisinde endikedir. MYREY, erişkinler ve 12 yaş ve üzerindeki adolesanlarda mevsimsel alerjik rinitin profılaksisinde endikedir. Profılaktik tedaviye polen mevsiminin beklenen başlangıcından 2-4 hafta önce başlanmalıdır. MYREY, ayrıca, 18 yaş veya üzerindeki erişkinlerde nazal poliplerin, konjesyon ve koku duyusu kaybı dahil ilgili semptomlann tedavisinde kullanılır. 4.2. Pozoloji ve uygulama şekli Pozoloji: ilk kullanımda veya sprey pompası 14 gün veya daha uzun bir süre kullanılmamışsa, kullanımdan önce sprey pompasını ayarlamak için, ilaç, düzgün bir şekilde püskürdüğü görülünceye kadar, genellikle 10 kez püskürtülmelidir. Her püskürtme 50 mikrogram mometazon flıroata eşdeğer mometazon furoat monohidrat içeren yaklaşık 100 mg mometazon furoat süspansiyonu içerir. Eğer sprey pompası 14 gün veya daha uzun süreyle kullanılmamış ise, bir sonraki kullanımdan önce, 2 kez püskürtülerek, ilaç, düzgün bir şekilde püskürdüğü görülünceye kadar yeniden ayarlanmalıdır. Mevsimsel alerjik ya da yıl boyu süren rinit: Erişkinler (yaslı hastalar dahil) ve adolesanlar:Profılaksi ve tedavi için genellikle önerilen günlük doz her burun deliğine günde bir kez iki püskürtme (50 mikrogram/1 püskürtme) olmak üzere toplam 200 mikrogram'dır. Semptomlann kontrol altına alınmasından sonra idame dozu her burun deliğine bir püskürtme olmak üzere günde toplam 100 mikrogram'a düşürülebilir.Semptomlar yeterince kontrol altına alınamamışsa, günlük maksimum doz her burun deliğine dört püskürtme olmak üzere toplam 400 mikrogram'a çıkarılabilir. Semptomların kontrol altma ahnmasmdan sonra dozun düşürülmesi önerilir. 6-11 yas arasmdaki çocuklar:Önerilen günlük doz her burun deliğine günde bir kez bir püskürtme (50 mikrogram/1 püskürtme) olmak üzere toplam 100 mikrogram'dır.MYREY, mevsimsel alerjik rinitli bazı hastalarda ilk dozdan sonra 12 saat içerisinde klinik etkinlik başlangıcı göstermektedir. Tam tedavi faydası ilk 48 saat içerisinde sağlanamayabilir. Bundan dolayı hasta tam tedavi faydası sağlayabilmek için tedaviye devam etmelidir. Nazal polipozis tedavisi:Erişkinler (yaslı hastalar dahil) ve 18 yasında veva daha büyük adolesanlar:Önerilen günlük doz her burun deliğine günde iki kez iki püskürtme (50 mikrogram/1 püskürtme) olmak üzere toplam 200 mikrogram'dır. Semptomlar 5-6 hafta içinde yeterince kontrol altına alınamamışsa, günlük maksimum doz her burun deliğine günde iki kez iki püskürtme ile toplam 400 mikrogram'a çıkanlabilir. Doz, semptomların etkin kontrolünü sağlayan en düşük doza ayarlanmalıdır. Günde iki kez uygulamayla 5-6 hafta içinde semptomlarda hiçbir iyileşme görülmezse, alternatif tedaviler düşünülmelidir. Mometazon furoatın nazal polipozis tedavisi için çalışmaları 4 ay sürelidir. İlk dozu uygulamadan önce, pompayı iyice çalkalayınız ve ilaç, düzgün bir şekilde püskürdüğü görülünceye kadar 10 kez püskürtünüz. Pompa 14 gün veya daha uzun süre kullanılmamışsa, pompayı ilaç, düzgün bir şekilde püskürdüğü görülünceye kadar 2 kez püskürtünüz. Her kullanımdan önce sprey pompasını çalkalayınız. İlk kullanımdan sonra 2 ay içerisinde ya da belirlenen sayıdaki püskürtmeden sonra sprey pompasını atabilirsiniz. Uygulama sıklığı ve süresi:Uygulama şekli:MYREY, burun deliklerine püskürtülerek kullanılır.Şişeyi yavaşça çalkalayınız ve kapağını çıkannız. 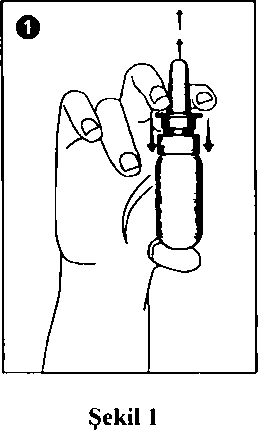 İlk kullanımda, kullanımdan önce sprey pompasını ayarlamak için, 10 kez ya da ilaç düzgün bir şekilde püskürdüğü görülünceye kadar püskürtülmelidir. Göze püskürtülmemelidir.Eğer bir haftadan uzun süre kullanılmamışsa tekrar kullanırken iki kez ya da düzgün bir şekilde püskürdüğü görülünceye kadar püskürtülerek ayarlanmalıdır. (Şekil 1)Burnunuzu yavaşça temizleyiniz. Bir burun deliğini kapayınız. Başınızı hafifçe öne eğip, sprey şişesini dik tutarak sprey pompasının ucunu diğer burun deliğine yerleştiriniz. (Şekil 2) 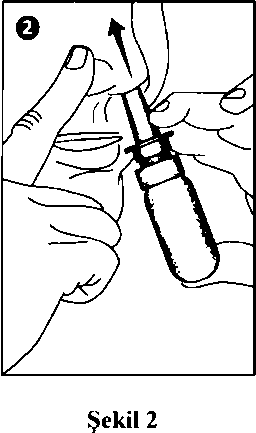 Doğrudan septuma (iki burun deliği arasındaki duvara) püskürtmeyiniz. Hafifçe burnunuzdan nefes alırken kuvvetlice bir kez püskürtünüz. (Şekil 2) Nefesinizi ağzınızdan veriniz. Gerekli durumlarda aynı işlemi aynı burun deliğine bir kez daha uygulayınız. Diğer burun deliği için de aynı uygulamayı yapınız. Püskürtme işlemi bitince spreyin ucunu temiz bir mendil ile silip kapağını kapatınız. Özel popülasyonlara ilişkin ek bilgiler:Böbrek/karaciğer yetmezliği:Böbrek ya da karaciğer yetmezliği olan hastalar için veri bulunmamaktadır.Pediyatrik popülasyon:Nazal kortikosteroidlerin sistemik etkileri, özellikle uzun sürelerle yüksek dozlarda kullanımda görülebilir. Ruhsatlı dozlarda nazal kortikosteroidler alan çocuklarda büyümede yavaşlama bildirilmiştir. Nazal kortikosteroidler ile uzun süre tedavi edilen çocuklarda boy uzunluğunun düzenli olarak takip edilmesi önerilir. Büyüme yavaşlarsa, nazal kortikosteroid dozunun mümkünse, etkin semptom kontrolü sağlayan en düşük doza indirilmesi amacıyla tedavi gözden geçirilmelidir. Aynca hastanın bir çocuk hastalıklan uzmanına şevki düşünülmelidir.Geriyatrik popülasyon:Geriyatrik popülasyon için nazal polipozis tedavisi erişkinler gibidir.4.3. KontrendikasyonlarMYREY'in bileşenlerinden herhangi birine aşın duyarlılık durumunda kullanılmamalıdır.MYREY, nazal mukoza ile ilişkili tedavi edilmemiş lokalize enfeksiyonların varlığında kullanılmamalıdır. Kortikosteroidlerin yara iyileşmesine olan inhibitör etkisinden dolayı yakın geçmişte burun ameliyatı veya travması geçirmiş olan hastalarda yara iyileşmeden önce nazal kortikosteroidler kullanılmamalıdır. 4.4. Özel kullanım uyarıları ve önlemleriMometazon füroat, aktif veya latent solunum yolu tüberküloz enfeksiyonlan, tedavi edilmemiş mantar, bakteri veya sistemik virüs enfeksiyonları veya oküler herpes simpleks enfeksiyonu olan hastalarda dikkatle kullanılmalıdır.Mometazon furoat ile 12 aylık bir tedaviden sonra nazal mukozada herhangi bir atrofı belirtisi gözlenmemiştir; aynı zamanda mometazon furoat nazal mukozayı normal histolojik fenotipine döndürme eğilimi göstermiştir. Her uzun süreli tedavide olduğu gibi birkaç ay veya daha uzun süre mometazon furoat kullanan hastalar muhtemel nazal mukoza değişikliği yönünden kontrol edilmelidir. Eğer burun veya farenkste lokalize mantar enfeksiyonu gelişirse, mometazon füroat ile tedavinin kesilmesi veya uygun tedavi uygulaması gerekebilir. Nazofarenkste inatçı iritasyon mometazon fııroat ile tedavinin kesilmesini gerektirebilir. Mometazon furoat hastaların çoğunda burun semptomları üzerinde kontrol sağlayacaktır; bununla birlikte uygun başka bir tedavinin eş zamanlı kullanımı diğer semptomlarda da (özellikle göz semptomları) ilave iyileşme sağlayabilir. Mometazon furoatın uzun süre kullanılması ile hipotalamo-hipofızeal-adrenal (HPA) aksın süpresyonuna ilişkin hiç bir delil yoktur. Bununla beraber uzun süren sistemik kortikosteroid kullanımından mometazon furoat kullanımına geçen hastalar için dikkatli bir ilgi gerekir. Bu hastalarda sistemik kortikosteroidin kesilmesi, HPA aksın fonksiyonları düzelinceye kadar bir kaç ay adrenal yetmezlik belirtileri ile sonuçlanabilir. Bu hastalar adrenal yetmezlik belirtileri gösterirlerse sistemik kortikosteroid tedavisine devam edilmeli ve diğer tedavi usulleri ve gerekli önlemler uygulanmalıdır. Sistemik kortikosteroidlerden mometazon flıroata geçişte bazı hastalarda nazal semptomlarda hafifleme görülmesine karşın sistemik kortikosteroid kesilme semptomlarından (örn. eklem ve/veya adale ağrısı, yorgunluk ve başlangıçta depresyon) şikayetçi olabilirler. Bu durumda mometazon furoat ile tedaviye devam etmeleri önerilmelidir. Böyle bir geçiş aynı zamanda aleıjik konjunktuvit veya ekzema gibi önceden var olan ve sistemik kortikosteroid tedavisi ile süprese olmuş alerjik durumların açığa çıkmasına da neden olabilir. Tek taraflı polipler, kistik fıbrozla ilişkili polipler veya burun boşluklarım tamamen bloke eden poliplerin tedavisinde mometazon furoatın güvenlilik ve etkililiği çalışılmamıştır. Görünümleri olağandışı veya düzensiz olan tek taraflı polipler, özellikle de ülserleşme veya kanama olanlar daha ileri düzeyde tetkik edilmelidir. Nazal kortikosteroidlerin sistemik etkileri, özellikle uzun sürelerle yüksek dozlarda kullanımda görülebilir. Ruhsatlı dozlarda nazal kortikosteroidler alan çocuklarda büyümede yavaşlama bildirilmiştir. Kortikosteroid kullanan potansiyel olarak immünosüprese olmuş hastalar bazı enfeksiyonlara (örn. su çiçeği, kızamık gibi) yakalanma riskine karşı uyarılmalı ve böyle bir durumla karşılaşıldığında tıbbi yardım alınmasının önemi belirtilmelidir. tntranazal kortikosteroid kullanımını takiben nazal septum perforasyonu veya intraoküler basınçta artış çok nadir olarak bildirilmiştir. Mometazon furoatın, 18 yaşından küçük çocuklarda ve adolesanlarda nazal poliplerin tedavisindeki güvenlilik ve etkinliği üzerinde çalışma yapılmamıştır. Nazal kortikosteroidler ile uzun süre tedavi edilen çocuklarda boy uzunluğunun düzenli olarak takip edilmesi önerilir. Büyüme yavaşlarsa, nazal kortikosteroid dozunun mümkünse, etkin semptom kontrolü sağlayan en düşük doza indirilmesi amacıyla tedavi gözden geçirilmelidir. Ayrıca hastanın bir çocuk hastalıkları uzmanına şevki düşünülmelidir. Tavsiye edilenden daha yüksek dozlarla tedavi klinik yönden anlamlı adrenal süpresyona yol açabilir. Önerilenden daha yüksek dozların kullanıldığına dair kanıtlar varsa, stres veya cerrahi dönemlerinde ilave sistemik kortikosteroid kullanımı düşünülmelidir. Yardımcı madde: Benzalkonyum klorür: MYREY, benzalkonyum klorür içermektedir. 1 püskürtmede 0,4 mg'a eşdeğer benzalkonyum klorür bulunur. Bu miktarın bronkospazma neden olması beklenmemektedir. 4.5. Diğer tıbbi ürünler ile etkileşimler ve diğer etkileşim şekilleriMometazon furoatın, loratadin ile birlikte klinik etkileşim çalışması yapılmıştır. Bu çalışmalarda, mometazon furoatın plazma konsantrasyonları düşük ölçüm limiti 50 pg/ml olan hassas analizlerle ölçülemez düzeydedir.4.6. Gebelik ve laktasyon Genel tavsiyeGebelik kategorisi C'dir.Çocuk doğurma potansiyeli bulunan kadmlar/Doğum kontrolü (Kontrasepsiyon)Çocuk doğurma potansiyeli bulunan kadınlarda kullanımına ilişkin yeterli veri mevcut değildir.Gebelik dönemiGebe kadınlarda yeterli ve kontrollü çalışma yapılmamıştır. Klinik olarak önerilen maksimum dozun intranazal uygulamasından sonra mometazon plazma konsantrasyonları ölçülememektedir; bu nedenle fetusun maruz kaldığı mometazonun ihmal edilebilir ve üreme toksisitesi potansiyelinin çok düşük olması beklenir.Laktasyon dönemiDiğer nazal kortikosteroid preparatlan ile olduğu gibi mometazon furoatın gebe, emziren veya gebelik riski taşıyan kadınlarda kullanımına karar verilirken anne, fetüs ve bebeğe verilebilecek olası zararlar, beklenen yararlarla karşılaştırılmalıdır. Gebeliği sırasında kortikosteroid tedavisi gören annelerin doğan bebekleri hipoadrenalizm yönünden dikkatle izlenmelidir.Üreme yeteneği/FertiliteMometazon furoatın insanlar üzerindeki üreme yeteneğine ilişkin yeterli veri mevcut değildir.4.7. Araç ve makine kullanımı üzerindeki etkilerAraç ve makine kullanımı üzerine etkisi bilinmemektedir.4.8. İstenmeyen etkilerKlinik çalışmalarda alerjik rinitli yetişkin ve adolesan hastalarda rapor edilen tedaviye bağlı istenmeyen olaylar aşağıda belirtilmiştir:Çok yaygın (> 1/10), yaygın (>1/100 ila <1/10), yaygın olmayan (>1/1000 ila <1/100), seyrek (> 1/10000 ila <1/1000), çok seyrek (< 1/10000) Solunum, göğüs bozuklukları ve mediastinal hastalıklar:Yaygın:Epistaksis, farenjit, nazal yanma, nazal iritasyon, nazal ülserasyonGenel bozukluklar ve uygulama bölgesine ilişkin bozukluklar:Yaygın:Baş ağrısıKas-iskelet bozuklukları ve bağ doku ve kemik hastalıkları:Bilinmiyor:Çocuklarda uzun süreli kullanımda büyüme hızında yavaşlamaNazal kortikosteroidler ile uzun süreli tedavi alan çocukların boy uzunluğunun düzenli takip edilmesi önerilir. Göz Hastalıkları:Bilinmiyor:Göz basıncında artışa (glokom) bağlı olarak görme bozukluklarıEpistaksis genelde hafif şiddette olup kendiliğinden geçmiştir. İnsidansı plaseboya kıyasla daha yüksek (%5) olmakla birlikte karşılaştınlan aktif kontrol nazal kortikosteroidlerle (%15'e kadar) kıyaslanabilir veya daha düşüktür. Diğer tüm etkilerin insidansı plasebo ile karşılaştırılabilir oranlardadır. Pediyatrik hastalarda, advers etki insidansı, ör. Baş ağnsı (%3), epistaksis (%6), burunda iritasyon (%2) ve hapşırma (%2) plasebo ile kıyaslanabilir düzeydedir. Mometazon furoat monohidratın intranazal uygulamasından sonra nadiren ani aşırı duyarlılık reaksiyonu (bronkospazm, dispne gibi) meydana gelebilir. Çok nadiren anaflaksi ve anjiyoödem bildirilmiştir. Çok nadir olarak tat ve koku alma bozukluğu bildirilmiştir. Nazal Polipozis:Nazal polipozis için tedavi edilen hastalarda, advers olaylann genel insidansı, plaseboyla kıyaslanabilir nitelikte olup alerjik rinitli hastalarda gözlemlenenlere benzerdir. Polipozis için yürütülen klinik çalışmalarda hastaların %1 veya daha fazlasında bildirilen tedaviye bağlı advers olaylar şunlardır;Solunum, göğüs bozuklukları ve mediastinal hastalıklar:Çok yaygın:Burun kanaması günde iki kez 200 mikrogram ile çok yaygınYaygın:Üst solunum yolu enfeksiyonu günde bir kez 200 mikrogram ile, burun kanamasıgünde bir kez 200 mcg ile Yaygın olmayan:Gastrointestinal bozukluklar:
|
İlaç BilgileriMyrey %0.05 Burun SpreyiEtken Maddesi: Mometazon furoat monohidrat Atc Kodu: R01AD09 Kullanma talimatı ve kısa ürün bilgileri
Google Reklamları
İlgili İlaçlar |
Ana Sayfa | Hakkımızda | İlaçlar | İlaç Ara | İlaç Firmaları | Gizlilik | Bize Ulaşın
Telif Hakkı 2008-2026 © İlaç Prospektüsü. Tüm Hakları Saklıdır.Uyarı: Sitemizde yayınladığımız ilaç bilgileri ile doktora danışmadan kesinlikle ilaç kullanmayınız!
Aksi halde doğabilecek sağlık sorunlarından ilacprospektusu.com sorumlu tutulamaz.