İnhafix 25/50 mcg İnhalasyon İçin Ölçülü Dozlu Aerosol Kısa Ürün BilgisiSolunum Sistemi » Solunum Sisteminde Tıkanma - Astım İlaçları » Adrenerjikler (İnhalan) » Adrenerjikli Kombinasyonlar » Salmeterol Kombinasyonları KISA URUN BILGISI1. BEŞERI TIBBI URUNUN ADIİNHAFİX 25/50 mcg inhalasyon için ölçülü dozlu aerosol2. KALITATIF VE KANTİTATIF BILEŞIM ETKIN MADDE:Salmeterol ksinafoat* 36,25 mcgFlutikazon propiyonat 50,00 mcg*: 25 mcg Salmeterol'e eşdeğer Yardımcı maddeler:Dehidrat alkol 3,693 mgYardımcı maddeler için 6.1'e bakınız.3. FARMASÖTIK FORMİnhalasyon için ölçülü dozlu aerosolAlüminyum inhaler kabı içinde basınçlı propellant gaz ile doldurulmuş süspansiyon.Alüminyum konteynere bir dozajlama valf eklidir.4. KLINIK ÖZELLIKLER4.1. Terapötik endikasyonlarAstım semptomlarının düzeltilmesi ve kontrol altına alınması amacıyla kullanılır. Astım hastalığının basamaklı tedavisinde 3. basamaktan itibaren verilir. Orta ve ağır KOAH olgularında semptomları ve atak sıklığını azaltır.4.2. Pozoloji ve uygulama şekli Pozoloji/uygulama sıklığı ve süresi:Hastalara semptomların görülmediği zamanlar da dahil olmak üzere, İNHAFİX'in optimum yarar sağlamak üzere günlük olarak kullanılması gerektiği yönünde bilgi verilmelidir.Hastalar düzenli olarak bir doktor tarafından değerlendirilmeli, aldıkları İNHAFİX dozunun optimum düzeyde kalması sağlanmalı ve doz sadece doktor önerisi ile değiştirilmelidir. Doz, belirtileri etkili olarak kontrol eden en düşük doza ayarlanmalıdır. Günde iki kez uygulanan en düşük kombinasyon dozajıyla semptomların kontrolü sağlandığında, bir sonraki adımda inhale kortikosteroidin tek başına kullanımı test edilmelidir.Alternatif olarak, uzun süre etkili beta-2 agonistlerinin kullanılması gereken hastalar, reçete eden hekimin görüşüne göre hastalık kontrolünü sağlamakta yeterli olacağı düşünülüyorsa, günde bir kez İNHAFİX alacak şekilde de titre edilebilirler. Hastada gece görülen semptom öyküsü varsa ve günde bir kez dozlam uygulanıyorsa, doz geceleri verilmeli; hastada genellikle gündüz görülen semptom öyküsü varsa, doz sabahları verilmelidir.Hastalara hastalıklarının şiddetine göre uygun flutikazon propiyonat dozu içeren İNHAFİX verilmelidir.Not: İNHAFİX 25 mikrogram/ 50 mikrogram dozu şiddetli astımı olan erişkinlerde ve çocuklarda kullanıma uygun değildir. Reçete eden hekim, astımlı hastalarda flutikazon propiyonatın mikrogram cinsinden günlük dozun yaklaşık yarısı kadar dozda diğer inhale steroidler kadar etkin olduğunun bilincinde olmalıdırlar. Örneğin, 100 mcg flutikazon propiyonat yaklaşık 200 mcg beklometazon dipropiyonata (CFC içeren) veya budesonide eşdeğerdir.Bireysel olarak bir hastada önerilen rejimin dışında dozajların gerekmesi durumunda, uygun beta-agonisti ve/veya kortikosteroid dozları reçete edilmelidir.Erişkinler ve 12 yaş ve üstündeki adolesanlar:Günde iki kez iki inhalasyon halinde 25 mikrogram salmeterol ve 50 mikrogram flutikazon propiyonat.Veya günde iki kez iki inhalasyon halinde 25 mikrogram salmeterol ve 125 mikrogram flutikazon propiyonatVeya günde iki kez iki inhalasyon halinde 25 mikrogram salmeterol ve 250 mikrogram flutikazon propiyonat.Astımın hızlı şekilde kontrol edilmesi gereken orta dereceli inatçı astımı olan erişkin veya adolesan hastalarda (hastanın günlük semptomlarına, günlük kurtarma ilacı kullanımına ve orta ila şiddetli hava yolu sınırlamasına göre tanımlanır), kısa süreli bir İNHAFİX denemesi başlangıç tedavisi olarak kabul edilebilir. Bu durumlarda, önerilen başlangıç dozu günde iki kez iki inhalasyon olarak 25 mikrogram salmeterol ve 50 mikrogram flutikazon propiyonattır. Astım kontrolü sağlandığında, tedavi tekrar gözden geçirilmeli ve hastaların tek başına inhale kortikosteroid alacak şekilde dozlarının azaltılması düşünülmelidir. Tedavide doz azaltılırken hastaların düzenli olarak incelenmesi önemlidir.Bir veya iki hastalık şiddeti kriteri eksik olduğunda, başlangıç tedavisi olarak tek başına inhale flutikazon propiyonat kullanımına kıyasla net bir yarar gösterilmemiştir. Genel olarak inhale kortikosteroidler hastaların büyük çoğunluğunda birinci basamak tedavi olmaya devam etmektedir. İNHAFİX'in hafif astımın ilk tedavisinde kullanımı amaçlanmamaktadır. İNHAFİX 25 mikrogram /50 mikrogram dozları, şiddetli astımı olan çocuklarda ve erişkinlerde kullanıma uygun değildir; şiddetli astım hastalarında herhangi bir sabit kombinasyonun kullanılmasından önce uygun inhale kortikosteroid dozunun gösterilmesi önemlidir.Hastalara inhalasyon için spreyi nasıl kullanacakları ve bakımını nasıl yapacakları konusunda bilgi verilmeli ve inhale ilacın akciğerlere optimum dağıtımını sağlamak üzere kullanım teknikleri kontrol edilmelidir. Hasta inhalasyon için spreyi kullanmada sıkıntı yaşarsa, bir hazne (spacer cihazı) kullanabilir. Spacer cihazlarının değiştirilmesi akciğerlere giden doz miktarında değişiklik meydana getirebileceğinden, hastalar aynı tip spacer cihazını kullanmaya devam etmelidirler.Bir spacer cihazı kullanılmaya başlandığında veya cihaz değiştirildiğinde daima tekrar en düşük doz titrasyonu gerçekleştirilmelidir.12 yaşın altındaki çocuklar aerosol püskürtmeyi, nefes alma ile senkronize hale getirme konusunda güçlükler yaşayabilir. Püskürtmeyi, nefes alma ile koordine etme konusunda güçlükler yaşayan veya yaşama ihtimali olan hastalarda İNHAFİX inhalasyon için sprey ile birlikte hazne (spacer cihazı) kullanımı tavsiye edilir.Uygulama şekli:İNHAFİX, sadece inhalasyon yolu ile uygulanır.İnhalasyon spreyinin doğru kullanımı doktor veya eczacı tarafından hastaya gösterilmelidir. İnhalasyon sırasında hastalar tercihen oturmalı veya ayakta durmalıdır. İnhalasyon spreyi dik konumda kullanım için tasarlanmıştır.İnhalasyon cihazı kullanma talimatı için bakınız ekli talimat.Özel popülasyonlara ilişkin ek bilgiler:Böbrek yetmezliği:Böbrek yetmezliği olan hastalarda dozun ayarlanmasına gerek yoktur.Karaciğer yetmezliği:Karaciğer yetmezliği olan hastalarda İNHAFİX kullanımına ilişkin bilgi yoktur.Pediyatrik popülasyon:4-12 yaş arası çocuklarda:Günde iki kez iki inhalasyon halinde 25 mikrogram salmeterol ve 50 mikrogram flutikazon propiyonat.Çocuklarda İNHAFİX inhalasyon için sprey ile verilen maksimum onaylı flutikazon propiyonat dozu, günde iki kez 100 mcg'dir.4 yaşından küçük çocuklarda İNHAFİX inhalasyon için sprey kullanımına ilişkin veri yoktur. Geriyatrik popülasyon:Yaşlı hastalarda dozun ayarlanmasına gerek yoktur.4.3. KontrendikasyonlarİNHAFİX, etkin madde veya yardımcı maddelerden birine karşı aşırı duyarlılığı olan hastalarda kontrendikedir.4.4. Özel kullanım uyarıları ve önlemleri- Uzun etkili beta agonist preparatlarına bağlı olarak nadiren, ciddi ve bazen ölümcül olabilen astım ile ilgili solunum problemleri meydana gelebilir.- İNHAFİX, astım hastalığının başlangıç tedavisi için önerilmez.- Uzun etkili beta agonistler astım semptom kontrolünü sağlayan en kısa süre boyunca kullanılmalı ve astım kontrolüne ulaşıldığında eğer mümkünse kullanımları durdurulmalıdır. Sonrasında hastaların kontrol edici bir tedaviyle idamesi sağlanmalıdır.- İnhale kortikosteroide ek olarak uzun etkili beta agonist kullanan pediatrik ve adölesan hastalarda, her iki ilaca uyumu garanti altına almak için, hem inhale kortikosteroid hem de uzun etkili beta agonist içeren bir kombinasyon preparatı kullanılması önerilir.- Hastalar alevlenme dönemlerinde ise ya da önemli ölçüde veya akut olarak kötüye giden astım şikayetleri varsa, uzun etkili beta agonistlerle tedaviye başlanmamalıdır.- Astım tedavisinde normalde kademeli bir program izlenmeli ve hasta yanıtı klinik olarak ve akciğer fonksiyon testleriyle izlenmelidir.- İNHAFİX hızlı ve kısa etkili bir bronkodilatörün gerektiği akut astım semptomlarının tedavisinde kullanılmamalıdır. Hastalara her zaman bir akut astım atağı durumunda semptomların hafifletilmesinde kullanılmak üzere ilaçlarını yanlarında bulundurmaları söylenmelidir.- Hastalarda bir alevlenme sırasında veya anlamlı şekilde kötüleşen veya akut şekilde şiddetlenen astım hastalıkları varsa İNHAFİX tedavisi başlatılmamalıdır.- İNHAFİX ile tedavi sırasında ciddi astım kaynaklı yan etkiler ve alevlenmeler meydana gelebilir. İNHAFİX tedavisine başlandıktan sonra astım semptomları kontrol edilmezse veya kötüleşirse hastalara tedaviye devam etmeleri, ancak doktorlarına danışmaları gerektiği söylenmelidir.- Astım semptomlarının hafifletilmesi için kısa etkili bronkodilatörlerin artan kullanımı astım kontrolünün kötüleştiğini göstermektedir ve hasta, bir hekim tarafından incelenmelidir.- Astım kontrolündeki ani ve progresif bir kötüleşme potansiyel anlamda yaşamı tehdit edicidir ve hastalar acil tıbbi yardım almalıdır. Kortikosteroid tedavisi dozunun artırılması düşünülmelidir. Hasta ayrıca mevcut İNHAFİX dozunun yeterli astım kontrolü sağlayamadığı durumlarda tıbbi açıdan incelenmelidir. Ek kortikosteroid tedavilerinin kullanımı düşünülmelidir.- Astım semptomları kontrol edildiğinde İNHAFİX dozunun kademeli şekilde azaltılması düşünülmelidir. Tedavi dozu azaltılırken hastaların düzenli şekilde incelenmesi önemlidir. İNHAFİX'in en düşük etkin dozu kullanılmalıdır. İNHAFİX ile tedavi aniden kesilmemelidir.- Tüm inhale ilaç içeren kortikosteroidlerde olduğu gibi İNHAFİX, pulmoner tüberkülozlu hastalarda dikkatli şekilde kullanılmalıdır.- Seyrek olarak İNHAFİX yüksek terapötik dozlarda kardiyak aritmi (örn, supraventriküler taşikardi, ekstrasistol ve atrial fibrillasyon) ve serum potasyumda hafif geçici bir düşmeye neden olabilir. Bu nedenle İNHAFİX şiddetli kardiyovasküler bozukluk, kalp ritim anomalileri, diabetes mellitus, tirotoksikoz, düzeltilmemiş hipokalemi veya düşük serum potasyum düzeylerine eğilimli olan hastalarda dikkatli şekilde kullanılmalıdır.- Seyrek olarak kan glukoz düzeylerinde artışlar bildirilmiş olup, diabetes mellitus öyküsü olan hastalara bu ilaç reçete edilirken bu dikkate alınmalıdır.- Diğer inhalasyon tedavilerinde olduğu gibi, dozlamdan sonra hırıltıda hızlı bir artışla paradoksikal bronkospazm meydana gelebilir. İNHAFİX derhal kesilmeli, hasta değerlendirilmeli ve gerektiğinde alternatif tedaviye başlanmalıdır.- Özellikle adrenal fonksiyonun önceki sistemik steroid tedavisi nedeniyle bozulduğunun düşünülmesi için herhangi bir gerekçe mevcutsa, hastalar İNHAFİX tedavisine geçirilirken dikkatli olunmalıdır.- Özellikle uzun süreli periyotlarda önerilenden yüksek dozlarda olmak üzere tüm inhale kortikosteroid ilaçlarla sistemik etkiler meydana gelebilir. Bu etkiler oral kortikosteroidlere kıyasla çok daha seyrek meydana gelmektedir. Olası sistemik etkiler Cushing sendromu, Cushingoid özellikleri, adrenal süpresyonu, çocuklar ve adolesanlarda gelişim geriliği, azalan kemik mineral yoğunluğu, katarakt ve glokomu içermektedir. Bu nedenle hastaların düzenli şekilde incelenmesi ve inhale kortikosteroid dozunun astımın etkinlik kontrolünün sürdürüldüğü en düşük doza indirilmesi önemlidir.- Salmeterol ve flutikazon propiyonatın sistemik emilimi büyük ölçüde akciğerlerde gerçekleşmektedir. Bir ölçülü doz inhaler ile bir spacer cihazının kullanımı akciğerlere ilaç salımını arttırabildiğinden, bunun sistemik yan etki riskinde bir artışa neden olma potansiyeli olduğu göz önünde bulundurulmalıdır.- İnhale flutikazon propiyonat tedavisinin yararları oral steroid ihtiyacını minimize edecektir, ancak oral steroidlerden bu ilaçla tedaviye geçirilen hastalarda uzun bir süre adrenal rezervde azalma riski devam edebilir. Daha önce yüksek doz acil kortikosteroid tedavisine ihtiyaç duyan hastalar da riskli olabilir. Strese neden olması muhtemel acil ve elektif durumlarda daima rezidüel yetmezlik olasılığı göz önünde bulundurulmalı ve uygun kortikosteroid tedavisi düşünülmelidir. Adrenal yetmezlik boyutu, elektif prosedürlerden önce uzman önerisi gerektirebilir. Ritonavir plazmadaki flutikazon propiyonat konsantrasyonunu ciddi şekilde artırabilir. Bu nedenle, hasta için potansiyel yararı sistemik kortikosteroid yan etkileri riskinden daha yüksek olmadığı sürece eşzamanlı kullanımdan kaçınılmalıdır. Ayrıca flutikazon propiyonat ile diğer potent CYP3A inhibitörleri birlikte kullanıldığında sistemik yan etki riski artmaktadır.- Plaseboya kıyasla salmeterol/flutikazon propiyonat kombinasyonu alan Kronik Obstrüktif Pulmoner Hastalık (COPD) bulunan hastalarda 3 yıllık bir çalışmada alt solunum yolu enfeksiyonları (özellikle pnömoni ve bronşit) daha sık bildirilmiştir. Üç yıllık COPD çalışmasında yaşlı hastalar, daha düşük vücut kitle endeksi olan (< 25 kg/m2- Büyük ölçekli bir klinik çalışmada (Salmeterol Çok Merkezli Astım Araştırma Çalışması-SMART) veriler Afro-Amerikalı hastalarda, plaseboya kıyasla salmeterol kullanımı sırasında solunum ile ilişkili ciddi olay veya ölüm riskinin daha yüksek olduğunu düşündürmüştür. Bu artışın farmakogenetiğe veya diğer faktörlere bağlı olup olmadığı bilinmemektedir. Bu nedenle siyah Afrikalı veya Afro-Karayip kökenli hastalara, İNHAFİX tedavisi sırasında astım semptomları kontrol edilmezse veya kötüleşirse tedaviye devam etmeleri gerektiği, ancak doktorlarına danışmaları gerektiği söylenmelidir.- Eşzamanlı sistemik ketokonazol kullanımı, salmeterol maruziyetini anlamlı şekilde artırmaktadır. Bu sistemik etki insidansında (örn, QTc aralığında uzama ve palpitasyonlar) bir artışa neden olabilir. Dolayısıyla, salmeterol tedavisinin yararları potansiyel anlamda artan sistemik yan etki riskinden daha fazla olmadığı sürece ketokonazol veya diğer potent CYP3A4 inhibitörleri ile eşzamanlı tedaviden kaçınılmalıdır.Pediyatrik popülasyon- İnhale kortikosteroidlerin yüksek dozlarıyla hastalarda uzun süreli tedavi adrenal süpresyon ve akut adrenal krize neden olabilir. Yüksek flutikazon dozu (tipik olarak >1000 mcg/gün) kullanan çocuklar ve <16 yaşındaki adolesanlarda özellikle riskli olabilir. Çok seyrek vakalarda ayrıca 500 ila <1000 mcg arasındaki flutikazon propiyonat dozlarıyla adrenal süpresyon ve akut adrenal kriz tanımlanmıştır. Akut adrenal krizi tetikleme potansiyeli olan durumlar travma, cerrahi, enfeksiyon veya dozdaki herhangi bir hızlı azalmayı içermektedir. Görülen semptomlar tipik olarak belirsizdir ve anoreksi, karın ağrısı, kilo kaybı, yorgunluk, baş ağrısı, bulantı, kusma, hipotansiyon, azalan bilinç düzeyi, hipoglisemi ve nöbetleri içerebilir. Stres veya elektif cerrahi periyotlarında ek sistemik kortikosteroid kullanımı düşünülmelidir.Bu tıbbi ürün az miktarda -her dozda 100 mg'dan daha az- alkol içerir.4.5. Diğer tıbbi ürünler ile etkileşimler ve diğer etkileşim şekilleriSelektif ve selektif olmayan beta blokerler, kullanımları için güçlü gerekçeler olmadığı sürece astım hastalarında kullanılmamalıdır.Diğer beta adrenerjik içeren ilaçların eşzamanlı kullanımı potansiyel aditif etkiye sahip olabilir. Flutikazon PropiyonatNormal şartlar altında, bağırsak ve karaciğerde sitokrom P450 3A4 enziminin aracılık ettiği yoğun ilk geçiş metabolizması ve yüksek sistemik klirens nedeniyle inhale dozlamdan sonra flutikazon propiyonatın düşük plazma konsantrasyonları elde edilmektedir. Bu nedenle flutikazon propiyonat aracılı klinik açıdan anlamlı ilaç etkileşimleri muhtemel değildir.Sağlıklı deneklerde intranazal flutikazon propiyonat ile yapılan bir etkileşim çalışmasında, günde iki kez ritonavir (oldukça potent bir sitokrom P450 3A4 inibitörü) 100 mg dozu flutikazon propiyonat plazma konsantrasyonlarını yüzlerce kat artırmış ve serum kortizol konsantrasyonlarının belirgin şekilde azalmasına neden olmuştur. Bu etkileşime ilişkin bilgiler inhale flutikazon propiyonat için mevcut değildir, ancak flutikazon propiyonat plazma düzeyinde belirgin bir artış beklenmektedir. Cushing sendromu ve adrenal süpresyon vakaları bildirilmiştir. Yararları, artan sistemik kortikosteroid yan etkiler riskinden daha yüksek olmadığı sürece bu kombinasyondan kaçınılmalıdır.Sağlıklı gönüllülerde yapılan küçük ölçekli bir çalışmada daha düşük potense sahip bir CYP3A inhibitörü olan ketokonazol, tek inhalasy ondan sonra flutikazon propiyonat maruziy etini %150 artırmıştır. Bu etki tek başına flutikazon propiyonata kıyasla plazma kortizol düzeyinde daha fazla düşüşe neden olmuştur. İtrakonazol gibi diğer potent CYP3A inhibitörleri ile birlikte tedavinin de, sistemik flutikazon propiyonat maruziyetini ve sistemik yan etki riskini artırması beklenmektedir. Dikkatli olunması ve bu ilaçlarla uzun süreli tedaviden mümkünse kaçınılması önerilmektedir.SalmeterolPotent CYP3A4 inhibitörleri15 sağlıklı denekte 7 gün süreyle birlikte salmeterol (inhalasyon yoluyla günde iki kez 50 mcg) ve ketokonazol (oral yolla günde bir kez 400 mg) uygulanımı, plazma salmeterol maruziyetinde anlamlı bir artışa neden olmuştur (Cmaks 14 kat ve EAA 15 kat). Bu etki tek başına salmeterol ve ketokonazol tedavisine kıyasla salmeterol tedavisinin diğer sistemik yan etki insidansında (örn, QTc aralığında uzama ve palpitasyonlar) bir artışa neden olabilir.Kan basıncı, kalp hızı, kan glukoz ve kan potasyum düzeylerinde klinik açıdan anlamlı etkiler görülmemiştir. Ketokonazol ile birlikte uygulanımı, salmeterol eliminasyon yarı ömrünü veya tekrarlı dozlamla salmeterol birikimini artırmamıştır.Ketokonazol ile eşzamanlı kullanımından, tedavinin yararları salmeterolün artan sistemik yan etkiler riskinden daha yüksek olmadığı sürece kaçınılmalıdır. Diğer potent CYP3A4 inhibitörleri ile benzer bir etkileşim riskinin olması muhtemeldir (örn, itrakonazol, telitromisin, ritonavir).Orta düzeyde CYP 3A4 inhibitörleri15 sağlıklı denekte 6 gün süreyle birlikte salmeterol (inhalasyon yoluyla günde iki kez 50 mcg) ve eritromisin (oral yolla günde bir kez 500 mg) uygulanımı, salmeterol maruziyetinde küçük ancak istatistiksel açıdan anlamlı olmayan bir artışa neden olmuştur (CmaÖzel popülasyonlara ilişkin ek bilgiler Pediyatrik popülasyon:İnhale kortikosteroid ile uzun süreli tedavi gören çocukların boyunun düzenli şekilde izlenmesi önerilmektedir.4.6. Gebelik ve laktasyon Genel tavsiyeGebelik kategorisi C.Çocuk doğurma potansiyeli bulunan kadınlar/Doğum kontrolü (Kontrasepsiyon)Tek ilaç veya kombinasyon halindeki ilaçlarla hayvanlar üzerinde yapılan üreme toksisite çalışmaları, güçlü bir beta2-adrenoreseptör agonistinin ve glukokortikosteroidin aşırı sistemik maruziyet seviyelerinde beklenen fötal etkilerini açığa çıkarmıştır.Gebelik dönemiİlaç kullanımı ancak anneye sağlaması beklenen yararı fetusa olan olası bir riskten fazla ise düşünülmelidir.Bu sınıftaki ilaçlarla ilgili geniş klinik deneyim, etkilerinin terapötik dozlarla ilişkili olduğuna dair bir kanıt ortaya koymamıştır. Ne salmeterol ksinafoatın ne de flutikazon propiyonatın genetik toksisite potansiyeline sahip olduğu gösterilmiştir.Laktasyon dönemiSalmeterol ksinafoat ve flutikazon propiyonatın gebelik ve emzirme döneminde kullanımı ile ilgili deneyimler yetersizdir. Emzirme döneminde tercihen kullanılmamalıdır.Salmeterol süte geçer. Terapötik dozlarda inhale edilen salmeterol ve flutikazon propiyonatın plazma düzeyleri çok düşüktür ve buna bağlı olarak anne sütündeki konsantrasyonların düşük olması muhtemeldir. Bu, sütünde düşük ilaç konsantrasyonları ölçülen emziren hayvanlar üzerinde yapılan çalışmalarla desteklenmiştir.Anne sütüyle beslenen yeni doğanlar/bebekler için mevcut risk göz ardı edilemez. Emzirmenin çocuk için ve tedavinin anne için faydası göz önünde bulundurularak emzirmeye veya İNHAFİX tedavisine son verilmelidir.Üreme yeteneği/FertiliteVeri bulunmamaktadır.4.7. Araç ve makine kullanımı üzerindeki etkilerAraç ve makine kullanımı üzerindeki etkilere ilişkin bir çalışma yapılmamıştır.4.8. İstenmeyen etkilerİNHAFİX salmeterol ve flutikazon propiyonat içerdiğinden, bileşiklerden her biriyle ilişkilendirilen tipte ve şiddette yan etkiler beklenebilir. İki bileşiğin eşzamanlı uygulanmasını takiben ek yan etki insidansı söz konusu değildir.Salmeterol/flutikazon propiyonat ile ilişkilendirilen yan etkiler aşağıda organ sistemi sınıfına ve frekansa göre liste halinde sunulmaktadır. Sıklıklar şu şekilde tanımlanmaktadır:Çok yaygın (>1/10), yaygın (>1/100 ila <1/10), yaygın olmayan (>1/1000 ila <1/100), seyrek (>1/10.000 ila <1/1000), çok seyrek (<1/10.000), bilinmiyor (eldeki verilerden hareketle tahmin edilemiyor).Çok yaygın, yaygın ve yaygın olmayan olaylar klinik çalışma verilerinden elde edilmiştir.Plasebo insidansı dikkate alınmamıştır. Çok seyrek olaylar pazarlama sonrası spontan verilerden elde edilmiştir.Enfeksiyonlar ve enfestasyonlarYaygın: Ağız ve boğazda kandidiyazis, pnömoni, bronşitBağışıklık sistemi hastalıklarıYaygın olmayan: Deride aşırı duyarlılık reaksiyonlarıÇok seyrek: Anjiyoödem (temelde ve orofaringeal ödem), solunum semptomları (dispne ve/veya bronkospazm), anafilaktik şok dahil, anafilaktik reaksiyonlarEndokrin hastalıklarıÇok seyrek: Cushing sendromu, Cushingoid özellikleri, adrenal süpresyonu, çocuklar ve adolesanlarda gelişim geriliği, azalan kemik mineral yoğunluğu,Metabolizma ve beslenme hastalıklarıYaygın: Hipokalemi Çok seyrek: HiperglisemiPsikiyatrik hastalıklarıÇok seyrek: Anksiyete, uyku bozuklukları ve hiperaktivite ve iritabilite (temelde çocuklarda) depresif agresif boukluklar dahil davranış değişiklikleriSinir sistemi hastalıklarıÇok yaygın: Baş ağrısı Yaygın: TremorGöz hastalıklarıÇok seyrek: Katarak, glokomKardiyak hastalıklarıYaygın: Palpitasyon Yaygın olmayan: TaşikardiÇok seyrek: Kardiyak aritmi (atrial fibrilasyon, supraventriküler taşikardi ve ekstrasistoller dahil)Solunum, göğüs bozuklukları ve mediastinal hastalıklarıÇok yaygın: NazofarenjitYaygın: Boğaz irritasyonu, ses kısıklığı/disfoni, sinüzit Çok seyrek: Paradoksikal bronkospazmDeri ve deri altı doku hastalıklarıYaygın: KontüzyonlarKas-iskelet bozukluklar, bağ doku ve kemik hastalıklarıYaygın: Kas krampları, travmatik özellikler Çok seyrek: Artralji, miyaljiSeçilen advers etkilerin tanımlanmasıBetaagonist tedavisinin tremor, çarpıntı ve baş ağrısı gibi farmakolojik yan etkileri bildirilmiştir ancak bu etkiler geçici olma ve düzenli tedavi ile azalma eğilimi gösterir.Flutikazon propiyonat içerdiği için, bazı hastalarda ses kısıklığı ve ağızda kandidiyaz (pamukçuk) görülebilir. Ürünün kullanımından sonra suyla gargara yapılarak hem ses kısıklığı hem de kandidiyaz insidansı hafifletilebilir. Semptomatik kandidiyaz, İNHAFİX kullanımına devam edilirken, topik anti-fungal ile tedavi edilebilir.Pediatrik popülasyonOlası sistemik etkiler Cushing sendromu, Cushingoid özellikler, adrenal süpresyon ve çocuklar ve ergenlerde büyüme geriliğidir. Çocuklarda, anksiyete, uyku bozuklukları ve hiperaktivite ve irritabilite de dahil olmak üzere davranış değişiklikleri görülebilir.4.9. Doz aşımı ve tedavisiİNHAFİX ile doz aşımına ilişkin klinik çalışmalardan elde edilmiş veri yoktur, ancak her iki madde ile doz aşımına yönelik veriler aşağıda sunulmaktadır:Salmeterol doz aşımının belirti ve semptomları tremor, baş ağrısı ve taşikardidir. Tercih edilen antidotlar, kardiyoselektif beta bloker maddelerdir, bu ilaçların bronkospazm öyküsü olan hastalarda dikkatli şekilde kullanılması gerekir. İNHAFİX tedavisi ilacın beta agonist bileşenindeki doz aşımı nedeniyle kesilirse, uygun replasman steroid tedavisinin sağlanması düşünülmelidir. Buna ek olarak hipokalemi meydana gelebilir ve potasyum replasmanı düşünülmelidir.Akut: Önerilenden yüksek flutikazon propiyonat dozlarının akut inhalasyonu adrenal fonksiyonunda geçici süpresyona neden olabilir. Adrenal fonksiyonu birkaç günde normale döndüğünden (plazma kortizol ölçümleri doğrulamaktadır) bu doz acil tedavi gerektirmemektedir.İnhale flutikazon propiyonat ile kronik doz aşımı adrenal süpresyon riskini doğurmaktadır.Adrenal rezervin izlenmesi gerekli olabilir. Flutikazon propiyonat ile doz aşımı vakalarında semptom kontrolü için uygun dozda İNHAFİX tedavisine yine de devam edilebilir.5. FARMAKOLOJIK ÖZELLIKLER5.1. Farmakodinamik özelliklerFarmakoterapötik grup: Adrenerjikler ve diğer antihistaminikler ATC Kodu: R03AK06Salmeterol/flutikazon propiyonat astım klinik çalışmalarıUzun süreli astımlı 3416 erişkin ve adolesanda 12 aylık bir çalışmada (Optimal AstımKontrolünün Sağlanması, OAKS) astım tedavisi hedeflerinin erişilebilir olup olmadığınınbelirlenmesi için, tek başına inhale kortikosteroidler (Flutikazon Propiyonat) ilesalmeterol/flutikazon propiyonatın etkinlik ve güvenilirliği karşılaştırılmıştır. Tedavi dozu**Toplam kontrol sağlanana veya çalışma ilacının en yüksek dozuna erişilene kadar 12 haftada bir artırılmıştır. OAKS salmeterol/flutikazon propiyonat verilen daha fazla hastada, tek başına İKS verilen hastalara kıyasla astım kontrolü sağlandığı ve bu kontrolün daha düşük kortikosteroid dozunda elde edildiğini göstermiştir.İyi kontrollü astım tek başına İKS'ye kıyasla, salmeterol/flutikazon propiyonat ile daha hızlı şekilde elde edilmiştir. İlk bireysel iyi kontrollü haftanın elde edilmesi için deneklerin %50'sindeki tedavi süresi salmeterol/flutikazon propiyonat için 16 gün ve İKS grubunda 37 gündü. Daha önce steroid tedavisi görmeyen bir hasta alt grubunda bireysel iyi kontrollü haftaya kadar geçen süre salmeterol/flutikazon propionat ile 16 gün olurken, İKS ile 23 gündü.Genel çalışma bulguları aşağıdakileri göstermiştir:12 Ayda 1Çalışma Öncesi TedaviSalmeterol/FPFPİKİKTKTKİKS yok (tek başına kısa etki süreli beta agonisti KESBA)%78%40%70%40Düşük doz İKS(< 500 mcg BDP veya eşdeğer/gün)%75%44%60%28Orta dozdipropiyanateşdeğer/gün)İKS (>500-1000mcg BDP veya%62%29%47%163 tedavi bulgular%71%41%59%28düzeyinde birleştirilmişolduğunu göstermiştir (örn, oral kandidiyazis; 16 hastaya [%8] karşı 6 [%6], ses kısıklığı; 4 hastaya [%2] karşı 2 [%2]). Salmeterol/flutikazon propiyonat dozunun ek kısa süreli (14 güne kadar) inhale kortikosteroid tedavisine ihtiyaç duyulan erişkin hastalarda iki katına çıkarılması düşünülürse, beta agonist ile ilişkili yan etkilerdeki küçük artış dikkate alınmalıdır.Salmeterol Çok Merkezli Astım Araştırma Çalışması (SMART)SMART çok merkezli, randomize, çift kör, plasebo kontrollü, paralel gruplu 28 haftalık bir çalışma olup ABD'de yapılan, hastanın normal astım tedavisinde ek olarak 13.176 hastanın salmeterol (günde iki kez 50 ^g) ve 13.179 hastanın plasebo grubuna atandığı bir çalışmaydı. >12 yaşında olan, astım tanısı konulan ve astım ilacı kullanmakta olan (ancak bir UESBA değil) hastalar çalışmaya dahil edilmiştir. Çalışma başlangıcında IKS kullanımı kaydedilmiş, ancak çalışmada buna gerek duyulmamıştır. SMART çalışmasında primer sonlanma noktası, solunum ile ilişkili ölüm ve solunum ile ilişkili yaşamı tehdit eden olayların kombine sayısıydı.SMART Çalışmasındaki Temel Bulgular: Primer Sonlanma Noktası (Endpoint)
(Koyu karakterle yazılan risk %95 düzeyinde istatistiksel olarak anlamlıdır.)SMART Çalışmasında Başlangıçta İnhale Steroidlerle İlişkili Temel Bulgular: Sekonder Sonlanma NoktalarıSekonder sonlanma olayı sayısı/hasta sayısıBağıl risk(%95 güven aralığı)SalmeterolPlaseboSolunum ile ilişkili mortaliteİnhale steroid kullanan hastalar10/61275/61382.01 (0.69, 5.86)İnhale steroid kullanmayan hastalar14/70496/70412.28 (0.88, 5.94)Kombine astım kaynaklı mortalite veya yaşamı tehdit eden deneyimİnhale steroid kullanan hastalar16/612713/61381.24 (0.60, 2.58)İnhale steroid kullanmayan hastalar21/70499/70412.39 (1.10, 5.22)Astım ile ilişkili mortaliteİnhale steroid kullanan hastalar4/61273/61381.35 (0.30, 6.04)İnhale steroid kullanmayan hastalar9/70490/7041
* (*=plasebo grubunda hiç olay bulunmadığından hesaplanamamıştır. Koyu rakamla yazılan risk %95 düzeyinde istatistiksel olarak anlamlıdır. Yukarıdaki tablodaki sekonder sonlanma noktaları tüm popülasyonda istatistiksel anlamlılığa erişmiştir). Kombine tüm nedenlere bağlı mortalite veya yaşamı tehdit edici deneyim, tüm nedenlere bağlı mortalite veya tüm nedenlere bağlı hastaneye yatma sekonder sonlanma noktaları, tüm popülasyonda istatistiksel anlamlılığa erişmemiştir.Etki mekanizması:İNHAFİX, farklı etki şekline sahip salmeterol ve flutikazon propiyonat içermektedir.İki etkin maddenin ilgili etki mekanizmaları aşağıdaki gibidir:Salmeterol:Salmeterol reseptörün sekonder bağlanma bölgesine bağlanan uzun bir yan zincire sahip selektif uzun etkili (12 saat) bir beta-2-adrenoseptör agonisttir.Salmeterol klasik kısa etkili beta-2-agonistlerin önerilen dozlarına kıyasla, en az 12 saat süren daha uzun süreli bronkodilatasyon sağlar ve bu etki en az 12 saat sürer.Flutikazon propiyonat:Önerilen dozlarda inhalasyon yoluyla verilen flutikazon propiyonat, akciğerlerde bir glukokortikoid antienflamatuvar etkiye sahiptir ve bu etki, kortikosteroidler sistemik yolla uygulandığında görülenden daha az yan etkiyle semptomlarda ve astım alevlenmelerinde azalma sağlamaktadır.5.2. Farmakokinetik özellikler Genel özelliklerSalmeterol ve flutikazon propiyonat inhalasyon yoluyla kombinasyon halinde uygulandığında her bileşenin farmakokinetiği, ilaçlar ayrı ayrı uygulandığında gözlenene benzerdi. Bu nedenle farmakokinetik açıdan her bileşik ayrı ayrı ele alınabilir.Salmeterol:Emilim:Salmeterol akciğerde lokal olarak etki eder, bu nedenle plazma düzeyleri terapötik etkinin bir belirleyicisi değildir. Terapötik dozlarda inhalasyondan sonra çok düşük plazma konsantrasyonları gösterdiği için (yaklaşık 200 pg/ml veya daha az), plazmadaki ilaç miktarının tayini teknik olarak zor olduğundan salmeterolün farmakokinetiği ile ilgili sadece sınırlı veriler bulunmaktadır. Salmeterol ksinafoatın düzenli kullanımını takiben, hidroksinaftoik asit sistemik dolaşımda tayin edilebilir ve kararlı durum konsantrasyonları yaklaşık 100 ng/ml'ye ulaşır. Bu konsantrasyonlar, toksisite çalışmalarında gözlenen kararlı durum konsantrasyonlarından 1000 kez daha düşüktür. Hava yolu tıkanıklığı olan hastalarda uzun süreli düzenli kullanımında (12 aydan fazla) herhangi bir zararlı etki görülmemiştir.Dağılım:Salmeterolün plazma proteinlerine bağlanma oranı % 96'dır.Biyotransformasyon:İn vitro bir çalışma salmeterolün sitokrom P450 (CYP3A4) tarafından büyük oranda a-hidroksisalmeterole (alifatik oksidasyon) metabolize edildiğini göstermiştir.Eliminasyon:Eliminasyon yarılanma ömrü 5.5 saattir. Salmeterol %60 dışkı ile, %25 idrar ile itrah edilir.Doğrusallık/ Doğrusal olmayan durum:İlk ruhsat tarihi: 28.06.2012 Ruhsat yenileme tarihi:10. KÜB'ÜN YENILENME TARIHI |
İlaç Bilgileriİnhafix 25/50 mcg İnhalasyon İçin Ölçülü Dozlu AerosolEtken Maddesi: Salmeterol ksinafoat/ Flutikazon propiyonat Atc Kodu: R03AK06 Kullanma talimatı ve kısa ürün bilgileri
Google Reklamları
|
||||||||||||||||||||||
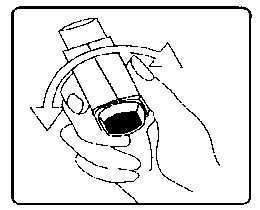
İnhalasyon spreyinin kullanım talimatı
İnhalasyon spreyinin test edilmesi:
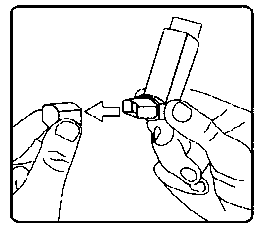
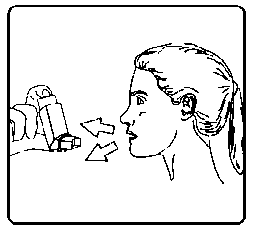
4. Ağızlığı dişlerinizin arasına koyunuz ve dudaklarınızı sıkıca kapatınız.

Ana Sayfa | Hakkımızda | İlaçlar | İlaç Ara | İlaç Firmaları | Gizlilik | Bize Ulaşın
Telif Hakkı 2008-2026 © İlaç Prospektüsü. Tüm Hakları Saklıdır.Uyarı: Sitemizde yayınladığımız ilaç bilgileri ile doktora danışmadan kesinlikle ilaç kullanmayınız!
Aksi halde doğabilecek sağlık sorunlarından ilacprospektusu.com sorumlu tutulamaz.