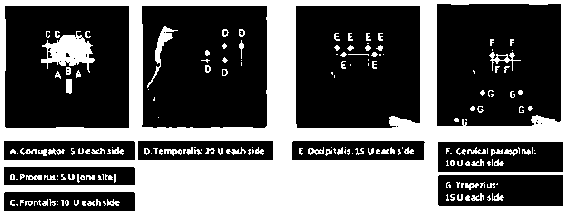
Botox Liyofilize Toz İçeren Flakon Kısa Ürün BilgisiKas İskelet Sistemi » Kas Gevşeticiler » Periferik Etkili Kas Gevşeticiler » Diğer İlaçlar » Botulinum Toksini KISA ÜRÜN BILGISI1. BEŞERI TIBBI ÜRÜNÜN ADIBOTOX® liyofilize toz içeren flakon2. KALITATIF VE KANTİTATIF BILEŞIMEtkin madde:OnabotulinumtoksinA*, 100 Allergan ünitesi/flakon.*Botulinum toksiniClostridium Botulinum'danelde edilmektedir. Botulinum toksini üniteleriürünler arasında birbirinin yerine kullanılamaz.Yardımcı maddeler:Yardımcı maddeler arasında, 0.9 mg sodyum klorür içermektedir. İlgili uyarı için 4.4 Özel kullanım uyarıları ve önlemleri bölümüne bakınız.Yardımcı maddelerin tam bir listesi için, Bölüm 6.1'e bakınız.3. FARMASÖTIK FORMEnjeksiyon solüsyonu için toz. Beyaz toz.4. KLİNIK ÖZELLIKLER4.1 Terapötik endikasyonlarBOTOX®, 2 yaş ve üzeri çocuklarda aşağıdaki tabloların tedavisi için endikedir:- Ambulatuar pediyatrik serebral palsi hastalarında, spastisiteye bağlı dinamik equinus ayak deformitesi ile ilişkili fokal spastisitedeBOTOX®, yetişkinlerde ve 12 yaş üstü çocuklarda aşağıdaki tabloların tedavisi için endikedir:- Blefarospazm, hemifasyal spazm ve ilişkili fokal distoniler- StrabismusBOTOX®, yetişkinlerde aşağıdaki tabloların tedavisi için endikedir:- Servikal distoni (spazmodik tortikolis)- Erişkin hastalarda inme sonrası gözlenen bilek ve el fokal spastisite- Kronik migreni (her ay en az 8 günü migren şeklinde olan, en az 15 gün süreyle başağrıları) olan erişkinlerde baş ağrılarının profilaksisiKronik migren yanı sıra aşırı ilaç kullanımı baş ağrısı olan hastalarda en az iki ay süre ile profilaksisiz ve profilaksili tedavi dönemine rağmen (kötü ilaç kullanımının bırakılması ve medikal tedavi) baş ağrılarının geçmediği hastalarda baş ağrılarının profilaksisi- Kronik dönemde (spinal şok sonrası dönem) subservikal omurilik hasarı veya multipl skleroza bağlı nörojenik detrusor aşırı aktivitesi olan erişkinlerde üriner inkontinansBOTOX erişkinlerde aksillada günlük yaşam aktivitelerini etkileyen ve topikal tedaviye dirençli olan, inatçı şiddetli primer hiperhidroz tedavisi için endikedir.BOTOX aynı zamanda, 65 yaşına gelmemiş erişkinlerde, kaşlar çatık iken aralarında oluşan orta ile ileri derecede derin vertikal çizgiler hastanın psikolojisini önemli oranda etkiliyorsa, bu çizgilerin görünümünde geçici iyileşme elde etmek için de endikedir.4.2 Pozoloji ve uygulama şekliPozoloji, uygulama sıklığı ve süresi/Uygulama şekli:Botulinum toksini üniteleriürünler arasında birbirinin yerine kullanılamaz. Allergan ünitesi olarak önerilen dozlar, başka botulinum toksini preparatlarından farklıdır.BOTOX® yalnızca steril sodyum klorür 9 mg/mL (%0.9) enjeksiyon solüsyonu ile sulandırılarak hazırlanmalıdır. Uygun miktardaki seyreltici (aşağıdaki seyreltim tablosuna bakınız) içeren enjektöre çekilmelidir.Nörojenik detrusor aşırı aktivitesi kaynaklı üriner inkontinans için 100 ünite flakonun seyreltme tablosu: 2 adet 100 ünite flakon BOTOX®'u her biri 6 ml %0.9 koruyucu içermeyen salin solüsyon ile seyreltip flakonları hafifçe karıştırın. 10 ml'lik iki şırınganın her birine her flakondan 4 ml çekin. Her bir flakondan geri kalan 2 ml'yi üçüncü 10 ml'lik şırıngaya çekin. Her 10 ml şırıngaya 6 ml % 0.9 koruyucu içermeyen salin solüsyon ilave edip hafifçe karıştırarak seyreltmeyi tamamlayın.Bu işlem sonucunda toplam 200 ünite seyreltilmiş BOTOX® içeren 3 adet 10 ml şırınga elde edilmiş olacaktır. Seyreltme işleminin ardından derhal ürünü kullanınız. Kullanılmamış salin solüsyonunu atınız.Diğer endikasyonlar için BOTOX® 100 Allergan ünitesi flakon büyüklüğü için seyreltim tablosu:
Bu ürün yalnızca tek kullanım içindir ve kullanılmayan çözelti atılmalıdır.Flakonların kullanımı, işlenmesi ve elden çıkarılması konusundaki talimatlar için lütfen bölüm 6.6'ya bakınız.BOTOX yalnızca uygun niteliklere sahip, tedavi ve gerekli ekipmanların kullanımı konusunda uzmanlık sahibi doktorlar tarafından uygulanmalıdır.Elektromiyografi rehberliği enjeksiyon hassasiyetini artırabilir. Enjeksiyon iğnesinin ucu tarafından kaydedilen elektrik aktivitesi, iğneyi hedef kas içerisinde pozisyonlandırırken bir rehber olarak kullanılır. Bu rehberlik strabismus tedavisi için zorunludur.BOTOX®, sulandırılarak hazırlandıktan sonra, her hastada yalnızca bir enjeksiyon uygulamaseansı için kullanılmalıdır.Bütün endikasyonlar için genel olarak geçerli optimum doz düzeyleri ve kas başına enjeksiyon bölgelerinin sayısı belirlenmemiştir. Dolayısıyla bu gibi durumlarda, doktor tarafından bireysel tedavi rejimleri planlanmalıdır. Optimum doz düzeyleri titrasyon yoluyla belirlenmeli, ancak önerilen maksimum doz aşılmamalıdır.Glabellar çizgiler için, her enjeksiyon bölgesi başına önerilen enjeksiyon hacmi 0.1 mL'dir. Aynı zamanda bölüm 6.6'daki seyreltim tablosuna da bakınız.Glabellar çizgiler içine enjekte edilirken, BOTOX®'un bir kan damarı içine enjekte edilmediğinden emin olunmalıdır.Pediyatrik serebral palsiSeyreltilmiş BOTOX® steril bir 23-26 gauge/0.60-0.45 mm iğne kullanılarak enjekte edilir. Doz bölünerek, tutulangastrocnemiuskasınınmedialvelateralbaşlarına tek enjeksiyonlar şeklinde uygulanır. Hemiplejide önerilen toplam başlangıç dozu, tutulan uzuvda 4 ünite/kg'dır. Diplejide önerilen toplam başlangıç dozu olan 6 ünite/kg, tutulan uzuvlar arasında bölünür. Toplam doz 200 üniteyi geçmemelidir.Klinik gelişim genel olarak, enjeksiyondan sonraki ilk iki hafta içerisinde ortaya çıkar. Tekrar dozları bir önceki enjeksiyonun klinik etkisi azaldığında uygulanmalı, ancak üç ayda birden daha sık olmamalıdır. Doz rejiminin, tedavi seansları arasında en az altı ay olacak şekilde uyarlanması mümkün olabilir.Blefarospazm/hemifasyal spazmSulandırılmış BOTOX® steril bir 27-30 gauge/0.40-0.30 mm iğne kullanılarak enjekte edilir. Elektromiyografi rehberliği gerekli değildir. Önerilen başlangıç dozu 1.25-2.5 ünitedir ve üst göz kapağındamedialvelateral orbicularis oculfyeve alt göz kapağındalateral orbicularis oculVyeenjekte edilir. Kaş alanındaki ek bölgeler olanlateral orbicularisve yüzün üst bölgesine de, eğer bu bölgelerdeki spazmlar görmeyi etkiliyor ise, enjeksiyon yapılabilir.Levator palpebrae superiorisyakınlarına enjeksiyon yapmaktan kaçınılması, pitozis komplikasyonunu azaltabilir. Alt göz kapağının medyaline enjeksiyon yapmaktan kaçınılması,inferior obliqueiçine difüzyonu azaltarak, diplopi komplikasyonunu azaltabilir. Aşağıdaki şekillerde enjeksiyon yapılabilecek olası bölgeler gösterilmektedir: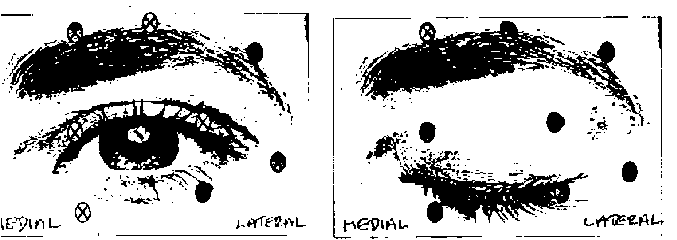
Genel olarak, enjeksiyonların etki başlangıcı üç gün içerisinde görülür ve tedavi sonrası bir ile iki haftada doruk düzeye ulaşılır. Her bir tedavi yaklaşık üç ay kalıcı olur, sonrasında prosedür ihtiyaca göre tekrarlanabilir. Eğer başlangıç tedavisine alınan yanıt yetersiz bulunmuşsa, tekrarlanan tedavi seanslarında doz iki katına kadar artırılabilir. Ancak, bölge başına 5 üniteden daha fazla enjekte edilmesinden sağlanan yararın az olduğu görülmektedir. Başlangıç dozu bir göz için 25 üniteyi aşmamalıdır. Olağan halde, üç ayda birden daha sık tedavi uygulamasından ek bir yarar elde edilmez.Blefarospazm tedavisinde toplam doz 12 haftada bir 100 üniteyi aşmamalıdır.Hemifasyal spazmı ya da VII. sinir bozuklukları olan hastalar unilateral blefarospazmdaki gibi tedavi edilmelidir; etkilenen diğer yüz kaslarına ihtiyaca göre enjeksiyon yapılmalıdır.Strabismus2.5 ünite/0.1 mL içeren bir solüsyon hazırlanır (Bkz. 6.6, Beşeri tıbbi üründen arta kalan maddelerin imhası ve diğer özel önlemler). 40 mm uzunluğunda 27-gauge bir iğne kullanılır.BOTOX® ekstra-oküler kaslar içine enjekte edilir ve elektromiyografi rehberliği gereklidir (Bkz. elektromiyografi rehberliği hakkındaki önceki bölüm).Gözün BOTOX® enjeksiyonuna hazırlanması için, enjeksiyondan birkaç dakika önce, birkaç damla lokal anestezik ve oküler dekonjestan uygulanmalıdır.Başlangıç dozları: Hafif sapmaların tedavisi için en düşük dozlar, daha belirgin sapmalarda ise daha yüksek dozlar kullanılır.Vertikal kaslar için ve 20 prizm diyoptriden düşük horizontal strabismus için: Herhangi bir kas tipinde 1.25 - 2.5 ünite (0.05 ile 0.10 mL).20 ile 50 prizm diyoptri arası horizontal strabismus için: Herhangi bir kas tipinde 2.5 ile 5 ünite (0.10 ile 0.20 mL).Bir ay ya da daha uzun süren inatçı eksternal okülomotor sinir felci için:Medial rectuskasına1.25 ile 2.5 ünite (0.05 ile 0.10 mL).Seyreltilmiş BOTOX 'un başlangıç için verilen dozları, genellikle, enjekte edilen kaslarda enjeksiyondan sonra 1 ya da 2 gün içinde paralizi oluşturur. Paralizinin yoğunluğu ilk hafta boyunca artar. Paralizi 2 ile 6 hafta sürer ve yaklaşık olarak benzer bir dönem içinde giderek azalır. Altı aydan uzun süren düzelmeler enderdir.Tedavi edilen hastaların yaklaşık yarısında, başlangıç dozundan sonra kasın yeterince paralize olmaması nedeniyle veya geniş sapmalar ya da kısıtlamalar gibi mekanik faktörlere bağlı olarak veya düzelmeyi stabilize etmek için gerekli olan binoküler motor füzyonun bulunmaması nedeniyle ilave dozlar gerekecektir.Hastaların her enjeksiyondan 7-14 gün sonra, o dozun etkisini değerlendirmek için yeniden muayene edilmesi önerilmektedir.Hedef kasta yeterli paralizi elde edilen hastalarda sonraki dozlar, başlangıçtaki doz ile kıyaslanabilir olmalıdır. Hedef kasta yeterli paralizi elde edilemeyen hastalarda sonraki dozlar, önceden uygulanan doza kıyasla iki katına kadar artırılabilir. Daha sonraki enjeksiyonlar önceki dozun etkileri kayboluncaya kadar uygulanmamalıdır; enjeksiyon yapılan kaslar ve komşu kaslarda fonksiyonun geri dönmesi, etki kaybının göstergesidir.Herhangi bir kas için önerilen maksimum tek enjeksiyon dozu 25 ünitedir. Strabismus tedavisi için enjekte edilmesi önerilen BOTOX® hacmi, kas başına 0.05 mL ile 0.15 mL'dir.Servikal distoniSulandırılmış BOTOX® uygun boyutlarda bir iğne kullanılarak enjekte edilir (genellikle 25-30 gauge/0.50-0.30 mm).Klinik araştırmalarda servikal distoni tedavisinde tipik olaraksternocleidomastoid, levator scapulae, scalene, splenius capitis, semispinalis, longissimusve/veyatrapeziuskası/kaslarına BOTOX® enjeksiyonları uygulanmıştır. Bu liste tam bir liste değildir, çünkü baş pozisyonunun kontrol edilmesinden sorumlu kaslardan herhangi biri tutulabilir ve dolayısıyla tedavi gerektirebilir.Kasın kütlesi ve hipertrofi ya da atrofi derecesi, uygun doz seçilirken dikkate alınması gereken faktörlerdir. Servikal distonide, distoninin klinik prezantasyonunda bir değişiklik olmaksızın, kas aktivasyon paternleri spontan olarak değişebilir.Kasların tek tek izole edilmesinde herhangi bir güçlük durumunda, enjeksiyonlar elektromiyografi yardımıyla yapılmalıdır. Servikal distonide güvenlilik ve etkililiğin belirlenmesi amacıyla, başlangıçta yürütülen kontrollü klinik araştırmalarda, sulandırılmış®BOTOX dozları 140 ile 280 ünite arasındaydı. Daha yeni çalışmalarda, 95 ile 360 ünite arasında değişen dozlar kullanılmıştır (ortalama yaklaşık 240 ünite). Herhangi bir ilaç tedavisinde olduğu gibi, daha önce BOTOX tedavisi görmemiş bir hastada başlangıç doz uygulaması etkili en düşük doz ile başlatılmalıdır. Herhangi bir bölgeye 50 üniteden fazlası verilmemelidir.Sternocleidomastoid'e100 üniteden fazlası verilmemelidir. Disfaji insidansını en aza indirmek için,sternocleidomastoid'ebilateral olarak enjekte edilmemelidir. İlk tedavi küründe toplam 200 üniteden fazlası enjekte edilmemeli ve daha sonraki kürlerde başlangıç yanıtına göre uyarlamalar yapılmalıdır. Herhangi bir seansta toplam 300 ünitelik doz aşılmamalıdır. Enjeksiyon bölgelerinin optimal sayısı kasın büyüklüğüne bağlıdır.Klinik gelişim genel olarak, enjeksiyondan sonraki ilk iki hafta içerisinde ortaya çıkar. Maksimum klinik yarar genel olarak, enjeksiyondan sonra yaklaşık altı haftada ortaya çıkar. On haftadan daha kısa tedavi aralıkları önerilmemektedir. Klinik araştırmalarda bildirilen yararlı etki süresi belirgin değişkenlik göstermiş (2 ile 33 hafta) ve tipik süre yaklaşık 12 hafta olmuştur.İnmeye bağlı fokal üst uzuv spastisitesiSulandırılmış BOTOX® yüzeyel kaslar için steril bir 25, 27 ya da 30 gauge iğne ve derin kaslar için daha uzun bir iğne kullanılarak enjekte edilir. Tutulan kasların lokalize edilmesinde elektromiyografi rehberliği ya da sinir stimülasyon teknikleri yararlı olabilir. Çok sayıda bölgeye enjeksiyon uygulaması, BOTOX 'un kastaki innervasyon alanlarıyla daha dengeli bir şekilde temasını sağlayabilir ve büyük kaslarda özellikle yararlıdır.Doğru dozaj ve enjeksiyon bölgelerinin sayısı; tutulan kasların büyüklük, sayı ve lokalizasyonu, spastisitenin şiddeti, lokal kas zayıflığı bulunması ve hastanın önceki tedaviye verdiği yanıt temelinde, bireye göre belirlenmelidir.Kontrollü klinik araştırmalarda aşağıdaki dozlar uygulanmıştır:Toplam DozBölge SayısıKasFlexor digitorum profundus Flexor digitorum sublimis Flexor carpi radialis Flexor carpi ulnaris Adductor pollicisFlexor pollicis longus_15 - 50 ünite; 1-2 bölge 15 - 50 ünite; 1-2 bölge 15 - 60 ünite; 1-2 bölge 10 - 50 ünite; 1-2 bölge 20 ünite; 1-2 bölge20 ünite; 1-2 bölge
a1IM enjeksiyon bölgesi = 0.1 mL = 5 ünite BOTOX bDoz bilateral olarak dağıtılır.Önerilen tekrar tedavi planı 12 haftada bir uygulamadır.Nörojenik detrusor aşırı aktivitesine bağlı üriner inkontinansHastalarda tedavi esnasında idrar yolu enfeksiyonu olmaması gerekir.Profilaktik antibiyotikler tedaviden 1-3 gün önce, tedavi günü ve tedaviden sonra 1-3 gün boyunca uygulanmalıdır.Hastaların enjeksiyon prosedüründen en az 3 gün önce antiplatelet tedavilerini bırakmaları tavsiye edilir. Antikoagülan tedavi gören hastaların tedavisi kanama riskini azaltacak şekilde adapte edilmelidir.Lokal alan uygulamalarında enjeksiyon öncesinde seyreltilmiş anesteziğin mesane içine uygulanması (sedasyonla ya da sedasyon olmadan) veya genel anestezi kullanılabilir. Eğer lokal anestezi uygulanırsa, enjeksiyon uygulamasının sonraki adımlarına geçmeden önce mesaneye drenaj yapılıp mesane steril salin ile yıkanmalıdır.Önerilen doz detrusorda 30 bölgeye yapılacak 1 ml (~6.7 ünite) enjeksiyonlar şeklinde 200 ünite BOTOX®'dur.Seyreltilmiş BOTOX® (200 ünite/30 ml) detrusor kasına esnek ya da sert sistoskop yardımı ile trigona dokunulmadan enjekte edilir. Enjeksiyonlar için gerekli görüntülemeyi sağlamak için mesaneye yeterince salin doldurulmuş olmalıdır, ancak aşırı şişme olmamasına dikkat edilmelidir.Enjeksiyonlar başlamadan önce havayı tamamen boşaltmak için enjektör yaklaşık 1 ml (iğne boyutuna bağlı olarak) doldurulmuş olmalıdır.İğne detrusora yaklaşık 2 mm sokulmalı ve her biri yaklaşık 1 ml olmak üzere yaklaşık 1cm ara ile 30 enjeksiyon (toplam hacim 30 ml) yapılmalıdır (Bkz. Şekil). En son enjeksiyon için yaklaşık 1 ml normal steril salin enjekte edilerek tam dozun verilmesi sağlanmalıdır. Enjeksiyonlar yapıldıktan sonra mesane duvarı görüntülemesi için kullanılan salin boşaltılmahdır. Enjeksiyon sonrası hasta en az 30 dakika gözetim altında tutulmalıdır.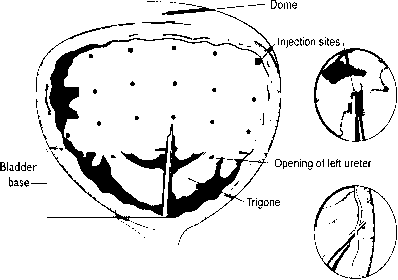
Klinik iyileşme genelde 2 hafta içinde gerçekleşir. Bir önceki enjeksiyonun klinik etkisi azalmaya başladığında (ortalama süre Faz 3 klinik çalışmalarda 200 ünite BOTOX® için 256-295 gün arasındaydı), bir önceki mesane enjeksiyonundan sonra 3 aydan erken olmamak kaydıyla, yeni enjeksiyon düşünülmeye başlanmalıdır.Primer aksiller hiperhidrozSulandırılmış BOTOX® (100 ünite/4 mL) 30 gauge iğne kullanılarak enjekte edilir. 50 ünite BOTOX®, her bir aksillanın hiperhidrotik alanı içerisinde 1-2 cm civarında aralıkları olan çok sayıda bölgeye eşit bir şekilde paylaştırılarak, intradermal olarak enjekte edilir. Hiperhidrotik alan standart boyama teknikleri, örn. Minor'un iyot-nişasta testi kullanılarak belirlenebilir. Aksilla başına 50 ünitenin dışındaki dozlar incelenmemiştir ve bu nedenle önerilmemektedir.Klinik düzelme genel olarak enjeksiyondan sonraki ilk hafta içinde ortaya çıkar. Bir önceki enjeksiyonun klinik etkisi azaldığında ve tedavi eden doktor gerekli gördüğünde BOTOX® enjeksiyonu tekrar edilebilir. İyileşmenin 4-7 ay kadar sürdüğü bildirilmiştir. Enjeksiyonlar 16 haftadan daha sık tekrarlanmamalıdır (Bkz. bölüm 5.1).Kaşlar arasındaki vertikal çizgiler (Glabellar Çizgiler)Seyreltilmiş BOTOX® (100 ünite/2.5 mL) steril bir 30 gauge iğne kullanılarak enjekte edilir. Beş enjeksiyon bölgesinin her birine 0.1 mL (4 ünite) uygulanır; toplam doz 20 ünite olacak şekilde hercorrugatorkasına 2 enjeksiyon veproceruskasına 1 enjeksiyon yapılır. Orbital rimin aşağılarına ekstravazasyonu önlemek amacıyla, enjeksiyondan önce baş parmak ya da işaret parmağı ile orbital rimin altına sıkıca bastırılmalıdır. Enjeksiyon esnasında iğne yukarıya ve medyale doğru yönlendirilmelidir. Özelliklebrow-depressor complex'" (depressor supercilii)'lihastalarda, pitozis riskini azaltmak için,levator palpebrae superioriskasının yakınına enjeksiyon yapmaktan kaçınılmalıdır.Corrugatorkasında enjeksiyonlar merkezi bölgeden yapılmalıdır. Uygulamada BOTOX®'un bir kan damarı içine enjekte edilmemesi için dikkatliolunması gerekir.
Kaşlar arasındaki vertikal çizgilerin (glabellar çizgiler) şiddetinde düzelme genel olarak tedaviden sonraki bir hafta içerisinde ortaya çıkar. Bu etkinin enjeksiyondan sonra 4 aya kadar kalıcı olduğu gösterilmiştir.Tedavi aralıkları üç ayda birden daha sık olmamalıdır. Tekrar enjeksiyonlarını izleyen tedavi başarısızlığı ya da etki azalması durumunda, alternatif tedavi yöntemleri uygulanmalıdır.Tüm endikasyonlarİlk tedavi seansından sonra tedavi başarısızlığı halinde, başka bir ifadeyle enjeksiyondan bir ay sonra, başlangıca göre anlamlı klinik düzelme olmadığında, aşağıdaki önlemler alınmalıdır:- Klinik doğrulama; bu süreçte toksinin enjekte edilen kas ya da kaslar üzerinde gösterdiği aktivitenin uzmanlar tarafından yapılacak elektromiyografik muayenesi de yer alabilir;- Başarısızlık nedenlerinin analizi, örn. enjekte edilecek kasların iyi seçilmemesi, yetersiz doz, kötü enjeksiyon tekniği, sabit kontraktür görünümü, antagonist kasların çok zayıf oluşu, toksini nötralize eden antikorların oluşması;- OnabotulinumtoksinA tedavisinin uygun olup olmadığının yeniden değerlendirilmesi;- İlk tedavi seansından sonra herhangi bir istenmeyen etki ortaya çıkmamış ise, aşağıdaki gibi bir ikinci tedavi seansı düzenleyiniz: i) Önceki tedavi başarısızlığının analizini dikkate alarak doz ayarlaması yapınız (glabellar çizgilerin tedavisinde, dozu 40 ya da 50 üniteye kadar çıkarmayı düşününüz); ii) EMG kullanınız; ve iii) İki tedavi seansı arasında üç aylık bir süre bırakınız.Tekrar enjeksiyonları izleyen tedavi başarısızlığı ya da etki azalması durumunda alternatif tedavi yöntemleri kullanılmalıdır.Özel popülasyonlara ilişkin ek bilgiler:Böbrek yetmezliği:Özel veri bulunmamaktadır.Karaciğer yetmezliği:Özel veri bulunmamaktadır.Pediyatrik popülasyon:BOTOX®'un çocuklarda (12 yaşından küçük) blefarospazm, hemifasyal spazm, strabismus, servikal distoni ve kronik migren tedavisindeki güvenlilik ve etkililiği kanıtlanmamıştır.BOTOX®'un 12 yaşından küçük çocuklarda, primer aksiller hiperhidroz tedavisindeki güvenlilik ve etkililiği araştırılmamıştır. BOTOX®'un 12 ile 17 yaş arası çocuklarda şiddetli aksiller hiperhidroz tedavisindeki güvenlilik ve etkililiği belirlenmemiştir. Halen elimizde bulunan veriler bölüm 4.8 ve 5.1'de açıklanmıştır, ama pozoloji konusunda bir öneri yapılamamaktadır.Bölüm 4.8 ve 5.1'e bakınız.®BOTOX 'un 18 yaşın altındaki bireylerde kronik migren tedavisindeki güvenliliği ve etkililiği kanıtlanmamıştır.®BOTOX 'un (18 yaş altı) çocuklarda detrusor aşırı aktivitesi kaynaklı üriner inkontinansda kullanımının etkililiği ve güvenliliği tespit edilmemiştir.BOTOX®'un 18 yaşın altındaki bireylerde kaşlar arasındaki vertikal çizgilerin (glabellar çizgiler olarak da bilinir) tedavisindeki güvenlilik ve etkililiği kanıtlanmamıştır. 18 yaşın altındaki bireylerde bu endikasyonda BOTOX® kullanımı önerilmemektedir (Bkz. bölüm 4.4).Bunların dışında, çocuklardaki endikasyonlara göre kullanım şekli için yukarıya bakınız.Geriyatrik popülasyon:Geriyatrik dozaj üzerinde yeterli çalışma yürütülmemiştir. Etkili en düşük dozun uygulanması ve enjeksiyonlar arasında klinik olarak endike en uzun sürenin bırakılması önerilmektedir. Tıbbi geçmişleri önemli olan ve aynı zamanda başka ilaçlar almakta olan yaşlı hastalar dikkatle tedavi edilmelidir.65 yaşın üzerindeki hastalarda, kaşlar arasındaki vertikal çizgilerin (glabellar çizgiler) tedavisi konusunda BOTOX® ile kısıtlı faz 3 klinik veri bulunmaktadır (Bkz. bölüm 5.1). Bu yaş grubunda daha fazla çalışma yapılıncaya kadar, 65 yaşın üzerindeki hastalarda BOTOX® önerilmemektedir.4.3 KontrendikasyonlarBOTOX® aşağıdaki durumlarda kontrendikedir:- OnabotulinumtoksinA ya da yardımcı maddelerden herhangi birine karşı aşırı duyarlığı olduğu bilinenlerde,- Planlanan enjeksiyon bölgesi ya da bölgelerinde enfeksiyon bulunması durumunda.Nörojenik detrusor aşırı aktivitesine bağlı üriner inkontinansın BOTOX® ile tedavisi aşağıdaki durumlarda kontrendikedir:- Tedavi esnasında idrar yolu enfeksiyonu olan hastalarda,- Tedavi esnasında akut idrar retansiyonu olan ve rutin olarak kateterize edilmeyen hastalarda,- Gerekli hallerde tedavi sonrası kateterizasyon kullanımı mümkün olmayan ve/veya başlatmak istemeyen hastalarda.4.4 Özel kullanım uyarıları ve önlemleri- Kullanan kişiler konu ile ilgili eğitilmelidir.- Kullanım talimatı ile verilen noktalara dikkat edilerek kullanılmalı ve ilgili formlar doldurulmalıdır.- İlacın dağıtımı ve saklanmasında talimatla belirlenmiş konulara uyulmalı ve kayıtlar tutulmalıdır.- Kullanılmış atıkların imhası ve ayrıcalıklı atımı talimatlarına uyulmalıdır.Not: Konu ile ilgili talimatlar dağıtıcıya, uygulayıcıya ve ilgili kişilere ayrıca verilmelidir.BOTOX uygulanmadan önce ilgili bölgenin anatomisi ve daha önceden yapılmış cerrahi prosedürlere bağlı anatomi değişiklikleri bilinmeli ve hassas anatomik yapılara enjeksiyon yapmaktan kaçınılmalıdır. Önerilen BOTOX® dozajı ve kullanım sıklığı aşılmamalıdır.Seyrek olarak, ciddi ve/veya ani aşırı duyarlılık reaksiyonları bildirilmiştir; anaflaksi, serum hastalığı, ürtiker, yumuşak doku ödemi ve dispne bunlar arasındadır. Bu reaksiyonların bazıları BOTOX®'un tek başına ya da diğer ürünler ile birlikte kullanılmasından sonra bildirilmiştir. Eğer böyle bir reaksiyon ortaya çıkar ise, BOTOX® enjeksiyonu kesilmeli ve derhal epinefrin (adrenalin) gibi bir ilaçla uygun tıbbi tedaviye başlanmalıdır. Uygun olmayan bir şekilde 5 mL %1 lidokain ile seyreltilmiş BOTOX® enjekte edildikten sonra hastanın yaşamını kaybettiği bir anaflaksi olgusu bildirilmiştir. Daha geniş bilgi için lütfen bölüm 4.8c'ye bakınız.Toksinin uygulama bölgesinden uzaklara yayılmasına bağlı yan etkiler bildirilmiştir (Bkz. bölüm 4.8); bunlar bazı olgularda disfaji, pnömoni ve/veya belirgin özürlülük ile ilişkilendirilen ölümlerle sonuçlanmıştır.Terapötik dozlar ile tedavi edilen hastalarda aşırı kas zayıflığı ortaya çıkabilir. Yutma güçlüğü gibi altta yatan nörolojik bozuklukları olan hastalarda bu tür yan etkilerin gelişme riski yüksektir. Botulinum toksini bu hastalarda uzman gözetimi altında ve yalnızca tedaviden edinilecek yararın risklere karşı üstün geldiği durumlarda kullanılmalıdır. Disfaji ve aspirasyon öyküsü olan hastalar son derecede dikkatli tedavi edilmelidir.Hastalara ve bakıcılara yutma, konuşma ya da solunum bozuklukları ortaya çıktığında derhal doktora başvurmaları önerilmelidir.Disfaji aynı zamanda, servikal kas yapısı dışındaki bölgelere enjeksiyon uygulamasından sonra da bildirilmiştir (daha fazla bilgi için Bkz. aşağıda 4.4 'servikal distoni' bölümü).Tekrarlı BOTOX® kullanımı sırasındaki klinik dalgalanmalar (bütün botulinum toksinlerinde olduğu gibi); farklı flakon sulandırma prosedürleri, enjeksiyon aralıkları, enjekte edilen kaslar ve kullanılan biyolojik test yöntemine göre verilen hafifçe farklı potens değerlerinin bir sonucu olabilir.OnabotulinumtoksinA'ya karşı nötralizan antikorların oluşması, toksinin biyolojik aktivitesini inaktive ederek, BOTOX® tedavisinin etkinliğini azaltabilir. Bazı çalışmalardan edinilen sonuçlar, daha sık aralıklarla ya da daha yüksek dozlarla yapılan BOTOX® enjeksiyonlarının, antikor oluşum insidansında artışa yol açabileceğini düşündürmektedir. Uygun durumlarda, antikor oluşma potansiyeli, enjeksiyonlar arasında klinik olarak endike en uzun süre bırakılarak ve etkili en düşük doz enjekte edilerek, en aza indirilebilir.Daha öncesinde sedanter yaşayan hastaların aktivitelerine başlamasını sağlayacak potansiyele sahip herhangi bir tedavide olduğu gibi, sedanter hasta, aktivitelerine aşamalı olarak başlaması konusunda uyarılmalıdır.Planlanan enjeksiyon bölgelerinde enflamasyon varlığında ya da hedef kasta aşırı zayıflık veya atrofi varsa, BOTOX® kullanılırken dikkatli olunmalıdır. Periferik motor nöropatik hastalığı (örn. amiyotrofik lateral skleroz ya da motor nöropati) olan kişilerin tedavisinde BOTOX® kullanılırken de dikkatli olunmalıdır.Myasthenia gravis ya da Eaton Lambert Sendromu gibi nöromüsküler ileti defektlerine yönelik subklinik ya da klinik verileri olan hastalarda, BOTOX® mutlaka son derecede dikkatle ve yakın gözetim altında kullanılmalıdır. Bu gibi hastalarda BOTOX® gibi ajanlara karşı duyarlık artışı11olabilir, ve bu durum aşırı kas zayıflığı ile sonuçlanabilir. Nöromüsküler bozuklukları olan hastalarda, tipik BOTOX® dozları ile şiddetli disfaji ve solunum sıkıntısı gibi klinik olarak anlamlı sistemik etki riski artabilir.Herhangi bir enjeksiyonda olduğu gibi, prosedüre bağlı yaralanma olabilir. Enjeksiyon sonucunda lokalize enfeksiyon, ağrı, enflamasyon, parestezi, hipoestezi, hassasiyet, şişme, eritem ve/veya kanama/morarma ortaya çıkabilir. İğneye bağlı ağrı ve/veya anksiyete sonucu, bayılma, hipotansiyon vb. gibi vazovagal yanıtlar görülebilir. Hassas anatomik yapılara yakın enjeksiyonlarda dikkatli olunmalıdır.Pediyatrik serebral palsiye bağlı fokal spastisite ve erişkin hastalarda inme sonrası el ve bilekspastisitesiBOTOX® fokal spastisite tedavisinde yalnızca, olağan standart bakım rejimleriyle birlikte incelenmiştir ve bu tedavi modalitelerinin yerine kullanılması düşünülmemiştir. Sabit kontraktür bulunan bir eklemde BOTOX®'un hareket aralığını düzeltmede etkili olması beklenmez.Başlıca serebral palsi olmak üzere, komorbiditeleri olan pediyatrik hastalarda, toksinin uzak bölgelere yayılma olasılığı, pazarlama sonrası raporlarda çok seyrek olarak bildirilmiştir. Genel olarak bu olgularda kullanılan doz, önerilen dozun üstündeydi (Bkz. bölüm 4.2).Şiddetli serebral palsisi olan çocuklarda botulinum toksiniyle tedaviden sonra, bazıları aspirasyon pnömonisiyle ilişkilendirilen, seyrek spontan ölüm raporları bulunmaktadır. Önemli nörolojik özürlülük hali, disfajisi ya da yakın geçmişinde aspirasyon pnömonisi veya akciğer hastalığı olan pediyatrik hastaları tedavi ederken dikkatli olunmalıdır.BlefarospazmÖzellikle VII. sinir bozuklukları olan hastalarda,orbiculariskası içine botulinum toksini enjeksiyonundan sonra göz kırpma hareketleri azalabilir ve bu durum korneal maruziyet, ısrarcı epitel defekti ve korneada ülserasyon ile sonuçlanabilir. Önceden opere edilmiş gözlerde dikkatli bir kornea hassasiyeti incelemesi yapılmalı, ektropiondan kaçınmak için alt göz kapağı alanına enjeksiyondan sakınılmalı ve herhangi bir epitel defekti yoğun bir şekilde tedavi edilmelidir. Bu süreç koruyucu damlalar, merhemler, terapötik yumuşak kontakt lensler kullanılmasını ya da gözün pet ya da başka yöntemlerle kapatılmasını gerektirebilir.Yumuşak göz kapağı dokusunda kolayca ekimoz oluşabilir. Bu durum, enjeksiyondan hemen sonra, enjeksiyon bölgesine hafif bir baskı uygulanarak en aza indirilebilir.Botulinum toksininin antikolinerjik aktivitesinden dolayı, anatomik olarak dar açısı olan hastalar dahil, dar açılı glokom riski taşıyan hastalar tedavi edilirken dikkatli olunmalıdır.StrabismusBOTOX® kronik paralitik strabismusda, karşıt kasın kalıcı olarak kasılmasını (antagonist kontraktür) cerrahi onarım ile birlikte azaltmak dışında etkisizdir. BOTOX®'un 50 prizm diyoptriden büyük sapmalarda, restriktif strabismusta,lateral rectuszayıflığı ile birlikte olan Duane sendromunda ve önceki bir cerrahi girişimde karşıt kasın fazla geri çekilmesiyle oluşan sekonder strabismusta etkinliği kuşkuludur. Etkinliği arttırmak için, zaman içinde tekrarlı enjeksiyonlara gerek duyulabilir.Strabismus tedavisi için BOTOX® uygulaması sırasında orbitada iğne penetrasyonuna bağlı olarak, retinal dolaşımı tehlikeye atmaya yetecek ölçüde retrobulber hemoraji oluşmuştur. Orbitayı incelemek ve dekomprese etmek için uygun enstrümanların hazır bulundurulması önerilmektedir. İğne ile oküler (glob) penetrasyonları da görülmüştür. Bu durumun tanısı için bir oftalmoskop hazır bulundurulmalıdır.Bir ya da daha çok ekstraoküler kasta indüklenen paralizi, uzaysal dezoriyentasyon, çift görme, ya da hareket takip bozukluğuna (past-pointing) neden olabilir. Tutulan gözün kapatılması bu semptomları hafifletebilir.Servikal distoniServikal distoni hastaları çok hafif, ancak şiddetli de olabilen bir disfaji geçirme olasılığı hakkında bilgilendirilmelidir. Disfaji enjeksiyondan sonra iki ile üç hafta sürebilir, ancak enjeksiyondan sonra beş aya kadar sürdüğü de bildirilmiştir. Disfaji ile birlikte aspirasyon, dispne olasılığı vardır ve bazen tüple beslenme ihtiyacı oluşabilir. Ender olgularda disfajiyi izleyen aspirasyon pnömonisi ve ölüm bildirilmiştir.Sternocleidomastoidkasına enjekte edilen dozun 100 ünite altında sınırlandırılması, disfaji oluşumunu azaltabilir. Boyun kas kütlesi daha küçük olan ya dasternocleidomastoidkasa bilateral enjeksiyon yapılan hastalarda, disfaji riskinin daha fazla olduğu bildirilmiştir. Disfaji, toksinin özofagus kas yapısına yayılmasına bağlı olabilir.Levator scapulaeiçine yapılan enjeksiyonlar, üst solunum yolu enfeksiyonu ve disfaji riskinde artış ile bağlantılı olabilir.
|
Hafta 24'te başlangıca göre ortalama değişim |
BOTOX® |
Plasebo |
|
|
|
N=688 |
N=696 |
P-değeri |
Baş ağrısı günlerinin sıklığı |
-8.4 |
-6.6 |
p <0.001 |
Orta derecede/şiddetli baş ağrısı günlerinin sıklığı |
-7.7 |
-5.8 |
p <0.001 |
Migren/muhtemel migren günlerinin sıklığı |
-8.2 |
-6.2 |
p <0.001 |
Baş ağrısı günlerinde %50 azalma olan hasta %'si |
47% |
35% |
p <0.001 |
Baş ağrısı günlerinde toplam kümülatif baş ağrısı saati |
120 |
80 |
p <0.001 |
Baş ağrısı episodlarının sıklığı |
-5.2 |
-4.9 |
p = 0.009 |
Total HIT-6* skorları |
-4.8 |
-2.4 |
p <0.001 |
Baş Ağrısı Etki Testi
Nörojenik detrusor aşırı aktivitesine bağlı üriner inkontinans
İki çift kör, plasebo kontrollü, randomize, çok merkezli Faz 3 klinik çalışma, nörojenik detrusor aşırı aktivitesine bağlı üriner inkontinansı olan, spontane boşaltım yapabilen ya da kateterize edilmiş hastaların katılımıyla gerçekleştirilmiştir. En az bir antikolinerjik ajanla hastalığı yeterince tedavi edilememiş toplam 691 omurilik hasarı ya da multipl skleroz hastası çalışmaya katılmıştır. Bu hastlar 200 ünite BOTOX® (n=227), 300 ünite BOTOX® (n=223), ya da plasebo (n=241) almak üzere randomize edilmişlerdir.
Hasta tarafından bildirilen inkontinansa bağlı yaşam kalitesi skorları İnkontinans Yaşam Kalitesi Anketi (I-QOL) (sınırlayan davranışlardan uzak durma, psikososyal etki ve sosyal mahcubiyeti de içerir) ile ölçülmüş ve plasebo ile karşılaştırıldığında anlamlı iyileşmeler olduğu görülmüştür. Bunların dışında BOTOX 300 ünitenin 200 üniteye karşı bir ilave üstünlüğü görülmemiştir ve 200 ünitede daha iyi bir güvenlik profili gözlemlenmiştir.
Merkezi çalışmaların toplu sonuçları aşağıda sunulmuştur:
Havuzlanmış Pivotal çalışmalarda primer ve sekonder son noktalar, başlangıç ve
|
|
BOTOX® 200 ünite(N=227) |
Plasebo(N=241) |
P-değer |
Haftalık Üriner inkontinans Sıklığı* |
|
|
|
Ortalama başlangıç |
32.4 |
31.5 |
|
2. Haftada Ortalama Değişim |
-17.7 |
-9.0 |
p<0.001 |
6. Haftada Ortalama Değişim |
-21.3 |
-10.5 |
p<0.001 |
12. Haftada Ortalama Değişim |
-20.6 |
-9.9 |
p<0.001 |
Maksimum Sistometrik Kapasite (ml) |
|
|
|
Ortalama başlangıç |
250.2 |
253.5 |
|
6. Haftada Ortalama Değişimb |
+153.6 |
+11.9 |
p<0.001 |
ilk istem Dışı Detrusor Kasılmasındaki Maksimum Detrusor Basıncı (cmHaG) |
|
|
|
Ortalama başlangıç |
51.5 |
47.3 |
|
6. Haftada Ortalama Değişimb |
-32.4 |
+1.1 |
p<0.001 |
Toplam inkontinans Yaşam Kalitesi Skorucd |
|
|
|
Ortalama başlangıç |
35.37 |
35.32 |
|
6. Haftada Ortalama Değişimb |
+25.89 |
+11. 15 |
p<0.001 |
12. Haftada Ortalama Değişim |
+28.89 |
+8.86 |
p<0.001 |
*Kuru hastaların (inkontinansı olmayan hastalar) yüzdesi 6. hafta sonuna kadar BOTOX® 200 ünite alan hastalarda %37, plasebo gurubunda ise %9 olmuştur.
İnkontinans epizotlarında başlangıçtan en az %75 azalmaya ulaşabilenlerin yüzdesi de sırasıyla %63 ve %24 olmuştur. Başlangıçtan en az %50 azalma sağlayabilenlerin yüzdesi sırasıyla %76 ve %39'dur.
a Primer son nokta b Sekonder son nokta
c I-QOL toplam skor aralığı 0'dan (maksimum sorun) 100'e kadardır (hiç sorun yok).
d Merkez çalışmalarda , I-QOL toplam skoru için önceden belirlenmiş minimal öneme sahip değişiklik (MID) nörojenik detrusor aşırı aktivitesi olan hastalarca bildirilen tahmini skor olan 4-11 puan baz alınarak 8 puan olarak tespit edilmiştir.
Hastanın tekrar kullanım isteği baz alındığında iki merkez çalışmada ortalama cevap süresi, 200 ünite grubunda 256-295 gün (36-42 hafta) olurken plasebo grubunda bu süre 92 gündür (13 hafta).
Her etkinlik son noktası için hastalar tekrar tedavilere tutarlı yanıtlar almışlardır.
Merkez çalışmalarda nörojenik detrüsor aşırı aktivitesi olan ve numuneleri analiz edilmiş 475 hastadan hiç birinde nötralize eden antikora rastlanmamıştır.
Primer aksiller hiperhidroz
Israrlı bilateral primer aksiller hiperhidroz ile başvuran hastalarda çift-kör, çok-merkezli bir klinik çalışma yürütülmüştür. Üç yüz yirmi hasta, 50 ünite BOTOX® (N=242) ya da plasebo (N=78) almak üzere randomize edildi. Tedaviye yanıt verenler, aksiller terlemede başlangıca göre en az %50 azalma gösteren olgular olarak tanımlandı. Enjeksiyon sonrası 4. haftadaki primer sonlanım noktasında, BOTOX® grubunda yanıt oranı %93.8 iken, plasebo grubunda %35.9 oldu (p< 0.001). BOTOX® ile tedavi edilen hastalar arasında yanıt verenlerin insidansı, 16 haftaya kadar, bütün tedavi sonrası zaman noktalarında, plasebo tedavisindeki hastalardakinden anlamlı düzeyde daha yüksek olmaya devam etti (p<0.001).
Açık tasarımlı bir izleme çalışmasına, 3 seansa kadar BOTOX® tedavisi uygulanan 207 elverişli hasta kaydedildi. Bütünüyle, 174 hasta kombine edilmiş 2 çalışmanın (4 ay çift-kör ve 12 ay açık tasarımlı devam) 16 aylık toplam süresini tamamladı. On altıncı haftada ilk (n=287), ikinci (n=123) ve üçüncü (n=30) tedavilerden sonra klinik yanıt insidansı, sırasıyla %85.0, %86.2 ve %80 oldu. Kombine tek-doz ve açık tasarımlı devam araştırması temelinde ortalama etki süresi, ilk tedaviyi izleyerek 7.5 aydı, ancak hastaların %27.5'i için etki süresi 1 yıl ya da daha uzun oldu.
12 ile 18 yaş arasındaki çocuklarda primer aksiller hiperhidroz tedavisi için BOTOX® kullanımına yönelik klinik araştırma deneyimi sınırlıdır. BOTOX®'un bu gruptaki etkililiği ve güvenliliği kesin bir şekilde belirlenmemiştir.
Kaşlar arasındaki vertikal çizgiler (Glabellar Çizgiler)
Kaşlar maksimum çatıklık durumunda iken aralarında orta derece ile şiddetli vertikal çizgiler (glabellar çizgiler) bulunan 537 hasta klinik çalışmalarda yer almıştır.
BOTOX® enjeksiyonları, glabellar çizgilerin şiddetini 4 aya kadar anlamlı derecede azalttı. Ölçümler, araştırıcının maksimum çatıklık durumunda glabellar çizgi şiddeti değerlendirmesini ve olgunun kaşları arasındaki vertikal çizgilerin görünümündeki değişikliğe yönelik global değerlendirmesinden oluşmaktaydı. Otuz gün enjeksiyondan sonra, BOTOX® tedavisindeki hastaların %80'i (325/405) araştırıcılar tarafından tedaviye yanıt veren olarak kabul edildi (maksimum çatıklıkta hiç yok ya da hafif şiddetli); plasebo tedavisindeki hastalarda ise bu oran %3 (4/132) oldu. Aynı zaman noktasında, BOTOX® tedavisindeki hastaların %89'u (362/405), orta derecede ya da daha iyi bir düzelme elde ettiklerini düşünürken, bu oran plasebo tedavisindeki hastalarda %7 (9/132) idi.
BOTOX® enjeksiyonları aynı zamanda, glabellar çizgilerin istirahat halindeki şiddetini de anlamlı ölçüde azalttı.
BOTOX® ile 65 yaş üzerindeki hastalarda Faz 3 klinik veriler kısıtlıdır. Olguların yalnızca %6.0'ı (32/537) 65 yaş üzerindeydi ve bu popülasyonda elde edilen etkililik sonuçları düşüktü.
5.2 Farmakokinetik özellikler
Genel özellikler
Bu ürünün doğası nedeniyle, etkin madde ile klasik emilim, dağılım, biyotransformasyon ve itrah çalışmaları insanlarda yapılmamıştır.
Emilim
®
Güncel analitik teknoloji ile BOTOX 'un tavsiye edilen dozlarda intramüsküler enjeksiyonundan sonra periferal kanda belirlenmesi mümkün değildir.
Dağılım
Sıçanlardaki dağılım çalışmalarında, 125I-botulinum nörotoksin A kompleksiningastrocnemiuskasına enjeksiyonundan sonra müsküler difüzyonunun yavaş olduğu ve bunu hızlı bir sistemik metabolizma ve idrarla atılımının izlediği gösterilmiştir.
Biyotransformasyon
Enjeksiyon yerinde, radyoaktivitenin büyük protein moleküllerine bağlı olduğu, plazmada ise küçük moleküllere bağlı olduğu bulunmuştur; bu durum, substratın hızlı bir sistemik metabolizmaya uğradığını göstermektedir.
Toksin muhtemelen proteazlar tarafından metabolize edilmektedir ve moleküler komponentler normal metabolik yollardan tekrar döngüye girmektedir.
İtrah
Kastaki radyoaktif işaretli madde miktarı, yaklaşık 10 saatlik bir yarılanma ömrü göstermiştir. Doz uygulamasından sonraki 24 saat içinde, radyoaktivitenin %60'ı idrarla atılmıştır.
Hastalardaki karakteristik özellikler
BOTOX®'un terapötik dozlarda sistemik dağılımının az olduğuna inanılmaktadır. Tek lif elektromiyografi tekniğinin kullanıldığı klinik çalışmalarda, enjeksiyon bölgesinden uzaktaki kaslarda elektrofizyolojik nöromüsküler aktivitenin arttığı ve buna herhangi bir klinik belirti ya da bulgunun eşlik etmediği gösterilmiştir.
5.3 Klinik öncesi güvenlilik verileri
Üreme çalışmaları
Hamile fare, sıçan ve tavşanlara organogenez sırasında intramüsküler BOTOX® enjeksiyonları uygulandığında, gelişimsel Maksimum Yan Etkisiz Doz (MYED) düzeyi, sırasıyla 4, 1 ve 0.125 ünite/kg idi. Daha yüksek dozlar, fetal vücut ağırlığında azalma ve/veya kemikleşmede gecikme ile ilişkiliydi ve tavşanlarda düşük olayları kaydedildi.
Diğer çalışmalar
Üreme toksikolojisine ek olarak, BOTOX® ile aşağıdaki klinik öncesi güvenlilik çalışmaları yapılmıştır: Akut toksisite, tekrarlı enjeksiyon toksisitesi, lokal tolerans, mutajenisite, antijenisite, insan kanı uyumluluğu. Bu çalışmalarda, insanlar için klinikle ilgili doz seviyelerinde özel bir zarar bulunmamıştır. İnsanlarda tek tedavi seansı için önerilen maksimum doz 300 ünitedir (50 kg'lık bir kişide 6 ünite/kg'a karşılık gelir). Jüvenil maymunlar için yayınlanan intramüsküler LD50, 39 ünite/kg'dır.
Farelerde detrusor içi tek enjeksiyonluk <50 ünite/kg BOTOX® uygulamasında sistemik toksisite gözlenmemiştir. Yanlışlıkla yapılan bir enjeksiyonu simüle etmek için tek doz BOTOX® (~7 ünite/kg) maymunların prostetik üretra ve proksima rektuma, seminal vezikül ve üriner mesane duvarına ya da rahime (~3 ünite/kg) uygulanmış ve istenmeyen bir klinik etki görülmemiştir. 9 ay süren detrusor içi tekrar dozlar (4 enjeksiyon) üzerine yapılan bir çalışmada 24 ünite/kg'da pitozis ve >24 ünite/kg dozlarda mortalite gözlenmiştir. 24 ünite/kg ve daha fazlası doz alan hayvanlarda iskelet kasında miyofibril dejenerasyonu/rejenerasyonu gözlenmiştir. Bu miyopatik değişimler sistemik maruziyetin ikincil etkileri olarak kabul edilmiştir. Ayrıca 12 ünite/kg doz alan bir hayvanda miyofibril dejenerasyonu görülmüştür. Bu hayvandaki lezyon minimal şiddetteydi ve herhangi bir klinik belirtiye bağlantılı kabul edilmemiştir. BOTOX® tedavisine bağlı olup olmadığı kesin olarak belirlenememiştir. 12 ünite/kg dozu nörojenik detrusor aşırı aktivitesine bağlı üriner inkontinans için önerilen klinik doz olan 200 ünitenin (50kg luk bir kişi baz alınmıştır) 3 katı daha fazla maruziyete denk gelmektedir.
6. FARMASOTIK ÖZELLİKLER
6.1 Yardımcı maddelerin listesi
İnsan albumini Sodyum klorür
6.2 Geçimsizlikler
Geçimlilik çalışmaları bulunmadığından, bu tıbbi ürün diğer tıbbi ürünler ile karıştırılmamalıdır.
6.3 Raf ömrü
Raf ömrü 36 aydır.
Mikrobiyoloji ve potens çalışmalarında, ürünün sulandırılarak hazırlandıktan sonra 2 - 8°C'de 5 güne kadar saklanabileceği gösterilmiştir.
Kullanım sırası saklama süreleri ve kullanım öncesi koşullar, kullanıcının sorumluluğundadır ve normal olarak, 2°C - 8°C'de 24 saatten daha uzun olmamalıdır. Sulandırılarak hazırlandıktan sonra, stabilitesinin 2°C - 8°C'de 24 saat korunduğu gösterilmiştir.
6.4 Saklamaya yönelik özel tedbirler
Buzdolabında (2°C - 8°C) veya dondurucuda (-5°C veya daha altında) saklanmalıdır. Sulandırılarak hazırlanmış tıbbi ürünün saklama koşulları için Bkz. bölüm 6.3.
6.5 Ambalajın niteliği ve içeriği
Kauçuk kapaklı ve aluminyum contalı, 10 ml kapasiteli renksiz tip 1 cam flakon.
6.6 Beşeri tıbbi üründen arta kalan maddelerin imhası ve diğer özel önlemler
Herhangi bir dökülmeye karşı önlem olarak, flakonun sulandırılması ve enjektörün hazırlanması, plastik astarlı bir kağıt havlu üzerinde yapılmalıdır. BOTOX® yalnızca steril sodyum klorür 9 mg/mL (%0.9) enjeksiyon solüsyonu ile sulandırılmalıdır. Enjektöre uygun miktarda (aşağıdaki sulandırma tablosuna bakınız) seyreltici çekilmelidir.
BOTOX® flakon 100 Allergan ünitesi için seyreltim tablosu:
|
|
100 ünite flakon |
Oluşan doz (ünite/0.1 mL) |
100 ünite flakona eklenen seyreltici miktarı (sodyum klorür 9 mg/mL (%0.9) enjeksiyon solüsyonu) |
20 ünite |
0.5 mL |
10 ünite |
1 mL |
5 ünite |
2 mL |
4 ünite |
2.5 mL |
2.5 ünite |
4 mL |
1.25 ünite 8 mL
Kauçuk kapağın orta kısmı alkol ile silinmelidir.
Eğer bir enjeksiyon seansında farklı doz büyüklüklerinde BOTOX® flakonları kullanılıyor ise, 0.1 mL başına istenilen özel ünite sayısının elde edilmesi için, doğru miktarda seyreltici kullanılmasına dikkat edilmelidir. Seyreltici miktarı BOTOX® 50 Allergan ünitesi ve BOTOX® 100 Allergan ünitesi arasında değişmektedir. Her enjektör içerdiği miktarı belirtecek şekilde etiketlenmelidir.
BOTOX® kabarcıklanma ya da benzeri bir kuvvetli çalkalama ile denatüre olduğundan, seyreltici flakon içine yavaşça enjekte edilmelidir. Eğer vakum seyrelticiyi flakon içine çekmiyor ise, flakon atılmalıdır. Sulandırılarak hazırlanmış BOTOX® berrak, renksiz ile hafif sarı renkte, taneciksiz bir çözeltidir. Seyreltilmiş çözelti kullanmadan önce, berraklık ve tanecik içermemesi yönleriyle, görsel olarak incelenmelidir. BOTOX® flakonda seyreltildiğinde, kullanım öncesinde 24 saate kadar buzdolabında (2-8°C) saklanabilir. Sulandırarak hazırlama işleminin tarih ve saati, etiket üzerindeki boşluğa kaydedilmelidir. BOTOX®, üriner inkontinans için enjektörde sulandırmayı takiben hemen kullanılmalıdr. Bu ürün yalnızca tek kullanım içindir ve kullanılmayan çözelti atılmalıdır.
®
Glabellar çizgilerin tedavisinde BOTOX 'un tek bir seansta, yalnızca tek bir hastanın tedavisiiçin kullanılması zorunludur.
BOTOX® için flakon, şırınga ve materyallerin güvenli bir şekilde bertaraf edilmesi içinprosedür:
Güvenlilik açısından, kullanılmayan flakonlar atılmadan önce az miktarda su ile sulandırılmalı ve daha sonra otoklavlanmalıdır. Kullanılmış flakonlar, enjektörler ve dökülmüş solüsyon vb.
®
otoklavlanmalı, ya da kalan BOTOX , 5 dakika süreyle dilüe hipoklorit solüsyonu (%0.5) kullanılarak inaktive edilmelidir.
Botulinum toksini işlenirken herhangi bir kaza durumunda öneriler:
Ürün işlenirken bir kaza oluşması durumunda, gerek vakumla kurutulmuş ürün halinde gerekse sulandırılmış halde iken, derhal aşağıda açıklanan uygun önlemler alınmalıdır.
Toksin ısıya ve belirli kimyasal ajanlara karşı çok duyarlıdır.
Herhangi bir döküntü silinmelidir. Vakumla kurutulmuş ürün için sodyum hipoklorit (Javel solüsyonu) ile ıslatılmış emici bir materyal, sulandırılarak hazırlanmış ürün için kuru bir emici materyal kullanılır.
Kontamine olmuş yüzeyler sodyum hipoklorit (Javel solüsyonu) ile ıslatılmış emici bir materyal ile temizlenmeli ve daha sonra kurutulmalıdır.
Flakon kırılırsa, cildin yaralanmasından kaçınılarak, cam parçaları dikkatle toplanmalı ve ürün yukarıda belirtildiği şekilde silinmelidir.
Eğer cilde sıçrarsa, önce sodyum hipoklorit solüsyonuyla ve daha sonra bol su ile iyice yıkayınız.
Eğer göze sıçrarsa, gözleri bol su ile ya da bir oftalmik göz yıkama solüsyonu ile iyice yıkayınız. Eğer enjeksiyonları yapan kişi kendini yaralarsa (kesme, batma), yukarıda belirtilenleri
27
uygulayınız ve enjekte edilen doza göre uygun tıbbi adımları atınız.
Bu kullanım, işleme ve elden çıkarma talimatlarına titizlikle uyulmalıdır.
Kullanılmamış olan ürün ya da atık materyaller, Tıbbi Atıkların Kontrolü ve Ambalaj ve Ambalaj Atıklarının Kontrolü yönetmeliklerine uygun olarak imha edilmelidir.
7. RUHSAT SAHİBİ
Allergan İlaçları Ticaret A.Ş.
Maslak Mah. Eski Büyükdere Cad.
İz Plaza Giz Kat: 12 Maslak-Şişili, 34398 İstanbul
Tel: (0212) 365 50 00
Faks: (0212) 290 72 11
8. RUHSAT NUMARASI
130/20
9. İLK RUHSAT TARİHİ/RUHSAT YENİLEME TARİHİ
İlk ruhsat tarihi: 06.10.2010 Ruhsat yenileme tarihi:
10. KÜB 'ÜN YENİLENME TARİHİ
Ağustos 2012
1Uygulamaya bağlı istenmeyen etkiler
İlaç Bilgileri
Botox Liyofilize Toz İçeren Flakon
Etken Maddesi: OnabotulinumtoksinA
Atc Kodu: M03AX01
Kullanma talimatı ve kısa ürün bilgileri
Google Reklamları
İlgili İlaçlar
Ana Sayfa | Hakkımızda | İlaçlar | İlaç Ara | İlaç Firmaları | Gizlilik | Bize Ulaşın
Telif Hakkı 2008-2026 © İlaç Prospektüsü. Tüm Hakları Saklıdır.Uyarı: Sitemizde yayınladığımız ilaç bilgileri ile doktora danışmadan kesinlikle ilaç kullanmayınız!
Aksi halde doğabilecek sağlık sorunlarından ilacprospektusu.com sorumlu tutulamaz.