Levmol 5 mg Efervesan Tablet Kısa Ürün BilgisiSolunum Sistemi » Sistemik Antihistaminikler » Sistemik Antihistaminik İlaçlar » Piperazin Türevleri » Levosetirizin KISA URUN BILGISI 1. BEŞERI TIBBI URUNUN ADILEVMOL 5 mg efervesan tablet2. KALITATIF VE KANTİTATIF BILEŞIMI ETKIN MADDE:Levosetirizin dihidroklorür 5 mgYardımcı maddeler:Sodyum bikarbonat (470,00 mg)Sorbitol (E420) (45,00 mg) Aspartam (E951) (30,00 mg) Asesülfam potasyum (20 mg) Sodyum, sorbitol, aspartam ve potasyum hakkında uyarı için ayrıca bölüm 4.4'e bakınız. Yardımcı maddeler için 6.1'e ba kınız.3. FARMASÖTIK FORMUEfervesan tablet.Sarı benekli, beyaz renkte, düz yüzeyli, yuvarlak efervesan tabletler. 4. KLİNIK ÖZELLIKLER4.1. Terapötik endikasyonlarLEVMOL, 6 yaşın üzerindeki hastalarda, alerjik rinit (intermittan / persistan veya mevsimsel / perenyial) ve kronik idiopatik ürtiker ile ilişkili semptomların giderilmesinde endikedir.4.2. Pozoloji ve uygulama şekli6-12 yaş arası çocuklardaÖnerilen günlük doz 5 mg'dır (1 efervesan tablet) 12 yaş ve üzeri ergenler ile yetişkinlerdeÖnerilen günlük doz 5 mg'dır (1 efervesan tablet).YaşlılardaOrta-ağır şiddette böbrek yetmezliği olan hastalarda dozun ayarlanması önerilir (bkz., Bölüm Böbrek yetmezliği)İntermitan alerjik rinit (haftada 4 günden az ya da 4 haftadan kısa süren belirtiler) hastalığa ve öyküye göre tedavi edilir; belirtiler geçtiğinde tedavi kesilebilir ve belirtiler tekrar görüldüğünde tedaviye yeniden başlanabilir. Persistan alerjik rinit durumunda (haftada 4 günden fazla ve 4 haftadan uzun süren belirtiler), hastanın alerjenlere maruz kaldığı dönem boyunca tedavinin sürdürülmesi önerilir. 5 mg levosetirizin ile klinik çalışmalar, 6 aylık bir tedavi dönemi için mevcuttur. Kronik ürtiker ve kronik alerjik rinit için; rasemat'a (setirizine) ait bir yıla kadar klinik deneyim mevcuttur. Uygulama şekli:LEVMOL bir bardak suda eritilip, bekletilmeden içilmelidir. Yemeklerle birlikte veya yemeklerden bağımsız olarak alınabilir. Günlük dozun tek seferde alınması önerilir.Özel popülasyonlara ilişkin ek bilgiler: Böbrek / Karaciğer yetmezliği:Doz aralıkları, kişinin böbrek fonksiyonlarına göre bireysellestirilir. Doz ayarlaması, aşağıdaki tablo uyarınca yapılır. Bu doz tablosunu kullanmak için, hastanın kreatinin klerensi (CLcr) ml/dak olarak hesaplanmalıdır. CLcr mI/dak değeri, serum kreatinin (mg/dI) değerlerinin aşağıdaki formüle uygulanmasıyla hesaplanır: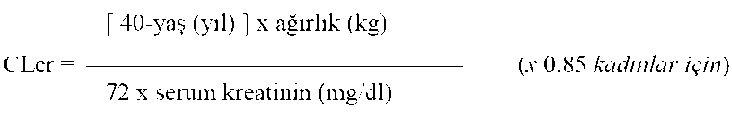 Böbrek Fonksiyon Bozukluğu olan Hastalar İçin Doz Ayarlaması:
Böbrek Fonksiyon Bozukluğu olan Hastalar İçin Doz Ayarlaması:Kreatinin klerensi (ml/dakika)GrupDozaj ve sıklığıGünde 1 kez 5 mg
Normal
> 80 Günde 1 kez 5 mg
Hafif
50-79 İki günde 1 kez 5 mg
Orta
30-49 Üç günde 1 kez 5 mg
< 30
Ağır Son dönem böbrek yetmezliği ve diyalizdeki hastalarda
< 10
Kontrendikedir Böbrek yetmezliği olan pediyatrik hastalarda doz, hastanın renal klerensi ve vücut ağırlığı göz önüne alınarak bireysel olarak ayarlanmalıdır. Böbrek yetmezliği olan çocuklar için spesifik veri bulunmamaktadır. Sadece karaciğer yetmezliği olan hastalarda herhangi bir doz ayarlamasına gerek yoktur. Karaciğer yetmezliği ve böbrek yetmezliği olan hastalarda doz ayarlaması önerilmektedir (bkz., Bölüm "Böbrekyetmezliği").Pediyatrik popülasyon:6-12 yaş arası çocuklar için önerilen günlük doz 5 mg'dır (1 efervesan tablet). 2-6 yaş arası çocuklarda efervesan tablet formuyla doz ayarlaması mümkün değildir.Geriyatrik popülasyon:Orta dereceli ve şiddetli böbrek yetmezliği olan yaşlı hastalarda doz ayarlaması önerilir(bkz., Bölüm 4.2 Pozoloji ve Uygulama Şekli, Böbrek/Karaciğer yetmezliği.).4.3. KontrendikasyonlarLEVMOL, herhangi bir piperazin türevi veya yardımcı maddelerden herhangi birine karşı aşırı duyarlılığı olanlarda kontrendikedir.Ağır böbrek yetmezliği (kreatinin klerensi 10 ml/dak'nın altında) olan hastalarda kontrendikedir. 44.4. Özel kullanım uyarıları ve önlemleriMevcut efervesan tabletlerin farmasötik şekli doz ayarlamasına imkan tanımadığından, LEVMOL'ün 6 yaşından küçük çocuklarda kullanımı önerilmez.Alkol ile bir lik(bkz., Bölüm 4.5 Diğer tıbbi ürünler ile etkileşimler ve diğer etkileşim şekilleri).2 yaşın altındaki çocuk ve bebeklerde veri bulunmaması sebebiyle, bu popülasyonda kullanılması öner ilmez.LEVMOL sorbitol (E420) içermektedir. Nadir kalıtımsal fruktoz intolerans problemi olan hastaların bu ilacı kullanmamaları gerekir. LEVMOL aspartam (E951) içermektedir. Fenilalanin için bir kaynak içermektedir. Fenilketonürisi olan insanlar için zararlı olabilir. LEVMOL her bir efervesan tablette 128,675 mg sodyum ihtiva eder. Bu durum, kontrollü sodyum diyetinde olan hastalar için göz önünde bulundurulmalıdır. LEVMOL 1 mmol (39 mg)'dan daha az potasyum ihtiva eder, yani esasında potasyum içermez. 4.5. Diğer tıbbi ürünlerle etkileşimler ve diğer etkileşim şekilleriLEVMOL ile yapılmış etkileşim çalışması yoktur (CYP3A4 indükleyicileri ile yapılan bir çalışma da yoktur). LEVMOL'ün rasemat bileşiği olan setirizin ile yapılan çalışmalarda, klinikte anlamlı advers etkileşimlerin (psödoefedrin, simetidin, ketokonazol, eritromisin, azitromisin, glipizid ve diazepam ile) olmadığı gösterilmiştir. Teofilin (günde bir kez 400 mg) ile yapılan çok dozlu bir çalışmada setirizin klerensinde küçük bir azalma (%16) gözlenmiş; ancak setirizin ile birlikte uygulandığında teofilinin dağılımı değişmemiştir.LEVMOL gıdalar ile bir likmiktarı değişmemektedir.Rasemat setirizinin alkolün etkisini artırmadığı gösterilmiş olsa da, hassas hastalarda, alkol veya diğer santral sinir sistemi depresanlarının setirizin veya LEVMOL ile birlikte eş zamanlı kullanımının, santral sinir sistemi üzerine etkisi olabilir. Ritonavir (günde iki kez 600 mg) ve setirizin (günde bir kez 10 mg) ile yapılan bir çoklu doz çalışmasında, setirizine maruziyet yaklaşık %40 artmış, setirizin ile birlikte uygulandığında ritonavirin dağılımı hafifçe azalmıştır (- %11). Özel popülasyonlara ilişkin ek bilgilerÖzel popülasyonlara ilişkin bir etkileşim çalışması bulunmamaktadır.Pediyatrik popülasyonPediyatrik popülasyona ilişkin herhangi bir etkileşim çalışması tespit edilmemiştir.4.6. Gebelik ve laktasyon:Genel tavsiyeGebelik kategorisi B'dir.Çocuk doğurma potansiyeli bulunan kadınlar/Doğum kontrolü (Kontrasepsiyon)Çocuk doğurma potansiyeli bulunan kadınlar LEVMOL ile tedavi edilebilir. LEVMOL'ün oral kontraseptiflerle eş zamanlı kullanımının kontrasepsiyon etkinliğini azaltması beklenmez.Gebelik dönemiLEVMOL'ün gebe kadınlarda kullanımına ilişkin yeterli veri mevcut değildir.Hayvanlar üzerinde yapılan çalışmalar, gebelik/ve-veya/embriyonal/fetal gelişim/ve- veya/doğum/ve-veya/doğum sonrası gelişim üzerindeki etkiler bakımından yetersizdir. İnsanlara yönelik potansiyel risk bilinmemektedir. Gebe kadınlara reçetelenirken dikkatli olunmalıdır. Laktasyon dönemiSetirizin insan sütüne geçmektedir.Emziren kadınların kullanması önerilmez. Üreme yeteneği/FertiliteHayvanlarda yapılan çalışmalar,levosetirizinin fertiliteye bir etkisinin olmadığını göstermiştir.4.7. Araç ve makine kullanımı üzerindeki etkilerKarşılaştırmalı klinik çalışmalar, levosetirizinin önerilen dozlarda kullanıldığında zihinsel dikkati, reaksiyonları veya araç kullanma yeteneğini olumsuz etkilediğine dair herhangi bir bulgu ortaya çıkmamıştır.Ancak, levosetirizin tedavisi altında iken bazı hastalarda somnolans, yorgunluk ve asteni görülebilir. Bu nedenle, araç kullanması gereken, potansiyel olarak tehlikeli aktivitelerde bulunan veya makine kullanmak zorunda olan hastalar, ilaca verdikleri yanıtı dikkate almalı ve dikkatli olmalıdırlar. 4.8. İstenmeyen etkiler12-71 yaş grubundaki kadın ve erkeklerde yapılan terapötik çalışmalarda, Levosetrizin 5 mg grubundaki hastaların %15,1'inde, plasebo grubundaki hastaların %11,3'ünde en az bir advers ilaç reaksiyonu görülmüştür.Terapötik çalışmalarda, advers olaylara bağlı olarak tedaviyi bırakanların oranı, Levosetrizin 5 mg ile %1,0 (9/935); plasebo ile %1,8 (14/771) idi. Levosetrizin ile yapılan klinik çalışmalarda 935 gönüllü, tavsiye edilen 5 mg'lık günlük dozu almıştır. Levosetrizin 5 mg ya da plasebo alan hastalarda elde edilen bu verilerde, %1 ya da daha fazla oranda (yaygın: >1/100, ? 1/10) aşağıdaki advers ilaç reaksiyon insidansları bildirilmiştir: Bu reaksiyonlar, sistem organ sınıfı ve görülme sıklığına göre verilmektedir: Çok yaygın (> 1/10), yaygın (> 1/100 ila ? 1/10), yaygın olmayan (> 1/1.000 ila ? 1/100), seyrek (> 1/10.000 ila ? 1/1.000) ve çok seyrek (? 1/10,000). Sinir sistemi hastalıklarıYaygın: Baş ağrısı, somnolansGastrointestinal hastalıklarıYaygın: Ağız kuruluğu Yaygın olmayan: Karın ağrısıGenel Bozukluklar ve Uygulama Bölgesine ilişkin HastalıklarıYaygın: Halsizlik Yaygın olmayan: AsteniSomnolans, yorgunluk ve asteni gibi sedatif advers ilaç reaksiyonlarının tamamı, Levosetrizin 5 mg'da (%8.1) plaseboya göre (%3.1) daha sıktır. Klinik çalışmalarda bildirilen ve yukarıda listelenen advers reaksiyonlara ilaveten, ilacın pazara sunulmasını takiben aşağıda listelenen advers etki vakaları çok seyrek bildirilmiştir. Bağışıklık sistemi hastalıklarıÇok seyrek: Anafilaktik şok dahil aşırı duyarlılıkPsikiyatrik hastalıklarÇok seyrek: Agresyon, ajitasyon, halüsinasyon, depresyonSinir sistemi hastalıklarıÇok seyrek: KonvülsiyonGöz hastalıklarıÇok seyrek: Görme bozukluğuKardiyak hastalıklarÇok seyrek: Palpitasyonlar, taşikardiSolunum, torasik ve mediastinal hastalıklarÇok seyrek: DispneGastro-intestinal bozukluklarÇok seyrek: BulantıHepato-bilier hastalıklarÇok seyrek: HepatitDeri ve derialtı doku bozukluklarıÇok seyrek: Anjiyonörotik ödem, sabit ilaç erüpsiyonu, kaşıntı, döküntü, ürtikerKas- iskelet bozuklukları, bağ dokusu ve kemik hastalıklarıÇok seyrek: Kas ağrısı (miyalji)TetkiklerÇok seyrek: Kilo artışı, karaciğer fonksiyon testlerinde anormallik4.9. Doz aşımı ve tedavisiDoz aşımının belirtileri erişkinlerde uyuşukluk; çocuklarda ise önce ajitasyon ve huzursuzluk, ardından da uyuşukluk olabilir.Tedavi: Levosetrizinin bilinen belirli bir antidotu yoktur. Doz aşımı söz konusuysa, semptomatik veya destekleyici tedavi önerilir. İlaç alındıktan sonra kısa bir süre geçmişse mide lavajı düşünülmelidir. LEVDAY, vücuttan hemodiyaliz ile etkili bir şekilde atılamaz. 5. FARMAKOLOJİK ÖZELLİKLER5.1. Farmakodinamik ÖzelliklerFarmakoterapötik grup: Sistemik antihistaminik, piperazin türevi ATC kodu: R06A E09Etki MekanizmasıLEVMOL, setirizinin (R) enantiomeri, güçlü ve selektif bir periferik Hı-reseptör antagonistidir. Bağlanma çalışmaları, levosetirizinin insan Hı-reseptörlerine yüksek afinitesi olduğunu göstermektedir (Ki = 3,2 nmol/l). Levosetirizin afinitesi, setirizininkinin (Ki = 6.3 nmol/l) iki katıdır.Levosetirizin, 115 ± 38 dakikalık bir yarılanma ömrü ile Hı-reseptörlerinden ayrılır.Tek uygulama sonrasında, levosetirizinin reseptör tutma oranı 4 saatte %90, 24 saatte %57'dir. Sağlıklı gönüllülerde yapılan farmakodinamik çalışmalar, yarı dozda Levosetirizinin, hem deride hem de burunda setirizin ile benzer aktiviteye sahip olduğunu göstermektedir. Farmakodinamik EtkilerLevosetrizinin farmakodinamik aktivitesi randomize, kontrollü çalışmalarda incelenmiştir: Levosetrizin 5 mg, desloratadin 5 mg ve plasebonun, histamin ile indüklenen kabarıklık ve kızarıklıklar üzerindeki etkilerini karşılaştıran bir çalışmada, plasebo ve desloratadin ile karşılaştırıldığında levosetirizin tedavisi kabarıklık ve kızarıklık oluşumunu, ilk 12 saatte en yüksek olmak üzere 24 saat süren etki ile anlamlı derecede (p<0.001) azaltmıştır.Alerjene maruziyet testi odası modelinde yapılan plasebo kontrollü çalışmalarda, polen ile indüklenen belirtilerin kontrolünde, Levosetrizin 5 mg'ın etki başlangıcı, ilaç alımından 1 saat sonra gözlenmiştir. In vitroİn vivo(skin chamber tekniği ile), 14 yetişkin hastada yapılan farmakodinamik deneysel bir çalışmada, polen ile indüklenen reaksiyonun ilk 6 saatinde, plaseboya kıyasla, Levosetrizin 5 mg'ın 3 ana inhibitör etkisi saptanmıştır: Vasküler Hücre Adhezyon Molekülü-1 (VCAM-1) salıverilmesinin inhibisyonu, vasküler permeabilitenin modülasyonu ve eozinofil toplanmasında azalma.Mevsimsel alerjik rinit, pereniyal alerjik rinit ya da persistan alerjik rinitli yetişkin hastalarda yapılan çok sayıda çift-kör, plasebo kontrollü klinik çalışmada, levosetrizinin etkililiği ve güvenliliği gösterilmiştir. Bazı çalışmalarda, levosetrizinin alerjik rinitin, nazal obstrüksiyon dahil, tüm belirtilerini önemli derecede iyileştirdiği gösterilmiştir. Persistan alerjik rinitli (belirtilerin haftada 4 gün ve en az 4 ardışık hafta sürmesi) ve ev tozu akarlarına ve çim polenine karşı duyarlı olan 551 yetişkin hastada (levosetirizin kullanan 276 hasta dahil) yapılan 6 aylık klinik çalışmada, 5 mg levosetrizinin, tüm çalışma süresi boyunca taşifilaksi gelişmeden, alerjik rinit toplam semptom skorunu azalttığı, plaseboya göre klinik ve istatistiksel olarak anlamlı derecede daha etkili olduğu gösterilmiştir. Tüm çalışma boyunca, levosetrizinin hastaların yaşam kalitesini anlamlı şekilde iyileştirdiği görülmüştür. Levosetrizinin pediyatrik güvenlilik ve etkililiği, sırasıyla, mevsimsel ve pereniyal alerjik rinit şikayeti olan 6-12 yaş arası hastaların katıldığı iki plasebo kontrollü klinik çalışmada araştırılmıştır. Her iki çalışmada da levosetrizin belirtileri anlamlı ölçüde düzeltmiş ve sağlıkla ilişkili yaşam kalitesini artırmıştır. Kronik idiyopatik ürtikerli, 166 hastayı içeren, plasebo kontrollü bir klinik çalışmada, 6 hafta boyunca 85 hastaya günde bir kez plasebo, 81 hastaya ise levosetrizin 5 mg verilmiştir. Plasebo ile karsılaştırıldığında, levosetrizin tedavisi, ilk haftada ve tüm tedavi dönemi boyunca kaşıntı şiddetini anlamlı ölçüde azaltmıştır. Dermatoloji Yaşam Kalite İndeksi ile değerlendirildiğinde, levosetrizin, plasebo ile karşılaştırıldığında hastaların sağlıkla ilişkili yaşam kalitesinde daha fazla iyileşme sağlamıştır. Histamin ile indüklenen deri reaksiyonlarına etkisi, plazma konsantrasyonlarına bağımlı değildir. EKG'lerde levosetrizinin QT aralığı üzerine etkisi görülmemiştir. 5.2. Farmakokinetik özellikler Genel özelliklerLevosetrizinin farmakokinetiği, denekler arası değişkenliği düşük, doz ve zamandan bağımsız olarak doğrusaldır. Farmakokinetik profili, tek enantiomer veya setirizin olarak verildiğinde aynıdır. Emilim ve atılım sürecinde hiç bir kiral inversiyon olmaz.Emilim:Levosetirizin, oral yolla alındığında hızla ve büyük oranda emilmektedir. Yetişkinlerde, plazma doruk konsantrasyonlarına dozdan 0,9 saat sonra ulaşılmaktadır. Kararlı duruma iki gün sonra ulaşılır. Tek ve tekrarlanan günde bir kez 5 mg'lık dozun uygulanmasını takiben saptanan doruk konsantrasyonları, sırasıyla 270 ng/ml ve 308 ng/ml'dir. Emilim miktarı dozdan bağımsızdır ve gıdalar ile birlikte alındığında değişmez fakat doruk konsantrasyonu azalır ve gecikir. Dağılım:Levosetirizinin insanlarda doku dağılımına ve kan-beyin-engelini aşmasına dair bilgi bulunmamaktadır. Sıçan ve köpeklerde, en yüksek doku konsantrasyonu karaciğer ve böbreklerde, en düşük olanı ise santral sinir sisteminde saptanmıştır. İnsanlarda, Levosetirizin plazma proteinlerine %90 oranında bağlanır. Levosetirizinin dağılım hacmi 0,4 l/kg olduğundan, dağılımı sınırlıdır. Biyotransformasyon:İnsanlarda Levosetirizin biyotransformasyon oranı dozun %14'ünden azdır ve bu nedenle genetik polimorfizmden veya enzim inhibitörlerinin eş zamanlı alımından kaynaklanan farkların ihmal edilebilir olması beklenmektedir. Metabolik yolaklar, aromatik oksidasyonu, N- ve O-dealkilasyonu ve taurin konjugasyonunu kapsar. Dealkilasyon yolaklarında birincil olarak CYP 3A4 ile düzenlenirken; aromatik oksidasyon, çoklu ve/veya tanımlanmamış CYP izoformlarını içerir. Levosetirizin 5 mg oral doz ile ulaşılan doruk konsantrasyonların üstünde bile 1A2, 2C9, 2C19, 2D6, 2E1 ve 3A4 CYP izoenzimlerinin aktiviteleri üzerinde herhangi bir etki göstermemiştir. Düşük metabolizması ve metabolik inhibisyon potansiyelinin olmamasından dolayı, Levosetirizinin diğer maddelerle, diğer maddelerin de Levosetirizin ile etkileşimi beklenmez. Elimina.syon:Yetişkinlerdeki plazma yarılanma ömrü 7,9 ± 1,9 saattir. Küçük çocuklarda yarılanma ömrü daha kısadır. Yetişkinlerde ortalama görünür toplam vücut klerensi 0,63 ml/dk/kg'dır. Levosetirizin ve metabolitlerinin başlıca eliminasyon yolu idrardır, dozun ortalama %85,4'ü, idrarla vücuttan atılırlar. Dozun sadece %12,9'u dışkı yoluyla atılmaktadır. Levosetirizin hem glomerüler filtrasyon, hem de aktif tübüler sekresyonla vücuttan atılır. Doğrusallık/doğrusal olmayan durum:Levosetirizin, doğrusal farmakokinetik sergiler. Hastalarda karakteristik özelliklerIrk:İlacın emilim ve biyotransformasyon özelliklerine bakılarak hastanın etnik orijininin Levosetirizinin farmakokinetik parametreleri üzerine bir etkisinin olmayacağı beklenir. Cinsiyet:Levosetirizin doruk plazma konsantrasyonları ve total emilimi erkeklere kıyasla kadınlarda yaklaşık %20 ve %15 daha yüksektir. Genellikle, yarılanma ömrü kadınlarda (7.1 saat), erkeklere (8.6 saat) göre kısmen daha kısa olma eğilimindedir. Bununla birlikte, vücut ağırlığına göre ayarlanmış klerensler kadınlarda (0.67 ml/dak/kg) erkeklerdekine (0.59 ml/dak/kg) benzerdir. Bu farklar klinik olarak anlamlı değildir ve bu nedenle benzer günlük dozlar ve dozlama aralıkları kadına ve erkeğe uygulanabilir. Böbrek/Karaciğer yetmezliği:Levosetirizinin vücuttan görünen temizlenmesi ile kreatinin klerensi arasında bir korelasyon vardır. Bu yüzden, levosetirizinin alım aralıklarının, orta ve ağır şiddette böbrek yetmezliği olan hastalarda, kreatinin klerensine göre ayarlanması önerilir. Anurik son evre böbrek hastası olan gönüllülerde, toplam vücut klerensi, normal gönüllülerle karşılaştırıldığında yaklaşık %80 azalmaktadır. Standart 4 saatlik bir hemodiyaliz sırasında atılan Levosetirizin miktarı <%10'dur. Pediyatrik hastalarda:Levosetirizinin 2 yaşın altındaki çocuk ve bebeklerde veri bulunmaması sebebiyle, bu popülasyonda kullanılması önerilmez 5.3. Klinik öncesi güvenlik verileriKlinik öncesi verilerde, geleneksel güvenlilik farmakolojisi, tekrarlı doz toksisitesi, üreme toksisitesi, genotoksisite veya karsinojenisite çalışmalarına dayalı olarak insanlar için herhangi bir özel tehlike ortaya çıkmamıstır.6. FARMASÖTİK ÖZELLİKLER6.1. Yardımcı maddelerin listesiSitrik Asit Sodyum Bikarbonat Maltodekstrin Sorbitol (E 420)Aspartam (E 951) Asesülfam Potasyum Böğürtlen aroması 6.2. GeçimsizliklerGeçerli değil.6.3. Raf ömrü24 ay6.4. Saklamaya yönelik özel tedbirler25 °C'nin altındaki oda sıcaklığında ve kuru yerde saklayınız.Kullandıktan sonra tüpün ağzını kapatmayı unutmayınız. 6.5. Ambalajın niteliği ve içeriği20 (2 x 10) ve 30 (3 x 10) efervesan tablet plastik tüp / silikajelli plastik kapak ve karton kutuda kullanma talimatı ile beraber ambalajlanır.6.6. Beşeri tıbbi üründen arta kalan maddelerin imhası ve diğer özel önlemlerKullanılmamış olan ürünler ya da atık materyaller 'Tıbbi atıkların kontrolü yönetmeliği' ve 'Ambalaj ve Ambalaj Atıklarının Kontrolü yönetmelikleri'ne uygun olarak imha edilmelidir.7. RUHSAT SAHİBICeltis İlaç San. ve Tic. A.Ş.Tozkoparan Mahallesi General Ali Rıza Gürcan Cad. Merter İş Merkezi Bağımsız Bölüm No:2/6 Güngören/İSTANBUL Telefon: 0 212 481 40 98 Faks: 0 212 481 40 98 e-mail: [email protected]8. RUHSAT NUMARASI224/769. İLK RUHSAT TARIHI / RUHSAT YENILEME TARIHIİlk ruhsat tarihi: 13.05.2010 Ruhsat yenileme tarihi:10. KÜB'ün YENİLENME TARİHİ |
İlaç BilgileriLevmol 5 mg Efervesan TabletEtken Maddesi: Levosetirizin Dihidroklorür Atc Kodu: R06AE09 Kullanma talimatı ve kısa ürün bilgileri
Google Reklamları
|
Ana Sayfa | Hakkımızda | İlaçlar | İlaç Ara | İlaç Firmaları | Gizlilik | Bize Ulaşın
Telif Hakkı 2008-2026 © İlaç Prospektüsü. Tüm Hakları Saklıdır.Uyarı: Sitemizde yayınladığımız ilaç bilgileri ile doktora danışmadan kesinlikle ilaç kullanmayınız!
Aksi halde doğabilecek sağlık sorunlarından ilacprospektusu.com sorumlu tutulamaz.