ROTARİX Oral Flakon Kısa Ürün BilgisiEnfeksiyona Karşı Kullanılan (Antienfektif) İlaçlar » Aşılar » AŞI KOMBİNASYONLARI » Rota virus diarrhea vaccines » Rota virus, live attenuated KISA URUNBILGISI1.BEŞERI TIBBI URUNUN ADIROTARIX, Oral Süspansiyon için liyofilize toz içeren flakon Rotavirüs aşısı, Canlı2.KALITATIF VE KANTİTATIF BİLEŞİMEtkin madde:Kullanıma hazırlandıktan sonra, 1 doz (1 mL) içeriği:İnsan rotavirus RIX4414 suşu (canlı, atenüe)*..........................en az 1060 CCID50 *Vero hücrelerinde üretilmiştir. Yardımcı maddeler:Sükroz........................................................................................9 mgSorbitol..................................................................................13.5 mg Yardımcı maddeler için 6.1'e bakınız. Kalıntılar:Porsin Sirkovirüs tip 1 (PCV-1) materyali ROTARIX aşısında tespit edilmiştir. PCV-1'in hayvanlarda hastalığa neden olmadığı ve insanlarda enfeksiyona veya hastalığa neden olmadığı bilinmektedir. PCV-1 varlığının güvenlilik riski taşıdığına yönelik bir kanıt yoktur.3.FARMASÖTIK FORMOral süspansiyon hazırlamak için liyofilize toz ve çözücü. Toz beyaz renktedir.Çözücü, renksiz bir üst faz ve yavaş çöken beyaz bir çökelti ile bulanık bir sıvıdır. 4.KLINIK ÖZELLIKLER4.1. Terapötik endikasyonlarROTARIX, rotavirüs enfeksiyonu kaynaklı gastroenterit oluşumunu önlemek için 6 haftalıktan itibaren bebeklerin aktif bağışıklanmasında endikedir (bakınız bölüm 4.2).Klinik çalışmalarda, G1P[8], G2P[4], G3P[8], G4P[8] ve G9P[8] rotavirüs tiplerinin sebep olduğu gastroenterite karşı etkin olduğu kanıtlanmıştır (bakınız bölüm 4.4 ve 5.1). ROTARIX kullanımı resmi tavsiyelere dayanmalıdır. 4.2. Pozoloji ve uygulama şekli Pozoloji / uygulama sıklığı ve süresi:Aşılama programı iki dozdan oluşmaktadır.İlk doz yenidoğanda 6. haftadan itibaren uygulanabilir. İki doz arasında en az 4 hafta ara verilmelidir. Aşılama tercihen 16.haftadan önce başlamalı, fakat 24. haftaya kadar tamamlanmış olmalıdır. ROTARIX, hamileliğin 27. haftasından itibaren olmak üzere erken doğan bebeklere aynı pozoloji ile uygulanır. Klinik çalışmalarda, aşının nadiren tükürüldüğü ya da kusarak çıkarıldığı tespit edilmiştir. Bu tür durumlarda, yeni bir doz verilmemiştir. Fakat, eğer yenidoğanın aşı dozunun çoğunu tükürmesi ya da kusması gibi bir istenmeyen durum olursa, aynı aşı ziyaretinde tek yineleme dozu verilebilir. ROTARIX'in ilk dozunu alan yenidoğanlarda, 2 doz aşılama programını ROTARIX ile tamamlanması önerilmektedir. Uygulama yolu:ROTARIX sadece oral yolla kullanılır.ROTARIX hiçbir koşulda enjekte edilmemelidir.Özel popülasyonlara ilişkin ek bilgilerBöbrek/Karaciğer yetmezliği:Veri yoktur.Pediyatrik popülasyon:ROTARIX 6 -24 haftalık arası bebeklerde kullanılabilir. Bunun dışında kullanılmamalıdır.Geriyatrik popülasyon:Çocuklarda kullanılması nedeniyle geçerli değildir.4.3. KontrendikasyonlarıEtkin madde ya da yardımcı maddelerden herhangi birine aşırı duyarlılık. Rotavirüs aşısının ilk uygulanmasından sonra aşırı duyarlılık. Daha önceden intususepsiyon hikayesi olanlar.İntususepsiyona eğilim oluşturabilecek gastrointestinal sistem konjenital malformasyonu olan tedavi edilmemiş kişiler (Örn: Meckel's diverticulum). Ciddi Kombine İmmün Yetmezlik (SCID) bozukluğu olanlar (bkz bölüm 4.8) Akut ateşli hastalığı olanlarda ROTARIX uygulaması ertelenmelidir. Minör enfeksiyon varlığı, bağışıklama için bir kontrendikasyon değildir. İshal veya kusma şikayeti olan kişilerde ROTARIX uygulaması ertelenmelidir. 4.4. Özel kullanım uyarıları ve önlemleriAşılama öncesi klinik muayene ve özellikle kontrendikasyonlara bağlı olarak tıbbi hikaye alınması gerekmektedir.Gastrointestinal hastalığı veya büyüme geriliği olan yenidoğanlarda ROTARIX'in etkinliği ve güvenliliğine dair veri mevcut değildir. Bu durumda olan yenidoğanlarda aşının uygulanmaması daha büyük bir riske neden olacak ise doktor onayı ile dikkatli bir şekilde ROTARIX uygulanmalıdır. Latin Amerika ve Finlandiya'da yapılmış olan büyük ölçekli bir güvenlilik çalışmasında (63225 yenidoğanı içermektedir) intususepsiyon riski değerlendirilmiştir. Bu klinik çalışmada plaseboya kıyasla ROTARIX uygulamasını takiben intususepsiyon riskinde artış gözlenmemiştir.(bks bölüm 4.8) Bununla birlikte, pazarlama sonrası güvenlilik verileri ilk ROTARIX dozunu takiben 31 günlük dönemde intususepsiyon riskinde olası bir artışı göstermektedir (Bkz Yan Etkiler). Bu nedenle önlem olarak sağlık çalışanları, intususepsiyonu gösteren herhangi bir semptomu izlemelidir (şiddetli karın ağrısı, uzun süreli kusma, kanlı dışkı, karında şişlik ve/veya yüksek ateş). Ebeveynler/bakıcılar bu tip semptomları derhal hekimlerine bildirmeleri konusunda uyarılmalıdır. Asemptomatik ve hafif semptomatik HIV enfeksiyonunun ROTARIX'in etkinlik veya güvenliliğini etkilemesi beklenmemektedir. Sınırlı sayıda asemptomatik ve hafif semptomatik HIV pozitif yenidoğanda yapılan bir klinik çalışma belli bir güvenlilik problemi olmadığını göstermektedir. Rotarix aşısı, bilinen veya şüpheli immün yetmezliği olan yenidoğanlarda olası risk ve yararları dikkate alınarak uygulanmalıdır. Aşı virüsünün dışkı ile atılımının aşılamadan sonra 7. gün civarında maksimum atılım ile gözlendiği bilinmektedir. İlk dozdan sonra ELISA ile dışkıda saptanan viral antijen partikülleri %50, ikinci dozdan sonra %4 bulunmuştur. Bu dışkılar canlı aşı suşu varlığı için test edildiğinde, sadece %17 pozitif sonuç elde edilmiştir. Atılan bu aşı virüsünün, aşılananların temas halinde olduğu seronegatif kişilere bulaştığı vakalar gözlenmiştir. Ancak herhangi bir klinik semptoma sebep olmamıştır. Malign tümörlü, immün yetmezlikli ya da immünosupresif tedavi gören kişiler gibi immün yetmezliği olan kişiler ile yakın temasta bulunan bireylerde ROTARIX uygulaması dikkatle yapılmalıdır. Yeni aşılanmış kişiler ile temas halinde bulunanlar kişisel hijyene dikkat etmelidirler (Örn: çocukların bezini değiştirdikten sonra ellerini yıkamalıdır). Çok erken doğan bebekler (gebeliğin 28. haftasından önce doğanlar) ve özellikle solunum sistemi gelişimi eksikliği hikayesi olanlarda primer bağışıklama serilerinin uygulanmasında potansiyel apne riskine karşı 48-72 saat solunum sisteminin izlenmesi gerekmektedir. Bu grup yenidoğanlarda aşılamanın yararı yüksek olduğundan, aşılama alıkonmamalı ve ertelenmemelidir. Aşılananların hepsinde koruyucu immün cevap oluşmayabilir (bakınız bölüm 5.1). Klinik çalışmalarda, G1P[8], G2P[4], G3P[8], G4P[8] ve G9P[8] rotavirüs tiplerinin sebep olduğu gastroenterite karşı etkinlik gösterilmiştir. Diğer serotiplere karşı ROTARIX'in koruyucu etkinliği bilinmemektedir. Etkinlik verilerinin elde edildiği klinik çalışmalar Avrupa, Orta ve Güney Amerika'da yapılmıştır (bakınız bölüm 5.1). Rotavirüs dışında diğer patojenlerin sebep olduğu gastroenterit vakalarında ROTARIX'in koruyucu etkinliği yoktur. Maruziyet sonrası profilaksi için ROTARIX kullanımına dair herhangi bir veri mevcut değildir. Aşı yardımcı madde olarak sükroz ve sorbitol içermektedir. Fruktoz intoleransı, glukoz-galaktoz malabsorpsiyon veya sükroz-izomaltaz yetmezliği gibi nadir kalıtsal problemleri olanlar bu aşıyı kullanmamalıdır. 4.5.Diğer tıbbi ürünlerle etkileşim ve diğer etkileşim türleriROTARIX aşağıdaki monovalan veya kombine aşılarla birlikte verilebilir [hekzavalan aşılarda (DTPa-HBV-IPV/Hib) dahil]: difteri-tetanoz-tam hücre boğmaca aşısı (DTPw), difteri-tetanoz-aselüler boğmaca aşısı (DTPa),Haemophilus influenzae tip b aşısı(Hib), inaktif polyo aşısı (IPV), hepatit B aşısı (HBV), pnömokok konjuge aşısı ve meningokok serogrup C konjuge aşısı. Klinik çalışmalar uygulanan aşının immün cevabı ve güvenlilik profilinin etkilenmediğini göstermiştir.ROTARIX ve oral polyo aşısının (OPV) birlikte uygulanması, polyo antijenlerinin immün cevabını etkilemez. OPV'nin birlikte uygulanmasının, rotavirüs aşısının immün cevabını hafif düşürmesine karşın, 4200'den fazla gönüllüye Rotarix ile birlikte OPV uygulandığı bir klinik çalışmada şiddetli rotavirüs gastroenteritine karşı klinik korumanın sağlandığı gösterilmiştir. Yenidoğanların aşılama öncesi veya sonrası gıda veya sıvı tüketimine dair bir kısıtlama yoktur. 4.6.Gebelik ve laktasyonGenel tavsiyeGebelik kategorisi: CÇocuk doğurma potansiyeli bulunan kadınlar/Doğum kontrolü (Kontrasepsiyon)Çocuklarda kullanılması nedeniyle geçerli değildir.Gebelik dönemiÇocuklarda kullanılmakta olup, gebelik esnasında kullanımına dair veri mevcut değildir.Laktasyon dönemiKlinik çalışmalarda toplanan veriler baz alındığında, emzirme ROTARIX'in rotavirüs gastroenteritine karşı sağladığı koruyucu etkiyi düşürmemektedir. Bu sebeple, bebeğin aşılama programı esnasında emzirmeye devam edilebilir.Üreme yeteneği / FertiliteÇocuklarda kullanılmakta olup, üreme yeteneği/fertiliteye dair veri mevcut değildir.4.7.Araç ve makine kullanımı üzerine etkisiÇocuklarda kullanıldığı için geçerli değildir.4.8.İstenmeyen etkilerKlinik çalışmalar:Aşağıda sunulmakta olan güvenlik profili ROTARIX'in liyofilize veya likit formülasyonu ile gerçekleştirilen klinik çalışmalardan elde edilen verilere dayanmaktadır. Toplam dört klinik çalışmada, yaklaşık 1900 yenidoğana yaklaşık 3800 doz ROTARIX likit formülasyonu uygulanmıştır. Bu çalışmalar, likit formülasyonun güvenlik profilinin liyofilize formülasyon ile karşılaştırılabilir olduğunu göstermiştir. Toplam 23 klinik çalışmada, yaklaşık 51000 yenidoğana yaklaşık 106000 doz ROTARIX (liyofilize veya likit formülasyon) uygulanmıştır. ROTARIX'in tek başına uygulandığı (rutin pediyatrik aşıların uygulanması kademelendirilmiştir) üç plasebo kontrollü klinik çalışmada (Finlandiya, Hindistan ve Bangladeş), ROTARIX ve plasebo uygulanan grup arasında beklenen etkiler (aşılamadan 8 gün sonra toplanmıştır), ishal, kusma, iştah kaybı, ateş, iritabilite ve öksürük/burun akıntısı insidansı ve şiddetinde belirgin bir fark saptanmamıştır. İkinci dozda da bu etkilerin insidansı veya şiddetinde artış saptanmamıştır. ROTARIX'in rutin pediyatrik aşılarla birlikte uygulandığı çalışmaların da dahil olduğu (bakınız bölüm 4.5) 17 plasebo kontrollü klinik çalışmanın havuzlanmış analizinde (Avrupa, Kuzey Amerika, Latin Amerika, Asya, Afrika) aşılama ile ilgili olabilecek aşağıdaki advers reaksiyonlar (aşılamadan 31 gün sonra toplanmıştır) tespit edilmiştir. Sistem organ sınıfı ve sıklığa göre advers reaksiyonlar aşağıda listelenmiştir : Sıklıkları aşağıdaki şekilde sınıflandırılmıştır: Çok yaygın (>1/10); yaygın (>1/100, <1/10); yaygın olmayan (>1/1.000, <1/100); seyrek (>1/10.000, <1/1.000), çok seyrek (<1/10.000), izole bildirimler dahil Gastrointestinal bozukluklarYaygın:İshal,Yaygın olmayan: Karın ağrısı, şişkinlik Deri ve deri altı doku bozukluklarıYaygın olmayan:Dermatit,dö^cüntüGenel bozukluklar ve uygulama bölgesi durumuYaygın:İritabiliteİntususepsiyon riski 63225 kişinin katıldığı Latin Amerika ve Finlandiya'da yapılan büyük güvenlilik çalışmalarında değerlendirilmiştir. Aşağıdaki tabloda gösterildiği gibi ROTARIX uygulanan hastalarda plasebo grubu ile karşılaştırıldığında intususepsiyon riskinde bir artış olmadığı kanıtlanmıştır.
Erken doğan bebeklerde güvenlilikBir klinik çalışmada erken doğan 670 bebeğe gebelik süresinin 27. ila 36. haftaları arasında Rotarix, 339 bebeğe ise plasebo uygulanmıştır. İlk doz doğumdan 6 hafta sonra uygulanmıştır. Rotarix uygulananların %5.1'inde, plasebo alanların ise % 6.8'inde ciddi yan etkiler gözlenmiştir. Diğer yan etkiler Rotarix ve plasebo alanlarda benzer oranlarda gözlenmiştir. İnsan Bağışıklık Yetmezliği Virüsü (HIV) ile enfekte yenidoğnalarda güvenlilikBir klinik çalışmada, HIV ile enfekte 100 yenidoğana Rotarix veya plasebo uygulanmıştır. Rotarix ve plasebo alanların güvenlilik profili benzerdir. Pazarlama sonrası veriler: Solunum, toraks ve mediastinal bozukluklar28 haftalıktan küçük yenidoğanlarda apne (bkz. Bölüm 4.4).Gastrointestinal bozukluklarİntususepsiyon* Hematokezi Ciddi Kombine İmmün Yetmezlik (SCID) bozukluğu olan bebeklerde dışkı ile saçılma sonucu gastroenterit. * Meksika'da büyük ölçekli bir pazarlama sonrası epidemiyolojik güvenlilik çalışmasından elde dilen ilk veriler, ilk dozu takiben 31 günlük sürede olası intususepsiyon riskinin arttığını göstermektedir. Spontan intususepsiyon raporları çoğunlukla ilk dozdan sonraki 7 günlük dönemde alınmıştır. Bu gözlemler ilk dozla sınırlı olup ikinci dozdan sonra görülmemektedir. ROTARIX aşısının genel intusussepsiyon insidansını etkileyip etkilemediği gösterilmemiştir (Bkz bölüm 4.4). 4.9. Doz aşımıDoz aşımı vakası rapor edilmemiştir.5.FARMAKOLOJIK ÖZELLIKLER5.1. Farmakodinamik özelliklerFarmakoterapötik grup: Rotavirüs diyare aşıları ATC kodu: J07BH01Koruyucu etkinlikAvrupa ve Latin Amerika'da ROTARIX'in şiddetli rotavirüs gastroenteritine karşı koruyucu etkinliğini değerlendirmek için klinik çalışmalar yapılmıştır. Avrupa'da yapılan bir klinik çalışmada, 4000 denekte farklı Avrupa programlamalarına göre (2., 3. aylar; 2.,4. aylar; 3.,4. aylar; 3.,5. aylar) verilen ROTARIX değerlendirilmiştir. Gastroenteritin şiddeti, ishal ve kusmanın şiddeti ve süresi, ateşin ve dehidratasyonun şiddeti ve tedavi gerekliliği göz önünde bulundurularak rotavirüs gastroenteritinin tam klinik tablosunu değerlendiren Vesikari 20 nokta skalasına göre tanımlanmıştır. İki doz ROTARIX sonrası, yaşamın birinci ve ikinci yılında gözlenen koruyucu aşı etkinliği aşağıdaki tabloda sunulmaktadır:
Yaşamın ilk yılındaki aşının etkinliği hastalık şiddeti arttıkça dereceli olarak artmış , >17 Vesikari skoru olanlar için %100 (95% CI: 84.7;100)'e ulaşmıştır. Latin Amerika'da yapılan bir klinik çalışmada 20.000'den fazla kişide ROTARIX değerlendirilmiştir. Gastroenterit şiddeti DSÖ kriterine göre tanımlanmıştır. Hastanede yatarak tedavi ve/veya tıbbi bir merkezde rehidrasyon tedavisi gerektiren şiddetli rotavirüs gastroenteritine karşı koruyucu aşı etkinliği ve iki doz ROTARIX sonrası tip spesifik aşı etkinliği aşağıdaki tabloda verilmiştir:
*İstatistiksel anlamlı (p < 0.05) #G4P[8] 'e karşı etkinliğin değerlendirildiği vaka sayısı çok azdır. (ROTARIX grubunda 1 vaka, plasebo grubunda 2 vaka) 5 etkinlik çalışmasının* havuzlanmış analizi, yaşamın ilk yılında G2P[4] tipi rotavirüsün sebep olduğu şiddetli rotavirüs gastroenteritine karşı (Vesikari skoru >11) %71.4 (%95 CI:20.1;91.1) etkinlik göstermiştir. * Bu çalışmalarda, nokta tahminleri ve güven aralıkları sırasıyla: %100 (%95 CI: -1858.0;100), %100 (%95 CI: 21.1;100), %45.4 (%95 CI: -81.5;86.6), 74.7 (%95 CI: -386.2;99.6). Diğer çalışmalar için nokta tahmini yoktur. İmmun yanıtROTARIX'in rotavirüs gastroenteritine karşı koruyucu immunolojik mekanizma tam olarak anlaşılamamıştır. Rotavirüs aşılamasına karşı antikor cevapları ve rotavirüs gastroenteritine karşı koruma arasındaki ilişki kanıtlanmamıştır. Aşağıdaki tabloda, Rotarix liyofilize formülasyonu ile yürütülen farklı çalışmalarda, ikinci doz aşı veya plasebodan 1 ila 2 ay sonrası gözlenen serum anti-rotavirüs IgA antikor titreleri > 20U/ml olan gönüllü yüzdesi (ELISA ile) gösterilmiştir.
Erken dofian bebeklerde immün cevabıHamileliğin en az 27. Haftasından sonra doğmuş olan erken doğan bebeklerde gerçekleştirilen bir klinik çalışmada, 147 gönüllüden oluşan bir alt kümede Rotarix bağışıklığı elde edilmiş ve Rotarix'in bu popülasyonda immünojenik olduğu gösterilmiştir; ikinci doz aşılamanın bir ay sonrasında serum anti-rotavirüs IgA antikor titreleri > 20U/ml (ELISA ile) olan gönüllü yüzdesi %85.7'dir (%95 CI: 79.0;90.9). 5.2. Farmakokinetik özelliklerAşılar için farmakokinetik özelliklerin değerlendirilmesi gerekmemektedir.5.3. Klinik öncesi güvenlilik verileriTekrarlanan doz toksisitesinin geleneksel çalışmaları baz alındığında, klinik dışı çalışmalarda insanlar için özel bir risk yoktur.6. FARMASÖTİK ÖZELLİKLER6.1. Yardımcı maddelerin listesiTozSükroz Dekstran Sorbitol Aminoasitler Dulbecco'nun modifiye eagle besiyeri (DMEM) ÇözücüKalsiyum karbonat Ksantan zamkı Steril su 6.2.GeçimsizliklerGeçimlilik çalışmaları olmadığından, bu ürün diğer tıbbi ürünlerle karıştırılmamalıdır.6.3.Raf ömrü36 aydır.6.4.Saklamaya yönelik özel uyarılarKullanıma hazırlanma sonrası:Kullanıma hazırlandıktan sonra, aşı hemen uygulanmalıdır. Buzdolabında saklanmalıdır (2°C - 8°C). Dondurulmamalıdır. Aşı donmuş ise çözüp kullanmayınız. Işıktan korumak için kendi ambalajında saklanmalıdır. 6.5.Ambalajın niteliği ve içeriğiBütil lastik tıpalı (tip I cam) cam flakonda 1 doz tozPistonlu tıpa ve koruyucu üst kapak ile 1 ml çözücü içeren oral aplikatör (tip I cam) Kullanıma hazırlamak için transfer aparatı (1/doz) Ambalaj boyutları: -1 cam flakonda toz ve 1 oral aplikatörde çözücü -5 cam flakonda toz ve 5 oral aplikatörde çözücü -10 cam flakonda toz ve 10 oral aplikatörde çözücü -25 cam flakonda toz ve 25 oral aplikatörde çözücü Tüm ambalajlar pazara sunulmayabilir. 6.6. Beşeri tıbbi üründen arta kalan maddelerin imhası ve diğer özel önlemlerÇözücüyü içeren oral aplikatör saklandıktan sonra beyaz çökelti ve berrak üstfaz gözlenmiştir.Çözücü herhangi bir yabancı partikül içerip içermediğini kontrol için ve kullanıma hazırlamadan önce anormal fiziksel görünüm için çalkalama öncesi ve sonrası görsel olarak incelenir. Kullanıma hazırlanan aşı çözücüden biraz daha bulanık ve görünümü süt beyazıdır. Kullanıma hazırlanan aşı aynı zamanda uygulama öncesi yabancı partiküller ve/veya anormal fiziksel görünüm için incelenmelidir. Gözlenmesi durumunda aşı kullanılmamalıdır. Kullanılmamış olan ürünler ya da atık materyaller "Tıbbi Atıkların Kontrolü Yönetmeliği" ve " Ambalaj ve Ambalaj atıklarının Kontrolü Yönetmeliği"ne uygun olarak imha edilmelidir. Kullanıma hazırlama ve aşının uygulanması :1.Toz içeren cam flakonun plastik kapağı çıkarılır. 2.Transfer aparatı cam flakon üzerine yerleştirilir, uygun ve güvenli bir şekilde yerleşene kadar bastırılır. 3.Çözücüyü içeren oral aplikatör güçlü bir şekilde çalkalanır. Çalkalanan süspansiyon yavaş çöken beyaz çökelti ile bulanık bir sıvı görünümündedir. 4.Oral aplikatörün koruyucu kapağı çıkarılır. 5.Oral aplikatör ile transfer aparatı bu aletin üzerine geçirilerek bağlantı kurulur. 6.Oral aplikatörün tüm içeriği tozu içeren cam flakona nakledilir. 7.Oral aplikatör hala takılı iken, cam flakon çalkalanır ve tozun tamamen süspansiyona dönüşüp dönüşmediği incelenir. Kullanıma hazırlanan aşı tek çözücüden daha bulanık görülür. Bu görünüm normaldir. 8.Tüm karışım tekrar oral aplikatöre alınır. 9.Oral aplikatör transfer aparatından çıkarılır. 10.Bu aşı sadece oral uygulama içindir. Çocuk yaslanma pozisyonunda oturtulmalı ve oral aplikatör ile oral yolla uygulanmalıdır (oral aplikatörün tüm içeriği yanağın iç tarafına uygulanmalıdır) 11. Enjekte etmeyiniz.12.Kullanıma hazırlanan aşı uygulama öncesi geçici olarak saklanabilir, oral aplikatörün üzerindeki koruyucu kapağı çıkarılır. Kullanıma hazır aşıyı içeren oral aplikatör, oral uygulama öncesi hafifçe çalkalanmalıdır.Enjekte etmeyiniz.1. Tozu içeren cam flakonun plastik kapağı çıkarılır.2. Transfer adaptörü cam flakonun üzerine yerleştirilir ve uygun ve güvenli bir şekilde yerleşene kadar bastırılır.3. Çözücüyü içeren oral aplikatör şiddetli biçimde çalkalanır. Çalkalanan süspansiyon hafif çöken beyaz çökelti ile bulanık sıvı şeklinde görünür.
7. Oral aplikatör hala takılı iken, cam flakon çalkalanır ve tozun tamamen süspansiyona dönüşümü incelenir. Kullanıma hazırlanan aşı tek çözücüden daha bulanıktır. Bu görünüm normaldir.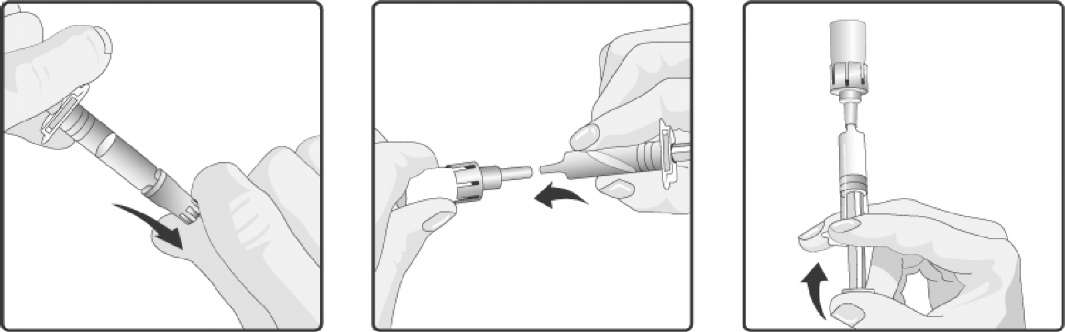
4. Oral aplikatörün koruyucu kapağı çıkarılır.5. Oral aplikatör bastırılarak transfer aparatına bağlanır .6. Oral aplikatörün tüm içeriği tozu içeren cam flakona nakledilir.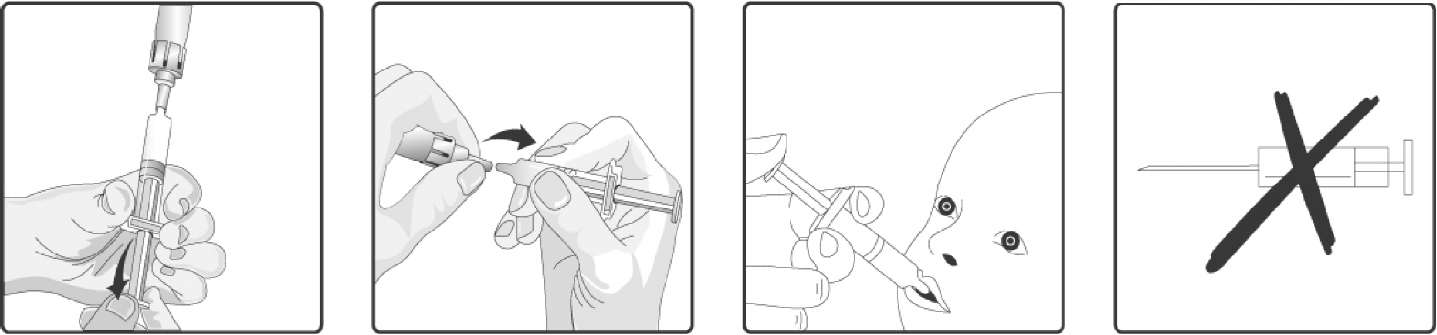
8. Tüm karışım tekrar oral aplikatöre nakledilir.9. Oral aplikatör transfer adaptöründen ayrılır.10. Bu aşı sadece oral uygulama içindir. Çocuk yaslanma pozisyonuna getirilir ve tüm içerik oral aplikatör ile yanak iç bölgesine uygulanır.11.Enjekte etmeyiniz.7. RUHSATSAHİBIGlaxoSmithKline İlaçları Sanayi ve Ticaret A.Ş. Büyükdere Cad. No:173 1.Levent Plaza B Blok 34394, 1.Levent / İSTANBUL Tel no: 0 212 339 44 00 Faks no: 0 212 339 45 008.RUHSAT NUMARASI:369.iLK RUHSATTARIHI/RUHSAT YENİLEME TARIHIİlk ruhsat tarihi: 24.06.2010 Ruhsat yenileme tarihi:10.KUB'UN YENILENME TARIHI:13.12.2010 |
İlaç BilgileriROTARİX Oral FlakonEtken Maddesi: İnsan rotavirüs RIX44414 suşu Atc Kodu: J07BH01 Kullanma talimatı ve kısa ürün bilgileri
Google Reklamları
İlgili İlaçlar |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
Ana Sayfa | Hakkımızda | İlaçlar | İlaç Ara | İlaç Firmaları | Gizlilik | Bize Ulaşın
Telif Hakkı 2008-2026 © İlaç Prospektüsü. Tüm Hakları Saklıdır.Uyarı: Sitemizde yayınladığımız ilaç bilgileri ile doktora danışmadan kesinlikle ilaç kullanmayınız!
Aksi halde doğabilecek sağlık sorunlarından ilacprospektusu.com sorumlu tutulamaz.