Lescol XL 80 mg kontrollü salımlı tablet Kısa Ürün BilgisiKalp Damar Sistemi » Lipid Metabolizması İlaçları » Yağ Metabolizması İlaçları » HMG CoA Redüktaz İnhibitörleri » Fluvastatin Sodyum KISA URUN BILGISI1. BEŞERI TIBBI ÜRÜNÜN ADILESCOL XL 80 mg kontrollü salımlı tablet2. KALITATIF VE KANTİTATIF BILEŞIMEtkin madde :Fluvastatin sodyum 84.24 mg (80 mg fluvastatin serbest asidine eşdeğer)Yardımcı maddeler:Yardımcı maddeler için 6.1'e bakınız.3. FARMASÖTIK FORMKontrollü salımlı tablet.Bir yüzünde oyularak LE, diğer yüzünde NVR ya da bir yüzünde LESCOL XL, diğer yüzünde 80 basılmış, kenarları konik kesimli, sarı, yuvarlak, hafifçe bikonveks tabletler. 4. KLİNIK ÖZELLIKLER4.1. Terapötik endikasyonlar DislipidemiDiyete ve diğer farmakolojik olmayan tedavilere (örneğin; egzersiz, kilo verme) cevabın yetersiz kaldığı durumlarda diyete ilave olarak, karma dislipidemili veya primer hiperkolesterolemili yetişkinlerin tedavisiKoroner kalp hastalığında sekonder korunmaPerkütanöz koroner müdahalelerden sonra koroner kalp hastalığı olan yetişkinlerde majör kardiyak advers olayların sekonder olarak korunması4.2. Pozoloji ve uygulama şekliPozoloji:YetişkinlerLESCOL XL ile tedaviye başlamadan önce hasta standart bir kolesterol düşürücü diyete alınmalıdır. Diyet, tedavi boyunca sürdürülmelidir.Önerilen başlangıç dozu 40 mg (günde bir kere 1 kapsül LESCOL 40 mg) ya da 80 mg'dır (günde bir kere 1 tablet LESCOL XL 80 mg ya da günde iki kere 1'er kapsül LESCOL 40 mg). Başlangıç dozları, başlangıç LDL-kolesterol düzeylerine ve önerilen tedavi hedefine göre bireysel olarak ayarlanmalıdır. Koroner transkateter tedavisinden sonra koroner kalp hastalığı olan kişilerde uygun doz günde 80 mg'dır. LESCOL XL monoterapide etkilidir. Fluvastatinin nikotinik asit, kolestiramin ya da fibratlarla kombinasyonunun etkili ve güvenli olduğunu destekleyen veriler mevcuttur (bkz. bölüm 4.5 Diğer tıbbi ürünler ile etkileşimler ve diğer etkileşim şekilleri). Uygulama sıklığı ve süresi:İlacın belirli bir dozu ile maksimum lipid düşürücü etkiye 4 hafta içinde ulaşılır. Doz ayarlaması hastanın tedaviye verdiği yanıta göre 4 hafta ya da daha uzun süreli aralıklarla yapılmalıdır. LESCOL'ün terapötik etkisi uzun süreli uygulamada da sürdürülür.Uygulama şekli:LESCOL XL, günün herhangi bir saatinde yemekle birlikte ya da aç karnına tek bir doz olarak alınabilir.LESCOL XL, bir bardak su ile bütün olarak yutulmalıdır. Özel popülasyonlara ilişkin ek bilgiler:Böbrek yetmezliği:Fluvastatin karaciğer tarafından metabolize edilir ve verilen dozun %6'sından daha azı idrarla atılır. Hafif ila şiddetli böbrek yetmezliği olan hastalarda fluvastatinin farmakokinetiği değişmez. Bu nedenle, söz konusu hastalarda doz ayarlaması gerekli değildir.Karaciğer yetmezliği:LESCOL XL, aktif karaciğer hastalığı ya da serum transaminazlarda açıklanamayan kalıcı yükselmeleri olan hastalarda kontrendikedir (Bkz. Bölüm 4.3 Kontrendikasyonlar ve Bölüm 4.4 Özel kullanım uyarıları ve önlemleri).Pediyatrik popülasyon:LESCOL'ün çocuk hastalarda kullanılması önerilmez.Geriyatrik popülasyon:LESCOL XL ile yapılan klinik çalışmalarda, hem 65 yaş altı hem de 65 yaş üzeri hastalarda etkililik ve tolerabilitesi gösterilmiştir. Yaşlı hastalarda (>65 yaş) tedaviye verilen yanıt artmıştır ve tolerabilitede azalma görülmemiştir. Bu nedenle dozun yaşa göre ayarlanması gerekli değildir.4.3. Kontrendikasyonlar Fluvastatine ya da yardımcı maddelerinden herhangi birine karşı aşırı duyarlılığı olduğu bilinen hastalarda, Aktif karaciğer hastalığı ya da serum transaminaz değerlerinde açıklanamayan, kalıcı yükselmeleri olan hastalarda, Gebelik ve emzirme döneminde (bkz. Bölüm 4.6 Gebelik ve laktasyon) kontrendikedir. 4.4. Özel kullanım uyarıları ve önlemleriKaraciğer fonksiyonu:Diğer lipid düşürücü ilaçlarla olduğu gibi, bütün hastalarda tedaviye başlamadan önce ve tedaviye başlandıktan 12 hafta sonra ya da doz artırılırken ve daha sonra periyodik olarak karaciğer fonksiyon testi yapılması önerilir. Aspartat aminotransferaz ya da alanin aminotransferaz değerlerinde normalin üst sınırının 3 mislini geçen bir artış olması ve bu durumun devam etmesi halinde tedaviye son verilmelidir. Çok nadir durumlarda, muhtemelen ilaçla ilişkili ve tedavinin kesilmesiyle düzelen hepatit vakaları gözlenmiştir. Karaciğer hastalığı geçmişi ya da aşırı alkol tüketimi olan hastalarda LESCOL XL dikkatle kullanılmalıdır. İskelet kasları: Fluvastatinle nadir olarak miyopati ve çok nadir olarak miyozit ve rabdomiyoliz vakaları bildirilmiştir. Açıklanamayan yaygın miyalji, kas hassasiyeti ya da güçsüzlüğü ve/veya kreatin kinaz (KK) değerlerinde belirgin yükselme olan hastalarda, miyopati, miyozit ya da rabdomiyoliz olasılığı düşünülmelidir. Bu nedenle, hastalara özellikle de halsizlik ve ateşin eşlik etmesi durumunda, açıklanamayan kas ağrısı, kas hassasiyeti ya da güçsüzlüğü durumlarını hemen doktora bildirmeleri söylenmelidir. Kreatin kinaz (KK) ölçümü: Statin kullanan asemptomatik hastalarda, plazma total kreatin kinaz ya da diğer kas enzimi düzeylerinin düzenli olarak izlenmesi gerektiğine dair kanıtlar mevcut değildir. Eğer kreatin kinaz düzeyinin ölçülmesi gerekiyorsa, bu ölçüm yorucu bir egzersiz sonrasında ya da KK artışına ilişkin diğer makul bir nedenin varlığında yapılmamalıdır, çünkü bu, değerlerin yorumlanmasını güçleştirecektir. Tedaviden önce: Diğer tüm statinlerle olduğu gibi, hekimler rabdomiyoliz ve komplikasyonları açısından yatkınlaştırıcı faktörler taşıyan hastalarda fluvastatini reçete ederken dikkatli olmalıdır. Aşağıdaki durumlarda, fluvastatin tedavisine başlamadan önce kreatin kinaz düzeyi ölçülmelidir: Böbrek yetmezliği, Hipotiroidizm, Hastada ya da ailesinde kalıtsal kas hastalığı öyküsü varlığı, Bir statin ya da fibrat tedavisiyle yaşanan kas toksisitesi geçmişi, Alkol bağımlılığı, Yaşlı hastalarda (70 yaş üzeri), bu ölçümün gerekli olup olmadığı rabdomiyoliz için diğer yatkınlaştırıcı faktörlerin varlığına göre değerlendirilmelidir. Bu tip durumlarda, tedavi riski olası faydasına göre değerlendirilmelidir; klinik izlem önerilir. Eğer KK düzeylerinin başlangıçta anlamlı düzeyde yükselmiş olduğu saptanırsa [>5 x NÜS (normalin üst sınırı)], düzeyler bulguları teyit etmek için 5 ila 7 gün sonra tekrar ölçülmelidir. Eğer KK düzeyleri başlangıçta hala anlamlı düzeyde yüksek ise (>5 x NÜS), tedaviye başlanmamalıdır. Tedavi sırasında: Fluvastatin kullanan hastalarda ağrı, güçsüzlük ya da kramp gibi kas semptomları gelişirse, KK düzeyleri ölçülmelidir. Bu düzeylerin anlamlı düzeyde yükselmiş (>5 x NÜS) olduğu saptanırsa, tedavi kesilmelidir. Kas semptomları şiddetliyse ve günlük yaşamda rahatsızlığa yol açıyorsa, KK değerleri 5xNÜS ya da altında bir düzeye yükselmişse bile tedavinin sonlandırılması düşünülmelidir. Semptomların iyileşmesi ve KK düzeylerinin normale dönmesi durumunda, fluvastatin ya da diğer bir statin ile en düşük dozda ve yakın gözlem altında yeniden tedaviye başlanması düşünülebilir. Diğer HMG-CoA redüktaz inhibitörleri ile birlikte immünosupresif ilaçlar (siklosporin dahil), fibratlar, nikotinik asit ya da eritromisin kullanan hastalarda miyopati riskinin arttığı bildirilmiştir. Bununla birlikte, yapılan klinik çalışmalarda fluvastatin ile birlikte nikotinik asit, fibratlar ya da siklosporin kullanan hastalarda miyopati gözlenmemiştir. Pazarlama sonrası çalışmalarda, fluvastatinin siklosporinle ve kolşişin ile eş zamanlı kullanımında nadir miyopati vakaları bildirilmiştir. LESCOL XL bu ilaçları eş zamanlı olarak alan hastalarda dikkatle kullanılmalıdır (bkz. Bölüm 4.5 Diğer tıbbi ürünlerle etkileşimler ve diğer etkileşim şekilleri). Pediyatrik hastalar: 18 yaş altı hastalarda, etkililik ve güvenlilik 2 yıldan uzun tedavi sürelerinde incelenmemiştir. Fluvastatin yalnızca heterozigot kalıtsal hiperkolesterolemili 9 yaş ve üzerindeki çocuklarda incelenmiştir (ayrıntılı bilgi için, bkz. bölüm 5.1 Farmakodinamik özellikler). Homozigot kalıtsal hiperkolesterolemi: Fluvastatinin, homozigot kalıtsal hiperkolesterolemi olarak bilinen nadir bir durumun gözlendiği hastalarda kullanımına ilişkin veri mevcut değildir. 4.5. Diğer tıbbi ürünler ile etkileşimler ve diğer etkileşim şekilleriBesin etkileşimleri:Akşam yemeklerinde ya da akşam yemeğinden 4 saat sonra alındığında fluvastatinin lipid düşürücü etkisinde belirgin bir farklılık görülmemektedir. Fluvastatinin diğer CYP3A4 substratlarıyla etkileşiminin olmaması nedeniyle greyfurt suyuyla etkileşmesi beklenmez. Diğer ilaçların fluvastatin üzerindeki etkileriFibrik asit türevleri (fibratlar) ve niasin (nikotinik asit):Fluvastatinin bezafibrat, gemfibrozil, siprofibrat ya da niasin (nikotinik asit) ile eş zamanlı kullanımı, fluvastatinin ya da diğer lipid düşürücü ilacın biyoyararlanımı üzerine klinik olarak anlamlı bir etkiye sahip değildir. Bununla birlikte, diğer HMG-CoA redüktaz inhibitörlerini bu moleküllerden herhangi biriyle birlikte kullanan hastalarda artmış bir miyopati riski gözlendiği için, bu kombinasyonlar dikkatle uygulanmalıdır (bkz. Bölüm 4.4 Özel kullanım uyarıları ve önlemleri). İtrakonazol ve eritromisin: Fluvastatinin, güçlü CYP 3A4 inhibitörleri olan itrakonazol ve eritromisinle birlikte kullanımının fluvastatinin biyoyararlanımı üzerine minimal etkileri vardır. Bu enzimin fluvastatinin metabolizmasında minimum bir rolü olduğu dikkate alındığında, diğer CYP3A4 inhibitörlerinin (ör: ketokonazol, siklosporin) fluvastatinin biyoyararlanımını etkilemesi beklenmez. Flukonazol: Daha önceden flukonazol (CYP2C9 inhibitörü) ile tedavi edilen sağlıklı gönüllülere fluvastatin verilmesi sonucunda fluvastatinin maruziyetinde ve pik konsantrasyonunda yaklaşık %84 ve %44 oranında bir artış gözlenmiştir. Daha önceden 4 gün boyunca flukonazol ile tedavi edilen hastalarda fluvastatinin güvenlilik profilinin değiştiğine dair bir klinik kanıt elde edilmemiş olmakla birlikte, fluvastatin flukonazol ile birlikte kullanılırken dikkatli olunmalıdır. Siklosporin: Renal transplant hastalarında yapılan çalışmalar, fluvastatinin (günde 40 mg'a kadar) biyoyararlanımının stabil siklosporin rejimlerinde olan hastalarda klinik olarak anlamlı bir düzeyde yükselmediğini göstermektedir. LESCOL XL'nin (80 mg fluvastatin) stabil siklosporin rejimlerinde olan renal transplant hastalarına verildiği diğer bir çalışmadan elde edilen bulgular fluvastatin maruziyetinin [EAA(Eğri altı alan)] ve maksimum konsantrasyonunun (Cmax) sağlıklı gönüllülerde elde edilen geçmiş verilere kıyasla 2 misli arttığını göstermiştir. Fluvastatin düzeylerindeki bu artışlar klinik açıdan anlamlı olmamakla birlikte, bu kombinasyon dikkatle kullanılmalıdır (bkz. Bölüm 4.4 Özel kullanım uyarıları ve önlemleri). Safra asidi sekestranları: Reçinenin ilaca bağlanması nedeniyle oluşabilecek anlamlı bir etkileşimi önlemek için, fluvastatin reçineden (örneğin; kolestiramin) en az 4 saat sonra alınmalıdır. Rifampisin (rifampin): Önceden rifampisinle (rifampin) tedavi edilen sağlıklı gönüllülere fluvastatin verildiğinde fluvastatinin biyoyararlanımı %50 oranında azalmıştır. Şu anda uzun vadeli rifampisin tedavisi gören (örneğin, tüberküloz tedavisi) hastalarda fluvastatinin lipid düzeylerini düşürme etkililiğinin değiştiğine ilişkin klinik bir kanıt olmamakla birlikte, lipid düzeylerinde yeterli bir düşüş sağlamak için fluvastatin dozunun uygun şekilde ayarlanması gerekebilir. Histamin H2-reseptör antagonistleri ve proton pompası inhibitörleri: Fluvastatinin simetidin, ranitidin ya da omeprazolle birlikte kullanımı fluvastatinin biyoyararlanımında bir artışa neden olur, ancak bu artış klinik açıdan anlamlı değildir. İlave etkileşme çalışmaları yapılmamış olmakla birlikte, diğer H2 reseptör antagonistleri / proton pompası inhibitörlerinin fluvastatinin biyoyararlanımını etkilemesi beklenmemektedir. Fenitoin: Fenitoinin fluvastatinin farmakokinetiği üzerindeki minimal etkisi, bu ilaçlar birlikte kullanıldığında fluvastatin dozunda ayarlama yapmanın gerekli olmadığını göstermektedir. Kardiyovasküler ajanlar: Fluvastatin propranolol, digoksin, losartan ya da amlodipin ile eş zamanlı olarak kullanıldığında, klinik olarak anlamlı farmakokinetik etkileşimler meydana gelmemektedir. Farmakokinetik verilere dayalı olarak, fluvastatin bu ajanlarla birlikte kullanıldığında herhangi bir izlem ya da doz ayarlaması gerekli değildir. Fluvastatinin diğer ilaçlar üzerindeki etkileriSiklosporin:Eş zamanlı olarak kullanıldıklarında, LESCOL (40 mg fluvastatin) ya da LESCOL XL'nin (80 mg fluvastatin) siklosporinin biyoyararlanımı üzerinde herhangi bir etkisi olmamıştır (ayrıca bkz. Diğer ilaçların fluvastatin üzerindeki etkileri). Kolşisinler: Fluvastatin ve kolşisinler arasındaki farmakokinetik etkileşmeye ilişkin herhangi bir bilgi mevcut değildir. Fakat, bu ilaçların eş zamanlı kullanımı ile kas ağrısı ve güçsüzlüğü ve rabdomiyoliz de dahil olmak üzere, anekdot olarak miyotoksisite bildirilmiştir. Fenitoin: Fluvastatin ile eş zamanlı kullanım sırasında fenitoin farmakokinetiğinde gözlenen değişimler genel olarak küçük ve klinik olarak anlamsız değişimlerdir. Bu nedenle, fluvastatin ile eş zamanlı kullanım sırasında fenitoin plazma düzeylerinin rutin olarak izlenmesi yeterlidir. Varfarin ve diğer kumarin türevleri: Sağlıklı gönüllülerde, fluvastatinin ve varfarinin (tek doz) birlikte kullanımı tek başına varfarin kullanımına kıyasla varfarinin plazma düzeylerini ve protrombin sürelerini olumsuz etkilememiştir. Ancak, fluvastatinle birlikte varfarin ya da diğer kumarin türevlerini kullanan hastalarda çok nadiren kanama epizotları ve/veya artmış protrombin süreleri bildirilmiştir. Varfarin ya da diğer kumarin türevlerini kullanan hastalarda fluvastatin tedavisine başlanırken, tedavi sonlandırılırken ya da dozunda değişiklik yapılırken protrombin sürelerinin izlenmesi önerilmektedir. Oral antidiyabetik ilaçlar: İnsüline bağımlı olmayan (tip 2) diyabet (NIDDM) için oral sülfonilüre (glibenklamid [gliburid], tolbutamid) tedavisi gören hastalarda, fluvastatin ilavesi glisemik kontrolde klinik olarak anlamlı değişikliklere yol açmamaktadır. Glibenklamid ile tedavi edilen NIDDM hastalarında (n=32), fluvastatin uygulaması (14 gün süresince günde iki kere 40 mg) glibenklamidin ortalama Cmax, EAA ve tı/2 değerlerini sırasıyla %50, %69 ve %121 oranında artırmıştır. Glibenklamid (günde 5 ila 20 mg) fluvastatinin ortalama Cmax ve EAA değerlerini sırasıyla %44 ve %51 oranında artırmıştır. Bu çalışmada, glukoz, insülin ve C-peptid düzeylerinde herhangi bir değişim gözlenmemiştir. Fakat, glibenklamid (gliburid) ve fluvastatin ile eş zamanlı tedavi gören hastalar fluvastatin dozu günde 80 mg'a çıkarıldığında uygun şekilde izlenmeye devam edilmelidir. Özel popülasyonlara ilişkin ek bilgilerÖzel popülasyonlara ilişkin hiçbir klinik etkileşim çalışması yürütülmemiştir.Pediyatrik popülasyon: Pediyatrik popülasyona ilişkin hiçbir klinik etkileşim çalışması yürütülmemiştir. 4.6. Gebelik ve laktasyonGenel tavsiyeGebelik kategorisi: X.Çocuk doğurma potansiyeli bulunan kadınlar/Doğum kontrolü (Kontrasepsiyon)Çocuk doğurma potansiyeline sahip kadınlar etkili bir doğum kontrol yöntemi uygulamalıdır.Fluvastatin gebelik döneminde uygulandığı takdirde ciddi doğum kusurlarına yol açtığından şüphelenilmektedir. LESCOL XL, gebelik döneminde kontrendikedir (bkz. Bölüm 4.3 Kontrendikasyonlar). Gebelik dönemiHMG-CoA redüktaz inhibitörleri, kolesterol ve muhtemelen kolesterolden türetilen diğer biyolojik olarak aktif maddelerin sentezini azalttığı için, hamile kadınlara verildiklerinde fetüse zarar verebilirler. Bu nedenle LESCOL XL, gebelik sırasında kontrendikedir.Bir hasta LESCOL XL kullanırken hamile kalırsa, tedavi sonlandırılmalıdır (bkz. Bölüm 4.3 Kontrendikasyonlar). Laktasyon dönemiLESCOL XL, emzirme döneminde kontrendikedir (bkz. Bölüm 4.3 Kontrendikasyonlar).Üreme yeteneği/FertiliteSıçanlarda yapılan ve dişilerde 0.6, 2 ve 6 mg/kg/gün, erkeklerde ise 2, 10 ve 20 mg/kg/gün doz düzeylerinin kullanıldığı bir çalışmada, fluvastatin fertilite ya da üreme performansı üzerinde herhangi bir advers etkiye yol açmamıştır (bkz. Bölüm 5.3 Klinik öncesi güvenlilik verileri).4.7. Araç ve makine kullanımı üzerindeki etkilerFluvastatinin araç ve makine kullanma yeteneği üzerindeki etkilerine ilişkin bilgi yoktur.4.8. istenmeyen etkilerEn yaygın olarak bildirilen advers ilaç reaksiyonları minör gastrointestinal semptomlar, uykusuzluk ve baş ağrısıdır.Advers reaksiyonlar, en sık gözlenenler ilk sırada olmak üzere, aşağıdaki sınıflama kullanılarak sıklıklarında göre sıralanmaktadır: çok yaygın (>1/10); yaygın (>1/100, <1/10); yaygın olmayan (>1/1000, <1/100); seyrek (>1/10.000, <1/1000); çok seyrek (<1/10.000) bilinmiyor (eldeki verilerden hareketle tahmin edilemiyor). Her bir sıklık grubunda, advers reaksiyonlar azalan bir ciddiyet sırasına göre listelenmektedir. 
Sinir sistemi hastalıklarıYaygın:Baş ağrısı. Çok seyrek: Temelde yatan hiperlipidemik bozukluklarla da ilişkili olduğu bilinen parestezi, distezi, hipostezi. Vasküler hastalıklarıÇok seyrek:Vaskülit. Gastrointestinal hastalıklarıYaygın:Hazımsızlık, karın ağrısı, bulantı. Çok seyrek: Pankreatit. Hepato-bilier hastalıklarıÇok seyrek:Hepatit. Deri ve deri altı doku hastalıklarıSeyrek:Döküntü, ürtiker gibi aşırı duyarlılık reaksiyonları. Çok seyrek: Diğer deri reaksiyonları (örneğin; egzama, dermatit, büllöz egzantem), yüzde ödem, anjiyoödem. Kas-iskelet bozukluklar ve bağ doku ve kemik hastalıklarıSeyrek:Miyalji, kas güçsüzlüğü, miyopati. Çok seyrek: Rabdomiyoliz, miyozit, lupus eritematöz benzeri reaksiyonlar. Pediyatrik hastalar: Fluvastatinin heterozigot kalıtsal hiperkolesterolemili çocuk ve adolesanlardaki iki klinik çalışmada değerlendirilen güvenlilik profili yetişkinlerde gözlenenle benzerlik göstermiştir. Her iki klinik çalışmada da, tüm çocuklar ve adolesanlarda normal bir gelişim ve cinsel olgunlaşma gözlenmiştir. Laboratuvar bulguları: HMG-CoA redüktaz inhibitörleri ve diğer lipid düşürücü ilaçlarla ilişkili olarak karaciğer fonksiyonunda biyokimyasal anormallikler gözlenmiştir. Az sayıda hastada (%1-2), transaminaz düzeylerinin normalin üst sınırının (NÜS) 3 mislinin üzerine çıktığı doğrulanmıştır. Çok az sayıda hastada (%0.3 ila %1.0), KK düzeylerinde 5 x NÜS'ün üzerinde belirgin yükselmeler gözlenmiştir. 4.9 Doz aşımı ve tedavisiHiperkolesterolemili 40 hastanın dahil edildiği plasebo kontrollü bir çalışmada, 2 hafta süresince LESCOL XL 80 mg tablet olarak verilen, 320 mg/gün'e kadar (her doz grubunda, n=7) dozlar iyi tolere edilmiştir. Aşırı doz tedavisi için spesifik bir öneride bulunulamaz. Aşırı doz durumunda, vaka semptomatik olarak tedavi edilmeli ve gerektiği şekilde uygun önlemler alınmalıdır.5. FARMAKOLOJİK ÖZELLİKLER5.1. Farmakodinamik özelliklerFarmakoterapötik grup: HMG-CoA redüktaz inhibitörleri ATC Kodu: C10AA04Fluvastatin tamamen sentetik kolesterol düşürücü bir ajan olup, HMG-CoA'nın kolesterol de dahil olmak üzere, sterollerin ön maddesi olan mevalonata dönüştürülmesinden sorumlu enzim, HMG-CoA redüktazın kompetitif bir inhibitörüdür. Fluvastatin ana etkisini karaciğerde göstermekte olup, biri farmakolojik aktiviteye sahip 2 eritro enansiyomerin rasemik bir karışımıdır. Kolesterol biyosentezinin inhibisyonu karaciğer hücrelerindeki kolesterolü azaltır ki bu LDL reseptörlerinin sentezini uyarıran ve böylelikle LDL partiküllerinin tutulumunu artırır. Bu mekanizmaların nihai sonucu plazma kolesterol konsantrasyonu azalır. LESCOL XL, primer hiperkolesterolemili ve karma dislipidemili hastalarda total kolesterol, LDL kolesterol, apolipoprotein-B ve trigliserid (TG) düzeylerinin düşürür ve HDL-kolestrolü artırır. Terapötik yanıt 2 hafta içerisinde iyi düzeyde sağlanır ve maksimum yanıt da tedavinin başlangıcını takiben 4 hafta içerisinde elde edilir ve kronik tedavi süresince sürdürülür. Primer hiperkolesterolemili ya da karma dislipidemili yaklaşık 1700 hastada gerçekleştirilen çok merkezli, çift kör, aktif kontrollü üç çalışmada, LESCOL XL 80 mg 24 haftalık süreçte yatmadan önce ya da günde iki kere verilerek LESCOL 40 mg ile karşılaştırılmıştır. Maksimum tedavi yanıtına erişildiğinde gözlenen yanıt oranları LESCOL 40 mg (ortalama LDL- kolesterol düşüşü: %26) ve LESCOL XL 80 mg (ortalama LDL- kolesterol düşüşü: %36) için Şekil 1'de gösterilmektedir. Şekil 14. haftada LDL- kolesterol'deki yüzde azalma kategorisine göre yanıt oranları (Karşılaştırmalı 3 yüksek doz çalışmasından elde edilen bulgular birleştirilmiştir)n ar ro y 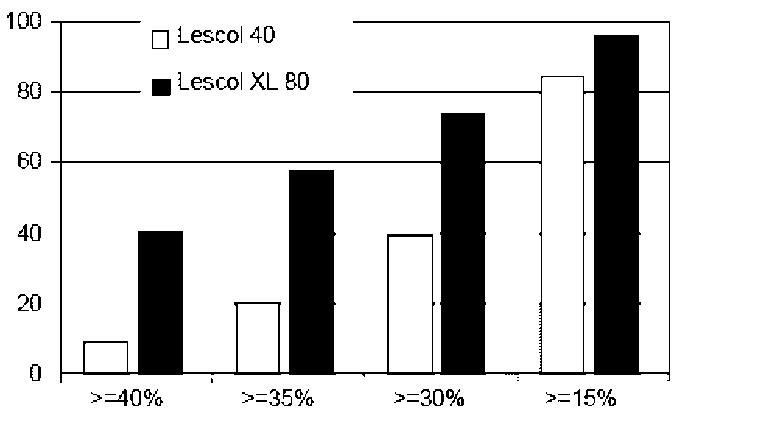 % LDL- kolesterol azalması
% LDL- kolesterol azalmasıBu çalışmalarda, LESCOL/LESCOL XL 24 haftalık tedavinin sonunda total- kolesterol, LDL- kolesterol, apolipoprotein-B ve trigliserid düzeylerini doza bağlı bir şekilde anlamlı olarak düşürmüş ve HDL- kolesterolü artırmıştır (Tablo 1). Tablo 1
LESCOL XL 80 mg'a randomize edilen 857 hastadan, >200 mg/dl başlangıç plazma trigliserit düzeyleri ile tanımlandığı üzere primer karma dislipidemisi (Fredrickson Tip Ilb) olan 271 hasta trigliserit düzeyinde ortalama %25'lik bir düşüş göstermiştir. Bu hastalarda, LESCOL XL HDL- kolesterolde %13 oranında anlamlı artışlar sağlamıştır. Bu etkinin başlangıçta çok düşük (yani, <35 mg/dl) HDL- kolesterol düzeylerine sahip olan ve HDL- kolesterolde %16'lık bir ortalama artış yaşayan hastalarda daha da belirgin olduğu görülmüştür. Ayrıca total-kolesterol, LDL-kolesterol ve apolipoprotein-B'de de anlamlı azalmalar sağlanmıştır (Tablo 2). Bu çalışmalara trigliserit düzeyi 400 mg/dl'nin üzerinde olan hastalar dahil edilmemiştir. Tablo 224 haftanın sonunda başlangıca göre gözlenen ortalama yüzde değişim (Primer Karma
Lipoprotein ve Koroner Ateroskleroz Çalışmasında (LCAS), koroner arter hastalığı ve hafif ila orta dereceli hiperkolesterolemisi olan (başlangıç LDL- kolesterol değeri: 115 - 190 mg/dl) erkek ve kadın hastalarda (35 ila 75 yaş arası) kantitatif koroner anjiyografi ile fluvastatinin koroner ateroskleroz üzerindeki etkisi değerlendirilmiştir. Bu randomize, çift kör, kontrollü klinik çalışmada, 429 hasta 40 mg/gün fluvastatin ya da plasebo ile tedavi edilmiştir. Kantitatif koroner anjiyogramlar başlangıçta ve 2.5 yıllık tedavinin sonunda değerlendirilmiştir. Fluvastatin tedavisi 2.5 yıllık süreçte, minimum lümen çapındaki değişim ile ölçüldüğü üzere (fluvastatin: -0.028 mm ve plasebo: -0.100 mm) koroner ateroskleroz lezyonlarının ilerlemesini 0.07 mm yavaşlatmıştır (-0.1222'den -0.022'ye tedavi farkı için %95 güven aralığı). LESCOL Girişim Önleme Çalışmasında (LIPS), çok farklı kolesterol düzeyleri (başlangıç TC: 3.5 ila 7.0 mmol/l) ve koroner kalp hastalığı olan kadın ve erkeklerde (18 ila 80 yaş arası) fluvastatinin majör istenmeyen kardiyak olaylar (MACE) üzerindeki etkisi değerlendirilmiştir. Bu randomize, çift kör, plasebo kontrollü çalışmada, 4 yıl süresince verilen günde 80 mg fluvastatin (N=844) ilk MACE riskini plaseboya (N=833) kıyasla anlamlı olarak %22 oranında (p=0.013) düşürmüştür. Bu faydalı etkiler özellikle diyabetli hastalarda ve çoklu damar hastalığı olan kişilerde dikkate değer bulunmuştur. Fluvastatin tedavisi kardiyak ölüm ve/veya miyokard infarktüsü riskini %31 oranında düşürmüştür (p=0.065). Pediyatrik hastalarİki açık etiketli doz titrasyon çalışmasında (ZA01 ve 2301), heterozigot kalıtsal hiperkolesterolemili toplam 113 çocuk ve adolesanda 2 yıllık bir tedavi sürecinde 20 ila 80 mg'lık dozlarda verilen fluvastatinin etkililiği ve güvenliliği incelenmiştir.Çalışmaya aşağıdaki şekilde tanımlanan heterozigot kalıtsal hiperkolesterolemi teşhisi konmuş 9 yaş ve üzerindeki hastalar dahil edilmiştir: LDL- kolesterol düzeyleri >190 mg/dl (4.9 mmol/l) ya da LDL-kolesterol düzeyleri >160 mg/dl (4.1 mmol/l) ve bir ya da daha fazla risk faktörü (ailede prematür koroner kalp hastalığı (CHD) geçmişi, sigara tiryakiliği, hipertansiyon, yüksek yoğunluklu lipoprotein kolesterolü (HDL-kolesterol) <35 mg/dl, diyabet) ya da kanıtlanmış LDL-kolesterol reseptörü deoksiribonükleik asit (DNA) defekti ve >160 mg/dl (4.1 mmol/l) LDL-kolesterol düzeyleri, <600 mg/dl serum trigliserit düzeyleri. Başlıca hariç tutulma kriterleri: homozigot kalıtsal hiperkolesterolemi; sekonder dislipoproteinemi formları; >600 mg/dl serum trigliserit düzeyleri; AST, ALT ya da kreatinin düzeyleri >1.5 x NÜS; serum KK ya da TSH >2 x NÜS; BMI >30 kg/m2. Fluvastatin tedavisine ilk hafta için 20 mg'lık dozda başlanmış ve LDL-kolesterol düzeylerinin >3.2 mmol/l ya da 3.4 mmol/l olması durumunda, doz sırasıyla 40 mg'a (6 hafta arayla) ve daha sonra 80 mg'a (iki kere 40 mg kapsül ya da 80 mg uzatılmış salımlı tablet) çıkarılmıştır. Fluvastatin 2 yıllık takip sürecinde total-kolesterol, LDL-kolesterol, apolipoprotein-B ve trigliserit plazma düzeylerini anlamlı olarak düşürmüş ve HDL-kolesterolü artırmıştır (bkz. Tablo 3). Tablo 3Fluvastatinin heterozigot kalıtsal hiperkolesterolemi çocuklarda ve adolesanlardaki lipid
Bu çalışmalar, çocuklarda statin tedavisine erken başlamanın kardiyovasküler sonuçlarına ilişkin çıkarımlarda bulunulmasına olanak vermemiştir. 5.2. Farmakokinetik özellikler Genel özelliklerFluvastatin sodyum, bir HMG-CoA redüktaz inhibitörüdür.Fluvastatin sodyum, beyaz ila soluk sarı arası renkli bir tozdur. Metanol, etanol ve suda çözünür. Emilim:Fluvastatin, çözeltinin gönüllülerde aç karnına oral yoldan uygulamasından sonra hızla ve tamamen (%98) emilmiştir. LESCOL XL 80'in oral yoldan uygulanmasından sonra fluvastatinin ortalama kalış süresi yaklaşık olarak 4 saat artarken, kapsüllerle karşılaştırıldığında, fluvastatinin emilim hızı yaklaşık %60 daha yavaş olmuştur. Tok karnına uygulandığında, ilaç daha düşük bir hızda emilmiştir. Dağılım:Fluvastatin asıl etkisini, metabolizmasında rol alan ana organ olan karaciğerde gösterir. Sistemik kan konsantrasyonlarıyla ölçülen mutlak biyoyararlanımı %24 düzeyindedir. İlacın görünen dağılım hacmi (Vz/f) 330 litredir. Dolaşımdaki ilacın %98'den fazlası plazma proteinlerine bağlanır ve bu bağlanma fluvastatin konsantrasyonundan ya da varfarin, salisilik asit ve gliburid varlığından etkilenmez. Biyotransformasyon:Fluvastatin esas olarak karaciğerde metabolize edilir. Kan dolaşımındaki önemli bileşenleri fluvastatin ve farmakolojik olarak inaktif olan N-desizopropil-propiyonik asit metabolitidir. Hidroksile metabolitler farmakolojik olarak aktiviteye sahiptirler ama sistemik olarak dolaşıma katılmazlar. Fluvastatinin insanlarda hepatik metabolizma yolu tam olarak aydınlatılamamıştır. Fluvastatin biyotransformasyonu için çeşitli alternatif sitokrom P450 (CYP450) yolları vardır ve bu nedenle fluvastatin metabolizması advers ilaç-ilaç etkileşimlerinin önemli bir nedeni olan CYP450 inhibisyonuna göreceli olarak duyarsızdır. Ayrıntılı birkaç in vitroçalışmada fluvastatinin yaygın CYP izoenzimleri üzerindeki inhibisyon potansiyeli araştırılmıştır. Fluvastatin, yalnızca CYP2C9 tarafından metabolize edilen bileşiklerin metabolizmasını inhibe etmektedir. Bu durumda diklofenak, fenitoin, tolbutamid ve varfarin gibi CYP2C9 substratı olan bileşikler ve fluvastatin arasındaki var olması gereken kompetitif etkileşim potansiyeline rağmen, klinik veriler bu etkileşimin olasılık dışı olduğunu göstermektedir.Eliminasyon:Sağlıklı gönüllülere 3H-fluvastatin uygulamasının ardından, radyoaktivitenin atılma oranı idrarda yaklaşık %6 ve feçeste %93 düzeyindedir ve atılan toplam radyoaktivitenin %2'sinden daha azından fluvastatin sorumludur. İnsanlarda fluvastatinin plazma klirensi (CL/f) 1.8 ± 0.8 l/dakika olarak hesaplanmıştır. Kararlı durum plazma konsantrasyonları, günlük 80 mg uygulamasından sonra fluvastatin birikimine ilişkin hiçbir belirti göstermemiştir. LESCOL 40 mg oral uygulamasından sonra, fluvastatinin terminal atılım yarılanma ömrü 2.3 ± 0.9 saattir. Fluvastatin akşam yemeği ile birlikte ya da akşam yemeğinden 4 saat sonra uygulandığında EAA değerlerinde anlamlı herhangi bir fark gözlemlenmemiştir. Hastalardaki karakteristik özelliklerFluvastatinin plazma konsantrasyonları genel popülasyonda yaş ya da cinsiyete bağlı olarak değişiklik göstermez. Ancak, kadınlarda ve yaşlı kişilerde tedaviye yanıtın arttığı gözlemlenmiştir.Fluvastatin, esas olarak biliyer yoldan elimine edildiği ve anlamlı düzeyde presistemik metabolizmaya maruz kaldığı için, karaciğer yetmezliği olan hastalarda ilaç birikimi potansiyeli söz konusudur (bkz. Bölüm 4.3 Kontrendikasyonlar ve Bölüm 4.4 Özel kullanım uyarıları ve önlemleri). 5.3. Klinik öncesi güvenlilik verileri Akut toksisiteFluvastatin yaklaşık oral LD50 düzeyi farelerde 2 g/kg'den daha büyük, sıçanlarda ise 0.7 g/kg'den daha büyüktür.Yinelenen doz toksisitesiFluvastatinin güvenliliği, sıçanlarda, tavşanlarda, köpeklerde, maymunlarda, farelerde ve hamsterlarda yürütülen toksisite çalışmalarında yoğun olarak araştırılmıştır. HMG-CoA redüktaz inhibitörleriyle ortak olan çeşitli değişiklikler, örneğin köpek, maymun ve hamsterlarda safra kesesi değişiklikleri, sıçanlarda tiroid ağırlığında artış ve hamsterlarda testis dejenerasyonu ile birlikte kemirgenlerde non-glandular mide hiperplazisi ve hiperkeratozu, köpeklerde katarakt, kemirgenlerde miyopati, çoğu laboratuar hayvanında hafif karaciğer değişiklikleri saptanmıştır. Bu sınıftan diğer bileşiklerle köpeklerde kaydedilen vasküler ve dejeneratif santral sinir sistemi değişiklikleri fluvastatinle gözlenmez.KarsinojeniteKesin bir maksimum tolere edilen dozun saptanması için sıçanlarda günde 6, 9 ve 18 mg/kg (1 yıl sonra günde 24 mg/kg'a yükseltilen) doz düzeylerinde bir karsinojenite çalışması yapılmıştır. Bu tedavi düzeyleri ile elde edilen plazma ilaç düzeyleri 40 mg oral dozdan sonra insandaki ortalama plazma ilaç konsantrasyonunun yaklaşık 9, 13 ve 26 ila 35 katı bulunmuştur. Günlük 24 mg/kg doz düzeyinde düşük insidansta ön mide skuamöz papillomları ve bir ön mide karsinomu gözlenmiştir. Ek olarak günde 18-24 mg/kg ile tedavi edilen erkek sıçanlarda tiroid foliküler hücre adenom ve karsinomları inisdansında artış kaydedilmiştir.Farelerde günde 0.3, 15 ve 30 mg/kg doz düzeylerinde yapılan karsinojenite çalışmasında sıçanda olduğu gibi dişi ve erkeklerde günde 30 mg/kg dozda ve dişilerde günde 15 mg/kg dozda ön mide skuamöz hücreli papillomlarda istatistiksel olarak anlamlı artış saptanmıştır. Bu tedavi düzeyleri ile elde edilen plazma ilaç düzeyleri 40 mg oral dozdan sonra insandaki ortalama plazma ilaç konsantrasyonunun yaklaşık 0.2, 10 ve 21 katı bulunmuştur. Sıçan ve farelerde gözlenen ön mide neoplazmaları, ilacın bir genotoksik etkisinden ziyade fluvastatine doğrudan temas maruziyetinin neden olduğu kronik hiperplaziyi yansıtmaktadır. Fluvastatin verilen erkek sıçanlarda tiroid foliküler hücre neoplazmalarının insidansının artması, diğer HMG-CoA redüktaz inhibitörlerindeki türe özgü bulgularla uyumlu gibi görünmektedir. Diğer HMG-CoA redüktaz inhibitörlerinden farklı olarak hepatik adenom ve karsinomlarda tedaviye bağlı artışlar gözlemlenmemiştir. MutajeniteAşağıdaki çalışmalarda,in vitro,Sal^^^ella typhimuriumEscherichiain vivomutajenite kanıtı bulunmamıştır.Üreme toksisitesiSıçanlarda yapılan ve dişilerde 0.6, 2 ve 6 mg/kg/gün, erkeklerde ise 2, 10 ve 20 mg/kg/gün doz düzeylerinin kullanıldığı bir çalışmada, fluvastatin fertilite ya da üreme performansı üzerinde herhangi bir advers etkiye yol açmamıştır. Sıçanlarda (1, 12 ve 36 mg/kg) ve tavşanlarda (0.05, 1 ve 10 mg/kg) yapılan teratoloji çalışmalarında yüksek doz düzeylerinde maternal toksisite gözlenmiş, ama embriyotoksik ya da teratojenik potansiyel ile ilgili herhangi bir kanıt bulunmamıştır. Dişi sıçanlara geç gebelik döneminde yavrular sütten kesilinceye kadar 12 ve 24 mg/kg/gün doz uygulamasının yapıldığı bir çalışmada, doğumda ya da doğuma yakın dönemde ve doğumdan sonra, fötal ve neonatal ölümlerin eşlik ettiği maternal mortalite gözlenmiştir. Düşük doz düzeyinde (2 mg/kg/gün) gebe dişiler ya da fetüsler üzerinde herhangi bir etki gözlenmemiştir.Geç gebelik ve erken laktasyon döneminde 2, 6, 12 ve 24 mg/kg/gün doz düzeylerinin uygulandığı ikinci bir çalışmada, 6 mg/kg/gün ve üzeri dozlarda kardiyotoksisiteye bağlı olarak benzer etkiler gözlenmiştir. Üçüncü bir çalışmada, gebe sıçanlara geç gebelik döneminde yavrular sütten kesilinceye kadar, eşzamanlı olarak mevalonik asit (kolesterol biyosentezi için gerekli olan bir HMG-CoA türevi) uygulanarak ya da uygulanmadan 12 ya da 24 mg/kg/gün doz uygulaması yapılmıştır. Eşzamanlı mevalonik asit uygulaması, kardiyotoksisiteyi ve maternal ve neonatal mortaliteyi tamamen önlemiştir. Bu nedenle, fluvastatin ile gözlenen maternal ve neonatal ölüm, gebelik döneminde farmakolojik etkinin abartılı olduğunu yansıtmaktadır. 6. FARMASÖTİK ÖZELLİKLER6.1. Yardımcı maddelerin listesi Mikrokristalize selüloz , hipromelloz/hidroksipropil metil selüloz, hidroksipropil selüloz, potasyum hidrojen karbonat/potasyum bikarbonat, povidon, magnezyum stearat, sarı demir oksit, titan dioksit, makrogol 8000. 6.2. GeçimsizliklerBilinen herhangi bir geçimsizliği bulunmamaktadır.6.3. Raf ömrü36 ay6.4. Saklamaya yönelik özel uyarılar30°C'nin altındaki oda sıcaklığında saklayınız. Tabletler kullanılana kadar blister paketin içerisinde tutulmalıdır.6.5. Ambalajın niteliği ve içeriğiPA/Alu/PVC blisterHerbirinde 7 yavaş salımlı tablet olan 4 adet çift taraflı alüminyum blisterler. 6.6. Beşeri tıbbi üründen arta kalan maddelerin imhası ve diğer özel önlemlerÖzel bir gereksinim yoktur.Kullanılmamış olan ürünler ya da atık materyaller Tıbbi Atıkların Kontrolü Yönetmeliği ve Ambalaj ve Ambalaj Atıklarının Kontrolü Yönetmeliğine uygun olarak imha edilmelidir. 7. RUHSAT SAHİBİNovartis Ürünleri 34912 Kurtköy - İstanbul Tel no: 0216 560 10 00 Faks no:0216 482 64 088. RUHSAT NUMARASI113/649. İLK RUHSAT TARİHİ / RUHSAT YENİLEME TARİHİİlk ruhsat tarihi: 26.02.2003Ruhsat yenileme tarihi: -10. KÜB'ÜN YENİLENME TARİHİ |
İlaç BilgileriLescol XL 80 mg kontrollü salımlı tabletEtken Maddesi: Fluvastatin sodyum Atc Kodu: C10AA04 Kullanma talimatı ve kısa ürün bilgileri
Google Reklamları
İlgili İlaçlar |
Ana Sayfa | Hakkımızda | İlaçlar | İlaç Ara | İlaç Firmaları | Gizlilik | Bize Ulaşın
Telif Hakkı 2008-2026 © İlaç Prospektüsü. Tüm Hakları Saklıdır.Uyarı: Sitemizde yayınladığımız ilaç bilgileri ile doktora danışmadan kesinlikle ilaç kullanmayınız!
Aksi halde doğabilecek sağlık sorunlarından ilacprospektusu.com sorumlu tutulamaz.