Lucrin Depot 1 Ay IM/SC 3.75 mg Kullanıma Hazır Toz ve Çözücü İçeren Çift Bölmeli Enjektör Kısa Ürün BilgisiAntineoplastik ve İmmünomodülatör Ajanlar » Hormonal Tedavi İlaçları » Hormonlar » Gonadotropin Salgılatıcı Hormon Analogları » Leuprorelin Asetat KISA URUNBILGISI1.BEŞERI TIBBI URUNUN ADILUCRİN DEPOT® 1 AY IM/SC 3.75 mg Kullanıma Hazır Toz ve Çözücü İçeren Çift Bölmeli Enjektör2.KALITATIF VE KANTİTATIF BİLEŞİMEtkin madde:Her bir flakonda etkin madde olarak 3.75 mg leuprolide asetat bulunur. Yardımcı maddeler:Yardımcı maddeler için bölüm 6.1'e bakınız. İçerikte bulunan mannitol hakkında uyarı için, ayrıca bkz: 4.4. 3.FARMASÖTIK FORMEnjeksiyon için liyofilize mikroküre toz içeren enjektörÖnceden doldurulmuş iki bölümlü bir enjektör içinde, seyreltici ile süspansiyon haline getirilmek üzere üretilmiş enjeksiyonluk liyofilize mikroküre tozdur. 4.KLINIK ÖZELLIKLER4.1 Terapötik endikasyonlarLUCRİN DEPOT®,Prostat KanseriLUCRİN DEPOT, hormonal müdahaleye uygun prostat kanserinde kullanılır.EndometriyozisLUCRİN DEPOT, altı aylık süreyle endometriyozis tedavisinde endikedir. Tek başına bir tedavi olarak veya cerrahiye ek olarak kullanılabilir.Uterus MiyomuLUCRİN DEPOT, uterus miyomu tedavisinde altı aya kadar olan bir süre için endikedir. Tedavi, miyomektomi veya histerektomi öncesinde preoperatif veya cerrahi istemeyen perimenopozal kadınlarda semptomatik düzelme sağlamaya yönelik olabilir.Meme KanseriLUCRİN DEPOT, hormon tedavisine uygun (östrojen ve/veya progesteron reseptörü pozitif) menopoz öncesi (premenopozal) veya menopoz sırasındaki (perimenopozal) kadınlarda görülen meme kanserinin tedavisinde endikedir. Santral Püberte Prekoks (gerçek erken püberte)LUCRİN DEPOT santral püberte prekoks (gerçek erken püberte - CPP) olan çocukların tedavisinde endikedir.Çocuklar aşağıdaki kriterler kullanılarak seçilmelidir: 1.Sekonder cinsel özelliklerin kızlarda sekiz yaşından önce ve erkeklerde dokuz yaşından önce başlamasıyla karakterize olan klinik CPP tanısı (idiyopatik veya nörojenik). 2.Klinik tanı tedaviye başlamadan önce doğrulanmalıdır: a Tanının GnRH stimülasyon testine pübertal bir yanıtla doğrulanması. Bu tayinin duyarlılığı ve metodolojisi anlaşılmalıdır. b. Kemik yaşının kronolojik yaşın bir yıl önünde olması. 3.Bazal değerlendirme aşağıdakileri de içermelidir: a.Boy ve ağırlık ölçümleri. b.Seks steroidi düzeyleri. c.Konjenital adrenal hiperplaziyi ekarte etmek için adrenal steroid düzeyi. d.Koriyonik gonadotropin salgılayıcı tümörü ekarte etmek için beta human koriyonik gonadotropin düzeyi e.Steroid salgılayan tümörü ekarte etmek için pelvis/adrenal/testis ultrasonu. f.İntrakraniyal tümör olasılığını ortadan kaldırmak için bilgisayarlı tomografi. 4.2 Pozoloji ve uygulama şekli GenelLUCRİN DEPOT bir doktor denetimi altında verilmelidir.Enjeksiyon şeklinde uygulanan diğer ilaçlarda olduğu gibi, enjeksiyon bölgesi periyodik olarak değiştirilmelidir. Sulandırılarak hazırlandıktan sonraki 24 saat boyunca süspansiyonun stabil kalmasına rağmen, ürünün içinde koruyucu madde olmamasından ötürü, süspansiyon hemen kullanılmadığı takdirde atılmalıdır. Pediyatrik PopülasyonSantral püberte prekoks tedavisi:LUCRİN DEPOT dozu her çocuk için bireysel olarak belirlenmelidir. Doz vücut ağırlığına göre mg/kg oranına göre belirlenmelidir. Daha küçük çocuklarda mg/kg oranında daha yüksek dozlar gerekir.Her dozaj formu için, tedaviye başlandıktan veya doz değiştirildikten bir iki ay sonra aşağı regülasyonu doğrulamak için GnRH stimülasyon testi, seks steroidleri ve Tanner evrelemesiyle çocuk izlenmelidir. Kemik yaşındaki ilerleme 6-12 ayda bir ölçümlerle izlenmelidir. Klinik açıdan ve/veya laboratuar parametreleri bakımından durumda hiç bir ilerleme görülmeyene kadar doz artırılmalıdır. Yeterli aşağı regülasyonla sonuçlandığı bulunan ilk dozla çocukların çoğunda tedavi süresince idame edilebilir. Ancak çok erken yaşlarda ve düşük dozlarda tedaviye başlanıldıktan sonra hastalar daha yüksek ağırlık kategorilerine doğru ilerleme göstereceğinden doz ayarlaması konusunda rehberlik edecek yeterli veri bulunmamaktadır. Tedavi esnasında ağırlığı anlamlı ölçüde artan hastalarda yeterli aşağı regülasyon olduğunun doğruluğunun kanıtlanması önerilir. Kızlarda 11 yaşından önce ve erkeklerde 12 yaşından önce LUCRİN DEPOTun kesilmesi göz önünde bulundurulmalıdır. Uygulama şekli:Prostat Kanseri, Endometriozis, Uterus Myomu ve Meme KanseriLUCRİN DEPOT 3.75 mg Kullanıma Hazır 1 Aylık Enjektör'ün prostat kanseri, endometriozis, uterus myomu ve meme kanseri için tavsiye edilen dozu bir seferde intramüsküler veya subkütan olarak uygulanan 3.75 mg'dır. Santral Püberte PrekoksBaşlangıç DozuLUCRİN DEPOT 3.75 mg Kullanıma Hazır 1 Aylık Enjektör'ün önerilen başlangıç dozu dört hafta için intramüsküler veya subkütan verilen 0.3 mg/kg dozudur (minimum 7.5 mg). Başlangıç dozu çocuğun ağırlığına göre aşağıdaki gibi belirlenir:
Not:Arzulanan toplam dozaja ulaşmak için iki enjeksiyon gerekiyorsa bunlar aynı zamanda uygulanmalıdır.İdame DozuHastanın vücut ağırlığına göre belirlenen başlangıç dozu ile toplam bir aşağı regülasyon sağlanamamışsa başlangıç dozu dört haftada bir 3.75 mg'lık basamaklarla yukarı doğru titre edilmelidir. Bu titrasyon işlemi sonucunda ulaşılan toplam doz idame dozu olarak kabul edilerek tedaviye dozla devam edilmelidir. Uygulama için hazırlamaÖnceden doldurulmuş çift bölmeli enjektörün en iyi performansı gösterebilmesi için aşağıdaki talimatları okuyunuz ve uygulayınız: 1.Enjeksiyonu hazırlamak için beyaz pistonu, en sondaki tıpa dönmeye başlayana kadar tıpanın içine vidalayınız.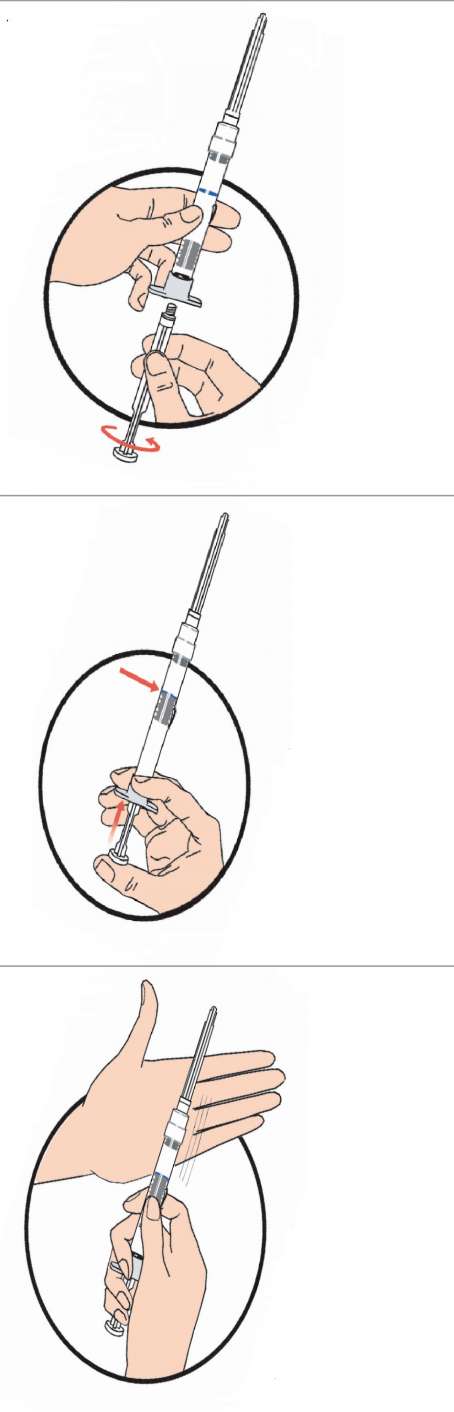 2.Enjektörü DİK KONUMDA tutunuz. Birinci tıpa haznenin ortasındaki mavi çizgiye gelene kadar pistonu yavaşça iterek (6 - 8 saniye) seyrelticiyi serbest bırakınız.3.Enjektörü DİK KONUMDA tutunuz. Homojen bir süspansiyon elde etmek üzere mikroküreleri yavaşça karıştırınız. Süspansiyon süt gibi görünecektir.4.Enjektörü DİK KONUMDA tutunuz. Diğer elinizle, iğneyi kılıfından çevirmeden çıkarınız.5.Enjektörü DİK KONUMDA tutunuz. Pistonu hafifçe iterek enjektördeki havayı çıkarınız.Not:Yanlışlıkla kan damarına girildiğinde, aspire olan kan iğne bağlantı bölümünün hemen altında görünür. Böyle bir durum olduğunda, iğnenin şeffaf kapağında kan görülebilir.Özel Popülasyonlara ilişkin Ek Bilgiler Böbrek/Karaciğer yetmezliğiBöbrek ve karaciğer yetmezliğinde kullanımı için herhangi bir veri yoktur.Geriyatrik PopülasyonYaşlı hastalarda kullanımına dair herhangi bir veri yoktur.4.3Kontrendikasyonlar-Etkin madde leuprolide asetata veya benzer nonapeptidlere ya da yardımcı maddelerden herhangi birine karşı aşırı duyarlılığı olduğu bilinen hastalarda,-Kesin tanısı konmamış vajinal kanamalı hastalarda, -Gebelikte kontrendikedir. 4.4Özel kullanım uyarıları ve önlemleriUYARILAR ve ÖNLEMLER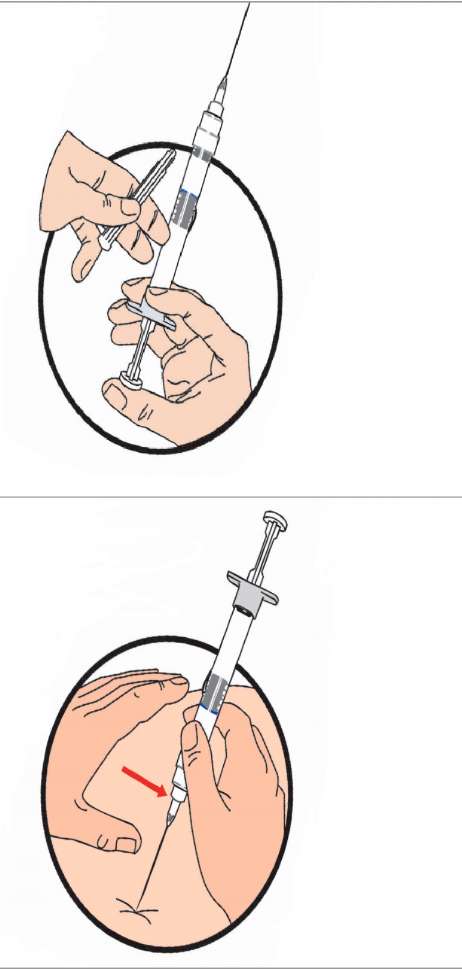 |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
Kadınlardaki yan etkilerin özeti | ||
Sistem, Organ Sınıfı |
Sıklık |
Yan etkiler |
|
Enfeksiyonlar |
Yaygın |
Vajinit |
|
Psikiyatrik rahatsızlıklar |
Yaygın |
Depresyon Libido azalması |
|
Üreme sistemi ve göğüs rahatsızlıkları |
Yaygın |
Göğüs ağrısı Göğüs hassasiyeti Göğüs boyutlarında küçülme Vajinal kuruluk |
|
|
Seyrek |
Cinsel ilişki sırasında ağrı |
|
Genel rahatsızlıklar ve uygulama bölgesi sorunları |
Seyrek |
Tahriş |
|
| ||
Erkeklerdeki yan etkilerin özeti | ||
Sistem, Organ Sınıfı |
Sıklık |
Yan etkiler |
|
Psikiyatrik rahatsızlıklar |
Seyrek |
Libido azalması |
|
Üreme sistemi ve göğüs rahatsızlıkları |
Yaygın |
Testis atrofisi Erektil disfonksiyon |
|
|
Seyrek |
Jinekomasti |
Genel yan etkilerin özeti | ||
Sistem, Organ Sınıfı |
Sıklık |
Yan etkiler |
|
Kan ve lenf sistemi rahatsızlıkları |
Seyrek |
Lökopeni Anemi Trombositopeni Eritrositoz |
|
Bağışıklık sistemi rahatsızlıkları |
Seyrek |
Anafilaktik reaksiyon |
|
Metabolizma ve beslenme rahatsızlıkları |
Seyrek |
Şeker hastalığı Hiperkalemi Anoreksi Yeme bozuklukları |
|
Psikiyatrik rahatsızlıklar |
Yaygın Seyrek |
Ruh hali değişiklikleri Uykusuzluk |
|
Sinir sistemi rahatsızlıkları |
Yaygın |
Baş ağrısı Baş dönmesi |
|
|
Seyrek |
Parestezi Zihinde karışıklık |
|
Kulak ve labirent rahatsızlıkları |
Seyrek |
İşitme kaybı Çınlama |
|
Kalp rahatsızlıkları |
Seyrek |
Anjina pektoris Taşikardi Aritmi |
|
Vasküler rahatsızlıklar |
Yaygın |
Sıcak basması |
|
|
Seyrek |
İskemi Hipertansiyon |
|
Solunum, torasik ve mediastinal rahatsızlıklar |
Yaygın |
Dispne |
|
Mide ve barsak rahatsızlıkları |
Yaygın |
Kusma Bulantı |
|
|
Seyrek |
İshal Kabızlık Stomatit Ağızda kuruluk |
|
Karaciğer ve safra rahatsızlıkları |
Seyrek |
Sarılık |
|
Deri ve deri altı doku rahatsızlıkları |
Yaygın |
Döküntü Akne Terleme |
|
|
Seyrek |
Dermatit Kaşıntı Hirsutizm Alopesi Tırnak bozuklukları |
|
Müsküloskeletal, bağ dokusu ve kemik rahatsızlıkları |
Yaygın |
Miyalji Artropati |
|
|
Seyrek |
Müsküloskeletal ağrı Bel ağrısı Kemik ağrısı Eklem ağrısı Kas sertleşmesi |
|
Renal ve üriner rahatsızlıklar |
Seyrek |
Miktürisyon bozuklukları Sık idrara çıkma Hematüri |
|
Genel rahatsızlıklar ve uygulama bölgesi sorunları |
Yaygın |
Ağrı Ödem Halsizlik Yorgunluk Enjeksiyon bölgesinde ağrı, iltihap, steril apse, skleroz ve hematom gibi lokal reaksiyonlar |
|
|
Seyrek |
Göğüste baskı hissi Ateş Üşüme Susama |
|
Diğer |
Seyrek |
EKG değişiklikleri Hepatik değerlerde transaminaz ve fosfataz artışı gibi değişiklikler Bilirubin, trigliserid ve ürik asid değerlerinde artış, Kilo alma |
Pazarlama Sonrası Gözlem
Leuprolide asetat enjeksiyonun bu ya da başka formülasyonları ile aşağıdaki yan etkiler gözlenmiştir. Leuprolidin birden çok endikasyonu, dolayısıyla birden çok hasta popülasyonu olduğu için, bu yan etkilerin tümü her hastada görülmeyebilir. Bu yan etkilerin çoğunluğu kullanılan ilaç ile ilişkilendirilmemiştir.Tüm vücut:
Abdomen genişlemesi, asteni, üşüme, ateş, genel ağrı, baş ağrısı, enfeksiyon, enflamasyon, fotosensitivite, şişme (temporal kemik), sarılıkKardiyovasküler sistem:
Anjina, bradikardi, kalp ritim bozukluğu, konjestif kalp yetersizliği, EKG değişiklikleri/ iskemi, hipertansiyon, hipotansiyon, üfürüm, miyokard enfarktüsü, flebit, akciğer embolisi, inme/geçici hafıza kaybı, taşikardi, trombosis, geçici iskemik atak, varisSindirim sistemi:
Kabızlık, diyare, ağız kuruluğu, duodenum ülseri, disfaji, gastrointestinal kanama, gastrointestinal bozukluk, hepatik disfonksiyon, iştah artışı, anormal karaciğer fonksiyon testleri, bulantı, peptik ülser, rektal polipler, susama, kusmaEndokrin sistem:
Diyabet, tiroid büyümesiKan ve lenf sistemi:
Anemi, ekimoz, lenfödem, protrombin zamanı artışı, parsiyel tromboplastin zamanı artışı, trombositopeni, lökopeni, lökositozMetabolizma ve beslenme:
BUN artışı, kalsiyum artışı, kreatinin artışı, dehidratasyon, ödem, hiperlipidemi (toplam kolesterol, LDL - kolesterol, trigliserid), hiperfosfatemi, hipoglisemi, hipoproteinemi, potasyum düşüşü, ürik asit artışı, bilirubin artışıKas ve iskelet sistemi:
Ankilozan spondilit, eklem bozuklukları, eklem ağrısı, miyalji, pelvik fibroz, omurga kırıkları, felç, tenosinovit semptomlarıSinir sistemi:
Anksiyete, delüzyonlar, depresyon, sersemlik, hipoestezi, uykusuzluk, letarji, libido artışı, baş dönmesi, hafıza bulanıklığı, ruh hali değişiklikleri, sinirlilik, nöromüsküler bozukluklar, uyuşukluk, parestezi, periferal nöropati, uyku bozuklukları, konvülsiyonSolunum sistemi:
Öksürük, dispne, burun kanaması, hemoptizi, farenjit, plevral efüzyon, plevral friksiyon, pnömoni, akciğer fibrozu, akciğer infiltrasyonu, solunum bozuklukları, sinüs konjesyonu, İntersitisyel akciğer hastalığıDeri ve ekleri:
Cilt/ kulak karsinomu, dermatit, kuru cilt, kıllanma, kıl ve saç kaybı, gırtlakta sert nodül, pigmentasyon, kaşıntı, raş, cilt lezyonları, ürtikerDuyu organları:
Anormal görme, ambliyopi, bulanık görme, göz kuruluğu, duyma bozukluğu, oftalmolojik bozukluklar, tat alma bozuklukları, kulak çınlamasıUrogenital sistem:
Mesane spazmları, göğüs ağrısı, göğüs hassasiyeti, jinekomasti, hematüri, inkontinans, anormal ve sürekli vajinal kanama dahil olmak üzere menstrual bozukluklar, penis şişmesi, penis bozuklukları, prostat ağrısı, testis atrofisi, testis ağrısı, testis boyutunda azalma, üriner bozukluklar, sık idrar yapma, üriner obstrüksiyon, üriner kanal enfeksiyonu, aciliyetİzole anafilaksi vakaları raporlanmıştır.
Ağrı, enflamasyon, steril apse, endurasyon ve hematom dahil olmak üzere enjeksiyon yeri reaksiyonları görülmüştür.
GnRH analogları ile prostat kanseri tedavisi gören hastalarda çok seyrek olarak intihar düşüncesi ve girişimleri raporlanmıştır.
Bu sınıftaki diğer ajanlar gibi, pituiter adenomu olan hastalarda ilk kullanım sonrasında çok seyrek de olsa pituiter apopleksi raporlanmıştır.
Kadınlar :
Derin ven trombozu, pulmoner emboli, miyokard enfarktüsü, inme ve geçici iskemik atak vakaları da dahil olmak üzere çeşitli ciddi venöz ve arteriyal tromboemboli vakaları bildirilmiştir. Bazı vakalarda zamansal ilişkiler bildirilmiş olsa da, vakaların çoğuna risk faktörleri ya da eşzamanlıilaç kullanımı neden olmaktadır. GnRH agonistlerinin kullanımıyla bu olaylar arasında bir neden-sonuç ilişkisi olup olmadığı bilinmemektedir.
4.9. Doz aşımı ve tedavisi
Klinik uygulamada, leuprolide asetat depo süspansiyonu ile doz aşımı görülmemiştir. Tavsiye edilen tedavi dozunun yaklaşık 133 katına kadar dozların uygulandığı hayvan çalışmalarında, dispne, aktivite azalması ve enjeksiyon yerinde lokal iritasyon görülmüştür. Doz aşımı durumunda hasta yakından izlenmeli ve semptomatik ve destekleyici tedavi uygulanmalıdır.5. FARMAKOLOJİK ÖZELLİKLER
5.1. Farmokodinamik özellikler
Farmakoterapötik grup: Gonadotropin serbestleştirici hormon (GnRH) analogları ATC Kodu: L02AE02Lucrin Depot, intramüsküler veya subkütan enjeksiyon olarak kullanılan leuprolide asetatın steril liyofilize mikrosferlerinden oluşmuştur. Lucrin Depot 'un etkin maddesi olan leuprolide asetat, doğal olarak oluşan gonadotropin serbestleştirici hormonun (GnRH veya LH-RH) sentetik, nonapeptid bir analogudur. Analogu doğal hormondan daha güçlü bir etki yapar.
Bir GnRH agonisti olan leuprolide asetat sürekli olarak ve terapötik dozlarda verildiğinde, gonadotropin sekresyonunun güçlü bir inhibitörüdür. Hayvan ve insan çalışmaları, başlangıçtaki stimülasyonu takiben leuprolide asetatın kronik uygulanmasının over ve testislerin steroidogenezinde supresyonla sonuçlandığını göstermiştir. Bu etki tedavinin kesilmesiyle birlikte geri dönüşümlüdür.
Leuprolide asetat uygulaması, hormona bağlı belirli tipteki tümörlerin (Nobel ve Dunning erkek sıçanlarda prostat tümörlerinin ve DMBA ile uyarılmış dişi sıçanlarda meme tümörlerinin) büyümesinin inhibisyonu ve üreme organlarının atrofisi ile sonuçlanır.
İnsanlarda leuprolide asetat uygulanması başlangıçta luteinizan hormon (LH) ve folikül stimülan hormonun (FSH) dolaşımdaki düzeylerinin artmasına, ve dolayısıyla gonadal steroidlerin düzeylerinde (erkeklerde testosteron ve dihidrotestosteron ve pre-menopozal kadınlarda östron ve östradiol) geçici bir artışa neden olur.
Ancak, leuprolide asetatın sürekli uygulanması, LH ve FSH ve seks steroidlerinin düzeylerinde düşmeyle sonuçlanır. Erkeklerde, testosteron kastrasyon veya prepuberte düzeylerine iner. Pre-menopozal kadınlarda östrojenler post-menopozal düzeylere iner. Söz konusu hormonal değişimler, önerilen dozlarda ilaç tedavisine başlandıktan sonra bir ay içinde gerçekleşir.
5.2 Farmakokinetik Özellikleri
Genel özellikler
Leuprolide asetat oral yoldan verildiğinde aktif değildir. Bu ajanın subkutan uygulama sonrasındaki biyoyararlanımı intramüsküler uygulama sonrasındaki biyoyararlanım ile kıyaslanabilir orandadır.
Emilim:
Prostat karsinomlu hastalarına LUCRİN DEPOT'un tek bir 3.75 mg dozunda subkutan ve intramuskuler yoldan uygulanmasıyla, bir ayın sonunda 0.7 ng/ml'lik ortalama leuprolide asetat plazma konsantrasyonları elde edilmiştir. İlaç birikimine ilişkin bir gösterge yoktur.Menopoz öncesi (pre-menopozal) meme kanseri olan 11 hastada 12 hafta süreyle leuprolide asetat 3.75 mg'ın serum düzeyleri ölçülmüştür. 4 hafta sonra ortalama leuprolide asetat düzeyleri 0.1 ng/ml'den yüksektir ve 8. ve 12. haftalardaki enjeksiyonlardan sonra da stabil kalmıştır. İlaç akümülasyon eğilimi göstermemiştir.
Dağılım:in vitro bağlanma oranı %43 ile %49 arasındadır.
Metabolizma:
Sağlıklı erkek gönüllülerde intravenöz olarak verilen 1 mg bolus leuprolidein ortalama sistemik klerensi 7.6 litre/saat olup terminal eliminasyon yarı-ömrü iki kompartmanlı bir modele göre ortalama üç saattir.Hayvan çalışmaları radyoaktif karbon 14 (14C) işaretli leuprolidin daha sonra yeniden katabolize edilen küçük inaktif peptidlere, bir pentapeptid (Metabolit I) tripeptid (Metabolit II ve III) ve bir dipeptid (Metabolit IV)'e metabolize olduğunu göstermiştir. Bu fragmanlar daha ileri metabolizasyona uğrayabilir.
Leuprolide Asetat Depo Süspansiyon verilen beş prostat kanseri hastasında ölçülen majör metabolitin (M-I) plazma konsantrasyonları dozdan iki ile altı saat sonra maksimuma erişmiş ve doruk ana ilaç konsantrasyonunun yaklaşık %6'sma ulaşmıştır. Dozdan bir hafta sonra ortalama M-I konsantrasyonları, ortalama leuprolide konsantrasyonlarının yaklaşık %20'si kadardır.
Atılım:
LUCRİN DEPOT 3.75 mg'ın üç hastadaki uygulamasını takiben, dozun %5'inden azı ana bileşik ve M-I metaboliti olarak 27 günde idrarla atılmıştır.
Hastalardaki karakteristik özellikler
Böbrek/Karaciğer yetmezliği
İlacın böbrek yetmezliği olan hastalardaki farmakokinetiği belirlenmemiştir. İlacın karaciğer yetmezliği olan hastalardaki farmakokinetiği belirlenmemiştir.
5.3 Klinik öncesi güvenlilik verileri
Karsinojenez ve mutajenez, fertilitede bozukluk
Sıçanlarda ve farelerde iki yıllık bir karsinojenesite çalışması yürütülmüştür. Sıçanlarda ilaç subkütan olarak yüksek dozlarda (0.6 ile 4 mg/kg) verildiğinde 24 ayda selim pitüiter hiperplazide ve selim pitüiter adenomlarda doza-bağlı artış saptanmıştır. Dişilerde pankreas adacık hücre adenomlarında ve erkeklerde testiküler interstisyel hücre adenomlarında doza-bağlı olmayan, ancak anlamlı bir artış olmuştur (düşük doz grubunda en yüksek insidans).
Farelerde iki yıl boyunca 60 mg/kg gibi yüksek bir dozda leuprolide asetata bağlı tümörler veya pitüiter anormallikler gözlenmemiştir. Hastalar üç yıla kadar olan sürelerle leuprolidee asetat ile 10 mg/gün gibi yüksek dozlarla ve iki yıl süreyle 20 mg/gün gibi yüksek dozlarla tedavi edildiğinde, demonstre edilebilen pitüiter anormallikler ortaya çıkmamıştır.
Leuprolide asetat ile bakteriyel ve memeli sistemleri kullanılarak mutajenesite çalışmaları gerçekleştirilmiştir. Bu çalışmalar mutajenik potansiyele ilişkin kanıtlar sağlamamıştır.
Erişkinlerde leuprolide asetat ve benzer analoglar ile yapılan klinik ve farmakolojik çalışmalarda, 24 haftaya kadar sürelerle sürekli uygulandıktan sonra ilacın kesilmesiyle fertilite süpresyonunun tümüyle geri döndüğü gösterilmiştir. Gebelik, üreme yeteneği ve üreme
Gebeliklerinin 6. gününde tavşanlara uygulanan 0.00024, 0.0024 ve 0.024 mg/kg (en yüksek insan dozunun 1/300 ila 1/3'sı) dozlarda, majör fetal anomalilerde doz-bağımlı bir artış ortaya koymuştur. Sıçanlarla yürütülen benzer çalışmalar fetal malformasyonlarda artış göstermemiştir. Leuprolide asetat aylık formülasyonunun ilk iki yüksek dozuyla tavşanlarda ve en yüksek dozuyla sıçanlarda fetal mortalitede artış ve fetüs ağırlığında düşme olmuştur. Fetal mortalite üzerindeki etkiler, bu ilacın hormon düzeylerinde yarattığı değişikliğin mantıklı bir sonucudur. Dolayısıyla, ilacın gebelik sırasında uygulanmasında spontan düşük oluşması ihtimali mevcuttur.
Çocuklarda fertilitenin süpresyonunun tam olarak geri dönüşlü olup olmadığını değerlendirmek için klinik çalışmalar tamamlanmamış olmakla birlikte hayvan çalışmaları (puberte öncesi ve erişkin sıçanlar ve maymunlar) leuprolide asetat ve diğer GnRH analoglarıyla fonksiyonun geri dönüşlü olduğunu göstermiştir. Ancak, leuprolide asetatla yapılan bir çalışmayı takiben, immatür sıçanlarda dozun kesilmesinden sonraki dönemde testislerde tübüler dejenerasyon görülmüştür. Histolojik düzelme olmamasına rağmen tedavi edilen erkekler kontrol grubundakiler kadar fertildir. Aynı protokolün izlendiği dişi sıçanlarda da histolojik değişimler gözlenmemiştir. Her iki cinsiyette, tedavi edilen hayvanların yavruları normal gözükmektedir. Anne babaya uygulanan tedavinin F1 jenerasyonunun üreme performansı üzerindeki etkisi test edilmemiştir. Söz konusu bulguların klinik anlamlılığı bilinmemektedir.
Çocuklardaki klinik çalışmalar
Santral puberte prekoksu (CPP) olan çocuklarda, stimüle olmuş ve bazal gonadotropinler, prepubertal düzeylere düşer. Devamında testosteron ve östradiol, erkek ve kızlarda prepubertal düzeylere düşer. Gonadotropinlerin azalması, normal fiziksel ve psikolojik büyüme ve gelişime izin verir. Leuprolide asetatın kesilmesini takiben gonadotropinler pubertal düzeylere geri döndüğünde doğal olgunlaşma gelişir.
Bu hasta populasyonunda uzun süreli leuprolide asetat uygulaması ile aşağıdaki fizyolojik etkiler bildirilmiştir.
1.İskelet yapısında büyüme:
Epifizler erken kapanmayacağından ötürü, vücut boyunda ölçülebilir bir artış olduğu farkedilebilir.
2.Organ Büyümesi:
Üreme organları prepubertal döneme geri dönecektir.
3.Adet görme:
Adet görülüyorsa kesilecektir.
Santral puberte prekoksu olan 22 çocuk ile yapılan bir çalışmada LUCRİN DEPOT, dört haftada bir verildi ve plazma leuprolide asetat düzeyleri aşağıdaki Tablo 1'de özetlendiği üzere ağırlık kategorilerine göre saptandı.
Tablo 1
Hasta Ağırlık Ağırlığı (kg) |
Grup Ağırlık Ortalaması (kg) |
Doz (mg) |
Vadi Plazma Leuprolide Düzeyi OrtalamasıSS** (ng/mL)* |
|
20.2 - 27.0 |
22.7 |
7.5 |
0.77 ± 0.33 |
|
28.4 - 36.8 |
32.5 |
11.25 |
1.25 ±.06 |
|
39.3 - 57.5 |
44.2 |
15 |
1.59 ± 0.65 |
Hafta 12 ve 24'deki ilaç düzeyleri, 4 haftalık düzeye benzerdi. ** SS: Standart sapma
FARMASÖTİK ÖZELLİKLER
6.1 Yardımcı maddelerin listesi
Liyofilize tozun hazırlanmasında kullanılan yardımcı maddeler:
BileşenlerMiktar/Enjektör
Jelatin0.65 mg
DL laktik asid/glikolik asid ko-polimeri33.10 mg (75:25) moleküler ağırlığı: 10000
Mannitol6.60 mg
Seyrelticinin hazırlanmasında kullanılan yardımcı maddeler:
Miktar/Enjektör
5.0 mg 50.0 mg 1.0 mg 1.0 ml'ye kadar
Bileşenler
Sodyum karboksimetilselüloz
Mannitol
Polisorbat 80
Enjeksiyonluk su
6.2 Geçimsizlikler
Böyle bir bilgi mevcut değildir.6.
6.3Raf ömrü
2 yıl6.4Saklamaya yönelik özel tedbirler
LUCRİN DEPOT Kullanıma Hazır Enjektörler, 25 °C'nin altındaki oda sıcaklığında saklanmalıdır. Dondurmayınız.Hazırlandıktan sonra süspansiyonun 24 saat süreyle stabil olduğu gösterilmiş olmakla birlikte ürünün içinde koruyucu madde bulunmadığından süspansiyon hemen kullanılmadığı takdirde atılmalıdır.
6.5Ambalajın niteliği ve içeriği
Liyofilize toz ve seyreltici çözeltisi, Tip I cam'dan (Avr. Farm) yapılmış iki bölümlü bir enjektör içinde ambalajlanmıştır.6.6Beşeri tıbbi üründen arta kalan maddelerin imhası ve diğer özel önlemler
Geçerli değil.7.RUHSAT SAHİBl
Abbott Laboratuarları İth. İhr. ve Tic. Ltd. Şti. Ekinciler Caddesi Hedef Plaza No: 3 34810 Kavacık - Beykoz İstanbulTel : 0216 538 74 00 Faks : 0216 425 85 37
8.RUHSAT NUMARASI:
122/119.İLK RUHSAT TARİHİ/RUHSAT YENİLEME TARİHİ:
07.03.2007 / -10.KUB'UN YENİLENME TARİHİ
İlk onay tarihi: 21.12.2009 Yenilenme tarihi:İlaç Bilgileri
Lucrin Depot 1 Ay IM/SC 3.75 mg Kullanıma Hazır Toz ve Çözücü İçeren Çift Bölmeli Enjektör
Etken Maddesi: Leuprolide
Atc Kodu: L02AE02
Kullanma talimatı ve kısa ürün bilgileri
Google Reklamları
Ana Sayfa | Hakkımızda | İlaçlar | İlaç Ara | İlaç Firmaları | Gizlilik | Bize Ulaşın
Telif Hakkı 2008-2026 © İlaç Prospektüsü. Tüm Hakları Saklıdır.Uyarı: Sitemizde yayınladığımız ilaç bilgileri ile doktora danışmadan kesinlikle ilaç kullanmayınız!
Aksi halde doğabilecek sağlık sorunlarından ilacprospektusu.com sorumlu tutulamaz.