Survanta İntratrakeal Süspansiyon Kısa Ürün BilgisiSolunum Sistemi » Diğer Solunum Sistemi İlaçları » Diğer » Akciğer Sürfaktanı » Doğal Fosfolipidler KISA URUN BILGISI 1. BEŞERI TIBBI ÜRÜNÜN ADISURVANTA İntratrakeal Süspansiyon2. KALITATIF VE KANTİTATIF BILEŞIMEtkin Madde: beraktant1.0 mL 'deToplam Fosfolipidler 25 mg Bovin Akciğer Lipidleri (ABD akciğerleri) q.s.* Bovin Akciğer Lipidleri (Yeni Zelanda yetişkin akciğerleri) Bovin Akciğer Lipidleri (Yeni Zelanda yenidoğan (buzağı), akciğerleri) kullanılır. Disatüre Fosfatidilkolin 11 - 15.5 mg Dipalmitoil fosfatidilkolin (L-Alfa), İngiltere kullanılır. q.s* Serbest Yağ Asidleri 1.4 - 3.5 mg Palmitik asid, UK kullanılır q.s.* Trigliseridler 0.5 - 1.75 mg Tripalmitin, UK kullanılır q.s.* Protein 0.1-1.0 mg/ml Yardımcı maddeler için 6.1'e bakınız. 3. FARMASÖTIK FORMSteril intratrakeal süspansiyon4. KLİNIK ÖZELLIKLER4.1 Terapötik endikasyonlarSURVANTA, prematüre bebeklerde, Respiratuvar Distres Sendromun (RDS) (hiyalin membran hastalığı) önlenmesinde ve tedavisinde ("kurtarma") endikedir. Survanta, RDS insidansını, RDS 'ye bağlı mortaliteyi ve hava kaçağı komplikasyonlarını belirgin olarak azaltır. Önleme: Doğum ağırlığı 1250 gramın altında olan ya da surfaktan yetmezliği bulunan prematüre bebeklerde Survanta, mümkün olduğu kadar çabuk, tercihen doğumdan sonra ilk 15 dakika içinde uygulanır.Kurtarma: RDS'si röntgenle teyit edilmiş ve mekanik ventilasyona ihtiyaç gösteren bebekleri tedavi etmek için mümkün olduğu kadar çabuk, tercihen doğumdan sonra ilk 8 saat içinde SURVANTA uygulanır.4.2 Pozoloji ve Uygulama Şekli Yalnızca intratrakeal kullanım içindir. Pozoloji/uygulama sıklığı ve süresi: SURVANTA entübasyon, ventilatör kullanımı ve prematüre bebek bakımı konusunda deneyimli hekimler tarafından ya da onların gözetiminde uygulanmalıdır. SURVANTA'nın uygulanımından sonraki dakikalar içinde oksijenasyonda belirgin iyileşmeler görülebilir. O nedenle hiperoksiyi önlemek için sistemik oksijenasyonun izlenmesi, sık ve özenli bir klinik gözetimin yapılması gereklidir. SURVANTA uygulanımından önce, doz ve uygulama yöntemlerini anlatan görsel - işitsel materyallerin gözden geçirilmesi önerilir. Materyaller Abbott Laboratuarları'ndan temin edilebilir. Önerilen doz aşağıdaki gibidir: SURVANTA'nın her dozu, doğum ağırlığı başına 100 mg fosfolipittir (4 ml/kg). SURVANTA DOZ CETVELİ değişik doğum ağırlıklarına ait dozları göstermektedir.
Özel Popülasyonlara İlişkin Ek Bilgiler Pediyatrik popülasyon Kullanma Talimatı Uygulamadan önce, renk değişikliği açısından SURVANTA gözle kontrol edilmelidir. SURVANTA 'nın rengi beyazımsı - açık kahverengidir. Saklama sırasında çökelti oluştuysa, dispersiyonu sağlamak için flakon yavaşça döndürülmelidir (ÇALKALAMAYINIZ). İşlemler sırasında yüzeyde biraz köpüklenme oluşabilir, bu ürünün doğal bir özelliğidir. SURVANTA, buzdolabında saklanır (2 0 - 8 0C). Uygulamadan önce, SURVANTA, oda sıcaklığında en az 20 dakika bırakılarak ya da elde en az 8 dakika tutularak ısıtılmalıdır. Yapay ısıtma yöntemleri kullanılmamalıdır. Önleyici doz verilecekse SURVANTA'nın hazırlanmasına bebeğin doğumundan önce başlanmalıdır. Oda sıcaklığında bekletilmiş olan, açılmamış ve kullanılmamış SURVANTA flakonları, ısıtma işleminden sonraki 24 saat içinde yeniden buzdolabına konarak ilerde kullanılabilir. SURVANTA 24 SAATTEN DAHA UZUN SÜRE BUZDOLABINDAN UZAKLAŞTIRILMAMALIDIR. İLACIN ODA SICAKLIĞINDA ISITILIP YENİDEN BUZDOLABINA KONMA İŞLEMİ BİR DEFAYI AŞMAMALIDIR. Bir defalık kullanıma mahsus SURVANTA flakonlarının her biri yalnızca bir defa kullanılmalıdır. İçinde ilaç kalmış olan flakonlar atılmalıdır. SURVANTA, KULLANIM ÖNCESİ, SULANDIRMA YA DA SES DALGALARINA MARUZ KALMA İHTİYACI GEREKTİRMEZ. Uygulama YöntemleriGenelSURVANTA intratrakeal olarak uygulanır. Endotrakeal tüpü ventilatörden ayırmak suretiyle, bebeğin endotrakeal tüpüne takılan 5 Fransız end-hole kateteri ile veya endotrakeal tüpü ventilatörden ayırmadan bir neonatal emme valfine kateteri takmak yoluyla veya bir çift lümenli endotrakeal tüpün sekonder lümeni ile uygulanır. Eğer ilaç end-hole kateter ile uygulanacaksa, kateterin ucu, bebeğin karina'sının üstündeki endotrakeal tüpün sonuna gelmelidir. SURVANTA ana bronşlara uygulanmamalıdır. SURVANTA 'nın akciğerlerde homojen dağılımının sağlanması için her doz fraksiyonel dozlara bölünür. Her doz iki yarım doza veya dört çeyrek doza bölünebilir. Her fraksiyonel doz, bebek farklı pozisyondayken uygulanır. SURVANTA'yı iki yarım dozda uygulamak için önerilen pozisyonlar şöyledir: Baş ve vücut yaklaşık 45 0 sağa dönmüş. Baş ve vücut yaklaşık 45 0 sola dönmüş. SURVANTA'yı dört çeyrek dozda uygulamak için önerilen pozisyonlar şöyledir: Baş ve vücut biraz (5 - 10 0) aşağı eğilmiş durumda, baş sağa dönmüş. Baş ve vücut biraz (5 - 10 0) aşağı eğilmiş durumda, baş sola dönmüş. Baş ve vücut biraz (5 - 10 0) yukarı kalkmış durumda, baş sağa dönmüş. Baş ve vücut biraz (5 - 10 0) yukarı kalkmış durumda, baş sola dönmüş. Dört çeyrek doz için pozisyonlar aşağıda resimlendirilmiştir. 1. Bebeğin başı ve vücudu aşağı doğru tutulmuş, baş sağa dönmüş. 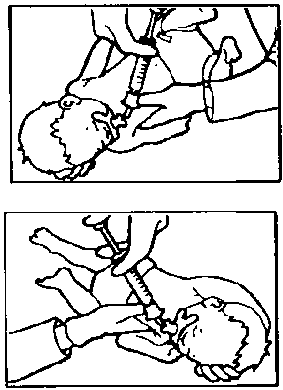 2. Baş ve vücut aşağı doğru tutulmuş, baş sola dönmüş. 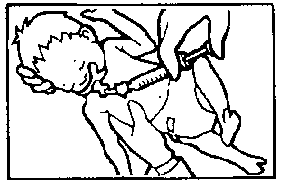 3. Baş ve vücut yukarı kaldırılmış, baş sağa dönmüş. 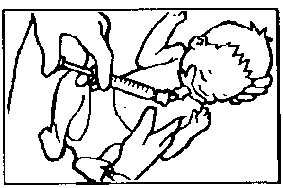 4. Baş ve vücut yukarı kaldırılmış, baş sola dönmüş. Bir kişi ilacı verirken diğer bir kişinin çocuğu uygun pozisyonda tutup; gözlemesi uygulamayı kolaylaştırır. SURVANTA'nın uygulanmasının değişik metodları klinik çalışmalarda değerlendirilmiştir. Emniyet ve etkinliği gösteren altı tek dozluk ve dört çoğul dozlu kontrollü klinik çalışmalarda, SURVANTA, endotrakeal tüpü ventilatörden ayırıp, bebeğin endotrakeal tüpüne takılan bir kateter aracılığıyla uygulanmıştır. Her doz yukarıda anlatıldığı gibi dört çeyrek doz olarak uygulanmıştır. Bu metod, çoğul-merkezli randomize klinik bir çalışmada (600 gram veya daha fazla ağırlıkta, mekanik ventilasyon gerektiren RDS 'li 299 bebeği kapsayan) diğer iki metodla mukayese edilmiştir. Bu iki metod şöyledir: İki yarım doz, endotrakeal tüpü ventilatörden ayırıp, kateteri endotrakeal tüpe yerleştirmek suretiyle verilir. İki yarım doz yukarıda anlatılan iki pozisyonda uygulanır. İki yarım doz, endotrakeal tüpü ventilatörden ayırmadan, kateteri endotrakeal tüpe bir neonatal emme valfi ile takarak verilir. İki yarım doz yukarıda anlatılan iki pozisyonda uygulanır. Her 3 grup arasında ortalama FiO2, a/APO2, doğumdan 72 saat sonra MAP, pulmoner hava kaçağı insidansı, pulmoner interstisyel anfizem, patent ductus arteriosus veya doğumdan 72 saat sonra ölüm açısından önemli farklılıklar yoktur. SURVANTA'nın çift lümenli endotrakeal tüp kullanılarak uygulanması, neonatal aspirasyon valfi kullanılmasına (yani SURVANTA'nın mekanik ventilasyonu kesmeden endotrakeal tüpün distal ucundan verilmesi) fonksiyonel olarak eşdeğerdir. Bu verme yöntemi daha az hipoksi ve dozdan hemen sonra daha az bradikardiye neden olabilir. Yinede, diğer uygulama metodlarıyla kıyaslandığında kısa ve uzun vadeli sonuçlar arasında farklılık görülmemiştir. Eğer bebek halihazırda tek lümenli endotrakeal tüp ile entübe edilmişse, sadece SURVANTA vermek amacıyla, çift lümenli endotrakeal tüp ile tekrar entübe edilmemelidir. İlk Doz"End - Hole" Kateter Yoluyla UygulamaSurvanta'nın toplam dozu, bebeğin doğum ağırlığına göre düzenlenmiş SURVANTA DOZ CETVELİ'nden hesaplanır. Büyük bir iğne (örneğin; en azından 20'lik) ile flakonun içeriği plastik bir enjektöre yavaşça alınır. SURVANTA SÜZÜLMEMELİ VE ÇALKALANMAMALIDIR. Önceden ölçülmüş 5 Fransız end-hole kateteri enjektöre takılır. Kateter SURVANTA ile doldurulur. Enjektörde tam gerekli doz kalsın diye SURVANTA'nın fazlası kateterden atılır. Survanta'yı uygulamadan önce, endotrakeal kanalın konumu ve açıklığı kontrol edilmelidir. SURVANTA'nın uygulanmasından önce endotrakeal kanalın aspirasyonu hekimin isteğine bağlıdır. Uygulamaya geçmeden önce bebek stabilize edilmelidir. Önleme uygulaması yapılıyorsa, bebek tartılmalı, entübe edilmeli ve stabilize edilmelidir. Doğumdan sonra mümkün olduğu kadar çabuk, tercihan ilk 15 dakika içinde uygulama yapılmalıdır. Bebek uygun pozisyona getirilmeli ve ilk çeyrek doz kateterden yavaşça, 2-3 saniye içinde verilmelidir. İlk fraksiyonel dozun uygulanmasından sonra, kateter endotrakeal tüpten çıkartılır. Siyanozu önlemek için, 60 nefes/dakika hızında, elle çalışan bir oksijen torbasıyla yeterli oksijen ve uygun hava değişimini ve göğüs duvarı hareketini sağlamak için yeterli pozitif basınç verilmelidir. Kurtarma işlemi yapılıyorsa, RDS tedavisi amacıyla bebek ventilatöre bağlandıktan sonra mümkün olduğu kadar kısa sürede ilk doz uygulanmalıdır. Klinik çalışmalarda, ilk fraksiyonel dozun uygulanmasından hemen önce, bebeğin bağlandığı ventilatörün hızı dakikada 60'a, solunum süresi 0.5 saniyeye, Fi02 1.0 'e ayarlanır. Bebek uygun pozisyona getirilir ve ilk fraksiyonel doz, kateterden 2-3 saniye içinde yavaşça verilir. İlk fraksiyonel dozun uygulanmasından sonra, kateter, endotrakeal tüpten çıkartılır ve mekanik ventilasyona devam edilir. Her iki uygulamada da (önleme/kurtarma) bebeğe en azından 30 saniye ya da stabil oluncaya kadar solunum yaptırılır. Bir sonraki doz için bebeğin pozisyonu yeniden ayarlanır. Diğer kalan fraksiyonel dozlar da aynı işlem uygulanarak verilir. Her dozun uygulanmasından sonra, kateter çıkartılır ve bebeğe en azından 30 saniye süreyle ya da stabil oluncaya kadar solunum yaptırılır. Son dozun verilmesinden sonra, içindekiler fışkırtılmadan kateter çıkartılır. Solunum yolu obstrüksiyonu belirtileri oluşmadıkça uygulamadan sonra 1 saat süreyle bebek aspire edilmez. UYGULAMA İŞLEMİ BİTTİKTEN SONRA, NORMAL SOLUNUM İŞLEMLERİNE VE KLİNİK BAKIM YÖNTEMLERİNE DÖNÜLÜR. Çift-Lümenli Endotrakeal Tüpün Sekonder Lümeni Yoluyla UygulamaBebeğin uygun ölçüdeki çift - lümenli endotrakeal tüp ile entübe edildiğinden emin olunuz. SURVANTA'nın toplam dozu bebeğin doğum ağırlığına göre düzenlenmiş SURVANTA DOZ CETVELİNDEN hesaplanır. Büyük bir iğne ile ( örneğin en azından 20 gauge) flakonun içeriği plastik bir enjektöre yavaşça alınır. SURVANTA SÜZÜLMEMELİ VE ÇALKALANMAMALIDIR. Survanta'yı uygulamadan önce, endotrakeal tüpün konumu ve açıklığı kontrol edilmelidir. SURVANTA'nın uygulanmasından önce endotrakeal tüpün aspirasyonu hekimin isteğine bağlıdır. Uygulamaya geçmeden önce bebek stabilize edilmelidir. Önleme uygulaması yapılıyorsa bebek tartılmalı, entübe edilmeli ve stabilize edilmelidir. Doğumdan sonra mümkün olduğu kadar çabuk, tercihen ilk 15 dakika içinde uygulama yapılmalıdır. SURVANTA'yı içeren enjektör sekonder lümene takılır. Bebek uygun pozisyona getirilir ve ilk fraksiyonel doz sekonder lümenden, 2-3 saniyede, ventilasyonu kesmeden, yavaşca enjekte edilir. Eğer ventilasyon elle yapılıyorsa, siyanozu önlemek için, 60 nefes/dakika hızında, elle çalışan bir oksijen torbasıyla yeterli oksijen ve uygun hava değişimini ve göğüs duvarı hareketini sağlamak için yeterli pozitif basınç verilmelidir. Kurtarma işlemi yapılıyorsa, RDS tedavisi amacıyla bebek ventilatöre bağlandıktan sonra mümkün olduğu kadar kısa sürede ilk doz uygulanmalıdır. İlk fraksiyonel dozun uygulanmasından sonra dakikada 60'a, solunum süresi 0.5 saniyeye, Fi02 1.0'e ayarlanır. Bebek uygun pozisyona getirilir ve ilk fraksiyonel doz, sekonder lümenden 2-3 saniyede mekanik ventilasyonu kesmeden enjekte edilir. Her iki uygulamada da (önleme/kurtarma) bebeğe en azından 30 saniye ya da stabil oluncaya kadar solunum yaptırılır. Bir sonraki doz için bebeğin pozisyonu yeniden ayarlanır. Diğer kalan fraksiyonel dozlar da aynı işlem uygulanarak verilir. Her dozun uygulanmasından sonra bebeğe, en az 30 saniye ya da stabil oluncaya kadar solunum yaptırılır. Son fraksiyonel dozun uygulanmasından sonra, enjektör sekonder lümenden çıkartılır. SEKONDER LÜMENİ YIKAMAK İÇİN 0.5 ml HAVA ENJEKTE EDİLİR VE KAPATILIR. UYGULAMA İŞLEMİ BİTTİKTEN SONRA, NORMAL SOLUNUM İŞLEMLERİNE VE KLİNİK BAKIM YÖNTEMLERİNE DÖNÜLÜR. TEKRAR DOZLARI (EK UYGULAMALAR)Tekrar dozlar için SURVANTA'nın dozu 100 mg fosfolipid/kg'dır ve bu doz bebeğin doğum ağırlığına bağlıdır. SURVANTA dozunu saptamak için bebek yeniden tartılmamalıdır. Toplam dozu saptamak için SURVANTA DOZ CETVELİ kullanılır. Ek SURVANTA uygulamasına duyulan ihtiyaç respiratuvar distresin sürmesiyle bağlantılıdır. SURVANTA ile yapılan çok dozlu klinik çalışmalarda ek uygulamaya ilişkin aşağıdaki kriterler kullanıldığında RDS'ye bağlı mortalitede belirgin azalmalar oluştuğu gözlenmiştir. Bebek entübe durumdaysa ve 80 torr'a eşit ya da ondan daha az Pa02'yi sağlamak için en azından %30 saf oksijene ihtiyaç gösteriyorsa önceki uygulamanın üstünden 6 saat geçmeden ikinci uygulama yapılmaz. Önleme işlemi uygulanan bebeklerde ek doz verilmeden önce RDS'nin radyografik teyidi sağlanmalıdır. SURVANTA hazırlanır ve önceden belirtildiği gibi bebek her çeyrek dozun uygulanması için uygun pozisyona getirilir. Her dozun uygulanmasından sonra, kateter, endotrakeal tüpten çıkartılır ve bebeğe en azından 30 saniye süreyle ya da stabil oluncaya kadar solunum uygulanır. Klinik çalışmalarda, ek dozlar için kullanılan ventilatör aksamı, ilk uygulamada kullanılandan farklıdır. Ek uygulamalarda, Fi02'ye ya da siyanozu önlemeye yeterli bir miktarda çıkartılmıştır. Ventilatör hızı dakikada 30, solunum süresi 1.0 saniyeden azdır. Eğer bebeğin tedavi öncesi hızı 30 ya da daha yüksekse SURVANTA uygulaması sırasında değiştirilmeden bırakılmıştır. Ek uygulamalarda elle çalışan oksijen torbası kullanılmamalıdır. UYGULAMA SIRASINDA, UYGUN OKSİJENASYON VE VENTİLASYON SAĞLAMAK AMACIYLA, VENTİLATÖR AKSAMININ AYARLANMASI HEKİMİN İSTEĞİNE BAĞLIDIR. UYGULAMA BİTTİKTEN SONRA, OLAĞAN SOLUMA VE KLİNİK BAKIM İŞLEMLERİNE DÖNÜLÜR. Uygulama ÖnlemleriUygulama sırasında bebekte bradikardi ya da oksijen desatürasyonu görülürse uygulama kesilir ve durumu düzeltecek önlemler alınır. Durum düzeldikten sonra uygulamaya devam edilir. SURVANTA'nın uygulanmasından sonra geçici olarak solunum seslerinde kabalaşma oluşabilir. Solunum yolu obstrüksiyonuna ilişkin kesin belirtiler olmadıkça, endotrakeal aspirasyon ya da diğer önlemler gerekmez. 4.3 Kontrendikasyonlar Bilinen bir kontrendikasyonu yoktur. 4.4 Özel kullanım uyarıları ve önlemleri SURVANTA yalnızca intratrakeal uygulama içindir. SURVANTA, oksijenasyonu ve akciğer uyumunu hızlı biçimde etkiler. Bu nedenle, kullanımı entübasyon, ventilatör uygulaması ve prematüre bebek genel bakımı konusunda deneyimli hekimleri el altında bulundurabilen, tam gözetim altındaki kliniklerle sınırlandırılmalıdır. SURVANTA uygulanan bebekler, sistemik oksijen ve karbondioksidin arteriyel ya da transkütan ölçümleriyle birlikte sıkı kontrol altında tutulmalıdır. SURVANTA'nın uygulanımından sonraki dakikalar içinde oksijenasyonda belirgin iyileşmeler görülebilir. O nedenle hiperoksiyi önlemek için sistemik oksijenasyonun izlenmesi, sık ve özenli bir klinik gözetimin yapılması gereklidir. Uygulama sırasında, geçici bradikardi nöbetleri ve oksijen doyumunda azalma bildirilmiştir. Böyle bir durumda, uygulama kesilmeli ve durumu düzeltecek uygun önlemler alınmalıdır. Durum düzeldikten sonra uygulamaya yeniden başlanır. Uygulama sonrasında geçici olarak, solunum seslerinde kabalaşma ve raller oluşabilir. Solunum yolu obstrüksiyon belirtileri kesinleşmedikçe endotrakeal aspirasyon ya da diğer önlemler gerekmez. Kontrollü klinik çalışmalarda, SURVANTA uygulanan bebeklerde tedavi sonrası nosokomial sepsis olasılığının arttığı gözlenmiştir. SURVANTA uygulanan bebeklerde sepsis riskinin artışı aynı bebeklerde mortalite artışıyla bağlantılı değildir. Olaya yol açan organizmalar tedavi ve kontrol grubu bebeklerinin her ikisinde de aynıdır. Sepsis dışında, tedavi sonrası enfeksiyon oranı açısından gruplar arasında anlamlı bir fark yoktur. Doğum ağırlığı 600 gramdan az ya da 1750 gramdan çok olan bebeklerde SURVANTA uygulanması, kontrollü çalışmalarda değerlendirilmemiştir. RDS'de uygulanan deneysel tedavilerle (örneğin; yüksek frekanslı ventilasyon ya da vücut dışı membran oksijenasyonu) birlikte SURVANTA kullanımına ilişkin kontrollü bir çalışma yoktur. Kilogram başına 100 mg fosfolipidi aşan dozların, dört kereyi aşan uygulamanın, 6 saatte birden daha çok sıklıkla yapılan uygulamanın ya da doğumdan 48 saat sonra yapılan uygulamanın etkilerine ilişkin bilgi bulunmamaktadır. 4.5 Diğer tıbbi ürünler ile etkileşimler ve diğer etkileşim şekilleri Herhangi bir etkileşim türü rapor edilmemiştir. 4.5 Gebelik ve Laktasyon Gebelik dönemi SURVANTA, sadece prematüre ve yenidoğan bebeklerde uygulanan bir üründür. Bundan dolayı gebelikde kullanımı yoktur. Laktasyon Dönemi SURVANTA, sadece prematüre ve yenidoğan bebeklerde uygulanan bir üründür. Bundan dolayı laktasyonda kullanımı yoktur. 4.7 Araç ve makina kullanımı üzerindeki etkiler 4.8 İstenmeyen Etkiler En sık görülen advers etkiler uygulama (dozaj prosedürü) ile bağlantılıdır. Çoğul dozlu kontrollü klinik çalışmalarda SURVANTA'nın her dozu dört çeyrek doza bölünür. Her çeyrek doz, endotrakeal tüp ventilatörden kısa süreli ayırılarak, endotrakeal tüpe sokulan bir kataterden instile edilmiştir. Spontan olarak bildirilen ya da klinik çalışmalarda gözlemlenen advers reaksiyonlar, aşağıdaki tabloda gösterilmiştir. Advers ilaç reaksiyonları, her sistem organ sınıfı içerisinde aşağıdaki düzene göre sıklık başlıkları altında sınıflandırılmıştır: çok yaygın (>1/10), yaygın (>1/100 ila <1/10), yaygın olmayan (>1/1.000 ila <1/100), seyrek (>1/10.000 ila <1/1.000), çok seyrek (<1/10.000), bilinmiyor (eldeki verilerden hareketle tahmin edilemiyor).
Kontrollü klinik çalışmalarda, beraktantın sık yapılan aşağıdaki laboratuar testlerinin sonuçları üzerinde bir etkisi olmamıştır: lökosit sayımı, serum sodyum, potasyum, bilirubin ve kreatinin. Prematüre bebeklerde birçok başka komplikasyonun oluştuğu bilinmektedir. Kontrollü klinik çalışmalarda aşağıdaki durumlar bildirilmiştir. Komplikasyon oranları tedavi edilen ve kontrol grubundaki bebeklerde farklı değildir. Komplikasyonların hiçbiri SURVANTA'ya yüklenmemiştir. Kan ve lenfatik sistem bozukluklarıKoagülopati, trombositopeni, dissemine intravasküler koagülasyon Endokrin bozukluklarAdrenal hemoraji, uygunsuz ADH sekresyonu Metabolizma ve nütrisyon bozukluklarıHiperfosfatemi, beslenme intoleransı Sinir sistemi bozukluklarıNöbetler Kardiyak bozukluklarTaşikardi, ventriküler taşikardi, kalp yetmezliği, kardiyo-respiratuvar arest, apikal nabız artışı, persistan fetal dolaşım, total pulmoner venöz dönüş anomalisi Vasküler bozukluklarHipotansiyon, hipertansiyon, aort trombozu, hava embolizmi Respiratuar, torasik ve mediastinal bozukluklarAkciğer konsolidasyonu, endotrakeal tüpte kan, ventilasyon cihazından ayrıldıktan sonra solunum durumunda bozulma olması, respiratuar dekompansasyon,subglottik stenoz, diyafragma paralizisi, solunum yetmezliği Gastrointestinal bozukluklarAbdominal distansiyon, gastrointestinal hemoraji, intestinal perforasyonlar, volvulus, barsak enfarktı, stres ülseri, inguinal herni Hepatobiliyer bozukluklarHepatik yetmezlik Renal ve üriner bozukluklarRenal yetmezlik, hematüri Genel bozukluklar ve uygulama yeri reaksiyonlarıAteş, genel durumda kötüleşme Bugüne dek SURVANTA tedavisiyle uzun dönemli komplikasyonlar veya sekeller bulunmamıştır. 4.9 Doz aşımı ve tedavisi SURVANTA'ya ilişkin bir doz aşımı bildirilmemiştir. Hayvan deneylerinden elde edilen bulgulara göre, doz aşımına bağlı olarak akut solunum yolu obstrüksiyonu oluşabilir. Tedavisi semptomatik ve destekleyici nitelikte olmalıdır. SURVANTA uygulamasından sonra geçici olarak solunum seslerinde kabalaşma ve raller duyulabilirse de bunlar doz aşımının işareti değildir. Solunum yolu obstrüksiyonuna ilişkin kesin belirtiler bulunmadıkça endotrakeal aspirasyon ya da diğer önlemler gerekmez. 5.1 Farmakodinamik Özellikleri Farmakoterapötik grup: Akciğer surfaktanları ATC kodu: R07AA02 SURVANTA, sığır akciğerlerinden elde edilen doğal protein ve lipidlerin steril ve apirojen salin süspansiyonudur. Yüzey aktivitesini optimize etmek amacıyla, sentetik olarak elde edilen 3 adet lipid ile takviye edilmiştir: Dipalmitoilfosfatidil kolin, palmitik asid ve tripalmitin. Sonuçta ortalama 25 mg/ml'lik fosfolipid ve 1 mg/ml'den daha az protein konsantrasyonu içeren bir kompozisyon sağlanır. İlaç beyazımsı açık kahverengi opak bir likittir. % 0.9 'luk sodyum klorür çözeltisinde süspande olup, ısı ile sterilize edilmiştir. Koruyucu madde içermez. Protein içeriği, yaygın olarak SP-B ve SP-C diye bilinen, surfaktanla alakalı iki adet hidrofobik ve düşük moleküler ağırlıklı proteinden oluşmuştur. SP-A diye bilinen hidrofilik ve yüksek moleküler ağırlıklı olan surfaktanla alakalı proteini içermez. Endojen pulmoner surfaktan, solunum sırasına alveollerin yüzeyindeki gerilimi azaltır ve dinlenme durumundaki transpulmoner basınçlarda kollapsa karşı alveolleri stabilize eder. Prematüre bebeklerde, pulmoner surfaktanın yetmezliği Respiratuvar Distres Sendromu'na (RDS) yol açar. SURVANTA, surfaktanın yerine geçerek bu bebeklerin akciğerlerindeki yüzey aktivitesini düzeltir. 5.2 Farmakokinetik Özellikleri Radyoaktif-etiketli fosfatidilkolin kullanılan klinik öncesi çalışmalarda, Survanta'nın üç günlük tavşanların akciğerlerinden temizlenme hızının, doğal dana ya da koyun surfaktanlarıyla benzer olduğu gösterilmiştir (24 saat içerisinde yaklaşık %13). Bunun yanı sıra, Survanta'nın metabolik olarak aktif surfaktan döngüsüne girdiğini belirten bazı geri alım ve salgılama durumları da gösterilmiştir. Survanta eksojen bir preparat olarak doğrudan akciğere verildiğinden, klasik klinik farmakokinetik parametreler (kan seviyeleri, plazma yarı ömrü, vb.) üzerinde çalışılmamıştır. 5.3 Klinik öncesi güvenlilik verileri Yeni doğan sıçanlara 500 mg fosfolipid/kg/gün'e kadar 5 gün boyunca subkütan olarak SURVANTA uygulanmıştır. Sıçanlar normal olarak üremişler ve yavrularında advers etkilere rastlanmamıştır. Mutajenite çalışmalarında negatif sonuçlar elde edilmiştir. SURVANTA ile karsinojenite çalışmaları yapılmamıştır. 6. FARMASÖTİK ÖZELLİKLER 6.1 Yardımcı maddelerin listesi: 1.0 mL 'deSodyum klorür, USP/EP/BP 9.0 mg Alkol (etanol),USP, 190 derece, Katıksız** q.s. Sodyum hidroksit, NF/EP/BP*** q.s. Hidroklorik asid, NF/EP/BP**** q.s. Distile su, USP/EP/BP***** q.s. Azot, NF q.s. ** İşlem sırasında kullanılır. *** pH ayarı içindir, işlem sırasında belirtilen başlangıç miktarı 20.0 g 'dır. **** pH ayarı içindir, işlem sırasında belirtilen başlangıç miktarı 30.0 g 'dır. ***** Test edildi, bakteri endotoksin limitlerine ve Enjeksiyonluk Su, USP gereklerine uyar. 6.2 Geçimsizlikler Sunulmamıştır. 6.3 Raf ömrü Ürünün raf ömrü 18 aydır. 6.4 Saklamaya yönelik özel tedbirler Açılmamış flakonlar buzdolabında (20 - 80 C) saklanır. Işıktan korunmalıdır. 6.5 Ambalajın niteliği ve içeriği USP Tip I cam flakon ve faultless 5153, gri, klorobutil kauçuk tıpa. Her mililitresinde, %0.9 sodyum klorür solüsyonunda süspanse edilmiş 25 mg fosfolipid bulunur. Rengi beyazımsı-açık kahverengidir. 6.6 Beşeri tıbbi üründen arta kalan maddelerin imhası ve diğer özel önlemler Geçerli olduğu takdirde kullanılmamış olan ürünler ya da atık materyaller 'Tıbbi Atıkların Kontrolü Yönetmeliği' ve 'Ambalaj ve Ambalaj Atıklarının Kontrolü Yönetmelik'lerine uygun olarak imha edilmelidir. 7. RUHSAT SAHİBİ Abbott Laboratuarları Ith. Ihr. ve Tic. Ltd.Şti. Ekinciler Cad., Hedef Plaza, Kat:6 Kavacık 81640 Beykoz-İstanbul Telefon: 0216 425 09 77 Fax: 0216 425 09 65 8. RUHSAT NUMARASI93/779. İLK RUHSAT TARIHI/RUHSAT YENILEME TARIHIİlk ruhsatlandırma tarihi:19/01/1994 Son yenileme tarihi:03.08.200510. KÜB'UN YENİLENME TARİHI |
İlaç BilgileriSurvanta İntratrakeal SüspansiyonEtken Maddesi: Beraktant Atc Kodu: R07AA02 Kullanma talimatı ve kısa ürün bilgileri
Google Reklamları
İlgili İlaçlar |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
Ana Sayfa | Hakkımızda | İlaçlar | İlaç Ara | İlaç Firmaları | Gizlilik | Bize Ulaşın
Telif Hakkı 2008-2026 © İlaç Prospektüsü. Tüm Hakları Saklıdır.Uyarı: Sitemizde yayınladığımız ilaç bilgileri ile doktora danışmadan kesinlikle ilaç kullanmayınız!
Aksi halde doğabilecek sağlık sorunlarından ilacprospektusu.com sorumlu tutulamaz.