Otrivine Doz Ayarlı Burun Spreyi 1 mg/ml Kısa Ürün BilgisiSolunum Sistemi » Burunla İlgili İlaçlar » Topikal Dekonjestanlar ve Diğer Nazal İlaçlar » Sempatomimetikler » Ksilometazolin HCL KISA ÜRÜN BİLGİSİ1.BEŞERİ TIBBİ ÜRÜNÜN ADIOTRIVINE doz ayarlı burun spreyi 1 mg/ml2.KALİTATİF VE KANTİTATİF BİLEŞİMEtkin madde:Yardımcı maddeler:Her 1 ml çözelti, 0.11 mg benzalkonyum klorür içerir. Yardımcı maddeler için 6.1'e bakınız.3.FARMASÖTİK FORMDoz ayarlı burun spreyiRenksiz, hemen hemen kokusuz berrak çözelti 4.KLİNİK ÖZELLİKLER4.1.TerapötikendikasyonlarOTRIVINE aşağıdaki durumlarda endikedir:-Soğuk algınlığı, saman nezlesi veya diğer alerjik rinitlere, sinüzite bağlı nazal konjesyonu gidermek, -Paranazal sinüs hastalıklarında sekresyonun drenajına yardımcı olmak, -Orta kulak iltihabında nazofarenks mukozasının dekonjesyonu için yardımcı tedavi olarak, -Rinoskopiyi kolaylaştırmak. 4.2.Pozoloji ve uygulama şekli Pozoloji/Uygulama sıklığı ve süresi:Doktora danışılmadan kullanılmamalıdır. Doktor tarafından başka şekilde tavsiye edilmediği takdirde aşağıdaki dozlarda kullanılır:Yetişkinler ve 6 yaşından büyük olan çocuklar: Günde 3-4 kez, her bir burun deliğine 1 defa püskürtülür. Diğer topikal vazokonstriktörlerde olduğu gibi, uzun süreli ya da aşırı kullanım rebound konjesyona neden olabileceğinden 5 günden uzun süreli kullanılmamalıdır. Uygulama şekli: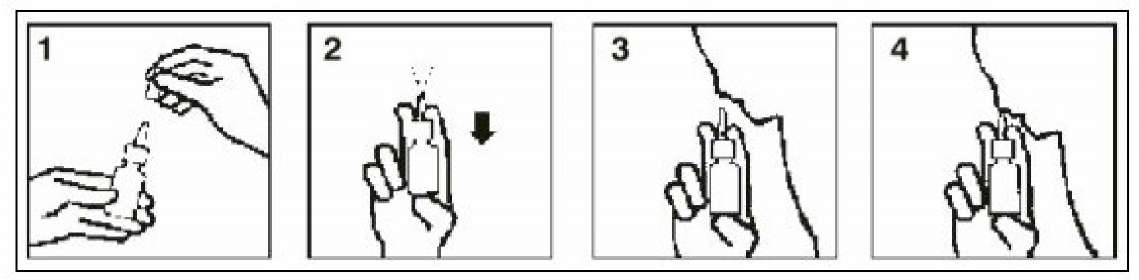 1.İlk uygulamadan önce, sprey bir defa havaya dağılana kadar, birkaç pompalama hareketi yaparak pompayı kullanıma hazır hale getiriniz.
1.İlk uygulamadan önce, sprey bir defa havaya dağılana kadar, birkaç pompalama hareketi yaparak pompayı kullanıma hazır hale getiriniz.2.Burnunuzu temizleyiniz. 3.İleriye doğru hafifçe eğiliniz ve başlığı burun deliğine yerleştiriniz. 4.Spreyin en uygun şekilde dağılmasını sağlamak için, pompayı bastırırken aynı anda nefes alınız. 5.Aynı işlemi diğer burun deliği için de tekrarlayınız. 6.Kullanımdan sonra kapağı kapatınız. Ölçülü doz veren sprey, OTRIVINE'nin burun mukozası yüzeyine iyice dağılmasını sağlar. Kapaktaki standardize valf, her defasında tam doz uygulanmasını sağlar ve kazara aşırı doz verilmesini engeller. Özel popülasyonlara ilişkin ek bilgiler: Böbrek/karaciğer yetmezliği:OTRIVINE'nin böbrek ya da karaciğer yetmezliği olan hastalarda kullanımı ile ilgili klinik çalışma bulunmamaktadır.Pediatrik popülasyon:OTRIVINE %0.1 Sprey, 6 yaşın altındaki çocuklarda kullanılmamalıdır.Geriyatrik popülasyon:OTRIVINE'nin yaşlı hastalarda kullanımı ile ilgili klinik çalışma bulunmamaktadır.4.3. KontrendikasyonlarOTRIVINE MENTHOL, aşağıdaki durumlarda kontrendikedir:Diğer vazokonstriktörler gibi transsfenoidal hipofizektomi ya da dura materin açığa çıkmasına neden olan ameliyat geçirmiş hastalar Etkin madde veya diğer adrenerjik ilaçlara veya bileşiminde bulunan yardımcı maddelerden herhangi birine karşı aşırı duyarlılık Rinitis sicca 6 yaşın altındaki çocuklar 4.4.Özel kullanım uyarıları ve önlemleriKardiyovasküler sistem hastalıklarıMonoamino oksidaz inhibitörleri (MAOI) veya trisiklik antidepresanlar (TSA) ile eş zamanlı kullanım Diabetes Mellitus Dar açılı glokom Hipertansiyon Feokromasitom Prostat hipertrofisi Tiroid fonksiyon bozukluklarında kullanımından kaçınılmalıdır. 5 günden uzun süreli kullanılmamalıdır. Akut alevlenmeler dışında ksilometazolin kronik rinit tedavisinde kullanılmamalıdır. Diğer sempatomimetik ilaçlarda olduğu gibi, adrenerjik maddelere şiddetli reaksiyon gösteren kişilerde uykusuzluk, sersemlik, titreme, kardiyak aritmiler ya da tansiyon artışına neden olabileceğinden dikkatle kullanılmalıdır. Özellikle çocuklarda ve yaşlılarda olmak üzere, önerilen doz aşılmamalıdır. 4.5.Diğer tıbbi ürünler ile etkileşimler ve diğer etkileşim şekilleriBütün sempatomimetikler gibi ksilometazolinin de sistemik etkilerinin, monoamino oksidaz inhibitörleri, trisiklik veya tetrasiklik antidepresanlarla birlikte kullanıldığı zaman, özellikle doz aşımı söz konusu olduğunda şiddetlenme olasılığı, göz önünde bulundurulmalıdır.Özelpopülasyonlara ilişkin ek bilgilerVeri yoktur. Pediatrik popülasyonVeri yoktur. 4.6.Gebelik ve Laktasyon Genel tavsiyeGebelik kategorisi: CÇocuk doğurma potansiyeli bulunan kadınlar/Doğum kontrolü (Kontrasepsiyon)Ksilometazolinin gebe kadınlarda kullanımına ilişkin yeterli veri mevcut değildir.Hayvanlar üzerinde yapılan çalışmalar, gebelik /ve-veya/ embriyonal/fetal gelişim /ve-veya/ doğum /ve-veya/ doğum sonrası gelişim üzerindeki etkiler bakımından yetersizdir. İnsanlara yönelik potansiyel risk bilinmemektedir. OTRİVİNE, gerekli olmadıkça gebelik döneminde kullanılmamalıdır. Gebelik dönemiOTRIVINE, olası sistemik vazokonstriktör etkileri nedeniyle gebelik süresince kullanılmamalıdır.Laktasyon dönemiOTRIVINE'nin emzirilen çocuk üzerinde herhangi bir advers etkisi olduğuna dair kanıt bulunmamaktadır. Bununla birlikte ksilometazolinin insan sütüyle atılıp atılmadığı bilinmediğinden dikkatli olunmalıdır. OTRIVINE emzirme döneminde yalnız reçete edildiği takdirde kullanılmalıdır.Üreme yeteneği (Fertilite)Hayvan çalışmaları, terapötik dozlardan yüksek dozlarda uygulamada, üreme toksisitesi olduğunu göstermiştir.4.7.Araç ve makine kullanımı üzerindeki etkilerAraç ve makine kullanımı üzerinde bilinen herhangi bir etkisi yoktur.4.8.İstenmeyen etkilerŞu terimler ve sıklık dereceleri kullanılmıştır:Çok yaygın (>1/10); yaygın (>1/100 ila <1/10); yaygın olmayan (>1/1.000 ila <1/100); seyrek (>1/10.000 ila <1/1.000); çok seyrek (<1/10.000), bilinmiyor (eldeki verilerden hareketle tahmin edilemiyor)Sinir sistemi hastalıklarıSeyrek: Baş ağrısıGastrointestinal hastalıklarSeyrek: BulantıGenel bozukluklar ve uygulama bölgesine ilişkin hastalıklarSeyrek: Lokal yanma hissi, burun mukozasında lokal iritasyon veya kurumaÇok seyrek: Sistemik alerjik reaksiyonlar, geçici görme bozuklukları ve düzensiz veya hızlı kalp atışı kaydedilmiştir. 4.9. Doz aşımı ve tedavisiÇocuklarda ender olarak görülen kaza sonucu zehirlenmelerde, başlıca hızlı ve düzensiz nabız, yüksek kan basıncı ve bazen bilincin bulanıklaşması gibi belirtilerden oluşan klinik tablo ortaya çıkar.Spesifik bir tedavi yoktur. Uygun destekleyici tedaviye başlanmalıdır. 5. FARMAKOLOJİK ÖZELLİKLER5.1.Farmakodinamik özelliklerFarmakoterapötik grup: Dekonjestanlar ve diğer topikal kullanılan nazal preparatlar, sempatomimetiklerATC kodu: R01A A07 Etki mekanizması Ksilometazolin, alfa adrenerjik reseptörlere etki eden sempatomimetik bir ajandır. Buruna uygulanmak üzere hazırlanan OTRIVINE, burundaki kan damarlarını daraltarak burun mukozasında ve komşu farenks bölgelerinde dekonjesyon sağlar. Bu sayede burun geçitlerinde dekonjesyon elde edildiğinden, burnu tıkalı olan hasta, burun yoluyla daha rahat soluk alıp verebilir. OTRIVINE, mukozası hassas olan hastalar tarafından bile iyi tolere edilir ve mukosilier fonksiyonu bozmaz. Ayrıca OTRIVINE nazal kavitenin pH aralığı içinde dengeli bir pH'a sahiptir. 5.2.Farmakokinetik özelliklerOTRIVINE'in etkisi birkaç dakika içinde başlar ve 12 saate kadar uzayabilen süreler boyunca devam eder. Soğuk algınlığı olan hastalarla yapılan çift kör, kontrollü (salin solüsyonu) bir çalışmada rinomometre ile yapılan ölçümlerde OTRIVINE'in dekonjestan etkisi salin solüsyonuna göre anlamlı derecede (p<0.0001) yüksek bulunmuştur. Tedaviden 5 dakika sonra salin solüsyonu ile karşılaştırıldığında burun tıkanıklığına etkisi iki kat daha hızlıdır.Lokal nazal uygulamayı takiben ksilometazolinin plazma konsantrasyonu, en duyarlı yöntemlerle bile ölçülemeyecek kadar düşüktür. 5.3.Klinik öncesi güvenlilik verileriKsilometazolinin mutajenik etkisi yoktur. Ksilometazolinin fare ve sıçanlara subkutan yoldan uygulandığı bir çalışmada teratojenik etki görülmemiştir.6.FARMASÖTİK ÖZELLİKLER6.1.Yardımcı maddelerin listesiBenzalkonyum klorür Disodyum edetat Disodyum fosfat Sodyum dihidrojen fosfat Sodyum klorür, saf, PH Saf su6.2.GeçimsizliklerBilinen herhangi bir geçimsizliği yoktur..6.3.Raf ömrüPreparatın raf ömrü 36 aydır.6.4.Saklamaya yönelik özel tedbirlerSıcaktan korunmalıdır. 30°C'nin altındaki oda sıcaklığında saklanmalıdır.6.5.Ambalajın niteliği ve içeriğiPrimer Ambalaj : Polietilen şişeBurun kısmına monte edilmiş koruyucu başlık Doz ayarlı pompa 6.6.Beşeri tıbbi üründen arta kalan maddelerin imhası ve diğer özel önlemler"Tıbbi Atıkların Kontrolü Yönetmeliği" ve "Ambalaj ve Ambalaj Atıklarının Kontrolü" yönetmeliklerine uygun olarak imha edilmelidir.7.RUHSAT SAHİBİNovartis Ürünleri 34912 Kurtköy-İSTANBUL Tel : 0 216 560 10 00 Faks : 0 216 482 42 068.RUHSAT NUMARASI114/849.İLK RUHSAT TARİHİ/RUHSAT YENİLEME TARİHİİlk ruhsat tarihi: 02.01.1973 Ruhsat yenileme tarihi: 14.04.200510.KÜB'ÜN YENİLENME TARİHİ |
İlaç BilgileriOtrivine Doz Ayarlı Burun Spreyi 1 mg/mlEtken Maddesi: ksilometazolin hidroklorür Atc Kodu: R01AA07 Kullanma talimatı ve kısa ürün bilgileri
Google Reklamları
İlgili İlaçlar |
Ana Sayfa | Hakkımızda | İlaçlar | İlaç Ara | İlaç Firmaları | Gizlilik | Bize Ulaşın
Telif Hakkı 2008-2026 © İlaç Prospektüsü. Tüm Hakları Saklıdır.Uyarı: Sitemizde yayınladığımız ilaç bilgileri ile doktora danışmadan kesinlikle ilaç kullanmayınız!
Aksi halde doğabilecek sağlık sorunlarından ilacprospektusu.com sorumlu tutulamaz.