Actiq 400mcg oromukozal aplikatörlü pastil Kısa Ürün BilgisiSinir Sistemi » Ağrı Kesici / Ateş Düşürücüler (Aneljezik) » Uyuşturucu Etkiye Sahip İlaçlar (Opioid) » Fenilpiperidin Türevleri » Fentanil KISA URUNBILGISI1.BEŞERI TIBBI URUNUN ADIActiq 400 mikrogram2.KALITATIF VE KANTİTATIF BİLEŞİMHer pastil 400 mikrogram fentanil (sitrat olarak) içerir.Her pastil dekstratlar (yaklaşık olarak 2 gram glukoza eşdeğer), sukroz (yaklaşık olarak 30 miligram pudra şekeri) ve propilen glikol (yapay çilek aroması ve baskı mürekkebinin bir bölümü olarak) içerir. Yardımcı maddeler için bölüm 6.1'e bakınız. 3.FARMASÖTlK FORMİntegral oromukozal aplikatörlü sıkıştırılmış pastil.Beyaz-kirli beyaz renkte, yenebilir yapıştırıcıyla, üzerinde dozu yazılı olan kırılmaya dayanıklı radyo opak aplikatöre yapıştırılmış, sıkıştırılmış ilaç tozundan ilaç matriksi şeklinde formüle edilmiştir. 4.KLINIK ÖZELLIKLER4.1Terapötik endikasyonlarActiq, kronik ağrıları için opioid idame tedavisi uygulanmakta olan kanser vakalarında, aniden ortaya çıkan şiddetli ağrıların (kaçak ağrı; breakthrough pain) kontrol altına alınmasında endikedir. Bu ağrılar, normalde kontrol altına alınabilen inatçı ağrıların geçici alevlenmesidir.4.2Pozoloji ve uygulama şekli Pozoloji, uygulama sıklığı ve süresi:Opioide bağlı yan etkilerin riskini azaltmak ve "en uygun" dozu belirlemek için titrasyon işlemi sırasında hastanın profesyonel sağlık personeli tarafından yakından izlenmesi gerekir. Preparatın kullanılmayan bölümü uygun bir şekilde atılmalıdır. Hastalar, Actiq'in çocukların ulaşamayacağı bir yerde saklanması gerektiği konusunda uyarılmalıdır.Uygulama şekli:Actiq, oromukozal kullanım için tasarlanmıştır; aplikatörü aracılığıyla ağızda dolaştırılarak emilmelidir. Böylelikle mukozal temas maksimize edilmiş olur. Preparat çiğnenmemelidir, emilmelidir, çünkü fentanilin bukkal mukoza tarafından emilimi, gastrointestinal yoldan sistemik emilimine oranla daha hızlıdır. Ağzı kuru olan hastalarda bukkal mukozanın nemlendirilmesi için su kullanılabilir.Preparat 15 dakikalık bir süre içinde tüketilmelidir. Ağız içindeki preparat tamamen bitmeden aşırı opioid etki gözlenmesi durumunda hemen çıkarılmalı ve daha sonraki dozların azaltılması konusu dikkate alınmalıdır. Doz titrasyonuYeterli analjezi ve minimum yan etkiyi sağlayan "en uygun" dozu belirlemek için dozaj bireysel olarak titre edilmelidir. Klinik deneylerde, ani şiddetli ağrılar için en uygun Actiq dozu belirlemede, hastada kullanılan günlük opioid idame dozundan faydalanılmamıştır. Actiq ile titre edilmeden önce, hastaların sürekli ağrıları opioid tedavi yoluyla kontrol altında tutuluyor olmalı ve günde 4 kezden fazla ani ağrı krizi yaşamamış olmalıdır. Tedavide başlangıç dozu 200 mikrogram olmalıdır; gerektiğinde mevcut formlar (200, 400 ve 800 mikrogram) kullanılarak, dozaj ayarlanır. Hastalarda dozaj, ani ve şiddetli bir ağrı krizine karşı, belirli bir dozda kabul edilebilir yan etkilerde uygun analjezi sağlanana kadar dikkatle izlenerek düzeltilmelidir. Bu doz, "en uygun" doz olarak tanımlanır. Titrasyon sırasında, hastanın bir doz Actiq kullanmasında 15 dakika sonra uygun analjezi elde edilemezse, aynı doz bir kez daha verilebilir. Ancak tek bir ağrı krizi için iki defadan fazla doz Actiq kullanılmamalıdır. 1600 mikrogramlık uygulama ile sadece hastaların azında nadiren ikinci bir doza ihtiyaç duyulur. Birbirini takip eden ani ve şiddetli ağrı krizlerinde, kriz başına birden fazla doza ihtiyaç duyuluyorsa dozun arttırılarak, bir yüksek dozdaki preparatın kullanılması gerekebilir. Actiq® Doz Titrasyonu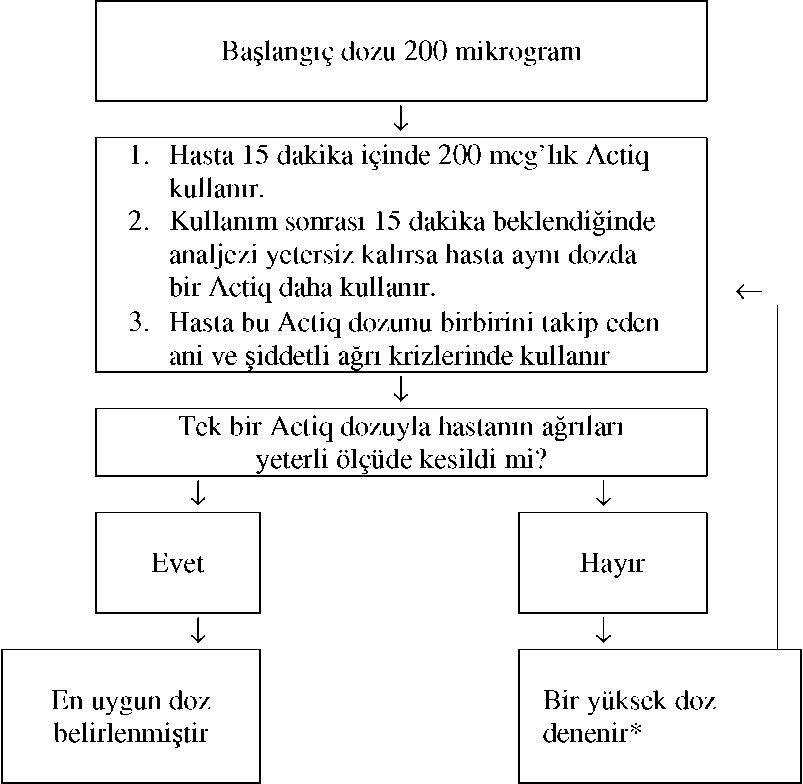 ¦ Türkiye'de mevcut dozaj formları: 200, 400 ve 800 mikrogram
¦ Türkiye'de mevcut dozaj formları: 200, 400 ve 800 mikrogramİdameUygun bir doz belirlendikten sonra (ortalama olarak, bir kriz tek bir dozaj formuyla tedavi edilebildiğinde), hasta bu dozla devam etmelidir ve günlük Actiq tüketimini en fazla dört doz ile sınırlamalıdır. Hastaların günde maksimum dört ünite Actiq limitini aşmadıklarından emin olunması için profesyonel sağlık personeli tarafından izlenmesi gerekir. Dozun yeniden ayarlanmasıBirbirini takip eden dört günden uzun bir süre boyunca günde dört ani ve şiddetli ağrı krizi yaşandığında, kalıcı ağrı için kullanılan uzun etkili opioid dozu tekrar değerlendirilmelidir. Uzun etkili opioid dozu arttırılırsa ani, şiddetli ağrıları tedavi etmek için kullanılan Actiq dozunun da tekrar gözden geçirilmesi gerekebilir. Her türlü analjezik doz yeniden ayarlanırken profesyonel bir sağlık personeli tarafından izlenmelidir. Tedavinin kesilmesiKalıcı ağrıları için kronik opioid tedavisine devam eden hastaların ani ve şiddetli ağrıları için Actiq'e gerek duyulmadığında, Actiq tedavisi hemen kesilebilir. Opioid tedavisinin tamamen kesilmesinin gerektiği durumlarda, ani geri-çekilme görülmemesi için opioid dozunun azaltılarak kesilmesi sırasında kullanılan Actiq dozu da dikkate alınmalıdır. Özel popülasyonlara ilişkin ek bilgiler: Böbrek /Karaciğer yetmezliği:Böbrek veya karaciğer yetmezliği olan hastalarda doz ayarlama işleminin özellikle dikkatle gerçekleştirilmesi gerekir.Pediyatrik popülasyon:Actiq'in, çocukluk ve adölesan dönemde kullanımıyla ilgili uygun pozoloji ve güvenlilik bilgisi bulunmamaktadır.Geriyatrik popülasyon:Yaşlı hastaların intravenöz yoldan uygulanan fentanilin etkilerine karşı daha hassas oldukları gözlenmiştir. Bu nedenle yaşlılarda doz titrasyonunda özellikle dikkat edilmesi gerekir. Yaşlılarda fentanil eliminasyonu daha yavaştır ve terminal eliminasyon yarılanma süresi daha uzundur; bu nedenle etkin madde birikimi olabilir ve bu da istenmeyen yan etki riskini arttırabilir.Yaşlılarda Actiq kullanımını araştırmak amacıyla klinik araştırmalar gerçekleştirilmemiştir. Ancak, klinik araştırmalarda 65 yaş üzeri hastalarda, ani başlangıçlı şiddetli ağrıların başarılı bir şekilde dindirilmesi için daha düşük dozlarda Actiq'in yeterli olduğu gözlenmiştir. 4.3. KontrendikasyonlarBileşimindeki etkin madde veya yardımcı maddelerden herhangi birine karşı aşırı duyarlılık durumunda.Monoamin-oksidaz (MAO) inhibitörlerinin eşzamanlı kullanımı veya MAO inhibitörlerinin kullanımınm bırakılmasından sonraki iki hafta içerisinde. İleri derecede solunum depresyonu veya şiddetli obstrüktif akciğer hastalığında kontrendikedir. 4.4 Özel kullanım uyarıları ve önlemleriActiq tedavisine başlamadan önce, hastanın kalıcı sürekli ağrısını tedavi etmek için kullanılan uzun süreli opioid tedavisinin stabilize edilmesi önemlidir.Fentanil gibi opioidlerin tekrar tekrar uygulanması sonucunda tolerans ve fiziksel ve/veya psikolojik bağımlılık oluşabilir. Ancak tedavi amaçlı opioid kullanımı sonrasında iatrojenik bağımlılık nadirdir. Tüm opioidlerde olduğu gibi Actiq kullanımı ile ilgili olarak da klinik açıdan önemli solunum depresyonu riski mevcuttur. Özellikle ileri derecede olmayan kronik akciğer yetmezliği veya kendilerini solunum depresyonuna iten başka bir rahatsızlığı olan hastalarda Actiq titrasyonu dikkatle yapılmalıdır, çünkü normal terapötik dozdaki Actiq bile solunum işlevlerini solunum yetmezliği noktasına kadar düşürebilir. Ürün, hiç opioid kullanmamış hastalara verilmemelidir, çünkü solunum depresyonu riski yüksektir ve bu hasta popülasyonu için en uygun doz henüz belirlenmemiştir. Preparat, intrakranial basıncı yüksek hastalar veya bilinç kaybı olan hastalar gibi CO2 retansiyonunun intrakranial etkilerine karşı duyarlılık gösterme ihtimali olan hastalarda çok dikkatli uygulanmalıdır. Opioidler kafa travmalı hastalarda klinik seyri saptırabilir ve bu hastalarda yalnızca klinik durumun gerektirdiği zaman kullanılmalıdır. İntravenöz fentanil bradikardiye neden olabildiğinden, preparatın bradiaritmisi olan hastalarda dikkatle kullanılması önerilir. Actiq, karaciğer veya böbrek yetmezliği olan hastlarda dikkatle kullanılmalıdır. Karaciğer ve böbrek yetmezliğinin ilacın farmakokinetiği üzerindeki etkisi değerlendirilmemiştir, ancak hepatik ve renal hastalık durumunda intravenöz olarak uygulandığında, metabolik klerens ve plazma proteinlerindeki değişikliklerden dolayı klerensinin değiştiği gözlenmiştir. Yetersiz karaciğer ve böbrek fonksiyonu, fentanilin biyoyararlanımını arttırıp sistemik klerensini düşürebilir, bu da arttırılmış ve daha uzun opioid etkiye yol açabilir. Bu nedenle orta ve ileri derecede hepatik veya renal hastalarda doz titrasyon işlemleri dikkatle yapılmalıdır. Hipovolemisi ve hipotansiyonu olan hastalarda özellikle dikkat edilmelidir. Diyabetik hastalar preparatın karbonhidrat içeriği konusunda uyarılmalıdır (%93 dekstroz monohidrat ve %7 maltodekstrin; Bir pastil yaklaşık 2 gram glukoz yükü oluşturur Glukoz galaktoz malabsorbsiyonu gibi nadir kalıtsal problemi olan hastalar bu ilacı kullanmamalıdır. Dişlere herhangi bir zarar gelmemesi için normal oral hijyen önerilmektedir. Hasta olmayanların, örneğin kaza sonucu çocukların ilaca maruz kalması olasılığı göz önünde bulundurulmalıdır. Preparat kullanımdan önce ve sonra daima çocukların ve hasta olmayanların görüş alanı dışında ve ulaşamayacakları yerlerde saklanmalıdır. Ürünün kullanımı ve atımı ile ilgili direktifler için bkz. bölüm 6.6. 4.5 Diğer tıbbi ürünler ile etkileşimler ve diğer etkileşim şekilleriFentanil karaciğerde ve intestinal mukozada CYP3A4 izoenzimi tarafından metabolize edilir. Makrolid antibiyotikler gibi, CYP3A4'e karşı etkili inhibitörler, örneğin eritromisin, azol antifungaller, (ketokonazol, itrokanazol, flukanazol)), ve belirli proteaz inhibitörleri, örneğin ritonavir, oral yoldan alınan fentanilin biyoyararlanımını artırabilir ve sistemik klerensini düşürebilir, bu da daha fazla ve uzun opioid etkilere yol açabilir. Benzer bir etki CYP3A4'ü inhibe ettiği bilinen greyfurt suyunun birlikte tüketilmesi sonucunda da görülebilir. Bu nedenle fentanil' in CYP3A4 inhibitörleriyle aynı anda verilmesi konusunda dikkatli davranılması önerilmektedir.Diğer opioidler, sedatifler veya hipnotikler, genel anestezikler, fenotiyazinler, sakinleştiriciler, çizgili kas gevşeticileri, sedatif etkili antihistaminikler dahil olmak üzere başka merkezi sinir sistemi depresanları ve alkolün kullanımı daha fazla depresan etki oluşmasına neden olabilir. Geri-çekilme bulguları, nalokson gibi opioid antagonist etkisi olan ilaçların veya agonist/antagonist karışımı analjeziklerin (örneğin pentazosin, butorfanol, buprenorfin, nalbufin) uygulanmasıyla bastırılabilir. 4.6Gebelik ve laktasyon Genel tavsiye:Gebelik Kategorisi: CÇocuk doğurma potansiyeli bulunan kadınlar / doğum kontrolü (kontrasepsiyon) Gebelik dönemiFentanilin hamile kadınlarda kullanımı konusunda yeterli veri mevcut değildir. Opioid analjezik ajanlar neonatal solunum depresyonuna yol açabilir. Hamilelik sırasında uzun süreli kullanımda neonatal geri-çekilme bulguları riski mevcuttur. Actiq, kesin gerekli olmadığı sürece hamilelerde kullanılmamalıdır.Doğum esnasında fentanil kullanımı önerilmemektedir çünkü fentanil plasentadan geçer ve fetüste solunum depresyonuna yol açabilir. Plasenta yoluyla transfer oranı 0.44'tür (fetal:maternal oran = 1:2.27). Laktasyon dönemiFentanil anne sütüne geçmektedir, bu nedenle çocuklarını emziren anneler, çocukta sedasyon ve/veya solunum depresyonu oluşma ihtimaline karşı Actiq kullanmamalıdır. Son fentanil kullanımının üzerinden en az 24 saat geçmeden emzirme işlemi tekrarlanmamalıdır.Üreme yeteneği / FertiliteHayvanlarla yapılan çalışmalarda fentanilin üremeye bağlı toksisiteye neden olduğu gözlenmiştir (bkz. Bölüm 5.3).4.7Araç ve makine kullanımı üzerindeki etkilerAraç ve makina kullanmaya etkisi konusunda herhangi bir çalışma gerçekleştirilmemiştir. Ancak opioid analjezikler, araç veya makina kullanımı gibi gerçekleştirmesi potansiyel tehlike taşıyan işler için gerekli olan zihinsel ve/veya fiziksel gücü olumsuz etkileyebilir.Hastalar, Actiq kullandıklarında uyku baş dönmesi ve görmede değişiklikler (bulanık görme, çift görme) hissederlerse araç veya makina kullanmamaları konusunda uyarılmalıdır. 4.8 İstenmeyen etkilerActiq kullanımıyla gözlenen advers etkiler tipik opioid yan etkilerdir. Sıklıkla bu opioid yan etkiler, preparatın kullanımına devam edildiği süre içinde ve hastaya en uygun doz ayarlaması yapıldığında yok olur veya şiddeti azalır. Buna rağmen en ciddi advers etkiler arasında apne ve soulunum durmasına yol açabilen solunum depresyonu, dolaşım depresyonu, hipotansiyon ve şok bulunmaktadır ve tüm hastalar bu nedenle yakından izlenmelidir.Pazarlama sonrası ilacın uygulama yeriyle ilgili aralarında dişeti kanamaları ve tahrişinin de bulunduğu yan etkiler bildirilmiştir. Preparatın etkinlik ve emniyet profilini belirlemek için gerçekleştirilen klinik araştırmalar, preparatın ani başlayan şiddetli ağrılara karşı etkinliği değerlendirmek amacıyla tasarlandığı için, tüm hastalar sürekli kalıcı ağrıları için modifiye salımlı morfin veya transdermal fentanil gibi opioidler kullanmaktaydı. Bu nedenle advers etkilerin yalnızca Actiq ile ilişkili olduklarını söylemek zordur. Görülen advers ilaç reaksiyonlarının sıklık sınıflandırması şu şekildedir: Çok yaygın (>1/10); yaygın (>1/100 ila <1/10); yaygın olmayan (>1/1.000 ila <1/100); seyrek (>1/10.000 ila <1/1.000), çok seyrek, izole raporlar dahil (<1/10.000); bilinmiyor (eldeki verilerden hareketle tahmin edilemiyor). Sinir sistemi hastalıkları:Çok yaygın:Uykuya meyil, sersemlik hali.Yaygın:Başağrısı, miyoklonus, tat algılama bozuklukları. Yaygın olmayan: Parestezi (hiperestezi ve ağız çevresi parestezi dahil), anormal yürüyüş/inkoordinasyon. Göz hastalıkları:Yaygın olmayan: Anormal görme (bulanık görme, çift görme).Solunum, göğüs bozuklukları ve mediastinal hastalıkları:Gastrointestinal hastalıkları:Çok yaygın:Bulantı, kabızlık.Yaygın:Kusma, ağızda kuruma, karın ağrısı, idpepsi, ağızda ülserler/stomatit, dil hastalıkları (örneğin dilde yanma hissi, ülserler) Yaygın olmayan: Flatulans, karında şişkinlik. Böbrek ve idrar hastalıkları:Yaygın olmayan: Üriner retansiyon.Deri ve deri altı doku hastalıkları:Yaygın:Kaşıntı, terleme.Yaygın olmayan: Döküntü. Metabolizma ve beslenme hastalıkları:Yaygın olmayan: Anoreksi.Yaralanma ve zehirlenme:Yaygın:Kazayla yaralanma (örneğin düşme)Vasküler hastalıklar:Yaygın:VazodilatasyonGenel bozukluklar ve uygulama bölgesine ilişkin hastalıklar:Yaygın:Asteni:Yaygın olmayan: Kırıklık. Psikiyatrik hastalıklar:Yaygın:Konfüzyon, anksiyete, halüsinasyon, anormal düşünce.Yaygın olmayan: Anormal rüya görme, depersonalizasyon, depresyon, emosyonel labilite, öfori 4.9 Doz aşımı ve tedavisiFentanil doz aşımının semptomlarının intravenöz fentanil ve diğer opioidlerle özellikleri açısından benzer olacağı beklenmektedir ve bu semptomlar farmakolojik etkilerinin bir uzantısı olup en ciddi olanı solunum depresyonudur.Opioid doz aşımının hemen kontrol altına alınması için, preparat hemen aplikatörü yoluyla uzaklaştırılır, temiz hava gelmesi sağlanır, hasta fiziksel ve sözle uyarılır, bilinç seviyesi, nefes ve dolaşım durumu değerlendirilir ve gerekirse solunum desteği verilir. Opioid kullanmamış kişide (kaza sonucu) gerçekleşen doz aşımının tedavisi için, klinik açıdan önerildiği üzere, intravenöz yoldan nalokson veya diğer bir opioid antagonisti kullanılmalıdır. Doz aşımını takip eden solunum depresyonunun etkisi opioid antagonistinin etkisinden uzun olabilir (örneğin, naloksonun yarılanma süresi 30 - 81 dakika arasındadır), bu nedenle tekrar tekrar uygulanması gerekebilir. Bu tür bir kullanım ile ilgili olarak ayrıntılı bilgi için kullanılan opioid antagonistinin Kısa Ürün Bilgisi'ne başvurulmalıdır. Opioid kullanıcısı olan hastalarda doz aşımının tedavisi için intravenöz yoldan müdahele gereklidir. Nalokson veya bir başka opioid antagonistinin kullanımı bazı durumlarda mantıklı olabilir, ancak bir akut geri-çekilme sendromuyla karşılaşma riski mevcuttur. Actiq kullanımından sonra kas sertleşmesine bağlı solunum güçlüğü gözlenmemiştir ancak bu durum fentanile benzer şekilde diğer opioidlerle de görülebilir. Böyle bir durum ile karşılaşılırsa, solunum desteği, bir opioid antagonisti ve son alternatif olarak bir nöromüsküler blokerle kontrol altına alınabilir. 5. FARMAKOLOJİK ÖZELLİKLER 5.1 Farmakodinamik özelliklerFarmakoterapötik grubu: Opioid analjezik, fenilpiperidon türevi ATC kodu: N02A B03.Saf bir opioid agonisti olan fentanil beyin, omuriliği ve düz kas dokusunda yer alan mü-opioid reseptörlerine bağlanarak etki eder. Terapötik etkisi, esas olarak merkezi sinir sistemi (MSS) üzerindendir. Fentanilin mü-opioid reseptörleriyle etkileşiminin klinik açıdan en faydalı farmakolojik etkisi analjezidir. Fentanilin analjezik etkisi etken maddenin, merkezi sinir sistemine girişi için uygun düzey sağlayan kan düzeyleriyle ilişkilidir. Opioid kullanmamış bireylerde analjezi, kandaki seviye 1-2ng/mL olduğunda gerçekleşirken, kandaki seviye 10-20 ng/mL olduğunda cerrahi anestezi ve ileri derecede solunum depresyonu oluşur. Actiq, sürekli kalıcı ağrılarının kontrolü için düzenli bir program kapsamında sabit bir dozda opioid kullanılan kronik kanser ağrılı hastalarda, plasebo ile karşılaştırıldığında, uygulamadan 15, 30, 45 ve 60 dakika sonra ani başlayan şiddetli ağrılara karşı çok daha etkili bulunmuştur. Fentanilin ikincil etkileri arasında gastro-intestinal düz kasların tonusunu arttırması ve kasılmalarını azaltması ile gastro-intestinal transit süresini uzatması yer almaktadır. Bu etkiler opioidlerin kabızlığa neden olmalarını açıklayabilir. Opioidler çoğunlukla idrar yollarının düz kaslarının tonusunu arttırmasına rağmen bunun idrar yapma üzerindeki etkisi değişkendir: bazı durumlarda sık idrar ihtiyacı yaratırken bazen de idrar güçlüğüne neden olabilir. Fentanil dahil tüm mü-reseptörü agonistleri doza bağlı solunum depresyonuna yol açar. Solunum depresyonu riski, ağrısı olan ve kronik opioid tedavisi altında olup solunum depresyonuna ve diğer opioid etkilerine karşı direnç kazanmış olan hastalarda daha azdır. Dirençsiz vakalarda, Actiq uygulamasından 15-30 dakika sonra tipik pik solunum etkileri gözlenir ve birkaç saat devam edebilir. 5.2 Farmakokinetik özelliklerFentanil ileri derecede lipofiliktir ve oral mukoza tarafından çok hızlı absorbe edilir. Gastro-intestinal yoldan daha yavaş absorbe edilir, bu yoldan alındığında hepatik ilk-geçiş etkisine ve intestinal metabolizamaya uğrar ve oluşan metabolitler fentanilin terapötik etkisine katkıda bulunmaz.Emilim:Actiq preparatındaki fentanilin absorbsiyon farmakokinetiği, hızlı oromukozal absorbsiyon ile mide-barsak sisteminden emilen fentanilin yavaş gastro-intestinal absorbsiyonunun bir kombinasyonudur. Uygulanan toplam dozun yaklaşık %25'i bukkal mukoza tarafından hızla absorbe edilir. Dozun geri kalan %75'i mide-barsak sistemine giderek buradan yavaşça absorbe edilir. Bu miktarın yaklaşık 1/3'ü (total dozun %25'i) hepatik ve intestinal ilk geçiş eliminasyonunu aşar ve sistemik terapötik etkiden sorumludur. İntravenöz fentanil ile karşılaştırıldığında nihai biyoyararlanım yaklaşık %50'dir; bunun yarısı hızlı oromukozal yarısı da yavaş gastro-intestinal absorbsiyon şeklindedir. 200-1600 mikrogram Actiq alımından sonra 0.39-2.51 ng/mL düzeyindeki Cmax değerlerine ulaşılır. Tmax süresine; bir Actiq dozunun alınmasında yaklaşık 20-40 dakika sonra (20-480 dakika) ulaşılır. DağılımHayvan deneyleri fentanilin hızla beyin, kalp, akciğerler, böbrek ve dalağa dağıldığını ve sonra daha yavaş bir şekilde kas ve yağ dokusuna dağıldığını göstermiştir. Fentanilin plazma proteine bağlanma oranı %80-85'tir. Ana bağlanma proteini alfa-1-asit glikoproteinidir, ancak albumin ve lipoproteinler de belirli bir oranda katkıda bulunmaktadır. Fentanilin serbest fraksiyonu asidozla birlikte artmaktadır. Sabit plazma düzeylerine ulaşıldığında ortalama dağılım hacmi (VSS) 4 litre/kg'dır. BiyotransformasyonFentanil karaciğer ve intestinal mukozada CYP3A4 isoform tarafından norfentanile metabolize edilir. Hayvan çalışmalarında norfentanil farmakolojik açıdan aktif değildir. Uygulanan fentanil dozunun %90'ından fazlası biyotransformasyon yoluyla N-dealkile edilmiş ve hidroksile edilmiş aktif olmayan metabolitlere dönüştürülerek elimine edilmiştir. EliminasyonDozun %7'sinden azı değişmeden idrarla atılır; değişmeden feçes ile atılan bölümü yalnızca %1 kadardır. Metabolitler çoğunlukla idrar ile atılırken feçes ile atılan miktarlar daha azdır. Fentanilin toplam plazma klerensi 0.5 litre/saat/kg'dır (0.3-0.7 litre/saat/kg aralığı). Nihai eliminasyon yarılanma süresi Actiq uygulamasından yaklaşık 7 saat sonradır. Doğrusallık / doğrusal olmayan durumActiq'in mevcut farmasötik dozaj şekilleri ile dozaj arasında (200 mikrogram-1600 mikrogram) doğru orantı olduğu gösterilmiştir. 5.3 Klinik öncesi güvenlilik verileriKlasik güvenlilik farmakolojisi, tekrarlayan doz toksisitesi ve genotoksisite çalışmalarından elde edilen klinik öncesi veriler insanlara yönelik özel bir zararın bulunmadığını göstermektedir.Dişi sıçanlarda yapılan çalışmalarda fertilitede azalma ve embryo mortalitesinde artış gösterilmiştir. Daha yakın zamanda yapılan çalışmalar embryo üzerindeki etkilerin, maddenin gelişmekte olan doğrudan etkisine bağlı olarak değil, maternal toksisiteyle ilişkili olduğunu göstermiştir. Pre ve postnatal gelişimle ilgili yapılan bir çalışmada, maternal ağırlığı hafifçe azaltan dozların, yavrulardaki sağkalım oranlarını anlamlı olarak düşürdüğü gösterilmiştir. Bu etki ya değişen maternal şartlara ya da fentanilin annelerdeki doğrudan etkisine bağlı olabilir. Yavruların somatik gelişiminde ve davranışlarında etki gözlenmemiştir. Teratojen etki gösterilmemiştir. Uzun dönem karsinojenite çalışmaları yapılmamıştır. 6. FARMASÖTİK ÖZELLİKLERİ 6.1 Yardımcı maddelerin listesiDekstratlar (glukoz içeren) Susuz sitrik asit Susuz disodyum fosfatYapay çilek aroması (maltodekstrin, propilen glikol, yapay aromalar ve trietilsitrat) Magnezyum stearat Pastili çubuğa tutturmak için kullanılan yenebilir yapıştırıcı:Modifiye gıda mısır nişastası (E1450) Şekerleme şekeri (sukroz ve mısır nişastası) Saf suBaskı için kullanılan mürekkep:Deiyonize su De-waxed beyaz shellac Propilen glikolSentetik mavi kömür zifti boyası (E133) 6.2GeçimsizliklerBulunmamaktadır.6.3Raf ömrü3 yıl.6.4Saklamaya yönelik özel tedbirler30 °C üzeri sıcaklıklarda saklanmamalıdır.6.5Ambalajın niteliği ve içeriğiHer bir dozdaki Actiq, folyo kaplı kağıt ve ısı ile şekillendirilmiş PVC/Aclar' ın yine ısı ile birleştirilmesinden oluşan blister ambalajlarda bulunmaktadır ve 3 ünite içeren karton kutularda sunulmaktadır.6.6Tıbbi üründen arta kalan maddelerin imhası ve diğer özel önlemler(Ayrıntılı kullanım bilgileri için bkz. 4.2)Hastalar ve bakıcıları Actiq'de bulunan aktif maddenin bir çocuk için fatal olabilecek miktarda olduğu konusunda uyarılmalıdır. Hastalar ve bakıcıları, tüm ünitelerin çocukların ulaşamayacakları yerlerde saklanması ve açılmış olan preparatın uygun şekilde atılması konusunda uyarılmalıdır. Üzerinde aktif madde kalıntısı olan pastil hiç bir zaman atılmamalı veya yanlış bir yere konmamalıdır. Kullanılmış olan ürün veya ürün ile ilgili herhangi bir artık madde yerel uygulamalar doğrultusunda imha edilmelidir. 7. RUHSAT SAHİBİAdı:Genesis İlaç ve Sağlık Ürünleri A.Ş.Adresi:Ömer Avni Mah. İnebolu Sokak. Sümbül Konak Apt. No: 85 K:2 D:334427 Beyoğlu, İstanbul Tel. No.:(+90) 212 - 245 55 80Faks No.:(+90) 212 - 245 57 33Üretim yeri:Cephalon Corporation, Salt Lake City, Utah 84116 ABD8.RUHSAT NUMARASI119/809.İLK RUHSAT TARİHİ / RUHSAT YENİLEME TARİHİİlk ruhsat tarihi:03.04.2006Ruhsat yenileme tarihi: 10.KÜB'ÜN REVİZYON TARİHİ |
İlaç BilgileriActiq 400mcg oromukozal aplikatörlü pastilEtken Maddesi: Fentanil Atc Kodu: N02AB03 Kullanma talimatı ve kısa ürün bilgileri
Google Reklamları
İlgili İlaçlar |
Ana Sayfa | Hakkımızda | İlaçlar | İlaç Ara | İlaç Firmaları | Gizlilik | Bize Ulaşın
Telif Hakkı 2008-2026 © İlaç Prospektüsü. Tüm Hakları Saklıdır.Uyarı: Sitemizde yayınladığımız ilaç bilgileri ile doktora danışmadan kesinlikle ilaç kullanmayınız!
Aksi halde doğabilecek sağlık sorunlarından ilacprospektusu.com sorumlu tutulamaz.