Spectracef pediyatrik saşe 30 mg Kısa Ürün BilgisiEnfeksiyona Karşı Kullanılan (Antienfektif) İlaçlar » Antibakteriyel (Antibiyotik) İlaçlar » Diğer BetaLaktam Antibakteriyeller » 3. Kuşak Sefalosporinler » Sefditoren Pivoksil KISA URUN BILGILERI1. BEŞERİ TIBBI ÜRÜNÜN ADISPECTRACEF PEDİATRİK saşe 30 mg/0.3 g2. KALITATIF VE KANTİTATIF BILEŞIMEtkin madde:Her 1 gramda 100 mg sefditoren pivoksil içerir.Yardımcı maddeler:Kroskarmelloz Sodyum 30 mgSukroz kafi miktarda Yağ asidi sükroz esterleri 0.3 mg Aspartam (E951) 120 mg Sodyum Klorür 1.0 mg Yardımcı maddeler için 6.1'e bakınız. 3. FARMASÖTIK FORMGranül4. KLİNIK ÖZELLIKLER4.1. Terapötik endikasyonlarSPECTRACEF PEDİATRİK, aşağıda belirtilen durumlarda, duyarlı mikroorganizmaların neden olduğu, hafif ve orta dereceli enfeksiyonların tedavisinde endikedir. Üst solunum yolu enfeksiyonları: farenjit/larenjit, tonsillit (peritonsilit ve peritonsiller abse dahil), otitis media, sinüzit, kızıl, boğmaca, Alt solunum yolu enfeksiyonları: akut bronşit, pnömoni, akciğer absesi, kronik solunum sistemi lezyonlarına ikincil gelişen enfeksiyonlar, Deri enfeksiyonları,travmaya bağlı ikincil enfeksiyonlar, perianal abse, lenfanj it/lenfadenit, Üriner enfeksiyonlar: sistit, piyelonefrit, Dental enfeksiyonlar: periodontal doku enflamasyonu.4.2. Pozoloji ve uygulama şekli Pozoloji/uygulama sıklığı ve süresi:Sefditoren Pivoksil çocuklarda genellikle oral yoldan günde 3 kez, her bir seferde 3 mg/kg olacak şekilde yemeklerden sonra uygulanır.Doz, hekim tarafından hastanın yaş ve semptomlarına göre ayarlanabilir. Hekim tarafından başka türlü önerilmediği takdirde: 3 ay -1,5 yaş arası çocuklarda:30 mg'lık saşeden 8 saat arayla (günde 3 kez)1 saşe önerilir.1,5 - 12 yaş arası çocuklar için Spectracef Pediatrik Saşe 50 mg/0.5g kullanılması önerilir. Erişkin dozunun üst sınırı olan günlük 600 mg aşılmamalıdır. Uygulama şekli:Saşe içeriği, şekilde görüldüğü gibi oda sıcaklığındaki bir miktar içme suyu ile karıştırılarak hazırlandıktan sonra bekletmeden içilmelidir. Su yerine yiyeceklere karıştırılarak da alınabilir.Şekil: Spectracef Pediatrik Saşe 30 mg/0.3 g'ın kullanıma hazırlanması 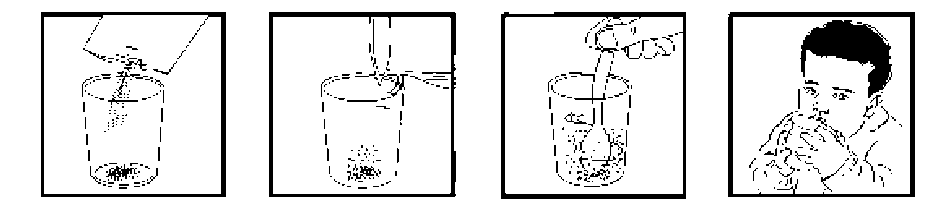
Özel popülasyonlara ilişkin ek bilgiler:Böbrek yetmezliği:Hafif böbrek yetmezliği (Kreatinin Klerensi 51-80 ml/dk) ve orta derecede böbrek yetmezliği (Kreatinin Klerensi 30-50 ml/dk) olan hastalarda doz 8 saatte bir 3 mg/kg'ı aşmamalıdır. Ağır böbrek yetmezliği (Kreatinin Klerensi<30 ml/dk) olan hastalarda doz 12 saatte bir 3 mg/kg'ı aşmamalıdır.Karaciğer yetmezliği:Özel bir kullanım şekli belirtilmemiştir.Pediyatrik popülasyon:Düşük doğum ağırlıklı bebekler ve düşük doğum ağırlıklı yenidoğanlarda güvenliği belirlenmemiştir.Geriyatrik popülasyon:Özel bir kullanım şekli belirtilmemiştir.4.3. KontrendikasyonlarSPECTRACEF PEDİATRİK, sefalosporin grubu antibiyotiklere veya bileşenlerinden birine alerjisi olduğu bilinen hastalarda, karnitin eksikliği olan veya klinik olarak anlamlı karnitin eksikliği ile sonuçlanabilen doğumsal metabolizma bozuklukları olan hastalarda kontrendikedir.Aspartam içerdiği için fenilketonürili hastalarda kullanılmamalıdır. Nadir kalıtımsal früktoz intoleransı, glikoz-galaktoz malabsorpsiyon veya sükraz-izomaltaz yetmezliği problemi olan hastaların bu ilacı kullanmamaları gerekir. 4.4. Özel kullanım uyarıları ve önlemleriTüm sefalosporin preparatlarında olduğu gibi, SPECTRACEF PEDİATRİK (sefditoren pivoksil) tedavisine başlamadan önce hastanın önceden sefditoren pivoksil, diğer sefalosporinler, penisilinler veya diğer ilaçlara aşırı duyarlılık reaksiyonu gösterip göstermediği dikkatlice araştırılmalıdır. Sefditoren pivoksile karşı alerjik bir reaksiyon ortaya çıkarsa, ilaç kesilmelidir. Ağır, akut aşırı duyarlılık reaksiyonları, epinefrin ve oksijen, intravenöz sıvı, intravenöz antihistaminikler, kortikosteroidler, pressör aminler ile tedaviyi gerektirebilir. Klinik olarak endike ise, hava yolunun açık tutulmasını gerektirebilir.Hastanın kendisinde veya ailesinde bronşiyal astım, döküntü, ürtiker gibi alerjik hastalıklara yatkınlığı olanlarda dikkatli kullanılmalıdır.Ağır böbrek yetmezliği olanlarda serum konsantrasyonları yüksek kalacağı için dikkatli kullanılmalıdır. Oral beslenmede problemleri olan ya da parenteral beslenen hastalarda ve genel sağlık durumu bozuk olan hastalarda K vitamini eksikliği olabileceği için dikkatli kullanılmalıdır. Sefditoren pivoksil dahil olmak üzere, hemen hemen tüm antibakteriyel ajanlarla, hafiften hayatı tehdit edici şiddete kadar değişen psödomembranöz kolit bildirilmiştir.Dolayısıyla, antibakteriyel ajanların uygulamasını takiben diyare olan hastalarda bu tanının göz önünde bulundurulması önemlidir. Antibakteriyel ajanlarla tedavi, normal kolon florasını değiştirir ve klostridiumlar üreyebilir. Çalışmalar, Clostridium difficile'ninClost^ridi^^ difficilekolitine karşı klinik olarak etkili bir antibakteriyel ilaç ile tedavi edilmelidir.Sefditoren pivoksilin serum karnitin düzeyini düşürdüğü bildirildiği için ürünün çocuklarda 2 haftadan daha uzun süreyle kullanılması tavsiye edilmemektedir. İki haftayı geçen zorunlukullanımlarda karnitin düzeyine bakılarak, eksiklik durumunda karnitin verilmelidir.Diğer antibiyotiklerle olduğu gibi, uzun süreli tedavi dirençli organizmaların ortaya çıkıp, üremesiyle sonuçlanabilir. Tedavi sırasında süperinfeksiyon ortaya çıkarsa, hastanın dikkatle gözlenmesi gerekir. Bu durumda uygun alternatif tedavi uygulanmalıdır. Sefalosporinler, protrombin aktivitesini azaltabilir. Renal veya hepatik bozukluğu olan hastalar, beslenme durumu kötü olanlar, uzun süreli antimikrobiyal tedavi alan hastalar ve antikoagülan tedavide stabilize edilen hastalar risk altındadır. Riskli hastalarda protrombin zamanı izlenmelidir ve endike olduğunda, ekzojen K vitamini uygulanmalıdır. Klinik çalışmalarda, protrombin zamanı artışı insidansında sefditoren ve karşılaştırılan sefalosporinler arasında farklılık bulunmamıştır. 4.5. Diğer tıbbi ürünler ile etkileşimler ve diğer etkileşim şekilleriAntasidler ve H2-reseptör antagonistleri:Sefditoren pivoksilin magnezyum ve aluminyum içeren antasidlerle birlikte kullanılması ilacın absorbsiyonunu azaltacağından önerilmez. Aynı etkileşim H2 reseptör antagonistleri ile de meydana geldiğinden sefditoren pivoksilin H2 reseptör antagonistleriyle birlikte verilmesi önerilmez. Probenesid: Diğer P-laktam antibiyotiklerle olduğu gibi, probenesidin sefditoren pivoksil ile birlikte verilmesi sefditorenin plazma düzeylerinde artışla sonuçlanmıştır; İlaç / Laboratuar testi etkileşmeleri: Sefalosporinlerin bazen, pozitif direkt Coombs testine yol açtığı bilinmektedir. Bakır indirgeme testleri ile idrarda yalancı pozitif glukoz reaksiyonu görülebilir, fakat enzim tabanlı testlerle glukozüri gözükmez. 4.6. Gebelik ve laktasyon Genel tavsiye Gebelik Kategorisi BÇocuk doğurma potansiyeli bulunan kadınlar/Doğum kontrolü (Kontrasepsiyon)SPECTRACEF için, gebeliklerde maruz kalmaya ilişkin klinik veri mevcut değildir.Gebe kadınlarda yeterli ve kontrollü çalışmalar yoktur. Hayvanlar üzerinde yapılan çalışmalar, gebelik/embriyonal/fetal gelişim/doğum ya da doğum sonrası gelişim ile ilgili olarak doğrudan ya da dolaylı zararlı etkiler olduğunu göstermemektedir. Gebe kadınlara verilirken tedbirli olunmalıdır. Gebelik dönemiHayvanlarda yapılan çalışmalarda teratojenik etkiler saptanmamakla birlikte, gebe kadınlarda yeterli ve kontrollü çalışmalar yoktur. Birçok ilaç anne sütüne geçtiğinden, emziren annelere sefditoren pivoksil uygulanırken dikkatli olunmalıdır.Laktasyon dönemiSefditoren pivoksil'in insan ya da hayvan sütü ile atılmasına ilişkin yetersiz/sınırlı bilgi mevcuttur. Memedeki çocuk açısından bir risk olduğu gözardı edilemez. Emzirmenin durdurulup durdurulmayacağına ya da sefditoren pivoksil tedavisinin durdurulup durdurulmayacağına/tedaviden kaçınılıp kaçınılmayacağına ilişkin karar verilirken, emzirmenin çocuk acısından faydası ve sefditoren pivoksil tedavisinin emziren anne açısından faydası dikkate alınmalıdır.Üreme yeteneği /Fertiliteİnsanlar üzerinde ya da klinik dışı üreyebilirlik çalışmalarından elde edilmiş veriler mevcut değildir.4.7. Araç ve makine kullanımı üzerindeki etkilerAraç ve makine kullanımı üzerine hafif ya da orta şiddette etkisi mevcuttur. Sefditoren pivoksil baş dönmesi ve uyku haline sebep olabilir.4.8. İstenmeyen etkilerÇok yaygın (>1/10); yaygın (>1/100 ila <1/10); yaygın olmayan (>1/1000 ila <1/100); seyrek (>1/10000 ila <1/1000); çok seyrek (< 1/10000), bilinmiyor (eldeki verilerden hareketle tahmin edilemiyor).EnfeksiyonlarSeyrek: Stomatit, kandidiazisKan ve lenf sistemi hastalıklarıSeyrek: Agranülositoz, hemolitik anemi, granülositopeni, trombositopeni, Vitamin K eksikliği belirtileri (hipoproteinemi, kanama eğilimi vb.)Bağışıklık sistemi hastalıklarıSeyrek: Şok, anafilaktoid reaksiyon, ateş, lenf düğümünde şişme, artraljiSinir sistemi hastalıklarıSeyrek: Vitamin B kompleksi eksikliği (glossit, stomatit, anoreksi, nörit vb.), baş ağrısı, baş dönmesi, ödem, uyuşuklukSolunum, göğüs bozuklukları ve mediastinal hastalıklarıSeyrek: İnterstisyel pnömoni, PİE sendromuGastrointestinal hastalıklarıYaygın: Diyare, gevşek dışkı, bulantı, karında rahatsızlık, karın ağrısıSeyrek:Psödomembranöz kolit, kanlı gaitanın görüldüğü ciddi kolit, karında büyüme hissi, kusma Hepato - bilier hastalıklarıSeyrek: Sarılık, Al-P artışıDeri ve deri altı doku hastalıklarıYaygın: DöküntüSeyrek: Muko-kutaneo-oküler sendrom (Stevens-Johnson sendromu), toksik epidermal nekrolizis (Lyell sendromu), ürtiker, eritem, kaşıntı Böbrek ve idrar hastalıklarıSeyrek: Akut renal yetmezlik, ciddi renal disfonksiyon, BUN artışıAraştırmalarYaygın: Eozinofili, AST artışı, ALT artışı (Uzun süreli tedavide daha sık görülme eğilimi vardır.)4.9. Doz aşımı ve tedavisiİnsanda sefditoren pivoksilin doz aşımıyla ilgili bilgi yoktur. Ancak, diğer P-laktam antibiyotiklerle, doz aşımını takip eden bulantı, kusma, epigastrik rahatsızlık, diyare ve konvülsiyonlar gibi advers etkiler görülmüştür. Hemodiyaliz, sefditorenin vücuttan uzaklaştırılmasına, özellikle böbrek fonksiyonu kısıtlı olanlarda neden olabilir (4 saat hemodiyalizi takiben plazma konsantrasyonlarında % 30 azalma). Doz aşımı semptomatik olarak tedavi edilir ve gerektiğinde destekleyici önlemler alınır.5. FARMAKOLOJIK ÖZELLIKLERI5.1. Farmakodinamik özelliklerFarmakoterapötik Grup: İnfeksiyona karşı kullanılan ilaçlar - Sefalosporinler (3. kuşak)ATC Kodu: J01DD16 SPECTRACEF PEDİATRİK, oral uygulama için yarı-sentetik bir sefalosporin olan sefditoren pivoksil içerir. Sefditoren pivoksil bir ön ilaç olup, absorbsiyon sırasında esterazlar tarafından hidrolize edilerek aktif formu olan sefditoren'e dönüşür. Sefditoren, gram-pozitif ve gram-negatif patojenlere karşı antibakteriyel aktivitesi olan bir sefalosporindir. Sefditorenin bakterisid aktivitesi, penisilin bağlayıcı proteinlere (PBPs) olan afinitesi yoluyla, bakteri hücre duvarı sentezinin inhibisyonuna dayanır. Sefditoren, penisilinaz ve bazı sefalosporinazlar da dahil olmak üzere, çeşitli P-laktamazların varlığında stabildir. Sefditorenin, Endikasyonlar bölümünde tanımlandığı gibi, hem in vitro,hem de klinik enfeksiyonlarda, aşağıdaki bakterilerin birçok suşuna karşı aktif olduğu gösterilmiştir:Stafilokok türleri, Streptokok türleri, Streptococcus pneumonia, Moraxella (Branhamella) catarrhalis, Escherichia coli, Sitrobakter türleri, Klebsiella türleri, Enterobakter türleri, Serratia türleri, Proteus türleri, Morganella morganii, Providencia türleri, Haemophilus influenzae, Bordetella pertussis, Peptostreptokok türleri, Bakteroides türleri, Prevotella türleri ve Propionibacterium acne'nin Sefditoren'e duyarlı olan suşları.5.2 Farmakokinetik özelliklerAbsorpsiyon ve dağılım:Böbrek fonksiyonu normal olan pediatrik hastalarda öğünlerden sonra verilen 3 mg/kg veya 6 mg/kg tek doz oral sefditorenin farmakokinetik parametreleri aşağıdaki tabloda gösterilmektedir:
Ultrafiltrasyon yöntemiyle belirlenen insan serum proteinine bağlanma oranı 25 ^g/ml'lik konsantrasyonda % 91.5 olarak tespit edilmiştir (in vitro'). Metabolizma ve atılım:Sefditoren pivoksil absorpsiyon sırasında, antibakteriyel aktivitesi olan sefditorene ve pivolik asite dönüşür. Pivolik asit karnitinle konjuge edilerek pivaloil karnitin olarak idrarla atılır. Sefditoren çok az metabolize olur ve esas olarak idrar ve safra ile atılır. Böbrek fonksiyonları normal olan pediatrik hastalarda yemeklerden sonra uygulanan 3 mg/kg ve 6 mg/kg dozundaki sefditorenin üriner atılım oranı (0-8 saat) sırasıyla % 20 ve % 17'dir. 5.3. Klinik öncesi güvenlilik verileriBilinen emniyet farmakolojisi, doz toksisitesi, genotoksisite ve üreme toksisitesi çalışmalarından gelen preklinik veriler insanlara zararına dair bir bulgu göstermemektedir.Sefditoren pivoksilin karsinojenik potansiyelini değerlendirmek için yapılacak olan çalışmalar henüz yapılmamıştır. 6. FARMASÖTİK ÖZELLİKLER6.1. Yardımcı maddelerin listesiKroskarmelloz Sodyum SukrozHidroksipropil metil selüloz 2910 Yağ asidi sükroz esterleri Aspartam (E951) Sodyum Klorür Muz Tozu (SK-043) Karışık Aroma Tozu (WH-11912) Sunset Sarısı (Food Yellow No:5) 6.2. GeçimsizliklerBildirilmemiştir.6.3. Raf ömrü36 ay6.4. Saklamaya yönelik özel tedbirler25°C'nin altında, oda sıcaklığında saklanmalıdır.Nem ve güneş ışığına maruz bırakılmamalıdır. 6.5. Ambalajın niteliği ve içeriği21 adet 0.3 mg'lık poşet içeren ambalajlarda.6.6. Beşeri tıbbi üründen arta kalan maddelerin imhası ve diğer özel önlemlerKullanılmamış olan ürünler ya da atık materyaller Tıbbi Atıkların Kontrolü Yönetmeliği ve Ambalaj ve Ambalaj Atıkları Kontrolü Yönetmeliğine uygun olarak imha edilmelidir.7. RUHSAT SAHİBİABDİ İBRAHİM İLAÇ PAZARLAMA AŞ.Reşitpaşa Mahallesi, Eski Büyükdere Caddesi No: 4 34397 Maslak/Sarıyer/İstanbul 8. RUHSAT NUMARASI123/609. İLK RUHSAT TARİHİ / RUHSAT YENİLEME TARİHİİlk ruhsat tarihi: 30.11.2007 Ruhsat yenileme tarihi:10. KÜB'ÜN YENİLENME TARİHİ |
İlaç BilgileriSpectracef pediyatrik saşe 30 mgEtken Maddesi: Sefditoren Atc Kodu: J01DD16 Kullanma talimatı ve kısa ürün bilgileri
Google Reklamları
İlgili İlaçlar |
Ana Sayfa | Hakkımızda | İlaçlar | İlaç Ara | İlaç Firmaları | Gizlilik | Bize Ulaşın
Telif Hakkı 2008-2026 © İlaç Prospektüsü. Tüm Hakları Saklıdır.Uyarı: Sitemizde yayınladığımız ilaç bilgileri ile doktora danışmadan kesinlikle ilaç kullanmayınız!
Aksi halde doğabilecek sağlık sorunlarından ilacprospektusu.com sorumlu tutulamaz.