Oculotect Fluid steril göz damlası Kısa Ürün BilgisiDuyu Organları » Göze Uygulanan İlaçlar » Diğer Göz İlaçları » Göz İle İlgili Diğer İlaçlar » Suni Gözyaşı KISA ÜRÜN BİLGİSİ1. BEŞERİ TIBBİ ÜRÜNÜN ADIOCULOTECT FLUID steril göz damlası2. KALİTATİF VE KANTİTATİF BİLEŞİMEtkin madde:1 ml çözeltide;Polividon 50 mg Yardımcı maddeler:1 ml çözeltide;Benzalkonyum klorür 0,05 mg Yardımcı maddeler için 6.1'e bakınız. 3. FARMASÖTİK FORMGöz damlası, çözeltiHemen hemen renksiz, berrak sulu çözelti 4. KLİNİK ÖZELLİKLER4.1. Terapötik endikasyonlarKuru keratokonjunktivit de dahil, göz kuruluğu durumlarının (gözyaşı filminin dayanıksız olduğu durumlarda gözyaşı yerine veya göz yüzeyinin nemlenmesinin yetersiz olduğu durumlarda) semptomatik tedavisi için kullanılır.4.2. Pozoloji ve uygulama şekli Pozoloji/uygulama sıklığı ve süresi:Doktor tarafından başka şekilde tavsiye edilmediği takdirde günde 4 defa 1 damla (veya hastalığın şiddetine göre gerektikçe) konjunktiva kesesi içine damlatılır.Orijinal kapak açılıncaya kadar solüsyon sterilitesini korur. Solüsyonun kontamine olması riski olduğundan, şişenin ucunun herhangi bir yüzeyle temasından ve göze hasar verebileceğinden gözle temasından kaçınılmalıdır. Açıldıktan sonra 4 haftadan daha uzun süre kullanmayınız; kalan kısmı atınız. Uygulama şekli:Yalnız oftalmik kullanım içindir. Göze damlatılarak uygulanır.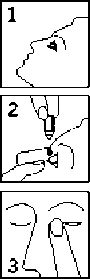 1. Başınızı arkaya doğru eğiniz; bir elinizle alt göz kapağınızı yavaşça aşağıya doğru çekiniz. 2. Diğer elinizle şişeyi başaşağı, gözünüzün üstünde dik olarak tutup yavaşça sıkarak bir damla damlatınız. Damlalığın ucunu gözünüze değdirmemeye dikkat ediniz. 3. Damlattıktan sonra gözünüzün iç ucuna parmak ucunuz ile 1-2 dakika bastırınız. Bu, ilacın gözyaşı kanallarından buruna akmasını önler. Özel popülasyonlara ilişkin ek bilgiler:Böbrek/Karaciğer yetmezliği:OCULOTECT FLUID'in böbrek veya karaciğer yetmezliğinde etkinlik ve güvenliliği çalışılmamıştır.Pediyatrik popülasyon:OCULOTECT FLUID'in çocuklarda etkinlik ve güvenliliği çalışılmamıştır.Geriyatrik popülasyon:Yaşlılarda özel bir doz ayarlamasına gerek yoktur.4.3. KontrendikasyonlarOCULOTECT FLUID'in içeriğindeki maddelerden herhangi birine karşı aşırı duyarlılığı olduğu bilinen hastalarda kontrendikedir.4.4. Özel kullanım uyarıları ve önlemleriKuru gözde iritasyon devam eder veya kötüleşirse, tedavi durdurulmalı ve hasta doktoruna başvurmalıdır.OCULOTECT FLUID koruyucu olarak benzalkonyum klorür içerdiğinden gözde irritasyona sebebiyet verebilir. Yumuşak kontakt lenslerle temasından kaçınınız. Uygulamadan önce kontakt lensi çıkartınız ve lensi takmak için en azından 15 dakika bekleyiniz. Yumuşak kontakt lenslerin renklerinin bozulmasına neden olduğu bilinmektedir. 4.5. Diğer tıbbi ürünler ile etkileşimler ve diğer etkileşim şekilleriOCULOTECT FLUID'e ek olarak başka göz ilaçları (örneğin glokom tedavisi için) kullanılması gerektiğinde, iki ilaç en az 5 dakika ara ile uygulanmalı ve OCULOTECT FLUID daima daha sonra damlatılan ilaç olmalıdır.4.6. Gebelik ve laktasyonGenel tavsiyeGebelik Kategorisi: CÇocuk doğurma potansiyeli bulunan kadınlar/Doğum kontrolü (Kontrasepsiyon)Çocuk doğurma potansiyeli bulunan kadınlarda ve doğum kontrolü (kontrasepsiyon) uygulayanlarda ilacın kullanımı yönünden bir öneri bulunmamaktadır.Gebelik dönemiOCULOTECT FLUID'in gebe kadınlarda kullanımına ilişkin yeterli ve kontrollü çalışmalar yoktur. Reprodüktif toksisite bazında hayvan çalışmaları yetersizdir.OCULOTECT FLUID gerekli olmadıkça gebelik döneminde kullanılmamalıdır. Laktasyon dönemiPolividonun insan sütüyle atılıp atılmadığı bilinmemektedir. Bu nedenle, OCULOTECT FLUID gerekli olmadıkça emzirme döneminde kullanılmamalıdır.Üreme yeteneği/FertiliteÜreme yeteneği üzerindeki etkisi araştırılmamıştır.4.7. Araç ve makine kullanımı üzerindeki etkilerGeçici görüş bulanıklığı araç veya makine kullanımı yeteneğini etkileyebilir. Görüş bulanıklığı oluşursa hastalar görüşleri düzelene kadar beklemelidirler.4.8. İstenmeyen etkilerİstenmeyen etkiler çok yaygın (>1/10); yaygın (>1/100 ila <1/10); yaygın olmayan (>1/1000 ila <1/100); seyrek (>1/10.000 ila <1/1000); çok seyrek (<1/10.000), bilinmiyor (eldeki verilerden hareketle tahmin edilemiyor) olarak listelenmiştir.Aşağıdaki advers etkiler klinik çalışmalarda bildirilmiştir: Bağışıklık sistemi hastalıklarıÇok seyrek:İritasyon veya hipersensitivite reaksiyonları. Göz hastalıklarıYaygın:Hafif, geçici yanma ya da yapışkanlık hissi. Aşağıdaki advers etkiler pazarlama sonrası advers etkilerdir: Göz hastalıklarıBilinmiyor (eldeki verilerden hareketle tahmin edilemiyor): Görüş bulanıklığı4.9. Doz aşımı ve tedavisiDoz aşımı vakası bildirilmemiştir.Çözeltinin fazlası gözden dışarıya akacağı için göze kazayla 1 damladan fazla damlatılması genelde bir sorun teşkil etmez. 5. FARMAKOLOJİK ÖZELLİKLER5.1. Farmakodinamik özelliklerFarmakoterapötik grup: Diğer oftalmolojikler ATC kodu: S01XA20OCULOTECT FLUID, farmakolojik bileşen içermemektedir. Tahriş edici olmayan suda çözünen polimerler fiziksel özellikleri nedeniyle göz yüzeyinde nemlendirme ve kaydırıcı özellikleri için kullanılabilir. OCULOTECT FLUID hemen hemen renksiz, steril, damla şeklinde kullanılan, berrak sulu bir çözeltidir. Uygulandıktan sonra konjunktiva ve kornea üzerine hızla yayılarak kaydırıcı ve koruyucu bir film oluşturur. Etkin madde olarak polividon içeren OCULOTECT FLUID'in yukarıda belirtilen bileşimi doğal gözyaşına çok benzer. Kornea yüzeyinin nemlendirilmesi başlıca, konjunktivada üretilen musin sayesinde olur. Musin kornea yüzeyine adsorbe edilir ve hidrofil bir yüzey oluşturur. Göz kuruluğu, yani yetersiz gözyaşı salgılanması veya yetersiz musin üretimi durumunda göz kırpmaları arasında gözyaşı filmi vaktinden önce dağılır. Önce korneada kuru benekler ve daha sonra yüzeysel benekli keratit (keratitis superficialis punctata) görülebilir. Bu, ışıktan çekinme, yanma ve yabancı cisim duygusu gibi güçlü sübjektif semptomlara yol açar. Özellikle musin yetersizliği halinde, toksik olmayan, suda çözünen polimerlerin göz damlası şeklinde verilmesinin, kısmen eksik musin üretimini telafi ederek, tedavi edici etkisi olduğu görülmüştür. Polividon bu gruba ait bir maddedir. 5.2. Farmakokinetik özelliklerPolividonun molekül büyüklüğü nedeniyle korneadan penetrasyonu mümkün değildir. Bu nedenle oküler kullanım sonrası farmakokinetik parametreleri mevcut değildir.5.3. Klinik öncesi güvenlilik verileriSıçanların besinlerine 2 yıl süresince % 5 ve % 10 PVP K25 (polividon) eklenmesinin ardından herhangi bir toksik etki gözlenmemiştir. Mutajenite ve teratojenite ile ilgili veri mevcut değildir.6. FARMASÖTİK ÖZELLİKLER6.1. Yardımcı maddelerin listesiBenzalkonyum klorür Borik asit Sodyum klorür Sodyum laktat Potasyum klorür Kalsiyum klorür Magnezyum klorür Enjeksiyonluk su6.2. GeçimsizliklerYüksek tuz konsantrasyonları (örneğin soğukta sodyum sülfat ve sıcakta sodyum klorür) polividonun çökmesi ile sonuçlanabilir. Çözeltinin iyonik gücüne bağlı olarak metil- ve propilhidroksibenzoatlar polividon ile kolayca kompleks oluşturabilir.6.3. Raf ömrü24 ayİlk kez açılmasının ardından: 4 hafta 6.4. Saklamaya yönelik özel tedbirler25°C'nin altındaki oda sıcaklığında saklayınız.Kullandıktan sonra kapağını hemen kapatınız. Işıktan korumak için şişeyi dış ambalajı içerisinde saklayınız. 6.5. Ambalajın niteliği ve içeriğiSaydam PP damlalık ve entegre güvenlik halkalı beyaz HDPE kapaklı saydam PP şişe.Bir şişe 10 ml çözelti içerir. 6.6. Beşeri tıbbi üründen arta kalan maddelerin imhası ve diğer özel önlemlerKullanılmamış olan ürünler ya da atık materyaller Tıbbi Atıkların Kontrolü Yönetmeliği ve Ambalaj Atıklarının Kontrolü Yönetmeliklerine uygun olarak imha edilmelidir.7. RUHSAT SAHİBİNovartis Ürünleri 34912 Kurtköy - İstanbul8. RUHSAT NUMARASI103 / 229. İLK RUHSAT TARİHİ/RUHSAT YENİLEME TARİHİİlk ruhsat tarihi:28.11.1997Ruhsat yenileme tarihi: 14.11.2007 tarihinde ruhsat yenileme başvurusu yapılmıştır.10. KÜB 'ÜN YENİLENME TARİHİ |
İlaç BilgileriOculotect Fluid steril göz damlasıEtken Maddesi: polividon Atc Kodu: S01XA20 Kullanma talimatı ve kısa ürün bilgileri
Google Reklamları
İlgili İlaçlar |
Ana Sayfa | Hakkımızda | İlaçlar | İlaç Ara | İlaç Firmaları | Gizlilik | Bize Ulaşın
Telif Hakkı 2008-2026 © İlaç Prospektüsü. Tüm Hakları Saklıdır.Uyarı: Sitemizde yayınladığımız ilaç bilgileri ile doktora danışmadan kesinlikle ilaç kullanmayınız!
Aksi halde doğabilecek sağlık sorunlarından ilacprospektusu.com sorumlu tutulamaz.