Zinnat Forte 250 mg/5 ml süspansiyon hazırlamak için granül Kısa Ürün BilgisiEnfeksiyona Karşı Kullanılan (Antienfektif) İlaçlar » Antibakteriyel (Antibiyotik) İlaçlar » Diğer BetaLaktam Antibakteriyeller » İkinci Kuşak Sefalosporinler » Sefuroksim KISA URUN BILGISI 1. BEŞERI TIBBI ÜRÜNÜN ADIZINNAT forte 250 mg/5 ml süspansiyon hazırlamak için granül2. KALITATIF VE KANTİTATIF BILEŞIM ETKIN MADDE:5 ml'de süspansiyonda:Sefuroksim 250 mg Yardımcı maddeler:Sukroz 2289 mgAspartam 45 mg Yardımcı maddeler için 6.1'e bakınız. 3. FARMASÖTIK FORMSüspansiyon hazırlamak için granülMüstahzar, sulandırıldığında beyaz - soluk sarı süspansiyon oluşturan, serbest akış gösteren, beyazımsı granüller halindedir. 4. KLİNIK ÖZELLIKLER4.1. Terapötik endikasyonlarZINNAT duyarlı mikroorganizmaların sebep olduğu enfeksiyonların tedavisinde endikedir. Endikasyonları aşağıdakileri içerir:Üst solunum yolu enfeksiyonları:Kulak, burun, boğaz enfeksiyonları, otitis media, sinüzit, tonsillit, farenjit gibi.Alt solunum yolu enfeksiyonları:Akut bronşit ve kronik bronşitin akut alevlenmeleri ve pnömoni gibi.Genito-üriner sistem enfeksiyonları:Piyelonefrit, sistit ve üretrit gibi.Deri ve yumuşak doku enfeksiyonları:Furonkül, piyoderma, impetigo gibi.Gonore:Akut ve komplike olmayan gonokokal üretrit ve servisit.Erken Lyme hastalığı tedavisinde ve takiben yetişkin ve 12 yaştan büyük çocuklarda geç Lyme hastalığı profilaksisinde. 4.2. Pozoloji ve uygulama şekli Pozoloji/uygulama sıklığı ve süresi:Olağan tedavi süresi 7 gündür (5-10 gün).Yetişkinlerde;
Ardışık tedaviSefuroksim aynı zamanda sefuroksim sodyum tuzu (ZINNAT Enjektabl) şeklinde parenteral uygulama için mevcuttur. Bu, parenteral tedaviden oral tedaviye geçişin klinik olarak endike olduğu durumlarda sefuroksim ile parenteral tedaviye oral (ZINNAT) tedavi ile devam olanağı sağlar.Parenteral ve oral tedavi süreleri enfeksiyonun şiddeti ve hastanın klinik durumuna göre belirlenir. Pnömoni:48 - 72 saat boyunca günde 3 veya 2 kez i.v. veya i.m. yolla uygulanan 1.5 g sefuroksim sodyum uygulamasını takiben 7-10 gün boyunca günde 2 kez oral yolla uygulanan 500 mg sefuroksim aksetil tedavisi.Kronik bronşitin akut alevlenmeleri:48 - 72 saat boyunca günde 3 veya 2 kez i.v. veya i.m. yolla uygulanan 750 mg sefuroksim sodyum uygulamasını takiben 5 - 10 gün boyunca günde 2 kez oral yolla uygulanan 500 mg sefuroksim aksetil tedavisi.Çocuklarda;Reçetelemede sabit doz tercih edildiğinde, birçok enfeksiyon için önerilen doz günde iki kez 125 mg'dır. Otitis mediası olan 2 yaşında veya daha büyük çocuklarda veya uygun olduğunda daha şiddetli enfeksiyonlarda doz maksimum günde 500 mg olmak üzere günde iki kez 250 mg'dır.Bebekler ve çocuklarda, dozu ağırlık veya yaşa göre ayarlamak tercih edilebilir. 3 ay-12 yaş arası bebek ve çocuklarda çoğu enfeksiyon için doz, günde maksimum 250 mg olmak üzere 10 mg/kg'dır. Otitis media veya daha şiddetli enfeksiyonlarda önerilen doz, maksimum günde 500 mg olmak üzere günde iki kez 15 mg/kg'dır. Aşağıdaki yaş ve kiloya göre hazırlanan dozaj tablosunda kolay uygulamayı sağlayacak kaşık ölçüleri (5ml'lik bir ölçek 250 mg sefuroksim içerir) de verilmiştir. Birçok enfeksiyon için dozaj 10 mg/kg'dır.
(kg)_
Doz (mg) Günde 2 kez
Yaş Ölçek (5ml'lik kaşık = 250 mg)_6 ay - 2 yaş
6 - 12
90 - 180 2 yaş - 12 yaş
180 - 250
12 - >20 Uygulama şekli:ZINNAT oral yolla alınır.Optimal absorpsiyon için sefuroksim aksetil yiyecekle birlikte alınmalıdır. Her dozu almadan önce süspansiyon şişenin içinde hareket ettiği görülene kadar çalkalanmalıdır. Arzu edilirse sulandırılmış süspansiyon soğuk meyve suyu, süt gibi içeceklere ilave edilerek verilebilir. Özel popülasyonlara ilişkin ek bilgiler:Böbrek yetmezliği:Sefuroksim aksetilin güvenilirlik ve etkinliği böbrek yetmezliği olan hastalarda belirlenmemiştir.Sefuroksim başlıca böbreklerle atılır. Benzer bütün antibiyotiklerde olduğu gibi, önemli derecede böbrek yetmezliği olan hastalarda yavaş atılımın kompanse edilmesi için sefuroksim dozunun azaltılması önerilir. Sefuroksim diyaliz ile etkin şekilde uzaklaştırılmaktadır.
Karaciğer yetmezliği:Veri yoktur.Pediatrik popülasyon:ZINNAT'ın 3 aydan küçük çocuklarda kullanımı ile ilgili klinik çalışma verisi bulunmamaktadır.Geriyatrik popülasyon:Veri yoktur.4.3. KontrendikasyonlarSefalosporin antibiyotiklerine ve ürünün herhangi bir bileşenine karşı aşırı duyarlı olduğu bilinen hastalarda kontrendikedir.4.4. Özel kullanım uyarıları ve önlemleriZİNNAT'a, diğer sefalosporinlere, penisilinlere veya diğer ilaçlara karşı aşırı duyarlılık geçmişi olan hastalarda tedaviye başlamadan önce dikkatli bir değerlendirme yapılmalıdır. Beta laktam antibiyotiklere karşı çapraz aşırı duyarlılık reaksiyonu gelişebileceğinden penisilin alerjisi olan hastalara verildiğinde, bu hastaların % 10kadarında çapraz aşırı duyarlılık reaksiyonu gelişebileceği bildirilmiştir. Klinik olarak anlamlı düzeyde alerjik reaksiyon gelişirse ilaç kullanımı kesilmeli ve uygun bir tedaviye başlanmalıdır. Ciddi ve akut hipersensitivite reaksiyonları geliştiğinde epinefrin tedavisi ve klinik olarak gerekli diğer acil uygulamaların (Oksijen, intravenöz sıvılar, intravenöz antihistaminler, kortikosteroidler, presör aminler, hava yollarına uygulanacak işlemler gibi uygulamalar) yapılması gerekli olabilir.Diğer antibiyotiklerde olduğu gibi sefuroksim aksetil kullanımı aşırıCandidaenterekoklar ve Clostridium difficile)aşırı çoğalmasına neden olarak tedavinin kesilmesini gerektirebilir.Geniş spektrumlu antibiyotiklerin kullanımında psödomembranöz kolit vakaları bildirilmiştir, bu nedenle antibiyotik kullanımı sırasında veya daha sonra ciddi diyare gelişen hastalarda, bu tanının göz önünde tutulması çok önemlidir. Pseudomembranöz kolit tanısını takiben uygun bir tedaviye başlanmalıdır. Hafif psöudomembranöz kolit vakaları genellikle sadece ilaç kullanımının kesilmesine yanıt verirler. Ancak orta dereceli ve şiddetli vakalarda sıvı ve elektrolit uygulamaları, protein takviyesi, Clostridium difficile'yekarşı etkili antibiyotik kullanımı gibi yöntemelerin kullanılması gerekli olabilir.Lyme hastalığının ZINNAT ile tedavisini takiben Jarisch-Herxheimer reaksiyonu (ateş, titreme, kas ağrısı, baş ağrısı, taşikardi gibi belirtileri vardır) görülebilir. Bu reaksiyon ZINNAT'ın Lyme hastalığına neden olan Borrelia burgdoferi mikroorganizması üzerindeki bakterisit etkisinin sonucudur. Hastalara bu reaksiyonun sık görülen ve genellikle Lyme hastalığının antibiyotiklerle tedavisinin kendi kendini kısıtlayıcı bir sonucu olduğu anlatılmalıdır. ZINNAT süspansiyon aspartam içerir ve aspartam fenilalanin kaynağı olduğundan fenilketonürisi olan insanlar için zararlı olabilir. ZINNAT süspansiyon sukroz içerir. Bu sebeple, nadir kalıtımsal früktoz intoleransı, glikoz-galaktoz malabsorbsiyon veya sükraz-izomaltaz yetmezliği problemi olan hastaların bu ilacı kullanmamaları gerekir. 4.5. Diğer tıbbi ürünler ile etkileşimler ve diğer etkileşim şekilleriZINNAT'ın probenesid ile birlikte uygulanması, serum konsantrasyonu-zaman eğrisi altında kalan alanı % 50 artırır. 1.5 g'lık tek doz ZINNAT'ın serum sefuroksim konsantrasyonu, 1 g probenesid ile birlikte (ortalama 14.8 mikrogram/ml) uygulandığında tek başına (ortalama 12.2 mikrogram/ml) uygulandığı duruma göre daha yüksektir.Mide asiditesini azaltan ilaçlar ZINNAT'ın açlık durumundaki biyoyararlanımını azaltabilir ve ZINNAT'ın yemek sonrası absorpsiyonundaki artışı ortadan kaldırabilir. Diğer antibiyotiklerde de olduğu gibi sefuroksim aksetil bağırsak florasını etkileyerek östrojen reabsorbsiyonunun azalmasına ve kombine oral östrojen/progesteron kontraseptiflerinin etkinliğinin azalmasına yol açabilir. Ferrisiyanid testinde yanlış negatif sonuçlar oluşabileceğinden sefuroksim alan hastalarda kan/plazma glukoz düzeylerini belirlemek için glukoz oksidaz veya heksokinaz metodlarının kullanılması önerilmektedir. Sefuroksim aksetil kreatinin için yapılan alkalin pikrat deneyini etkilemez. Sefalosporin grubu ilaçlar kırmızı kan hücrelerinin membranlarından absorbe olma ve ilaca karşı gelişen antikorlarla reaksiyona girme eğilimi göstererek Coombs testinin pozitif sonuç vermesine ve çok seyrek olarak da hemolitik anemiye yol açabilirler. 4.6. Gebelik ve laktasyon Genel tavsiyeGebelik kategorisi: BÇocuk doğurma potansiyeli bulunan kadınlar/Doğum kontrolü (Kontrasepsiyon)Kombine oral östrojen/progesteron kontraseptiflerinin etkinliğinin azalmasına yol açabilir.Gebelik dönemiSefuroksim aksetilin deneysel olarak kanıtlanmış hiç bir teratojenik veya embriyopatik etkisi bulunmamakta ise de, bütün diğer ilaçlarda olduğu gibi gebeliğin erken dönemlerinde dikkatli kullanılmalıdır.Laktasyon dönemiSefuroksim anne sütü ile de atıldığından emziren annelere verildiğinde dikkatli olunmalıdır.Üreme yeteneği/FertiliteVeri yoktur.4.7. Araç ve makine kullanımı üzerindeki etkilerZINNAT baş dönmesine yol açabileceğinden hastalar araç veya makine kullanırken dikkatli olmaları konusunda uyarılmalıdır.4.8. İstenmeyen etkilerSefuroksim aksetilin yan etkileri genellikle hafif ve geçici özelliktedir.Yan etkiler için belirlenen sıklık kategorileri tahminidir, plasebo kontrollü çalışmalarda da olduğu gibi bir çok reaksiyonda insidansı hesaplamak için elverişli veri (örneğin plasebo kontrollü çalışmalardan sağlanan veriler) bulunmamaktadır. Ayrıca sefuroksim aksetile bağlı yan etkilerin insidansları, endikasyona göre değişebilmektedir. Çok yaygından seyreğe, istenmeyen etkilerin sıklıklarının belirlenmesinde geniş klinik çalışmalardan elde edilen veriler kullanılmıştır. Bunun dışında kalan istenmeyen etkilerin sıklıkları (<1/10 000), esas olarak pazarlama sonrası deneyimlerden yola çıkarak belirlenmiştir ve rapor edilme oranına işaret etmektedir. Plasebo kontrollü çalışma verileri mevcut değildir. Insidanslar klinik çalışma verilerinden hesaplanmıştır ve bunlar ilaç ile ilişkili verilere dayanmaktadır. Sıklıklar, çok yaygın (>1/10 ), yaygın (>1/100 ve <1/10), yaygın olmayan (>1/1.000 ve <1/100), seyrek (>1/10.000 ve <1/1.000), çok seyrek (<1/10.000) ve bilinmiyor (eldeki verilerden tahmin edilemiyor) şeklinde tanımlanmıştır. Enfeksiyon ve EnfestasyonlarYaygın: Candida çoğalmasıKan ve lenfatik sistem bozukluklarıYaygın: EozinofiliYaygın olmayan: Pozitif Coomb's testi, trombositopeni, lökopeni Çok seyrek: Hemolitik anemi Sefalosporin grubu antibiyotikler alyuvar membranının yüzeyine absorbe olmaya ve ilaca yönelmiş antikorlarla etkileşmeye eğilimlidir; böylece pozitif Coomb's testi (kanın çapraz etkileşmesini etkileyebilir) ve çok nadiren hemolitik anemi oluşturabilirler. Bağışıklık sistemi bozukluklarıAşağıdakiler dahil olmak üzere aşırı duyarlılık reaksiyonlarıYaygın olmayan: Deri döküntüleri Seyrek: Ürtiker, kaşıntı Çok seyrek: Ilaç ateşi, serum hastalığı, anafilaksi Sinir sistemi bozukluklarıYaygın: Baş ağrısıBaş dönmesi Gastrointestinal bozukluklarYaygın: Diyare, bulantı, karın ağrısı gibi gastrointestinal rahatsızlıklarYaygın olmayan: Kusma Seyrek: Psödomembranöz kolit Karaciğer ve safra kesesi bozukluklarıYaygın: Hepatik enzim düzeylerinde (LDH, ALT (SGPT), AST (SGOT)) geçiciyükselmeler Çok seyrek: Sarılık (ağırlıklı olarak kolestatik), hepatit Deri ve derialtı doku bozukluklarıÇok seyrek: Eritem multiforme, Stevens-Johnson sendromu, toksikepidermal nekroliz (ekzantematik nekroliz) Bkz. Bağışıklık sistemi bozuklukları Pazarlama sonrası deneyimlerden edinilen verilere göre ürolojik bozukluklardan biri olan böbrek fonksiyon bozukluğu da görülen yan etkiler arasında bulunmaktadır. 4.9. Doz aşımı ve tedavisiSefalosporinler aşırı dozda serebral irritasyon sonucu konvülsiyonlara neden olabilirler. Sefuroksimin serum düzeyleri hemodiyalizle ya da periton diyalizi ile düşürülebilir. Ağır doz aşımı durumlarında destekleyici tedavi uygulanmalı ve hasta yakından izlenmelidir. Konvülsiyon oluşması halinde tedavi derhal kesilmeli, gerektiğinde antikonvülsif tedavi uygulanmalıdır.5.1 Farmakodinamik özelliklerFarmakoterapötik grup: ikinci kuşak sefalosporinler ATC kodu: J01D C02Etki mekanizmasıSefuroksim aksetil, bakterisit bir antibiyotik olan sefuroksimin oral ön ilacıdır. Sefuroksim, bakteriyel beta-laktamazlara karşı iyi bir stabilite gösterir ve sonuç olarak ampisilin veya amoksisiline dirençli suşların pek çoğuna etkilidir. Sefuroksim önemli hedef proteinlere bağlanarak bakterilerde hücre duvarı sentezini önleyerek bakterisit etki gösterir.Farmakodinamik etkiler Bakteriyoloji:Aerob Gram-negatif Mikroroganizmalar: Haemophilus influenzaefampisiline dirençli türler dahilj Haemophilus parainfluenzae Moraxella catarrhalis Neisseria gonorrhoeaefpenisilinaz üreten ve üretmeyen türler dahilj Escherichia coli Klebsiellatürleri Proteus mirabilis Providenciatürleri Prividencia rettgeriAerob Gram-pozitif Mikroorganizmalar: Staphylococcus aureus(Penisilinaz üreten türler dahil, metisiline dirençli suşlar hariç) Staphylococcus epidermidis(Penisilinaz üreten türler dahil, metisiline dirençli suşlar hariç) Streptococcuspyogenesfve diğer beta hemolitik streptokoklar^ Streptococcus pneumoniae B grubu streptokoklar (Streptococcus agalactiae)Anaerob Mikroorganizmalar: o Gram pozitif koklar (PeptococcusPeptostreptococcusGram negatif koklar (PeptococcusPeptostreptococcusGram-pozitif basiller (ClostridiumGram-negatif basiller (BacteroidesFusobacteriumPropionibacteriumtürleri.Diğer organizmalar: Borrelia burgdorferiAşağıdaki organizmalar sefuroksime duyarlı değildir: Clostridium difficile Pseudomonastürleri Campylobactertürleri Acinetobacter calcoaceticus Listeria monocytogenes Staphylococcus aureusStaphylococcus epidermidis'inmetisiline dirençli suşları LegionellatürleriAşağıdaki türlerin bazı suşları sefuroksime duyarlı değildir: Enterococcus faecalis Morganella morganii Proteus vulgaris Enterobactertürleri Citrobactertürleri Serratiatürleri Bacteroides fragilis5.2. Farmakokinetik özellikler Genel özelliklerEmilim:Sefuroksim aksetil oral yoldan alınmayı takiben gastrointestinal kanaldan absorbe olur ve intestinal mukozada ve kanda süratle hidrolize uğrayarak serbest sefuroksimi kan dolaşımına bırakır. Sefuroksim aksetil süspansiyonun absorpsiyonu yiyecekle artar. Sefuroksim aksetil tabletleri yemeklerden sonra alındığında, yaklaşık 2.4 saat sonra ulaşılan doruk plazma düzeyleri 125 mg'lık doz için 2.9 mg/l, 250 mg'lık doz için 4.4 mg/l, 500 mg'lık doz için 7.7 mg/l ve 1 g'lık doz için 13.6 mg/l olarak saptanmıştır. Sefuroksim süspansiyonun absorpsiyon hızı tabletlere nazaran daha az olup, doruk serum seviyeleri daha düşüktür ve sistemik biyoyararlanımı azalmıştır (% 4 - 17 daha az). Dağılım:Proteine bağlanma oranı kullanılan metodolojiye göre % 33 - 50 arasında değişir. Biyotransformasyon:Sefuroksim metabolize olmaz Eliminasyon:Serum yarılanma ömrü 1 - 1,5 saattir. Sefuroksim glomerular filtrasyon ve tubüler sekresyon ile elimine edilir. Probenesid ile birlikte verilmesi ortalama serum konsantrasyonları - zaman eğrisinin altında kalan alanı % 50 oranında artırır. Serum sefuroksim seviyesi diyaliz ile düşürülebilir. Hastalardaki karakteristik özelliklerVeri yoktur.5.3. Klinik öncesi güvenlilik verileriHayvan toksisite çalışmaları sefuroksim aksetilin anlamlı bir bulgu olmaksızın düşük toksisitesi olduğunu göstermiştir.6. FARMASÖTİK ÖZELLİKLER6.1. Yardımcı maddelerin listesiStearik asit SukrozTutti frutti aroması Asesulfam potasyum Aspartam Povidone K30 Ksantan gam Saf su 6.2. GeçimsizliklerVeri yoktur.6.3. Raf ömrü24 aySüspansiyon haline getirildikten sonra buzdolabında 2 - 8 oC arasında 10 güne kadar saklanabilir. 6.4. Saklamaya yönelik özel tedbirlerIlacı toz halde iken 30 oC'nin altındaki oda sıcaklığında, sulandırdıktan sonra da buzdolabında 2 - 8 oC arasında saklayınız.6.5. Ambalajın niteliği ve içeriğiZINNAT, sulandırıldığında 100 ml süspansiyon veren kuru granül içeren, çocuk kilidi olan HDPE kapaklı amber renkli cam şişelerde bulunmaktadır. Beraberinde 5 ml'lik bir ölçü kaşığı ve 35 ml'lik bir ölçü kabı bulunmaktadır.6.6. Beşeri tıbbi üründen arta kalan maddelerin imhası ve diğer özel önlemler Kullanma TalimatıDiğer bütün ilaçlarda olduğu gibi ZINNAT'ı hekimin tavsiye ettiği miktarda almanız çok önemlidir.ZINNAT süspansiyon her kullanımdan önce kuvvetle sallanarak çalkalanmalıdır. Hazırlanan süspansiyon buzdolabında 2 - 8 oC sıcaklıkta 10 gün saklanabilir. A- SÜSPANSİYONUN HAZIRLANIŞI: ZINNAT toz halindedir, bu yüzden ilk önce sulandırmak gerekir. 1. Sulandırmadan önce granülleri gevşetmek için şişeyi şekilde gördüğünüz gibi çalkalayınız. Kapağı ve şişenin ağzındaki membranı açınız. Eğer bu membran zarar görmüşse veya yoksa ilacı eczaneye iade ediniz. 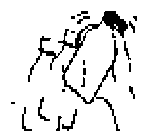 2. Ölçü kabı ile 35 ml su ilave ediniz ve şişenin kapağını tekrar kapatınız.
2. Ölçü kabı ile 35 ml su ilave ediniz ve şişenin kapağını tekrar kapatınız.3. Şişeyi başaşağıya çeviriniz ve şekilde görüldüğü gibi sağa sola (homojen bir süspansiyon elde edilene kadar, en az 15 saniye) kuvvetlice sallayınız. 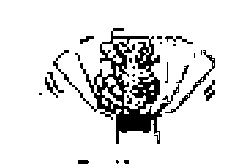 4. Şişeyi ilk duruma getirerek tekrar kuvvetle çalkalayınız.
4. Şişeyi ilk duruma getirerek tekrar kuvvetle çalkalayınız.5. Hazırlanan süspansiyon ilk dozdan önce bir saat bekletilmelidir. 
6. Süspansiyon 5ml'lik ölçü kaşığı ile uygulanabilir.  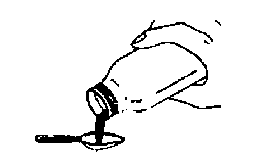
Her kullanımdan önce şişeyi çalkalamayı unutmayınız.7. RUHSAT SAHİBİAdı: GlaxoSmithKline Ilaçları San. ve Tic. A.Ş.Adresi: Büyükdere Cad. No.173, 1. Levent Plaza B Blok 34394 1. Levent / Istanbul Tel. no: 212 - 339 44 00 Fax. no: 212 339 45 00 8. RUHSAT NUMARASI216/639. İLK RUHSAT TARIHI/RUHSAT YENILEME TARIHIIlk ruhsat tarihi: 11.08.2008 Ruhsat yenileme tarihi:10. KÜB'ÜN YENİLENME TARİHI |
İlaç BilgileriZinnat Forte 250 mg/5 ml süspansiyon hazırlamak için granülEtken Maddesi: Sefuroksim Atc Kodu: J01DC02 Kullanma talimatı ve kısa ürün bilgileri
Google Reklamları
|
||||||||||||||||||||||||||||||||
Ana Sayfa | Hakkımızda | İlaçlar | İlaç Ara | İlaç Firmaları | Gizlilik | Bize Ulaşın
Telif Hakkı 2008-2026 © İlaç Prospektüsü. Tüm Hakları Saklıdır.Uyarı: Sitemizde yayınladığımız ilaç bilgileri ile doktora danışmadan kesinlikle ilaç kullanmayınız!
Aksi halde doğabilecek sağlık sorunlarından ilacprospektusu.com sorumlu tutulamaz.