Cissor 10mg/g Oral Damla Kısa Ürün BilgisiSinir Sistemi » Psikoanaleptikler » Anti Demans İlaçlarAlzheimer İlaçları » Diğer » Memantin 1. BEŞERİ TIBBİ ÜRÜNÜN ADI CİSSOR 10 mg/g oral damla2. KALİTATİF VE KANTİTATİF BİLEŞİM Etkin madde: Pompaya her bir basışta 0.5 mİ (0.5 g)'sinde; 5 mg memantin hidroklorür (4.16 mg memantine eşdeğer) içeren çözelti akar. Memantin hidroklorür (4.16 mg memantine eşdeğer) 5 mg Yardımcı maddeler: Her bir gram çözelti; Potasyum sorbat 2.10 mg Sorbitol % 70 E420 100.00 mg Yardımcı maddelerin tam listesi için 6.1'e bakınız. 3. FARMASÖTİK FORM Oral damla. Berrak çözelti. 4. KLİNİK ÖZELLİKLER 4.L Terapötik endikasyonlar Orta ve şiddetli evre Alzheimer hastalığı tedavisinde kullanılır. 4.2. Pozoloji ve uygulama şekli Pozoloj i/uygu lama sıklığı ve süresi: Tedavi, Alzheimer hastalığı tanı ve tedavisinde deneyimli bir hekim tarafından başlatılmalı ve kontrol edilmelidir. Tedaviye sadece, hastanın ilaç almasını düzenli olarak izleyecek bir bakıcının varlığında başlanmalıdır. Tanı, güncel rehberler doğrultusunda yapılmalıdır. Yetişkinler:Doz titrasyonu Önerilen maksimum günlük doz günde 20 mg'dır. İstenmeyen etki riskini azaltmak için, idame dozuna ilk üç hafta boyunca, haftada 5 mg'lik artışlarla şu şekilde ulaşılmalıdır: 1. hafta (gün 1-7): Hasta 7 gün boyunca, günde bir basışa eşit olan 0.5 mİ çözelti (5 mg) almalıdır. 2. hafta (gün 8-14): Hasta 7 gün boyunca, günde, iki basışa eşit olan 1.0 mİ çözelti (10 mg) almalıdır. 3. hafta (gün 15-21): Hasta 7 gün boyunca günde, üç basışa eşit olan 1.5 mİ çözelti (15 mg) almalıdır. 4. haftadan itibaren: Hasta günde dört basışa eşit olan 2.0 mİ çözelti (20 mg) almalıdır. İdame dozu: Önerilen idame dozu günde 20 mg'dır . Uygulama şekli:CİSSOR günde bir defa ve her gün aynı saatte alınmalıdır. Yemeklerle veya ayn olarak alınabilir. Çözelti şişeden veya pompadan direkt olarak ağıza dökülmemeli ve pompalanmamalıdır. Çözelti, pompa kullanılarak, bir kaşığa veya bir bardak suya konularak dozlanmalıdır.Ürünün hazırlanması ve kullanımına ilişkin detaylı bilgi için bkz. 6.6. Özel popülasyoniara ilişkin ek bilgiler :Böbrek yetmezliği: Hafif şiddette böbrek yetmezliği olan hastalarda (kreatinin klerensi 50-80 ml/dak) doz ayarlaması gerekmez. Orta şiddette böbrek yetmezliği olan hastalarda (kreatinin klerensi 30-49 ml/dak) günlük doz 10 mg (iki basışa eşit olan 1 mİ çözelti) olmalıdır. Tedavinin en az 7 günü boyunca iyi tolere edilirse, standart titrasyon programı uygulanmak koşuluyla, günlük doz, 20 mg düzeyine arttınlabilir. Ağır böbrek yetmezliği olan hastalar (kreatinin klerensi 5-29 ml/dak) için günlük doz 10 mg (iki basışa eşit olan 1 mİ çözelti) olmalıdır.Karaciğer yetmezliği: Hafif veya orta şiddette karaciğer yetmezliği olan hastalarda (Child-Pugh A ve Child-Pugh B) doz ayarlamasına gerek yoktur. Ağır karaciğer yetmezliği olan hastalarda memantin kullanımı hakkında veri bulunmamaktadır. Ağır karaciğer yetmezliği olan hastalarda CİSSOR kullanılması önerilmez.Pediyatrik popülasyon: Memantinin çocuklar ve adolesanlar üzerindeki güvenlilik ve etkililiği saptanmamıştır. Bu nedenle 18 yaşından küçük çocuklarda kullanılması önerilmez.Geriyatrik popülasyon: Yapılan klinik çalışmalara göre, 65 yaş üstü hastalara önerilen doz, yukanda anlatıldığı biçimde, günde 20 mg'dır (dört basışa eşit olan 2.0 mİ çözelti).4.3. KontrendikasyonlarEtkin madde veya yardımcı maddelerden herhangi birine karşı aşın duyarlılığı olan hastalarda kontrendikedir.4.4. Özel kullanım uyarıları ve önlemleriEpilepsisi, geçmişinde konvülsiyon öyküsü veya epilepsiye eğilimi olan hastalarda dikkatli olunmalıdır.Amantadin, ketamin veya dekstrometorfan gibi NMDA antagonistleri ile birlikte kullanımından kaçınılmalıdır. Bu bileşikler memantin ile aynı reseptör sistemine etki edip, advers etkilerin (özellikle santral sinir sistemi ile ilişkili olanlar) daha sık ya da daha kuvvetli görülmesine sebep olabilir {bkz. 4.5 Diğer tıbbi ürünler ile etkileşimler ve diğer etkileşim şekilleri).İdrar pH'smı yükselten faktörler var ise {bkz. 5.2 Elimimsyon)Proteus bacteria'mnneden olduğu ciddi üriner sistem enfeksiyonlan ile de yükselebilir.Birçok klinik çalışmada yakın tarihte geçirilmiş miyokard enfarktüsü, kompanse edilmemiş konjestif kalp yetmezliği (New York Kalp Cemiyeti (NYHA) endeks III-IV) veya kontrol altında olmayan hipertansiyonlu hastalar çalışma dışı bırakılmıştır. Sonuç olarak, sınırlı veri mevcut olduğundan bu durumdaki hastalar yakın gözlem altında bulundurulmalıdır. CİSSOR oral damla sorbitol içerir. Nadir kalıtımsal früktoz intolerans problemi olan hastalann bu ilacı kullanmamalan gerekir. 4.5. Diğer tıbbi ürünler ile etkileşimler ve diğer etkileşim şekilleriMemantinin farmakolojik etkileri ve etki mekanizması nedeni ile aşağıdaki etkileşmeler oluşabilir: Memantinin etki şekli sebebiyle; L-dopa, dopamineıjik agonistler ve antikolineıjiklerin etkileri, memantin gibi NMDA antagonistleri ile birlikte kullanıldığında artabilir. Barbitüratlann ve nöroleptiklerin etkilerini azaltabilir. Memantinin antispazmodik ajanlar, dantrolen veya baklofen ile birlikte kullanımı; etkilerini modifiye edebilir ve doz ayarlaması gerektirebilir. Farmakotoksik psikoz riski nedeni ile memantinin amantadin ile birlikte kullanımından kaçınılmalıdır. Her iki madde de NMDA-antagonistidir. Aynı yaklaşım ketamin ve dekstrometorfan için de geçerli olabilir {bkz. 4.4 Özel kullanım uyarıları ve önlemleri).Memantin ve fenitoinin kombine kullanımının olası riskine ilişkin yayınlanmış bir tane vaka raporu bulunmaktadır. Amantadin ile aynı renal katyonik nakil sistemini kullanan simetidin, ranitidin, prokainamid, kinidin, kinin ve nikotin de muhtemel olarak memantin ile etkileşip, plazma düzeyinde artış riski oluşturabilir. Memantin, hidroklorotiazid (HCT) veya HCT'li herhangi bir kombinasyon ile birlikte kullanılırsa, HCT serum seviyesinde azalma muhtemeldir. Pazarlama sonrası deneyimlerde varfarin ile birlikte memantin kullanan hastalarda INR (Uluslararası normalize edilmiş oran) artışı olan izole durumlar rapor edilmiştir. Nedensel bir ilişki kurulmamış olsa da oral antikoagülanlarla birlikte tedavi edilen hastalar için protrombin zamanının veya INR'nin yakından izlenmesi tavsiye edilmektedir. Karbonik anhidraz inhibitörleri ve sodyum bikarbonat ile kullanımında klerens düşebilir Sağlıklı genç gönüllülerde yürütülen tek-doz farmakokinetik çalışmalannda memantin ile gliburid/metformin kombinasyonu veya donezepil arasında anlamlı bir ilaç etkileşimi gözlenmemiştir. Sağlıklı genç gönüllülerde yürütülen bir klinik çalışmada, memantinin galantamin farmakokinetiği üzerinde hiçbir anlamlı etkisi gözlenmemiştir. Memantin; CYP1A2, 2A6, 2C9, 2D6, 2E1, 3A, flavin içeren monoksijenaz, epoksit hidrolaz veya sülfasyonu in vitroolarak inhibe etmemiştir.Özel popülasyonlara ilişkin ek bilgiler:Etkileşim çalışması yapılmamıştır.Pediyatrik popülasyon:Etkileşim çalışması yapılmamıştır.4.6.Gebelik ve laktasyonGenel tavsiyeGebelik kategorisi C'dir.Çocuk doğurma potansiyeli bulunan kadınlar / Doğum kontrolü (Kontrasepsiyon)Memantinin gebelikte kullanımına ilişkin klinik bilgi mevcut değildir.Hayvanlar üzerinde yapılan çalışmalar, gebelik /ve-veya/ embriyonal/fetal gelişim /ve-veya/ doğum /ve-veya/ doğum sonrası gelişim üzerindeki etkiler bakımından yetersizdir (bkz. 5.3). İnsanlara yönelik potansiyel risk bilinmemektedir. CİSSOR gerekli olmadıkça gebelik döneminde kullanılmamalıdır. Gebelik dönemiİnsanlardaki potansiyel riski bilinmemektedir. Memantin kesinlikle gerekli olmadıkça gebelikte kullanılmamalıdır.Laktasyon dönemiMemantinin insan sütüne geçişine ilişkin bilgi yoktur. Ancak, maddenin lipofilitesi nedeni ile bunun olması muhtemeldir. Memantin kullanan kadınlar emzirmemelidir.Üreme yeteneği / FertiliteHayvan çalışmaları, insanlardakine eşit veya az daha yüksek maruziyet düzeylerinde rahim içi büyümede azalma oluşturduğuna işaret etmektedir(bkz. 5.3 Klinik öncesi güvenlilik verileri).4.7. Araç ve makine kullanımı üzerindeki etkilerOrta ve şiddetli Alzheimer hastalığı genellikle araba kullanma performansının veya makine kullanma yeteneğinin azalmasına neden olur. Buna ilave olarak, memantinin araba ve makine kullanma yeteneğine az veya orta derecede etkisi vardır. Bu nedenle ayaktan tedavi gören hastalann dikkatli olmalan konusunda uyanimalan gerekmektedir.Hafif, orta ve şiddetli demansta yapılan ve memantin ile tedavi edilen 1784 ve plasebo ile tedavi edilen 1595 hastayı kapsayan klinik çalışmalarda memantin ile görülen advers olaylann toplam insidans oranı plasebo ile görülenlerden farklılık göstermemiştir; advers olaylar genellikle hafif ve orta şiddettedir. Memantin grubunda plasebo grubundan daha yüksek insidans ile en sık oluşan advers olaylar: sersemlik hali (sırasıyla %6.3-%5.6), baş ağnsı (%5.2-%3.9), kabızlık (%4.6- %2.6), uyuklama hali (%3.4-%2.2) ve hipertansiyon (%4.1-%2.8). Aşağıdaki tabloda listelenen advers ilaç reaksiyonlan memantinin klinik çalışmalanndan ve tıbbın hizmetine sunumundan itibaren toplanmıştır. Her sıklık grubunda istenmeyen etkiler ciddiyetteki azalmaya göre sunulmuştur. Advers etkiler sistem-organ smifina göre şu esaslar kullanılarak sıralandmlmaktadır; Çok yaygın (> 1/10); yaygın (> 1/100 - <1/10); yaygın olmayan (> 1/1000 - <1/100); seyrek (>1/10000 - <1/1000); çok seyrek (<1/10000); bilinmiyor (mevcut veriden tahmin edilemeyen)
Alzheimer hastalığı, depresyon, intihar düşüncesi ve intihar ile ilişkilendirilmiştir. Pazarlama sonrası deneyimlerde memantin ile tedavi edilen hastalarda bu olaylar bildirilmiştir. Klinik çalışmalarda veya pazarlama sonrası aşamalarda elde edilen aşın doz ile ilgili deneyim sınırlıdır. Semptomlar:Göreceli büyük aşın dozlar (sırası ile 3 gün süreyle günde 200 mg ve 105 mg) ya sadece yorgunluk, ^çsüzlük ve/veya diyare semptomlan ile ilişkilendirilmiştir ya da hiçbir semptom görülmemiştir. İlacın 140 mg'ın altında veya bilinmeyen dozda alındığı aşın doz vakaları, santral sinir sistemi (konfuzyon, uyuklama, uyku basması, vertigo, ajitasyon, saldırganlık, halüsinasyon ve yürüyüş bozukluklan) ve/veya gastrointestinal (kusma ve diyare) kaynaklı semptomlar göstermiştir.En uç doz aşımı vakasında, hasta oral yolla toplam 2000 mg memantin alımından sonra santral sinir sistemi üzerine etkiler ile (10 gün koma ve ardından diplopi ve ajitasyon) hayatta kalmıştır. Hasta semptomatik tedavi ve plazmaferez almıştır. Hasta daimi sekel kalmadan iyileşmiştir. Başka bir büyük doz aşımı vakasında da hasta yaşamış ve iyileşmiştir. Hasta oral yolla 400 mg memantin almıştır. Hasta, huzursuzluk, psikoz, görsel halusinasyonlar, prokonvulsiflik, uyuklama hali, stupor ve bilinç kaybı gibi santral sinir sistemi semptomlan yaşamıştır. Tedavi:Doz aşımı durumunda, tedavi semptomatik olmalıdır. Zehirlenme veya doz aşımı için spesifik bir antidot mevcut değildir. İlaç maddesini uzaklaştırmak için Standard klinik prosedürler, örn. gastrik lavaj, aktif kömür (potansiyel entero-hepatik geri dönüşün durdurulması), idrann asitleştirilmesi, zorunlu diürez uygun olan şekilde kullanılmalıdır.Genel santral sinir sistemi aşın uyanimasma dair belirtiler veya semptomlar varsa, dikkatli semptomatik klinik tedavi düşünülmelidir. 5. FARMAKOLOJİK ÖZELLİKLER5.L Farmakodinamik özelliklerFarmakoterapötik grup: Antidemans ilaçları ATC kodu: N06DX01Özellikle N-metil-D-aspartat (NMDA) reseptörlerindeki glutamateijik nörotransmisyon fonksiyon bozukluğunun, nörodejeneratif demansta semptomlann ortaya çıkması ve hastalığın ilerlemesine katkıda bulunduğuna dair gittikçe artan kanıtlar mevcuttur. Memantin; voltaj-bağımlı, orta afiniteli ve kompetitif olmayan bir N-metil-D-aspartat (NMDA) reseptör antagonistidir. Patolojik olarak yükselmiş, nöron işlev kaybına yol açabilen, glutamat tonik seviyelerinin etkilerini modüle eder. Klinik çalışmalar:Orta ve şiddetli Alzheimer hastalannda (MMSE-Mini mental durum muayenesi başlangıç toplam skorlan 3-14 olan) yapılan bir pivotal monoterapi çalışmasına ayaktan tedavi gören 252 hasta dahil edilmiştir. Çalışma, 6 ayda, memantin tedavisinin, plaseboya kıyasla, yararlı etkileri olduğunu göstermiştir (CIBIC-plus (Klinisyenin görüşmeye dayalı değişim izlenimi): p=0.025; ADCS-ADLsev (Alzheimer Hastalığı İşbirliği Çalışması-Günlük yaşam aktiviteleri): p=0.003; SIB-Şiddetli yıkım ölçeği p=0.002 için gözlemlenen vakalann analizi).Hafif ve orta şiddette Alzheimer hastalığı (MMSE başlangıç toplam skorlan 10-22 olan) tedavisinde memantin pivotal monoterapi çalışmasına 403 hasta dahil edilmiştir. Memantin ile tedavi edilen hastalar, plasebo ile tedavi edilen hastalara göre, şu primer sonlanma noktalan açısından istatistiksel olarak anlamlı şekilde daha iyi etki göstermiştir: 24. haftada (LOCF-İleri taşınmış son gözlem), ADAS-cog (Alzheimer hastalığı değerlendirme ölçeği) (p=0.003) ve CIBIC- plus (p=0.004). Hafif ve orta şiddetli Alzheimer Hastalığının bir başka monoterapi çalışmasına toplam 470 hasta (MMSE başlangıç toplam skorlan 11 - 23) randomize edilmiştir. Prospektif olarak tanımlanmış primer analizde, 24. haftada primer etkinlik sonlanma noktasında istatistiksel olarak anlam taşıyan bir değere ulaşılmamıştır. Orta ve şiddetli Alzheimer hastalığı (MMSE toplam skorlan <20) olan hastalarla yürütülen 6 farklı faz III, plasebo kontrollü, 6 aylık çalışmadaki (monoterapi çalışmalan ve asetilkolinesteraz inhibitörlerinin stabil bir dozunu alan hastalann katıldığı çalışmalar dahil) hastalann meta-analizi, memantin tedavisinin, kognitif, global ve fonksiyonel alanlarda istatistiksel olarak anlamlı şekilde daha iyi etki oluşturduğunu göstermiştir. Hastalar bu üç alanda eşzamanlı meydana gelen kötüleşme ile tanımlandığında, sonuçlar, plasebo verilen birçok hastada bu kötüleşmenin memantin tedavisi gören hastalann iki katı şeklinde ortaya çıkması ile, memantinin kötüye gidişi önleyici etkisinin, istatistiksel olarak anlamlı olduğunu göstermiştir (%21 ve %11, p<0.0001). 5.2. Farmakokinetik özellikler Emilim:Memantin yaklaşık %100'lük mutlak biyoyararlanıma sahiptir, tmaks değeri 3-8 saattir. Memantin emilimi gıda alımından etkilenmez.Dağılım:Günlük olarak alınan 20 mg dozlar, 70-150 ng/ml (0.5-1 |imol) arasında kişiden kişiye büyük değişim gösteren sabit durum plazma konsantrasyonlan ile sonlanmıştır. 5-30 mg'lık günlük dozlar alındığında, ortalama beyin omurilik sıvısı (BOS)/serum oranı 0.52 olarak hesaplanmıştır. Dağılım hacmi yaklaşık 10 1/kg'dır. Memantinin % 45'i plazma proteinlerine bağlanır.Bivotransformasvon:İnsanlarda dolaşımdaki memantinle ilişkili maddelerin % 80'i ana bileşik biçimindedir. İnsanlardaki ana metabolitler N-3,5-dimetil-gludantan, 4- ve 6-hidroksi-memantin izomerik kanşımı ve l-nitrozo-3,5-dimetil-adamantandır.Bu metabolitlerin hiçbirinin NMDA-antagonisti aktivitesi yoktur. in vitroçalışmalarda sitokrom P450 enzimlerinin katalizlediği metabolizma tespit edilmemiştir.Oral yoldan alman '"'C-memantin ile yapılan bir çalışmada, dozun %99'dan fazlası renal yoldan olmak üzere dozun ortalama %84'ü 20 gün içerisinde atılmıştır. Eliminasvon:Memantin terminal yan ömrü (tı/2) 60-100 saattir. Monoeksponansiyel biçimde elimine olur. Normal böbrek fonksiyonuna sahip gönüllülerde, toplam klirens (Cl,ot) 170 ml/dak/1.73 m^'dir ve toplam renal kürensin bir kısmı tübüler sekresyon ile sağlanır.Renal klirens, muhtemelen katyon nakil proteinleri vasıtasıyla, tübüler reabsorbsiyonu da içerir. Memantinin renal eliminasyon hızı alkali idrar koşullarında 7-9 faktör azaltılabilir (bkz. 4.4 Özel kullanım uyarılan ve önlemleri).İdrar alkalizasyonu, diyetteki köklü değişim (örneğin etoburluktan vejetaryen diyete geçiş gibi) veya alkalizan mide tamponlannm çok miktarda alınması sonucu oluşabilir.Doğrusallık:Gönüllülerde yapılan çalışmalarda, 10-40 mg'lık dozlarda lineer farmakokinetik gösterdiği saptanmıştır.Farmakokinetik/farmakodinamik ilişkiler:Günde 20 mg memantin dozunda, beyin omurilik sıvısı (BOS) seviyeleri memantinin frontal kortekste 0.5 ı^mol olan ki değerini (ki = inhibisyon sabiti) karşılamaktadır.5.3. Klinik öncesi güvenlilik verileriSıçanlarda yapılan kısa dönem çalışmalannda, memantin, benzeri diğer NMDA-antagonistleri gibi, sadece çok yüksek düzeyde serum konsantrasyonlanna neden olan dozlardan sonra, nöronal vakuolizasyon ve nekroz (Oiney lezyonlan) oluşturmuştur. Ataksi ve diğer preklinik işaretler, vakuolizasyon ve nekrozdan önce görülmektedir. Kemirgen ve kemirgen olmayan deney hayvanlannda uzun süreli yapılan çalışmalarda bu etkiler görülmediğinden, bu bulgulann klinik bağlantısı bilinmemektedir.Tekrarlanan doz toksisite çalışmalannda kemirgenlerde ve köpeklerde, oküler değişiklikler gözlemlenmiştir fakat bu durum maymunlarda görülmemiştir. Memantin ile yapılan klinik çalışmalarda, özgün oftalmoskopik incelemeler, herhangi bir oküler değişikliği ortaya koymamıştır. Lizozomlarda memantin birikimine bağlı olarak, pulmoner makrofajlardaki fosfolipidoz, kemirgenlerde gözlemlenmiştir. Bu etki, katyonik amfıfılik özellikteki diğer ilaçlarla da görülmektedir. Bu birikme ile akciğerlerde görülen vakuolizasyon arasında bir ilişki olması olasıdır. Etki, kemirgenlerde, sadece yüksek dozlarda görülmektedir. Bu bulgulann klinik bağlantısı bilinmemektedir. Memantin ile yapılan standart deneyler sonucu, genotoksisite gözlenmemiştir. Fareler ve sıçanlarda, ömür boyu yapılan çalışmalarda, hiçbir karsinojenite bulgusuna rastlanmamıştır. Memantin, matemal toksik dozlarda dahi, sıçanlarda ve tavşanlarda teratojenik etki göstermemiş ve üretkenliğe ilişkin hiçbir advers etki saptanmamıştır. Sıçanlarda, insanlara uygulanan düzeydeki dozlara eşdeğer veya biraz yüksek oranlarda yapılan uygulamalarda, fetal büyümenin azaldığı görülmüştür. 6. FARMASÖTİK ÖZELLİKLER6.L Yardımcı maddelerin listesiPotasyum sorbat Sorbitol % 70 E420 Deiyonize su6.2. GeçimsizliklerYoktur.6.3. Raf ömrü24 ayŞişe açıldıktan sonra, 3 ay içinde tüketilmelidir. 6.4. Saklamaya yönelik özel tedbirler25 ^C'nin altındaki oda sıcaklığında saklayınız.Pompası takılmış şişe, mutlaka dikey durumda tutulmalı ve taşınmalıdır. 6.5. Ambalajın niteliği ve içeriğiKutuda 50 ve 100 g çözelti içeren kahverengi cam şişe.6.6. Beşeri tıbbi üründen arta kalan maddelerin imhası ve diğer özel önlemlerKullanılmamış olan ürünler ya da atık materyaller Tıbbi Atıklann Kontrolü Yönetmeliği ve Ambalaj ve Ambalaj Atıklan Kontrolü Yönetmeliğine uygun olarak imha edilmelidir.İlk kez kullanımdan önce dozlama pompası şişeye monte edilmelidir. Vidalı kapağı şişeden çıkarmak için, kapak saat yönünün tersinde çevrilmeli ve tamamen sökülmelidir (Şekil 1). 1 . 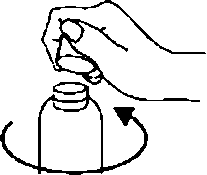 Dozlama pompasının şişeye monte edilmesi:
Dozlama pompasının şişeye monte edilmesi:Dozlama pompası plastik torbadan çıkanlır (Şekil 2) ve altındaki plastik tüp dikkatlice şişenin içine kaydmlarak şişenin ağzına yerleştirilir. Sonra dozlama pompası şişenin boynunda tutulur ve sıkıca yerleşene kadar saat yönünde çevrilir (Şekil 3). İlaç kullanılmaya başlandığında, dozlama pompası sadece bir defa çevrilir ve asla tekrar sökülmez. 3. 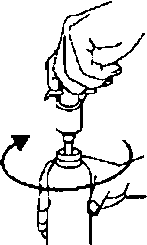 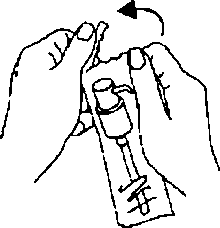 Dozlama pompasının başı iki pozisyonda bulunur ve saat yönünün tersinde (açık pozisyon) ve saat yönünde (kilitli pozisyon) çevirmesi kolaydır. Dozlama pompasının başı kilitli pozisyonda iken aşağı bastınimamalıdır. Çözelti sadece açık pozisyonda iken alınabilir. Bunu yapmak için, dozlama pompasının başı direnç hissedilinceye kadar, ok yönünde yaklaşık sekizde bir dönüş kadar çevrilmelidir. (Şekil 4).
Dozlama pompasının başı iki pozisyonda bulunur ve saat yönünün tersinde (açık pozisyon) ve saat yönünde (kilitli pozisyon) çevirmesi kolaydır. Dozlama pompasının başı kilitli pozisyonda iken aşağı bastınimamalıdır. Çözelti sadece açık pozisyonda iken alınabilir. Bunu yapmak için, dozlama pompasının başı direnç hissedilinceye kadar, ok yönünde yaklaşık sekizde bir dönüş kadar çevrilmelidir. (Şekil 4).4. 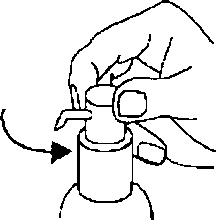 Dozlama pompası bundan sonra kullanıma hazırdır.
Dozlama pompası bundan sonra kullanıma hazırdır.Dozlama pompasının hazırlanması: İlk defa kullanılacağı zaman, dozlama pompası doğru miktarda oral çözelti vermez. Bu nedenle, dozlama pompasının başına ardarda beş defa tam olarak basılarak pompa hazırlanmalıdır (Şekil 5). 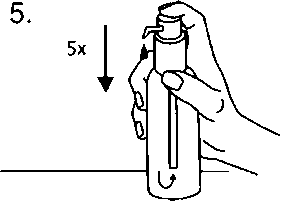 Bu şekilde alınan çözelti atılır. Daha sonra dozlama pompası tamamen aşağı bastınlır, böylece doğru doz alınır (1 dozlama birimi/bir basma 0.5 mL oral çözeltiye eşdeğerdir ve yaklaşık 5 mg memantin hidroklorür etkin maddesi içerir; Şekil 6).
Bu şekilde alınan çözelti atılır. Daha sonra dozlama pompası tamamen aşağı bastınlır, böylece doğru doz alınır (1 dozlama birimi/bir basma 0.5 mL oral çözeltiye eşdeğerdir ve yaklaşık 5 mg memantin hidroklorür etkin maddesi içerir; Şekil 6).6. 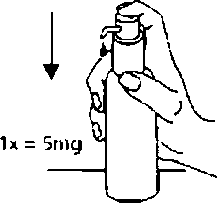 Şişe düz, yatay bir yüzeye, örneğin bir masa üstüne yerleştirilmeli ve sadece dik pozisyondayken kullanılmalıdır. Pompa ağzının altına bir miktar su içeren bir bardak veya bir kaşık tutularak, dozlama pompası başı kuvvetlice ama sakin ve sürekli şekilde (çok yavaş değil) sonuna kadar aşağı doğru bastınimalıdır (Şekil 7, Şekil 8 ).
Şişe düz, yatay bir yüzeye, örneğin bir masa üstüne yerleştirilmeli ve sadece dik pozisyondayken kullanılmalıdır. Pompa ağzının altına bir miktar su içeren bir bardak veya bir kaşık tutularak, dozlama pompası başı kuvvetlice ama sakin ve sürekli şekilde (çok yavaş değil) sonuna kadar aşağı doğru bastınimalıdır (Şekil 7, Şekil 8 ).8. 7.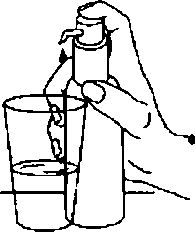 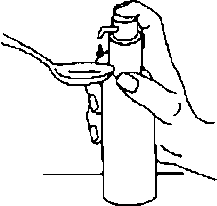 Dozlama pompasının başı daha sonra serbest bırakılabilir ve bir dahaki basış için hazırdır.
Dozlama pompasının başı daha sonra serbest bırakılabilir ve bir dahaki basış için hazırdır.Dozlama pompası sadece bu ürünün şişesinde bulunan memantin hidroklorür çözeltisi ile kullanılabilir, diğer maddeler ve kaplar için uygun değildir. Eğer pompa kullanım sırasında anlatılan şekilde çalışmaz ise, hasta doktoruna veya bir eczacıya danışmalıdır. Dozlama pompası kullanıldıktan sonra kilitlenmelidir. 7. RUHSAT SAHİBİTripharma İlaç San. ve Tic. A.Ş.Reşitpaşa Mah. Eski Büyükdere Cad. No: 4 34467 Maslak/Sanyer/İSTANBUL 0212 366 84 00 0212 276 20 20 8. RUHSAT NUMARASI236/179. İLK RUHSAT TARİHİ/ RUHSAT YENİLEME TARİHİİlk ruhsat tarihi: 26.10.2011 Ruhsat yenileme tarihi:10. KÜB'ÜN YENİLENME TARİHİ |
İlaç BilgileriCissor 10mg/g Oral DamlaEtken Maddesi: Memantin HCl Atc Kodu: N06DX01 Kullanma talimatı ve kısa ürün bilgileri
Google Reklamları
İlgili İlaçlar |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||
Ana Sayfa | Hakkımızda | İlaçlar | İlaç Ara | İlaç Firmaları | Gizlilik | Bize Ulaşın
Telif Hakkı 2008-2026 © İlaç Prospektüsü. Tüm Hakları Saklıdır.Uyarı: Sitemizde yayınladığımız ilaç bilgileri ile doktora danışmadan kesinlikle ilaç kullanmayınız!
Aksi halde doğabilecek sağlık sorunlarından ilacprospektusu.com sorumlu tutulamaz.