Nuvaring Vajinal Halka Kısa Ürün BilgisiÜrogenital Sistem ve Cinsiyet Hormonları » Diğer Jinekolojik İlaçlar » Hamilelik (Gebelik) Önleyici İlaçlar » Gebelik Önleyici Halka » Progesteron ve Östrojen Vajinal Halka KISA URUNBILGILERILGILERI1.BEŞERITIBBI URUNUN ADINUVARING Vajinal Halka24 saatte 0.120 mg/0.015 mg, vajinal halka 2.KALITATIF VE KANTİTATIF BİLEŞİMEtkin madde:NUVARING 11.7 mg etonogestrel ve 2.7 mg etinilöstradiol içerir.Halka 3 haftalık bir dönemde, günde ortalama sırasıyla 0.120 mg ve 0.015 mg etonogestrel ve etinilöstradiol salınımı yapar. Yardımcı maddeler için 6.1'e bakınız. 3.FARMASÖTIK FORMVajinal halka.NUVARING; Dış çapı 54 mm ve kalınlığının çapı 4 mm olan, esnek, saydam, renksiz ya da neredeyse renksiz bir halkadır. 4.KLINIK ÖZELLIKLER4.1Terapötik endikasyonlarKontrasepsiyon.4.2Pozoloji ve uygulama şekli Pozoloji/uygulama sıklığı ve süresi: NUVARING kullanmaya nasıl başlamalıÖnceki siklusta hormonal kontraseptif kullanılmadığında:NUVARING menstrüasyonun ilk gününde yerleştirilmelidir (örn. menstrüel kanamanın ilk gününde). Başlangıç 2.-5. günlerde olabilir, fakat NUVARING kullanımının ilk 7 günü sırasında ek olarak prezervatif gibi bir bariyer yöntemi kullanımı önerilmektedir. Bir kombine hormonal kontraseptiften geçiş yapmak:Kadın NUVARING'i en geç daha önce kullandığı kombine hormonal kontraseptifin, olağan tabletsiz, flastersiz ya da plasebo tabletli dönemi sonrasındaki gün yerleştirmelidir. Eğer kadın önceki metodunu sürekli ve doğru olarak kullanıyorsa ve eğer kadının gebe olmadığı kesin ise, döngünün herhangi bir gününde önceki kombine hormonal kontraseptiften geçiş yapabilir. Önceki metodun hormonsuz periyodunda önerilen süre kesinlikle aşılmamalıdır. Progestogen-only yönteminden (minipil, implant veya enjeksiyon) veya bir progestogen-salgılayan intrauterin sisteminden (IUS) geçiş yapmak:Kadın minipill'den (implanttan veya hormon içeren rahim içi araç çıkarıldığı gün, enjeksiyon yönteminde bir sonraki enjeksiyonun uygulanma tarihinde) herhangi bir günde geçiş yapabilir fakat bu olguların tamamında NUVARING kullanımının ilk 7 gün boyunca ek bir bariyer yöntemi kullanmalıdır.İlk trimester düşüğü sonrasında:Kadın derhal başlayabilir. Böyle davrandığı taktirde, ek kontraseptif önlem alma gereği ortadan kalkar. Eğer ani bir geçiş istenmiyorsa, kadın kendilerine bildirilen 'önceki siklusta hormonal kontraseptif kullanmayın' uyarısını dikkate almalıdır. Ara dönemde alternatif bir kontrasepsiyon yöntemi kullanması önerilir. Doğum ya da ikinci trimester düşüğü sonrasında:Meme emziren kadın için Bölüm 4.6.'ya bakınız.Kadınlara doğum ya da ikinci trimester düşüğünü izleyen dördüncü hafta sırasında kullanıma başlamaları önerilmelidir. Daha geç başlangıç yapan kadınlara NUVARING kullanımının ilk 7 gününde ek bir bariyer yöntemi kullanmaları önerilmelidir. Bununla birlikte, öncesinde cinsel ilişkisi bulunanlarda, NUVARING kullanmaya başlamadan önce hamilelik ekarte edilmeli ya da kadın ilk adet dönemine kadar beklemelidir. Önerilen rejimden sapmalarKadın önerilen rejime aykırı davranırsa, kontraseptif etkinlik ve siklus kontrolü bozulabilir. Bir sapma durumunda kontraseptif etkinlik kaybını önlemek amacıyla şunlar önerilebilir:Halkasız dönemin uzamış olması durumunda ne yapmalıKadın anımsadıktan sonra derhal yeni bir halka yerleştirmelidir. Yerleştirmeyi izleyen 7 gün boyunca prezervatif gibi ek bir bariyer yöntemi kullanılmalıdır. Halkasız dönemde bir cinsel ilişki gerçekleşmiş ise, hamilelik olasılığı düşünülmelidir. Hamilelik riski, halkasız dönemin uzunluğu ölçüsünde yüksek olacaktır.Halka geçici olarak vajina dışına çıkmış ise ne yapmalıNUVARING 3 haftalık bir kesintisiz dönem boyunca vajina içinde bırakılmalıdır. Eğer halka yanlışlıkla çıkarılmış ise soğuk-ılık (sıcak değil) sıcaklıkta su ile çalkalanarak derhal yeniden yerleştirilmelidir.Eğer NUVARING vajinanın dışında 3 saatten kısa bir süreboyunca kalmış ise kontraseptif etkinlikte bir azalma olmaz. Kadın mümkün olan en kısa sürede, ancak en geç 3 saat içinde halkayı yeniden yerleştirmelidir.Eğer NUVARING vajina dışında ise veya vajina dışında olduğundan şüpheleniliyorsa, kullanımın 1. veya 2. haftalarında 3 saati aşan bir süredekontraseptif etkinliğinde azalma olabilir. Kadın anımsamasını takiben halkayı derhal geri yerleştirmelidir. NUVARING vajina içinde kesintisiz 7 gün bulunma süresini tamamlayana kadar, ek olarak prezervatif gibi bir bariyer yöntemi kullanılmalıdır. NUVARING'in uzun süre vajina dışında kalması ve halkasız dönemde cinsel ilişkiye girme, gebelik riskini artırır.Eğer NUVARING vajina dışında ise veya vajina dışında olduğundan şüpheleniliyorsa, 3 haftalık kullanım periyodunun 3. haftasında 3 saati aşan süredekontraseptif etkinliğinde azalma olabilir. Kadın halkayı çıkarmalı ve aşağıdaki iki seçenekten birini seçmelidir:1.Hemen yeni bir halka yerleştiriniz. Not: Yerleştirilen yeni halka ile sonraki üç haftalık kullanım periyodu başlayacaktır. Kadın önceki siklusundan geri çekilme kanamasına maruz kalmayabilir. Ancak ani kanama ve lekelenme meydana gelebilir. 2.Geri çekilme kanaması gerçekleşmesinden ve önceki halkanın çıkarılmasından veya atılmasından sonra 7 gün geçmeden (7x24 saat) bir yeni halka yerleştiriniz. Not: Bu seçenek sadece, eğer halka önceki 7 günde devamlı kullanıldıysa seçilmelidir. Halka kullanım süresi aşılmış ise ne yapmalıNUVARINGmaksimum 4 hafta4 haftadan uzunbir süre bırakıldığında, kontraseptif etkinlik azalabilir ve yeni bir NUVARING halkası yerleştirilmeden önce hamilelik ekarte edilmelidir.Kadın önerilen rejime bağlı kalmamış ve sonrasında izleyen halkasız dönemde herhangi bir çekilme kanaması olmamış ise yeni bir NUVARING yerleştirme öncesinde hamilelik ekarte edilmelidir. Adet dönemi nasıl kaydırılır ya da geciktirilirBir dönemigeciktirmekisteyen bir kadın halkasız dönem geçirmeden yeni bir halka yerleştirebilir. Bir sonraki halka yine 3 hafta süreyle kullanılabilir. Kadın kanama ya da lekelenme yaşayabilir. Düzenli NUVARING kullanımına daha sonra bir haftalık olağan halkasız dönemden sonra yeniden başlanır.Dönemi olağan mevcut programında yer alandan başka bir hafta gününe kaydırmakisteyen kadına, bir sonraki halkasız dönemini istediği sayıda gün kısaltması önerilebilir. Halkasız dönem kısaldıkça, kadının bir sonraki halka kullanımında çekilme kanaması olmaması ve ani kanama ya da lekelenme yaşaması riski artış göstermektedir.Uygulama şekli:NUVARING nasıl kullanılırNUVARING vajinaya kadının kendisi tarafından yerleştirilebilir. Hekim, kadına NUVARING'in nasıl yerleştirileceği ve çıkartılacağı konusunda önerilerde bulunmalıdır. Yerleştirme sırasında kadın, örn. bir bacağını kaldırma, çömelme ya da uzanma gibi kendisi için en uygun pozisyonu seçecektir. NUVARING iki yandan sıkıştırılmalı ve rahat hissedilene kadar vajina içine sokulmalıdır. NUVARING'in vajina içindeki kesin konumu halkanın kontraseptif etkisi açısından kritik değildir (bkz. Şekil 1-4).NUVARING bir kez yerleştirildikten sonra (bkz. 'NUVARING kullanmaya nasıl başlamalı') 3 hafta boyunca sürekli olarak vajina içinde bırakılır. NUVARING'in varlığını düzenli teyit etmek alışkanlık haline getirilmelidir. NUVARING yanlışlıkla dışarı alındığında, 'Eğer halka vajinadan kısmen çıkar ise ne yapılır' Bölüm 4.2'de (daha fazla bilgi için, bkz Bölüm 4.4 'Çıkarma') verilen talimatlar izlenmelidir. NUVARING, yerleştirme sonrasında 3 hafta kullanıldıktan sonra yine haftanın aynı günü çıkartılmalıdır. Yeni halka, bir haftalık halkasız dönem sonrası yerleştirilir (örn. NUVARING Çarşamba günü saat 22:00 dolayında yerleştirilmiş ise 3 hafta sonra yine Çarşamba günü saat 22:00 dolayında çıkartılacaktır. Onu izleyen Çarşamba günü yeni halka yerleştirilecektir).(Şekil5). Kullanılmış halka poşete yerleştirilmeli (çocuk ve ev hayvanlarından uzak tutunuz) ve Bölüm 6.6' da tanımlandığı üzere çöpe atılmalıdır. NUVARING'in çıkartılmasından genellikle 2-3 gün sonra çekilme kanaması başlar ve yeni halka yerleştirene dek tamamen kesilmeyebilir.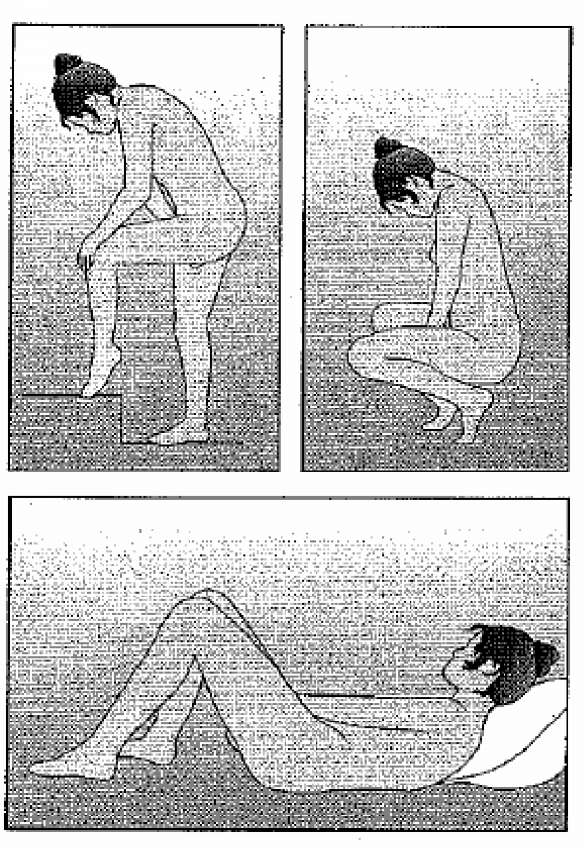
Şekil 3Halkayı yerleştirmek için rahat bir konum seçin.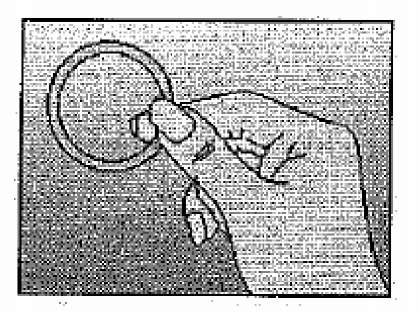
Şekil 1NUVARING'i poşetinden çıkartın.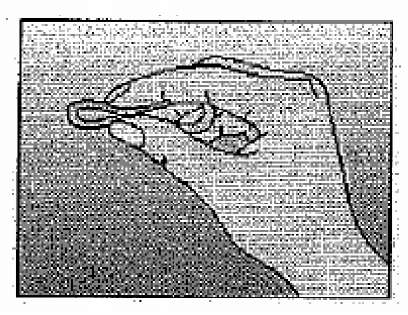
Şekil 2Halkayı iki yandan sıkıştırın.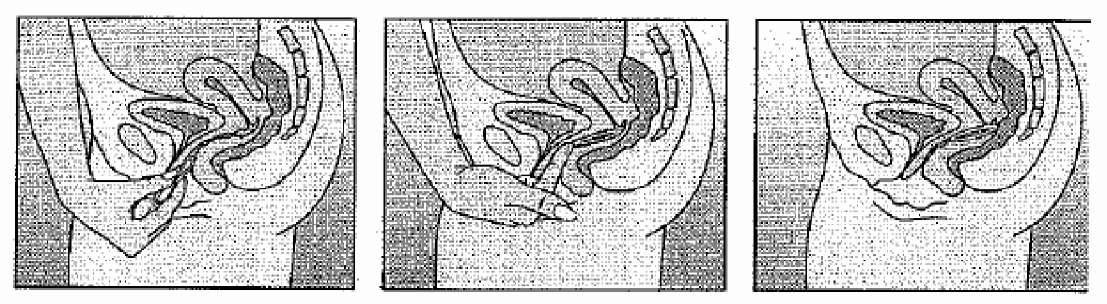
Şekil 4AŞekil 4BŞekil 4CHalkayı tek eliniz ile vajina içine sokunuz (Şekil 4A), gerekliyse labiumlar kolaylık için yana açılabilir. Halkayı rahat bir konum elde edene kadar vajina içine itiniz (Şekil 4B). Halkayı 3 hafta süreyle yerinde bırakınız (Şekil 4C).Şekil 5NUVARING işaret parmağının kanca şeklinde kıvrılması ve halkanın işaret parmağı ve orta parmak arasında kavranması ve dışarı doğru çekilmesi yoluyla çıkartılabilir.Özel popülasyonlara ilişkin ek bilgiler:Geriyatrik popülasyon:Pediyatrik popülasyon:NUVARİNG fertil dönemdeki kadınlar için tasarlanmıştır. NUVARİNG'in güvenliliği ve etkinliği 18-40 yaş arası kadınlarda belirlenmiştir. Puberte sonrası ergenler için de etkinlik ve güvenliliğin aynı olması beklenir. NUVARİNG kullanımı menarş öncesi endike değildir.Böbrek/Karaciğer yetmezliği:Böbrek/Karaciğer yetmezliği olan hastalar ile ilgili herhangi bir çalışma yoktur.4.3 KontrendikasyonlarNUVARING aşağıda belirtilen koşulların herhangi birinin varlığında kullanılmamalıdır. NUVARING kullanımı sırasında bu koşulların herhangi biri ilk kez ortaya çıktığında halka derhal çıkartılmalıdır.Pulmoner emboli ile ilişkili ya da ilişkisiz venöz trombozun varlığı ya da öyküsü, Tromboz öncüsü olaylar (örn. angina pektoris veya geçici iskemik atak) veya arteryel trombozun (serebrovasküler olay, miyokart infarktüsü) varlığı ya da öyküsü, Aktive protein C (APC) direnci, antitrombin III eksikliği, protein C eksikliği, protein S eksikliği, hiperhomosisteinemi ve antifosfolipid antikorları (antikardiolipin antikorları, lupus antikoagulan) gibi kalıtsal hastalıklarla ilişkili ya da ilişkisiz, arteryel veya venöz tromboz için bilinen predispozisyon, Fokal nörolojik semptomların eşlik ettiği migren öyküsü, Vasküler tutulumun eşlik ettiği diabetes mellitus, 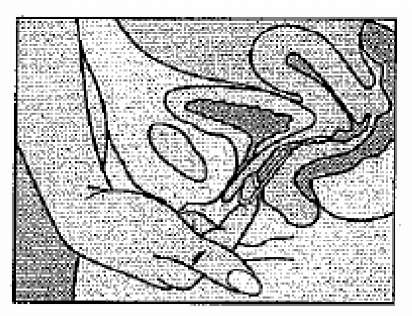 Pankreatit veya ciddi hipertrigliseridemi ile birlikte pankreatit öyküsü, Karaciğer fonksiyonu ile ilgili değerlerin normale dönmediği ciddi karaciğer hastalığı varlığı veya öyküsü, Karaciğer tümörlerinin (selim ya da habis) varlığı ya da öyküsü, Bilinen veya kuşkulanılan, seks-steroidlerinin etkili olduğu genital organların veya memelerin habis durumlar, Tanısı konmamış vajinal kanama, Bilinen veya kuşkulanılan hamilelik, NUVARING aktif bileşenlerine ya da herhangi bir yardımcı maddeye aşırı duyarlılık. 4.4. Özel kullanım uyarıları ve önlemleriUyarılar:Aşağıda belirtilen durumlar ya da risk faktörlerinden herhangi birinin varlığında, NUVARING kullanımının yararları her bir kadındaki olası risklere karşı tartılmalı ve kullanıma başlama kararı alması öncesinde kendisi ile tartışılmalıdır. Bu durumlar ya da risk faktörlerinin herhangi birinde ağırlaşma, şiddetlenme ya da ilk kez ortaya çıkma söz konusu olduğunda kadın derhal hekimi ile temasa geçmelidir. Hekim daha sonra kullanıma devam konusunda karar verecektir. Aşağıda sunulan verilerin tümü kombine oral kontraseptifleri (KOK) ile elde edilen epidemiyolojik verilere dayanmaktadır. Hormonların vajinal uygulama yolu üzerine herhangi bir epidemiyolojik veri bulunmamakla birlikte uyarıların NUVARING kullanımına da uyarlanabilir olduğu düşünülmektedir. 1. Dolaşım bozukluklarıEpidemiyolojik çalışmalar kombine oral kontraseptif (KOK) kullanımı ile miyokart infarktüsü, felç, derin venöz trombozu ve akciğer embolisi gibi artan arteriyal ve venöz trombotik ve tromboembolik rahatsızlıklar riski arasında bir bağlantı kurmuştur. Bunlar nadiren gerçekleşir. Herhangi bir kombine oral kontraseptifin kullanımı, hiç kullanmayanlarla kıyaslandığında artan venöz tromboembolizm (VTE) riski taşır. VTE'nin artan riski, kombine oral kontraseptif kullanan bir kadının ilk yılı süresince yüksektir. Bu artmış risk, gebelikle ilişkili 10.000 gebenin 6'sında görülen VTE'nin riskinden azdır. VTE olguların %1-2'sinde fataldır. Diğer kombine hormonal kontraseptifler ile risk kıyaslandığında NUVARING'in nasıl bir etkisi olduğu bilinmemektedir. KOK kullanıcılarında hepatik, mezenterik, renal, serebral ya da retinal venler ve arterler gibi diğer kan damarlarında son derece seyrek olarak tromboz bildirilmiştir. Bu oluşumların KOK kullanımı ile ilişkisi konusunda bir fikir birliği bulunmamaktadır. Venöz ve arteryel trombozun semptomları: mutad olmayan tek taraflı bacak ağnsı ve/veya şişkinliği; sol kola yayılan ya da yayılmayan ani ve şiddetli göğüs ağrısı; ani soluk kesilmesi; ani öksürük başlangıcı; herhangi bir olağandışı, şiddetli, uzun süreli baş ağrısı; ani kısmi ya da tam görme kaybı, diplopi, konuşma bozukluğu ya da afazi; vertigo; fokal nöbet gösteren ya da göstermeyen çöküntü hali; vücudun bir yanını ya da bir bölümünü aniden etkileyen halsizlik ya da çok belirgin uyuşukluk; motor bozuklukları; 'akut' abdomen. Venöz tromboembolizm (VTE) riski artış nedenleri: -ileri yaş, -pozitif bir aile öyküsü (örn. görece erken yaşta bir kardeş veya ebeveynde venöz tromboembolizm). Kalıtsal bir yatkınlıktan kuşkulanılan durumlarda kadın, herhangi bir hormonal kontraseptif kullanımına başlamadan önce bir hekime başvurmalıdır, -uzun süreli hareketsizlik, ciddi bir cerrahi girişim, bacaklarda herhangi bir cerrahi ya da ciddi bir travma. Bu gibi durumlarda kullanımın kesilmesi (elektif cerrahi durumunda en az dört hafta öncesinden) ve yeniden tam hareketlilik kazanılmasını izleyen en az iki hafta sonrasına kadar yeniden başlanmamalıdır, -obezite (vücut kütle endeksi >30kg/m2), -olası süperfisyal tromboflebit ve variköz venler. Venöz trombozun etiyolojisinde bu durumların muhtemel rolü hakkında fikir birliği bulunmamaktadır. Arteriyel tromboembolik komplikasyonların risk artış nedenleri: -ileri yaş; -sigara (özellikle 35 yaş üzeri kadınlarda yoğun sigara tüketimi ve artan yaş ile risk daha da artış gösterir); -dislipoproteinemi; -obesite ( vücut kitle endeksi >30kg/m2); -hipertansiyon; -migren; -kalp kapağı hastalığı; -atriyal fibrilasyon; -pozitif bir aile öyküsü (örn. görece erken yaşta bir kardeş veya ebeveynde venöz tromboembolizm). Kalıtsal bir yatkınlıktan kuşkulanılan durumlarda kadın herhangi bir hormonal kontraseptif kullanımına başlamadan önce bir hekime başvurmalıdır. Venöz veya arteriyel trombozun kalıtsal ya da edinilmiş yatkınlık göstergeleri olabilecek biyokimyasal faktörler, aktive protein C (APC) direnci, hiperhomosisteinemi, antitrombin-III eksikliği, protein C eksikliği, protein S eksikliği ve antifosfolipid antikorlarıdır (antikardiolipin antikorları, lupus antikoagülan). Advers dolaşım bozuklukları ile ilişkili diğer tıbbi şartların içine diabetes mellitus, sistemik lupus eritematozus, hemolitik üremi sendromu, kronik inflamatuvar bağırsak hastalığı (örn. Crohn hastalığı ya da ülseratif kolit) ve orak hücre hastalığı girmektedir. Puerperiumda artmış tromboembolizm riski düşünülmelidir ('Hamilelik ve Emzirme'deki oluşumu için bkz. Bölüm 4.6). Hormonal kontraseptif kullanımı sırasında migrenin sıklığı veya şiddetinde bir artış (bir serebrovasküler olayın habercisi olabilir) hormonal oral kontraseptif kullanımının aniden kesilmesini gerektirebilir. Doktor, risk/fayda ilişkisini değerlendirirken, bu durumun yeterli tedavisinin tromboz ile ilişkili riski azaltabileceğini ve hamilelik ile ilişkili riskin hormonal kontraseptif kullanımı ile ilişkili olandan daha yüksek olduğunu göz önünde bulundurmalıdır. 2.TümörlerServikal kanserin en önemli risk faktörü persistan human papilloma virus (HPV) enfeksiyonudur. Epidemiyoljik çalışmalar, uzun süre KOK kullanılmasının bu risk artışına katkıda bulunduğunu göstermiştir ama; söz konusu bulgunun; servikal taramaların daha sık yapılması ve bariyer kontraseptif kullanımı dahil cinsel davranış farklılıkları gibi, sonuç üzerinde etkili olabilecek diğer faktörlere ne derece bağlı olduğu veya arada bir nedensellik ilişkisi olup olmadığı konusundaki belirsizlik, devam etmektedir. Bu etkinin NUVARING ile nasıl ilişkili olduğu bilinmemektedir. 54 epidemolojik çalışmanın bir meta-analizi, halen KOK kullanmakta olan kadınlarda meme kanseri tanısı görece riskin (NR=1.24) bir miktar daha yüksek olduğunu bildirmektedir. Bu yüksek risk, KOK kullanımının bırakılmasını izleyen 10 yıl boyunca kademeli olarak azalır. Meme kanserinin 40 yaş altı kadınlarda seyrek görülmesinden ötürü, halen ya da yakın tarihlerde KOK kullananlarda yüksek meme kanseri tanı sayısı meme kanseri genel riskine kıyasla düşük olmaktadır. Herhangi bir zamanda NUVARING kullanmış olan kadınlarda konulan meme kanseri tanısı, hiç NUVARING kullanmamış olan kadınlardakiyle karşılaştırıldığında daha az ilerlemiş olma eğilimini taşır. Gözlemlenen yüksek risk patterni, KOK kullanıcılarında meme kanserine daha erken tanı konulmasına, KOK'ların biyolojik etkilerine ya da her ikisine birden bağlı olabilir. Seyrek olgularda, KOK kullanıcılarında, selim karaciğer tümörleri ve daha seyrek olarak habis karaciğer tümörleri bildirilmiştir. İzole olgularda bu tümörler yaşamı tehdit eden intra-abdominal hemorajilere yol açmıştır. Bu nedenle, NUVARING kullanan kadınlarda ciddi üst abdomen ağrısı, karaciğer büyümesi ya da intra-abdominal hemoraji oluşması durumunda, ayırıcı tanıda karaciğer tümörü düşünülmelidir. 3.Diğer durumlarHipertrigseridemisi ya da bu hastalıkla ilgili aile öyküsü bulunan kadınlar, hormonal kontraseptif kullandıklarında yüksek pankreatit riski altında olabilir. Hormonal kontraseptif kullanan kadınların kan basınçlarında küçük artışlar bildirilmiş olmasına karşın, klinik olarak önemli artışlar seyrektir. Hormonal kontraseptif kullanımı ve klinik hipertansiyon arasında kesin bir ilişki kanıtlanmış değildir. Bununla birlikte, NUVARING kullanımı sırasında sürekli ve klinik olarak anlamlı bir hipertansiyon gelişirse, hekimin halka kullanımını askıya alması ve hipertansiyonu tedavi etmesi doğru olacaktır. Antihipertansif tedavi ile normotansif değerler elde edilirse, uygun görülen durumlarda NUVARING kullanımına yeniden başlanabilir. Gerek hamilelik gerekse hormonal kontraseptif kullanımı sırasında aşağıdaki durumlara ilişkin belirti ya da kötüleşme bildirilmiş olmakla birlikte kullanımı ile ilişkinin kanıtı kesin değildir: sarılık ve/veya kolestaza bağlı sarılık, safra taşı oluşumu, porfiri, sistemik lupus eritematozus, hemolitik üremik sendrom, Sydenham koresi, herpes gestationis, otosklerozla ilişkili işitme kaybı, anjiyoödem (kalıtımsal). Akut ya da kronik karaciğer bozukluklarında karaciğer fonksiyonları belirteçleri normale dönene kadar NUVARING kullanımına ara verilmesi gerekebilir. İlk olarak hamilelik ya da daha önceki seks steroidi kullanımları sırasında ortaya çıkmış olan kolestatik sarılık ve/veya kolestaz ile ilişkili pruritin tekrarlaması halka kullanımının bırakılmasını gerektirebilir. Östrojen ve progesteronların periferik insülin direnci ve glukoz toleransı üzerine bir etkisi olabilse de, hormonal kontraseptif kullanan diabetiklerde terapötik rejim değişikliği gereğine işaret eden bir kanıt bulunmamaktadır. Bununla birlikte, NUVARING kullanan diabetik kadınlar özellikle ilk kullanım aylarında dikkatle izlenmelidir. Crohn hastalığında ve ülseratif kolitte, hormonal kontraseptif kullanımı ile ilişkin bir kötüleşme bildirilmiştir. Özellikle chloasma gravidarum öyküsü bulunan kadınlarda nadir olarak chloasma oluşabilir. Chlosma'ya eğilimli kadınlarda NUVARING kullanımı sırasında güneş ya da ultraviyole ışınlarına maruz kalmaktan kaçınmalıdır. Aşağıdaki durumlardan herhangi biri bulunan kadınlar NUVARING'i doğru olarak yerleştirmede başarılı olmayabilir ya da halkayı kaybedebilirler: uterus boynu prolapsusu, sistosel ve/veya rektosel, ciddi ya da kronik konstipasyon. Çok nadir olarak, NUVARING'in üretraya ve mesane çıkışına yanlışlıkla yerleştirildiği bildirilmiştir. Sistit semptomları karşısında ayırıcı tanıya gidilirken, bu nedenle halkanın yanlış yere yerleştirilmiş olma olasılığı üzerinde durulmalıdır. NUVARING kullanımı sırasında kadınlar, çok seyrek olarak vajinit yaşayabilirler. Ne NUVARING etkinliğinin vajinit tedavisinden etkilendiği ve ne de NUVARING kullanımının vajinit tedavisini etkilediğine ilişkin bir kanıt bulunmamaktadır (bakınız Bölüm 4.5.1 'Etkileşimler'). Halkanın vaginal dokuya, bir doktor ya da hemşire tarafından çıkarılmasını zorunlu kılacak derecede yapıştığı, çok seyrek bildirilmiştir. Tıbbi muayene/Konsültasyon: NUVARING ilk başta ve yeniden yerleştirilmeden önce eksiksiz bir tıbbi öykü (ailenin tıbbi öyküsü dahil) alınmalı ve gebelik ekarte edilmelidir. Kontrendikasyonlar (Bölüm 4.3) ve uyarılar (Bölüm 4.4) kılavuzluğunda kan basıncı ve fiziki muayene alınmalıdır. Kadına, kullanma talimatının dikkatlice okunması ve verilen talimatların izlenmesi önerilmelidir. Bu kontrollerin sıklığı ve yapısı belirlenirken, yerleşik klinik uygulamalar esas alınmalı ve her bir kadına göre özel olarak uyarlanmalıdır. Kadınlara NUVARING'in HIV infeksiyonlarına (AIDS) ve cinsel yoldan geçen diğer hastalıklara karşı koruma sağlamadığı belirtilmelidir. Azalmış etkinlik: Uyumsuzluk (non-kompliyans) (Bölüm 4.2) ya da eşzamanlı ilaç uygulamaları (Bölüm 4.5) NUVARING' in etkinliğini azaltabilir. Azalmış siklus kontrolü: NUVARING kullanımı sırasında düzensiz kanamalar (lekelenme ya da ani kanamalar) oluşabilir. Kanama düzensizliklerinin, daha önce NUVARING önerilen rejim uyarınca kullanılırken gerçekleşen düzenli sikluslar sonrasında oluşması durumunda, hormon dışı nedenler düşünülmeli ve malignite ya da hamileliğini ekarte etmek için uygun tanı önlemleri alınmalıdır. Bunlara kürtaj da dahil olabilir. Bazı kadınlarda halkasız dönem sırasında bir çekilme kanaması oluşmayabilir. NUVARING Bölüm 4.2'deki talimatlar uyarınca kullanılırsa, kadının gebe kalması olası değildir. Bununla birlikte, olmadığı fark edilen ilk çekilme kanaması öncesinde NUVARING' in ilgili talimatlara göre kullanılmamış ya da iki çekilme kanamasının atlandığının fark edilmesi durumunda, NUVARING kullanmayı sürdürmeden önce hamilelik ekarte edilmelidir. Erkeklerin etinilöstradiol ve etonogestrel maruziyeti: Cinsel partner olan erkeklerin, etinilöstradiol ve etonogestrel'in penis vasıtasıyla emilmesi yoluyla maruz kaldıkları etkinin kapsamı ve muhtemel farmakolojik rolü henüz incelenmiş bir konu değildir. Kopan halkalar: Çok nadir durumlarda kullanımı sırasında NUVARING'in koptuğu bildirilmiştir (bakınız Bölüm 4.5 'Etkileşimler'). NUVARING'in çekirdek bölümü katı olduğundan, içeriği bozulmayacak ve hormonların salınımı önemli ölçüde etkilenmeyecektir. Halka kopacak olursa, olasılıkla dışarıya atılır. NUVARING koparsa, kadın bunu çıkarmalı ve yerine yeni bir halka yerleştirmelidir Çıkma: NUVARING, eğer halka doğru yerleştirilmediyse, bir tampon çıkarılırken, cinsel ilişki esnasında veya şiddetli veya kronik kabızlıkta çıktığı bildirilmiştir. Bu yüzden NUVARING'in varlığını düzenli olarak kontrol edilmesi kadın için iyi bir alışkanlıktır. Eğer NUVARING kazara çıktıysa, kadın Bölüm 4.2 'Halka geçici olarak vajina dışına çıkmış ise ne yapmalı' kısmında verilen talimatları izlemelidir. 4.5 Diğer tıbbi ürünler ile etkileşimler ve diğer etkileşim şekilleriEtkileşimler:Hormonal kontraseptifler ve diğer ilaçlar arasındaki etkileşim ani kanamalara ve/veya yetersiz kontrasepsiyona yol açabilir. Literatürde aşağıdaki etkileşimler bildirilmiştir. Hepatik metabolizma: seks hormonlarının klirensinde artışa sebep olan mikrozomal enzimleri indükleyen ilaçlarla (örn. fenitoin, fenobarbital, pirimidon, karbamazepin, rifampisin ve muhtemelen de okskarbazepin, topiramat, felbamat, ritonavir, griseofulvin ve St. John' s wort içeren ürünler) etkileşimler ortaya çıkabilir. Bu ilaçları kullanan kadınların NUVARING'e ilaveten geçici olarak ek bir bariyer metodunu kullanmaları veya başka bir kontrasepsiyon metodunu seçmeleri önerilir. Mikrozomal enzim indükleyici ilaçlarla bariyer metodu eş zamanlı ilaç uygulamaları sırasında ve ilacın kesilmesini izleyen 28 gün boyunca kullanılmalıdır. Eş zamanlı ilaç uygulamasının 3 haftalık bir halka siklusunu aşması durumunda, olağan halkasız dönem atlanarak derhal bir sonraki halka yerleştirilmelidir. Kontraseptif yetersizlikler ayrıca penisilinler ve tetrasiklinler gibi antibiyotikler ile birlikte bildirilmiştir. Bu etkinin mekanizması açıklığa kavuşturulmamıştır. Bir farmakokinetik etkileşim çalışmasında, NUVARING kullanımı süresince 10 gün boyunca amoksisilin (875 mg, günde 2 kere) veya doksisiklinin (birinci günde 200 mg, takip eden günlerde günde 100 mg) oral olarak alınması, etinilöstradiol (EÖ) ve etonogestrelin farmakokinetiklerini anlamlı olarak etkilememiştir. Antibiyotiklerle (amoksisilin ve doksisiklin haricinde) tedavi olan kadınlar, verilen ara sonrası 7 güne kadar bariyer yöntemi kullanmalıdırlar. Eş zamanlı ilaç uygulamasının 3 haftalık bir halka siklusunu aşması durumunda, olağan halkasız dönem atlanarak derhal bir sonraki halka yerleştirilmelidir. Farmakokinetik verileri esas aldığımızda, vajinal yoldan uygulanan antimikotikler ve spermisidlerin NUVARING'in kontraseptif etkinliği ve güvenirliği etkileme olasılığı bulunmamaktadır. Halkanın bağlanmama şansı, eş zamanlı antimikotik ovüller kullanılırken kısmen artabilir (bakınız Bölüm 4.4 'Kopan Halkalar'). Hormonal kontraseptifler diğer ilaçların metabolizması ile etkileşebilir. Buna göre, plazma ve doku konsantrasyonları hem artabilir (örn. siklosporin) hem de azalabilir (örn. lamotrigin). Potansiyel etkileşimlerin tanımlanması amacıyla eş zamanlı ilaç uygulamalarının reçetesindeki bilgilere başvurulmalıdır. Laboratuar testleri: Kontraseptif steroidlerin kullanımı; karaciğer, tiroid, adrenal ve böbrek fonksiyonunun biyokimyasal parametreleri, taşıyıcı proteinlerin (örn. kortikosteroid bağlayan globulin ve seks hormonu bağlayan globulin) plazma düzeyleri, lipid/lipoprotein fraksiyonları, karbonhidrat metabolizması parametreleri ve koagülasyon ve fibrinoliz parametreleri dahil belirli laboratuar sonuçlarını etkileyebilmektedir. Değişimler genellikle normal laboratuar aralıkları içinde kalmaktadır. Tamponlarla etkileşim: Farmakokinetik veriler gösteriyor ki, tamponların kullanımının, NUVARING tarafından salınan hormonların sistemik emilimi üzerinde hiçbir etkisi yoktur. Nadir durumlarda NUVARING tampon çıkarılırken çıkarılabilir (bakınız öneri için 'Halka geçici olarak vajina dışına çıkmış ise ne yapmalı'). Özel popülasyonlara ilişkin ek bilgilerPediyatrik popülasyon:Pediyatrik popülasyon ve özel popülasyonlarla ilgili herhangi bir etkileşim çalışması yoktur.4.6. Gebelik ve laktasyonGenel tavsiyeGebelik kategorisi X'dir.Çocuk doğurma potansiyeli bulunan kadınlar/Doğum kontrolü (Kontrasepsiyon)NUVARING gebelik döneminde uygulandığı taktirde ciddi doğum kusurlarına yol açmaktadır/yol açtığından şüphelenilmektedir.Gebelik dönemiNUVARING hamilelik sırasında endike değildir. Eğer hamilelik NUVARING doğal yerindeyken gerçekleşirse, halka yerinden çıkartılmalıdır. Yaygın epidemiyolojik çalışmalar, hamilelik öncesinde KOK kullanmış kadınların doğurduğu çocuklarda doğum kusuru riski artışı ve KOK' lar erken hamilelik sırasında yanlışlıkla kullanıldığında bir teratojenik etki ortaya koymamıştır. Bunun tüm KOK'lar için geçerlilik taşıması yüksek olasılık olmakla birlikte NUVARING için de söz konusu olup olmadığı açık değildir.Az sayıda kadının dahil olduğu bir klinik çalışma gösteriyor ki, intravajinal uygulama dolayısıyla, NUVARING'deki kontraseptif steroidlerin intrauterin konsantrasyonları KOK kullanıcılarında gözlenen seviyeler ile benzerdir (bakınız Bölüm 5.2). NUVARING'e maruz kalmış hamileliklerin klinik sonuçları bildirilmemiştir. Laktasyon dönemiEmzirme, meme sütünün miktarını azaltabilen ve bileşimini değiştirebilen östrojenlerden etkilenebilmektedir. Bu nedenle, çocuk sütten tamamen kesilene kadar geçen sürede NUVARING kullanımı genellikle önerilmemelidir. Küçük miktarlarda kontraseptif steroidler ve/veya metabolitleri süt ile atılabilmektedir ancak bunun bebeğin sağlığını olumsuz etkilediğine ilişkin bir kanıt bulunmamaktadır.Üreme yeteneği/FertiliteBu tıbbi ürünün endikasyonu kontrasepsiyon olduğu için bu başlık geçerli değildir.4.7.Araç ve makine kullanımı üzerindeki etkilerFarmakodinamik profilin temelinde, NUVARING'in araç ve makine kullanımı üzerinde herhangi beklenen bir etkisi yoktur.4.8.İstenmeyen etkilerHormonal kontraseptiflerin kullanılmasına eşlik eden en ciddi istenmeyen etkilerin listesi, Uyarılar bölümde verilmektedir.NUVARING kullanıcılarında bildirilmiş olan advers ilaç reaksiyonlarının listesi, aşağıdaki Tablo'da verilmektedir. Listede, belirli advers olayların tanımlanması amacıyla en uygun MedDRA terimi (versiyon 11.0) kullanılmıştır.
Üreme sistemi ve meme hastalıklarıMemede hassasiyet, Genital kaşıntı, Dismenore, Pelvik ağrı, Vajinal akıntıAmenore, Meme ağrısı,Meme büyümesi, Meme kütlesi, Servikal polip, Koital kanama, Disparanü, Serviksin ektropiyonu, Fibrokistik meme hastalığı, Menoraji, Metroraji, Pelvik ağrısı, Premenstrüel sendrom, Uterin spazm, Vajinal yanma hissi, Vajinal koku, Vajinal ağrı, Vulvovajinal ağrı, Vulvovajinal kuruluk
Penis rahatsızlıkları2
Yorgunluk, İrritabilite, Halsizlik, Ödem, yabancı cisim hissetme Genel hastalıklar ve uygulama alanı koşullarıKan basıncı artışıAraştırmalarKilo kaybıYaralanma, Zehirlenme ve Prosedürelkomplikasyonlar |
İlaç BilgileriNuvaring Vajinal HalkaEtken Maddesi: Etonogestrel,Etinilöstradiol Atc Kodu: G02BB01 Kullanma talimatı ve kısa ürün bilgileri
Google Reklamları
İlgili İlaçlar |
Ana Sayfa | Hakkımızda | İlaçlar | İlaç Ara | İlaç Firmaları | Gizlilik | Bize Ulaşın
Telif Hakkı 2008-2026 © İlaç Prospektüsü. Tüm Hakları Saklıdır.Uyarı: Sitemizde yayınladığımız ilaç bilgileri ile doktora danışmadan kesinlikle ilaç kullanmayınız!
Aksi halde doğabilecek sağlık sorunlarından ilacprospektusu.com sorumlu tutulamaz.