Balance %4.25 Glukoz 1.75mmol/L Kalsiyum Periton Diyaliz Solüsyonu Kısa Ürün BilgisiKan ve Kan Yapıcı Organlar » Kan ve Perfüzyon Solüsyonları KISA ÜRÜN BİLGİLERİ ( KÜB )1. BEŞERİ TIBBİ ÜRÜNÜN ADIBALANCE %4.25 GLUKOZ 1.75 MMOL/L KALSİYUM Periton Diyaliz Solüsyonu 2. KALİTATİF VE KANTİTATİF BİLEŞİM BALANCE %4.25 GLUKOZ 1.75 MMOL/L KALSİYUM Periton Diyaliz Solüsyonu iki bölmeli bir torba sistemi içinde sunulmaktadır. Bir bölmede alkalin laktat solüsyonu, diğerinde ise asidik glukoz-bazlı elektrolit solüsyonu bulunur. İki bölme arasındaki orta dikiş açılarak ile bu iki solüsyon karıştırılır ve nötral, kullanıma hazır solüsyon elde edilir. KARIŞTIRMA ÖNCESİNDE:1000 ml asidik glukoz-bazlı elektrolit solüsyonu içinde: Etken Maddeler
Dozu 11.279 g 0.5145 g 0.2033 g 85.0 g Sodyum klorür Kalsiyum klorür dihidrat Magnezyum klorür hekzahidrat Anhidröz glukoz (glukoz monohidrat olarak)1000 ml alkalin laktat solüsyonu içinde: Etken Maddeler
Dozu 7.85 Sodyum laktat
g (sodyum laktat solüsyonu olarak)KARIŞTIRMA SONRASINDA:1000 ml nötral, kullanıma hazır solüsyon içinde: Etken Maddeler
Dozu 5.640 g 3.925 g 0.2573 g 0.1017 g 42.5 g Sodyum klorür Sodyum laktat ( sodyum laktat solüsyonu olarak(glukoz monohidrat olarak)Na+ 134 mmol/l Ca++ 1.75 mmol/l Mg++ 0.5 mmol/l Cl- 101.5 mmol/l Laktat 35 mmol/l Glukoz 235.8 mmol/l Teorik Osmolarite 511 mOsm/l pH 7.0 Yardımcı maddeler için 6.1'e bakı nız.3. FARMASÖTİK FORM Periton diyalizinde kullanılan steril çözelti. 4. KLİNİK ÖZELLİKLER 4. 1. Terapötik endikasyonlar Periton diyaliz tedavisi yapılan son dönem kronik böbrek yetmezliği hastalarında kullanılır. 4. 2. Pozoloji ve uygulama şekli Pozoloji/ uygulama sıklığı ve süresi: Bu solüsyon intraperitoneal olarak kullanılır. Başka şekilde reçete edilmemişse günde 4 defa olmak üzere değişim her uygulamada 2000 ml. solüsyon kullanılır. 2-10 saat arası bir bekleme süresinden sonra solüsyon boşaltılır. Dozajın, solüsyon hacminin ve değişim sayısının hastalar için bireysel olarak ayarlanması gereklidir. Tedavinin başlangıcında hastanın abdominal distansiyondan dolayı ağrısı oluyorsa, değişim başına solüsyon hacmi bir süre için 500-1500 ml olarak uygulanabilir. İri yapılı yetişkinlerde, renal residüel fonksiyon kaybolmuşsa, daha yüksek hacimlerde diyaliz solüsyonu uygulanması gerekir. Bu hastalarda veya daha yüksek hacimleri tolere edebilen hastalarda değişim başına 2500-3000 ml solüsyon verilebilir. Aralıklı veya sürekli uygulanan siklik peritoneal diyaliz için bir makine kullanılıyorsa, birden fazla solüsyon değişimine olanak veren büyük hacimli torbalar önerilir. Çocuklarda değişim başına solüsyon hacmi yaş, boy ve vücut ağırlığına bağlı olarak daha az yaşa ve büyüklüğe bağlı olarak ayarlanır (30-40 ml/kg, kg olarak vücut ağırlığı). Yaşlı hastalar için özel dozaj önerileri bulunmamaktadır. Yüksek glukoz konsantrasyonlarındaki (%2.3 veya %4.25) periton diyaliz solüsyonları, vücut ağırlığı istenen kuru ağırlığın üzerinde ise, kullanılır. Periton diyaliz solüsyonunun glukoz konsantrasyonuna bağlı olarak vücuttan sıvı çekişi artar. Bu solüsyonlar; periton zarına zarar verilmemesi, dehidratasyonun önlenmesi ve glukoz yükünün mümkün olduğunca düşük seviyede tutulabilmesi için dikkatle kullanılmalıdır. Reçetelendiği şekilde diyaliz günlük olarak uygulanmalıdır. Periton diyalizi sürekli solüsyon uygulamasını gerektiren uzun süreli bir tedavidir. BALANCE %4.25 GLUKOZ 1.75 MMOL/L KALSİYUM, 1000 ml solüsyon içinde 42.5 g glukoz içerir. Uygulama şekli: Hekimin talimatlarına uygun olarak, solüsyon periton boşluğunda 2-10 saat (dengelenme süresi) bekletilmeli ve sonra boşaltılmalıdır. İstenen osmotik basınca bağlı olarak, BALANCE %4.25 GLUKOZ 1.75 MMOL/L KALSİYUM, daha düşük glukoz içeriğine sahip (daha düşük osmolarite) diğer periton diyaliz solüsyonları ile dönüşümlü olarak kullanılabilir. Hasta evde periton diyalizine başlamadan önce uygulamalar konusunda eğitilmeli, tekniğin pratiğini yapmalı ve bu konuda yeterli seviyeye gelmelidir. Eğitimler kalifiye personel tarafından gerçekleştirilmelidir. Hekim, hastanın bu teknikleri evde uygulamaya başlamasından önce yeterli eğitimi almış olmasını sağlamalıdır. Herhangi bir problemi veya sorusu olması durumunda hasta hekimle temasa geçmelidir. Renal fonksiyon replasman tedavisi gerektiği sürece, periton diyalizine devam edilmelidir. Sadece tek kullanım içindir. Solüsyonun kullanılmayan kısmı imha edilmelidir. ^ıtay safe balance:Stay safe balance için ilk olarak solüsyon torbası vücut sıcaklığına kadar ısıtılır. Isıtma bir ısıtıcı tepsi ile yapılır. 2000 ml bir torba için 22°C'de ısıtma süresi yaklaşık 120 dakikadır. Bölgesel olarak fazla ısıtmaya sebep olabileceği için bu amaçla mikrodalga fırın kullanılmamalıdır. Kullanımdan önce torbanın iki bölmesindeki solüsyonlar karıştırılmalıdır.Slee^ safe balance/ Safe lock balance:.Solüsyon torbası, bir cihaz ile birlikte kullanılır. Isıtma işlemi bu cihazın ısıtıcısı tarafından otomatik olarak gerçekleştirilir.Solüsyonun ısıtılma işlemi tamamlandıktan sonra torba değişimine başlanır. Stay safe balance sistem için kullanma talimatları1- Solüsyonun hazırlanması: Solüsyon torbası kontrol edilir (etiket, son kullanma tarihi, solüsyonun berraklığı, torba ve koruyucu torbanın hasar görüp görmediği, dikişlerin bütünlüğü). Torba sert bir zemine konur. Koruyucu torba açılır. Eller antimikrobiyal bir losyon ile yıkanır. Torba koruyucu torba üzerine konur ve kenarından yana doğru orta dikiş açılana kadar kıvrılır. İki bölmede bulunan solüsyonlar otomatik olarak karışır. Daha sonra torba üst kenardan aşağı doğru alttaki üçgen kısmın dikişleri tamamen açılana kadar kıvrılır. Tüm bölmelerin tamamen açık olup olmadığı kontrol edilir. Solüsyonun berraklığı ve sızıntı olup olmadığı kontrol edilir. 2- Torba değişiminin hazırlanması: Solüsyon torbası infüzyon askısının üst deliğine asılır, solüsyon torbasının tüp hattı açılır ve DİSK organizere yerleştirilir. Drenaj torbasına giden hat sistemi açıldıktan sonra, drenaj torbası infüzyon askısının alt deliğine asılır ve dezenfeksiyon kapağı organizere yerleştirilir. Kateter konektörü organizere yerleştirilir. Eller dezenfekte edilir ve DİSK'ten koruma kapağı çıkarılır. Kateter konektörü DİSK'e bağlanır. 3- Boşaltım: Kateter ara bağlantısı klempi açılır. Boşaltım başlar: ^ Pozisyon d' 4- Yıkama: Boşaltım işlemi tamamlandıktan sonra solüsyon torbası ve DİSK arasındaki hat drenaj torbasına taze solüsyon akıtılarak yıkanır(yaklaşık 5 saniye). ^ Pozisyon d'd' 5- Dolum: Kontrol düğmesi çevrilerek dolum başlatılır: ^ Pozisyon o'O'd' 6- Güvenlik adımı: Pin, kateter bağlantısına takılarak kateter ara bağlantısı kapatılır. ^ Pozisyon d'd'd'd'. 7- Bağlantının açılması: Yeni dezenfeksiyon kapağının koruma kapağı çıkarılır ve eskisine vidalanır. Kateter konektörü, DİSK'ten çevrilerek ayrılır ve yeni dezenfeksiyon kapağına vidalanarak takılır. 8- DİSK'in kapatılması: Organizerin sağ tarafında bulunan, kullanılmış dezenfeksiyon kapağının koruyucu kapağının açık ucu ile DISK kapatılır. 9- Boşaltılmış diyalizatın bulanıklığı ve ağırlığı kontrol edilir, sıvı berrak ise imha edilir. 1- Hat sistemi 2- Enjeksiyon/numune portu 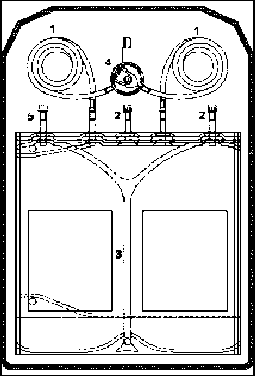 3- Lambda dikişi 4- DİSK sistem konektörü 5- Tıpa 3000 ml sleep safe balance sistemi için kullanma talimatları1- Solüsyonun hazırlanması: Solüsyon torbası kontrol edilir (etiket, son kullanma tarihi, solüsyonun berraklığı, torba ve koruyucu torbanın hasar görüp görmediği, dikişlerin bütünlüğü). Torba sert bir zemine konur. Koruyucu torba açılır. Eller antimikrobiyal bir losyon ile yıkanır. Torba koruyucu torba üzerine konur ve kenarından yana doğru lambda dikişi açılana kadar kıvrılır. İki bölmede bulunan solüsyonlar otomatik olarak karışır. Daha sonra torba üst kenardan aşağı doğru alttaki üçgen kısmın dikişleri tamamen açılana kadar kıvrılır. Tüm bölmelerin tamamen açık olup olmadığı kontrol edilir. Solüsyonun berraklığı ve sızıntı olup olmadığı kontrol edilir. 2- Torbanın hat sistemi (1) açılır. 3- Koruma kapağı çıkarılır. 4- Torba konektörü, sleep safe cyclercihazının boş bir tepsi portuna yerleştirilir.5- Torba şimdi sleep safe setile kullanıma hazırdır._1 T^nKn-trr TITI tU i-ın r1 - Torba konektörü ile hat sistemi  2- Enjeksiyon portu 3- Tıpa 4- Lambda dikişi 5000 ml ve 6000 ml sleep safe balance sistemi için kullanma talimatları1- Solüsyonun hazırlanması: Solüsyon torbası kontrol edilir (etiket, son kullanma tarihi, solüsyonun berraklığı, torba ve koruyucu torbanın hasar görüp görmediği, dikişlerin bütünlüğü). Torba sert bir zemine konur. Koruyucu torba açılır. Eller antimikrobiyal bir losyon ile yıkanır. Orta dikiş ve torba konektörü açılır. Torba koruyucu torba üzerine konur, diagonal köşeden torba konektörüne doğru torba kıvrılır. Orta dikiş (4) açılır. Küçük bölmenin (5) orta dikişi açılana kadar devam edilir. Tüm orta dikişlerin tamamen açık olup olmadığı kontrol edilir. Solüsyonun berraklığı ve sızıntı olup olmadığı kontrol edilir. 2- Torbanın hat sistemini (1) açılır. 3- Koruma kapağı çıkarılır. 4- Torba konektörü, sleep safe cyclercihazının boş bir tepsi portuna yerleştirilir.5- Torba şimdi sleep safe setile kullanıma hazırdır.1- Torba konektörü ile hat sistemi 2- Enjeksiyon portu 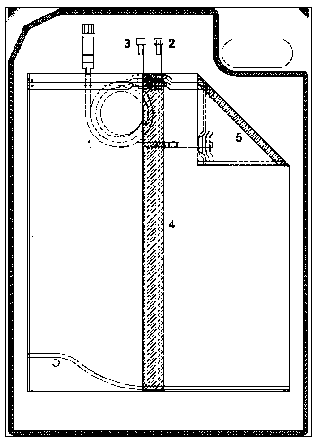 3- Tıpa 4- Orta dikiş 5- Küçük bölmenin orta dikişi Safe lock balance sistemi için kullanma talimatları1- Solüsyonun hazırlanması: Solüsyon torbası kontrol edilir (etiket, son kullanma tarihi, solüsyonun berraklığı, torba ve koruyucu torbanın hasar görüp görmediği, dikişlerin bütünlüğü). Torba sert bir zemine konur. Koruyucu torba açılır. Eller antimikrobiyal bir losyon ile yıkanır. Orta dikiş ve torba konektörü açılır. Torba koruyucu torba üzerine konur, diagonal köşeden torba konektörüne doğru torba kıvrılır. Orta dikiş (4) açılır. Küçük bölmenin (5) orta dikişi açılana kadar devam edilir. Tüm orta dikişlerin tamamen açık olup olmadığı kontrol edilir. Solüsyonun berraklığı ve sızıntı olup olmadığı kontrol edilir. 2- Konektörün (1) koruyucu kapağı, bağlantı hattı hazırlanmak üzere çıkarılır. 3- Bağlantı hattı ile torba arasındaki bağlantıları yapılır. 4- Hattı ve PİN'i her iki tarafa 90° den fazla bükerek iç kilidi kırılır. 5- Torba artık kullanıma hazırdır.
Tüm uygulama sistemleri için geçerli genel kullanma talimatları: Kullanıma hazır solüsyon hemen kullanılmalıdır, bunun mümkün olmadığı durumlarda ise karıştırma sonrası maksimum 24 saat içinde kullanılmalıdır. Reçetelenmesi durumunda, kullanıma hazır solüsyona enjeksiyon portundan (2) kontaminasyona yol açmayacak şekilde diğer ilaçlar ilave edilebilir. Sadece aşağıdaki ilaçlar hekim tarafından reçete edildiğinde belirtilen konsantrasyona kadar olmak üzere ilave edilebilir: Heparin 1000 I.U./l, insülin 20 I.U/l, vankomisin 1000 mg/l, teikoplanin 400 mg/l, sefazolin 500 mg/l, seftazidim 250 mg/l, gentamisin 8 mg/l. İyice karıştırıldıktan ve bulanıklık veya parçacıkların olmadığından emin olunduktan sonra ve zaman geçirmeden solüsyon kullanılmalıdır, saklama yapılamaz. Özel popülasyonlara ilişkin ek bilgiler: Böbrek/ Karaciğer yetmezliği: Diyalizin etkinliği, hastanın vücut ağırlığı, beslenme durumu, kan ve diğer ilgili testler hekim tarafından değerlendirilerek düzenli olarak izlenir. Pediyatrik popülasyon: Çocuklarda yaş,boy ve vücut ağırlığına bağlı olarak, değişim başına doz belirlenir. Geriyatrik popülasyon: Yetişkinler için belirlenmiş olan doz kullanılır. 4. 3. Kontrendikasyonlar Bu periton diyaliz solüsyonuna spesifik olarakBALANCE %4.25 GLUKOZ 1.75 MMOL/L KALSİYUM ciddi hipokalemi, ciddi hiperkalsemi, hipovolemi, arteriyel hipotansiyonu olan hastalarda kullanılmamalıdır. Genel olarak periton diyaliz ile ilgili olarakAşağıdakilerden herhangi birisi söz konusu ise periton diyalizine başlanmamalıdır: - Yakın zamandaki abdominal cerrahi veya yaralanma; fibröz adezyonlu abdominal operasyon hikayesi, barsak perforasyonu, abdominal yanıklar - Abdominal deride yaygın enflamatuvar durum (dermatit), - Enflamatuvar bağırsak hastalıkları (Chrohn' s hastalığı, ülseratif kolit, divertikülit), - Peritonit, - İç veya dış abdominal fistula, - Umbilikal, inguinal veya diğer abdominal herniler, - İntra-abdominal tümorler - İleus, - Pulmoner hastalık (özellikle pnömoni), - Sepsis, - Laktik asidoz, - Çok yüksek hiperlipidemi, - Periton diyalizi ile tedavi edilemeyen nadir üremi vakaları - Kaşeksi ve ciddi kilo kaybı, özellikle beslenme ile yeterli protein desteğinin alınamadığı vakalarda. - Fiziksel veya zihinsel olarak periton diyalizini hekim tarafından tarif edildiği şekilde uygulama kapasitesinde olmayan hastalar. Periton diyalizi sırasında yukarıdaki durumlardan herhangi birinin gelişmesi durumunda, tedavinin nasıl sürdürüleceğine hekim karar verir. 4.4. Özel kullanım uyarıları ve önlemleri Bu solüsyon yalnızca aşağıdaki durumların dikkatli yarar-risk analizlerinin yapılmasından sonra kullanılabilir: - Kusma ve/ veya diyareye bağlı olarak elektrolitlerin kaybı (bir süre için potasyum içeren periton diyaliz solüsyonuna geçiş gerekli olabilir). - Hiperkalsemi, örn. kalsiyum içeren fosfat bağlayıcıların ve/veya D vitamininin uygulanmasına bağlı (bu durumda daha düşük kalsiyum konsantrasyonuna sahip bir diyaliz solüsyonuna bir süre için veya kalıcı olarak geçiş düşünülmelidir). - Digital tedavisi yapılan hastalar: Serum potasyum seviyesinin düzenli olarak izlenmesi şarttır. Ciddi hipokalemide potasyum içeren diyaliz solüsyonunu kullanımı ve diyet için danışmanlık gerekli olabilir. - Büyük polikistik böbreklere sahip hastalar. Dışarı çekilen sıvı, berraklığı ve hacmi açısından kontrol edilmelidir. Abdominal ağrı ile birlikte bulanıklık veya sadece abdominal ağrı yada sadece bulanıklık peritonit belirtileridir. Periton diyalizi sırasında proteinler, aminoasitler ve suda çözünen vitaminlerde kayıp meydana gelir. Eksiklikleri önlemek için uygun bir diyet veya takviye sağlanmalıdır. Periton zarının transport karakteristikleri uzun dönem peritoneal diyaliz sırasında değişebilir, bu durum ilk olarak ultrafiltrasyonda kayıp olarak ortaya çıkar. Ciddi vakalarda periton diyalizi durdurulmalı ve hemodiyalize başlanmalıdır. Aşağıdaki parametrelerin düzenli izlenmesi tavsiye edilir:- Aşırı hidrasyon ya da dehidrasyonun erken tanısı için vücut ağırlığı - Serum sodyum, potasyum, kalsiyum, magnezyum, fosfat, asit baz durumu, kan gazları ve kan proteinleri, - Serum kreatinin ve üre - Parathormon ve kemik metabolizmasının diğer göstergeleri, - Kan şekeri - Periton diyalizinde adaptasyonda residüal renal fonksiyon Yaşlı hastalarYaşlı hastalarda periton diyalizine başlarken, bu hastalarda herni insidansının artmış olduğu göz önünde bulundurulmalıdır. Kullanıma hazır solüsyonun raf ömrüKullanıma hazır solüsyon hemen kullanılmalıdır, karıştırma sonrasında en fazla 24 saat içinde kullanılabilir. TaşımaPlastik torbalar nakliye veya depolama sırasında zarar görebilir. Bu durum kontaminasyona ve diyaliz solüsyonunda mikroorganizmaların üremesine neden olabilir. Torbalar bağlantılar yapılmadan ve periton diyalizi kullanılmadan önce her hangi bir hasara karşı dikkatlice kontrol edilmelidir. Bağlantılarda, kapanışta, torbanın birleşim noktaları ve köşelerde küçük de olsa herhangi bir hasarın kontaminasyona yol açmış olabileceği dikkate alınmalıdır. Hasar görmüş veya içeriği bulanık olan torbalar kesinlikle kullanılmamalıdır. Bu solüsyon yalnızca berraksa ve torbası zarar görmemiş ise kullanılmalıdır. Solüsyonun kullanılmayan kısmı imha edilmelidir. Koruyucu torba sadece uygulama öncesinde açılmalıdır. İki solüsyon karıştırılmadan kullanılmamalıdır. Enfeksiyon riskini azaltmak için diyalizat değişimi sırasında da aseptik koşullar sürdürülmelidir. Bu solüsyon periton diyalizi içindir ve intravenöz infüzyon için kullanılmamalıdır. 4.5 Diğer tıbbi ürünler ile etkileşimler ve diğer etkileşim şekilleri Periton diyaliz solüsyonunun kullanımı, periton zarından diyaliz olabilen diğer ilaçların etkinliklerinde azalmaya sebep olabilir. Doz ayarlaması gerekli olabilir. Serum potasyum seviyesinin fazla düşmesi digitale bağlı advers reaksiyonların sıklığını arttırabilir. Potasyum seviyeleri digital tedavisi sırasında yakından izlenmelidir. Kalsiyum içeren ilaçlar veya D vitamininin diyaliz solüsyonu ile birlikte kullanılması hiperkalsemiye neden olabilir. Diüretik ajanların kullanımı residüel diürezi sürdürmeye yardımcı olabilir, fakat bunun yanı sıra su ve elektrolit dengesizlikleri ile neticelenebilir. Diabetik hastalarda günlük insülin veya hipoglisemik ilaçların dozu, artmış glukoz yükü dikkate alınarak ayarlanmalıdır. 4. 6. Gebelik ve laktasyon Genel tavsiye Gebelik kategorisi B'dir. Çocuk doğurma potansiyeli bulunan kadınlar/ Doğum kontrolü (Kontrasepsiyon) Hayvanlar üzerinde yapılan çalışmalar, gebelik/ ve-veya/ embriyonal / fetal gelişim/ ve-veya / doğum/ ve-veya / doğum sonrası gelişim üzerindeki etkiler bakımından yetersizdir (Bkz. Bölüm 5.3). İnsanlara yönelik potansiyel risk bilinmemektedir. Doğum kontrol ilaçları ile etkileşimi bildirilmemiştir. Gebelik dönemi BALANCE solüsyonlarının gebe veya emzirme dönemindeki kadınlarda kullanımına ilişkin yeterli veri mevcut değildir. Hayvanlar üzerinde yapılan çalışmalar, gebelik/ ve-veya/ embriyonal / fetal gelişim/ ve-veya / doğum/ ve-veya / doğum sonrası gelişim üzerindeki etkiler bakımından yetersizdir (Bkz. Bölüm 5.3). İnsanlara yönelik potansiyel risk bilinmemektedir. Gebe kadınlara verilirken tedbirli olunmalıdır. Potansiyel yarar/ risk değerlendirmesi sonrasında kullanılması gerekmektedir. Laktasyon dönemi BALANCE solüsyonlarının emzirme dönemindeki kadınlarda kullanımına ilişkin yeterli veri mevcut değildir. Emzirme dönemindeki kadınlara verilirken tedbirli olunmalıdır. Üreme yeteneği/ Fertilite Üreme yeteneği/ Fertilite üzerinde herhangi bir etkisi bildirilmemiştir. 4.7. Araç ve makine kullanımı üzerindeki etkiler BALANCE %4.25 GLUKOZ 1.75 MMOL/L KALSİYUM periton diyaliz solüsyonunun araç ve makine kullanma yeteneği üzerinde herhangi bir etkisi bulunmamaktadır. 4. 8. İstenmeyen etkiler BALANCE, insan kanında bulunan elektrolitlere benzeyen içerikte bir solüsyondur. Ayrıca solüsyonun fizyolojik pH değerine benzerlik gösteren nötral bir pH'ı vardır. Olası yan etkiler periton diyaliz tekniğinin kendisinden kaynaklanabilir veya solüsyon tarafından indüklenebilir. Sıklık şu şekilde tarif edilmiştir: çok yaygın (> 1/10); yaygın (> 1/100 ve <1/10); yaygın olmayan (>1/1,000 ve <1/100); seyrek (>1/10,000 ve <1/1,000); çok seyrek (<1/10,000), bilinmiyor (eldeki verilerden hareketle tahmin edilemiyor). Periton diyaliz solüsyonundan kaynaklanan potansiyel advers reaksiyonlar:Metabolizma ve beslenme bozuklukları Bilinmiyor: Artmış şeker seviyeleri; hiperlipidemi; periton diyaliz solüsyonundan devamlı glukoz alımına bağlı olarak vücut ağırlığında artış. Kardiyak ve vasküler bozukluklar Bilinmiyor: Taşikardi; hipotansiyon; hipertansiyon. Respiratuvar, torasik ve mediastinal bozukluklar Bilinmiyor: Dispne Renal ve üriner bozukluklar Çok yaygın: Elektrolit dengesi bozuklukları (Örn: Hipokalemi) Bilinmiyor: Artmış kalsiyum alımının görüldüğü hiperkalsemi, örn. kalsiyum içeren fosfat bağlayıcıların uygulanması ile. Genel bozukluklar Bilinmiyor: Baş dönmesi; ödem; vücut ağırlığında hızlı azalma (dehidrasyon) veya artış (hidrasyon) şeklinde görülen hidrasyon bozuklukları. Daha yüksek glukoz konsantrasyonlarını kullanırken ciddi dehidrasyon görülebilir. Periton diyaliz tekniğinden kaynaklanan potansiyel advers reaksiyonlar:Enfeksiyonlar ve enfestasyonlar Çok yaygın: Peritonit; kateter çıkış yeri ile tünelde enfeksiyon. Çok seyrek: Sepsis Respiratuvar, torasik ve mediastinal bozukluklar Bilinmiyor: Diyaframın yükselmesi nedeniyle dispne, omuz ağrısı Gastrointestinal bozukluklar Çok yaygın: Herni Bilinmiyor: Abdominal distansiyon ve şişkinlik hissi. Diyare, konstipasyon. Genel bozukluklar ve uygulama/ katater yeri bozuklukları Bilinmiyor: Genel malez, katater çıkış bölgesinde kızarıklık, ödem, eksüdasyonlar, kabuklanma ve ağrı. Periton diyalizi prosedürleri ile ilgili bozukluklar Bilinmiyor: Boşaltılan solüsyonun bulanık olması; periton diyaliz solüsyonunun içeri ve dışarı akış bozuklukları. Boşaltılan diyalizatın bulanık olması peritonitin işaretleridir. Daha sonra karında ağrı, ateş ve genel malez hali, çok seyrek olarak ise sepsis gelişebilir.Hastanın derhal tıbbi destek alması gerekir. Boşaltılan bulanık diyalizatın bulunduğu torba steril bir kapak ile kapatılmalı ve mikrobiyolojik kontaminasyon ve beyaz kan hücreleri açısından analiz edilmelidir. Derinin çıkış bölgesi ve tünel enfeksiyonlarında en kısa sürede hekime danışılmalıdır. 4. 9. Doz aşımı ve tedavisi Aşırı doz ile ilgili olarak acil herhangi bir durum rapor edilmemiştir. Yüksek miktarda dolumu yapılan diyaliz solüsyonunun fazla kısmı kolayca boş bir torbaya çekilebilir. Buna rağmen, torba değişimleri çok sık veya çok hızlı yapıldığında, acil tıbbi müdahale gerektiren dehidrasyon ve/ veya elektrolit bozuklukları durumları meydana gelebilir. Bir değişimin unutulması durumunda kural olarak sonraki torbaların bekleme süreleri, bir günde gereken toplam diyaliz solüsyonu miktarına ulaşacak şekilde (örn. 4x 2000 ml) göre kısaltılmalıdır. Hatalı dengeleme hiperhidrasyona veya dehidrasyona ve elektrolit bozukluklarına yol açabilir. BALANCE %4.25 GLUKOZ 1.75 MMOL/L KALSİYUM Periton Diyaliz Solüsyonunun aşırı dozda kullanılmasının sonucu olarak dehidrasyon meydana gelmesi muhtemeldir. Dozajın altında tedavi, tedavinin aksaması veya kesilmesi; periferal ödem, kardiyak dekompansasyon ve/ veya diğer üremi semptomlarının eşlik ettiği hayati tehlike arz eden hiperhidrasyona sebep olabilir. Acil tedavi ve yoğun bakım için genel olarak kabul edilen kurallar uygulanmalıdır. Hasta acil hemodiyaliz yapılmasına ihtiyaç duyabilir. 5. FARMAKOLOJIK ÖZELLIKLER5. 1. Farmakodinamik özelliklerFarmakoterapötik grup: Periton diyaliz solüsyonu ATC kodu: B05D B BALANCE %4.25 GLUKOZ 1.75 MMOL/L KALSİYUM Periton Diyaliz Solüsyonu herhangi bir nedenden kaynaklanan son dönem böbrek yetmezliğinin tedavisinde intraperitoneal olarak uygulanan laktat tamponlu, glukoz içeren bir elektrolit solüsyondur. Sürekli ayaktan periton diyalizinin (CAPD) karakteristiği, periton boşluğunda sürekli olarak genellikle yaklaşık 2 litre diyaliz solüsyonunun bulunmasıdır. Bu diyaliz solüsyonu günde 35 kez taze solüsyon ile yer değiştirilir. Her periton diyaliz tekniğinin temel prensibi, solütlerin ve suyun kan ve diyaliz solüsyonu arasında fizikokimyasal özelliklerine göre difüzyon veya konveksiyon ile yer değişimine olanak veren peritoneumun yarı geçirgen bir membran olarak kullanılmasıdır. Solüsyonun elektrolit profili temelde serum fizyolojik ile aynıdır, intraperitoneal madde ve sıvı alışverişi yoluyla renal replasman tedavisi için üremik hastalarda kullanılmak üzere adapte edilmiştir. Normalde idrar ile elimine edilen üre ve kreatinin gibi üremik atık maddeler, inorganik fosfat, ürik asit, diğer solütler ve su vücuttan diyaliz solüsyonuna geçer. Sıvı dengesi, farklı glukoz konsantrasyonlarına sahip solüsyonların uygulanması ve daha verimli sıvı çekişi (ultrafiltrasyon) ile sürdürülebilir. Son dönem böbrek yetmezliğinde sekonder olarak gelişen metabolik asidoz solüsyondaki laktat ile dengelenir. Laktatın tamamen metabolizasyonu bikarbonat oluşumu ile neticelenir. 5. 2. Farmakokinetik özellikler Genel özellikler Üremik atık ürünleri (örn. üre, kreatin, ürik asit), inorganik fosfat ve sodyum, potasyum, kalsiyum ve magnezyum gibi elektrolitler diffüzyon ya da konveksiyon yolu ile vücuttan diyaliz solüsyonuna geçer. Diyalizattaki glukoz, BALANCE %4.25 GLUKOZ 1.75 MMOL/L KALSİYUM periton diyaliz solüsyonunda ozmotik bir ajan olarak kullanılır. Diyaliz solüsyonu ve ekstraselüler sıvı arasındaki difüzyon gradyentini azaltarak yavaşça absorbe olur. Bekleme zamanının başında maksimal olan ultrafiltrasyon yaklaşık 2-3 saatte pik değere ulaşır. Sonrasında absorpsiyon, ultrafiltratın progresif kaybı ile başlar. 6 saatlik diyaliz periyodunda diyalizat glukozunun %60-80 kadarlık kısmı absorbe olur. Kalsiyum transferi; diyaliz solüsyonundaki glukoz konsantrasyonuna, çıkan sıvının hacmine, serum iyonize kalsiyumuna ve diyaliz solüsyonundaki kalsiyum konsantrasyonuna bağlıdır. Glukoz konsantrasyonu, çıkan sıvının hacmi, serum iyonize kalsiyumu arttıkça ve diyaliz solüsyonundaki kalsiyum konsantrasyonu azaldıkça hastadan diyalizata kalsiyum transferi artar. 5. 3. Klinik öncesi güvenlilik verileri BALANCE %4.25 GLUKOZ 1.75 MMOL/L KALSİYUM periton diyaliz solüsyonu ile preklinik toksisite çalışmaları yapılmamıştır, fakat karşılaştırılabilir periton diyaliz solüsyonları ile yapılan klinik çalışmalarda herhangi bir majör toksisite riski görülmemiştir. 6. FARMASÖTİK BİLGİLER 6. 1. Yardımcı maddelerin listesi Hidroklorik asit Sodyum hidroksit Sodyum hidrojen karbonat Enjeksiyonluk su 6.2 Geçimsizlikler Geçimsizlik ve kontaminasyon riskinden dolayı diğer ilaçlar yalnızca hekim tarafından reçetelendiğinde kullanılmalıdır. Bu ilaç kullanma talimatları bölümünde belirtilenler hariç diğer ilaçlarla birlikte kullanılmamalıdır. 6.3. Raf ömrü 24 ay Karıştırma işlemi sonrası raf ömrü: Kullanım esnasındaki kimyasal ve fiziksel stabilitesi 20°C'de 24 saattir. 6. 4. Saklamaya yönelik özel tedbirler 25° C altındaki oda sıcaklığında saklanmalıdır. 4° C'nin altında saklamayınız. 6. 5. Ambalajın niteliği ve içeriği Çift bölmeli torba Laktat solüsyonu : glukoz temelli elektrolit solüsyonu = 1:1 Çift bölmeli torba sistemi: Çok tabakalı poliolefin torbalarından yapılmış koruyucu torba içinde non-PVC çift bölmeli solüsyon torbası. Stay safe balance sistemdeçift odacıklı bir torba sistemi, poliolefinlerden yapılmış bir hat sistemi, döner düğmeli (polipropilen) bir sistem bağlantısı (DİSK) ve yine çok tabakalı poliolefin filmden yapılmış bir drenaj torbası bulunmaktadır.Sleep safe balance sistemindeçift bölmeli torba sistemi ve polipropilenden oluşan bir torba bağlantısı bulunmaktadır.Safe lock balance sistemindeçift bölmeli torba sistemi ve polikarbonattan oluşan bir torba bağlantısı bulunmaktadır.6. 6. Tıbbi üründen arta kalan maddelerin imhası ve diğer özel önlemler Özel bir gereklilik yoktur. Kullanılmamış ürünler ya da atık materyaller Tıbbi Atıkların Kontrolü Yönetmeliği ve Ambalaj ve Ambalaj Atıklarının Kontrolü Yönetmeliğine uygun olarak imha edilmelidir. 7. RUHSAT SAHİBİ FRESENIUS MEDİKAL HİZMETLER A.Ş. Eski Büyükdere Cad. Giz 2000 Plaza No : 7, Kat : 17 34398 Maslak / İstanbul / TÜRKİYE Tel : (0212) 335 72 00 Faks : (0212) 335 72 29 8. RUHSAT NUMARASI(LARI) 119/83 9. İLK RUHSAT TARİHİ/ RUHSAT YENİLEME TARİHİ İlk ruhsat tarihi: 03.04.2006 Ruhsat yenileme tarihi: 03.04.2011 10. KÜB'ÜN YENİLENME TARİHİ |
İlaç BilgileriBalance %4.25 Glukoz 1.75mmol/L Kalsiyum Periton Diyaliz SolüsyonuEtken Maddesi: KÜB içeriğine bakınız Atc Kodu: B05DB Kullanma talimatı ve kısa ürün bilgileri
Google Reklamları
|
Ana Sayfa | Hakkımızda | İlaçlar | İlaç Ara | İlaç Firmaları | Gizlilik | Bize Ulaşın
Telif Hakkı 2008-2026 © İlaç Prospektüsü. Tüm Hakları Saklıdır.Uyarı: Sitemizde yayınladığımız ilaç bilgileri ile doktora danışmadan kesinlikle ilaç kullanmayınız!
Aksi halde doğabilecek sağlık sorunlarından ilacprospektusu.com sorumlu tutulamaz.