Brecur 100 mikrogram İnhalasyon İçin Ölçülü Dozlu Aerosol Kısa Ürün BilgisiSolunum Sistemi » Solunum Sisteminde Tıkanma - Astım İlaçları » Adrenerjikler (İnhalan) » Selektif Beta 2 Adrenoreseptör Agonistleri » Salbutamolİnhalant (çekilerek alınan) KISA URUN BILGISI 1. BEŞERI TIBBI ÜRÜNÜN ADIBRECUR 100 mikrogram inhalasyon için ölçülü dozlu aerosol2. KALITATIF VE KANTİTATIF BILEŞIM ETKIN MADDE:100 mikrogram Salbutamol'e eşdeğer 120 mikrogram Salbutamol Sülfat içerir.Yardımcı maddeler:Dehidrat alkol 4,320 mgYardımcı maddeler için 6.1'e bakınız. 3. FARMASÖTIK FORMİnhalasyon için ölçülü dozlu aerosolAlüminyum inhaler kabı içinde basınçlı propellant gaz ile doldurulmuş süspansiyon. Alüminyum konteynere bir dozajlama valf eklidir. 4. KLİNIK ÖZELLIKLER4.1. Terapötik endikasyonlarBRECUR, Reversibl hava yolu tıkanmasında çabuk başlayan etkisiyle (etkisi 5 dakika içinde başlar) kısa süreli (4-6 saat) bronkodilatasyon sağlar. Astmatik semptomların giderilmesinde ve önlenmesinde uygundur. BRECUR semptomlar oluştuğunda rahatlamak için ve hasta tarafından bilinen, astım krizinin ortaya çıkmasına neden olabilecek koşullarda (ör. egzersiz öncesi veya kaçınılması mümkün olmayan alerjene maruz kalma durumlarında) semptomları önleyici olarak kullanılabilir. BRECUR özellikle hafif, orta ve şiddetli astımda hemen rahatlatıcı ilaç olarak kullanılır; ancak salbutamole güvenilerek düzenli inhale kortikosteroid tedavisine başlanılması ve kullanılması geciktirilmemelidir. 4.2. Pozoloji ve uygulama şekli Pozoloji/uygulama sıklığı ve süresi:BRECUR, sadece oral inhalasyon yolu ile uygulanır.Nefes alma ile (inspirasyon) aerosol uygulamasının aynı anda olmasında (senkronizasyonunda) zorluk yaşayan hastalar, BRECUR'u uygun bir aygıt (volumatic spacer gibi) ile kullanabilir. Yetişkinler (Yaşlılar dahil): Bronkospazm dahil akut astım semptomlarının rahatlatılması için, 1 inhalasyon (100 mikrogram) tek minimum başlangıç dozu olarak uygulanabilir. Eğer gerekli ise bu doz 2 inhalasyona arttırılabilir. Alerjen veya egzersiz tarafından indüklenen semptomların önlenmesi için, maruziyetten 10-15 dakika önce 2 inhalasyon uygulanmalıdır. Kronik tedavi için, günde 4 kereye kadar 2 inhalasyon kullanılabilir. Çocuklar: Bronkospazm dahil akut astım semptomlarının rahatlatılması için veya alerjene maruziyet veya egzersizden önce, 1 inhalasyon veya gerekli ise iki inhalasyon kullanılabilir. Kronik tedavi için, günde 4 kereye kadar 2 inhalasyon kullanılabilir. 5 yaşın altındaki çocuklarda uygulamanın kolaylaştırılması için, uygun bir alet (babyhaler spacer gibi) kullanılabilir. BRECUR'un gerektikçe kullanımı 24 saat içerisinde 8 inhalasyonu geçmemelidir. Bu tür bir gerektikçe sık bir şekilde kullanımı ve dozdaki ani artışlar, astımın yeterli şekilde kontrol edilemediğini veya astımın kötüleştiğini gösterir. Uygulama şekli:BRECUR, sadece inhalasyon yolu ile uygulanır.İnhalasyon spreyinin doğru kullanımı doktor veya eczacı tarafından hastaya gösterilmelidir. İnhalasyon sırasında hastalar tercihen oturmalı veya ayakta durmalıdır. İnhalasyon spreyi dik konumda kullanım için tasarlanmıştır. İnhalasyon cihazı kullanma talimatı için bakınız ekli talimat. Özel popülasyonlara ilişkin ek bilgiler:Böbrek yetmezliği:Böbrek yetmezliği olan hastalarda doz ayarlanması gerektiğini gösteren veri bulunmamaktadır.Karaciğer yetmezliği:Karaciğer yetmezliği olan hastalarda doz ayarlanması gerektiğini gösteren veri bulunmamaktadır.Pediyatrik popülasyon:Pediyatrik popülasyonda kullanım için Bölüm 4.2'ye bakınız.Geriyatrik popülasyon:Doz ayarlanması gerekli değildir.4.3. KontrendikasyonlarBRECUR, bileşenlerinden herhangi birine karşı aşırı duyarlılığı olan hastalarda kontrendikedir. İntravenöz salbutamol ve bazen salbutamol tabletleri plasenta previa, doğum öncesi kanamalar veya gebelik toksemisi gibi komplikasyonların eşlik etmediği erken doğum sancılarının önlenmesinde kullanılmasına rağmen, inhale salbutamol preparatları erken doğumun tıbbi idaresinde uygun değildir. Salbutamol preparatları düşük tehtidi için de kullanılmamalıdır.4.4. Özel kullanım uyarıları ve önlemleriİlacın akciğerlere optimum ulaşması için hastanın inhalasyon tekniği kontrol edilerek nefes alma ile (inspirasyon) aerosol uygulamasının aynı anda olmasına (senkronizasyonuna) dikkat edilmelidir. Hastalar daha önceki inhalerleri ile karşılaştırıldığında inhalasyonu takiben farklı bir tat hissedebilecekleri konusunda uyarılmalıdır.Bronkodilatörler şiddetli veya stabil olmayan astımlı hastalarda tek ya da başlıca tedavi yöntemi olmamalıdır. Şiddetli astım, şiddetli atak ve ölüm riski taşıdığı için akciğer fonksiyon testleri dahil düzenli medikal değerlendirme gerektirir. Doktorlar bu hastalarda, inhale kortikosteroid ve/veya oral kortikosteroid tedavisinin önerilen maksimum dozunun kullanımını göz önünde bulundurmalıdır. Uygulama dozu veya sıklığı sadece doktora danışılarak arttırılmalıdır. İnhale salbutamolün daha önce kullanılan etkili dozları ile en az üç saat rahatlama sağlanmadığı takdirde, hasta gerekli ilave önlemleri almak için doktora danışmalıdır. Semptomların rahatlatılması için bronkodilatörlerin (özellikle kısa etkili inhale3 2-agonistlerin) kullanımının artması, astım kontrolünün kötüleştiğini gösterir. Kısa etkili kurtarıcı bronkodilatör tedavisinin daha az etkili olmaya başlaması veya normalden daha fazla inhalasyona ihtiyaç duyulması hastalığın kötüleştiğini gösterdiği için, bu gibi durumlarda hastalar tıbbi yardım almaları konusunda bilgilendirilmelidir. Bu gibi durumlarda hasta değerlendirilmeli ve artan antiinflamatuvar tedavi ihtiyacı göz önünde bulundurulmalıdır (ör. daha yüksek dozlarda inhale kortikosteroid veya oral kortikosteroid tedavi süreci). Şiddetli astım alevlenmeleri normal yolla tedavi edilmelidir. Salbutamol dahil sempatomimetik ilaçlar ile kardiyovasküler etkiler gözlenebilir. Pazarlama sonrası verilerden ve yayınlanan literatürlerden, salbutamol ile ilişkili olarak nadir miyokardiyal iskemi olguları geliştiğine dair bazı kanıtlar mevcuttur. Şiddetli kalp hastalığı olan (örneğin iskemik kalp hastalığı, aritmi veya şiddetli kalp yetmezliği) ve salbutamol kullanan hastalar, göğüs ağrısı veya kalp hastalığının kötüleştiğini gösteren diğer semptomlar ile karşılaştığı durumlarda doktora danışmaları konusunda uyarılmalıdır. Dispne ve göğüs ağrısı gibi semptomlar değerlendirilirken, bu semptomlar solunumsal veya kardiyak kökenli olabileceğinden dikkatli olunmalıdır. Salbutamol, tirotoksikozlu hastalarda dikkatli kullanılmalıdır. Parenteral veya nebulize uygulama ile beta-2 agonist tedavisi potansiyel olarak ciddi hipokalemiye neden olabilir. Akut şiddetli astımda bu etki ksantin türevleri, steroidler ve diüretikler ile ve hipoksi nedeniyle şiddetlenebileceğinden özel dikkat gösterilmelidir. Bu gibi durumlarda serum potasyum düzeyleri monitörize edilmelidir. Bu tıbbi ürün az miktarda -her dozda 100 mg'dan daha az- alkol içerir. 4.5. Diğer tıbbi ürünler ile etkileşimler ve diğer etkileşim şekilleriSalbutamol ve selektif olmayan beta-blokör ilaçlar (propranolol gibi) birlikte kullanılmamalıdır.Özel popülasyonlara ilişkin ek bilgilerÖzel popülasyonlara ilişkin herhangi bir etkileşim çalışması tespit edilmemiştir.Pediyatrik popülasyon:Pediyatrik popülasyona ilişkin herhangi bir etkileşim çalışması tespit edilmemiştir.4.6. Gebelik ve laktasyon Genel tavsiyeGebelik kategorisi C.Çocuk doğurma potansiyeli bulunan kadınlar/Doğum kontrolü (Kontrasepsiyon)Çocuk doğurma potansiyeli bulunan kadınların etkin doğum kontrol (kontrasepsiyon) yöntemleri uygulaması önerilmektedir.Gebelik dönemiBRECUR'un gebe kadınlarda kullanımına ilişkin yeterli veri mevcut değildir.Hayvanlar üzerinde yapılan araştırmalar üreme toksisitesinin bulunduğunu göstermiştir. İnsanlara yönelik potansiyel risk bilinmemektedir. Salbutamole intrauterin maruziyet sonrasında çeşitli konjenital anomalilerin (yarık damak, ekstremite kusurları ve kardiyak bozukluklar) meydana geldiğini gösteren nadir raporlar alınmıştır. Bu raporlarda bazı annelerin gebelik dönemi süresince çoklu ilaç tedavisi aldığı bildirilmiştir. BRECUR açık bir şekilde gerekli değilse gebelik sırasında kullanılmamalıdır. İlaç kullanımı ancak anneye sağlaması beklenen yararı fetüse olan olası bir riskten fazla ise düşünülmelidir. Laktasyon dönemiSalbutamol muhtemelen anne sütüne geçtiğinden, emziren annelerde kullanımı özel dikkat gerektirmektedir. Anne sütündeki salbutamolün yenidoğana zararlı bir etkisi olup olmadığı bilinmemektedir. Salbutamol'ün beklenen yararları herhangi bir potansiyel riskini dengelemedikçe emziren annelerde kullanımı tavsiye edilmez.Üreme yeteneği/FertiliteVeri mevcut değildir.4.7. Araç ve makine kullanımı üzerindeki etkilerBRECUR'un içeriğindeki salbutamol sülfatın araç ve makine kullanımı üzerine etkisi olduğu bildirilmemiştir. BRECUR'un araç ve makine kullanımı üzerinde etkisi olması beklenmez.4.8. İstenmeyen etkilerBRECUR ile ilgili advers olaylar aşağıda verilmiştir:Yan etkilerin görülme sıklığı aşağıda belirtilmektedir: Çok yaygın 3^1/10), yaygın (>1/100 ila <1/10), yaygın olmayan (>1/1000 ila <1/100), seyrek (>1/10.000 ila <1/1000), çok seyrek (<1/10.000), bilinmiyor (eldeki verilerden hareketle tahmin edilemiyor). Çok yaygın ve yaygın olgular genel olarak klinik çalışma verilerinden; seyrek, çok seyrek ve sıklığı bilinmeyen olgular genellikle spontan verilerden belirlenmiştir. Bağışıklık sistemi hastalıklarıÇok seyrek: Anjiyoödem, ürtiker, bronkospazm, hipotansiyon ve kollaps dahil aşırı duyarlılık reaksiyonlarıMetabolizma ve beslenme hastalıklarıSeyrek: HipokalemiBeta2 agonist tedavisi ile potansiyel olarak ciddi hipokalemi meydana gelebilir. Sinir sistemi hastalıklarıYaygın: Tremor, baş ağrısı Çok seyrek: HiperaktiviteKardiyak hastalıklarYaygın: TaşikardiYaygın olmayan: Palpitasyonlar Çok seyrek: Kardiyak aritmiler (atriyal fibrilasyon, supraventriküler taşikardi ve ekstrasistoller dahil) Bilinmiyor: Miyokardiyal iskemi1 (Bakınız 4.4 Özel kullanım uyarıları ve önlemleri) Vasküler hastalıklarıSeyrek: Periferal vazodilatasyonSolunum, torasik ve mediastinal hastalıklarÇok seyrek: Paradoksikal bronkospazmDiğer inhalasyon tedavilerinde olduğu gibi, doz uygulamasının ardından hırıltıda ani bir artış ile paradoksikal bronkospazm meydana gelebilir. Bu durum hemen alternatif bir presezantasyon ile veya farklı bir hızlı etkili inhale bronkodilatör ile tedavi edilmelidir. Böyle bir durumda BRECUR ile tedavi hemen sonlandırılmalı, hasta değerlendirilmeli ve gerekli ise alternatif bir tedavi başlatılmalıdır. Gastrointestinal hastalıklarYaygın olmayan: Ağız ve boğaz tahrişiKas-iskelet bozukluklar, bağ dokusu hastalıklarıYaygın olmayan: Kas krampları4.9. Doz aşımı ve tedavisiSalbutamol ile doz aşımının en yaygın belirtileri ve semptomları taşikardi, tremor, hiperaktivite ve hipokalemi da dahil metabolik etkiler gibi beta agonistlerin farmakolojisinden kaynaklanan geçici olaylardır.Aşırı doz salbutamol uygulamasını takiben hipokalemi meydana gelebilir. Serum potasyum seviyeleri monitörize edilmelidir. Kardiyak semptomlar (ör. taşikardi, palpitasyon) meydana gelen hastalarda, tedavinin sonlandırılması ve kardiyoselektif beta-blokör ilaçlar gibi uygun semptomatik tedavi uygulanması göz önünde bulundurulmalıdır. Bronkospazm öyküsü olan hastalarda beta blokörler dikkatli kullanılmalıdır. 5. FARMAKOLOJIK ÖZELLIKLER5.1. Farmakodinamik özelliklerFarmakoterapötik grup: Selektif Beta-2-Adrenoseptör Agonistleri ATC Kodu: R03 AC 02Salbutamol selektif bir beta-2 adrenoseptör agonistidir. Terapötik dozlarda bronşiyal kasınp 2-adrenoseptörleri üzerinde etki göstererek reversibl hava yolu tıkanmasında çabuk başlayan etkisiyle (etkisi 5 dakika içinde başlar) kısa süreli (4-6 saat) bronkodilatasyon sağlar. 5.2. Farmakokinetik özellikler Genel özelliklerEmilim:İnhale yoldan uygulamayı takiben dozun %10-20'si alt hava yollarına ulaşır. Geri kalanı ilaç uygulama sisteminde veya orofarinkste birikir ve buradan yutulur. Hava yollarında biriken kısım pulmoner dokulara ve dolaşıma absorbe olur. Yutulan kısım gastrointestinal kanaldan emilir. Dağılım:Salbutamol plazma proteinlerine %10 oranında bağlanır. Biyotransformasyon:Hava yollarında biriken kısım pulmoner dokulara ve dolaşıma absorbe olur, fakat akciğerde metabolize olmaz. Sistemik dolaşıma ulaştığında hepatik metabolizmaya uğrar ve başlıca idrarla değişmemiş ilaç ve fenolik sülfat şeklinde atılır. Yutulan kısım önemli ölçüde ilk-geçiş metabolizmasına uğrayarak fenolik sülfata dönüşür. Eliminasyon:Salbutamol intravenöz olarak verildiğinde yarılanma ömrü 4-6 saat arasındadır, kısmen renal yolla kısmen de başlıca idrar ile atılan inaktif 4-O-sülfata (fenolik sülfat) metabolize olarak elimine edilir. Dışkı minör atılım yoludur. İntravenöz, oral olarak veya inhalasyon ile verilen dozun büyük bir kısmı 72 saat içinde atılır. Değişmemiş ilaç ve konjugatı başlıca idrar ile atılır. Doğrusallık/Doğrusal Olmayan Durum:Veri mevcut değildir. 5.3. Klinik öncesi güvenlilik verileriDiğer potent selekti|f 2-agonistlerde olduğu gibi, subkutan yoldan uygulanan salbutamolün farelerde teratojenik olduğu gösterilmiştir. Gerçekleştirilen bir üreme çalışmasında, 2.5 mg/kg dozunda, fetüslerin %9.3'ünde yarık damak oluşumu gözlenmiştir. Sıçanlarda, gebelik süresince oral 0.5, 2.32, 10.75 ve 50 mg/kg/gün tedavi dozları anlamlı fötal anomalilere neden olmamıştır. En yüksek dozda meydana gelen tek toksik etki, maternal bakım eksikliğinden kaynaklanan yeni doğan ölümünde artış olmuştur. Oral 50 mg/kg/gün dozlarında (insanlarda kullanılan normal dozdan çok daha fazla) tavşanlarda gerçekleştirilen üreme çalışmaları fetüslerde tedavi ile ilişkili değişiklikler göstermiştir; bu değişiklikler doğuştan göz kapağı yokluğu (ablefarin), sekonder damak yarıkları (palatoşizis), kafatasının ön kemiklerinde kemikleşmede (kraniyosisiz) ve kemik eğriliğindeki değişiklikler olmuştur. Salbutamolün basınçlı doz inhaleri olarak yeniden formüle edilmesi, salbutamolün bilinen toksikolojik profilini değiştirmemiştir.HFA 134a'nın çok yüksek buhar konsantrasyonlarında, iki yıllık bir süreç boyunca günlük maruziyet uygulanan çeşitli hayvan türlerinde toksik etkiye neden olmadığı gösterilmiştir. 6. FARMASÖTİK ÖZELLİKLER6.1. Yardımcı maddelerin listesiHFA134a Dehidrat alkol Oleik asit6.2. GeçimsizliklerBilinen geçimsizliği yoktur.6.3. Raf ömrü24 ay (25°C'nin altında saklandığında)6.4. Saklamaya yönelik özel tedbirler25°C'nin altındaki oda sıcaklığında saklayınız. Direk gün ışığından ve donmaktan koruyunuz. Aerosol kutusu soğuk olduğunda terapötik etkisi azalabilir.Aerosol kutusu delinmemeli, boş olsa bile kırılmamalı, ateşten uzak tutulmalıdır. 6.5. Ambalajın niteliği ve içeriğiBRECUR 100 mcg inhalasyon için ölçülü dozlu aerosol, 200 dozluk aerosol tüplerde karton kutuda kullanma talimatı ile birlikte sunulmaktadır.6.6. Beşeri tıbbi üründen arta kalan maddelerin imhası ve diğer özel önlemlerKullanılmamış olan ürünler ya da atık materyaller 'Tıbbi atıkların kontrolü yönetmeliği' ve 'Ambalaj ve Ambalaj Atıklarının Kontrolü Yönetmelikleri'ne uygun olarak imha edilmelidir.7. RUHSAT SAHİBİVitalis İlaç San. Tic. A.Ş.General Ali Rıza Gürcan Cad. Merter İş Merkezi Bağımsız Bölüm No:2/2 Güngören/İSTANBUL Tel : 0 212 481 20 95 Faks : 0 212 481 20 95 e-mail : [email protected] 8. RUHSAT NUMARASI (LARI)240/89. İLK RUHSAT TARİHİ / RUHSAT YENİLEME TARİHİİlk ruhsat tarihi: 08.02.2012 Ruhsat yenileme tarihi:10. KÜB'ÜN YENİLENME TARİHİİlk kez kullanımdan önce hastalar ağızlık kapağını, kapağın yanlarından hafifçe sıkarak çıkarmalı, inhalasyon spreyini iyi bir şekilde sallamalı, baş parmak ağızlığın altında inhalasyon spreyinin tabanında olacak şekilde parmaklar ve baş parmak arasında tutmalı ve inhalasyon spreyinin çalıştığından emin olmak için sayaç 200'ü gösterene kadar boşluğa sıkım yapmalıdır. İnhalasyon spreyi her sıkımdan önce sallanmalıdır.İnhalasyon spreyi bir hafta veya daha uzun süre kullanılmadığında hastalar ağızlık kapağını çıkarmalı, inhalasyon spreyi ile boşluğa iki kez sıkım yapılmalıdır. İnhalasyon spreyi tarafından sayaç üzerinde aktifleştirilen sayı her sıkımda birer birer geriye sayar. Inhalasyon spreyinin kullanım talimatıİnhalasyon spreyinin test edilmesi: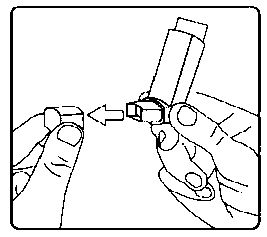 İnhalasyon spreyinizi kullanacağınız zaman oturunuz veya ayakta dik durunuz. 1. İlk resimde gösterildiği gibi ağızlık kapağını çıkarınız. Ağızlığın temiz olduğundan emin olmak için içini ve dışını kontrol ediniz. 2. İnhalasyon spreyinizi her kullanımdan önce iyice çalkalayınız. 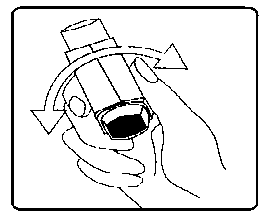 3. İnhalasyon spreyinizi baş parmağınız ağızlığın altında, inhalasyon spreyinizin tabanında olacak şekilde dik tutunuz.
3. İnhalasyon spreyinizi baş parmağınız ağızlığın altında, inhalasyon spreyinizin tabanında olacak şekilde dik tutunuz.5. Ağzınızdan yavaş ve derin nefes alınız ve aynı anda bir puf doz boşaltmak için inhalasyon spreyinizin üst kısmına basınız.  6. Nefesinizi birkaç saniye veya rahatça tutabildiğiniz kadar tutunuz ve ağızlığı ağzınızdan çıkarıp parmağınızı inhalasyon spreyinizin üst kısmından çekiniz.
6. Nefesinizi birkaç saniye veya rahatça tutabildiğiniz kadar tutunuz ve ağızlığı ağzınızdan çıkarıp parmağınızı inhalasyon spreyinizin üst kısmından çekiniz.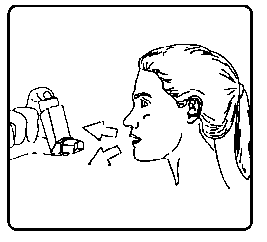
4. Ağızlığı dişlerinizin arasına koyunuz ve dudaklarınızı sıkıca kapatınız.   7. Her bir puf ilaç alımı arasında yaklaşık yarım dakika bekleyiniz ve sonra 2-6. basamakları tekrarlayınız.
7. Her bir puf ilaç alımı arasında yaklaşık yarım dakika bekleyiniz ve sonra 2-6. basamakları tekrarlayınız.8. Kullanımdan sonra tozdan korumak için ağızlığın kapağını hemen kapatınız. Ağızlık kapağı doğru bir şekilde yerleştirildiğinde tam yerine oturacaktır. Eğer yerine oturmuyorsa, ağızlık kapağını diğer yöne çeviriniz. Çok fazla güç uygulamayınız. Hastalar 4, 5 ve 6. basamakları hızlı bir şekilde yapmamalıdır. Hastaların inhalasyon spreyini etkin hale getirmeden hemen önce mümkün olduğunca yavaş bir şekilde nefes almaya başlaması önemlidir. Hastalar aynanın önünde ilk birkaç uygulama için pratik yapmalıdırlar. Eğer hastalar inhalasyon spreyinin üstünden veya ağızlarının yanından buhar geldiğini görürse, 2. basamaktan itibaren uygulamaya tekrar başlamalıdırlar. Hastalar sayaç 020'yi gösterdiğinde inhalasyon spreyini değiştirmeyi göz önünde bulundurmalıdırlar. Sayaç 000'ı gösterdiğinde önerilen tüm puflar kullanılmış olduğundan inhalasyon spreyini kullanmayı durdurmalıdırlar. Sayaç 000'ı gösterdiğinde inhalasyon spreyi değiştirilmelidir. Hastalar sayaç üzerindeki sayıları asla değiştirmemeli veya metal tüpten sayacı çıkarmamalıdırlar. Sayaç sıfırlanamaz ve daimi olarak metal tüpe bağlıdır. İnhalasyon spreyinin temizlenmesiİnhalasyon spreyinizi haftada en az bir kez temizleyiniz.1. Ağızlık kapağınız çıkarınız. 2. Tüpü plastik gövdeden çıkarmayınız. 3. Kuru bir bez veya kumaş ile ağızlığın içini ve dışını ve plastik gövdeyi siliniz. 4. Ağızlık kapağını doğru bir şekilde yerleştiriniz. Kapağı yerleştirmek için çok fazla güç uygulamayınız. 1 Pazarlama sonrası veriler spontan olarak bildirilmiştir, bu nedenle sıklığı bilinmiyor olarak belirtilmiştir. |
İlaç BilgileriBrecur 100 mikrogram İnhalasyon İçin Ölçülü Dozlu AerosolEtken Maddesi: Mikrogram salbutamol sülfat Atc Kodu: R03AC02 Kullanma talimatı ve kısa ürün bilgileri
Google Reklamları
İlgili İlaçlar |
Ana Sayfa | Hakkımızda | İlaçlar | İlaç Ara | İlaç Firmaları | Gizlilik | Bize Ulaşın
Telif Hakkı 2008-2026 © İlaç Prospektüsü. Tüm Hakları Saklıdır.Uyarı: Sitemizde yayınladığımız ilaç bilgileri ile doktora danışmadan kesinlikle ilaç kullanmayınız!
Aksi halde doğabilecek sağlık sorunlarından ilacprospektusu.com sorumlu tutulamaz.