İnhawell 100 mcg İnhalasyon İçin Toz İçeren Kapsül Kısa Ürün BilgisiSolunum Sistemi » Solunum Sisteminde Tıkanma - Astım İlaçları » Adrenerjikler (İnhalan) » Selektif Beta 2 Adrenoreseptör Agonistleri KISA URUN BILGISI 1. BEŞERI TIBBI ÜRÜNÜN ADIINHAWELL 100 mcg inhalasyon için toz içeren kapsül2. KALITATIF VE KANTİTATIF BILEŞIM ETKIN MADDE:Levosalbutamol Sülfat* 120,47 mcgYardımcı madde(ler):Laktoz 12,87953 mg*100 mcg Levosalbutamol'e eşdeğer Yardımcı maddeler için, 6.1'e bakınız. 3. FARMASÖTIK FORMInhalasyon Için Toz içeren KapsülFlesh opak, natural transparan renk kapsül içinde, beyaz toz. 4. KLİNIK ÖZELLIKLER4.1. Terapötik endikasyonlarINHAWELL, reversibl obstrüktif solunum yolu hastalığı olan 4 yaş ve üzeri çocuklarda, adölesanlarda ve yetişkinlerde bronkospazmın önlenmesinde ve tedavisinde endikedir.4.2. Pozoloji ve uygulama şekli Pozoloji/ uygulama sıklığı ve süresi:Yetişkin ve pediyatrik astım:Bronkospazmın akut epizodlarının tedavisinde veya astmatik semptomların önlenmesinde: 4 yaş ve üzeri çocuklarda ve yetişkinlerde önerilen doz her 4-6 saatte bir, 1 inhalasyon dozunun inhale edilmesidir. Daha sık doz uygulaması veya daha fazla sayıda inhalasyon dozunun inhale edilmesi önerilmemektedir. Eğer daha önceki etkili INHAWELL tedavi dozu yeterli astım kontrolünün sağlanmasında başarısız olursa, bu durum hastalığın kötüleştiğinin bir belirtisi olabilir. Böyle bir durum hasta tedavi rejiminin yeniden değerlendirilmesini ve ek tedavi seçeneklerinin (örneğin kortikosteroidler) göz önünde bulundurulmasını gerektirir. Uygulama şekli:INHAWELL inhaler kapsül; ağız yoluyla inhalasyon şeklinde kullanılır.İnhalasyon cihazı yoluyla nefes alındığında ilaç akciğerlere ulaşır. Bu nedenle, cihazın ağız parçası aracılığıyla derin ve güçlü nefes alınması önemlidir. Inhalasyon cihazının kullanımı doktor veya eczacı tarafından hastaya gösterilmelidir. Kapsüllerin kesinlikle ağız içine alınarak yutulmaması ve kesinlikle inhaler içine yerleştirildikten sonra soluk alma yoluyla kullanılması gerektiği konusunda hasta bilgilendirilmelidir. Jelatin kapsülün parçalanabileceği ve inhalasyondan sonra ağız veya boğaza küçük jelatin parçacıklarının ulaşabileceği hastaya anlatılmalıdır. Bu olasılık kapsülün birden fazla delinmemesi ile en aza indirilir. Kapsüller blister ambalajdan ancak kullanım öncesi çıkarılmalıdır. İnhalasyon cihazı kullanma talimatı için bakınız ekli talimat. Özel popülasyonlara ilişkin ek bilgiler:Böbrek yetmezliği:Böbrek yetmezliği olan hastalara yüksek doz INHAWELL uygulanacağı zaman dikkatli olunmalıdır.Karaciğer yetmezliği:Karaciğer yetmezliği olan hastalar için özel doz önerisi bulunmamaktadır.Pediyatrik popülasyon:4 yaşın altındaki çocuklarda levosalbutamolün etkinliği ve güvenirliği belirlenmemiştir. 4 yaş ve üzerindeki çocuklar İNHAWELL'i yetişkinler için önerilen dozlarda kullanabilirler (4.2. Pozoloji ve uygulama şekli'ne bakınız).Geriyatrik popülasyon:Yaşla birlikte böbrek fonksiyonlarında azalma olabileceğinden, geriyatrik popülasyonda doz seçiminde dikkatli olunmalıdır ve renal fonksiyonun izlenmesi yararlı olabilir.4.3. KontrendikasyonlarINHAWELL, levosalbutamole, rasemik salbutamole ve içeriğindeki bileşenlerden herhangi birine karşı aşırı duyarlılığı olduğu bilinen kişilerde kontrendikedir.4.4. Özel kullanım uyarıları ve önlemleriParadoksikal BronkospazmLevosalbutamol, diğer inhale beta-adrenerjik agonistler gibi yaşamı tehdit edebilecek paradoksikal bronkospazma neden olabilir. Eğer paradoksikal bronkospazm meydana gelirse levosalbutamol hemen bırakılmalıdır ve alternatif tedavi başlatılmalıdır. Paradoksikal bronkospazmın inhale formülasyonlar ile ilişkili olduğu, sıklıkla yeni bir kutunun ilk kullanımıyla meydana geldiği ayırt edilmelidir. Astımın kötüleşmesi Astım, birkaç saatlik periyottan sonra akut olarak veya birkaç gün veya daha uzun zaman sonra kronik olarak kötüleşebilir. Eğer hastalar her zamankinden daha fazla dozda levosalbutamole ihtiyaç duyuyorsa, bu astımın destabilizasyonunun göstergesi olabilir ve antiinflamatuvar tedavi (örneğin kortikosteroidler) için olası ihtiyacın özel olarak göz önünde bulundurulması ile hasta ve tedavi rejiminin yeniden değerlendirilmesini gerektirir. Antiinflamatuvar ilaçların kullanımı Bir beta-adrenerjik agonistin tek başına kullanılması çoğu hastada astımın kontrolünde yeterli olmayabilir. Tedavi rejimine antiinflamatuvar ilaçların (örn. kortikosteroidler) eklenmesi düşünülmelidir. Kardiyovasküler etkiler Levosalbutamol, bazı hastalarda diğer beta-adrenerjik agonistler gibi, kalp atışı, kan basıncı ve/veya semptomlar ile ölçülen, klinik olarak anlamlı kardiyovasküler etkilere neden olabilir. Bu gibi etkiler önerilen dozlarda levosalbutamol uygulanmasından sonra yaygın olmamasına rağmen, meydana geldiği takdirde, ilacın kullanılmasına devam edilmemesi gerekebilir. Ek olarak beta-agonistlerin T-dalgası düzleşmesi, QTc aralığının uzaması, ve ST segment depresyonu gibi elektrokardiyogram değişikliklerine neden olduğu bildirilmiştir. Bu bulguların klinik olarak önemi bilinmemektedir. Bu nedenle, levosalbutamol gibi tüm sempatomimetik aminler, kardiyovasküler rahatsızlığı, özellikle koroner yetmezliği, kardiyak ritim bozukluğu, konvülsif hastalığı, hipertansiyonu, hipertiroidizmi, diyabeti olan ve sempatomimetik aminlere genellikle duyarlılığı olan hastalarda dikkatli kullanılmalıdır. Sistolik ve diyastolik kan basınçlarında klinik olarak anlamlı değişimler belirli hastalarda görülmüştür ve herhangi bir beta-adrenerjik bronkodilatörün kullanımından sonra bazı hastalarda meydana gelmesi olasıdır. Önerilen dozun aşımı Astımlı hastalarda inhale sempatomimetik ilaçların aşırı kullanımıyla ilişkili olarak ölümler bildirilmiştir. Ölümün asıl sebebi bilinmemektedir, fakat şiddetli akut astım krizlerinin beklenmeyen gelişimini takiben kardiyak arrest (kalp durması) ve sonrasında gelişen hipoksiden şüphelenilmektedir. Ani aşırı duyarlılık reaksiyonları Ürtiker, anjiyoödem, döküntü, bronkospazm, anafilaksi ve orofaringeal ödemin seyrek vakaları ile gösterildiği gibi, rasemik salbutamol uygulanmasından sonra ani aşırı duyarlılık reaksiyonları meydana gelebilir. Levosalbutamol alırken ani aşırı duyarlılık reaksiyonları gözlenen hastaların klinik değerlendirmesinde aşırı duyarlılık potansiyeli dikkate alınmalıdır Yüksek doz kullanımı Intravenöz rasemik salbutamolün yüksek dozlarının mevcut diyabeti ve ketoasidozu şiddetlendirdiği bildirilmiştir. Diğer beta adrenerjik agonist ilaç tedavileri ile olduğu gibi levosalbutamol bazı hastalarda, muhtemelen hücre içi yer değiştirme ile advers kardiyovasküler etkiler oluşturma potansiyeli olan hipokalemiye neden olabilir. Azalma genellikle geçicidir, potasyum ilavesi gerektirmez. Laktoz uyarısı INHAWELL yardımcı madde olarak laktoz içermektedir. Nadir kalıtımsal galaktoz intoleransı, Lapp laktoz yetmezliği ya da glukoz-galaktaz malabsorpsiyon problemi olan hastaların bu ilacı kullanmamaları gerekir. 4.5. Diğer tıbbi ürünler ile etkileşimler ve diğer etkileşim şekilleriKısa süreli etki gösteren diğer sempatomimetik aerosol bronkodilatörler veya epinefrin, INHAWELL ile birlikte dikkatli kullanılmalıdır. Eğer ek adrenerjik ilaçlar herhangi bir yolla uygulanacaksa, istenmeyen kardiyovasküler etkilerden kaçınmak için dikkatli olunmalıdır.Beta-Blokör ilaçlar Beta-adrenerjik reseptör bloke edici ilaçlar levosalbutamol gibi beta adrenerjik ilaçların pulmoner etkilerini engellemekle kalmaz, aynı zamanda astımlı hastalarda şiddetli bronkospazm üretebilir. Bu yüzden, astımlı hastalar normal olarak beta-blokörlerle tedavi edilmemelidir. Bununla birlikte miyokart enfarktüsünden sonra profilaksi gibi bazı şartlar altında, astımlı hastalarda beta-adrenerjik bloke edici ilaçların kullanımına kabul edilebilir seçenekler olmayabilir. Bu durumda, dikkatli kullanılmaları gerekmekle birlikte, kardiyoselektif beta-blokörler düşünülmelidir. Diüretikler Potasyum tutucu olmayan diüretiklerin (loop veya tiazid diüretikleri gibi) uygulanmasından sonra oluşan EKG değişiklikleri ve/veya hipokalemi özellikle beta-agonistlerin önerilen dozları aşıldığında akut olarak kötüleşebilir. Bu etkilerin klinik önemi bilinmemesine rağmen, potasyum tutucu olmayan diüretikler ile beta agonistlerin birlikte kullanımında dikkatli olunması tavsiye edilir. Digoksin 10 gün boyunca digoksin almış normal gönüllü bireylere sırasıyla tek doz intravenöz ve oral rasemik salbutamol uygulamasından sonra serum digoksin seviyelerinde ortalama %16-22 oranında düşüşler meydana gelmiştir. Levosalbutamol ve digoksin alan obstrüktif solunum yolu hastalığına sahip hastalar için bu bulguların klinik önemi kronik temelde belirsizdir. Yine de digoksin ve levosalbutamol almakta olan hastalarda serum digoksin seviyeleri değerlendirilirken dikkatli olunmalıdır. Monoamin Oksidaz İnhibitörleri veya Trisiklik Antideprasanlar Monoamin oksidaz inhibitörleri veya trisiklik antidepresanlar ile tedavi edilen hastalarda veya bu tür ilaçların bırakılmasının ardından 2 hafta içerisinde INHAWELL kullanımında son derece dikkatli olunmalıdır, çünkü levosalbutamolün vasküler sistem üzerindeki etkileri güçlenebilir. Özel popülasyonlara ilişkin ek bilgilerÖzel popülasyonlara ilişkin herhangi bir etkileşim çalışması tespit edilmemiştir.Pediyatrik popülasyon:Pediyatrik popülasyona ilişkin herhangi bir etkileşim çalışması tespit edilmemiştir.4.6. Gebelik ve laktasyon Genel tavsiyeGebelik kategorisi C dir.Çocuk doğurma potansiyeli bulunan kadınlar/Doğum kontrolü (kontrasepsiyon)INHAWELL gerekli olmadıkça gebelik döneminde kullanılmamalıdır.Çocuk doğurma potansiyeli bulunan kadınların etkin doğum kontrol (kontrasepsiyon) yöntemleri uygulaması önerilmektedir. Gebelik dönemiHayvanlar üzerinde yapılan çalışmalar, gebelik ve/veya embriyonal/fetal gelişim ve/veya doğum ve/veya doğum sonrası gelişim üzerindeki etkiler bakımından yetersizdir. Insanlara yönelik potansiyel risk bilinmemektedir.Hastaya yönelik potansiyel yarar, fetüse yönelik potansiyel riskten fazla olmadıkça, gebe kadınlarda INHAWELL kullanılmamalıdır. Laktasyon dönemiINHAWELL'in anne sütüne geçişi hakkında bilgi mevcut değildir. Emzirmenin durdurulup durdurulmayacağına ya da INHAWELL tedavisinin durdurulup durdurulmayacağına ilişkin karar verilirken emzirmenin çocuk açısından faydası ve INHAWELL tedavisinin emziren anne açısından faydası dikkate alınmalıdır.Üreme yeteneği/FertiliteSıçanlarda rasemik salbutamol sülfat ile gerçekleştirilen üreme çalışmalarında 50 mg/kg/gün dozlarına kadar olan oral rasemik salbutamol sülfat dozlarının fertilitenin bozulmasına neden olmadığı gösterilmiştir.4.7. Araç ve makine kullanımı üzerindeki etkilerINHAWELL'in araç ve makine kullanımı üzerine etkisi bildirilmemiştir.4.8. İstenmeyen etkilerYetişkinlerde ve adölesanlardaAstımlı yetişkinlerde ve adölesanlarda (n=748) levosalbutamol tartarat inhalasyon aerosolü ile ilgili istenmeyen etki bilgisi, gerçekleştirilen 8 haftalık, çok merkezli, randomize, çift-kör, aktif ve plasebo kontrollü 2 çalışmadan elde edilmiştir. Çalışmada 90 mcg levosalbutamol tartarat inhalasyon aerosolü (HFA) ile 180 mcg rasemik salbutamol HFA-inhaleri ve HFA-134a plasebo inhaleri karşılaştırılmıştır. HFA-134a plasebo inhalerinden daha sık gözlenen ve levosalbutamol tartarat inhalasyon aerosolü ile tedavi edilen grupta en az %2 oranında görülen istenmeyen etkiler ağrı, baş dönmesi, astım, faranjit ve rinit olmuştur. Levosalbutamol tartarat kullanımına bağlı yan etkiler, görülme sıklığına göre aşağıda belirtilmektedir: Çok yaygın (>1/10), yaygın (>1/100 ila <1/10), yaygın olmayan (>1/1000 ila <1/100), seyrek (>1/10.000 ila <1/1000), çok seyrek (<1/10.000), bilinmiyor (eldeki verilerden hareketle tahmin edilemiyor). Genel bozukluklar ve uygulama bölgesine ilişkin hastalıklarıYaygın: AğrıSinir sistemi hastalıklarıYaygın: Baş dönmesiSolunum, göğüs bozuklukları ve mediastinal hastalıklarıYaygın: Astım, faranjit, rinitLevosalbutamol tartarat inhalasyon aerosolü alan yetişkin ve ergen hastaların en az 2'si tarafından bildirilen ve insidansı %2'den az olan, HFA-134a plasebo inhaleri alanlardan daha fazla oranda gözlenen yan etkiler kist, grip sendromu, viral enfeksiyon, konstipasyon, gastroenterit, miyalji, hipertansiyon, epistaksis, akciğer rahatsızlığı, akne, uçuk, konjunktivit, kulak ağrısı, dismenore, hematüri ve vajinal moniliyasis'dir. Bu çalışmalarda anlamlı ölçüde laboratuar anormallikleri gözlemlenmemiştir. Çocuklarda Çocuklarda (4-11 yaş arası astımlı 150 çocuk) levosalbutamol tartarat inhalasyon aerosolü ile ilgili istenmeyen etki bilgisi, gerçekleştirilen 4 haftalık, randomize çift-kör çalışmadan elde edilmiştir. Çalışmada 90 mcg levosalbutamol tartarat inhalasyon aerosolü (HFA), 180 mcg rasemik salbutamol HFA-inhaleri ve HFA-134a plasebo inhaleri uygulanmıştır. HFA-134a plasebo inhalerinden daha sık gözlenen ve levosalbutamol tartarat inhalasyon aerosolü ile tedavi edilen grupta en az %2 oranında görülen istenmeyen etkiler kazayla yaralanma, kusma, bronşit ve faranjit olmuştur. Levosalbutamol tartarat kullanımına bağlı yan etkiler, görülme sıklığına göre aşağıda belirtilmektedir: Çok yaygın (>1/10), yaygın (>1/100 ila <1/10), yaygın olmayan (>1/1000 ila <1/100), seyrek (>1/10.000 ila <1/1000), çok seyrek (<1/10.000), bilinmiyor (eldeki verilerden hareketle tahmin edilemiyor). Genel bozukluklar ve uygulama bölgesine ilişkin hastalıklarıYaygın: Kazara yaralanmaSindirim sistemi hastalıklarıÇok yaygın: KusmaSolunum, göğüs bozuklukları ve mediastinal hastalıklarıYaygın: Bronşit, faranjitSistemik beta-adrenerjik istenmeyen etkilerin (örneğin titreme, sinirlilik) insidansı düşük ve plasebo dahil tüm tedavi gruplarından karşılaştırılabilir olmuştur. Pazarlama sonrası deneyimlerKlinik çalışmalardan elde edilen yan etkilere ek olarak, aşağıdaki yan etkiler pazarlama sonrası gözlenmiştir. Bu olaylar ciddiyetlerine, bildirilme sıklıklarına ya da beta-aracılı mekanizmalarına göre seçilmiştir: anjiyoödem, anafilaksi, aritmiler (atriyal fibrilasyon, supraventriküler taşikardi, ekstrasistoller dahil), astım, göğüs ağrısı, artan öksürük, nefes darlığı, bulantı, sinirlilik, döküntü, taşikardi, titreme, ürtiker. Bu olayların sıklık tahminleri bildirilmemiştir çünkü olaylar bilinmeyen büyüklükteki bir popülasyondan spontan olarak bildirilmiştir. Levosalbutamol diğer sempatomimetik ilaçlar gibi hipertansiyona, anjinaya, vertigoya, santral sinir sistemi uyarılmasına, uykusuzluğa, baş ağrısına ve orofarinksin kurumasına ya da irritasyonuna sebep olabilir. 4.9. Doz aşımı ve tedavisiBeta-adrenerjik reseptörlerin aşırı dozda kullanılmasına yönelik beklenen semptomlar aşırı beta-adrenerjik reseptör uyarılması ve/veya advers reaksiyon altında yer alan semptomların herhangi birinin meydana gelmesi veya alevlenmesidir: örneğin, nöbetler, anjina,hipertansiyon veya hipotansiyon, dakikada 200 kalp atışı ile taşikardi, düzensiz kalp atışı, sinirlilik hali, baş ağrısı, titreme, ağız kuruluğu, kalp çarpıntısı, mide bulantısı, baş dönmesi, halsizlik, kırgınlık ve uykusuzluk. Aynı zamanda hipokalemi de meydana gelebilir. Diğer tüm sempatomimetik ilaçlarda olduğu gibi, aşırı levosalbutamolün kullanımı kalp durmasına ve ölüme neden olabilir. Tedavi uygun semptomatik tedavi ile birlikte levosalbutamolün bırakılmasını gerektirebilir. Kardiyoselektif beta-reseptör blokörlerin uygun kullanımı düşünülebilir, fakat bu tür bir ilacın bronkospazm yaratma ihtimali göz önünde bulundurulmalıdır. Diyalizin, levosalbutamolün doz aşımı tedavisinde yararlı olup olmayacağına dair yeterli kanıt yoktur. 5. FARMAKOLOJİK ÖZELLİKLER5.1. Farmakodinamik özelliklerFarmakoterapötik grubu: Selektif Beta-2-Adrenoreseptör Agonistleri ATC kodu: R03ACLevosalbutamol, adenozin trifosfatın (ATP) siklik-3', 5'adenozin monofosfata dönüşümünü katalizleyen bir enzim olan hücre içi adenil siklazda artışa yol açıcı etkisi olan oldukça seçici bir beta2 adrenerjik-agonisttir. Solunum yolu düz kasları üzerindeki beta2 adrenerjik-reseptörlerin aktivasyonu adenilat siklazın aktivasy onuna ve cAMP'nin hücre içi konsantrasyonunda artışa yol açar. cAMP'deki artış, protein kinaz A aktivasyonu ile ilişkilidir. Protein kinaz A miyozin fosforilasyonunu inhibe eder ve hücre içi iyonik kalsiyum konsantrasyonlarını düşürür, bu da kas rahatlamasıyla sonuçlanır. Levosalbutamol trakeden terminal bronşiyollere kadar tüm solunum yolu düz kaslarını rahatlatır. Artan cAMP konsantrasyonları ayrıca solunum yollarında mast hücrelerinden mediyatörlerin salınımının engellenmesiyle de ilişkilidir. Levosalbutamol solunum yolunu rahatlatmak için bronkokonstriksiyonda rol oynayan spazmojenden bağımsız olarak fonksiyonel antagonist olarak etki gösterir, böylece tüm bronş ve bronşiyolleri bronkokonstriktör sorunlara karşı koruyucu olur. Beta2 adrenerjik reseptörler bronşiyal düz kaslar üzerinde en etkili reseptörler olarak tanımlanmakla birlikte, veriler insan kalbinde %10-50'si beta2 adrenerjik reseptörler olan beta-reseptörlerin olduğunu göstermektedir. Ancak bu reseptörlerin kesin fonksiyonu kanıtlanmamıştır. Bununla birlikte, tüm beta adrenerjik agonist ilaçlar bazı hastalarda nabız atışı, kan basıncı, semptomlar ve/veya elektrokardiyografik değişimler ile ölçülen önemli kardiyovasküler etkiye sebep olabilirler. Levosalbutamol tartarat HFA inhalasyon aerosolün etkinliği ve güvenirliği yaşları 12-81 arasında değişen 748 yetişkin ve adölesan astım hastasında 8 haftalık, çok merkezli, randomize, çift-kör, aktif ve plasebo kontrollü 2 çalışmada değerlendirilmiştir. 2 çalışmada levosalbutamol tartarat HFA inhalasyon aerosolü (403 hasta), HFA-134a plasebo inhaleri (166 hasta) ile karşılaştırılmıştır ve çalışmalarda pazarlanan 180 mcg rasemik salbutamol HFA-134a inhaleri (179 hasta) aktif kontrol olarak yer almıştır. Seri halde ölçülen 1 saniyedeki zorlu ekspiratuvar hacim (FEV1) ölçümleri, 90 mcg levosalbutamol tartarat inhalasyon aerosolünün (iki inhalasyon) plaseboya göre FEV1'de anlamlı oranda daha fazla iyileşme sağladığını göstermiştir. İkinci çalışmadan elde edilen sonuçlar birinci çalışmanın sonuçları ile benzer olmuştur. Levosalbutamol tartarat HFA inhalasyon aerosolünün etkinliği ve güvenirliği yaşları 4-11 arasında değişen 150 pediyatrik astım hastasında 4 haftalık, çok merkezli, randomize, çift-kör, aktif ve plasebo kontrollü bir çalışmada değerlendirilmiştir. Çalışmada 90 mcg levosalbutamol tartarat inhalasyon aerosolü (45 mcgx2) (76 hasta), HFA-134a plasebo inhaleri (35 hasta) ile karşılaştırılmıştır ve çalışmalarda pazarlanan rasemik salbutamol HFA-134a inhaleri (39 hasta) aktif kontrol olarak yer almıştır. Seri halde ölçülen 1 saniyedeki zorlu ekspiratuvar hacim (FEV1) ölçümleri, 90 mcg levosalbutamol tartarat inhalasyon aerosolünün plaseboya göre FEV1'de anlamlı oranda daha fazla iyileşme sağladığını göstermiştir. Bu çalışmadan elde edilen sonuçlar yetişkinlerle gerçekleştirilen etkinlik bulgularıyla tutarlı olmuştur. 5.2. Farmakokinetik özellikler Genel özelliklerEmilim:Üç büyük çalışmadan 4-81 yaşları arasındaki 632 astım hastasının (R)-salbutamol plazma konsantrasyonları kullanılarak bir popülasyon farmakokinetiği modeli geliştirilmiştir. 90 mcg levosalbutamol tartarat inhalasyon aerosolü veya ölçülü doz inhaleri ile 180 mcg rasemik salbutamol alan adölesan/yetişkin ve pediyatrik hastalarda (R)-salbutamol için popülasyon farmakokinetiği modelinden elde edilmiş farmakokinetik parametreler Tablo 1'de verilmiştir. Bu farmakokinetik parametreler, verilen rasemik salbutamolün karşılaştırılabilir dozu ile karşılaştırıldığında (R)-salbutamole maruziyetin levosalbutamol tartarat inhalasyon aerosolü uygulanan pediyatrik hastalarda %30-%32 ve yetişkinlerde %13-16 oranında daha düşük olduğunu göstermektedir. Yetişkin hastalarla karşılaştırıldığında, 90 mcg levosalbutamol verilen pediyatrik hastalarda (R)-salbutamol maruziyeti %17 oranında daha düşük olmuştur. Tablo 1.Ortalama Model-Hesaplı (R)-Salbutamol Farmakokinetik ParametreleriTedavi
Ölçülü doz inhaleri ile rasemik salbutamol
Çalışma popülasyonu
Levosalbutamol inhalasyon aerosolü
Parametre
Cmaks (ng/mL)
0.199
0.238
Tmaks (sa)
0.54
0.53
EAA (0-6) (ng-sa/mL)
0.695
0.798
Adölesan/Yetişkin Hastalar (>12 yaş)
Cmaks (ng/mL)
0.163
0.238
Pediyatrik hastalar (4-11 yaş)
Tmaks (sa)
0.76
0.78
EAA (0-6) (ng-sa/mL)
0.579
0.828 Dağılım:Veri mevcut değildir. Biyotransformasyon:Yayınlanan literatürlerdeki mevcut bilgiler, insanlarda salbutamol enantiyomerlerinin metabolizmasından sorumlu primer enzimin SULT1A3 (sülfotransferaz) olduğunu ileri sürmektedir. Rasemik salbutamol oral organik kömür uygulamasından sonra inhalasyon yoluyla veya intravenöz olarak uygulandığında (R)- ve (S)-salbutamol enantiyomerlerinin konsantrasyon zaman eğrileri altındaki alan arasında 3-4 katlık bir fark meydana gelmiştir, (S)-salbutamol konsantrasyonları devamlı olarak daha yüksek olmuştur. Bununla birlikte, organik kömür ön tedavisi olmadan, ya oral ya da inhalasyon uygulaması sonrasında farklılıklar 8-24 kat olmuştur. Bu durum (R)-salbutamolün muhtemelen SULTT1A3 tarafından gastrointestinal yoldan metabolize olduğunu ileri sürmektedir. Eliminasyon:Salbutamol enantiyomerlerinin eliminasyonunun primer yolu böbrekler aracılığıyla (%80-100) ya ana bileşik ya da primer metabolit olarak olmaktadır. ilacın %20'sinden daha azı dışkıda saptanabilmektedir. Rasemik salbutamolün intravenöz uygulamasını takiben (R)-salbutamol fraksiyon dozunun %25'i ve %46'sı değişmemiş (R)-salbutamol olarak idrarla atılmıştır. Doğrusallık/doğrusal olmayan durum:Levosalbutamol, 0.31-0.63 mg nebulize doz aralığında doğrusal bir farmakokinetik sergilemiştir. Hastalardaki karekteristik özelliklerKaraciğer yetmezliği:Karaciğer yetmezliğinin levosalbutamolün farmakokinetiği üzerindeki etkisi değerlendirilmemiştir. Böbrek yetmezliği:Böbrek yetmezliğinin rasemik salbutamolün farmakokinetiği üzerindeki etkisi kreatinin klerensi 7-53 mL/dak olan 5 kişide değerlendirilmiştir ve sonuçlar, sağlıklı gönüllü bireylerden elde edilen sonuçlarla karşılaştırılmıştır. Böbrek hastalığının yarı-ömür üzerinde etkisi olmamakla birlikte, rasemik salbutamol klerensinde %67 oranında bir düşüş meydana gelmiştir. Böbrek yetmezliği olan hastalara salbutamolün yüksek dozları uygulanırken tedbirli olunmalıdır. 5.3. Klinik öncesi güvenlilik verileriSprague-Dawley sıçanlarıyla gerçekleştirilen 2 yıllık çalışmada >2 mg/kg/gün diyetsel dozlarda rasemik salbutamol sülfat, mezovaryum benign düz kas tümörlerinin insidansında doza bağlı olarak anlamlı ölçüde artışa neden olmuştur (mg/m2 temelinde yetişkinler için önerilen günlük maksimum levosalbutamol tartarat inhalasyon dozunun yaklaşık 30 katı ve mg/m2 temelinde çocuklar için önerilen günlük maksimum levosalbutamol tartarat inhalasyon dozunun yaklaşık 15 katı). Başka bir çalışmada bu etkinin selektif olmayan beta adrenerjik antagonist olan propranolol ile birlikte uygulanması ile engellendiği gösterilmiştir. CD-1 farelerinde gerçekleştirilen 18 aylık bir çalışmada 500 mg/kg/gün diyetsel dozlarına kadar olan rasemik salbutamol sülfat dozları tümör oluşumuna neden olmamıştır (mg/m2 temelinde yetişkinler için önerilen günlük maksimum levosalbutamol tartarat inhalasyon dozununyaklaşık 3800 katı ve mg/m2 temelinde çocuklar için önerilen günlük maksimum levosalbutamol tartarat inhalasyon dozunun yaklaşık 1800 katı). Golden hamsteriyle gerçekleştirilen 22 aylık bir çalışmada 50 mg/kg/gün diyetsel dozlarına kadar olan rasemik salbutamol sülfat dozları tümör oluşumuna neden olmamıştır (mg/m2 temelinde yetişkinler için önerilen günlük maksimum levosalbutamol tartarat inhalasyon dozunun yaklaşık 500 katı ve mg/m2 temelinde çocuklar için önerilen günlük maksimum levosalbutamol tartarat inhalasyon dozunun yaklaşık 240 katı). Levosalbutamol HCl'nin Ames testinde veya CHO/HPRT Memeli Ileri Gen Mutasyon Testi'nde mutajenik olmadığı gösterilmiştir. Levosalbutamol HCl, fare kemik iliğinde in vivo mikronükleus testinde klastojenik olmamıştır. Rasemik salbutamol sülfat, CHO hücre kültürlerinde in vitro kromozomal aberasyon testinde negatif bulunmuştur. Sıçanlarda rasemik salbutamol sülfatla gerçekleştirilen üreme çalışmalarında 50 mg/kg/gün dozlarına kadar olan oral rasemik salbutamol sülfat dozlarının fertilitenin bozulmasına neden olmadığı gösterilmiştir (mg/m2 temelinde yetişkinler için önerilen günlük maksimum levosalbutamol tartarat inhalasyon dozunun yaklaşık 750 katı). Rasemik salbutamol sülfatın farelerde ve tavşanlarda teratojenik olduğu gösterilmiştir. Deri altı yoluyla rasemik salbutamol sülfat verilen CD-1 fareleriyle yapılmış bir çalışmada 0.25 mg/kg/gün dozda 111 fetüsün 5'inde (%4,5) (mg/m2 temelinde yetişkinler için önerilen günlük maksimum levosalbutamol tartarat inhalasyon dozunun yaklaşık 2 katı) 2.5 mg/kg/gün dozda 108 fetusun 10'unda (%9,3) yarık damak oluşumu gösterilmiştir (mg/m2 temelinde yetişkinler için önerilen günlük maksimum levosalbutamol tartarat inhalasyon dozunun yaklaşık 20 katı). ilaç deri altı yoluyla 0.025 mg/kg/gün dozda uygulandığı zaman yarık damak oluşumunu indüklememiştir (mg/m2 temelinde yetişkinler için önerilen günlük maksimum levosalbutamol tartarat inhalasyon dozundan daha düşük). Yarık damak oluşumu 2.5 mg/kg/gün dozda isoproterenol (pozitif kontrol) ile deri altı yoluyla tedavi edilen 72 fetüsün 22'sinde (%30,5) de meydana gelmiştir. Stride Dutch tavşanlarıyla yürütülen bir üreme çalışmasında 50 mg/kg/gün oral rasemik salbutamol sülfat dozu ile tedavi sonrasında 19 tavşanın 7'sinin (%37) kafatasında konjenital çatlaklık gözlenmiştir (mg/m2 temelinde yetişkinler için önerilen günlük maksimum levosalbutamol tartarat inhalasyon dozunun yaklaşık 1500 katı). Radyoaktif olarak işaretlenmiş rasemik salbutamol sülfat uygulanan hamile sıçanlarda ilaç ile ilişkili maddenin maternal sirkülasyondan fetüse transfer edildiği gösterilmiştir. Rasemik salbutamolün pazarlanma süreci boyunca rasemik salbutamol ile tedavi gören hastaların çocuklarında nadir olarak yarık damak ve uzuv kusurları dahil çeşitli konjenital anomaliler bildirilmiştir. Annelerden bazıları hamilelikleri boyunca çoklu ilaç tedavisi alıyordu. Rasemik salbutamol kullanımı ve konjenital anomaliler arasında ilişki kanıtlanmamıştır. 6. FARMASÖTIK ÖZELLIKLER6.1. Yardımcı maddelerin listesiLaktoz6.2. GeçimsizliklerBilinen geçimsizliği yoktur.6.3. Raf ömrü24 ay6.4. Saklamaya yönelik özel tedbirler25°C'nin altındaki oda sıcaklığında ve kuru yerde saklayınız.6.5. Ambalajın niteliği ve içeriğiİNHAWELL 100 mcg inhalasyon için toz içeren , 60 veya 120 kapsül içeren PVC/PVDC/Alü blister ambalajlarda, inhalasyon cihazı ve kullanma talimatı ile birlikte karton kutuda sunulmaktadır.6.6 Beşeri tıbbi üründen arta kalan maddelerin imhası ve diğer özel önlemlerKullanılmamış olan ürünler ya da atık materyaller Tıbbi Atıkların Kontrolü Yönetmeliği ve Ambalaj ve Ambalaj Atıklarının Kontrolü Yönetmeliklerine uygun olarak imha edilmelidir.7. RUHSAT SAHİBİMentis İlaç San. Tic. Ltd. ŞtiAdresi: Florya Asfaltı Florya İş Merkezi B Blok No:88/6 Bakırköy/İSTANBUL Telefon: 0 212 481 79 52 Faks: 0 212 481 79 52 e-mail: [email protected] 8. RUHSAT NUMARASI (LARI)243/689. İLK RUHSAT TARİHİ/RUHSAT YENİLEME TARİHİİlk ruhsat tarihi: 12.07.2012 Ruhsat yenileme tarihi:10. KÜB'ÜN YENİLENME TARİHİ |
İlaç Bilgileriİnhawell 100 mcg İnhalasyon İçin Toz İçeren KapsülEtken Maddesi: Levosalbutamol sülfat Atc Kodu: R03AC Kullanma talimatı ve kısa ürün bilgileri
Google Reklamları
İlgili İlaçlar |
Ana Sayfa | Hakkımızda | İlaçlar | İlaç Ara | İlaç Firmaları | Gizlilik | Bize Ulaşın
Telif Hakkı 2008-2026 © İlaç Prospektüsü. Tüm Hakları Saklıdır.Uyarı: Sitemizde yayınladığımız ilaç bilgileri ile doktora danışmadan kesinlikle ilaç kullanmayınız!
Aksi halde doğabilecek sağlık sorunlarından ilacprospektusu.com sorumlu tutulamaz.
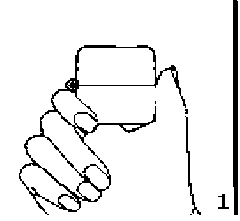
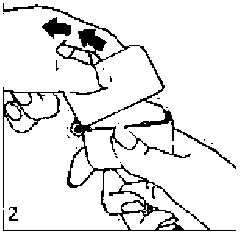
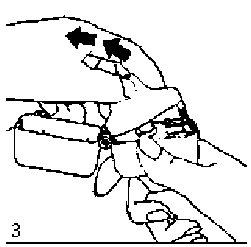 1., 2. ve 3. Toz başlığını yukarı doğru çekerek açınız. Daha sonra ağızlık parçasını açınız.
1., 2. ve 3. Toz başlığını yukarı doğru çekerek açınız. Daha sonra ağızlık parçasını açınız.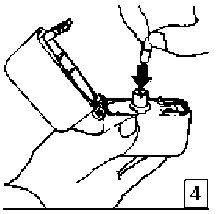 4. Blister ambalajından bir INHAWELL inhalasyon için toz içeren kapsülü çıkarınız (kullanımdan hemen önce çıkarınız) ve şekilde gösterildiği gibi merkezi hazneye yerleştiriniz. Kapsülün hazneye hangi yönde yerleştirildiği önemli değildir.
4. Blister ambalajından bir INHAWELL inhalasyon için toz içeren kapsülü çıkarınız (kullanımdan hemen önce çıkarınız) ve şekilde gösterildiği gibi merkezi hazneye yerleştiriniz. Kapsülün hazneye hangi yönde yerleştirildiği önemli değildir.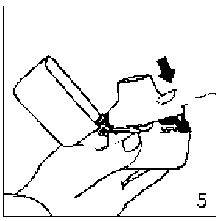 5. Ağızlık parçasını bir klik sesi duyuncaya değin
5. Ağızlık parçasını bir klik sesi duyuncaya değin 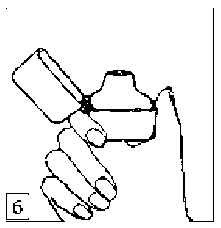 6. ve 7. İnhalasyon cihazını ağızlık parçası yukarıda olacak şekilde tutunuz ve kapağı bastırarak kapatınız.
6. ve 7. İnhalasyon cihazını ağızlık parçası yukarıda olacak şekilde tutunuz ve kapağı bastırarak kapatınız.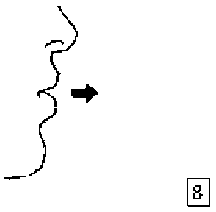 8. Nefesinizi tam olarak veriniz.
8. Nefesinizi tam olarak veriniz.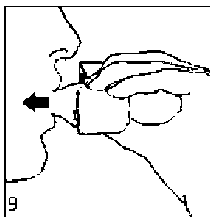 9. Inhalasyon cihazının ağzını açıp, cihazı ağzınıza kadar kaldırınız ve dudaklarınızı ağızlık parçasının çevresinde sıkıca kapayınız. Başınızı dik bir şekilde tutarak, yavaş ve derin bir nefes alınız; nefes alma hızınızı, kapsülün titreştiğini algılayacak şekilde ayarlayınız. Akciğerleriniz doluncaya kadar nefes alınız; nefesinizi sizi zorlamayacak bir süreyle tutunuz ve bu esnada inhalasyon cihazını ağzınızdan çıkarınız. Şimdi normal nefes alıp vermeye başlayabilirsiniz.
9. Inhalasyon cihazının ağzını açıp, cihazı ağzınıza kadar kaldırınız ve dudaklarınızı ağızlık parçasının çevresinde sıkıca kapayınız. Başınızı dik bir şekilde tutarak, yavaş ve derin bir nefes alınız; nefes alma hızınızı, kapsülün titreştiğini algılayacak şekilde ayarlayınız. Akciğerleriniz doluncaya kadar nefes alınız; nefesinizi sizi zorlamayacak bir süreyle tutunuz ve bu esnada inhalasyon cihazını ağzınızdan çıkarınız. Şimdi normal nefes alıp vermeye başlayabilirsiniz.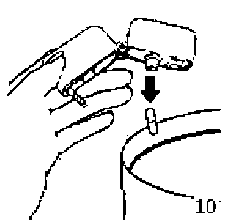 10. Ağızlık parçasını yeniden açınız. Cihazı çevirerek kullanılmış kapsülü çıkarınız ve atınız. Ağızlık parçasını ve toz başlığını kapatınız ve inhalasyon cihazınızı yerine kaldırınız.
10. Ağızlık parçasını yeniden açınız. Cihazı çevirerek kullanılmış kapsülü çıkarınız ve atınız. Ağızlık parçasını ve toz başlığını kapatınız ve inhalasyon cihazınızı yerine kaldırınız.