Nimbex 5mg/2.5ml Enjektabl Ampul Kısa Ürün BilgisiKas İskelet Sistemi » Kas Gevşeticiler » Periferik Etkili Kas Gevşeticiler » Diğer Kuaterner Amonyumlar » Sisatrakuryum KISA URUN BILGISI1. BEŞERİ TIBBİ ÜRÜNÜN ADINİMBEX 5 mg /2.5 mİ enjektabl ampul2. KALİTATİF VE KANTİTATİF BİLEŞİM Etkin madde:Bir 2.5 ml'lik ampulde;5 mg sisatrakuryuma eşdeğer sisatrakuryum besilat (2 mg/ml) Yardımcı maddeler:Yardımcı maddeler için 6.1,'e bakmız.3. FARMASÖTİK FORMAmpulSteril solüsyon, pH=3.3-3.8 4. KLİNİK ÖZELLİKLER4.1.Terapdtik endikasyonlar
NİMBEX, intravenöz olarak uygulanan orta etki süreli, non-depolarizan nöromüsküler blokördür. NİMBEX'in cerrahi, diğer uygulamalar sırasında ve yoğun bakımda kullammı endikedir. NİMBEX'in kardiyak cerrahiyi de içine alan cerrahi girişimlerde kullanımı endikedir. Genel anesteziye ek olarak veya yoğun bakım ünitelerinde sedasyon için, iskelet kaslannı gevşetmek ve trakeal entübasyonu ve mekanik ventilasyonu kolaylaştırmakta kullanılır. NİMBEX antimikrobiyal koruyucu taşımaz ve tek bir hasta kullanımı içindir.İntravenöz bolus enjektabl şeklinde kullanımıErişkinler;Trakeal entübasyon; NİMBEX'in erişkinler için önerilen entübasyon dozu 5-10 saniyede hızlı olarak 0.15 mg/kg'dır. Bu doz, enjeksiyonu takiben 120 saniye içinde trakeal entübasyon için iyi veya mükemmel koşullar oluşturur. Yüksek dozlar nöromüsküler blokun oluşma süresini kısaltır. Aşağıdaki tablo NİMBEX'in sağlıklı erişkinlere opioid veya propofol anestezisi sırasında 0.1-0.4 mg/kg dozlarında uygulandığında ortalama farmakodinamik verilerini özetlemektedir. |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
Başlangıç |
Uygulanan |
%90Tla |
Maks. Tl a |
%25 spontan |
|
NİMBEX |
anestetik |
supresyona |
supresyona |
Tla |
|
dozu |
|
ulaşma süresi |
ulaşma |
düzelme süresi |
|
(mg/kg) |
|
(dak.) |
süresi (dak.) |
(dak.) |
|
0.1 |
Opioid |
3.4 |
4.8 |
45 |
|
0.15 |
Propofol |
2.6 |
3.5 |
55 |
|
0.2 |
Opioid |
2.4 |
2.9 |
65 |
|
0.4 |
Opioid |
1.5 |
1.9 |
91 |
Enfluran veya izofluran anestezisi, NİMBEX'in başlangıç dozunun klinik etki süresini %15 kadar uzatabilir.
İdame;
Nöromüsküler blok, NİMBEX'in idame dozları ile uzatılabilir. 0.03mg/kg'lık doz opioid veya propofol anestezisi sırasında yaklaşık olarak 20 dakika ilave klinik olarak etkili nöromüsküler blok sağlar. Birbirini takip eden İdame dozlar etkide ilerleyici bir uzama ile sonuçlanmaz.Kendiliğinden düzelme:hızı
uygulanmış olan NİMBEX dozundan bağımsızdır. Opioid veya propofol anestezisi sırasında %25'ten %75'e ve %5'ten %95'e medyan düzelme süreleri sırasıyla yaklaşık olarak 13 dakika ve 30 dakikadır.Etkinin geriye döndürülmesi;
NİMBEX uygulamasını takiben oluşan nöromüsküler blok antikolinesteraz ilaçlann standart dozlarıyla geriye döndürülür. Etkiyi tersine çeviren ilaç uygulamasını takiben (ör. %13 Tl düzelmesi) %25'ten %75'e ve %25'ten tam klinik düzelme (T4:T1> 0.7) için geçen ortalama süre sırasıyla yaklaşık olarak 2 dakika ve 5 dakikadır.İntravenöz infüzyon şeklinde kullanımı.
Erişkinler ve 2 -12 yaş arası çocuklar;
Nöromüsküler blokun devamlı olması NİMBEX'in infüzyon olarak uygulanması ile elde edilebilir. Erken spontan düzelme belirtisinden sonra %89-99 Tl supresyonunu yeniden sağlamak için başlangıç infüzyon hızı 3 mikrogram/kg/dak. (0.18mg/kg/saat) olarak önerilir. Nöromüsküler bloğun stabilizasyonu için geçen başlangıç periyodundan sonra 1-2 mikrogram/kg/dak.'lık (0.06-0.12 mg/kg/sa) hız bu gruptaki birçok hastada idame blok için yeterlidir. Isofluran veya enfluran anestezisi sırasında NİMBEX uygulandığında infüzyon hızının %40 kadar azaltılması gerekli olabilir. İnfüzyon hızı; infüzyon solüsyonundaki sisatrakuryum konsantrasyonuna, istenilen nöromüsküler bloğun derecesine ve hastamn kilosuna bağlıdır. Aşağıdaki tablo dilüe edilmemiş NİMBEX'in dağılımını göstermektedir.
NİMBEX 2 mg/ml'nin infüzyon dağılım hızı
|
Hastanın ağırlığı (kg) |
Doz (mikrogram/kg/dak) 1.0 1.5 2.0 3.0 |
İnfüzyon hızı | |||
|
20 |
0.6 |
0.9 |
1.2 |
1.8 |
ml/saat |
|
70 |
2.1 |
3.2 |
4.2 |
6.3 |
ml/saat |
|
100 |
3.0 |
4.5 |
6.0 |
9.0 |
ml/saat |
Uygulama şekli:
NİMBEX i.v. enjeksiyon yoluyla uygulanır.Dilüe edilmiş NİMBEX, 0.1 ila 2.0mg/ml konsantrasyonları arasında, aşağıdaki infüzyon sıvılarında, polivinil klorür (PVC) veya polipropilen kaplar içinde, 5° C ve
25°
C'de en az 12 saat fiziksel ve kimyasal olarak stabil kalır.Sodyum klorür (% 0.9 a/h) i.v. infiizyon Glukoz (% 5 a/h) i.v. infüzyon
Sodyum klorür (% 0.18 a/h) ve Glukoz (% 4 a/h) i.v. infuzyon Sodyum klorür (% 0.45 a/h) ve Glukoz (% 2.5 a/h) i.v. infüzyon
Ancak, NİMBEX hiçbir antimikrobiyal koruyucu içermediğinden dilüsyon kullanmadan hemen önce yapılmalı, mümkün olduğu kadar çabuk, hemen uygulama başlatılmalı ve artan solüsyon atılmahdır. NİMBEX Laktath Ringer enjeksiyonu ile seyre İtildiğinde kimyasal olarak stabil değildir. NİMBEX, Y-bölgesi enjeksiyon yerinden uygulanmakta olan intravenöz infüzyon içine verilmesine benzer şekilde karıştırıldığında, aşağıdaki ameliyat sırasında kullanılan ilaçlarla geçimli olduğu görülmüştür: alfentanil hidroklorür, droperidol, fentanil sitrat, midazolam hidroklorür ve sufentanil sitrat. NİMBEX'in uygulandığı iğne ya da kanülden uygulanacak olan diğer ilaçların sodyum klorür % 0.9'luk intavenöz infüzyon gibi uygun bir intravenöz sıvı içinde, yeterli hacimde uygulanması önerilir.
Özel popülasyonlara ilişkin ek bilgiler:
Böbrek yetmezliği:
Böbrek yetmezliği olan hastalarda herhangi bir doz değişikliği gerekmemektedir. Bu grup hastalarda NİMBEX normal böbrek fonksiyonu olan hastalarda gözlenene benzer farmakodinamİk profil gösterir, fakat etkinin başlangıcı biraz daha yavaş olabilir.Karaciğer yetmezliği:
İleri derecede karaciğer hastalığı olan hastalarda herhangi bir doz değişikliği gerekmemektedir. Bu grup hastalarda NİMBEX normal hepatik fonksiyonu olan hastalarda gözlenene benzer farmakodinamİk profil gösterir, fakat etkinin başlangıcı biraz daha hızlı olabilir.Pediyatrik popülasyon:
İntravenöz boius enjektabi şeklinde kuiiammı
1 ay-12 yaş arası çocuklar;Trakeal enlübasyon;
Erişkinlerde olduğu gibi NİMBEX önerilen başlangıç entübasyon dozu 5-10 saniyede hızlı şekilde 0.15 mg/kg'dır. Bu doz NİMBEX'i takiben 120 saniyede trakeal entübasyon için iyi ve mükemmel koşulları oluşturur. Bu doz için farmakodinamİk veriler aşağıdaki tabloda gösterilmiştir. Eğer kısa klinik süre istenirse, 0.1 mg/kg'hk dozun 120-150 saniyede benzer entübasyon koşulları sağladığını farmakodinamİk veriler göstermektedir. 1 ay- 12 yaş arasındaki pediyatrik hastalarda NİMBEX, benzer anestezik koşullarda, erişkinde gözlenenden daha kısa klinik etki süresi ve daha hızlı spontan düzelme profiline sahiptir.Farmakodinamik profilde 1 ay-11 ay ile 1 yaş-12 yaş arasındaki yaşlarda aşağıdaki tabloda özetlenmiş olan çok küçük değişiklikler gözlenmiştir.
1 ay -11 ay arasındaki çocuk hastalar;
Başlangıç NİMBEX dozu (mg/kg)
Uygulanan
anestetik
% 90 supresyon oluşturma süresi (dak.)
Maksimum
supresyon
oluşturma
süresi
(dak.)
% 25 spontan Tl düzelme süresi (dak.)
52
2.0
Halotan
1.4
0.15
2.0
Opioid
1.4
47
0.15
1 yaş - 12 yaş arasındaki çocuk hastalar
|
Başlangıç NİMBEX dozu (mg/kg) |
Uygulanan anestetik |
% 90 supresyon oluşturma süresi (dak.) |
Maksimum supresyon oluşturma süresi (dak.) |
% 25 spontan Tl düzelme süresi (dak.) |
|
0.08 |
Halotan |
1.7 |
2.5 |
31 |
|
0.1 |
Opioid |
1.7 |
2.8 |
28 |
|
0.15 |
Halotan |
2.3 |
3.0 |
43 |
|
0.15 |
Opioid |
2.6 |
3.6 |
38 |
İdame:Kendiliğinden düzelme;Bir kez nöromüsküler bloktan geri dönme (dfizelme) başlamışsa, düzelme hızı uygulanmış olan NİMBEX dozundan bağımsızdır.Opioid anestezisi
sırasında % 25'ten % 75'e ve % 5'ten % 95'e düzelme medyan süresi sırasıyla yaklaşık olarak 11 dak. ve 28 dakikadır.
Etkinin tersine çevrilmesi;
NİMBEX uygulamasını takiben oluşan nöromüsküler blok antikolinesteraz ilaçların standart dozlarıyla tersine çevrilir. Etkiyi tersine çeviren ilaç uygulamasını (ort. % 13 Tl düzelme) takiben % 25'ten % 75'e düzelme ve % 25'ten tam klinik olarak düzelme (T4: Tl >0.7) için geçen ortalama süre 2 dakika ve 5 dakikadır.
1 aylıktan büyük çocuklarda intravenöz infiizyon şeklinde kullanımı Pozoloji/uygulama sıklığı ve süresi başlığı altında verilmiştir.
Yeni doğanlar ve 1 ayın altındaki çocuklar:
NİMBEX bu hasta populasyonunda çalışılmadığı için yeni doğanlarda herhangi bir doz önerilmemektedir.
Geriyatrik popülasyon:
Yaşlı hastalarda herhangi bir doz değişikliği gerekmemektedir. Bu grup hastalarda NİMBEX genç erişkinlerde gözlenene benzer farmakodinamik profil gösterir, fakat diğer nöromüsküler blokör ilaçlarda olduğu gibi etkinin başlangıcı biraz daha yavaş olabilir.
Diğer:
Kardiyovasküler hastalığı olan hastalar:
Kardiyak cerrahisi uygulanan hastalarda norömusküler blok sağlamak İçin NİMBEX etkin olarak uygulanmıştır. Yapılan hiçbir çalışmada ciddi kardiyovasküler hastalığı olanlarda NİMBEX'in hızlı bolus (5-10 saniye) şeklinde kullanımı klinik
olarak anlamlı kardiyovasküler etkiler oluşumu ile ilişkili bulunmamıştır.
Yoğun bakım ünitesindeki hastalar:
NİMBEX yoğun bakım ünitesindeki erişkin hastalara bolus ve/veya infuzyon olarak uygulanabilir. Yoğun bakım ünitesindeki erişkin hastalar için önerilen NİMBEX başlangıç infüzyon hızı 3 mikrogram/kg/dak.'dır (0.18 mg/kg/sa). Doz gereksinimlerinde hastaİ£ir arasında geniş değişiklikler olabilir ve bu zamanla artar veya azalabilir. Klinik çalışmalarda ortalama infiizyon hızı 3 mikrogram/kg/dak.'dır [0.5-10.2 mikrogram/kg/dak aralığında (0.03-0.6 mg/kg/sa)]. Yoğun bakım ünitesindeki hastalarda uzun dönem (6 güne kadar) NİMBEX infüzyonu takiben tam spontan düzelme medyan süresi yaklaşık olarak 50 dakikadır.
5 mg/ml NİMBEX'in infüzyon dağılım oranı
|
Hasta ağırlığı |
Doz (mikrogram/kg/dak) 1.0 1.5 2.0 3.0 |
İnfüzyon hızı | |||
|
70 |
0.8 |
1.7 |
1.2 |
2.4 |
ml/saat |
|
100 |
1.2 |
2.5 |
1.8 |
3.6 |
ml/saat |
Hipotermik kalp cerrahisi uygulanan hastalar:
Cerrahi uygulanan hipotermi oluşturulmuş (25'^C-28"C) hastalara NİMBEX uygulamasını içeren çahşmalar bulunmamaktadır. Diğer nöromüsküler blokör ilaçlarda olduğu gibi bu koşullar altmda yeterli cerrahi rölaksasyonu idame ettirmek için gerekli olan infüzyon hızmm anlamlı derecede azaltılması beklenir.4.3. Kontrendikasyonlar
NİMBEX, sisatrakuryum, atrakuryum veya benzensülfonik aside aşırı duyarlılığı olduğu bilinen hastalarda kontrendikedir.4.4. Özel kullanıın uyarılan ve önlemleri
Sisatrakuryum diğer iskelet kaslarını olduğu gibi solunum kaslannı da felce uğratır, fakat bilinç veya ağrı eşiği üzerine bilinen bir etkisi yoktur. NİMBEX sadece deneyimli anestezist tarafından veya gözetiminde veya nöromüsküler blokör ilaçların kullanımım ve etkilerini bilen diğer klinİsyenler tarafından uygulaımıalıdır. Trakeal entübasyon için uygun koşullar ve pulmoner ventilasyonun ve yeterii arteryel oksijenasyonun idamesi sağlanmalıdır. NİMBEX, nöromüsküler blokör ilaçlar arasında çapraz reaksiyon rapor edildiğinden diğer nöromüsküler blokör ilaçlara alerjik aşın duyariilık gösteren kişilere uygulandığında dikkat gösterilmelidir. Sisatrakuryumun önemli bir vagolitik veya gangliyon bloke edici özellikleri yoktur. Bu nedenle, NİMBEX'in kalp atım hızı üzerine klinik olarak anlamlı etkisi yoktur ve birçok anestetik ilaç veya ameliyat sırasında vagal stimülasyon ile oluşan bradikardi üzerine etkisi yoktur. Myastenia gravisi ve nöromüsküler hastalıkların diğer formlarını taşıyan hastalar non-depolarizan blokör ilaçlara büyük oranda artmış bir duyarlılık gösterirler. Bu hastalara 0.02mg/kg'ı geçmeyen başlangıç dozunda NİMBEX Önerilir. Ciddi asid-baz ve/veya serum elektrolit anormallikleri hastanın nöromüsküler blokör ilaçlara karşı duyarlılığını arttırabilir veya azaltabilir. NİMBEX malign hipertermi hikayesi olan hastalarda denenmemiştir. Sisatrakuryum yanıklan olan hastalarda denenmemiştir, fakat diğer non-depolarizan nöromüsküler blokör ilaçlarla olduğu gibi, eğer NİMBEX bu hastalara uygulanacaksa doz gereksinmelerinin artmış ve etki süresinin kısalmış olabileceği dikkate alınmalıdır. NİMBEX bir hipotoniktir ve kan transfüzyonun infuzyon yolu içinde verilmelidir.Yoğun bakım hastalarında kullanımı:
Laboratuvar hayvanlarına yüksek dozda uygulandığında sisatrakuryum ve atrakuryumun bir metaboliti olan laudanosin geçici hipotansiyon ve bazı türlerde serebral eksitatör etkilerle ilişkili bulunmuştur. Sisatrakuryumun azalan infuzyon oranı ile tutarlı olarak pla2ana laudanosin konsantrasyonlan, atrakuryum infüzyonunu takip eden konsantrasyonun yaklaşık üçte biri kadardır. Atrakuryum ve diğer ajanları alan yoğun bakım hastalarında nadiren nöbetler rapor edilmiştir. Bu hastalarda genellikle bir veya daha fazla nöbete yol açabilecek tibbi koşullar mevcuttur (Kranyal travma, hipoksik ensefalopati, serebral ödem, viral ensefalopati, üremi gibi). Laudanosin ile ilişkili bir neden tesbit edilememiştir.4.5. Diğer tıbbi ürünler ile etkileşim ve diğer etkileşim şekilleri
Aşağıdakiler de dahil olmak üzere birçok ilacın non-depolarizan nöromüsküler blokör ilaçların şiddet ve/veya etki süresini etkilediği gösterilmiştir.Artırıcı etkiler
Anestetikler:
Enfluran, isofluran, desfIurane, sevofluran ve halotan gibi uçucu ilaçlar ve ketamin; diğer non-depolarizan nöromüsküler blokör ilaçlar.Diğer ilaçlar:
Aminoglikozidler, polimiksinler, spektinomisin, tetrasiklinler, linkomisin ve klindamisin dahil antibiyotikler, propranolol, kalsiyum kanal blokörleri, lignokain, prokainamid ve kinidin dahil anti-aritmik ilaçlar, furosemid ve olasılıkla tiyazid, mannitol ve asetazolamid dahil diüretikler, magnezyum tuzları, lityum tuzları, trimetafan, hekzametonyum gibi gangliyon blokör ilaçlar.Azaltıcı etkiler
Önceden fenitoin veya karbamazepinin kronik uygulaması; önceden süksametonyum uygulamasının NİMBEX bolus dozunu takiben nöromüsküler bloğun süresine veya infuzyon hızı gereksinimleri üzerine etkisi yoktur. Non-depolarizan nöromüsküler blokör ilaçlarm etkilerini uzatmak için süksametonyum uygulaması antikolinesterazlar ile geri dönmeyi zorlaştıran uzamış ve kompleks bir blok ile sonuçlanabilir. Nadiren, belli ilaçlar latent Myastenia Gravis'i şiddetlendirebilir veya ortaya çıkarabilir veya gerçekten myastenik sendrom oluşumuna yol açabilir. Non-depolarizan nöromüsküler blokör ilaçlara aşırı duyariilıkta artış meydana gelebilir. Bu gibi ilaçlara çeşitli antibiyotikler, beta-blokörler (propranolol, oksprenolol), anti-aritmik ilaçlar (prokainamid, kinidin), anti-romatizmal ilaçlar (klorokin, D-penisilamin), trimetafan, klorpromazin, steroidler, fenitoin ve lityum dahildir. Eşzamanlı kullanılan bazı ilaçlar (öm. furosemid, fenitoin, teofılin, karbamazepin) nöromüsküler blokajı antagonize edebilir.
Özel popülasyonlara ilişkin ek bilgiler
Veri bulunmamaktadır.Pediyatrik popülasyon:
Veri bulunmamaktadır.4.6. Gebelik ve laktasyon Genel tavsiye
Gebelik Kategorisi: CÇocuk doğurma potansiyeli bulunan kadınlar/Doğum kontrolü (Kontrasepsiyon)
Hayvanlar üzerinde yapılan çalışmalar, gebelik/ve-veya/ embriyonal/fetal gelişim/ve-veya /doğum /ve-veya doğum sonrası gelişim üzerindeki etkiler bakımından yetersizdir. İnsanlara yönelik potansiyel risk bilinmemektedir.Gebelik dönemi
NİMBEX gebelikte ancak anneye sağlaması beklenen yararlan fetüse olan herhangi bİr potansiyel riskinden fazla ise kullanılmalıdır. Gerekli olmadıkça gebelik döneminde kullanılmamalıdır.Laktasyon dönemi
Sisatrakuryum veya metabol itlerinin anne sütüne geçip geçmediği bilinmemektedir.Üreme yeteneği/Fertilite
NİMBEX'in üreme yeteneği ve fertilite üzerindeki etkisi bilinmemektedir.4.7. Araç ve makine kullanımı üzerindeki etkiler
Bu önlem NİMBEX kullanımı ile ilgili değildir. Fakat genel anesteziyi takiben görev performansı ile ilgili her zamanki önlemler göz önünde tutulmalıdır.4.8. İstenmeyen etkiler
^ Klinik geliştirme programı süresince NİMBEX'e atfedilebilen herhangi bir yan etki oluşmamıştır.Çok yaygın (>1/10); yaygm (>1/100 ila <1/10); yaygın olmayan (>1/1.000 ila <l/100); seyrek (>1/10.000 ila <1/1.000); çok seyrek (<1/10.000), bilinmiyor (eldeki verilerden hareketle tahmin edilemiyor).
Vasküler hastalıklar
Yaygın: Hipotansiyon Yaygın olmayan; Ciltte kızarmaKardiyak hastalıklar
Yaygm: BradikardiSolunum, göğüs bozuklukları ve mediastinal hastalıklar
Yaygın olmayan: BronkospazmÇok seyrek: Ani hırıltı, göğüs ağrısı veya göğüs sıkışması
Deri ve deri altı doku hastalıkları
Yaygm olmayan: Kızarıklık, döküntüÇok seyrek: Modüler döküntü veya vücudun herhangi bir yerinde kurdeşen
Kas-iskelet bozukluklar, bağ doku ve kemik hastalıkları
Çok seyrek:Kas
güçsüzlüğü ve/veya miyopati. Yoğun bakım ünitelerindeki ağır hastalarda kas gevşeticilerinin uzun süre kullanımı sonrası miyopati ve/veya kas zayıflığına ait bazıraporlar bildirilmiştir, Çoğu hasta birlikte kortikosteroid kullanmaktaydı. Bu olaylar NİMBEX ile birlikte, seyrek olarak rapor edilmektedirler ve nedensel bir ilişki gösterilememiştir.
Bağışıklık sistemi hastalıkları
Çok seyrek: Anafılaksi. NİMBEX ile birlikte, bir ya da daha fazla anestezik ilaç verilen hastalarda çok ciddi anaflaktik reaksiyonlar bildirilmiştir.4.9. Doz aşımı ve tedavisi
NİMBEX aşırı dozajına bağlı olduğu beklenilen başlıca belirtiler uzayan kas paralizisi ve bunun sonuçlandır. Tedavi; yeterli spontan respirasyon geri dönene kadar pulmoner ventilasyon ve arteryel oksijenasyonun idamesi esastır. NİMBEX bilinci etkilemediğinden tam sedasyon gerekli olabilir. Spontan düzelme belirtisi bir kez başlamışsa antikolinesteraz ilaç uygulaması düzelmeyi hızlandırabilir.5. FARMAKOLOJİK ÖZELLİKLER
5.1. Farmakodinamik özellikler
Farmakoterapötik grup: Non-depolarizan nöromüsküler blokör ATC kodu: M03AC11Sisatrakuryum, motor sinir dallarının kas içinde sonlanan uç kısmındaki kolineıjik reseptörlere bağlanarak asetilkolinin etkisini antagonize eder ve sonuç olarak nöromüsküler iletiyi kompetitif olarak bloke eder. Bu etki neostigmin veya edrofonyum gibi antikolinesteraz ilaçlarla tersine çevrilir. Sisatrakuryum için ED95 (ulnar sinirin stimülasyonu ile adductor pollicis kasının seğirme cevabında % 95 depresyon oluşturmak İçin gerekli olan doz) opioid anestezisi (tiyopenton/fentanil/midazolam) sırasında 0.05 mg/kg vücut ağırlığı olduğu tahmin edilmektedir. Sisatrakuryumun halotan anestezisi sırasında çocuklardaki ED95 değeri 0.04 mg/kg'dır.
5.2. Farmakokinetik özellikler Genel Özellikler
Sisatrakuryumun kompartımanlı olmayan farmakokinetiği çalışılan doz aralığında doza bağımlı değildir (0.1-0.2 mg/kg, öm. 2 ila 4 x ED95). Popülasyon farmakokinetik modelleri bu bulguları 0.4 mg/kg'a (8xED95) kadar doğrular. Sağlıklı erişkin ameliyat hastalarına 0.1 ve 0.2 nıg/kg dozlarında NİMBEX uygulanmasından sonra farmakokinetik parametreler aşağıdaki tabloda özetlenmiştir.ORTALAMA DEĞERLERİN YAYILIMI
PARAMETRE
Klerens
4.7 - 5.7 ml/dak/kg 121 -161 ml/kg 22 - 29 dak
Kararlı durumda dağılım hacmi
Eliminasyon yanlanma ömrü
Emilim
:Veri yoktur.
Da£ılım:
Veri yoktur.
Bivotransformasvon:
Sisatrakuryum, vucutta laudanozin ve monokuaterner akrilat metaboliti oluşturmak üzere fizyolojik pH ve sıcaklıkta Hofmann eliminasyonu ile parçalanır. Monokuaterner akrilat spesifik olmayan plazma esterazları ile monokatemer alkol metabolitini oluşturacak şekilde hidrolize uğrar. Sisatrakuryumun eliminasyonu organ bağımsız olmakla beraber, karaciğer ve böbrekler metabolitlerinin klerensi için temel yoldur. Bu metabolitler nöromüsküler blokör etki taşımazlar.
Elimin
as
yon:Veri yoktur.
Hastalardaki karekteristik özellikler
Yaslı hastalarda farmakokinetik:
Sisatrakuryumun yaşlı ve genç erişkin hastalarda farmakokinetiğinde klinik olarak önemli bir fark yoktur.
Böbrek yetmezliği olan hastalarda farmakokinetik:
Sisatrakuryumun böbrek yetmezliği olan hastalar ile sağlıklı erişkin hastalar arasında farmakokinetiğinde klinik olarak önemli bir fark yoktur.
Hepatik vetmezli&i olan hastalarda farmakokinetik:
Sisatrakuryumun karaciğer yetmezliği olan hastalar ile sağhkh erişkin hastalar arasında farmakokinetiğinde klinik olarak önemli fark yoktur.
İnflizvon sırasmda farmakokinetik
:İnfüzyonundan sonra sisatrakuryumun farmakokinetiği ile tek bolus enjeksiyondan sonraki farmakokinetiği aynıdır.
YoSun bakım ünitelerindeki hastalarda farmakokinetik:
Sisatrakuryumun farmakokinetiği yoğun bakım ünitelerinde uzun süreli infuzyon alan hastalardaki farmakokinetiği ile infuzyon veya tek bolus enjeksiyon alan, sağlıklı iuneliyat hastalanndaki farmakokinetiği ile benzerdir. Sisatrakuryumun ortalama klerensi 7.5 ml/kg/dak ve yan ömür eliminasyonu 27 dak'dır. Yoğun bakım hastalannda NİMBEX infüzyonu sonrası geri dönüş profili infuzyonun süresi ile bağımsızdır. Normal hepatik ve/veya renal fonksiyonlu hastalarla karşılaştırılınca metabol iti erin konsantrasyonu yoğun bakım hastalarında daha yüksektir.
5.3. Klinik öncesi güvenlilik verileri
Subakut toksisite çalışmalarında köpek ve maymunlara tekrarlayan doz 3 haftalık uygulama özel bir toksisite göstermemiştir.Sisatrakurium in vitro mikrobiyal mutajenite testinde 5000 mikrogranVtabla konsantrasyonunda mutajenik bulunmamıştır. Sıçanlarda yürütülen bir in vivo Sitogenetik çalışmada 4 mg/kg doz düzeyine dek anlamlı kromozomal anormallik gözlenmemiştir. Sisatrakurium in vitro fare lenfoma hücresi mutajenite tayininde 40mikrogram/ml ve üzerindeki konsatrasyonlarda mutajenik bulunmuştur. Seyrek ve/veya kısa süreli kullanılan bir ilaç için tek bir mutajenik yanıtın klinik önemi şüphelidir.
Karsinojenite çalışması yürütülmemiştir.
Fertilite çalışması yürütülmemiştir. Sıçanlarda yürütülen üreme çalışmaları fotal gelişim üzerinde advers etki göstermemiştir.
Tavşanlarda yürütülen intraarteriyal çalışmada Nimbex enjeksiyonu iyi tolere edilmiş ve İlaç ile ilişkili değişiklik görülmemiştir.
6. FARMASÖTİK ÖZELLİKLER
6.L Yardımcı maddelerin listesi
pH ayan için benzen sülfonik asit çözeltisi Enjeksiyonluk su6.2. Geçimsizlikler
NİMBEX, Laktatlı Ringer enjeksiyonu ile seyreltildiğinde kimyasal olarak stabil değildir. NlMBEX sadece asidik solüsyonlarla stabil olduğu için aynı şırıngada alkali solüsyonlarla (öm.: sodyum tiyopenton) karıştırılmamalı veya aynı iğneden alkali solüsyonu takiben uygulanmamalıdır. NİMBEX, ketorolak, trometamol ve propofol enjektabl emülsiyon ile geçimli değildir. İntravenöz olarak uygulanan diğer ilaçlarda olduğu gibi, enjeksiyon bölgesi olarak küçük bir ven seçildiği zaman NİMBEX uygulamasını takiben damar, uygun bir i.v. sıvısı ile (öm.: sodyum klorür i.v. infüzyon (% 0.9 a/h) ile) ven yıkanmalıdır.İzleme:
Diğer nöromüsküler blokör ilaçlarla olduğu gibi NİMBEX uygulaması sırasında bireysel doz ihtiyacını belirlemek için nöromüsküler fonksiyonun izlenmesi önerilir.6.3. Raf ömrü
24 ay6.4. Saklamaya yönelik Özel tedbirler
2°C ve 8°C arasında saklayınız. Işıktan koruyunuz. Dondurmaymız. NİMBEX antimikrobiyal koruyucu içermez, bu nedenle dilüsyon işlemi kullanılmadan hemen önce yapılmalıdır ve seyreltmeyi takiben mümkün olduğu kadar çabuk, hemen uygulanmalıdır. İnfüzyon sıvısı ile seyreltilmiş solüsyon veya kullanılmış açık ampul atılmalıdır.6.5. Ambalajm niteliği ve içeriği
2.5 mİ, 5 ampul (2mg/ml), karton kutuda6.6 Beşeri tıbbi üründen arta kalan maddelerinimhası ve diğer özel önlemler
Tüm kullanılmayan ürün ve atık maddeler Tıbbi Atıklann Kontrolü Yönetmeliği ve Ambalaj ve Ambalaj Atıklarının Kontrolü Yönetmeliği ne uygun olarak imha edilmelidir.Ampul açma talimatları:
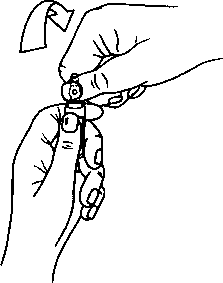
Ampuller OPC (Tek Kırma Noktası) açma sistemi ile donatılmışlardır ve aşağıdaki talimatlar doğrultusunda açılmalıdırlar:
Ampulü, resim 1 'de gösterildiği gibi alt kısmmdan tutunuz
Resim 2'de gösterildiği gibi diğer elinizin başparmağmı ampuldeki renkli noktaya
bastırınız
Şekil 1


Şekil 2
7. RUHSAT SAHİBİ
GlaxoSmithKline İlaçları San. ve Tic. A.Ş., Levent/İstanbul.Büyükdere cad. No.l73, 1.Levent Plaza, B Blok 34394 1 .Levent/İstanbul
Tel no: Faks no:
0 212 339 44 00 0 212 339 45 00
8. RUHSAT NUMARASI
104/969. İLK RUHSAT TARİHİ/RUHSAT YENİLEME TARİHİ
İlk Ruhsat Tarihi: 23.11.1998 Ruhsat Yenileme Tarihi:10. KÜB'ün YENİLEME TARİHİ
İlaç Bilgileri
Nimbex 5mg/2.5ml Enjektabl Ampul
Etken Maddesi: Sisatrakuryum besilat
Atc Kodu: M03AC11
Kullanma talimatı ve kısa ürün bilgileri
Google Reklamları
İlgili İlaçlar
Ana Sayfa | Hakkımızda | İlaçlar | İlaç Ara | İlaç Firmaları | Gizlilik | Bize Ulaşın
Telif Hakkı 2008-2026 © İlaç Prospektüsü. Tüm Hakları Saklıdır.Uyarı: Sitemizde yayınladığımız ilaç bilgileri ile doktora danışmadan kesinlikle ilaç kullanmayınız!
Aksi halde doğabilecek sağlık sorunlarından ilacprospektusu.com sorumlu tutulamaz.