Deslodin 2.5mg/5ml Şurup Kısa Ürün BilgisiSolunum Sistemi » Sistemik Antihistaminikler » Sistemik Antihistaminik İlaçlar » Diğer Sistemik Antihistaminikler » Desloratadin KISA ÜRÜN BİLGİSİ1. BEŞEEÛ TIBBİ ÜRÜNÜN ADIDESLODİN 2,5mg/5ml Şurup2. KALİTATİF VE KANTİTATİF BİLEŞİM Etkin Madde:Her 1 ml'de 0.5 mg desloratadin içerir.Yardımcı madde(ler):Sukroz 500 mg/mlSorbitol (%70) 400 mg/ml Sodyum benzoat 4 mg/ml Sodyum sitrat dihidrat 5 mg/ml Disodyum edetat 1 mg/ml Yardımcı maddeler için ö.l'e bakınız. 3. FARMASÖTİK FORMŞurupBerrak renksiz çözelti. 4. KLİNİK ÖZELLİKLER4.1. Terapötik endikasyonlarDESLODİN, alerjik rinit ile ilişkili, hapşınk, burunda akıntı ve kaşınma, konjesyon/burun tıkamklığı, aym zamanda gözlerde kaşınma, yaşarma ve kızanklık, damakta kaşınma ve öksürük gibi semptomlarm giderilmesinde endikedir.DESLODİN, aynca, ürtiker ile birlikte görülen, kaşıntının giderilmesi, derideki kabartı ve kızanklık gibi semptomların ortadan kaldınimasmda endikedir. 4.2. Pozoloji ve uygulama şekli Pozoloji /uygulama sıklığı ve süresi:Semptomlan haftada 4 gün veya 4 haftadan daha az süren intermitan alerjik rinit, hastanın hastalık öyküsü değerlendirmesine göre tedavi edilmeli ve semptomlann giderilmesi ve tekrarlanması durumımda tedaviye ara verilmelidir. Semptomlan haftada 4 gün veya daha fazla ve 4 haftadan fazla görülen persistan aleıjik rinitte, hastanın aleıjinin ortaya çıkması durumunda sürekli tedavisi önerilmelidir.Uygulama şekli:Kutunun içinde ilaçla birlikte 0.25 mİ dereceli 5 ml'lik ölçülü doz pipeti sunulmaktadır. Doz ayarlanırken beyaz pistonun üzerindeki miktar şekildeki gibi şeffaf muhafaza kabının halkasına kadar çekilmelidir. Alınacak doz, halka hizasında yazılı olan miktardır.muhafaza kabının 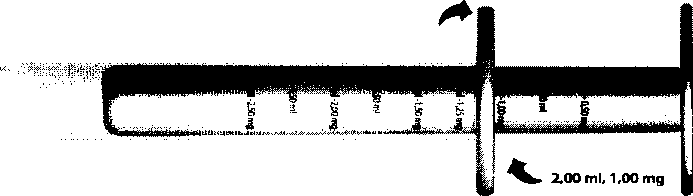 6 ay ila 11 aylık çocuklar: DESLODİN, intermitan ve persistan aleıjik riniti içeren alerjik rinit, ürtikerle birlikte gelişen semptomların giderilmesinde günde bir kere 2 mİ (1 mg) tek babına veya besinlerle.
6 ay ila 11 aylık çocuklar: DESLODİN, intermitan ve persistan aleıjik riniti içeren alerjik rinit, ürtikerle birlikte gelişen semptomların giderilmesinde günde bir kere 2 mİ (1 mg) tek babına veya besinlerle.Ölçülü doz pipetini 2 mi'ye kadar çekerek kullanınız. 1 ila 5 yaşa kadar olan çocuklar: DESLODİN, intermitan ve persistan aleıjik riniti içeren alerjik rinit, ürtikerle birlikte gelişen semptomların giderilmesinde günde bir kere 2.5 mİ (1.25 mg) tek başına veya besinlerle. Ölçülü doz pipetim 2.5 ml'ye kadar çekerek kull anınız.6 ila 11 yaşa kadar olan çocuklar: DESLODİN, intermitan ve persistan alerjik riniti içeren alerjik rinit, ürtikerle birlikte gelişen semptomların giderilmesinde günde bir kere 5 mİ (2.5 mg) tek başına veya besinlerle. Ölçülü doz pipetini 5 ml'ye kadar çekerek kullamnız. Erişkinler ve 12 yaş ve üzerindeki çocuklar: DESLODtN, intermitan ve persistan aleıjik riniti içeren alerjik rinit, ürtikerie birlikte gelişen semptomlann giderilmesinde günde bir kere 10 mİ (5 mg), tek başma veya besinlerle. ölçülü doz pipetini 5 mİ'ye kadar çekerek 2 kez kullanmız. Özel popülasyonlara ilişkin ek bilgiler:Böbrek yetmezliği:Şiddetli böbrek yetmezliği olan hastalarda dikkatli kullanılmalıdır.Karaciğer yetmezliği:Karaciğer yetmezliği olan hastalarda kullanımına ilişkin veri yoktur.^ Pediyatrik popülasyon:Pediyatrik popülasyonda uygulama şekli yukarıda verilmektedir.Geriyatrik popülasyon:Geriyatrik popülasyonda etkinlik ve güvenliliği henüz belirlenmemiştir.4.3. KontrendikasyonlarEtkin madde, yardımcı maddelerden herhangi birine veya loratadine karşı aşın duyarlılığı olan hastalarda kontrendikedir.4.4. Özel kullanım uyarılan ve önlemleri^ DESLODİN'in 6 aydan küçük çocuklarda etkinlik ve güvenliliği henüz belirlenmemiştir (bkz.bölüm 5.1). 2 yaşından küçük çocuklarda alerjik rinit tanısının, diğer rinit çeşitlerinden ayırt edilmesi oldukça zordur. Hastada üst solunum yolu enfeksiyonu veya yapısal anormallikler bulunmaması durumımda, ayrıca hastanın anamnez, fiziki muayene ve uygun laboratuvar ve deri testlerinin sonuçlan da göz önünde bulımdurulmalıdır. Erişkinlerin ve 2-11 yaş arasmdaki çocuklann yaklaşık %6'sı, desloratadini fenotipik olarak zayıf metabolize ederler ve yüksek düzeyde maruziyet gösterirler. DESLODtN'i zayıf metabolize eden 2-11 yaş arasmdaki çocuklarda güvenliliği, ilacı normal metabolize eden çocuklardaki ile aynıdır. DESLODİN'in, desioratadini iyi metabolize edemeyen 2 yaşından küçük çocuklardaki etkileri incelenmemiştir. Desloratadin kullanımı, kardiyovasküler sistem problemi olan kişilerde dikkatli gözlem gerektirmektedir. DESLODİN şiddetli böbrek yetmezliği olan hastalarda dikkatli kullanılmalıdır (bkz. bölüm 5.2). Sukroz ve sorbitol: Bu tıbbi ürün sukroz ve sorbitol içermektedir; bundan dolayı nadir kalıtımsal fhıktoz intoleransı, glikoz-galaktoz malabsorpsiyonu veya sükraz-izomaltaz yetmezliği problemi olan hastaların bu ilacı kullanmamaları gerekir. Sodyum: Bu tıbbi ürün her dozunda 1 mmol (23 mg)'dan daha az sodyum ihtiva eder, bu dozda sodyuma bağlı herhangi bir etki beklenmemektedir. 4.5. Diğer tıbbi ürünler ile etkileşimler ve diğer etkileşim şekilleriEritromisin ya da ketokonazolun birlikte kullanıldığı, desloratadinle yapılmış klinik çalışmalarda klinik bir etkileşim gözlenmemiştir.Desloratadin'in alkolle bir arada alındığı klinik farmakoloji çalışmalannda, desloratadin alkolün performansı zayıflatıcı etkisini artırmamıştır (bkz. bölüm 5.1). DESLODİN oral yolla alman doğum kontrol ilaçlan ile etkileşime geçmektedir. Bu nedenle, tedavi süresince alternatif, etkili ve güvenilir bir doğum kontrol yöntemi uygulanmalıdır. 4.6. Gebelik ve laktasyon Genel tavsiyeGebelik kategorisi C'dir.Çocuk doğurma potansiyeli bulunan kadmlar/Doğum kontrolü (Kontrasepsiyon)DESLODİN oral yolla alman doğum kontrol ilaçlan ile etkileşime geçmektedir. Bu nedenle, tedavi süresince alternatif, etkili ve güvenilir bir doğum kontrol yöntemi uygulanmalıdır.Gebelik donemiDESLODİN'in gebe kadınlarda kullanımına ilişkin yeterli veri mevcut değildir. Hayvanlar üzerinde yapılan araştırmalarda üreme toksisitesi bulunmamaktadır.İnsanlara yönelik potansiyel risk bilinmemektedir (bkz. bölüm 5.3.). Bu nedenle hamilelik süresince kullanılması tavsiye edilmez. Laktasyon dönemiDesloratadin anne sütünde DESLODiN'in terapötik dozlan emziren kadınlara uygulandığı takdirde memedeki çocuk üzerinde etkiye neden olabilecek ölçüde atılmaktadır. DESLODİN emzirme döneminde kullanılmamalıdır.Üreme yeteneği/FertüiteHayvanlar üzerinde yapılan araştırmalarda üreme toksisitesi bulunmamaktadır. İnsanlara yönelik potansiyel risk bilinmemektedir.4.7. Araç ve makine kullanımı üzerindeki etkilerDESLODiN'in araç ve makine kullanma becerisi üzerine etkisi gözlenmemiştir. Ancak çok seyrek de olsa, bazı hastalarda uyku hali oluşabileceği ve bu durumun onlann araç ve makine kullanımım etkileyebileceği belirtilmelidir.4.8. İstenmeyen etkilerPediyatrik popülasyondaki klinik çalışmalarda, desloratadin, 6 ay ila 11 yaş arasındaki 246 çocuğa veribniştir. 2 ila 11 yaş arasındaki çocuklarda advers olay sıklığı, desloratadin şurup ve plasebo kullanan gruplarda benzer bulunmuştur. 6 ila 23 aylık bebeklerde plaseboya kıyasla daha fazla görülen en yaygın bildirilen yan etkiler diyare (%3.7), ateş (%2.3) ve uykusuzluktur (%2.3).Alerjik rinit ve kronik idiyopatik ürtikerin de içinde bulunduğu endikasyonlan kapsayan erişkin ve adolesanlardaki klinik çalışmalarda, önerilen dozlarda, desloratadin kullanan hastalann %3'ünde plasebodan daha fazla yan etki görülmüştür. Plasebodan daha fazla görülen ve en yaygın bildirilen yan etkiler, bitkinlik (%1.2), ağız kuruluğu (%0.8) ve baş ağrısı (%0.6)'dır. İstenmeyen olaylar aşağıda sistem organ smıfma göre listelenmiştir. Sıklıklar şu şekilde tanımlanmıştır: Farklı organ sistemlerinde; Çok yaygın (> 1/10), yaygın (> 1/100 ila <1/10), yaygın olmayan (> 1/1.000 ila <1/100), seyrek (> 1/10.000 ila <1/1.000), çok seyrek (<1/10,000), bilinmiyor (eldeki verilerden hareketle tahmin edilemiyor). Sinir sistemi bozuklukları:Yaygın: Bitkinlik Yaygın olmayan; Baş ağrısı^ Gastrointestinal bozukluklar:Yaygın olmayan: Ağız kuruluğuPazarlama sonrası deneyim :Pazarlama sonrası deneyimlerde bildirilen çok seyrek yan etkiler aşağıdadır. Psikiyatrik hastalıkları:Çok seyrek: Halüsinasyonlar.Sinir sistemi bozuklukları:Çok seyrek: Sersemlik, uyku hali, uykusuzluk, psikomotor hiperaktivite, inmeKardiyak bozukluklar:Çok seyrek: Taşikardi, palpitasyon.Gastrointestinal bozukluklar:Çok seyrek: Abdominal ağn, bulantı, kusma, dispepsi, diyare.Hepato-bilier hastalıkları:Çok seyrek: Karaciğer enzimlerinde yükselme, hepatit ve bilirubinde artış.Kas-iskelet bozukluklar, bağ doku ve kemik hastalıkları:Çok seyrek: Miyalji.Genel bozukluklar ve uygulama bölgesine ilişkin bozukluklar:Çok seyrek: Hipersensitivite reaksiyonlan (anafılaksi, anjiyoödem, dispne, pruritus, döküntü ve ürtiker).4.9. Doz aşımı ve tedavisiDoz aşımı durumunda, absorbe edilmemiş etkin maddeyi uzaklaştıracak standart önlemler alınmalıdır.Semptomatik ve destekleyici tedavi önerilir. Erişkinler ve adolesanlarda 45 mg'a kadar desloratadin uygulanan (klinik dozun 9 katı) çok dozlu bir klinik araştırmada, klinik olarak önemli herhangi bir etki gözlenmemiştir. Desloratadin hemodiyaliz ile elimine edilmemektedir; periton diyalizi ile elimine olup olmadığı bilinmemektedir. 5. FARMAKOLOJİK ÖZELLİKLER5.1. Farmakodinamik özelliklerFarmakoterapötik grup; Sistemİk kullanım için diğer antihistaminler ATC Kodu: R06A X27Etki mekanizması: Desloratadin sedasyon yapmayan, uzun etkili, potent, selektif periferik histamin Hı - reseptör antagonistidir. Desloratadin, oral uygulamadan sonra santral sinir sistemine girememesi nedeniyle, periferik histamin Hı - reseptörlerini selektif olarak bloke eder. Desloratadin in vitroçalışmalarda antialeijik özellikler göstermiştir. Bunlar IL-4, IL-6, IL8 ve IL-13 gibi proinflamatuvar sitokinlerin insan mast hücrelerinden/bazofillerden salınımımn inhibisyonunu ve endotel hücrelerinde adezyon molekülü P-selektinin ekspresyonunun inhibe edilmesini içerir. Bu gözlemlerin klinik önemi henüz doğrulanmamıştır.Desloratadin şurubun etkinliği ayrı pediyatrik çalışmalarda incelenmemiştir. Desloratadin'in güvenliliği üç pediyatrik çalışmada gösterilmiştir. 6 ay ila 11 yaşındaki antihistaminik tedavisi almaya aday olan çocuklar, 1 mg (6 ila 11(111 yaş) günlük doz almıştır. Klinik laboratuvar testleri, vital bulgular ve QTc (corrected QT) içeren EKG (Elektrokardiyografi) verileri, tedavinin iyi tolere edildiğini göstermiştir. Önerilen dozda verildiğinde, desloratadinin farmakokinetik aktivitesi pediyatrik ve erişkin popülasyonlarda karşılaştınlabilir düzeydedir. Mevsimsel alerjik rinit/kronik idiopatik ürtiker seyri ve desloratadin profili erişkin ve pediyatrik hastalarda benzer olduğundan, desloratadinin erişkinlerdeki etkinliği, pediyatrik popülasyona ekstrapole edilebilir.14 gün boyunca, günde 20 mg'a kadar desloratadin uygulanan çok dozlu bir klinik araştırmada, istatistik ya da klinik açıdan önemli hiçbir kardiyovasküler etki gözlenmemiştir. Desloratadinin on gün süreyle günde 45 mg (klinik dozun dokuz katı) verildiği bir klinik farmakolojik çalışmada, QTc (EKG'de Q dalgası ile T dalgası arasındaki süre) aralığında uzama gözlenmemiştir, Desloratadin santral sinir sistemine kolayca penetre olmaz. Önerilen günlük 5 mg dozda, somnolans insidansında, plaseboya kıyasla bİr artış olmamıştır. Desloratadin tabletler, klinik araştırmalarda, 7.5 mg günlük dozda bile, psikomotor performansı etkilememiştir. Bir tek-doz çalışmasında, desloratadin 5 mg, sübjektif uyku halinin şiddetlenmesi veya uçuşla ilgili faaliyetleri de kapsayan, uçuş performansının standart Ölçümlerini etkilemez. Klinik farmakoloji çalışmalannda, alkolle birlikte uygulama alkolün neden olduğu performans zayıflaması ya da uykusuzluk artışına neden olmaz. Desloratadin ve plasebo gruplan arasında yapılan psikomotor test sonuçİannda anlamlı bir fark bulunmamıştır. Desloratadin, tek başına ya da alkol ile birlikte alındığında, alkolün performans bozucu etkilerini artırmamıştır. Çok dozlu, ketokonazol ve eritromisin etkileşim çalışmalarında, desloratadin plazma konsantrasyonlarında klinik olarak önemli bir değişiklik gözlenmemiştir. Alerjik rinitli yetişkin ve adolesan hastalarda, desloratadin tabletler, hapşınk, burunda akıntı ve kaşınma, konjesyon / burun tıkanıklığı, aynı zamanda gözlerde kaşınma, yaşarma ve kızankhk ve damakta kaşınma gibi semptomlann giderilmesinde etkili olmuştur. Alerjik rinit, mevsimsel ve tekrarlayan alerjik rinit olarak sınıflandırıldığı gibi, semptomlann süresine göre intermitan ve persistan alerjik rinit olarak da sınıflandınlabilir. İntermitan alerjik rinit, semptomlann bir haftada 4 günden az veya 4 haftadan daha az bir sürede görülmesi olarak tanımlanabilir. Persistan aleıjik rinit, semptomlann bir haftada 4 gün veya daha fazla ve 4 haftadan daha fazla görülmesi olarak tammlanabilir. Desloratadin tabletler mevsimsel aleıjik rinitin alevlermıesini azaltmada, rino-konjunktivit yaşam kalitesi anketindeki toplam skorlamada etkindir. En büyük iyileşme, semptomlarca kısıtlanan günlük aktiviteler ve pratik problemlerinin alanında görülmüştür. Kronik idiyopatik ürtiker, etiyolojisi ne olursa olsun arka plandaki fizyopatolojinin benzer olması ve prospektif çalışmalara katılacak kronik hastalann daha kolay bulunabilmesi nedeniyle, ürtikere bir klinik model olarak incelenmiştir. Histamin salınması tüm ürtikaryal hastalıklara yol açan bir neden olduğundan, desloratadinin klinik kılavuzlarda da önerildiği gibi, kronik idiyopatik ürtikere ilave olarak diğer ürtikaryal hastalıklardaki semptomlann giderilmesinde de etkili olması beklenir. Kronik idiyopatik ürtikeri olan hastalarda yürütülen 6 haftalık iki plasebo-kontrollü çalışmada, Desloratadin, tedavinin birinci gününden itibaren, kaşıntımn hafiflemesinde ve derideki kabartı ve kızanklıklann büyüklük ve sayısınm azalmasında etkili olmuştur. Her iki çalışmada da, etki, 24 saatlik dozlama aralığı süresince değişmeden devam etmiştir. Kronik idiyopatik ürtikerdeki diğer antihistaminik çalışmalannda, antihistaminiklere yanıt vermeyen hastalann bir kısmı çalışmadan çıkarılmıştır. Desloratadinle tedavi edilen %55 oramndaki hastalann %50'sinde plaseboyla tedavi edilen %19 oramndaki hastaya göre pruritusta iyileşme gözlemlenmiştir. Desloratadin ile tedavi aynı zamanda, uyku ve günlük rutin aktiviteler ile etkileşimde azalma ile dört puanlı skalada ölçülen, uyku ve günlük fonksiyonlarda iyileşme sağlamıştır. 5.2. Farmakokinetik özellikler Genel özelliklerEmilim:Desloratadin plazma konsantrasyonlan, yetişkin ve adolesanlarda uygulamadan sonra 30 dakika içinde saptanabilir düzeye gelir. Desloratadinin emilimi iyidir ve maksimum konsantrasyona yaklaşık 3 saat sonra ulaşılır. Desloratadinin terminal faz yanlanma ömrü yaklaşık 27 saattir. Desloratadinin birikim derecesi, yanlanma ömrü (yaklaşık 27 saat) ve günde tek doz dozlama sıklığı ile uyumludur. Desloratadinin biyoyararlammı 5 ile 20 mg arasında doz ile orantılıdır. DaSılım:Bir dizi farmakokinetik ve klinik çalışmalarda, gönüllülerin %6'sı daha yüksek desloratadin konsantrasyonuna ulaşmıştır. Desloratadini az raetabolize eden bu fenotipin prevalansı erişkin (%6) ve 2-11 yaş arası pediyatrik gönüllülerde (%6) benzer iken, her iki popülasyonda siyahlarda (%18 erişkin, %16 pediyatrik) beyazlara (%2 erişkin, %3 pediyatrik) kıyasla daha yüksek bulunmuştur. Sağlıklı erişkin gönüllülerde tablet formülasyonuyla yürütülen bir çoklu-doz farmakokinetik çalışmasında, dört gönüllünün desloratadini daha az metabolize ettiği saptanmıştır. Bu kişilerde Cmaks konsantrasyonu yaklaşık 7 saatte 3 kat daha yüksekti ve terminal faz yan-ömrü yaklaşık 89 saatti. Aleijik rinit tanısı koyulmuş, 2-11 yaş arası zayıf metabolize eden pediyatrik hastalarda şurup formülasyonuyla yapılmış çoklu doz farmakokinetik çalışmalannda benzer farmakokinetik parametreler gözlemlenmiştir. Desloratadİne maruziyette (EAA) 6 kat daha yüksek ve Cmaks 3-6 saatte yaklaşık 3-4 kat daha yüksek olan 120 saat terminal yarı Ömürdür. Yaşa uygun dozlarda pediyatrik zayıf metabolize edenler ve yetişkinlere maruz kalım benzerdir. Bu hastalarda genel güvenlİlik profili genel popülasyona göre farklı değildir. Desloratadinin 2 yaşın altmdaki zayıf metabolize edenlerde etkileri incelenmemiştir. Desloratadin plazma proteinlerine orta derecede (% 83 - % 87 ) bağlanır. 14 gün süreyle günde tek doz (5 mg ile 20 mg) desloratadin uygulamasını takiben, klinik olarak önem taşıyan herhangi bir ilaç birikim belirtisi bulunmamıştır. Desloratadin ile yürütülen bir çapraz tasarımlı, tekli doz çalışmasında, tablet ve şurup formülasyonlannm biyoeşdeger oldukları saptanmıştır. Ayrı tekli doz çalışmalannda, tavsiye edilen dozlarda pediyatrik hastalann desloratadin için EAA ve Cmaks değerleri desloratadin şurubun 5 mg'lık bir dozunu alan erişkinlerle benzer bulurunuştur. Bivotransformasvon:Desloratadin metabolizmasından sorumlu enzim henüz tanımlanmamış olduğundan diğer ilaçlarla olabilecek bazı etkileşimler tamamen gözardı edilememektedir. CYP3A4 ve CYP2D6 nın spesifik inhibitörleri ile in vivoçalışmalar bu enzimlerin desloratadin metabolizmasında etkili olmadığını göstermiştir. Desloratadin CYP3A4 veya CYP2D6'yı inhibe etmemektedir ve P-glikoprotein substratı veya inhibitörü değildir.Sağlıklı erişkin olgularda tablet formülasyonuyla yürütülen bir çok-dozlu farmakokinetik çalışmada, dört olgunun desloratadini yavaş metabolize ettiği bulunmuştur. Bu olgularda 7. saat civanndaki Cmaks konsantrasyonu yaklaşık 3 kat daha yüksektir ve terminal fazdaki yanlanma ömrü 89 saat civarındadır. Bir farmakolojik ve klinik araştırmalar serisinde, olguların %6'smda desloratadinin plazma konsantrasyonları daha yüksek bulunmuştur. Bu yavaş metabolize edici fenotipin prevelansı erişkin (%6) ve 2-11 yaş arası pediyatrik (%6) olgularda karşılaştınlabilir nitelikte ve siyahlarda (erişkinler %18, pediyatrik olgularda %16) beyazlara (erişkinler %2, pediyatrik olgularda %3) kıyasla daha yüksektir; ancak bu olgulardaki güvenlilik profili, genel popülasyondakinden farklı değildir. Eliminasvon:Desloratadinin 7.5 mg dozda kullanıldığı tek dozlu bir çalışmada, besinlerin (yağ ve kaloriden zengin kahvaltı) desloratadinin dispozisyonu üzerinde hiçbir etkisi olmadığı gösterilmiştir. Diğer bir çalışmada da, greyfiırt suyunun desloratadinin dispozisyonu üzerinde bir etkisi bulunmamıştır. 5.3. Klinik öncesi güvenlilik verileriDesloratadin, loratİdinin primer aktif metabolitidir. Desloratadin ve loratadin ile gerçekleştirilen klinik dışı çalışmalar, önerilen dozda desloratadin uygulandığında, loratadin ile benzer kalitatif ve kantitatif toksisite profili olduğunu göstermiştir.Güvenlilik farmakolojisi, tekrarlanan doz toksisitesi, genotoksisite ve üreme toksisitesinin yer aldığı, desloratadin ile gerçekleştirilen klinik dışı çalışmaların verileri, insanlar için bİr tehlike olmadığını göstermiştir. Loratadin ile yürütülen çalışmalarda, karsinojenik potansiyelin bulunmadığı kamtlanmıştır. 6. FARMASÖTİK ÖZELLİKLER6.1. Yardımcı maddelerin listesiSorbitol (%70)Sitrik asit monohidrat Sodyum sitrat dihidrat Sodyum benzoat Disodyum edetat Sukroz Muz aroması Saf Su 6.2. GeçimsizliklerBilinen herhangi bir geçimsizliği bulunmamaktadır.6J. Raf ömrü24 aydır.6.4. Saklamaya yönelik özel tedbirler25°C'nin altındaki oda sıcaklığında saklayınız.6.5. Ambalajm niteliği ve içeriği Amber renkli cam şişelerŞişeler Av. Farm. 3.2.1 cam kaplar monografmdaki Tip III cam için belirtilen spesifıkasyonlara uygun amber renkli camdan yapılmıştır.Cam şişelerin kapaklarıPlastik, 25/160, PV MDS ALU kilitli kapak sistemi olan beyaz, termoplastik, profax (polietilen-polipropilen) 2g ağırlığında kapaklar kullanılmıştır.Ölçülü doz pipetiÖlçülü doz pipeti düşük dansiteli polietilenden yapılmış bir hazne ve polistirenden yapılmış bir pompa pistonundan oluşmaktadır.6.6. Beşeri tıbbi üründen arta kalan maddelerin imhası ve diğer özel önlemlerGeçerli olduğu takdirde kullanılmamış olan ürünler ya da atık materyaller 'Tıbbi Atıklann Kontrolü yönetmeliği' ve 'Ambalaj Atıklanmn Kontrolü yönetmelikleri'ne uygun olarak imha edilmelidir.7. RUHSAT SAHİBİVEM İlaç San. ve Tic. Ltd. Şti.Adres: Cinnah Cad. Yeşilyurt Sok. No: 3/2 ÇANKAYA /ANKARA Telefon :(312) 427 43 57-58 Faks :(312) 427 43 59 8. RUHSAT NUMARASI239/519. İLK RUHSAT TARİHİ / RUHSAT YENİLEME TARİHİİikruhsattarihi: 24/01 / 2012 Ruhsat yenileme tarihi:10. KÜB'ÜN YENİLEME TARİHİ |
İlaç BilgileriDeslodin 2.5mg/5ml ŞurupEtken Maddesi: Desloratadin Atc Kodu: R06AX27 Kullanma talimatı ve kısa ürün bilgileri
Google Reklamları
İlgili İlaçlar |
Ana Sayfa | Hakkımızda | İlaçlar | İlaç Ara | İlaç Firmaları | Gizlilik | Bize Ulaşın
Telif Hakkı 2008-2026 © İlaç Prospektüsü. Tüm Hakları Saklıdır.Uyarı: Sitemizde yayınladığımız ilaç bilgileri ile doktora danışmadan kesinlikle ilaç kullanmayınız!
Aksi halde doğabilecek sağlık sorunlarından ilacprospektusu.com sorumlu tutulamaz.