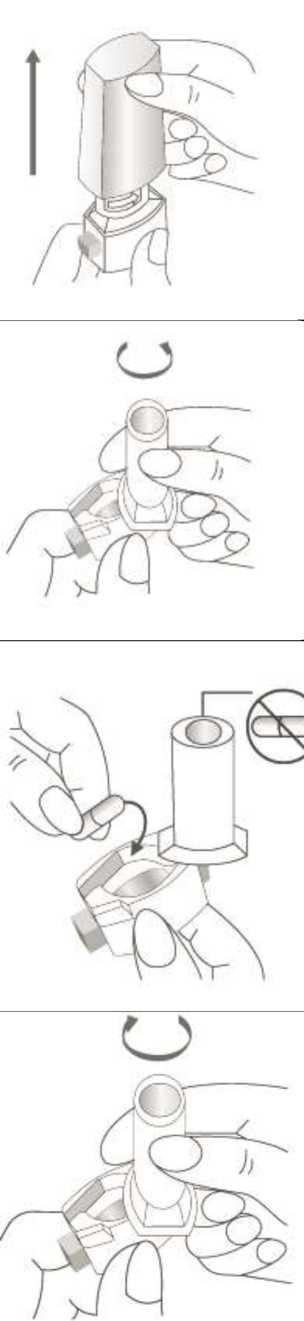
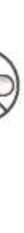Forales 12 Mcg İnhaler Kapsül Kısa Ürün BilgisiKISA ÜRÜN BİLGİSİ1. BEŞERİ TIBBİ ÜRÜNÜN ADIFORALES 12 mcg inhalasyon için kapsül 2. KALİTATİF VE KANTİTATİF BİLEŞİMİEtkin madde:Formoterol fumarat dihidrat 12,536 mcg (12,000 mcg Formoterol fumarat'a eşdeğer) Yardımcı maddeler:Laktoz monohidrat (inek sütü kaynaklı) 24987,464 mcg Yardımcı maddeler için 6.1'e bakınız. 3. FARMASÖTİK FORMİnhaler KapsülBeyaz veya beyazımsı toz içeren şeffaf kapsüller 4. KLİNİK ÖZELLİKLER4.1. Terapötik endikasyonlar Astım semptomlarının düzeltilmesi ve kontrol altına alınması amacıyla bir inhalekortikosteroid ile birlikte kullanılır. Astım hastalığının basamaklı tedavisinde 3.basamaktan itibaren (inhaler steroidlerle kontrol altına alınamayan astımlı hastalarda)kullanılır. Orta ve ağır KOAH olgularında uzun etkili p agonistler, hem semptomları kontrol altına almada hem de yaşam kalitesini düzeltmede ve alevlenme sıklığını azaltmada etkilidir. İnhale alerjenler, soğuk hava ya da egzersizle indüklenen bronkospazm profilaksisi. 4.2. Pozoloji ve uygulama şekliPozoloji/ Uygulama sıklığı ve süresi:Astım:Yetişkinler: FORALES'in etkin maddesi formoterolün de dahil olduğu uzun etkili beta 2 agonist sınıfı ilaçlar, astımlı hastalarda, yalnızca düzenli ve yeterli dozda inhale kortikosteroid alanhastalarda bu tedaviye ek olarak kullanılır. FORALES dozu, hastanın kişisel ihtiyacına göreayarlanmalı ve terapötik amaca ulaşılmasını sağlayan en düşük dozda uygulanmalıdır. Doz,önerilen maksimum dozu aşacak şekilde artırılmamalıdır. 1 / 17 İnhalasyondan 12 saat sonra FORALES, hala önemli derecede bronkodilatör etki gösterdiğinden, çoğu olguda günde iki defa uygulama şeklindeki idame tedavisi, kronikdurumlarla ilişkili gündüz ve gece görülen bronkokonstriksiyonu kontrol altına alır. Düzenli idame tedavisi için, günde iki defa 1 inhaler kapsül (12 mikrogram formoterole eşdeğer) kullanılması önerilir. Daha ciddi vakalarda günde 2 kez 2 inhaler kapsül verilir.Önerilen en yüksek idame dozu günde 48 mikrogramdır. Gerekirse belirtilerin hafifletilmesi için önerilen en yüksek günlük doz olan 48 mikrogramı aşmamak kaydıyla her gün 1-2 ilave kapsül kullanılabilir. Ancak haftada iki günden fazlailave dozlara ihtiyaç olduğu takdirde doktora danışılmalı ve tedavi yenidendeğerlendirilmelidir, çünkü bu durum hastalığın ağırlaştığının belirtisi olabilir. FORALES,astım ataklarının akut semptomlarını hafifletmek için kullanılmamalıdır. Akut atakdurumunda, kısa etkili bir beta2-agonist kullanılmalıdır (bkz. Bölüm 4.4). Çocuklar (5 yaş ve üzeri): FORALES sadece inhale bir kortikosteroide ilave olarak reçete edilmeli ve kullanılmalıdır. Düzenli idame tedavisi için, günde iki defa 1 inhaler kapsül (12 mikrogram) kullanılmasıönerilir. İnhale kortikosteroid ile uzun etkili beta2 agonistin ayrı kullanılmasının gerekli olduğu durumlar dışında 5-12 yaş arası çocuklarda, inhale kortikosteroid ile uzun etkili beta2 agonist(LABA) içeren bir kombinasyon preparatla tedavi uygulanması tavsiye edilir (bkz. Bölüm4.4. ve 4.8). Önerilen en yüksek doz günde 24 mikrogramdır. FORALES, bir astım atağının akut semptomlarını hafifletmek için kullanılmamalıdır. Akut atak durumunda, kısa etkili bir beta2-agonist kullanılmalıdır (bkz. Bölüm 4.4). FORALES, 5 yaşın altındaki çocuklarda önerilmez. Egzersizin neden olduğu bronkospazma karşı veya bilinen kaçınılamaz bir allerjen ile temastan önce profılaksi:Yetişkinler: Egzersizden veya allerjenle temastan en az 15 dakika önce 1 inhaler kapsül (12 mikrogram) inhale edilmelidir. Ciddi bronkospazm öyküsü olan hastalarda profilaktik olarak 2 inhalerkapsül (24 mikrogram) gerekli olabilir. Persistan astımı olan hastalarda, egzersizin neden olduğu bronkospazma karşı ya da bilinen kaçınılamaz bir allerjen ile temastan önce FORALES'in kullanılması klinik açıdan endikeolabilir. Ancak astım tedavisi bir inhale kortikosteroid de içermelidir. Çocuklar (5 yaş ve üzeri): Egzersizden veya allerjenlerle temastan en az 15 dakika önce 1 inhaler kapsül (12 mikrogram) inhale edilmelidir. FORALES, sadece bir inhale kortikosteroide ek olarak kullanılmalıdır. 2 / 17 Persistan astımı olan hastalarda, egzersizin neden olduğu bronkospazma karşı ya da bilinen kaçınılamaz bir allerjen ile temastan önce FORALES'in kullanılması klinik açıdan endikeolabilir. Ancak astım tedavisi bir inhale kortikosterid de içermelidir. Kronik obstrüktif akciğer hastalığı (KOAH):Düzenli idame tedavisi için, günde iki defa 1 inhaler kapsül (12 mikrogram) kullanılması önerilir. Çocuklar (5 yaş ve üzeri): Uygulama Şekli:Yetişkinlerde ve 5 yaş ve üzerindeki çocuklarda inhalasyonla kullanılır. FORALES inhalasyon tozu kapsülleri, yalnızca FORALES ambalajındaki inhaler cihaz ile kullanılmalıdır. İlacın uygun kullanımından emin olmak için doktor veya bir başka sağlık personeli: hastaya inhaler cihaz'ı nasıl kullanacağını göstermelidir, kapsüllerin sadece inhaler cihaz aracılığıyla inhalasyon yolu ile uygulanması gerektiğive yutulmaması konusunda hastayı uyarmalıdır. Kullanıma ilişkin detaylı bilgi kullanma talimatında mevcuttur. Hipromelloz kapsülün parçalanabileceğini ve küçük kapsül parçalarının inhalasyondan sonra ağız veya boğaz bölgesine ulaşabileceğini hastaların bilmesi önemlidir. Hastayakapsülün zararsız olduğu, ağızda yumuşayacağı ve yutulabildiği söylenmelidir. Kapsülübir defadan fazla delmemek suretiyle parçalanma olasılığı asgari düzeye indirilebilir.Kapsüller blister ambalajından kullanımdan hemen önceçıkarılmalıdır.İnhaler cihaz aşağıdaki bölümlerden oluşmaktadır: 1. Tabanın ağızlığını koruyan beyaz birkapak, 2. İlacın kapsülden düzgün olaraksalınmasını sağlayan bir taban, Taban kısmı aşağıdaki bileşenlerden oluşur: 3. Bir ağızlık, 4. Bir kapsül bölmesi, 5. Her bir yanda kulakçıkları (çıkıkyan taraflar) ve her bir tarafındaiğnesi olan kırmızı bir düğmesi, 6. Bir hava giriş kanalı. 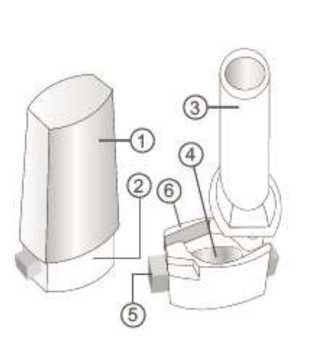 3 / 17 1. Kapağı çekip çıkarınız.
2. Kapsül bölmesini açınız. İnhalerin tabanını sıkıca tutup, açmak için ağızlığı üzerinde yer alan okişareti yönünde döndürünüz.
kuru
3. Parmaklarınızın tamamenolduğundan emin olunuz. Blisterden bir kapsül çıkarınız ve bu kapsülü cihazın tabanındaki kapsülbölmesine yatık olarak yerleştiriniz.Kapsülü, kullanımdan hemen önceambalajından çıkarınız. ÖNEMLİ: Kapsülü ağızlığın içerisine yerleştirmeyiniz!4. Tık sesini duyana kadar ağızlığıgeri döndürerek kapsül bölmesinikapayınız. 4 / 17 5. Tozu kapsülden serbestlemek için: 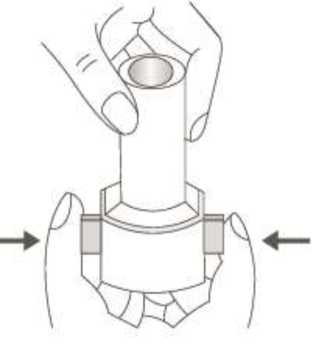 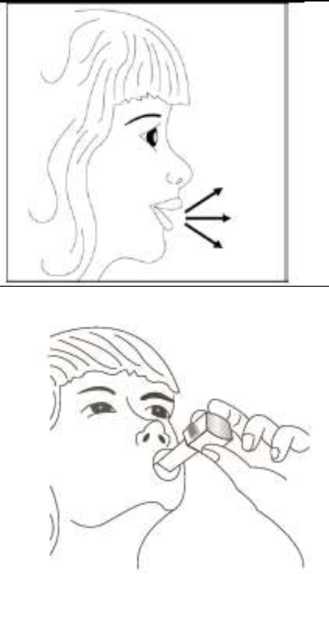 İnhaler cihazı ağızlık yukarı doğrubakacak şekilde dik olaraktutunuz. Kenarlardaki iki kulakçığa(düğmelere) aynı andasadecebir kezsıkıca basarak kapsülüdeliniz. Sonra düğmeleribırakınız.Not:değildir._6. Nefesinizi olabildiğince dışarıyaveriniz. 7. İlacı derin bir şekilde hava yollarınızaçekmek için: Ağızlığı ağzınıza yerleştiriniz vebaşınızı hafifçe geriye doğrueğiniz. Dudaklarınızla ağızlığın etrafınısıkıca sarınız. Hızlı, duraksamadan vealabildiğiniz kadar derin bir nefesalınız. Not:Kapsülün, kapsül bölmesininüzerindeki alanda dönmesine bağlı olarak bir vızıldama sesi duymalısınız. Eğer buvızıldama sesini duymazsanız, kapsülbölmesini açınız ve kapsülün, kapsülbölmesinde sıkışıp sıkışmadığını kontrolediniz. Daha sonra 7. basamağıtekrarlayınız. Kapsülü sıkıştığı yerdenkurtarmak için düğmelere tekrar tekrar BASMAYINIZ. 5 / 17 İnhaler cihaz içerisinden nefes aldıktan sonra, nefesinizi rahatsızolmayacak şekilde, tutabildiğinizkadar tutunuz ve inhaleri ağzınızdançıkarınız. Sonra burnunuzdan nefesveriniz. Kapsül bölmesini açınız vekapsülde toz kalıp kalmadığınıkontrol ediniz. Eğer kalmış ise 6-8. basamakları tekrarlayınız._Tüm tozu kullandıktan sonra kapsül bölmesini açınız (bkz. basamak 2).Boş kapsülü çıkarınız ve içeride kalantozları temizlemek için kuru bir kağıtmendil ya da yumuşak bir fırçakullanınız. 8.
9.  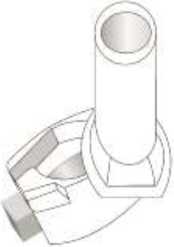 Not: İnhaler cihazı temizlemek için SU KULLANMAYINIZ.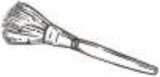 10. Önce ağızlığı, ardından kapağı kapatınız. Özel popülasyonlara ilikin ek bilgiler:Böbrek yetmezliği/ Karaciğer yetmezliği:Formoterolün karaciğer veya böbrek yetmezliği olan hastalardaki kullanımına ilişkin klinik çalışma yapılmamıştır. Ancak, FORALES'in böbrek ve karaciğer yetmezliği olan hastalardakullanımında doz ayarlaması gerektiği konusunda teorik bir sebep bulunmamaktadır. Pediyatrik popülasyon:FORALES, 5 yaşından küçük çocuklara tavsiye edilmez. Geriyatrik popülasyon:FORALES, 65 yaş ve üzerindeki hastalarda diğer yetişkinlerle aynı dozlarda kullanılabilir. 4.3. KontrendikasyonlarEtkin madde formoterole ya da içeriğindeki yardımcı maddelerden herhangi birine karşı aşırı duyarlılıkta kontrendikedir. 4.4. Özel kullanım uyarıları ve önlemleriFormoterol astımlı hastalarda tek başına monoterapi olarak kullanılmamalıdır.FORALES'in etkin maddesi formoterol, uzun etkili p2-adrenerjik agonistler sınıfına dahildir. Uzun etkili diğer bir p2-agonist olan salmeterol ile yapılan bir çalışmada, salmeterol ile tedavi 6 / 17 edilen hastalarda plasebo grubu ile karşılaştırıldığında astım nedeniyle ölüm oranının daha yüksek olduğu gözlemiştir (sırasıyla 13/13176 ve 3/13179). Astımla ilişkili ölüm oranınınFORALES ile artıp artmadığına dair yeterli çalışma yürütülmemiştir. Uzun etkili beta agonist preparatlarına bağlı olarak nadiren, ciddi ve bazen ölümcül olabilen astım ile ilgili solunum problemleri meydana gelebilir. FORALES, astım hastalığının başlangıç tedavisi için önerilmez Uzun etkili beta agonistler astım semptom kontrolünü sağlayan en kısa süre boyunca kullanılmalı ve astım kontrolüne ulaşıldığında eğer mümkünse kullanımları durdurulmalıdır.Sonrasında hastaların kontrol edici bir tedaviyle idamesi sağlanmalıdır. İnhale kortikosteroide ek olarak uzun etkili beta agonist kullanan pediatrik ve adölesan hastalarda, her iki ilaca uyumu garanti altına almak için, hem inhale kortikosteroid hem deuzun etkili beta agonist içeren bir kombinasyon preparatı kullanılması önerilir. Hastalar alevlenme dönemlerinde ise ya da önemli ölçüde veya akut olarak kötüye giden astım şikayetleri varsa, uzun etkili beta agonistlerle tedaviye başlanmamalıdır. FORALES başka bir uzun etkili beta2-agonist ile birlikte kullanılmamalıdır. Antiinflamatuvar tedavi: Astım hastalarını tedavi ederken uzun etkili bir beta2 agonist (LABA) olan FORALES, tek başına bir inhale kortikosteroid ile yeterli düzeyde kontrol edilemeyen ya da hastalığınınşiddeti bir LABA ve inhale kortikosteroidin her ikisi ile tedavinin başlatılmasını kesin olarakgerektiren hastalarda bir inhale kortikosteroide ilave tedavi olarak kullanılmalıdır. İnhale kortikosteroid ile uzun etkili beta2 agonistin ayrı kullanılmasının gerekli olduğu durumlar dışında 5-12 yaş arası çocuklarda, inhale kortikosteroid ile uzun etkili beta2 agonist(LABA) içeren bir kombinasyon preparatla tedavi uygulanması tavsiye edilir (bkz. Bölüm4.2. ve 4.8). İnhale kortikosteroide ek olarak uzun etkili beta agonist kullanan pediyatrik veadolesan hastalarda, her iki ilaca uyumu garanti altına almak için, hem inhale kortikosteroidhem de uzun etkili beta agonist içeren bir kombinasyon preparatı kullanılması önerilir. FORALES reçete edildiğinde hastalar aldıkları antiinflamatuvar tedavinin yeterliliği açısından değerlendirilmelidirler. Hastalara, FORALES almaya başladıktan sonra, belirtilerde düzelmeolduğunda bile antiinflamatuvar tedaviye değişiklik yapmaksızın devam etmeleriöğütlenmelidir. Günlük FORALES dozu, önerilen maksimum dozu aşmamalıdır. Astım semptomları kontrol altına alındıktan sonra, FORALES dozunun kademeli olarak azaltılması düşünülmelidir. Tedavinin azaltılması sırasında hastalar yakından izlenmeli veFORALES etkili en düşük dozda kullanılmalıdır. 7 / 17 Astım atakları: FORALES ile yapılan klinik çalışmalar, FORALES kullanan hastalarda (özellikle 5-12 yaş arası hastalarda) ciddi astım ataklarının sıklığının plasebo alanlara göre daha yüksek olduğunudüşündürmüştür (bkz. Bölüm 4.8). Bu çalışmalar, ciddi astım alevlenme oranları açısındantedavi grupları arasındaki farkların doğru olarak ölçülmesine imkan vermemektedir. Semptomlar devam ettiği takdirde ya da semptomların kontrol edilebilmesi için gereken FORALES dozlarının sayısı arttığı takdirde, doktorlar böyle bir gelişmenin genellikle alttayatan durumun kötüleştiğini gösteriyor olması nedeniyle kullanılan astım tedavisini yenidendeğerlendirmelidir. Astım alevlenmesi esnasında FORALES tedavisine başlanmamalı ya da doz artırılmamalıdır. Hastalar alevlenme döneminde ise ya da önemli ölçüde veya akut olarak kötüye giden astımşikayetleri varsa, uzun etkili beta agonistlerle tedaviye başlanmamalıdır. FORALES, akut astım semptomlarının rahatlatılması için kullanılmamalıdır. Akut ataklarda kısa etkili bir beta2-agonist kullanılmalıdır. Hastalar, astımları aniden kötüleştiği takdirdetıbbi tedavi almaları gerektiği konusunda bilgilendirilmelidir. Eşlik eden şartlar: FORALES kullanan hastalarda aşağıdaki durumların varlığında, özellikle doz sınırları konusunda olmak üzere, özel dikkat ve denetleme gereklidir: İskemik kalp hastalığı, kardiyakaritmiler (özellikle üçüncü derece atriyoventriküler blok), şiddetli kardiyak dekompansasyon,idiyopatik subvalvüler aortik stenoz, şiddetli hipertansiyon, anevrizma, feokromositoma,hipertrofik obstrüktif kardiyomiyopati, tirotoksikoz, QT aralığında bilinen veya şüphe edilenuzama (QTc > 0.44 saniye; bkz. Bölüm 4.5). Daha önceden kardiyak problemleri bulunan ve teofilin ile formoterol'ü bir arada kullanan hastalarda dikkatli olunmalıdır. FORALES dahil beta2 uyarıcıların hiperglisemik etkileri nedeniyle, diyabetik hastalarda FORALES tedavisi başlatıldığında kan glukoz değerlerinin izlenmesi tavsiye edilir. Hipokalemi : FORALES dahil beta2-agonist tedavisi sonucunda ciddi hipokalemi görülebilir. Hipokalemi, kardiyak aritmilere duyarlılığı artırabilir. Hipoksi ve birlikte uygulanan tedavi hipokalemiyişiddetlendirebileceğinden, şiddetli astımlı hastalarda özel bir dikkat önerilir (bkz. Bölüm 4.5).Böyle durumlarda serum potasyum düzeylerinin izlenmesi tavsiye edilir. Paradoksal bronkospazm : Diğer inhalasyon tedavilerinde olduğu gibi paradoksal bronkospazm ihtimali akılda tutulmalıdır. Böyle bir durum görüldüğünde, FORALES tedavisi derhal kesilmeli ve alternatiftedavi başlatılmalıdır. Formoterol gibi uzun etkili beta2-agonistler kullanılırken, özellikle astım ile ilgili advers olaylar bakımından, bu ilaç başlandıktan sonra ilk üç ay hastalar yakından takip edilmelidir. 8 / 17 FORALES inhaler kapsüller laktoz (inek sütü kaynaklı) içermektedir. Nadir kalıtımsal galaktoz intoleransı, Lapp laktoz yetmezliği ya da glikoz-galaktoz malabsorpsiyon problemiolan hastaların bu ilacı kullanmamaları gerekir. 4.5. Diğer tıbbi ürünler ile etkileşimler ve diğer etkileşim şekilleriDiğer beta2-agonistleri gibi FORALES de; kinidin, disopiramid, prokainamid, fenotiyazinler, antihistaminikler, makrolidler, monoamin oksidaz inhibitörleri ve trisiklik antidepresanlar gibiilaçlarla veya QTc aralığını uzattığı bilinen herhangi bir ilaçla birlikte dikkatli kullanılmalıdır.Çünkü bu ilaçlar, adrenerjik agonistlerin kardiyovasküler sistem üzerindeki etkilerinigüçlendirebilir. QTc-aralığını uzattığı bilinen ilaçlara ventriküler aritmi eşlik etme riski artar(bkz. Bölüm 4.4). Diğer sempatomimetik maddelerin birlikte verilmesi, FORALES'in istenmeyen etkilerini güçlendirebilir. Atomoksetin formoterolden kaynaklanan taşikardiyi artırabilir. Ksantin türevleri, steroidler veya diüretikler ile birlikte tedavi beta2-agonistlerin muhtemel hipokalemik etkisini kuvvetlendirebilir (bkz. Bölüm 4.4). Halojenli hidrokarbonlarla eşzamanlı anestezi alan hastalarda aritmi riski artmaktadır. Beta-adrenerjik blokerler FORALES'in etkisini zayıflatabilirler veya antagonize edebilirler. Bu yüzden FORALES, zorunlu olmadıkça, beta-adrenerjik blokerler (göz damlaları dahil) ilebirlikte verilmemelidir. Formoterol, beta-blokerlerin (beta1-selektif) bradikardik etkisini azaltabilir. Antikolinerjik ilaçlar formoterolün bronkodilatör etkisini artırabilir. Özel popülasyonlara ilikin ek bilgilerÖzel popülasyonlara ilişkin hiçbir klinik etkileşim çalışması yürütülmemiştir. Pediyatrik popülasyon:Pediyatrik popülasyona ilişkin hiçbir klinik etkileşim çalışması yürütülmemiştir. 4.6. Gebelik ve laktasyonGenel tavsiyeGebelik kategorisi: C. Çocuk doğurma potansiyeli bulunan kadınlar/Doğum kontrolü(Kontrasepsiyon)Çocuk doğurma potansiyeli bulunan kadınlar için FORALES tedavisi sırasında özel bir gereklilik bulunmamaktadır. Eğer gebelik tespit edilirse, devam eden FORALES tedavisininalternatif tedavilere karşı yarar/risk oranı değerlendirilmelidir. Gebelik dönemiFORALES, gerekli olmadıkça gebelik döneminde kullanılmamalıdır. 9 / 17 FORALES'in gebelik döneminde emniyeti henüz tespit edilmemiştir. Daha güvenli bir alternatif olduğu takdirde gebelik dönemi (özellikle hamileliğin sonunda ve doğum esnasında)süresince kullanımından kaçınılmalıdır. Diğer beta2-adrenerjik uyarıcılar gibi formoterol deuterus düz kası üzerine gevşetici etkisi nedeniyle, doğum sürecini baskılayabilir. Hayvandeneylerinde teratojenik etki görülmemiştir. Oral verildikten sonra formoterol emzirensıçanların sütünde tespit edilmiştir. Hamilelikte sadece anneye sağlayacağı yarar, fetusa olabilecek riskten daha fazlaysa kullanılmalıdır. Laktasyon dönemiFORALES'in emzirme döneminde emniyeti henüz tespit edilmemiştir. Ancak, FORALES kullanan anneler emzirmemelidir. Formoterolün insan sütüne geçip geçmediğibilinmemektedir. Etkin madde emziren sıçanların sütünde tespit edilmiştir. Üreme yeteneği/ FertiliteBölüm 5.3'e bakınız. 4.7. Araç ve makine kullanımı üzerindeki etkilerBaş dönmesi veya buna benzer yan etkiler gelişen hastalara, araç veya makine kullanmamaları önerilmelidir. 4.8. İstenmeyen etkilerCiddi astım atakları: FORALES ile uygulanan en az 4 haftalık plasebo-kontrollü klinik çalışmalar, FORALES alan hastalarda ciddi astım ataklarının sıklığının (günde iki kez 10-12 mikrogram için %0.9, gündeiki kez 24 mikrogram için %1.9) plasebo alanlardakine (%0.3) göre daha yüksek olduğunudüşündürmüştür (özellikle 5 - 12 yaş arası hastalarda). Astımlı adolesan ve yetişkin hastalardaki deneyimler: ABD'de ruhsatlandırma için yapılan ve 12 yaş ve üstü toplam 1095 hastanın katıldığı 12 haftalık iki önemli kontrollü çalışmada, ciddi astım ataklarının (astımın hastanın hastaneyeyatırılmasını gerektiren akut kötüleşmesi) günde iki kez verilen FORALES 24 mikrogramuygulamasında (9/271, %3.3) günde iki kez verilen FORALES 12 mikrogram uygulamasına(1/275, %0.4), plaseboya (2/277, %0.7) ya da albuterole (2/272, %0.7) göre daha sık ortayaçıktığı gözlenmiştir. Bu gözlemi araştırmak amacıyla daha sonra yapılan ve 2085 hastanın katıldığı bir klinik çalışmada, yüksek ve düşük doz gruplarında astımla ilgili ciddi advers olaylarkarşılaştırılmıştır. 16 hafta süren bu klinik çalışmada elde edilen sonuçlar, FORALES dozuylaaçık bir ilişki göstermemiştir. Bu çalışmada, ciddi astım ataklarının görüldüğü hastalarınyüzde oranının FORALES'de plaseboya göre biraz yüksek olduğu görülmüştür (üç çift-körtedavi grubu için: FORALES 24 mikrogram günde iki kez (2/527, %0.4), FORALES 12mikrogram günde iki kez (3/527, %0.6) ve plasebo (1/514, %0.2) ve açık-etiketli tedavi grubuiçin: FORALES 12 mikrogram günde iki keze ilave olarak ayrıca günde en fazla iki ek doz(1/517, %0.2). 10 / 17 5 yaş ve üzerindeki astımlı çocuklardaki deneyimler: Günde iki kez verilen FORALES 12 mikrogram dozun günde iki kez verilen FORALES 24 mikrogram doza ve plaseboya göre güvenliliği; günlük bronkodilatör ve antienflamatuvartedaviye ihtiyaç duyan astım hastası 518 çocuğun (5-12 yaş arasındaki) katıldığı 52 haftalık,çok merkezli, randomize, çift-kör büyük bir çalışmada araştırılmıştır. Günde iki kezFORALES 24 mikrogram (11/171, %6.4) ya da günde iki kez FORALES 12 mikrogram alan(8/171, %4.7) çocuklarda görülen ciddi astım ataklarının plasebo alan çocuklardakine (0/176,%0.0) göre daha fazla olduğu görülmüştür. Diğer istenmeyen etkiler: Advers ilaç reaksiyonları, en sık görülen advers reaksiyon ilk sırada olacak şekilde sıklıklarına göre aşağıda sıralanmıştır. Her sıklık grubunda advers reaksiyonlar azalanciddiyet derecesine göre sıralanmıştır. Advers ilaç reaksiyonları MedDRA'daki sistem organsınıflarına göre listelenmektedir. Her bir sistem organ sınıfı içinde advers ilaç reaksiyonlarıazalan ciddiyet sırasına göre sunulmaktadır: Çok yaygın (>1/10); yaygın (>1/100 ila <1/10); yaygın olmayan (>1/1.000 ila <1/100); seyrek (>1/10.000 ila <1/1000); çok seyrek (<1/10.000), bilinmiyor (eldeki verilerden hareketletahmin edilemiyor). Bağışıklık sistemi hastalıklarıÇok seyrek: Aşırı duyarlılık (hipotansiyon, ürtiker, anjiyonörotik ödem, kaşıntı, egzantem dahil). Psikiyatrik hastalıklarıYaygın olmayan: Ajitasyon, anksiyete, asabiyet, uykusuzluk. Yaygın olmayan: Baş dönmesi. Çok seyrek: Tat alma duyusu bozuklukları. Sinir sistemi hastalıklarıYaygın: Baş ağrısı, titreme. Kardiyak hastalıklarıYaygın: Palpitasyonlar. Yaygın olmayan: Taşikardi. Çok seyrek: Periferik ödem. Solunum, göğüs bozuklukları ve mediastinal hastalıkları11 / 17 Yaygın olmayan: Paradoksal bronkospazm dahil bronkospazm, boğaz irritasyonu, akut astım alevlenmesi. Gastrointestinal hastalıklarıÇok seyrek: Bulantı. Kas-iskelet bozukluklar, bağ doku ve kemik hastalıklarıYaygın olmayan: Kas krampları, miyalji. Pazarlama sonrası spontan bildirimlerden elde edilen istenmeyen etkilerFormoterol ile tedavi edilen hastalarda aşağıdaki pazarlama sonrası advers ilaç reaksiyonları bildirilmiştir. Bu reaksiyonlar büyüklüğü kesin olmayan bir popülasyondan isteğe bağlı olarakbildirilmiş olduğundan, güvenilir bir şekilde sıklığı belirlemek mümkün değildir; dolayısıylabilinmiyor olarak kategorize edilmiştir. Metabolizma ve beslenme hastalıklarıBilinmiyor: Hipokalemi, hiperglisemi. Kardiyak hastalıklarBilinmiyor: Elektrokardiyogramda QT uzaması, anjina pektoris, atriyal fibrilasyon gibi kardiyak aritmiler, ventriküler ekstrasistol, taşiaritmi. Solunum, göğüs bozuklukları ve mediastinal hastalıklarBilinmiyor: Öksürük. Deri ve deri altı doku hastalıklarıBilinmiyor: Deri döküntüsü. AraştırmalarBilinmiyor: Kan basıncında artış (hipertansiyon dahil). Şüpheli advers reaksiyonların raporlanmasıRuhsatlandırma sonrası şüpheli ilaç advers reaksiyonlarının raporlanması büyük önem taşımaktadır. Raporlama yapılması, ilacın yarar/risk dengesinin sürekli olarak izlenmesineolanak sağlar. Sağlık mesleği mensuplarının herhangi bir şüpheli advers reaksiyonu TürkiyeFarmakovijilans Merkezi (TÜFAM)'ne bildirilmeleri gerekmektedir (www.titck.gov.tr; e-posta: [email protected]; tel: 0 800 314 00 08; faks: 0 312 218 35 99). 4.9. Doz aşımı ve tedavisiBelirtiler: 12 / 17 FORALES'in aşırı dozuna bağlı olarak beta2-adrenerjik uyarıcıların tipik etkilerinin görülmesi beklenir: bulantı, kusma, baş ağrısı, tremor, sedasyon, palpitasyonlar, taşikardi,ventriküler aritmiler, metabolik asidoz, hipokalemi, hiperglisemi, hipertansiyon. Tedavi: Destekleyici ve semptomatik tedavi uygulanır. Ciddi vakalarda hastalar hastaneye yatırılmalıdır. Kardiyoselektif beta-blokerlerin kullanılması düşünülebilir, fakat beta-adrenerjik bloker kullanımı bronkospazma neden olabileceğinden bu tedavi yalnızca doktor gözetimi altında veçok dikkatli uygulanmalıdır. 5. FARMAKOLOJİK ÖZELLİKLER5.1. Farmakodinamik özelliklerFarmakoterapötik grup: Selektif beta2-adrenoreseptör agonisti ATC kodu: R03AC13 Formoterol güçlü, seçici bir beta2-adrenerjik uyarıcıdır. Geri dönüşlü soluk yolu tıkanmaları olan hastalarda bronkodilatör bir etki gösterir. Etkisi çabuk (1-3 dakika içinde) başlar veinhalasyondan 12 saat sonra hala belirgindir. Terapötik dozlarda kardiyovasküler etkileriönemsizdir ve ara sıra görülür. Formoterol, pasif olarak duyarlı hale getirilen insan akciğerlerinden lökotrienlerin ve histaminin salıverilmesini inhibe eder. Hayvanlarda yapılan deneylerde; ödemin ve iltihaphücrelerinin toplanmasının inhibisyonu gibi bazı antiinflamatuvar özellikler gözlenmiştir.Kobay trakeasındaki invitro çalışmalar; rasemik formoterolün ve bunun (R,R)- ve (S,S)-enantiomerlerinin, ileri derecede selektif beta2-adrenoseptör agonistleri olduklarınıgöstermiştir. (R,R)-enantiomerden 800-1000 kat daha az potent olan (S,S)-enantiomeri, (R-R)-enantiomerin trakea düz kası üzerindeki aktivitesini etkilemez. Enantiomerlerden herhangibirinin rasemik karışıma tercih edilmesini gerektirecek herhangi bir farmakolojik nedenyoktur.İnsanda inhale edilen alerjenlerin, egzersizin, soğuk hava, histamin veya metakolinin neden olduğu bronkospazmı önlemede FORALES'in etkili olduğu gösterilmiştir. İnhaler cihaz ile günde iki defa 12 mikrogram ve günde iki defa 24 mikrogram dozlarda inhale edilen formoterolün, stabil kronik obstrüktif akciğer hastalığı (KOAH) olan hastalardahızlı etki ile bronkodilatasyon sağladığı, etkisinin en az 12 saat sürdüğü ve Saint GeorgeSolunum Yolları Anketi sonucuna göre yaşam kalitesi açısından kişisel faydayı beraberindegetirdiği gösterilmiştir. 5.2. Farmakokinetik özelliklerGenel özelliklerFORALES'in terapötik doz aralığı günde iki kez 12-24 mikrogramdır. Formoterolün plazma farmakokinetiği verileri sağlıklı gönüllülerde önerilen doz aralığından daha yüksek dozlar veKOAH hastalarında terapötik dozların inhale edilmesi ile derlenmiştir. İdrarda saptanan ve 13 / 17 sistemik maruziyetin dolaylı bir göstergesi olarak kullanılan değişime uğramamış formoterol düzeyleriyle, plazmadaki ilaç farmakokinetiği verileri arasında korelasyon vardır. İdrar veplazma için hesaplanan eliminasyon yarı ömürleri birbirine yakındır. Emilim:Sağlıklı gönüllülerde formoterol fumaratın 120 mikrogramlık tek bir doz inhalasyonunu takiben, formoterol hızla plazmaya geçerek inhalasyonu izleyen 5 dakika içerisinde,maksimum konsantrasyon olan 266 pmol/l'ye ulaşmıştır. 12 hafta boyunca günde iki defa 12veya 24 mikrogram formoterol fumarat ile tedavi edilen KOAH hastalarında inhalasyondan10 dakika, 2 saat ve 6 saat sonraki ortalama plazma formoterol konsantrasyonları; sırasıyla11.5-25.7 ve 23.3-50.3 pmol/l arasında değişmiştir. Formoterolün ve/veya (R,R) ve (S,S) enantiomerlerinin kümülatif üriner itrahını araştıran çalışmalar, dolaşımdaki formoterol miktarının inhale edilen doz ile orantılı olarak arttığınıgöstermiştir (12- 96 mikrogram). 12 hafta süreyle günde 2 defa 12 mikrogram veya 24 mikrogram inhalasyonundan sonra idrarla atılan, değişikliğe uğramamış formoterol düzeyleri, astım hastalarında %63 ve %73(ilk dozla son doz karşılaştırıldığında), KOAH hastalarında %19 ve %38 arasında değişenoranlarda yükselmiştir. Bu veriler, tekrarlanan dozlarda kullanılan formoterolün plazmadasınırlı olarak biriktiği izlenimini vermektedir. Tekrarlayan dozlardan sonra enantiomerlerdenbirinin, diğerinden daha fazla biriktiğine tanık olunmamıştır. İnhale edilen diğer ilaçlar için bildirildiği üzere inhaler aracılığıyla kullanılan formoterol dozunun çok büyük bölümü yutulmakta ve daha sonra gastrointestinal kanaldan emilmektedir.3H ile işaretlenmiş 80 mikrogram formoterolün, iki gönüllüye oral olarak verilmesininardından dozun en az %65'i emilmiştir. Dağılım:Formoterolün plazma proteinlerine bağlanma oranı %61-64'tür. Bunun önemli bir kısmı (%34) insan serum albüminine bağlanır. Terapötik dozlar ile erişilen konsantrasyon aralığındabağlanma yerlerinde doyma olmaz. Biyotransformasyon:Formoterol başlıca metabolizma ile elimine edilir; doğrudan glukuronidasyon biyotransformasyonun ana yoludur. Glukuronidasyonun izlediği O-demetilasyon, diğer birbiyotransformasyon yoludur. Formoterolün sülfat konjügasyonu ve ardından yine sülfatkonjügasyonun gerçekleştiği deformilasyon, minör metabolik yollardır. Formoterolünglukuronidasyonunda (UGT1A1, 1A3, 1A6, 1A7, 1A8, 1A9, 1A10, 2B7 ve 2B15) ve O-demetilasyonunda (CYP2D6, 2C19, 2C9 ve 2A6) çok sayıda izoenzimin katalizör rolünüoynuyor olması; formoterol metabolizmasındaki spesifik bir izoenzimin inhibisyonuüzerinden ilaç-ilaç etkileşim potansiyelinin düşük olduğu izlenimini vermektedir. Terapötikdozlarla elde edilen konsantrasyonlardaki formoterol, sitokrom P450 izoenzimlerini inhibeetmemiştir veya indüklememiştir. Eliminasyon:12 hafta boyunca günde 2 defa 12 veya 24 mikrogram formoterol fumaratla tedavi edilen astım ve KOAH hastalarında, verilen dozun sırasıyla yaklaşık %10'u ve %7'si değişikliğeuğramamış olarak idrarda saptanmıştır. İdrardaki, değişikliğe uğramamış formoterolün; 12- 14 / 17 120 mikrogram arasında değişen tek dozların verildiği sağlıklı gönüllülerdeki ve tek ve tekrarlanan dozlar kullanan astım hastalarındaki %40'ının (R-R), %60'ının (S,S)-enantiomeriolduğu görülmüştür. İlaç ve metabolitleri vücuttan tamamen atılırlar; bir oral dozun yaklaşık 2/3'si idrarla ve 1/3'i feçesle atılır. Kandaki formoterolün renal klerensi 150 ml/dakikadır. Sağlıklı gönüllülerde 120 mikrogram tek doz formoterol fumarat inhalasyonundan sonra, idrarla atılma oranlarından hesaplanan, plazmadaki eliminasyon yarı-ömrü, formoterolde 10saat; (R,R) ve (S,S)- enantiomerlerinde ise sırasıyla 13.9 ve 12.3 saat ölçülmüştür. Doğrusallık / Doğrusal olmayan durum:Doğrusallık / doğrusal olmayan durum hakkında mevcut veri bulunmamaktadır. Hastalardaki karakteristik özelliklerKaraciğer/böbrek yetmezliği:Formoterolün karaciğer veya böbrek yetmezliği bulunan hastalardaki farmakokinetiği incelenmemiştir. Pediyatrik popülasyon:5-12 yaş grubundaki astımlı çocuklara 12 hafta boyunca inhalasyon yoluyla günde iki defa 12 veya 24 mikrogram formoterol fumarat verilerek yapılan bir çalışmada; değişimeuğramaksızın idrarla atılan formoterol miktarı, ilk dozdan sonrakine kıyasla %18 ile %84arasında değişen oranda artmıştır. Çocuklardaki birikim, erişkin hastalardakinden farklı olmamış ve %63 ile %73 arasında değişen bir oranda artmıştır (bkz. Emilim). İncelenen çocuklarda verilen formoterol dozununyaklaşık %6'sı, değişmemiş formoterol olarak idrarda bulunmuştur. Geriyatrik popülasyon:Formoterolün yaşlı hastalardaki farmakokinetiği incelenmemiştir. Cinsiyet:Formoterol farmakokinetiği, hastaların kilosuna göre düzeltildikten sonra, erkeklerle kadınlar arasında, istatistik anlama sahip fark göstermemiştir. 5.3. Klinik öncesi güvenlilik verileriMutajenisite: Deneysel bitiş noktaları geniş bir alanı kapsayan mutajenik etki testleri yapılmış; hiç bir in vitroin vivotestte genotoksik etki bulunmamıştır.Karsinojenisite: Sıçanlarda ve farelerde yapılan iki yıllık çalışmalarda, herhangi bir karsinojenik potansiyel görülmemiştir. Çok yüksek dozlarla muamele edilmiş erkek farelerde selim adrenalsubkapsüler hücre tümörleri görülme sıklığı hafifçe yüksek bulunmuştur. Ancak bu bulgu,yüksek dozlarda dişi genital organındaki selim düz kas tümörlerinin ve her iki cinsiyettegörülen karaciğer tümörlerinin görülme sıklığında artış şeklinde patolojik değişikliklerinolduğu ikinci bir fare çalışmasında görülmemiştir. 15 / 17 Çeşitli doz aralıklarında sıçanlarda yapılan iki çalışmada, mezovariyal leyomiyomlarda artış görülmüştür. Bu selim neoplazmalar sıçanların beta2-adrenerjik ilaçların yüksek dozları ileuzun süreli tedavisinde genellikle görülürler. Over kistleri ve selim granulosa/tekal hücrelitümörlerde de artış görülmüştür; beta-agonistlerin sıçanlarda overlere, çok muhtemelenkemiricilere has olan, etkileri olduğu bilinmektedir. Daha yüksek dozların kullanıldığı birinciçalışmada bildirilen diğer birkaç tip tümör, kontrol grubundakilere benzer sıklıkta görülmüşve daha düşük doz kullanılan çalışmalarda görülmemiştir. Tümör sıklıklarının hiçbiri ikinci çalışmada kullanılan en düşük doz (insanlarda formoterolün tavsiye edilen maksimum dozundan beklenenden 10 kat daha yüksek sistemik düzeye yolaçan bir doz) da istatistiksel olarak anlamlı bir dereceye yükselmemiştir. Bu bulgulara ve mutajenik potansiyelinin olmamasına dayanarak, formoterolün terapötik dozlarda kullanımının karsinojenik bir riski olmadığı hükmüne varılmıştır. 6. FARMASOTIK ÖZELLİKLER6.1. Yardımcı maddelerin listesiLaktoz monohidrat (inek sütü kaynaklı) Kapsül yapısındaki yardımcı maddeler:Hipromelloz 6.2. GeçimsizliklerBilinen geçimsizliği yoktur. 6.3. Raf ömrü24 ay 6.4. Saklamaya yönelik özel tedbirler25°C'nin altındaki oda sıcaklığında saklayınız. Nemden koruyunuz. 6.5. Ambalajın niteliği ve içeriğiBir Alu/OPA-Alu-PVC blister içinde ambalajlanır. Her karton kutu kullanma talimatı ile birlikte 60 kapsül ve 1 adet Medical cihaz içerir. 6.6. Beeri tıbbi üründen arta kalan maddelerin imhası ve diğer özel önlemlerKullanılmamış olan ürünler ya da atık materyaller Tıbbi Atıkların Kontrolü Yönetmeliği ve Ambalaj ve Ambalaj Atıklarının Kontrolü Yönetmeliğine uygun olarak imha edilmelidir. 7. RUHSAT SAHİBİWorld Medicine İlaç San. ve Tic. A.Ş. 16 / 17 Bağcılar/İstanbul 8. RUHSAT NUMARASI2018/172 9. İLK RUHSAT TARİHİ/RUHSAT YENİLEME TARİHİİlk ruhsat tarihi: 29.03.2018 Ruhsat yenileme tarihi: 10. KÜB'ÜN YENİLENME TARİHİ
17 / 17 |
İlaç BilgileriForales 12 Mcg İnhaler KapsülEtken Maddesi: Formoterol Fumarat Kullanma talimatı ve kısa ürün bilgileri
Google Reklamları
İlgili İlaçlar |
Ana Sayfa | Hakkımızda | İlaçlar | İlaç Ara | İlaç Firmaları | Gizlilik | Bize Ulaşın
Telif Hakkı 2008-2026 © İlaç Prospektüsü. Tüm Hakları Saklıdır.Uyarı: Sitemizde yayınladığımız ilaç bilgileri ile doktora danışmadan kesinlikle ilaç kullanmayınız!
Aksi halde doğabilecek sağlık sorunlarından ilacprospektusu.com sorumlu tutulamaz.