Foster 200 Mcg/6 Mcg Aerosol İnhalasyon Çözeltisi Kısa Ürün BilgisiKISA ÜRÜN BİLGİSİ1. BEŞERİ TIBBİ ÜRÜNÜN ADIFOSTER 200 mcg/6 mcg aerosol inhalasyon çözeltisi2. KALİTATİF VE KANTİTATİF BİLEŞİMEtkin maddeler:Her bir ölçülü doz;200 mikrogram (177,7 mikrogram aktarılan .....6 mikrogram (5,1 mikrogram aktarılanAnhidröz beklometazon dipropiyonat (BDP) doz)Formoterol fumarat dihidrat...................doz) içerir.Yardımcı madde:Susuz etanol......................................................8.856 mgYardımcı maddeler için 6.1'e bakınız.3. FARMASÖTİK FORMBasınçlı inhalasyon çözeltisi.Çözelti renksiz veya hafif sarımsı görünümlüdür.Kutular, ağızlığı ve kapağı olan plastik aktüatörler içerisine yerleştirilmiştir.4. KLİNİK ÖZELLİKLER4.1. Terapötik endikasyonlarUzun etkili beta 2-agonist+inhale kortikosteroid kombinasyonları ile tedavilerde olduğu üzere FOSTER, astım semptomlarının düzeltilmesi ve kontrol altına alınması amacıyla kullanılır. Astımhastalığının basamaklı tedavisinde 3. basamaktan itibaren endikedir.4.2. Pozoloji ve uygulama şekli:Pozoloji:FOSTER sadece inhalasyon yoluyla uygulanır.FOSTER astımın başlangıç tedavisi yönetimine yönelik değildir. FOSTER'in içerdiği bileşenlerin dozları farklı olduğu için ilaç, hastalığın şiddetine göre ayarlanmalıdır. Bu yalnızcasabit doz kombinasyon ilaçları ile tedaviye başlandığı zaman değil aynı zamanda, dozayarlamasının yapıldığı durumda da dikkate alınmalıdır. Eğer bir hastada kombinasyoninhalerde mevcut olan kombinasyon dozlarından daha farklı bir doz kombinasyonu gerekirse,farklı inhalerlerdeki uygun beta2-agonist ve/veya kortikosteroid dozları reçete edilmelidir.FOSTER içerisindeki beklometazon dipropiyonat ekstra ince partikül boyutu dağılımı ile tanımlanmaktadır ve bu ekstra ince partikül boyutu dağılımına sahip olmayan beklometazondipropiyonata göre daha güçlü etki göstermektedir (FOSTER içerisindeki 100 mikrogramekstra ince beklometzon dipropiyonat, 250 mikrogram ekstra ince olmayan beklometazondipropiyonata eşdeğerdir). Bu nedenle, FOSTER için günlük uygulanan beklometazondipropiyonat miktarı, ekstra ince olmayan beklometazon dipropiyonatın günlük toplammiktarından düşük olmalıdır.Hastaların daha önce almakta olduğu tedavi değiştirildiğinde, FOSTER için önerilen günlük toplam beklometazon dipropiyonat dozunun beklometazon dipropiyonat içeren ve ekstra inceolmayan mevcut ürün için verilen dozun altında olmasına ve dozun her bir hastanın ihtiyacınagöre ayarlanmasına dikkat edilmelidir.Uygulama sıklığı ve süresi:18 yaş ve üstü erişkinler için doz önerileri Astım:Günde iki kez iki inhalasyon halinde uygulanır.Maksimum günlük doz dört inhalasyondur.200 mcg beklometazon dipropiyonat ve 6 mcg formoterol fumarat içeren FOSTER yalnızca idame tedavisi için kullanılır. İdame tedavisi ve rahatlatıcı tedavi için daha düşük bir yitilik (100mcg beklometazon/6 mcg formoterol kombinasyonu) mevcuttur.Ayrı bir hızlı etkili bronkodilatör kullanım gerekliliği her zaman göz önünde bulundurulmalıdır.Dozajın uygun bir şekilde devam etmesi için hastalar düzenli olarak bir doktor tarafından değerlendirilmeli ve doz sadece tıbbi öneriye göre değiştirilmelidir. Tedavi dozu,semptomların etkili biçimde kontrol altına alındığı en düşük doza düşürülmelidir. Semptomlaren düşük dozla kontrol altına alındığında bir sonraki adım, tek başına inhale edilenkortikosteroidin testini içermelidir.FOSTER doz azaltma tedavisinde kullanılmamalıdır ancak, aynı inhaler içerisinde beklometazon dipropiyonat içeriğinin daha düşük olduğu bir yitilik, doz azaltma tedavisinde kullanılabilmeküzere mevcuttur (100 mcg beklometazon/6 mcg formoterol kombinasyonu).Hastalara asemptomatik olduklarında dahi FOSTER'i hergün almaları konusunda bilgi verilmelidir.Uygulama şekli:FOSTER inhalasyon yolu ile kullanılır.İlacın uygun kullanılması için, hastaya zaman zaman bir doktor veya başka sağlık personeli tarafından inhalerin nasıl kullanılacağı gösterilmelidir. Tedavinin başarılı olması için basınçlıölçülü doz inhalerin doğru kullanılması gerekir. Hastalara Kullanma Talimatını dikkatli birşekilde okumaları ve kullanma talimatlarına uymaları tavsiye edilmelidir. FOSTER'ın doğru birşekilde kullanılmasına yönelik açıklamalar kolaylık olması bakımından kullanma talimatları,Bölüm 6.6'da bulunmaktadır.İnhalasyon esnasında hasta mümkün ise oturmalı ya da ayakta dik durmalıdır.Özel popülasyonlara ilişkin ek bilgiler:Böbrek/ Karaciğer yetmezliği:FOSTER kullanımına ilişkin veri bulunmamaktadır. (bakınız bölüm 5.2).Pediyatrik popülasyon:FOSTER çocuklar ve 18 yaşın altındaki ergenlerde kullanılmamalıdr.Geriyatrik popülasyon:Yaşlılarda doz ayarlanması gerekli değildir.4.3. KontrendikasyonlarBeklometazon dipropiyonat, formoterol fumarat dihidrat ve/veya ürün içeriğindeki maddelerden herhangi birine karşı bilinen aşırı duyarlılık halinde FOSTER kontrendikedir.4.4. Özel kullanım uyarıları ve önlemleriFOSTER kardiyak aritmi, özellikle üçüncü derece atriyoventriküler blok ve taşiaritmiler, idiyopatik subvalvular aortik stenoz, hipertrofik obstrüktif kardiyomiyopati, iskemik kalphastalığı, ağır kalp yetersizliği, miyokart enfarktüsü, oklüzif vasküler hastalık, arterioskleroz,şiddetli arteriyel hipertansiyon ve anevrizma geçirmiş hastalarda dikkatle kullanılmalı, hastamonitorize edilmelidir.Konjenital veya ilaçla indüklenen, bilinen veya şüpheli QTc aralığı uzaması (QTc > 0,44 saniye) izlenen hastalar tedavi edilirken dikkatli olunmalıdır. Formoterol, QTc aralığının uzamasınıindükleyebilir.FOSTER tirotoksikoz, feokromositoma ve tedavi edilmemiş hipokalemi hastalarında dikkatle kullanılmalıdır.Beta2-agonist tedavisi potansiyel olarak ciddi hipokalemiye neden olabilir. Bu etki hipoksiyi potansiyalize edebileceği için şiddetli astım tedavisinde özel dikkat gösterilmesi önerilmektedir.Hipokalemi ayrıca, hipokalemiyi indükleyen ksantin türevleri, stereoid ve diüretik gibi ilaçlar ileeş zamanlı tedavi uygulaması ile de potansiyalize edilebilmektedir (bakınız bölüm 4.5).Rahatlatıcı bronkodilatörlerin kullanılabildiği kararsız astımda da özel dikkat gerekmektedir. Bugibi durumlarda serum potasyum düzeylerinin monitorize edilmesi önerilmektedir.Yüksek dozda formoterol inhalasyonu kan şekeri düzeyinde artışa neden olabilir. Bu nedenle diyabetiklerde bu parametre yakından izlenmelidir.Halojenli anestezikler ile anestezi planlandığında, kardiyak aritmi riski nedeniyle anestezi başlamadan en az 12 saat öncesinde FOSTER kullanılmadığından emin olunması gereklidir.Kortikosteroid içeren tüm inhale ilaçlar gibi FOSTER de aktif veya latent pulmoner tüberkülozu olan ve solunum yollarında fungal ve viral enfeksiyonları olan hastalarda dikkatliolarak uygulanmalıdır.FOSTER'in ani olarak kesilmemesi önerilmektedir.Hasta tedaviyi etkisiz buluyorsa tıbbi olarak dikkat gösterilmelidir. Kısa etkili rahatlatıcı bronkodilatörlerin kullanımındaki artış, hastalığın kötüleştiğini gösterir ve astım tedavisininyeniden değerlendirilmesini gerektirir. Astım kontrolündeki ani ve artan seyirdeki kötüleşmepotansiyel olarak yaşamı tehdit edicidir ve tedavi modifikasyonu için hasta acil tıbbideğerlendirmeden geçmelidir. Oral ya da inhale kortikosteroid tedavisine ihtiyacın artmasıdurumunda dikkat gösterilmelidir veya enfeksiyon şüphesi var ise antibiyotik tedavisibaşlanmalıdır.Alevlenme durumunda veya belirgin şekilde kötüleşmiş akut astım atakları var olan hastalarda FOSTER ile tedaviye başlanmamalıdır. Eğer astım semptomları düzelmez veya FOSTER iletedaviye başladıktan sonra kötüleşir ise hastalar tedavilerine devam etmeli ancak tıbbi yardım almaları konusunda uyarılmalıdır.Diğer inhalasyon tedavilerinde olduğu gibi doz uygulaması sonrasında hırıltılı solunum (wheezing), öksürük ve nefes darlığında ani bir artışla beraber paradoksal bronkospazmgelişebilir. Bu durumda FOSTER kullanımı derhal kesilmelidir, hasta tekrar değerlendirilmelive gerekli ise alternatif tedavi uygulanmalıdır.FOSTER astımın ilk tedavisi olarak kullanılmamalıdır.Akut astım ataklarının tedavisi için hastaların FOSTER'i ve/veya hızlı etkili bronkodilatörlerini sürekli yanlarında bulundurmaları önerilir.Asemptomatik durumlarda da reçete edildiği üzere hastanın FOSTER'i düzenli olarak her gün alması önerilir.Astım semptomları bir kez kontrol altına alındıktan sonra FOSTER dozunun zamanla azaltılması göz önünde bulundurulmalıdır. Tedavide hastaların düzenli kontrolü önemlidir. Kontrol altınaalınan astımda FOSTER'ın minimum etkili dozu kullanılmalıdır (bakınız bölüm 4.2).KOAH hastalarında pnömoniKortikosteroid içeren inhale ilaçları alan KOAH hastalarında, hastaneye yatış gerektiren pnömoni dahil, pnömoni insidansında artış gözlemlenmiştir. Artan steroid dozu ile pnömoni riskinde artışkanıtları bulunmaktadır, ancak bu durum çalışmaların tamamında kesin olarak gösterilmemiştir.Kortikosteroid içeren inhale ilaçlar arasında pnömoni riskinin büyüklüğü konusunda sınıf içi farklılık bakımından kesin klinik kanıt bulunmamaktadır.Hekimler, KOAH hastalarında olası pnömoni gelişimine karşı, enfeksiyonların klinik özellikleri ile KOAH semptomlarının alevlenme durumunun karışması ihtimali dolayısıyla dikkatliolmalıdır.KOAH hastalarındaki pnömoni risk faktörleri arasında; sigara içilmesi, ileri yaş, düşük vücut kitle indeksi ve ağır KOAH bulunmaktadır.İnhale kortikosteroidler, özellikle uzun süreli ve yüksek dozlarda reçete edildiklerinde sistemik etkiler oluşturabilirler. Bu etkilerin görülme olasılığı oral kortikosteroidlere nazaran inhalekortikosteroidler ile çok daha düşüktür. Olası sistemik etkiler şunlardır: Cushing sendromu,adrenal baskılanma, kemik mineral yoğunluğunda azalma, çocuk ve ergenlerde büyümegeriliği, katarakt ve glokom ve daha seyrek olarak fizikomotor hiperaktivitesi, uyku bozukluğu,anksiyete, depresyon veya saldırganlık (özellikle çocuklarda) da içeren çeşitli psikolojik vedavranışsal etkiler.Bu nedenle, tedavi altındaki hastanın düzenli olarak kontrolü ve inhale kortikosteroid dozunun, astımın etkin olarak kontrolünün sağlandığı en düşük doza düşürülmesi önemlidir.Tek doz farmakokinetik verileri (bakınız bölüm 5.2), FOSTER'in Aerochamber Plus® spacer cihazı ile kullanımının standart aktüatöre göre, formoterolün toplam sistemik maruziyetiniarttırmadığını, beklometazon-17-monopropiy onatın sistemik maruziy etini azalttığını veakciğerdeki sistemik dolaşıma ulaşan değişmemiş beklometazon dipropiyonatı arttırdığınıgöstermektedir. Bununla beraber, beklometazon dipropiyonat ve aktif metabolitinin sistemikmaruziyeti değişmediğinden, FOSTER'i bu cihaz ile kullanmak sistemik etki riskini arttırmaz.İnhale kortikosteroidler ile yüksek dozlarda uzun süreli tedavi, adrenal baskılanma ve akut adrenal krize neden olabilir. Önerilenden yüksek doz beklometazon dipropiyonat inhale eden 16yaşından küçük çocuklar risk altında olabilirler. Akut adrenal krizi tetikleyebilecek potansiyeldurumlar travma, ameliyat, ciddi enfeksiyon ve dozun hızla azaltılmasıdır. Oluşan semptomlarçok belirgin olmamakla beraber iştahsızlık, karın ağrısı, kilo kaybı, yorgunluk, baş ağrısı,bulantı, kusma, hipotansiyon, bilinç düzeyinde azalma, hipoglisemi ve/veya konvülsiyonlarıiçerebilir. Stres ve elektif cerrahi sırasında ilave sistemik kortikosteroid verilmesi düşünülmelidir.Özellikle daha önceki sistemik steroid tedavisi nedeni ile adrenal fonksiyonun bozulmuş olduğu düşünülüyorsa, bu grup hastalar FOSTER tedavisine geçirilirken dikkatli olunmalıdır.Oral kortikosteroidlerden inhale steroidlere geçen hastalar oldukça uzun bir zaman adrenal rezerv eksikliği riski altında kalırlar. Geçmişte, yüksek doz acil kortikosteroid tedavisi gerekliolmuş hastalar da risk altında olabilirler. Bu bozukluk olasılığı strese neden olabilecek acil veelektif durumlarda daima akılda bulundurulmalıdır ve uygun kortikosteroid tedavisiuygulanmalıdır. Adrenal bozukluğunun derecesi elektif işlemlerden önce uzman tavsiyesinigerektirebilir.Orofarengeal kandida enfeksiyonu riskini en aza indirmek için reçete edilen dozu kullandıktan sonra hastaların ağızlarını su ile çalkalamaları veya dişlerini fırçalamaları önerilmelidir.Sistemik ve topikal kortikosteroid kullanımına bağlı görme bozuklukları bildirilebilir. Eğer hastada bulanık görme veya diğer görme bozuklukları meydana gelirse hasta; katarakt, glokomveya sistemik ve topikal kortikosteroid kullanımdan sonra bildirilen santral seröz korioretinopati(SSKR) gibi nadir hastalıkları da içerebilen olası nedenleri değerlendirmek üzere bir gözdoktoruna yönlendirilmelidir.FOSTER az miktarda susuz etanol (alkol) içerir (puf başına 100 mg'den az). Normal dozlarda etanol miktarı ihmal edilebilirdir ve hastalar için risk oluşturmaz.4.5. Diğer tıbbi ürünler ile etkileşimler ve diğer etkileşim şekilleriFarmakokinetik etkileşimlerBeklometazon dipropiyonat esteraz enzimleri yoluyla hızla metabolize olur.Beklometazon diğer bazı kortikosteroidlere göre CYP3A metabolizmasına daha az bağımlıdır ve genel olarak etkileşimler olası değildir; ancak güçlü CYP3A inhibitörlerinin (örneğin ritonavir,kobisistat) birlikte kullanımı ile sistemik etkilerin olma ihtimali göz ardı edilemez ve bu nedenlebu tür ajanlar kullanılması durumunda dikkatli olunması ve hastanın uygun bir şekildegözlemlenmesi önerilir.Farmakodinamik etkileşimlerBeta-adrenerjik blokerler formoterolün etkisini azaltabilir ya da ortadan kaldırabilir. Bu nedenle FOSTER zorunlu olmadıkça, beta-adrenerjik blokerler (göz damlası dahil) ile birlikteverilmemelidir.Diğer yandan beta-adrenerjik ilaçların eş zamanlı kullanımının olası ilave etkileri olabilir, bu nedenle formoterol ile eş zamanlı olarak teofilin ya da diğer beta-adrenerjik ilaçlarınreçetelenmesi dikkat gerektirir.Kinidin, disopramid, prokainamid, fenotiyazinler, antihistaminikler, mono amino oksidaz inhibitörleri ve trisiklik antidepresanlar ile yapılan eş zamanlı tedavi, QTc-aralığını uzatarakventriküler aritmi riskini arttırabilir.Ayrıca, L-Dopa, L-tiroksin, oksitosin ve alkol, beta2sempatomimetiklere karşı kardiyak tolerans azalabilir.Furazolidon ve prokarbazin gibi benzer özellikler gösteren mono amino oksidaz inhibitörleri ile eş zamanlı tedavi hipertansif reaksiyonları başlatabilir.Halojenli hidrokarbonlar ile eş zamanlı anestezi alan hastalarda aritmi riski artabilir.Ksantin türevleri, steroidler veya diüretikler ile eş zamanlı tedavi beta2agonistlerinin olası hipokalemik etkilerini güçlendirebilir (bakınız bölüm 4.4). Hipokalemi, dijital glikozitlerle tedavialtında olan hastalarda aritmiye olan yatkınlığı arttırabilir.Disülfiram veya metronidazol kullanan duyarlı hastalarda FOSTER içeriğindeki düşük düzeydeki alkol etkileşime neden olabilir.Özel popülasyonlara ilişkin ek bilgiler:Böbrek/Karaciğer yetmezliği halinde FOSTER ile yapılmışetkileşimçalışmasıbulunmamaktadır.Pediyatrik popülasyon:18 yaşın altındaki astım ve KOAH hastalarında FOSTER ile yapılmış etkileşim çalışması bulunmamaktadır.4.6. Gebelik ve laktasyonGenel tavsiyeGebelik kategorisi CÇocuk doğurma potansiyeli bulunan kadınlar/Doğum kontrolü (Kontrasepsiyon):FOSTER'ın çocuk doğurma potansiyeli olan kadınlarda ve doğum kontrolünde kullanımına ilişkin yeterli veri bulunmamaktadır.Gebelik dönemiİtici gaz HFA-134a'nın gebe veya emziren kadınlarda kullanımına veya güvenliliğine ilişkin yeterli veri mevcut değildir. Bununla beraber, HFA-134a'nın üreme işlevi ve embriyofötalgelişim üzerine hayvanlarda gerçekleştirilen çalışmalar, klinik olarak advers etkisi olmadığınıortaya koymuştur.Gebe kadınlarda FOSTER kullanımına ilişkin yeterli klinik veri mevcut değildir. Beklometazon dipropiyonat ve formoterol kombinasyonunun kullanıldığı hayvan çalışmaları yüksek sistemikmaruziyet sonrasında üreme üzerine toksisite bulunduğuna dair kanıtlar göstermiştir (bakınız.bölüm 5.3). Beta2-sempatomimetik ajanların tokolitik etkisinden dolayı doğumun yaklaşmasındagerekli önlemler alınmalıdır. Başka bir yerleşik alternatif (daha güvenli) tedavi bulunmadıkçaformoterol gebelik süresince ve özellikle gebeliğin sonlarında ya da doğum esnasındakullanılmamalıdır.FOSTER gebelik sırasında ancak beklenen yararlar potansiyel risklerden fazla olduğunda kullanılmalıdır.Laktasyon dönemiİnsanlarda laktasyon döneminde FOSTER kullanımına ilişkin yeterli klinik veri mevcut değildir.Hayvan deneylerinde veri elde edilememiş olmasına karşın, beklometazon dipropiyonatın diğer kortikosteroidler gibi anne sütüne geçtiği varsayılabilir.Formoterol'ün anne sütüne geçip geçmediğinin bilinmemesine karşın, hayvanların sütünde saptanmıştır.Bu nedenle, emziren kadınlarda FOSTER yalnızca anne için beklenen yarar, çocuk için söz konusu olası riskten daha fazla ise uygulanmalıdır.Çocuk için emzirmenin ve anne için tedavinin faydası dikkate alınarak, emzirmenin veya FOSTER ile tedavinin kesilip kesilmemesi konusunda bir karar verilmelidir.Üreme yeteneği / Fertiliteİnsanlarda veri mevcut değildir. Sıçanlardaki üreme çalışmaları, kombinasyondaki yüksek dozdaki beklometazon, dişilerde üreme yeteneğinin azalması ve embriyotoksisite ileilişkilendirilmiştir (bakınız bölüm 5.3).4.7. Araç ve makine kullanımı üzerindeki etkilerFOSTER'in araç ve makine kullanma yeteneği üzerinde etkisi yoktur.4.8. İstenmeyen etkilerFOSTER, beklometazon dipropiyonat ve formoterol fumarat dihidrat içerdiği için, her bir bileşik ile ilişkili türden ve şiddette advers reaksiyonların olması beklenir. Her iki bileşiğinbirlikte uygulanmasını takiben ek advers etki artışı gözlemlenmemiştirSabit kombinasyon olarak uygulanan beklometazon dipropiyonat ve formoterol fumarat ile ilişkili istenmeyen etkiler aşağıda verilmiştir ve sistematik olarak organ sınıfına göre ve sıklığagöre gösterilmiştir.Klinik çalışmalardan elde edilen istenmeyen etki görülme oranları şu şekilde tanımlanmıştır: Çok yaygın (>1/10); yaygın (>1/100 ve <1/10); yaygın olmayan (>1/1,000 ila <1/100); seyrek(>1/10,000 ila <1/1,000); çok seyrek (<1/10,000); bilinmiyor (mevcut verilerden tahminedilemiyor).Yaygın ve yaygın olmayan advers ilaç reaksiyonları, astım ve KOAH hastalarında yapılan klinik çalışmalardan elde edilmiştir.Enfeksiyonlar ve enfestasyonlarYaygın : Farenjit, oral kandidiaz, pnömoni (KOAH'lı hastalarda)*Yaygın olmayan : Grip, oral mantar enfeksiyonu, orofarengeal ve özofagalkandidiaz, vajinal kandidiaz, gastroenterit, sinüzit, rinitKan ve lenf sistemi hastalıklarıYaygın olmayan : GranülositopeniÇok seyrek : TrombositopeniBağışıklık sistemi hastalıkları
Metabolizma ve beslenme hastalıklarıYaygın olmayan : Hipokalemi, hiperglisemiPsikiyatrik hastalıklarYaygın olmayan : Yerinde duramamaBilinmiyor : Psikomotor hiperaktivite, uyku bozuklukları, anksiyete, depresyon,saldırganlık, davranış değişiklikleri (genellikle çocuklarda)
Kulak ve iç kulak hastalıklarıYaygın olmayan : Otosalpenjit
Gastrointestinal hastalıklarıYaygın olmayan : İshal, ağız kuruluğu, dispepsi, disfaji, dudaklarda yanma hissi, bulantı,tat alma bozukluğuDeri ve deri altı doku hastalıklarıYaygın olmayan : Kaşıntı, döküntü, hiperhidroz, ürtikerSeyrek : AnjiyoödemKas-iskelet bozuklukları, bağ doku ve kemik hastalıklarıYaygın olmayan : Kas krampı, miyaljiÇok seyrek : Çocuk ve adolesanlarda büyüme geriliğiBöbrek ve idrar yolu hastalıklarıSeyrek : NefritGenel bozukluklar ve uygulama bölgesine ilişkin hastalıklarÇok seyrek: Periferik ödemAraştırmalarYaygın olmayanSeyrek Çok seyrek: C-reaktif proteinde artış, trombosit sayısında artma, serbest yağ asidinde artma, kan insülininde artış, kan keton cisimlerinde artış, kankortizolünde azalma*: Kan basıncında artma veya azalma : Kemik yoğunluğunda azalma* 100 mcg beklometazon/6 mcg formoterol kombinasyonu ile tedavi edilen KOAH hastalarında gerçekleştirilen bir pivotal çalışmadaki bir hastada ciddi olmayan pnömoni olgusu bildirilmiştir.KOAH klinik çalışmalarında 100 mcg beklometazon/6 mcg formoterol kombinasyonu içingözlenen diğer advers reaksiyonlar: kan kortizolünde azalma ve atriyal fibrilasyon.Diğer inhalasyon tedavilerinde de görüldüğü gibi paradoksal bronkospazm oluşabilir (bakınız bölüm 4.4.).Formoterol ile tipik olarak ilişkili gözlemlenen advers olaylar şunlardır: hipokalemi, baş ağrısı, tremor, çarpıntılar, öksürük, kas krampları ve QTc aralığı uzaması.Beklometazon ile tipik olarak ilişkili gözlemlenen advers olaylar şunlardır: oral mantar enfeksiyonları, oral kandidiaz, disfoni, boğazda tahriş.Disfoni ve kandidiyazisi azaltmak için, ürün kullanıldıktan sonra gargara veya su ile ağız yıkanabilir veya dişler fırçalanabilir. FOSTER tedavisi devam ederken ortaya çıkan semptomatikkandidiyazis, topikal anti fungal terapisi ile tedavi edilebilir.İnhale kortikosteroidlerin (örn., beklometazon dipropiyonat) sistemik etkileri özellikle uzun süreli olarak yüksek dozda uygulandığında ortaya çıkabilir. Bu etkiler şunlardır: adrenalbaskılanma, kemik mineral yoğunluğunda azalma, çocuklarda ve ergenlerde büyüme geriliği,glokom ve katarakt (bakınız bölüm 4.4).Aşırı duyarlılık reaksiyonları arasında döküntü, ürtiker şeklinde kaşıntı, eritem, göz, yüz, dudaklarda ve boğazda ödem vardır.Şüpheli advers reaksiyonların raporlanmasıRuhsatlandırma sonrası şüpheli ilaç advers reaksiyonlarının raporlanması büyük önem taşımaktadır. Raporlama yapılması, ilacın yarar / risk dengesinin sürekli olarak izlenmesineolanak sağlar. Sağlık mesleği mensuplarının herhangi bir şüpheli advers reaksiyonu TürkiyeFarmakovijilans Merkezi (TÜFAM)'ne bildirmeleri gerekmektedir.(www.titck.gov.tr;eposta;[email protected]; tel:0 800 314 00 08; faks:0 312 218 35 99)4.9. Doz aşımı ve tedavisiPeş peşe 12 kümülatif uygulamaya kadar inhale 100 mcg beklometazon/6 mcg formoterol kombinasyonu dozları (toplam 1200 mikrogram beklometazon dipropiyonat ve 72 mikrogramformoterol) astımlı hastalarda incelenmiştir. Kümülatif tedavi, vital bulgularda anormal bir etki göstermemiştir ve ciddi veya şiddetli advers olaylar da gözlemlenmemiştir.Aşırı formoterol dozları beta-2-adrenerjik agonistler için tipik olan etkilere yol açabilir: bulantı, kusma, baş ağrısı, tremor, uyku hali, çarpıntılar, taşikardi, ventrikül aritmileri, QTc aralığınınuzaması, metabolik asidoz, hipokalemi, hiperglisemi.Formoterol ile doz aşımı durumunda, destekleyici ve semptomatik tedavi endikedir. Ciddi vakalar hastaneye yatırılmalıdır. Kardiyoselektif beta-adrenerjik blokörlerin kullanılmasıdüşünülebilir ancak çok dikkatli olarak uygulanmalıdır, çünkü beta-adrenerjik blokör kullanımıbronkospazma yol açabilir. Hastanın serum potasyumu izlenmelidir.Önerilenden fazla akut beklometazon dipropiyonat dozları inhalasyonu, adrenal fonksiyonun geçici olarak baskılanmasına neden olabilir. Bu acil önlem gerektirmez, çünkü, plazma kortizolölçümleri ile doğrulandığı üzere, baskılanma birkaç gün içinde ortadan kalkar. Bu hastalardatedavi, astımı kontrol etmeye yetecek dozlarda sürdürülmelidir.Kronik alımlı fazla beklometazon dipropiyonat dozları inhalasyonu: adrenal baskılanma riski (bakınız bölüm 4.4). Adrenal rezervinin monitorizasyonu gerekli olabilir. Bu grup hastalarda datedavi, astımın kontrol altına alınabildiği en uygun dozda sürdürülmelidir.5- FARMAKOLOJİK ÖZELLİKLER 5.1 Farmakodinamik özelliklerFarmakoterapötik grup:Obstrüktif hava yolu hastalıkları için kullanılan ilaçlar; Adrenerjikler, inhalanlarATC Kodu:R03AK08Etki mekanizması ve farmakodinamik etkiler:FOSTER beklometazon dipropiyonat ve formoterol içermektedir; bunların farklı etki mekanizmaları vardır. Diğer inhale kortikosteroidler ve beta2-agonist kombinasyonları gibi,astım alevlenmelerini azaltmak bakımından ilave etkileri görülür.Beklometazon dipropiyonatİnhalasyon yolu ile önerilen dozlarda verilen beklometazon dipropiyonatın akciğerlerde glukortikoidlere bağlı antiinflamatuvar etkisi vardır ve bu etki astım belirtileri vealevlenmelerinde azalma sağlamakla birlikte sistemik uygulanan kortikosteroidlere nazarandaha az advers etkiye neden olur.FormoterolFormoterol selektif bir beta2-adrenerjik agonisttir ve reversibl solunum yolu obstrüksiyonu olan hastalarda bronş düz kaslarının gevşemesini sağlar. Bronş genişletici etkisi hızla,inhalasyondan 1-3 dakika sonra etkisini gösterir ve tek bir dozun etki süresi 12 saattir.Beklometazon/formoterol kombinasyonunun idame tedavide klinik etkililiği ve güvenliliği 1701 astım hastasının dahil edildiği 48 haftalık paralel grup çalışmasında; astımı kontrol altındaolmayan orta veya ağır astımlı yetişkin hastalarda 100 mcg beklometazon/6 mcg formoterolfumarat kombinasyonunun idame dozu (günde iki kez bir inhalasyon) ve rahatlatıcı (gündetoplam 8 pufa kadar) tedavi olarak uygulaması, idame uygulaması (günde iki kez bir inhalasyon)artı ihtiyaç duyulduğunda salbutamol kullanımı ile karşılaştırılmıştır. Sonuçlar; idame verahatlatıcı tedavi olarak uygulanan 100 mcg beklometazon/6 mcg formoterol fumaratkombinasyonunun, idame artı ihtiyaç duyulduğunda salbutamol kullanan gruba göre (ITT ve PPpopülasyonlarını her ikisi için p<0.001) ilk ciddi alevlenme süresini belirgin şekilde uzattığınıgöstermiştir. İdame ve rahatlatıcı tedavi grubunda ciddi astım alevlenmelerinin oranı, salbutamolgrubuna kıyasla (hasta/yıl başına) belirgin şekilde azalmıştır (sırasıyla 0,1476 ve 0,2239istatistiksel olarak belirgin düşüş: p<0.001). 100 mcg beklometazon/6 mcg formoterol fumaratkombinasyonu verilen idame ve rahatlatıcı tedavi grubundaki hastalar, astım kontrolünde klinikolarak anlamlı başarı kaydetmişlerdir. Rahatlatıcı tedavinin ortalama inhalasyon sayısı verahatlatıcı tedavi uygulanan hasta sayısı her iki grupta da benzer şekilde azalmıştır.Not: Ciddi alevlenmeler, hastaneye yatış ile sonuçlanan astımda kötüleşme veya acil tedavi veya sistemik steroid ihtiyacında 3 günden fazla artış olarak tanımlanmıştır.Diğer bir klinik çalışmada, astımlı hastalarda metakolin ile bronkokonstriksiyon geliştirilmiş ve 100 mcg beklometazon/6 mcg formoterol fumarat kombinasyonunun tek dozu ile (100/6 mcg)bronkodilatasyon sağlanması, salbutamol 200 mcg ile karşılaştırılmıştır. 100 mcgbeklometazon/6 mcg formoterol fumarat kombinasyonu tek doz ile, 200 mcg salbutamole benzerşekilde hızlı bronkodilatasyon ve dispne semptomlarında hızlı iyileşme sağlamıştır.Günde iki kez 2 puf verilen 200 mcg beklometazon/6 mcg formoterol kombinasyonu HFA'nın etkililiği, daha önceki tedavi ile (yüksek dozda İKS veya orta dozda İKS+LABAkombinasyonları) yeterince kontrol altına alınamayan astım hastalarında akciğer işlevlerininkarşılaştırıldığı 12 haftalık pivotal bir çalışmada değerlendirilmiştir. Çalışma, 200 mcgbeklometazon/6 mcg formoterol kombinasyonu HFA'nın ortalama doz öncesi sabah PEFdeğerinde başlangıca göre elde edilen değişiklik bakımından beklometazon dipropiyonat HFA'yagöre üstünlüğünü göstermiştir (ayarlanan ortalama fark 18.53 L).24 haftalık bir pivotal çalışmada, günde iki defa 2 puf 200 mcg beklometazon/6 mcg formoterol kombinasyonu HFA güvenlilik profili, onaylanmış bir sabit doz kombinasyonuyla(flutikazon/salmeterol 500/50, günde iki kez 1 puf) karşılaştırılabilir düzeydedir. 6 aylıktedaviden sonra HPA ekseni üzerinde 200 mcg beklometazon/6 mcg formoterol kombinasyonuHFA ile herhangi bir klinik etki gözlenmedi. Çalışma, 200 mcg beklometazon/6 mcg formoterolkombinasyonunun ve onaylanmış sabit doz kombinasyonunun, doz öncesi sabah FEVfdekideğişiklik ve astım semptomları olmadan tam gün yüzdesinde ekstra ince olmayan beklometazondipropionat monoterapisinden (2000 gg/gün) üstün olmadığını göstermiştir.5.1. Farmakokinetik özelliklerGenel özellikler200 mcg beklometazon/6 mcg formoterol kombinasyonunun sistemik etkileri, içeriğindeki aktif maddeler olan beklometazon dipropiyonat (BDP) ve formoterol'ün sistemik etkileri ile klinikçalışmada karşılaştırılmıştır.Sağlıklı gönüllülere tek bir doz 100 mcg beklometazon/6 mcg formoterol içeren sabit doz kombinasyonu (4 puf) veya tek bir doz beklometazon dipropiyonat CFC (4 puf/250 mikrogram)ve formoterol HFA (4 puf 6 mikrogram) verilen bir farmakokinetik çalışmada, beklometazondipropiyonat aktif metaboliti (beklometazon-17-monopropiyonat) ve maksimal plazmakonsantrasyonunun Eğri Altındaki Alanı (EAA), sabit kombinasyon için ekstra ince olmayanbeklometazon dipropiyonat CFC formülasyonuna göre sırasıyla %35 ve %19 daha düşüktür, bunakarşın emilim hızı ), sabit kombinasyon için ekstra ince olmayan beklometazon dipropiyonat CFCformülasyonuna göre daha hızlıdır (0.5'e karşın 2 saat).Formoterol için maksimum plazma konsantrasyonu sabit veya serbest kombinasyon uygulamalarından sonra benzer bulunmuştur ve 200 mcg beklometazon/6 mcg formoterolkombinasyonu ile sistemik etki, serbest kombinasyona göre biraz daha yüksek bulunmuştur.Beklometazon dipropiyonat ve formoterol arasında farmakokinetik veya farmakodinamik (sistemik) etkileşim gözlemlenmemiştir.Aktif kömür blokajı ile sağlıklı gönüllülerde yapılan bir farmakokinetik çalışma, 200 mcg beklometazon/6 mcg formoterol içeren formülasyondaki beklometazon-17-monopropiyonat'ınakciğerdeki biyoyararlanabilirliğinin sadece EAA için 100/6 yitiliğine göre doz orantılı olduğunuortaya koymuştur {200/6 formülasyonu ve 100/6 yitiliğindeki sistemik biyoyararlanım arasındakiortalama oran 91.63'e eşittir (%90 Güven Aralığı: 83.79; 100.20)}. Formoterol fumarat için, 200/6formülasyonu ve 100/6 yitiliğindeki sistemik biyoyararlanım arasındaki ortalama oran 86.15'eeşittir (%90 Güven Aralığı: 75.94; 97.74).Aktif kömür blokajı olmadan sağlıklı gönüllülerde yapılan başka bir farmakokinetik çalışma, 200 mcg beklometazon/6 mcg formoterol kombinasyonundaki beklometazon-17-monopropiyonat'ınsistemik maruziyetinin 100/6 yitiliğine göre doz orantılı olduğunu ortaya koymuştur {200/6formülasyonu ve 100/6 yitiliğindeki sistemik biyoyararlanım arasındaki ortalama oran 89.2'yeeşittir (%90 Güven Aralığı: 79.8; 99.7)}.Formoterol fumarat için toplam sistemik maruz kalmadeğişmemiştir; {200/6 formülasyonu ve 100/6 yitiliğindeki sistemik biyoyararlanım arasındakiortalama oran 102.2'ye eşittir (%90 Güven Aralığı: 90.4; 115.5).200 mcg beklometazon/6 mcg formoterol kombinasyonunun Aerochamber Plus® ile kullanımı, sağlıklı gönüllülerde beklometazon dipropiyonat aktif metaboliti beklometazon-17-monopropiyonatın ve formoterolün akciğer aktarımını sırasıyla %25 ve %32 oranında arttırırken,toplam sistemik maruz kalım beklometazon 17-monopropiyonat (%17) ve formoterol (%17) içinaz miktarda azalmış ve değişmeyen beklometazon dipropiyonat için (%54 oranında) artmıştır.Sağlıklı gönüllülerde yapılan bir çalışmada, 200 mcg beklometazon/6 mcg formoterol kombinasyonunun Aerochamber Plus spacer ile kullanımı, beklometazon dipropiyonatın aktifmetaboliti olan 17-monopropiyonat ve formoterol fumarat için akciğer erişimini sırasıyla % 25ve % 32 arttırmıştır, toplam sistemik etki, beklometazon-17-monopropiyonat (%17) veformoterol (%17) için düşüş göstermiş ve değişmemiş beklometazon dipropiyonat için artmıştır(%54).Beklometazon dipropiyonatEmilim:İnhale edilen beklometazon dipropiyonat akciğerlerden hızla emilir; emilimden önce beklometazon dipropiyonat, çoğu dokuda bulunan esteraz enzimleri ile, büyük oranda aktifmetaboliti beklometazon-17-monopropiyonata dönüşür. Aktif metabolitin sistemik biyoyararlılığıakciğer (%36) ve yutulan dozun gastrointestinal emilimi ile ortaya çıkar. Yutulan beklometazondipropiyonat'ın biyoyararlılığı ihmal edilebilir düzeydedir, ancak, sistemik dolaşım öncesindebeklometazon-17-monopropiyonata dönüşüm emilimin %41'inin aktif metabolit olarakgerçekleşmesini sağlar.İnhale edilen dozun artışı ile birlikte sistemik etkide yaklaşık olarak lineer bir artış vardır.İnhalasyon sonrasındaki mutlak biyoyararlılık değişmemiş beklometazon dipropiyonat ve beklometazon-17-monopropiyonata için sırası ile nominal dozun %2 ve %62'si kadar olmuştur.Dağılım:İntravenöz dozdan sonra, beklometazon dipropiyonat ve aktif metabolitinin dağılımı yüksek plazma klerensi ile karakterizedir (sırasıyla 150 ve 120 L/saat) ve sabit durumdabeklometazon dipropiyonat için dağılım hacmi az (20L), aktif metabolit için doku dağılımı dahafazladır (424L).Plazma proteinine bağlanma orta derecede yüksektir.Biyotransformasyon:Glukokortikoid reseptörlerine bağlanma afinitesi zayıf bir ön ilaç olan beklometazon dipropiyonat, esteraz enzimleriyle aktif metabolit olan beklometazon-17-monopropiyonatahidrolize olur. Beklometazon-17-monopropiyonat, ön ilaç olan beklometazon dipropiyonatagöre daha güçlü bir topikal anti-inflamatuvar etkinliğe sahiptir.Eliminasyon:Beklometazon dipropiyonatın başlıca atılım şekli polar metabolitler şeklinde feçesle atılımdır. Beklometazon dipropiyonat ve metabolitlerinin idrarla atılımı önemsiz miktardadır.Beklometazon dipropiyonat ve beklometazon-17-monopropiyonat için terminal eliminasyonyarılanma ömrü sırasıyla 0,5 ve 2,7 saattir.Hastalardaki karakteristik özelliklerRenal veya hepatik bozukluğu olan hastalarda beklometazon dipropiyonatın farmakokinetikleri çalışılmamıştır; ancak beklometazon dipropiyonat bağırsak sıvısında, serum, akciğerler vekaraciğerde bulunan esteraz enzimleri ile çok hızlı metabolize olarak, daha polar ürünler olanbeklometazon-21-monopropiyonat, beklometazon-17-monoproiyonat ve beklometazon halinedönüştüğü için karaciğer yetersizliğinin beklometazon dipropiyonat farmakokinetik ve güvenlikprofilini değiştirmesi beklenmemektedir.Beklometazon dipropiyonat veya metabolitlerine idrarda rastlanmadığı için, böbrek yetersizliği olan hastalarda sistemik maruziyette artış gözlemlenmemiştir.FormoterolEmilim:İnhalasyondan sonra formoterol hem akciğerden hem de gastrointestinal yoldan emilmektedir. Ölçülü doz inhalatör (MDI) ile oral uygulamadan sonra yutulan inhale dozun fraksiyonu%60 ile%90 arasında bulunabilir. Yutulan dozun en az % 65'lik bir kısmı gastrointestinal sistemde emilir.Değişmemiş ilaç zirve plazma konsantrasyonuna oral uygulamadan 0.5 saat-1 saat sonra ulaşır.Dağılım:Formoterol'ün plazma proteinlerine bağlanma oranı %61-64'tür ve %34'ü albümine bağlanır. Terapötik dozlarda ulaşılan konsantrasyon aralığında bağlanmada doygunluk gerçekleşmez.Oral uygulamadan sonra saptanan eliminasyon yarılanma ömrü 2-3 saattir. Formoterol emilimi12-96 mikrogram inhale formoterol fumarat aralığı boyunca lineerdir.Biyotransformasyon:Formoterol yaygın biçimde metabolize olur ve öne çıkan metabolik yol fenolik hidroksil grubundaki doğrudan konjugasyondur. Glukoronik asit konjugatı inaktiftir. İkinci majör yolfenolik 2'-hidroksil grubunda demetilasyon ve bunu izleyen konjugasyondur. Sitokrom P-450izoenzimleri CYP2D6, CYP2C19, CYP2C9, formoterol O - demetilasyonuna katılırlar.Karaciğer, primer metabolizma bölgesi olarak görülmektedir. Formoterol terapötik geçerlikonsantrasyonlarda CYP-450 enzimlerini inhibe etmez.Eliminasyon:Formoterolün idrardan kümülatif atılımı bir KTI (kuru toz inhaler)'den tek inhalasyon sonrasında 12-96 pg doz aralığında lineer artış göstermiştir. Sırası ile ortalama, %8 ve %25 oranındaki dozdeğişmeden ve total formoterol olarak atılmıştır.12 sağlıklı olguda tek bir 120 pg doz inhalasyonunu takiben ölçülen plazma konsantrasyonlarına dayanılarak, ortalama terminal eliminasyon yarılanma ömrünün 10 saatolduğu belirlenmiştir. (R,R) ve (S,S) enantiomerleri idrarda atılan değişmemiş ilacın sırasıylayaklaşık %40 ve %60'ını temsil etmektedir. İki enantiomerin oranı araştırılan doz aralığındasabit kalmıştır ve yinelenen dozlardan sonra bir enantiomerin diğerine nispetle daha fazlabiriktiğine ilişkin kanıt bulunamamıştır.Oral uygulamadan sonra (40-80 pg) dozun %6-%10'a varan oranı sağlıklı olgularda idrarda değişmemiş ilaç olarak bulunmuştur ve %8'e varan oranı ise glukuronid olarak bulunmuştur.Oral formoterol dozunun toplam %67'si idrarla (başlıca metabolitleri şeklinde) ve kalanı feçesle atılır. Formoterolün renal klirensi 150 ml/dakika'dir.Karaciğer/böbrek yetersizliği:Formoterolün farmakokinetiği karaciğer ve böbrek yetersizliği olan hastalarda araştırılmamıştır, ancak formoterol büyük oranda hepatik metabolizmaaracılığıyla atıldığı için, ciddi karaciğer sirozu bulunan hastalarda maruziyetin artmasıbeklenebilir.5.2. Klinik öncesi güvenlilik verileriKombinasyon halinde veya tek başına verilen beklometazon dipropiyonat (BDP) ve formoterol ile yapılan hayvan deneylerinde gözlenen toksisite, abartılmış farmakolojik aktivite ile ilişkilietkilerdir. Bu etkiler başlıca köpeklerde beklometazon dipropiyonatın bağışıklığı baskılayıcıetkileri ve formoterolün bilinen kardiyovasküler etkileri ile ilişkilidir. Kombinasyonunuygulanmasından sonra toksisitede artış veya beklenmedik bulgular gözlemlenmemiştirKarsinojenite:Önerilen kombinasyonla karsinojenisite çalışmaları gerçekleştirilmemiştir. Bununla birlikte, ayrı ayrı bileşenler için bildirilen hayvanlardan elde edilen veriler, insanlarda herhangi birpotansiyel karsinojenisite riskini akla getirmemektedir.Mutajenite:Beklometazon dipropiyonat/formoterol kombinasyonuyla gerçekleştirilen genotoksisite çalışmaları mutajenik bir potansiyele işaret etmemektedir.Üreme üzerine toksisitesi:Sıçanlarda yapılan üreme çalışmaları doza bağlı etkileri göstermiştir. Kombinasyon, dişilerde azalmış doğurganlık ve embriyofetal toksisite ile ilişkilendirilmiştir. Gebe hayvanlara göreyüksek kortikosteroid dozlarının, damak yarığı ve rahim içi büyüme geriliği dahil fötal gelişimanomaliliklerine neden olduğu bilinmektedir ve beklometazon dipropiyonat/formoterolkombinasyonuyla görülen etkiler muhtemelen beklometazon dipropiyonattan ötürüdür. Buetkiler yalnızca, aktif metabolit olan beklometazon-17-monopropiyonata yüksek sistemikmaruz kalımla fark edilmiştir (hastalarda beklenen plazma düzeylerinin 200 katından daha fazla).Ayrıca, hayvanlarda yapılan çalışmalarda, beta2-sempatomimetiklerin bilinen tokolitiketkilerine dayandırılabilen bir etki olan gebelik ve doğum süresinin uzaması görülmüştür.Bu etkiler, 200 mcg beklometazon/6 mcg formoterol kombinasyonu ile tedavi edilen hastalarda maternal plazma formoterol düzeyleri beklenen düzeylerin altında olduğunda kaydedilmiştir.CFC içermeyen itici gaz HFA-134a ile ilişkili klinik öncesi konvansiyonel güvenlilik farmakolojisi, tekrar doz toksisitesi, genotoksisite, karsinojenik potansiyel ve üreme toksisitesiçalışmalarında insanlar için herhangi bir özel risk ortaya çıkmamıştır.6. FARMASÖTİK ÖZELLİKLER6.1. Yardımcı maddelerin listesiNorfluran (kloroflorokarbon CFC içermeyen bir itici gaz olan HFA-134a )Susuz etanol Hidroklorik asit6.2. GeçimsizliklerBilinen bir geçimsizliği yoktur.6.3. Raf ömrü20 ay6.4. Saklamaya yönelik özel tedbirlerEczane ve Depolar için Talimatlar2-8 °C'de buzdolabında saklanmalıdır (en fazla 15 ay).Hastalar için Talimatlar25 C'nin altındaki oda sıcaklığında saklanmalıdır (en fazla 5 ay).Uyarı:Kap yüksek basınç altında sıvı ihtiva eder. Kap 50 °C üzerindeki sıcaklıklara maruz bırakılmamalı, delinmemeli ve açılmaya çalışılmamalıdır.6.5. Ambalajın niteliği ve içeriğiİnhalasyon çözeltisi, ölçüm valfi ile kapatılmış, ağızlığı ve polipropilen plastik kapağı olan bir polipropilen plastik aktüator içerisine yerleştirilmiş basınçlı bir alüminyum kap içerisinde bulunur.Her kutuda;120 pufluk 1 basınçlı kap bulunur.6.6. Beşeri tıbbi üründen arta kalan maddelerin imhası ve diğer özel önlemlerHastaya veriliş tarihi kutunun üzerinde belirtilmelidir.Hastaya veriliş tarihi ve kutunun üzerindeki son kullanma tarihi arasında en az 5 ay olmasına dikkat edilmelidir.Kullanılmamış olan ürünler ya da atık materyaller, Tıbbi Atıkların Kontrolü Yönetmeliği ve Ambalaj ve Ambalaj Atıklarının Kontrolü Yönetmeliği ne uygun olarak imha edilmelidir.Sağlık çalışanlarına faydası olması bakımından, FOSTER kullanım talimatları aşağıda sunulmuştur.FOSTER AEROSOL ÇÖZELTİ KULLANMA TALİMATLARIİnhalerin test edilmesiİnhaler ilk kez kullanılacağı zaman ve 14 günden daha fazla bir süre kullanılmadığında hatasız işlev için havaya bir kez sıkım yapılmalıdır.İnhalerin kullanılmasıİnhaler aşırı soğuğa maruz kaldıysa, kullanmadan once ellerinizle bir kaç dakika ısıtınız. Hiçbir zaman başka araçlarla ısıtmayınız.Mümkün olduğu ölçüde, ilacı inhale ederken (solurken) ayakta durunuz veya sırtınız dik pozisyonda oturunuz.1. Koruyucu kapağı ağızlıktan çıkarınız ve ağızlığın temiz olduğunu, üzerinde toz, kir veya başkaherhangi bir yabancı madde olup olmadığını kontrol ediniz.2. Ağzınızdan mümkün olduğunca yavaş ve derin nefes veriniz.3. Tüpü alt kısmı yukarı bakacak biçimde dikey halde tutunuz ve ağızlığı ısırmadan dudaklarınızın arasına koyunuz.4. Ağzınızdan yavaş ve derin nefes alırken, aynı anda bir puf boşaltmak için inhalerin üst kısmınabasınız.5. Nefesinizi mümkün olduğunca tutunuz ve en sonunda inhaleri ağzınızdan çıkarıp yavaşça nefes veriniz. İnhalerin içine doğru nefes vermeyiniz.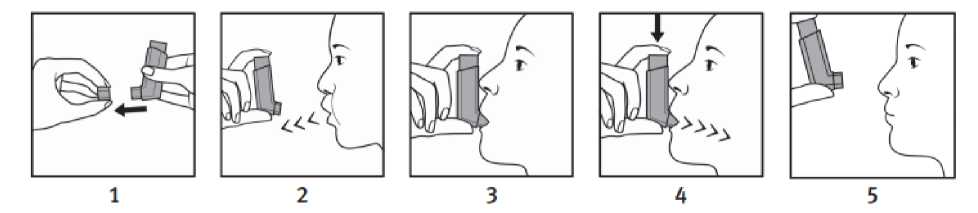
Bir puf daha gerekiyorsa, inhaleri yarım dakika kadar dikey halde tutunuz ve sonra 2 - 5 arasındaki işlemleri tekrarlayınız.Önemli:2 - 5 arası işlemleri çok çabuk yapmayınız.Eğer inhalerin üst kısmından veya ağzınızın yanlarından buğu geldiğini görürseniz, işlemlere yeniden 2. adımdan başlamalısınız.Eğer elleriniz güçsüz ise, inhaleri her iki elle tutmak daha kolay olabilir; bu durumda inhalerin üst kısmını her iki işaret parmağıyla tutunuz ve alt kısmını da her iki baş parmağınızlatutunuz.Ağızda ve boğazda mantar enfeksiyonu riskini azaltmak için, inhalasyon sonrasında ağzınızı su ile çalkalayınız veya dişlerinizi fırçalayınız (bakınız bölüm 4.4).TemizlikTemizlik talimatları için Kullanma Talimatını okuyunuz. İnhalerin düzenli temizliği için ağızlıktan kapağı çıkarın ve ağızlığın içini ve dışını kuru bir bez ile siliniz. Kutuyu aktüatördençıkarmayınız ve ağızlığı temizlemek için su veya diğer sıvıları kullanmayınız.Aerosol aktüasyonunu ve nefes almayı aynı anda gerçekleştirmeyi zor bulan hastalar AeroChamber Plus spacer cihazını kullanabilir. İnhalerin ve spacer cihazının düzgün kullanımıiçin doktor, hemşire veya eczacınıza danışınız. İlacın akciğerlere optimum seviyede ulaştığındanemin olunması için tekniğiniz kontrol edilmelidir. AeroChamber Plus kullanan hastalarda bu,aktüasyon ve inhalasyon arasında gecikme olmadan, spacer cihazından tek bir devamlı uzun vederin nefes alınmasıyla sağlanabilir.7. RUHSAT SAHİBİChiesi İlaç Ticaret A.Ş.Büyükdere Cad. No:122 Özsezen İş Merkezi C Blok Kat:3 Esentepe Şişli 34394, İstanbul Tel: 0212 370 9100Fax: 0212 370 91278. RUHSAT NUMARASI2019/5299. İLK RUHSAT TARİHİ/ RUHSAT YENİLEME TARİHİİlk ruhsat tarihi: 15.10.2019 Ruhsat yenileme tarihi: -10. KÜB'ÜN YENİLENME TARİHİ |
İlaç BilgileriFoster 200 Mcg/6 Mcg Aerosol İnhalasyon ÇözeltisiEtken Maddesi: Beklometazon Dipropiyonat Anhidr - Formoterol Fumarat Dihidrat Kullanma talimatı ve kısa ürün bilgileri
Google Reklamları
|
Ana Sayfa | Hakkımızda | İlaçlar | İlaç Ara | İlaç Firmaları | Gizlilik | Bize Ulaşın
Telif Hakkı 2008-2026 © İlaç Prospektüsü. Tüm Hakları Saklıdır.Uyarı: Sitemizde yayınladığımız ilaç bilgileri ile doktora danışmadan kesinlikle ilaç kullanmayınız!
Aksi halde doğabilecek sağlık sorunlarından ilacprospektusu.com sorumlu tutulamaz.