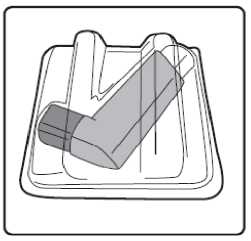
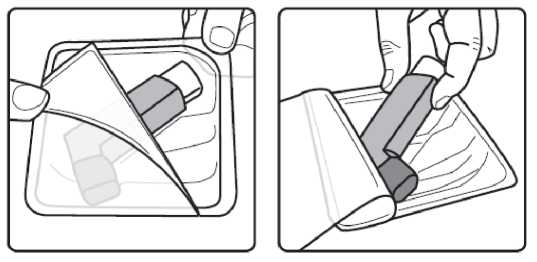
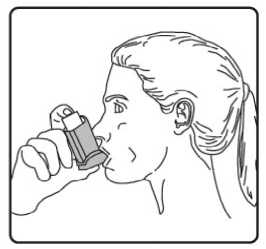
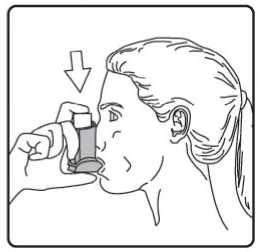
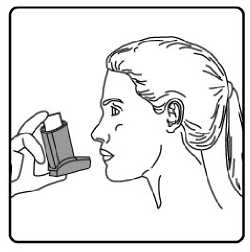
Forpack 6/100 Mcg İnhalasyon İçin Ölçülü Dozlu Aerosol Kısa Ürün BilgisiKISA ÜRÜN BİLGİSİ1. BEŞERİ TIBBİ ÜRÜNÜN ADIFORPACK® 6 mcg/100 mcg aerosol inhalasyonu, süspansiyon 2. KALİTATİF VE KANTİTATİF BİLEŞİMEtkin madde:Formoterol fumarat dihidrat 6 mcg Budesonid 100 mcg Hastaya ulaşan her doz (ağızlıktan çıkan doz) : 4,5 mcg formoterol fumarat dihidrat ve 80 budesonid içerir. Yardımcı madde(ler):Yardımcı maddeler için, 6.1'e bakınız. 3. FARMASÖTİK FORMİnhalasyon için ölçülü dozlu aerosol Alüminyum inhaler kabı içinde basınçlı propellant gaz ile doldurulmuş süspansiyon. Alüminyum konteynere bir dozajlama valf eklidir. 4. KLİNİK ÖZELLİKLER4.1. Terapötik endikasyonlarFORPACK, astım semptomlarının düzeltilmesi ve kontrol altına alınması amacıyla kullanılır. FORPACK şiddetli astımı olan hastalar için uygun değildir. 6-12 yaş grubundaki çocuklar içinuygundur. 4.2. Pozoloji ve uygulama şekliPozoloji/uygulama sıklığı ve süresi:PozolojiFORPACK, astımın başlangıç tedavisine yönelik değildir. FORPACK'in içindeki maddelerin dozu her hasta için farklıdır ve hastalığın şiddetine göre belirlenmelidir. Bu durum, sadece tedaviye kombinasyon ile başlandığında değil, idame dozayarlanırken de göz önünde tutulmalıdır. Hasta, kombinasyon preparatının içindeki dozlarındışında bir doz kombinasyonuna gereksinim duyarsa uygun dozda beta 2-agonist ve/veyakortikosteroidi tek başına içeren preparatlar verilmelidir.Doz, semptomların efektif kontrolünün idame ettirildiği en düşük değere titre edilmelidir. Hastalar hekimleri tarafından, en uygun FORPACK dozunu kullanmaları açısından düzenliolarak değerlendirilmelidirler. Önerilen en düşük doz ile kontrol altına alındığında, bir sonrakiadım tek başına inhale steroid tedavisinin denenmesini içerebilir. 1 FORPACK için iki tedavi yaklaşımı söz konusudur: A. FORPACK idame tedavisi:Düzenli idame tedavi olarak FORPACK ile birliktekurtarıcı nitelikte ayrıca bir hızlı etki eden bronkodilatör alınır.B. FORPACK idame ve semptom giderici tedavi:A. FORPACK idame tedavisi:Hastalara, kurtarıcı olarak yanlarında ayrıca bir hızlı etki eden bronkodilatör bulundurmaları önerilmelidir. Önerilen dozlar: Erişkinler (18yaş ve üzeri):Günde iki kez 1-2 inhalasyon. Bazı hastalar için, günde toplamiki kez 4 inhalasyon dozunu aşmamak üzere daha yüksek doz kullanılması gerekebilir. Adolesanlar (12-17yaş):Günde iki kez 1-2 inhalasyon. Çocuklar (6yaş ve üzeri):Günde iki kez 2 inhalasyon.Genel uygulamada günde iki kez kullanım ile semptomlar kontrol altına alındığında, semptomların kontrolünün sürdürülebilmesi için hekim tarafından hastanın inhalekortikosteroidle kombine uzun etkili bronkodilatöre ihtiyacı olduğu düşünülüyor ise, doz titreedilerek ulaşılan etkili en düşük doz, günde tek doz FORPACK olarak kullanılabilir. Ayrı bir hızlı etkili bronkodilatör kullanımının artması, altta yatan bir kötüleşme olduğunu göstermektedir ve astım tedavisinin yeniden gözden geçirilmesi gerekmektedir. 6 yaşın altındaki çocuklar:B. FORPACK idame ve semptom giderici tedavi:FORPACK düzenli idame tedavi olarak ve ihtiyaç halinde semptomları gidermek amaçlı alınır. Hastalara, kurtarıcı olarak FORPACK'i her zaman yanlarında bulundurmaları öğütlenmelidir. FORPACK'in idame ve semptom giderici tedavi şeklinde kullanımı özellikle aşağıdaki durumlarda dikkate alınmalıdır: Yetersiz astım kontrolü ve sık sık semptom giderici tedavi ihtiyacı Tıbbi müdahale gerektiren geçmişe yönelik astım alevlenmeleri Gerekli durumlarda çok sayıda ve sık FORPACK alan hastalarda, doza bağımlı advers etkiler açısından yakın takibe ihtiyaç vardır. Önerilen dozlar:Erişkinler ve adolesanlar (12 yaş ve üzeri):Önerilen idame doz günde 2 inhalasyondur. Doz, sabah ve akşam birer inhalasyon veya sabah 2 ya da akşam 2 inhalasyon olarak alınabilir.Hastalar, ihtiyaç halinde semptomların giderilmesine yönelik, ilave olarak 1 inhalasyon2 almalıdırlar. Birkaç dakika sonra semptomlar devam ederse ilave bir inhalasyon uygulanmalıdır. Bir defada 6 inhalasyondan fazla uygulanmamalıdır. Normal şartlarda ihtiyaç duyulan toplam günlük doz 8 inhalasyondan fazla değildir. Bununla birlikte sınırlı bir süre için toplam günlük doz 12 inhalasyona kadar çıkabilir. Günde 8inhalasyondan fazla kullanan hastalara mutlaka medikal yardım almaları önerilmelidir. Buhastalar tekrar değerlendirilmeli ve idame tedavileri tekrar gözden geçirilmelidir. 12 yaşın altındaki çocuklar:Çocuklar için FORPACK'in idame ve semptom giderici tedavi şeklinde kullanımı önerilmemektedir.Uygulama şekli:FORPACK, sadece oral inhalasyon yolu ile uygulanır. İnhalasyon spreyinin doğru kullanımı doktor veya eczacı tarafından hastaya gösterilmelidir. İnhalasyon sırasında hastalar tercihen oturmalı veya ayakta durmalıdır. İnhalasyon spreyi dikkonumda kullanım için tasarlanmıştır. Olası bir kandida enfeksiyonu riskini azaltmak için her uygulamadan sonra ağzın su ile iyice çalkalanması ve tükürülmesi önerilmektedir. Ayrıca ağzın su ile çalkalanması boğazirritasyonunu engellemeye ve sistemik etki riskinin azaltılmasına muhtemelen yardımcıolabilir. Kullanıma ilişkin detaylı bilgi, kullanma talimatında mevcuttur. İnhalasyon spreyinin doğru kullanımı için aşağıda verilen kuralları dikkatle izleyiniz. inhalasyon spreyinin kullanım talimatıKarton kutuda piyasaya sunulan inhalasyon için aerosol, güvenlik amaçlı koruyucu ambalaj içerisinde yer almaktadır. İnhalasyon için aerosolü kullanmadan önce şekilde gösterildiği gibi ambalajından çıkarınız. 3
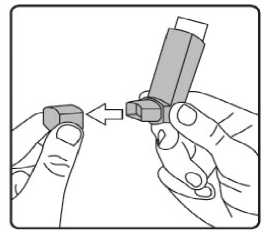
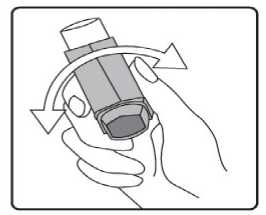
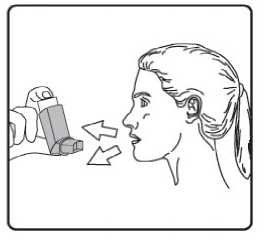
İlk kez kullanımdan önce hastalar ağızlık kapağını, kapağın yanlarından hafifçe sıkarak çıkarmalı, inhalasyon spreyini iyi bir şekilde sallamalı, başparmak ağızlığın altında inhalasyonspreyinin tabanında olacak şekilde parmaklar ve baş parmak arasında tutmalı ve boşluğa sıkımyapmalıdır. İnhalasyon spreyi her sıkımdan önce sallanmalıdır. İnhalasyon spreyi bir hafta veya daha uzun süre kullanılmadığında hastalar ağızlık kapağını çıkarmalı, inhalasyon spreyi ile boşluğa iki kez sıkım yapılmalıdır. İnhalasyon spreyinizi kullanacağınız zaman oturunuz veya ayakta dik durunuz. 1. İlk resimde gösterildiği gibi ağızlık kapağını çıkarınız. Ağızlığın temiz olduğundan eminolmak için içini ve dışını kontrol ediniz. 2. İnhalasyon spreyinizi her kullanımdan önce iyice çalkalayınız. 3. İnhalasyon spreyinizi başparmağınız ağızlığın altında, inhalasyon spreyinizin tabanındaolacak şekilde dik tutunuz. 4 4. Ağızlığı dişlerinizin arasına koyunuz ve dudaklarınızı sıkıca kapatınız. 5. Ağzınızdan yavaş ve derin nefes alınız ve aynı anda bir puf doz boşaltmak için inhalasyonspreyinizin üst kısmına basınız. 6. Nefesinizi yaklaşık 10 saniye veya rahatça tutabildiğiniz kadar tutunuz ve ağızlığıağzınızdan çıkarıp parmağınızı inhalasyon spreyinizin üst kısmından çekiniz. Sonrayavaşça ağzınızdan nefes veriniz. İnhalerin içine nefes vermekten kaçınız. 5 7. Her bir puf ilaç alımı arasında yaklaşık yarım dakika bekleyiniz ve sonra 2-6. basamaklarıtekrarlayınız. 8. Daha sonra, ağzınızı su ile çalkalayınız ve tükürünüz. Bunu yapmanız ağzınızda pamukçukoluşumunun ve ses kısıklığının önlenmesine yardımcı olmak için önemlidir. 9. Kullanımdan sonra tozdan korumak için ağızlığın kapağını hemen kapatınız. Ağızlıkkapağı doğru bir şekilde yerleştirildiğinde tam yerine oturacaktır. Eğer yerine oturmuyorsa,ağızlık kapağını diğer yöne çeviriniz. Çok fazla güç uygulamayınız. Hastalar 4, 5 ve 6. basamakları hızlı bir şekilde yapmamalıdır. Hastaların inhalasyon spreyini etkin hale getirmeden hemen önce mümkün olduğunca yavaş bir şekilde nefes almayabaşlaması önemlidir. Hastalar aynanın önünde ilk birkaç uygulama için pratik yapmalıdırlar.Eğer hastalar inhalasyon spreyinin üstünden veya ağızlarının yanından buhar geldiğini görürse, 2. basamaktan itibaren uygulamaya tekrar başlamalıdırlar. inhalasyon spreyinin temizlenmesi İnhalasyon spreyinizi haftada en az bir kez temizleyiniz. 1. Ağızlık kapağını çıkarınız. 2. Tüpü plastik gövdeden çıkarmayınız. 3. Kuru bir bez veya kumaş ile ağızlığın içini ve dışını ve plastik gövdeyi siliniz. 4. Ağızlık kapağını doğru bir şekilde yerleştiriniz. Kapağı yerleştirmek için çok fazla güçuygulamayınız. Özel popülasyonlara ilişkin ek bilgiler: Böbrek/Karaciğer yetmezliği: Karaciğer ya da böbrek yetmezliği olan hastalarda FORPACK kullanımı ile ilgili veri yoktur. Ancak budesonid ve fomoterol ilk geçiş sırasında hepatik metabolizma ile elimineedildiklerinden, ağır karaciğer sirozu olanlarda maruziyet artabilir. Pediyatrik popülasyon: 12 yaşın altındaki çocuklar için FORPACK'in idame ve semptom giderici tedavi şeklinde kullanımı önerilmemektedir. Geriyatrik popülasyon: Yaşlılarda özel doz gereksinimleri yoktur. 4.3. Kontrendikasyonlar Etkin maddelere veya Bölüm 6.1'de listelenen herhangi bir yardımcı maddeye karşı aşırı duyarlılığı olanlarda kullanılmamalıdır. 6 4.4. Özel kullanım uyarıları ve önlemleriUzun etkili beta agonist preparatlarına bağlı olarak nadiren, ciddi ve bazen ölümcül olabilen astım ile ilgili solunum problemleri meydana gelebilir. FORPACK astım hastalığının başlangıç tedavisi için önerilmez. Uzun etkili beta agonistler astım semptom kontrolünü sağlayan en kısa süre boyunca kullanılmalı ve astım kontrolüne ulaşıldığında eğer mümkünse kullanımları durdurulmalıdır.Sonrasında hastaların kontrol edici bir tedaviyle idamesi sağlanmalıdır. İnhale kortikosteroide ek olarak uzun etkili beta agonist kullanan pediyatrik ve adölesan hastalarda, her iki ilaca uyumu garanti altına almak için, hem inhale kortikosteroid hem de uzunetkili beta agonist içeren bir kombinasyon preparatı kullanılması önerilir. Hastalar alevlenme dönemlerinde ise ya da önemli ölçüde veya akut olarak kötüye giden astım şikayetleri varsa, uzun etkili beta agonistlerle tedaviye başlanmamalıdır. Hasta tedaviyi etkisiz bulduğunda ya da FORPACK'in önerilen en yüksek dozundan daha fazla inhalasyon gerektiğinde doktoruna başvurmalıdır (Bkz. Bölüm 4.2). Astımın ani ve giderekkötüleşmesi hayatı tehdit eden bir durumdur, hasta acil olarak doktor kontrolüne alınmalıdır.Bu durumda kortikosteroid tedavisinin artırılması örneğin oral yoldan bir kortikosteroidverilmesi ya da bir enfeksiyon varsa antibiyotik verilmesi uygundur. Hastalara kurtarıcı inhaler olarak FORPACK'i (FORPACK'i idame ve semptom giderici tedavi kullanan hastalar için) veya başka hızlı etki eden bronkodilatatör ilaçlarını (sadece idametedavide FORPACK kullanan tüm hastalar) her zaman yanlarında bulundurmalarıöğütlenmelidir. Hastalar, aseptomatik olsa bile FORPACK idame dozunu doktorun önerdiği şekilde almaları konusunda bilgilendirilmelidir. FORPACK'in profilaktik kullanımı (örneğin egzersizden önce)henüz araştırılmamıştır. Astım semptomlarına karşılık FORPACK'in semptom giderici dozlarıalınmalıdır, fakat bu dozlar, örneğin egzersizden önce, düzenli profilaktik kullanım amaçlıdeğildir. Bu tür bir amaç için başka bir hızlı etki eden bronkodilatör kullanılmalıdır. Tedavi sonlandırılacağı zaman, dozun azaltılarak bırakılması ve aniden kesilmemesi önerilir. Tedavi, birden kesilmemelidir. Astım semptomları kontrol altına alındıktan sonra, FORPACKdozunun yavaş yavaş azaltılması düşünülebilir. Tedavi dozu azaltılırken hastaların düzenliolarak kontrol edilmesi önemlidir. FORPACK'in etkili en düşük dozu kullanılmalıdır (Bkz.Bölüm 4.2). FORPACK ile tedavi sırasında, astımla ilişkili advers etkiler ve alevlenmeler görülebilir. Hastadan FORPACK ile tedaviye devam etmesi, fakat FORPACK'e başlandıktan sonra astımsemptomları kontrol altına alınamazsa veya kötüleşirse, tıbbi destek alması istenmelidir. 7 İnhalasyon yoluyla uygulanan diğer tedavilerde olduğu gibi, ilaç alındıktan sonra hırıltılı soluk alıp vermede ani bir artış ile birlikte paradoksikal bronkospazm görülebilir. Bu durumdaFORPACK ile tedavi kesilmeli, tedavi tekrar değerlendirilmeli ve gerekirse başka bir tedaviyegeçilmelidir. Paradoksal bronkospazm hızlı-etkili bir inhale bronkodilatöre yanıt verir ve hızlatedavi edilmelidir (Bkz. Bölüm 4.8). Uzun süre özellikle yüksek dozda inhalasyon yoluyla herhangi bir kortikosteroid kullanıldığında sistemik etkiler görülebilir. Bu etkilerin görülme olasılığı oralkortikosteroidlere oranla daha azdır. Oluşabilecek sistemik etkiler; Cushing's sendromu,Cushing benzeri özellikler, adrenal yetmezlik kemik mineral yoğunluğunda azalma, katarakt,glokom ve daha nadir olarak çeşitli psikolojik veya psikomotor hiperaktivite, uykubozuklukları, anksiyete, depresyon veya agresyonu kapsayan davranışsal etkilerdir (özellikleçocuklarda). İnhalasyon yoluyla kullanılan budesonid ile yapılan uzun süreli çalışmalar, çocuklarda günlük ortalama 400 mikrogram (ölçülü doz) veya yetişkinlerde günlük 800 mikrogram (ölçülü doz)dozun kemik mineral yoğunluğu üzerinde belirgin bir etkisinin olmadığını göstermiştir.FORPACK'in daha yüksek dozları ile görülen etkilerine ilişkin bilgi yoktur. Daha önceki sistemik steroid tedavisi nedeniyle adrenal yetmezliğinin belirtileri varsa, böyle hastalar FORPACK tedavisine alınırken dikkatli olunmalıdır. İnhalasyonla alınan budesonid tedavisinin yararı, oral steroide duyulan gereksinimi en aza indirmesidir, ancak oral steroid tedavisinden inhalasyon tedavisine geçen hastalar uzun zamanadrenal yetmezlik riski ile karşı karşıya olabilirler. Geçmişte acil olarak yüksek dozkortikosteroid tedavisi görmüş olan ya da uzun süre yüksek dozda inhalasyon yoluyla steroidkullanmış hastalar da risk altında olabilir. Bu gibi durumlarda HPA axis fonksiyonu düzenliolarak kontrol edilmelidir. Yüksek dozlarda inhale kortikosteroidler ile uzun süreli, özellikle önerilenden daha yüksek dozlarla tedavi, klinik açıdan önemli adrenal baskılanmaya neden olabilir. Bu nedenle ağırenfeksiyonlar gibi stres durumlarında veya elektif operasyon uygulanan dönemlerde ilavesistemik kortikosteroid tedavisi düşünülmelidir. Steroid dozlarında hızlı azalma, akut adrenalkrizleri tetikleyebilir. Akut adrenal kriz sırasında görülebilecek belirti ve işaretler kısmenbelirsiz olabilir, ancak anoreksi, abdominal ağrı, kilo kaybı, yorgunluk, baş ağrısı, bulantı,kusma, bilinç seviyesinde azalma, nöbet, hipotansiyon ve hipoglisemiyi kapsayabilir. İnhale budesonid ve destek olarak kullanılan sistemik steroid tedavisi aniden kesilmemelidir. Oral tedaviden FORPACK'e geçilirken, alerjik veya artiritik belirtiler görünümünde rinit, egzama ve kas eklem ağrısı gibi genel olarak daha düşük bir sistemik steroid etki görülecektir.Bu durumlar için özel tedavi başlatılmalıdır. Nadir olarak, yorgunluk, baş ağrısı, bulantı vekusma oluşması halinde, genel yetersiz bir glukokortikosteroid etkiden şüphelenmek gerekir.Böyle durumlarda oral glukokortikosteroid dozlarının geçici olarak artırılması gerekebilir. 8 Hastalara, ağız ve boğaz bölgesinde pamukçuk oluşma riskini azaltması için idame dozun her inhalasyonundan sonra ağızlarını suyla çalkalamaları öğütlenmelidir. Pamukçuk oluşmasıdurumunda, ihtiyaç halinde kullanılan inhalasyonun ardından ağızlarını su ile çalkalamalıdırlar. FORPACK ile itrakonazol ve ritonavir veya diğer güçlü CYP3A4 inhibitörleri birlikte kullanılmamalıdır (Bkz. Bölüm 4.5). Bunun mümkün olmadığı durumlarda, etkileşen ilaçlarınuygulanmaları arasındaki süre mümkün olduğu kadar uzun olmalıdır. Güçlü CYP3A4inhibitörleri kullanan hastalarda, FORPACK tedavisi önerilmemektedir. FORPACK tirotoksikoz, feokromasitoma, diabetes mellitus, tedavi edilmemiş hipokalemi, hipertrofik obstrüktif kardiyomiyopati, idiyopatik subvalvular aort stenozu, şiddetlihipertansiyon, anevrizma veya iskemik kalp hastalığı, taşiaritmi ya da kalp yetmezliği gibi ağırkardiyovasküler hastalığı olanlarda dikkatli kullanılmalıdır. QTc-aralığı uzamış hastalarda FORPACK kullanılırken dikkatli olunmalıdır. Formoterol QTc-aralığının uzamasına neden olabilir. Aktif ya da pasif akciğer tüberkülozu, solunum yollarında fungal ve viral enfeksiyonu olan hastalarda, inhalasyonla kullanılan kortikosteroidlere gerek olup olmadığı ve dozu yenidendeğerlendirilmelidir. Yüksek dozda beta 222-agonistlerin olası hipokalemik etkisiniartırabilir. Hipokalemi yan etki olasılığının arttığı; değişken sıklıkta hızlı etkilibronkodilatörlerin kullanıldığı stabil olmayan astım, hipoksi nedeniyle hipokalemi riskininartabileceği akut ağır astım ve bu riskin artabileceği diğer durumlarda özel dikkat gösterilmesiönerilmektedir. Bu tür durumlarda serum potasyum düzeylerinin dikkatle izlenmesiönerilmektedir.Bütün beta 2-agonistlerde olduğu gibi, diyabetik hastalarda kan glukoz düzeyleri daha sık izlenmelidir.Sistemik ve topikal kortikosteroid kullanımı ile görme bozukluğu görülebilir. Hasta, bulanık görme veya diğer görme bozuklukları gibi semptomlarla karşılaşırsa, sistemik ve topikalkortikosteroidlerin kullanımından sonra rapor edilen katarakt, glokom gibi olası hastalıklarınveya merkezi seröz korioretinopati (CSCR) gibi nadir görülen hastalıkların değerlendirilmesiiçin bir göz doktoruna sevk edilmeleri düşünülmelidir. Pediyatrik popülasyonlarİnhale kortikosteroidler ile uzun süreli tedavi gören çocukların boylarının düzenli olarak görüntülenmesi önerilir. Eğer büyümede yavaşlama olursa, mümkün ise inhale kortikosteroiddozunu etkili astım kontrolünü devam ettiren en düşük doza düşürmek amacıyla tedavi yeniden 9 değerlendirilmelidir. Ayrıca, hastaya pediyatrik göğüs hastalıkları uzmanına görünmesi önerilebilir. Uzun vadeli çalışmalardan elde edilen sınırlı veriler, inhale budesonid ile tedavi edilen çocuk ve adolesanların çoğunun sonuçta erişkin hedef boylarına ulaştıklarını düşündürmektedir.Bununla birlikte, büyümede başlangıçta küçük fakat geçici bir azalma (yaklaşık 1 cm)gözlenmiştir. Bu genellikle tedavinin ilk yılında gerçekleşir. 4.5. Diğer tıbbi ürünler ile etkileşimler ve diğer etkileşim şekilleriFarmakokinetik etkileşimler:CYP P4503A4 ile metabolize olan maddeler (örn. ketokonazol, itrakonazol, vorikonazol, posakonazol, klaritromisin, telitromisin, nefazodon ve HIV proteaz inhibitörleri (ritonavir))budesonidin plazma düzeylerini artırabileceklerinden bu ilaçlarla birlikte kullanımındankaçınılmalıdır. Bunun mümkün olmadığı durumlarda inhibitör ile budesonidin kullanımıarasındaki zaman aralığı mümkün olduğunca uzun olmalıdır. Güçlü CYP3A4 inhibitörlerinikullanan hastalarda, FORPACK tedavisi önerilmemektedir. Günde 1 kez 200 mg şeklinde uygulanan güçlü CYP3A4 inhibitörü ketokonazol, eşzamanlı olarak oral yoldan uygulanan budesonidin (3 mg'lık tek doz) plazma düzeylerini ortalama 6 katarttırmıştır. Ketokonazol, budesonid uygulamasından 12 saat sonra verildiğinde konsantrasyonortalama sadece 3 kat artmıştır ve bu durum, uygulama zamanlarının birbirinden ayrılmasınınplazma düzeylerindeki artışı azaltabileceğini göstermektedir. Yüksek doz inhale budesonid ileilgili bu etkileşim hakkındaki sınırlı veriler, günde 1 kez 200 mg itrakonazol, inhale budesonid(1000 ^g'lık tek doz) ile eşzamanlı uygulandığında plazma düzeylerinde belirgin artışlarolabileceğini (ortalama dört 4 kat) ortaya koymaktadır. Farmakodinamik etkileşimler:Beta-adrenerjik blokör ilaçlar, formoterolün etkisini zayıflatabilir ya da tamamen inhibe edebilirler. Bu nedenle zorunlu olmadıkça, FORPACK, beta-adrenerjik blokör ilaçlarla(göz damlaları dahil) birlikte kullanılmamalıdır. Kinidin, disopiramid, prokainamid, fenotiyazinler, antihistaminikler (terfenadin) ve trisiklik antidepresanlarla birlikte kullanıldığında QTc aralığı uzayabilir ve ventriküler aritmi riski artar. Ayrıca L-dopa, L-tiroksin, oksitosin ve alkol, beta 2-sempatomimetiklere karşı kardiyak toleransı azaltabilir.Monoamino oksidaz inhibitörleri ve furazolidon ve prokarbazin gibi benzer özellikteki ilaçlarla birlikte kullanıldığında hipertansif reaksiyonlar artabilir. Halojenli hidrokarbon yapısındaki anestezik ilaçlarla birlikte kullanıldığında aritmi riski artar. Diğer beta-adrenerjik ilaçlarla veya antikolinerjik ilaçlarla birlikte kullanıldığında aditif bronşları genişleten etki görülebilir. 10 Dijital glikozitleri ile tedavi edilen hastalarda hipokalemi, aritmiye eğilimi arttırabilir. Hipokalemi, beta 2-agonisti tedavisinden kaynaklanabilir ve etkisi ksantin türevleri, kortikosteroidler ve diüretiklerle eşzamanlı tedavi nedeniyle güçlenebilir (Bkz. Bölüm 4.4).Budesonid ve formoterolün astım tedavisinde kullanılan diğer ilaçlarla etkileşimi gözlenmemiştir. Özel popülasyonlara ilişkin ek bilgiler:Özel popülasyonlara ilişkin herhangi bir etkileşim çalışması tespit edilmemiştir. Pediyatrik popülasyon:Etkileşim çalışmaları sadece erişkinlerde yapılmıştır. 4.6. Gebelik ve laktasyonGenel tavsiyeGebelik kategorisi C'dir. Çocuk doğurma potansiyeli bulunan kadınlar / Doğum kontrolü (Kontrasepsiyon)Çocuk doğurma potansiyeline sahip astımlı kadınlar ve gebe olan astımlı kadınları da içeren astımlı hastalarda genel olarak yetersiz astım kontrolü riski bulunması nedeniyle, çocukdoğurma potansiyeline sahip astımlı kadınları da içeren bu hastaların ideal bir anti-astmatiktedavi almaları son derece önemlidir. Formoterol/budesonid kombinasyonu ile tedavi, gebe kadın ya da fetüsü için herhangi birilave anlamlı klinik risk oluşturmaz ve bu nedenle herhangi bir aktif kontrasepsiyonkullanılması gerekli değildir. Formoterol/budesonid kombinasyonunun bugün bilinen kontrasepsiyon yöntemleri üzerindeherhangi bir etkisi yoktur. Gebelik dönemiFormoterol/budesonid kombinasyonunun gebe kadınlarda kullanımına ilişkin yeterli veri mevcut değildir. Hayvanlar üzerinde yapılan araştırmalar üreme toksisitesinin bulunduğunugöstermiştir (Bkz. Bölüm 5.3). İnsanlara yönelik potansiyel risk bilinmemektedir. FORPACK gebelikte ancak sağlanan fayda ortaya çıkabilecek risklerden fazla olduğunda kullanılabilir. Budesonidin, yeterli astım kontrolünü idame ettirecek etkili en düşük dozukullanılmalıdır. Gebelikte, FORPACK tedavisine veya formoterol ve budesonidin birlikte kullanılmasına yönelik herhangi bir klinik veri mevcut değildir. Sıçanlardaki bir embriyofetal gelişimçalışmasının verileri kombinasyondan kaynaklanan herhangi bir artmış etkiyi işaret etmemiştir. 11 Formoterolün hamile kadınlarda kullanımına yönelik yeterli veri mevcut değildir. Hayvan çalışmalarında çok yüksek sistemik dozların kullanıldığı üreme çalışmalarında formoteroladvers etkilere neden olmuştur (Bkz. Bölüm 5.3). Yaklaşık 2000 gebeden elde edilen veriler, inhale budesonidin kullanılması ile ilişkili olarak teratojenik riskin artmadığını göstermektedir. Hayvan çalışmalarında glukokortikosteroidlerinmalformasyonlara neden olduğu gösterilmiştir (Bkz. Bölüm 5.3). Bu durum, önerilen dozlarınverildiği insanlarda aynı değildir. Hayvan çalışmalarında, glukokortikoidlerin doğumdan önce aşırı miktarda alınmasının intrauterin gelişmede gecikme, yetişkin kardiyovasküler hastalık ve glukokortikoid reseptöryoğunluğunda, teratojenik doz aralığının altında görülen nörotransmitter döngüsü ve etkilerindekalıcı değişikliklere yönelik bir ilişki saptanmıştır. Laktasyon dönemiBudesonid anne sütüne geçer. Ancak tedavi dozlarında kullanıldığında bebeğe zararlı etkisi olması beklenmez. Formoterolün insanlarda anne sütüne geçip geçmediği bilinmemektedir.Sıçanlarda, az miktarda formoterolün anne sütüne geçtiği belirlenmiştir. FORPACK, emziren annelere, ancak anneye sağlanan faydanın, çocukta görülebilecek riskten daha fazla olması halinde verilebilir. Üreme Yeteneği/ FertiliteBudesonidin fertilite üzerindeki potansiyel etkisi hakkında herhangi bir veri bulunmamaktadır. Formoterol ile yapılan hayvan üreme çalışmaları, yüksek sistemik maruziyette erkek sıçanlardabir miktar azalmış fertilite (üreme yeteneği) göstermiştir. 4.7. Araç ve makine kullanımı üzerindeki etkilerFORPACK içeriğinde yer alan formoterol / budesonid kombinasyonunun araç ve makine kullanmaya herhangi bir etkisi yoktur ya da ihmal edilebilir düzeydedir. 4.8. İstenmeyen etkilerFORPACK, hem budesonid hem de formoterol içerdiğinden bu maddelerin her birine ait, aynı tipte ve aynı sıklıkta advers etkiler görülebilir. Bu iki maddenin birlikte kullanılmasına bağlıolarak advers etkilerde bir artış gözlenmemiştir. En yaygın yan etkiler; beta 2-agonistlerletedavide görülen tremor ve palpitasyon gibi yan etkilerdir. Bu etkiler hafiftir ve tedavinin birkaçgünü içinde kaybolurlar.Budesonid ya da formoterole bağlı aşağıdaki yan etkiler organ sınıfı ve sıklığa göre sıralanmıştır. Sıklık tanımlaması: çok yaygın (>1/10), yaygın (>1/100 ila <1/10), yaygınolmayan (>1/1.000 ila <1/100), seyrek (>1/10.000 ila <1/1.000), çok seyrek (<1/10.000) vebilinmiyor (eldeki verilerden hareketle tahmin edilemiyor). 12
Orofarinksteki Candida enfeksiyonu ilaç birikmesinden kaynaklanmaktadır. Hastalara her idame dozundan sonra ağızlarının su ile çalkalanmasının önerilmesi, riski en aza indirir.Orofarinksteki Candida enfeksiyonu genelde inhale kortikosteroid tedavisini kesmeye gerekkalmadan topikal antifungal tedaviye cevap verir. Eğer orofarinkste pamukçuk oluşursa da, 13 hastalar gerekli inhalasyonlardan sonra da ağızlarını su ile çalkalamalıdır. Diğer inhalasyon tedavilerinde olduğu gibi çok nadiren paradoksal bronkospazm ortaya çıkabilir. Bu durum 10.000'de 1 kişiden azını etkilemekte, doz uygulamasının ardından hırıltıve nefes darlığında hızlı bir artış meydana gelmektedir. Paradoksal bronkospazm hızlı etkili birinhale bronkodilatöre yanıt verir ve derhal tedavi edilmelidir. FORPACK derhal bırakılmalı,hasta değerlendirilmeli ve gerekiyorsa bir alternatif tedavi başlanmalıdır (Bkz. Bölüm 4.4). Uzun süre özellikle yüksek dozda inhalasyon yoluyla herhangi bir kortikosteroid kullanıldığında sistemik etkiler görülebilir. Bu etkilerin görülme olasılığı oralkortikosteroidlere oranla daha azdır. Oluşabilecek sistemik etkiler; Cushing's sendromu,Cushing benzeri belirtiler, adrenal yetmezlik, çocuklar ve adölesanlarda büyüme geriliği, kemikmineral yoğunluğunda azalma, katarakt ve glokomdur. Enfeksiyonlara karşı artmış hassasiyetve stres koşullarına adapte olmakta azalma da meydana gelebilir. Etkiler muhtemelen doza,uygulama süresine, birlikte kullanılan veya daha önceki steroid maruziyetine ve bireyselhassasiyete bağlıdır. Beta 2Pediyatrik popülasyonlarUzun süreli inhale kortikosteroid tedavisi gören çocukların boylarının düzenli olarak görüntülenmesi önerilir (Bkz. Bölüm 4.4.). Şüpheli advers reaksiyonların raporlanmasıRuhsatlandırma sonrası şüpheli ilaç advers reaksiyonlarının raporlanması büyük önem taşımaktadır. Raporlama yapılması, ilacın yarar/risk dengesinin sürekli olarak izlenmesineolanak sağlar. Sağlık mesleği mensuplarının herhangi bir şüpheli advers reaksiyonu TürkiyeFarmakovijilans Merkezi (TÜFAM)'ne bildirmeleri gerekmektedir (www.titck.gov.tr;e-posta: [email protected]; tel: 0 800 314 00 08; faks: 0 312 218 35 99). 4.9. Doz aşımı ve tedavisiFormoterolün doz aşımı durumunda tremor, baş ağrısı ve palpitasyon gibi beta 2- agonistlere bağlı tipik etkiler görülebilir. İzole vakalarda bildirilen belirtiler; taşikardi, hiperglisemi,hipokalemi, QTc-aralığında uzama, aritmi, bulantı ve kusmadır. Destekleyici ve semptomatiktedavi uygulanabilir. Akut bronşiyal obstrüksiyonu olan hastaya 3 saat içinde verilen 90mikrogramlık bir doz güvenlilik konusunda sorun yaratmamıştır.Çok yüksek dozlarda olsa bile, akut budesonid doz aşımının klinik açıdan sorun oluşturması beklenmez. Uzun süre çok yüksek dozlarda kullanılırsa, hiperkortisizm ve adrenal baskılanmasıgibi sistemik glukokortikosteroid etkileri ortaya çıkabilir. Formoterol doz aşımına bağlı olarak FORPACK tedavisinin kesilmesi gerekirse, inhalasyon yoluyla kullanılan uygun bir kortikosteroid tedavisinin uygulanması düşünülmelidir. 14 5. FARMAKOLOJİK ÖZELLİKLER5.1. Farmakodinamik özelliklerFarmakoterapötik grup: Adrenerjikler ve obstrüktif solunum yolu hastalıklarında kullanılan diğer ilaçlar ATC kodu: R03AK07 Etki mekanizması ve farmakodinamik özellikleri:FORPACK, formoterol ve budesonid içerir ve her ikisinin de etki mekanizmaları farklıdır ve astım alevlenmelerinin azalabilmesi için aditif etki gösterirler. Budesonid ve formoterolünspesifik özellikleri bu kombinasyonun, hem idame hem de semptom giderici tedavidekullanılmasını sağlamaktadır. Budesonid Budesonid inhale edildiğinde, solunum yollarında doza bağımlı antienflamatuvar etki gösteren, semptomlarda ve astım alevlenmelerinde azalma sağlayan bir glukokortikosteroiddir.İnhalasyon yolu ile kullanılan budesonid, sistemik kortikosteroidlere göre daha az ciddi adversetkilere sahiptir. Glukokortikosteroidlerin bu antienflamatuvar etkisinden sorumlu olan esasmekanizma bilinmemektedir. Formoterol Formoterol, geri dönüşümlü solunum yolu obstrüksiyonu olan hastalarda inhale edildiğinde, bronş düz kasında hızlı ve uzun etkili gevşeme sağlayan, selektif bir beta 2-adrenerjik agonisttirBronş genişletici etkisi doza bağımlı olarak 1-3 dakika içinde hızla başlar ve tek bir dozdansonra etkisi en az 12 saat sürer.Klinik etkililik ve güvenlilikFormoterol / Budesonid kombinasyonunun idame tedavisinde klinik etkililik2-agonist kullanılmıştır. Anti-astmatik etkinin zamanlaazaldığına dair hiçbir bilgi yoktur.Pediyatrik hastalarda yapılan 12 haftalık bir çalışmada, 6-11 yaş arasındaki 265 çocuk formoterol / budesonid kombinasyonu idame dozu ile (4,5/80 mikrogram/inhalasyonkombinasyonu ile günde iki kez, 2 inhalasyon) ve gerekli hallerde kısa etkili bir beta 2-agonistile tedavi edilmişlerdir. Akciğer fonksiyonunda düzelme görülmüştür ve tedavi, budesonidinkarşılık gelen dozu ile kıyaslandığında, iyi tolere edilmiştir.15 Formoterol / Budesonid kombinasyonunun idame ve semptom giderici tedavisinde klinik etkililikAltı veya on iki ay süren 5 adet çift-kör etkililik ve güvenlilik çalışmasında (4.447 hasta formoterol/budesonid kombinasyonu idame ve semptom giderici tedavi için rastgeleseçilmiştir.) toplam 12.076 astım hastası yer almıştır. İnhale glukokortikosteroidlerinkullanılmasına rağmen çalışmalara alınan hastaların semptomatik olması gerekmiştir. Beş adet çalışmadaki bütün karşılaştırma gruplarında, formoterol/budesonid kombinasyonu idame ve semptom giderici tedavinin şiddetli alevlenmelerde hem istatistiksel hem de klinikaçıdan anlamlı azalmalar sağladığı gösterilmiştir. Bu çalışmalardan ikisinde formoterol /budesonid kombinasyonu idame ve semptom giderici tedavi, yüksek idame dozundaformoterol/ budesonid kombinasyonu ile birlikte semptom giderici olarak terbutalin (çalışma735), benzer idame dozda formoterol / budesonid kombinasyonu ile birlikte semptom gidericiolarak terbutalin ya da formoterolün kullanılması (çalışma 734) (Tablo 1) karşılaştırılmıştır.Çalışma 735'te akciğer fonksiyonu, semptom kontrolü ve semptom giderici tedavi kullanımıtüm tedavi guplarında benzerdir. Çalışma 734'te, her iki tedavi ile karşılaştırıldığında,semptomlar ve semptom giderici tedavi azaltılmış, akciğer fonksiyonu düzelmiştir. 5çalışmanın kombine analizinde, formoterol / budesonid kombinasyonu idame ve semptomgiderici tedavi uygulanan hastalara, tedavi günlerinin %57'sinde herhangi bir semptom gidericitedavi uygulanmamıştır. Tolerans gelişimine dair herhangi bir bulgu elde edilmemiştir.
16 b Alevlenme sıklığında azalma her iki karşılaştırmada için istatistiksel (P değeri < 0,01) olarak önemlidir. Yukarıda belirtilen 5 çalışma ile 160/4,5 mikrogram ile günde iki kez iki inhalasyon düzeyindeki daha yüksek bir idame dozunun kullanıldığı ek bir çalışmayı kapsayan altı çift-körçalışmada adolesanlar ve erişkinlerde kıyaslanabilir bir etkililik ve güvenlilik ortaya konmuştur,Bu değerlendirmeler 1.847'si adolesan olan 14.385 astım hastasını temel almıştır.Budesonid/formoterol idame tedavisi ve semptom giderici olarak en az bir gün boyunca 8'denfazla inhalasyon alan adolesan hastaların sayısı sınırlıdır ve bu biçimde kullanım seyrek birdurumdur. Akut astım semptomlarından ötürü medikal dikkat gerektiren hastalar ile yapılan diğer iki çalışmada formoterol / budesonid kombinasyonu, bronkokonstrüksiyonda, salbutamol veformoterola benzer hızda ve etkinlikte rahatlama sağlamıştır. 5.2. Farmakokinetik özelliklerGenel özelliklerEmilimFormoterol/budesonid kombinasyonu ve bileşimindeki budesonid ve formoterolü tek başına içeren ilaçların, budesonid ve formoterolün sistemik yararlanımları açısından biyoeşdeğerolduğu gösterilmiştir. Buna rağmen bileşimindeki maddeleri tek başına içeren ilaçlarlakıyaslandığında, formoterol/budesonid kombinasyonu ile kortizol baskılanmasında hafif birartış görülmüştür. Bu farkın klinikteki güvenlilik üzerine bir etkisi yoktur. Budesonid ve formoterolün farmakokinetik etkileşime ilişkin bir kanıt yoktur. Budesonid ve formoterolü tek başına içeren preparatların veya formoterol/budesonid kombinasyonunun uygulanmasından sonra her bir maddenin farmakokinetik parametrelerikarşılaştırılabilir. Budesonid, kombinasyon şeklinde uygulandığında, eğri altındaki alanı(EAA) biraz yüksek, emilimi daha hızlı ve doruk plazma konsantrasyonu biraz daha yüksektir.Formoterol tek başına ya da kombinasyon şeklinde kullanıldığında, doruk plazmakonsantrasyonları birbirine yakındır. İnhalasyonla alınan budesonid hızla emilir ve dorukplazma konsantrasyonuna 30 dakika içinde ulaşılır. Yapılan çalışmalarda, inhalasyon cihazıaracılığıyla inhale edilen budesonidin akciğerlere ulaşan miktarı, hastaya ulaşan dozun %32-44'ü kadardır. Uygulanan dozun sistemik yararlanımı, hastaya ulaşan dozun yaklaşık %49'ukadardır. 6-16 yaş çocuklarda akciğerdeki depozisyonu, aynı doz verilen yetişkinler ile aynıaralığa denk gelmektedir, sonuç plazma konsantrasyonları saptanmamıştır. İnhale edilen formoterol hızla emilir ve 10 dakika içinde doruk plazma konsantrasyonuna ulaşır. Yapılan çalışmalarda, inhalasyon cihazı aracılığıyla inhale edilen formoterolün akciğerlereulaşan miktarı, hastaya ulaşan dozun %28-49'udur. Sistemik yararlanım, hastaya ulaşan dozunyaklaşık %61'i kadardır. 17 Dağılım:Formoterol yaklaşık %50, budesonid %90 oranında plazma proteinlerine bağlanır. Dağılım hacmi, formoterol için yaklaşık 4 L/kg, budesonid için ise yaklaşık 3 L/kg'dır. Biyotransformasyon:Formoterol konjugasyon reaksiyonları ile metabolize olur (aktif O-demetilasyon ve deformilasyon metabolitleri oluşur, ancak bunlar inaktif konjugatlar olarak görülür). Budesonidkaraciğerden ilk geçişi sırasında (yaklaşık %90) ilk geçiş metabolizmasına uğrayarakglukokortikosteroid aktivitesi düşük metabolitlerine dönüşür. En önemli metabolitleri olan 6-P-hidroksibudesonid ve 16-a-hidroksiprednizolonun glukokortikosteroid aktivitesibudesonidin aktivitesinin %1'inden azdır. Budesonid ve formoterol arasında herhangi birmetabolik etkileşim ya da yer değiştirme reaksiyonları olduğuna ilişkin bulgu yoktur. Eliminasyon:Formoterol dozunun büyük bir kısmı karaciğerde metabolize olarak böbrekler aracılığıyla atılır. İnhalasyondan sonra hastaya ulaşan formoterol dozunun %8-13'lük miktarı metabolizeedilmeden idrarla atılır. Formoterolün sistemik klerensi yüksektir (yaklaşık 1,4 L/dak.) veplazma yarılanma süresi ortalama 17 saattir. Budesonid, CYP3A4 enziminin katalize ettiği reaksiyonlar ile metabolize olarak atılır. Budesonid metabolitleri, aynen ya da konjuge edilerek böbrekler aracılığıyla atılır. İdrardadeğişmemiş halde budesonid miktarı ihmal edilebilir düzeydedir. Budesonidin sistemik klerensiyüksektir (yaklaşık 1,2 L/dak.) ve intravenöz yoldan uygulandığında plazma eliminasyonyarılanma süresi ortalama 4 saattir. Formoterol ve budesonidin, çocuklarda ve böbrek yetmezliği olan hastalardaki farmakokinetiği konusunda bilgi yoktur. Karaciğer yetmezliği olanlarda budesonid ve formoterolün sistemikyararlanımı artabilir. Doğrusallık / Doğrusal olmayan durum:Hem formoterol hem de budesonid için sistemik maruziyet uygulanan doz ile doğrusal bir ilişki içindedir. 5.3. Klinik öncesi güvenlilik verileriBudesonid ve formoterolün tek başına ya da ikisinin kombinasyonu ile hayvanlarda yapılan toksisite çalışmalarında görülen etkileri, abartılmış farmakolojik etkilerdir. Üreme ile ilgili hayvan çalışmalarında budesonid gibi kortikosteroidlerin malformasyonlara (yarık damak, iskelet malformasyonları) sebep olduğu gösterilmişse de bu etkilerin önerilendozlarla tedavi edilen insanlar için geçerli olmadığı görülmüştür. Hayvanlarda, formoterol ileyapılan üreme çalışmalarında, sistemik yararlanımın yüksek olduğu erkek sıçanlarda fertilitedeazalma ve sistemik yararlanımın klinikteki kullanımdan önemli ölçüde yüksek olduğudurumlarda, implantasyon kayıpları ile birlikte postnatal yaşam süresinde ve doğum kilosundaazalma gözlenmiştir. Ancak bu hayvan deneylerinin sonuçları insanlar için geçerli değildir. 18 6. FARMASÖTİK ÖZELLİKLER6.1. Yardımcı maddelerin listesiHFA 227EA Oleik asitEtanol 6.2. GeçimsizliklerGeçerli değil. 6.3. Raf ömrü24 ay 6.4. Saklamaya yönelik özel tedbirler25°C altındaki oda sıcaklığında saklayınız. Direkt gün ışığından ve donmaktan koruyunuz. Aerosol kutusu delinmemeli, boş olsa bile kırılmamak, ateşten uzak tutulmalıdır. 6.5. Ambalajın niteliği ve içeriğiFORPACK 6 mcg/100 mcg aerosol inhalasyonu, süspansiyon, koruyucu ambalaj içerisinde, 120 dozluk aerosol tüplerde karton kutuda kullanma talimatı ile birlikte sunulmaktadır. 6.6. Beşeri tıbbi üründen arta kalan maddelerin imhası ve diğer özel önlemlerKullanılmamış olan ürünler ya da atık materyaller Tıbbi Atıkların Kontrolü Yönetmeliği ve Ambalaj ve Ambalaj Atıklarının Kontrolü Yönetmeliğine uygun olarak imha edilmelidir. 7. RUHSAT SAHİBİNeutec İnhaler İlaç San. ve Tic. A.Ş. Arifiye / Sakarya Telefon: 0 850 201 23 23Faks: 0 212 481 61 11E-mail: [email protected] 8. RUHSAT NUMARASI (LARI)255/53 9. İLK RUHSAT TARİHİ/RUHSAT YENİLEME TARİHİİlk ruhsat tarihi: 25.12.2013 Ruhsat yenileme tarihi: 10. KÜB'ÜN YENİLENME TARİHİ19 |
İlaç BilgileriForpack 6/100 Mcg İnhalasyon İçin Ölçülü Dozlu AerosolEtken Maddesi: Formoterol Fumarat Dihidrat,budesonid Kullanma talimatı ve kısa ürün bilgileri
Google Reklamları
|
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
Ana Sayfa | Hakkımızda | İlaçlar | İlaç Ara | İlaç Firmaları | Gizlilik | Bize Ulaşın
Telif Hakkı 2008-2026 © İlaç Prospektüsü. Tüm Hakları Saklıdır.Uyarı: Sitemizde yayınladığımız ilaç bilgileri ile doktora danışmadan kesinlikle ilaç kullanmayınız!
Aksi halde doğabilecek sağlık sorunlarından ilacprospektusu.com sorumlu tutulamaz.