Diane 2 Mg/ 35 Mcg Kaplı Tablet Kısa Ürün BilgisiKISA ÜRÜN BİLGİSİ¡ Bu ilaç ek izlemeye tabidir. Bu üçgen yeni güvenlilik bilgisinin hızlı olarak belirlenmesini sağlayacaktır. Sağlık mesleği mensuplarının şüpheli advers reaksiyonları TÜFAM'abildirmeleri beklenmektedir. Bakınız Bölüm 4.8 Advers reaksiyonlar nasıl raporlanır? 1. BEŞERİ TIBBİ ÜRÜNÜN ADIDIANE ® 2 mg/35 mcg kaplı tablet 2. KALİTATİF VE KANTİTATİF BİLEŞİMEtkin madde:2 mg siproteron asetat 0,035 mg etinilestradiol Yardımcı maddeler:30,965 mg laktoz monohidrat (sığır kaynaklı) 19,371 mg sukroz Yardımcı maddeler için bölüm 6.1'e bakınız. 3. FARMASÖTİK FORMKaplı tablet Bej renkli, bombeli, yuvarlak tabletler 4. KLİNİK ÖZELLİKLER4.1. Terapötik endikasyonlar Doğurganlık çağındaki kadınlarda androjen duyarlılığına bağlı orta dereceli ila şiddetli akne (sebore ile birlikte veya tek başına) ve/veya hirsutizm tedavisi. Akne tedavisinde yalnızca topikal veya sistemik antibiyotik tedavisinin başarısız olduğudurumlarda. Hormonal kontraseptif gibi etki gösterdiğinden, diğer hormonal kontraseptiflerle birlikte kullanılmamalıdır (bkz. Bölüm 4.3). 4.2. Pozoloji ve uygulama şekliPozoloji / uygulama sıklığı ve süresi:DIANE ovülasyonu inhibe eder ve böylece gebeliği önler. DIANE kullanan hastalarda ek bir hormonal kontraseptif, hasta aşırı doz hormona maruz kalacağından ve aşırı doz alımı etkilikontrasepsiyon için gerekli olmadığından kullanılmamalıdır. Kullanım süresiSemptomların hafiflemesine kadar geçen süre en az üç aydır. Tedaviyi sürdürme ihtiyacı, tedavi eden hekim tarafından düzenli olarak değerlendirilmelidir. Uygulama şekli:Oral kullanım İlk tedavi kürü: Menstrual siklusun ilk gününde başlanmak üzere 21 gün boyunca, her gün 1 tablet (menstrüasyonun ilk günü 1. gün olarak sayılır) alınır. Sonraki kürler: Sonraki her küre, ilk tedavi kürü olan 21 günlük uygulamayı takiben, tablet kullanılmadan geçen 7 günün ardından başlanır. 1/19 DIANE'in kontraseptif olarak kullanıldığı durumlarda, yukarıdaki koşullara kesin olarak uyulmalıdır. Tablet alınmayan dönemde beklenen çekilme kanaması görülmezse, sonrakipakete geçilmeden önce gebelik olasılığı ortadan kaldırılmalıdır. Kontraseptif etkinlik için, oral yolla kullanılan bir kontraseptiften DIANE'e geçiş durumunda aşağıdaki talimatlara uyulmalıdır: 21 günlük kombine oral kontraseptiflerden (KOK) geçiş: İlk DIANE önceki oral kontraseptif kürünün bitimini takiben, ilk gün hemen alınmalıdır. Ek kontraseptif önlemler gereklideğildir. DIANE'in ilk paketi kullanılırken kanama meydana gelmeyecektir. İlk paketinbitiminden sonra kanama başlayacaktır. 28 günlük KOK'lardan geçiş: DIANE, günlük hap paketindeki son aktif hap alımını takip eden gün alınmalıdır. Ek kontraseptif önlemler gerekli değildir. Yalnızca progesteron içeren haplardan geçiş: İlk DIANE tablet, o gün progesteron içeren hap alınmış bile olsa, kanamanın başladığı ilk gün alınmalıdır. Ek kontraseptif önlemler gereklideğildir. Kalan progesteron içeren haplar atılmalıdır. Doğum veya düşük sonrası kullanım: Gebelik sonrasında hasta tamamen yürüyebilir durumdaysa ve doğumsal bir komplikasyonu yoksa, DIANE kullanımına, doğumdan 21 günsonra başlanılabilir. İlacın alındığı ilk 7 gün, ek kontraseptif önlemler alınmalıdır. Doğumsonrası ilk ovulasyon, ilk kanamadan önce gerçekleşebileceği için, doğum ve ilk tedavi kürüarasındaki dönemde başka bir kontrasepsiyon yöntem kullanılmalıdır. DIANE laktasyonsüresince kontrendikedir. İlk trimester düşüğünden sonra DIANE'e hemen başlanılabilir. Bunun anlamı ilk tabletin alınmasıyla birlikte doğum kontrolü başlamış olacağıdır. Bu durumda ek bir kontraseptif önlem gerekli değildir. Doğumu veya ikinci trimestr düşüğünü takiben 21-28. günlerde başlanması önerilir. Daha sonra başlandığı takdirde tablet alımının ilk 7 günü ek birbariyer yöntemi kullanılmalıdır. Eğer o zamana kadar ilişki gerçekleştiyse, DIANE kullanımınabaşlamadan önce gebelik ekarte edilmeli veya ilk menstrüel kanama beklenmelidir. İlave kontrasepsiyonun gerekli olduğu özel durumlar: uygulama: Tablet alımı unutulduğunda, alımı geciken tablet hemen alınmalıdır. Tablet, 12 saatlik doğru süre içerisinde alınabilirse, tabletin kontraseptif koruyucu özelliği değişmez.Ancak daha uzun süreli gecikmelerde, ek kontrasepsiyon gerekir. Bu durumda yalnızca enyakın zamanlı gecikmiş tablet alınmalı, daha önce unutulan tablet/tabletler atlanmalı ve 7 günboyunca tablet alımına devam ederken, ek olarak hormonal olmayan kontrasepsiyon metodu(ritim veya sıcaklık metodu dışındaki) uygulanmalıdır. Ek olarak, paket içerisindeki son 7günlük tablet/tabletlerin alımı unutulursa, sonraki pakete geçmeden önceki ara verilmemelidir.Bu durumda çekilme kanamasının yeni paket bitene kadar olması beklenmez. Tabletlerinalındığı günlerde bazı ara kanamalar oluşabilir; ancak, bu klinik olarak önemli değildir.Hastada, ikinci paket bitimini takiben, tablet kullanılmayan ara dönemde beklenen çekilmekanaması gerçekleşmezse, sonraki pakete geçilmeden önce, gebelik olasılığı ortadankaldırılmalıdır. Gastrointestinal bozukluk: Kusma ve diyare hali oral kontraseptiflerin tam emilimini engelleyerek etkilerini azaltabilir. Böyle bir durumda mevcut paketteki tabletlerin kullanımınadevam edilmelidir. Ek olarak, hormonal olmayan (ritim veya sıcaklık metodu dışındaki)kontrasepsiyon metodu gastrointestinal bozukluğun devam ettiği sürece ve onu takip eden 7gün boyunca kullanılmalıdır. Eğer, bu 7 günlük süre içerisinde paketteki tüm tabletler biterise, bir sonraki pakete ara verilmeden başlanmalıdır. Bu durumda çekilme kanamasının ikincipaket bitimine kadar olması beklenmez. Hastada, ikinci paket bitimini takiben, tabletkullanılmayan ara dönemde beklenen çekilme kanaması gerçekleşmezse, sonraki pakete 2/19 geçilmeden önce, gebelik olasılığı ortadan kaldırılmalıdır. Gastrointestinal bozukluğun uzadığı durumlarda, diğer kontrasepsiyon yöntemleri düşünülmelidir. Özel popülasyonlara ilişkin ek bilgiler:Böbrek yetmezliği:DIANE böbrek yetmezliği olan hastalarda özel olarak araştırılmamıştır. Mevcut veriler bu hasta popülasyonu için tedavide bir değişiklik yapılmasınıgöstermemektedir.Karaciğer yetmezliği:DIANE şiddetli karaciğer hastalıkları olan kadınlarda kontrendikedir. Ayrıca '4.3 Kontrendikasyonlar' bölümüne bakınız.Pediyatrik popülasyon:DIANE yalnızca menarştan sonra endikedir.Geriyatrik popülasyon:4.3. KontrendikasyonlarÖstrojen/progesteron kombinasyonları içeren preparatlar aşağıdaki koşulların varlığında kullanılmamalıdır ve kullanımları sırasında bunlardan herhangi biri ortaya çıkacak olursa,tedavi hemen kesilmelidir. Etkin ya da yardımcı maddelerden herhangi birine karşı aşırı duyarlılık. Diğer hormonal kontraseptiflerle eşzamanlı kullanım (bkz. Bölüm 4.1) Geçmişte veya devam etmekte olan venöz tromboz (derin venöz tromboz, pulmonerembolizm) Geçmişte veya devam etmekte olan arteriyel tromboz (örn. miyokard enfarktüsü) ya daön belirtileri (örn. anjina pektoris ve geçici iskemik atak) Serebrovasküler kaza bulgusu veya öyküsü Venöz veya arteriyel trombozla ilgili şiddetli veya birden fazla risk faktörünün varlığı(bkz. Bölüm 4.4), örneğin; Vasküler semptomların eşlik ettiği diyabet Şiddetli hipertansiyon Şiddetli dislipoproteinemi Aktifleşmiş protein (APC) direnci, antitrombin-III eksikliği, protein C eksikliği, protein Seksikliği, hiperhomosisteinemi ve antifosfolipid antikorları (antikardiyolipin antikorları,lupus antikoagülanı) gibi venöz veya arteriyel trombozla ilgili kalıtsal veya edinilmişyatkınlık Fokal nörolojik belirtili migren öyküsü Karaciğer fonksiyon değerleri normale dönmediği sürece aktif viral hepatit ve şiddetlisiroz gibi şiddetli karaciğer hastalığı varlığı veya öyküsü. Ombitasvir, paritaprevir, ritonavir veya dasabuvir ve bunların kombinasyonlarını içerendoğrudan etkili antiviral (DEA) tıbbi ürünlerin kullanımı (bkz. Bölüm 4.4. ve 4.5) Karaciğer tümörü varlığı veya öyküsü (iyi veya kötü huylu) Devam eden meme kanseri veya meme kanseri öyküsü. Menenjiyom veya menenjiyom öyküsü Tanı konulmamış vajinal kanamanın altında yatan şüpheli nedenler araştırılmalıdır. Bilinen gebelik varlığı veya gebelik şüphesi (bkz. Bölüm 4.6) Laktasyon (bkz. Bölüm 4.6) DIANE erkeklerde kullanılmaz. 3/19 4.4. Özel kullanım uyarıları ve önlemleriTıbbi MuayeneOral kontraseptif kullanmaya başlamadan önce (ve sonrasında düzenli aralıklarla) her bir kadının ve ailesinin tıbbi öyküsü değerlendirilmelidir. Fizik muayene bu şekilde ve bu ürünleilgilikontrendikasyonlar (Bölüm 4.3) ile uyarılar (Bölüm 4.4) doğrultusunda yönlendirilmelidir. Bu değerlendirmelerin içeriği ve sıklığı ilgili kılavuzlar doğrultusunda olmalı ve kadına özgü şekilde uyarlanmalı, ancak kan basıncı ölçümünü içermeli, doktorungerekli görmesi halinde meme, batın ve pelvik incelemelerinin yanı sıra servikal sitolojideğerlendirilmelidir. Tedaviye başlanmadan önce gebelik olasılığı dışlanmalıdır. Uyarılar DIANE, aylık döngünün 21 günü süresince kullanılmak üzere progesteron olarak siproteron asetat, östrojen olarak etinilestradiol içermektedir. KOK benzeri bir bileşime sahiptir. Kullanım süresi Semptomların hafiflemesine kadar geçen süre en az üç aydır. Tedaviyi sürdürme ihtiyacı, tedavi eden hekim tarafından düzenli olarak değerlendirilmelidir (bkz. Bölüm 4.2). Kadınlara DIANE'in HIV enfeksiyonlarına (AIDS) ve diğer cinsel yolla bulaşan hastalıklara karşı koruma sağlamadığı söylenmelidir. Sıkı tıbbi gözetim gerektiren durumlarAşağıdaki durum/risk faktörlerinin mevcut olması halinde, hastaya özgü olası risklere karşın DIANE kullanımına ilişkin yarar tartışılmalı ve DIANE kullanmaya başlamadan öncehastayla kullanım konusu değerlendirilmelidir. Bu durum veya risk faktörlerinin herhangibirinin ilk kez ortaya çıkması, şiddetlenmesi veya alevlenmesi halinde hasta hekimiyle irtibatageçmelidir. Doktor da DIANE kullanımına devam edilip edilmemesi konusunda kararvermelidir. Hafif vasküler hastalık veya hafif nefropati, retinopati ya da nöropatiyle birlikte diyabet Sistolik kan basıncı >140 ila 159 mm Hg veya diyastolik kan basıncı >90 ila 94 mm Hg olacak şekilde yeterli düzeyde kontrol edilen hipertansiyon (bkz. ayrıca Bölüm 4.4DIANE'in derhal kesilmesini gerektiren nedenler) Porfiria Klinik depresyon Obezite Migren Kardiyovasküler hastalıklar Kloazma Depresyon veya yukarıda bahsedilen durumların herhangi birine ilişkin öyküsü olan hastalar DIANE tedavisi sırasında takip edilmelidir. Depresif duygudurumu ve depresyon hormonal kontraseptif kullanımıyla sık görülen yan etkilerdir (bkz. Bölüm 4.8). Depresyon ciddi olabilir ve intihar davranışı ve intihar için iyibilinen bir risk faktörüdür. Duygudurum dalgalanmaları ve depresif semptomlar olmasıhalinde, bu semptomlar tedavinin başlamasından kısa bir süre sonra ortaya çıksa dahikadınlara doktorlarına başvurmaları önerilmelidir. 4/19 DIANE'in derhal kesilmesini gerektiren nedenlerOral kontrasepsiyonu keserken, gerekli olması halinde kontraseptif korumanın sürdürülmesini sağlamak için hormonal olmayan kontrasepsiyon kullanılmalıdır. 1. Migren ağrılarının ilk kez ortaya çıkması veya şiddetlenmesi veya olağan olmayan sıklıkta veya şiddette baş ağrılarının oluşması 2. Ani görme veya duyma bozuklukları veya diğer algısal bozukluklar durumu 3. Tromboz veya kan pıhtılarına ilişkin ilk belirtiler (örn., bacak/bacaklarda şişme veya olağan olmayan ağrı, nefes alırken hissedilen keskin ağrı veya nedensiz öksürmeler).Göğüste ağrı ve darlık hissi. 4. Elektif majör operasyonlardan en az dört hafta önce (örn., abdominal veya ortopedik),bacaklara herhangi bir cerrahi müdahale uygulanması halinde, varislerin medikal tedavisiveya uzun süreli hareketsizlik durumunda; örn., kaza veya operasyon sonrası durumlar.Tamamen iyileştikten sonraki 2 hafta boyunca ilaca başlanılmamalıdır. Acil cerrahimüdahalenin gerektiği durumlarda, genellikle trombotik profilaksi uygulanır;örn.,subkutan heparin. 5. Sarılık, hepatit ve tüm vücutta kaşıntı 6. Kan basıncında belirgin artış 7. Şiddetli depresyon başlangıcı 8. Şiddetli üst abdominal ağrı veya karaciğerde büyüme 9. Hormonal kontraseptif kullanımı veya gebelik sırasında bozulduğu bilinen koşullarda belirgin kötüleşme (bkz. Bölüm 4.4 'Diğer Durumlar' başlığı altındaki 'Gebelik veyaönceki KOK veya DIANE kullanımı sırasında kötüleşen durumlar') 10. Gebelik hemen kesilmesini gerektiren nedenlerden biridir (bkz. Bölüm 4.6). Dolaşım bozuklukları DIANE kullanımı, venöz tromboembolizm (VTE) riskini bu ilacın kullanılmamasıdurumuna kıyasla arttırmaktadır. Artan VTE riskinin en yüksek olduğu dönem DIANEkullanımına başlandıktan sonraki bir yıllık dönem veya doğum kontrol hapı kullanımına enaz bir ay ara verildikten sonra tedaviye başlanan veya tedavinin değiştirildiği dönemdir.Venöz tromboembolizm olgularının %1-2'si ölümcül olabilmektedir. Epidemiyelojik çalışmalar, VTE insidansının DIANE kullanan kişilerde levonorgestreliçeren KOK kullanan kişilerden 1,5 ila 2 kat yüksek olduğunu vedesogestrel/gestoden/drospirenon içeren KOK'lara ilişkin riske benzer olabileceğinigöstermiştir. DIANE kullananlar arasında polikistik over sendromuyla ilişkili durumda olduğu gibikardiyovasküler riskin doğuştan artmış olduğu hastalar olabilir. Epidemiyolojik çalışmalar hormonal kontraseptif kullanımını arteriyel tromboembolizm(miyokard enfarktüsü, geçici iskemik atak) riskindeki artışla da ilişkilendirmiştir. Son derece nadir olmakla birlikte, hormonal kontraseptif kullananlarda diğer kandamarlarında (örn. Hepatik, mezenterik, renal, serebral veya retinal ven ve arterlerde)tromboz geliştiği bildirilmiştir. Venöz veya arteriyel tromboz ya da serebrovasküler olay semptomları arasında; tek taraflıolağan dışı bacak ağrısı/ bacakta şişme; göğüste ani ve şiddetli ağrı (sol kola yayılıpyayılmasına bakılmaksızın); ani soluksuzluk; aniden başlayan öksürük; herhangi bir olağandışı, şiddetli, uzun süreli baş ağrısı; ani kısmi veya tam görme kaybı; diplopi; geveleyerekkonuşma veya afazi; vertigo; fokal nöbetlerde birlikte veya nöbet olmaksızın bayılma;aniden başlayan, vücudun bir tarafını veya tamamını etkileyen güçsüzlük ya da belirginuyuşukluk; motor bozukluklar; 'akut' abdomen yer alabilir. Venöz tromboembolik olay riski aşağıdaki durumlarda artmaktadır: 5/19 - Artan yaş; - Sigara kullanımı (risk özellikle 35 yaş üzerindeki kadınlarda tiryakilikle ve yaşınilerlemesiyle daha da artmaktadır). 35 yaş üzerinde olup DIANE kullanmak isteyenkadınlarda kesinlikle sigara içmemeleri önerilmelidir; - Pozitif aile öyküsü (kardeş veya ebeveynde nispeten genç yaşta venöz tromboembolizmgelişmesi). Kalıtsal yatkınlıktan şüphelenilmesi halinde, kadının herhangi bir hormonalkontraseptif kullanımıyla ilgili karar vermeden önce bir uzmana sevk edilmesigerekmektedir; - Uzun süreli hareketsizlik, majör ameliyat, herhangi bir bacak ameliyatı veya majörtravma. Bu durumlarda kullanımının bırakılması (elektif ameliyat durumunda en az dörthafta önceden) ve hareketin tamamen kazanılmasından sonraki iki haftaya kadar tekrarbaşlanılmaması önerilebilir. DIANE kullanımının kesilmemiş olduğu durumlardaantirombotik tedavi düşünülmelidir. - Obezite (vücut kitle indeksinin 30 kg/m2 'den fazla olması). Venöz tromboembolizmde yüzeysel tromboflebit ve varikoz venlerin olası rolü konusunda herhangi bir görüş birliği yoktur. Arteriyel tromboembolik komplikasyon veya serebrovasküler olay riski aşağıdakilerleartmaktadır: - Artan yaş; - Sigara kullanımı (risk özellikle 35 yaş üzerindeki kadınlarda tiryakilikle ve yaşınilerlemesiyle daha da artmaktadır) 35 yaş üzerinde olup DIANE kullanmak isteyenkadınlara kesinlikle sigara içmemeleri önerilmelidir; - Dislipoproteinemi; - Obezite (vücut kitle indeksinin 30 kg/m2 'den fazla olması); - Hipertansiyon; - Migren; - Valvüler kalp hastalığı; - Atriyal fibrilasyon; - Pozitif aile öyküsü (kardeş veya ebeveynde nispeten genç yaşta arteriyel trombozgelişmiş olması) Kalıtsal yatkınlıktan şüphelenilmesi halinde, kadının herhangi birhormonal kontraseptif kullanımıyla ilgili karar vermeden önce bir uzmana sevk edilmesigerekmektedir. Dolaşımla ilgili advers olaylarla ilişkilendirilmiş olan diğer tıbbi durumlar arasındadiyabet, sistemik lupus eritematozus, hemolitik üremik sendrom, kronik inflamatuvarbağırsak hastalığı (örn. Crohn hastalığı veya ülseratif kolit) ve orak hücreli anemi vardır. Lohusalık döneminde tromboembolizm riskinin arttığı mutlaka dikkate alınmalıdır('Gebelik ve Emzirme' ile ilgili bilgi için bkz. Bölüm 4.6). DIANE kullanımı sırasında migrenin sıklık veya şiddetinde artış olması (serebrovasküler olaya ilişkin ön belirti olabilir) DIANE kullanımın derhal kesilmesini gerektirebilir. DIANE kullanan kadınların olası tromboz semptomlarıyla karşılaşmaları halindedoktorlarıyla irtibata geçmeleri gerektiği özellikle vurgulanmalıdır. Trombozdanşüphelenilmesi veya doğrulanması halinde, DIANE kullanımı kesilmelidir. Antikoagülantedavinin (kumarinler) teratojenisitesi nedeniyle uygun kontrasepsiyona başlanmalıdır. Dolaşım olaylarını etkileyen diğer faktörler Akne veya orta derecede şiddetli hirsutizme yönelik tedavi olarak DIANE kullanan hastalar genellikle polikistik over sendromu gibi kardiyovasküler riskin doğuştan artmış olduğu bireylerdir. 6/19 Venöz veya arteriyel trombozla ilgili kalıtsal veya edinilmiş yatkınlık göstergesi olabilen biyokimyasal faktörler arasında APC direnci, hiperhomosisteinemi, antitrombin-III eksikliği,protein C eksikliği, protein S eksikliği, antifosfolipid antikorları (antikardiyolipin antikorları,lupus antikoagülanı) yer almaktadır. Risk/yarar değerlendirmesi yaparken, hekim bir duruma yönelik yeterli tedavinin ilişkili tromboz riskini azaltabileceğini ve gebelikle ilişkili riskin KOK veya DIANE kullanımı ileilişkili riskten daha yüksek olduğunu hesaba katmalıdır. TümörlerDiğer birçok steroidlerde olduğu gibi, DIANE'in de çok yüksek dozda verilmesiyle, sıçan karaciğerinde karsinom dahil tümör insidansında artışa neden olduğu bulunmuştur. Bu bilginininsanlarla ilişkisi bilinmemektedir. Birçok epidemiyolojik çalışma KOK kullanan kadınlarda over, endometrium, serviks ve meme kanseri riskiyle ilgili bilgi sağlamıştır. Kanıtlar yüksek dozda KOK'ların over veendometrium kanseri bakımından önemli oranda koruma sağladığını açıkça ortayakoymaktadır. Bununla birlikte, düşük doz KOK'ların veya DIANE'in aynı düzeyde koruyucuetki sağlayıp sağlamadığı net değildir. Meme kanseri 54 epidemiyolojik çalışmanın meta analizleri sonucu, halen KOK kullanan kadınlarda tanı konan meme kanseri relatif riskinde (RR=1,24) hafif bir artış olduğunu göstermektedir. Gözlenen artmışrisk örneğin, KOK kullananlarda meme kanserinin daha erken tanısına, KOK'ların biyolojiketkilerine veya bu ikisinin kombinasyonuna bağlı olabilir. Meme kanseri tanısı almış halen KOKkullanan veya son on yıl içinde KOK kullanmış kadınlarda, KOK kullanmamış kadınlara oranlamemede lokalize olması olasılığı daha yüksektir. Meme kanseri 40 yaşın altındaki kadınlarda, KOK kullanmış olsun ya da olmasın seyrek görülür. Arka plandaki riskler yaşla birlikte artarken halen KOK kullanan veya KOKkullanmış kadınlardaki meme kanseri tanılarındaki artış, tüm meme kanseri riski ilekarşılaştırıldığında düşüktür (grafiğe bakınız). KOK kullanıcılarında meme kanseri için en önemli risk faktörü kadının KOK'u bırakma yaşıdır; bırakma yaşı daha büyük kadınlarda, meme kanseri tanısı daha fazladır. Kullanımsüresi daha az önemlidir ve 10 yıl kullanım aşırı risk oluşturmadığı gibi risk aşımı da KOKkullanmayı bıraktıktan sonra 10 yıl içinde kaybolur. Meme kanseri riskindeki olası artış KOK kullanan kadınlara anlatılmalı, kombine oral kontraseptiflerin diğer kanser riski oluşumlarına (over ve endometriyum kanseri) karşı önemlikoruma sağlıyor olması göz önüne alınarak yarar ve risk değerlendirilmelidir. 7/19 Hiç KOK kullanmamış olan 10.000 kadında meme kanseri tanısı alanların sayısına kıyasla 5 yıllık KOK kullanımı ve kullanım sonrası 10 yıla kadar olan süre içinde meme kanseri tanısıalan 10.000 kadına ilişkin tahmini kümülatif sayı: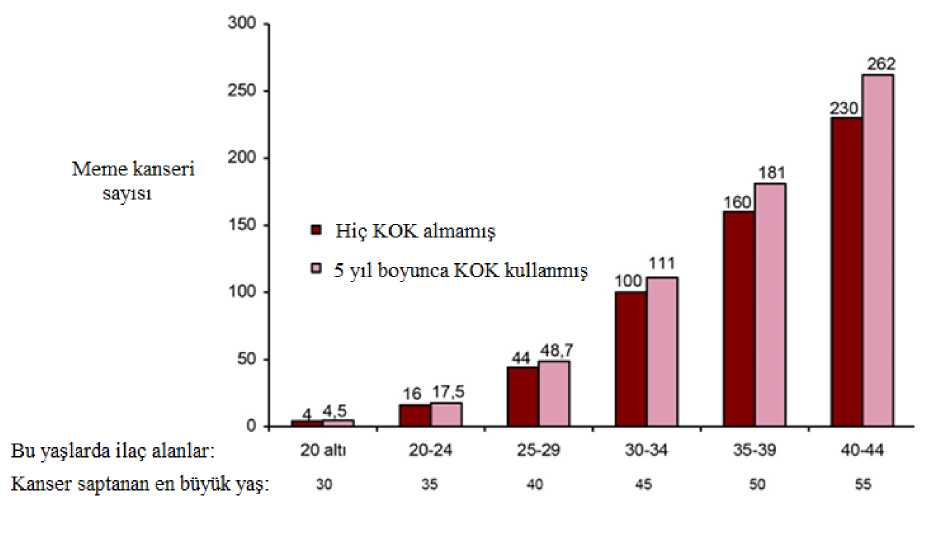
Serviks kanseri Serviks kanseriyle ilgili en önemli risk faktörü kalıcı HPV enfeksiyonudur. Bazı epidemiyolojik çalışmalar uzun süreli KOK kullanımının bu risk artışını daha daartırabileceğini göstermiş olmakla birlikte, bu bulgunun etki karışımı yapan faktörlere, örn.servikal tarama ve bariyer kontraseptif kullanımı dahil cinsel davranışa ne ölçüdeatfedilebileceği tartışmalı bir konudur. Karaciğer kanseri Hormonal maddelerin (DIANE'in içeriğinde bulunanlar gibi) kullanımından sonra, izole durumlarda hayati tehlike oluşturan ve intraabdominal kanamaya neden olan karaciğertümörleri (seyrek olarak benign ve daha seyrek olarak malign) gözlenmiştir. Üst abdomendeşiddetli şikayetler, karaciğer büyümesi veya intraabdominal kanama belirtileri meydanagelirse, ayırıcı tanıya karaciğer tümörü de dahil edilmelidir. Menenjiyom Özellikle 25 mg ve üzeri yüksek dozlarda ve uzun süreli siproteron asetat kullanımı ile ilişkili olarak menenjiyomların (tekli ve birden fazla) ortaya çıktığı bildirilmiştir (bkz. Bölüm 5.1).Bir hastaya menenjiyom teşhisi konulursa, ihtiyati tedbir olarak DIANE dahil olmak üzeresiproteron içeren tüm tedaviler durdurulmalıdır. 8/19 Diğer durumlar DIANE kullanımı sırasında birtakım kronik hastalıkların zaman zaman kötüleşmesi olasılığı göz ardı edilemez. Bilinen hiperlipidemiler Hipertrigliseridemi veya ilgili aile öyküsü bulunan kadınlarda KOK ya da DIANE kullanımı sırasında pankreatit bakımından risk artışı olabilir. Hiperlipidemisi olan kadınlar arteriyel hastalık bakımından artmış risk altındadır (bkz. Bölüm 4.4 'Dolaşım bozuklukları'). Bununla birlikte, KOK veya DIANE kullanan kadınlarda rutintarama yapılması uygun değildir. Kan basıncı Hipertansiyon inme ve miyokard enfarktüsüyle ilgili bir risk faktörüdür (bkz. Bölüm 4.4 'Arteriyel tromboembolik durumlar'). KOK veya DIANE gibi östrojen/progesteronkombinasyonları kullanan birçok kadında kan basıncında hafif artış bildirilmiş olmasınakarşın, klinik açıdan anlamlı artış nadiren gözlenmektedir. Bununla birlikte, DIANE kullanımısırasında kalıcı hipertansiyon gelişmesi halinde, antihipertansif tedavi komplike olmayanhastalar için 160/100 mm Hg düzeyinde, hedef organ hasarı, tanı almış kardiyovaskülerhastalık, diyabet ya da kardiyovasküler risk faktörlerinde artış olanlarda ise 140/90 mm Hgdüzeyinde başlatılmalıdır. DIANE kullanımına devam edilip edilmemesi konusu daha düşükkan basıncı düzeylerinde kararlaştırılmalıdır ve alternatif kontrasepsiyon tavsiye edilmelidir. Gebelikle veya önceki KOK veya DIANE kullanımı ile kötüleşen durumlar: Aşağıdaki durumların hem gebelik hem de bir KOK veya DIANE gibi östrojen/progesteron kombinasyonunun kullanımı ile meydana geldiği veya kötüleştiği bildirilmiştir.Aşağıdakilerin herhangi birinin kullanım sırasında meydana gelmesi halinde, DIANEbırakılmalıdır: Kolestaz ile ilişkili sarılık ve/veya kaşıntı KOK'lar veya DIANE safra kesesi taşı oluşumu riskini artırabilir veya mevcuthastalığı kötüleştirebilir Sistemik lupus eritematozus Herpes gestationis Otoskleroza bağlı işitme kaybı Orak hücre anemisi Renal disfonksiyon Herediter anjiyoödem Epilepsi Gebelik sırasında veya önceki KOK kullanımı veya DIANE kullanımı sırasındakadının kötüleşme yaşadığı herhangi bir diğer durum Karaciğer fonksiyonu bozuklukları Karaciğer fonksiyonlarının akut veya kronik bozuklukları, karaciğer fonksiyonu belirteçleri normale dönene dek KOK veya DIANE kullanımına ara verilmesini gerektirebilir. Diyabet (vasküler tutulum olmayan) 9/19 Vasküler hastalığı olmayan, insüline bağlı diyabetik hastalar DIANE kullanabilir. Ancak tüm diyabetli hastaların arteriyel hastalık bakımından artmış risk altında olduğu unutulmamalı veKOK veya DIANE reçete edilirken bu durum dikkate alınmalıdır. Mevcut vasküler hastalığıolan diyabetli hastaların DIANE kullanması kontrendikedir (bkz. Bölüm 4.3Kontrendikasyonlar) 'KOK'lar veya DIANE gibi östrojen/progesteron kombinasyonları periferik insülin direnci ve glukoz toleransı üzerinde etki gösterebilmekle birlikte, düşük doz KOK (0,05 mgetinilestradiolden az) kullanan diyabetli hastalarda terapötik kürün değiştirilmesiyle ilgilikanıt bulunmamaktadır. Bununla birlikte, diyabetli kadınlar KOK veya DIANE kullanımısırasında dikkatle izlenmelidir. Kloazma Zaman zaman, özellikle kloazma gravidarum öyküsü olan kadınlarda, kloazma ortaya çıkabilmektedir. Kloazma yatkınlığı olan kadınlar DIANE kullanırken güneş veya ultraviyoleradyasyon maruziyetinden kaçınmalıdır. Menstrual değişiklikler Menstrual akışın azalması: Bu durum olağan dışı değildir ve bazı hastalarda olması beklenir. Elbette önceden şiddetli periyod geçirenlerde bu durum yararlı olabilir. Menstruasyon atlaması: Bazen çekilme kanaması hiç olmaz. Tabletler doğru olarak alındıysa gebelik olası değildir. Çekilme kanamasında aksama tablete ara verilen dönemdegerçekleşirse, gebelik olasılığı diğer pakete başlanmadan önce ortadan kaldırılmalıdır. Intermenstrual kanama: Düzensiz kanama (lekelenme veya ara kanama) özellikle kullanımın ilk aylarında ortaya çıkabilir. Bu nedenle, düzensiz kanamaların oluşumu ancak yaklaşık üçdöngü süren adaptasyon döneminden sonra önem kazanmaktadır. Önceden düzenli olandöngüler sonrasında kanama düzensizlikleri ortaya çıktığı veya var olan düzensizlikler devamettiği takdirde, hormonal olmayan nedenler değerlendirilmeli ve malignite veya gebeliğindışlanması için uygun tanı amaçlı yöntemler kullanılmalıdır. Buna kürtaj da dahildir. Bazı kadınlarda DIANE kesildikten sonra amenore veya oligomenore (özellikle önceden bu tip sorunları olanlarda) gelişebilir. Kadınlar bu olasılık konusunda bilgilendirilmelidir. ALT yükselmeleri Hepatit C virüsü enfeksiyonları (HCV) için tedavi gören hastalarda, ribavirinli veya ribavirinsiz, ombitasvir/paritaprevir/ritonavir ve dasabuvir içeren tıbbi ürünlerle yapılan klinikçalışmalar sırasında, normalin üst sınırının (ULN) 5 katından fazla transaminaz (ALT)yükselmeleri, kombine hormonal kontraseptifler (KHK'lar) gibi etinilestradiol içeren ilaçlarkullanan kadınlarda önemli ölçüde daha sık meydana gelmiştir (bkz. Bölüm 4.3 ve Bölüm4.5). DIANE, 30,965 mg laktoz monohidrat (sığır kaynaklı) içermektedir. Nadir kalıtımsal galaktoz intoleransı, Lapp laktaz yetmezliği ya da glukoz galaktoz malabsorpsiyon problemi olanhastaların bu ilacı kullanmaması gerekir. Her bir tablet 19,371 mg sukroz içerir. Nadir kalıtımsal fruktoz intoleransı, glikoz-galaktoz malabsorpsiyon veya sükraz-izomaltaz yetmezliği problemi olan hastaların bu ilacıkullanmamaları gerekir. 10/19 4.5. Diğer tıbbi ürünler ile etkileşimler ve diğer etkileşim şekilleriEtkileşimler Karaciğer enzimi indükleyiciler Hepatik enzimleri (özellikle sitokrom P450 3A4) indükleyen ilaçlar kontraseptif steroidlerin metabolizmasını artırdığından ara kanama ve gebeliğe yol açabilir. Aşağıdaki durumların KOK'lar ve DIANE gibi östrojen/progesteron kombinasyonları ile klinik açıdan önemli etkileşimler sergilediği gösterilmiştir: Antiretroviral ajanlar Ritonavir Nelfinavir Nevirapin Antikonvülzanlar Barbitüratlar (fenobarbiton dahil) Primidon Fenitoin Karbamazepin Okskarbazepin Topiramat Antibiyotikler/antifungaller Griseofulvin Rifampisin Bitkisel ürünler Sarı kantaron (Hypericum perforatum) Karaciğer enzimi indükleyicileri ile etkileşimlerin yönetilmesi Mikrozomal enzimleri uyaran ilaçlarla (özellikle sitokrom P450 3A4) etkileşim gelişebilir, bu etkileşimler cinsiyet hormonu klirensinde artışa neden olabilir, bu durum da kanama ve/veyakontraseptif başarısızlıkla sonuçlanabilir. Birkaç günlük tedavinin ardından enzim indüksiyonu gözlemlenebilir. En fazla enzim indüksiyonu genellikle birkaç hafta içinde görülür. Enzim indüksiyonu, ilaç tedavisininkesilmesinin ardından 4 hafta kadar sürebilir. Bu ilaçlardan herhangi biriyle kısa süreli tedavi alan kadınların geçici olarak KOK'a ilave olarak bir bariyer yöntemi kullanmaları veya diğer bir kontrasepsiyon yöntemi seçmelerigerekmektedir. Bariyer yöntemi, eşzamanlı ilaç tedavisi ve bunu takip eden 28 gün süresincekullanılmalıdır. Bariyer yönteminin kullanıldığı dönem bir paketin içeriğini geçecek olursa,tablet alınmayan herhangi bir ara verilmeksizin sonraki kutuya başlanmalıdır. Bu durumda,ikinci kutunun sonuna kadar geri çekilme kanaması beklenmemelidir. Hastada ikinci kutununbitiminden sonraki tablet kullanılmayan aralıkta geri çekilme kanaması olmadığı takdirde,sıradaki kutuya devam edilmeden önce gebelik olasılığı dışlanmalıdır. Hepatik enzim indükleyicilerle uzun süreli tedavi gören kadınlarda farklı bir kontrasepsiyon yöntemi kullanılmalıdır. 11/19 DIANE klirensini artıran maddeler (enzimlerin uyarılmasıyla DIANE etkililiğinin azalması), örn.:Fenitoin, barbitüratlar, primidon, karbamazepin, rifampisin ve muhtemelen oksakarbazepin, topiramat, felbamat, griseofulvin ve sarı kantaron içeren ürünler. DIANE klirensi üzerine değişken etkilere sahip maddeler; örneğin: DIANE ile birlikte uygulandığında birçok HIV/HCV proteaz inhibitörü ve nükleozid olmayan ters transkriptazinhibitörleri plazma östrojen veya progesteron konsantrasyonlarını azaltabilmekte ya daartırabilmektedir. Bu değişiklikler bazı olgularda klinik açıdan anlamlı olabilir. DIANE klerensini azaltan maddeler (enzim inhibitörleri): Azol antifungaller (örn. itrakonazol, vorikonazol, flukonazol), verapamil, makrolidler (örn. klaritromisin, eritromisin), diltiazem vegreyfurt suyu gibi güçlü ve orta düzeyde CYP3A4 inhibitörleri östrojenin veya progestininveya her ikisinin plazma konsantrasyonunu artırabilir. 60 - 120 mg/gün dozlarında etorikoksibin, 0,035 mg etinilestradiol içeren kombine bir hormonal kontraseptif ile eşzamanlı olarak alındığında etinilestradiolplazma konsantrasyonlarını sırasıyla 1,4 - 1,6 kat arttırdığı görülmüştür. Diğer ilaçlar üzerine etkiler Oral kontraseptifler ve DIANE gibi östrojen/progesteron kombinasyonları diğer bazı ilaçların metabolizmasını etkileyebilir. Bunun sonucu olarak, plazma ve doku konsantrasyonlarıartabilmekte (örn. siklosporin) veya azalabilmektedir (örn. lamotrijin). in vitroetinilestradiol hem CYP2C19, CYP1A1 ve CYP1A2'nin geri döndürülebilir inhibitörü, hem de CYP3A4/5, CYP2C8, ve CYP2J2'nin mekanizma temelli inhibitörüdür.Klinik çalışmalarda etinilestradiol içeren bir hormonal kontraseptifin uygulanması, CYP3A4substratlarının (ör. midazolam) plazma konsantrasyonlarında herhangi bir artışa yol açmaz yada sadece zayıf bir artışa yol açarken, CYP1A2 substratlarının plazma konsantrasyonları hafif(ör. teofilin) veya orta düzeyde (ör. melatonin ve tizanidin) artabilmektedir.Not: Olası etkileşimlerin tanımlanması için eşzamanlı ilaçların reçeteleme bilgilerine bakılmalıdır. Farmakodinamik etkileşimler Ombitasvir, paritaprevir, ritonavir veya dasabuvir ve bunların ribavirinle veya ribavirinsiz kombinasyonlarını içeren doğrudan etkili antiviral (DEA) tıbbi ürünlerin etinilestradiol içerentıbbi ürünlerle birlikte uygulanmasının, ALT seviyelerinde sağlıklı kadın deneklerdeki veHCV ile enfekte kadınlardaki normal değerin üst sınırının 20 katından daha yüksek artışlarlailişkili olduğu gösterilmiştir (bkz. Bölüm 4.3 Kontrendikasyonlar). Bu nedenle, DIANEkullanıcıları, bu kombinasyona sahip ilaç rejimiyle tedaviye başlamadan önce alternatif birkontrasepsiyon yöntemine (örneğin, sadece progestajenle kontrasepsiyon veya hormonalolmayan yöntemler) geçmelidir. DIANE, bu kombinasyona sahip ilaç rejimi ile tedaviyitamamladıktan 2 hafta sonra yeniden başlatılabilir. Laboratuvar testleri Oral kontraseptif kullanımı karaciğer, tiroid, adrenal ve renal fonksiyonlara ilişkin biyokimyasal parametreleri, plazma taşıyıcı protein ve lipid/lipoprotein fraksiyonu düzeyleri,karbonhidrat metabolizması parametreleri ve pıhtılaşma ile fibrinoliz parametreleri gibi bazılaboratuvar testlerinin bulgularını etkileyebilir. Dolayısıyla, laboratuvar personeli laboratuvartestleri talep edildiğinde oral kontraseptif kullanımı konusunda bilgilendirilmelidir. 12/19 Özel popülasyonlara ilişkin ek bilgilerPediyatrik popülasyon:DIANE yalnızca menarştan sonra endikedir. Pediyatrikpopülasyonda yapılmış etkileşim çalışması bulunmamaktadır. 4.6. Gebelik ve laktasyonGenel tavsiye:Gebelik kategorisi: X Çocuk doğurma potansiyeli bulunan kadınlar / Doğum kontrolü (Kontrasepsiyon):DIANE kontraseptif gibi etki gösterdiğinden, kullanıldığı sürece fertiliteyi engeller. Gebelik dönemi:Gebelik süresince DIANE'in kullanımı kontrendikedir. DIANE kullanımı sırasında gebelik oluşursa kullanım derhal kesilmelidir. Laktasyon dönemi:DIANE kullanımı laktasyon süresince de kontrendikedir. Laktasyon döneminde DIANE kullanımı üretilen süt hacminde azalmaya ve sütün bileşiminde değişime neden olabilir. Etkinmaddelerin eser miktarları anne sütüne geçer. Bu miktarlar özellikle doğumdan sonraki ilk 6haftada bebeği etkileyebilir. Emziren annelere çocuklarını sütten kesene kadar DIANEalmamaları söylenmelidir. Üreme yeteneği / Fertilite:Hayvan çalışmalarında, dış genital farklılıkların oluştuğu embriyogenez fazında siproteron asetat kullanılması durumunda erkek fetusta feminizasyona neden olabileceği görülmüştür.Her ne kadar bu sonuçların insanlara uyması beklenmese de, gebeliğinin 45. gününden sonrakadınlara DIANE verilmesinin erkek fetüsün feminizasyonuna neden olabileceği olasılığıdikkate alınmalıdır. Buradan çıkan sonuç DIANE ile tedavi için gebelik, mutlakkontrendikasyon sebebidir ve tedaviye başlanmadan önce mutlaka ekarte edilmelidir. 4.7. Araç ve makine kullanımı üzerindeki etkilerB ilinmemektedir. 4.8. İstenmeyen etkilerDIANE ile en yaygın olarak bildirilen advers reaksiyonlar mide bulantısı, abdominal ağrı, kilo artışı, baş ağrısı, depresif ruh hali, duygu durum bozukluğu, meme ağrısı, memehassasiyetidir. Kullanıcıların > %1'inde meydana gelir. Ciddi advers reaksiyon tromboembolizmdir. Advers reaksiyonlar, aşağıda sistem-organ sınıfı (MedDRA) ve sıklık derecesine göre listelenmektedir. Sıklık dereceleri şu şekilde tanımlanmaktadır: Çok yaygın (>1/10); yaygın(>1/100 ila <1/10); yaygın olmayan (>1/1.000 ila <1/100); seyrek (>1/10.000 ila <1/1.000);çok seyrek (<1/10.000), bilinmiyor (eldeki verilerden hareketle tahmin edilemiyor). Bağışıklık sistemi hastalıklarıSeyrek: Aşırı duyarlılık Kalıtsal anjiyoödem alevlenmesi* 13/19 Metabolizma ve beslenme hastalıklarıYaygın olmayan: Sıvı tutulumu Hipertrigliseridemi* Psikiyatrik hastalıklarYaygın: Depresif duygu durumu, duygu durum değişiklikleri Yaygın olmayan: Libido azalmasıSeyrek: Libido artışı Sinir sistemi hastalıklarıYaygın: Baş ağrısı Yaygın olmayan: MigrenKorea alevlenmesi* Göz hastalıklarıSeyrek: Kontakt lense toleranssızlık Vasküler hastalıklarıSeyrek: Tromboembolizm Kan basıncında artış* Gastrointestinal hastalıklarYaygın: Bulantı, karın ağrısı Yaygın olmayan: Kusma, diyareCrohn hastalığı*, ülseratif kolit* Hepato-bilier hastalıklarıKaraciğer fonksiyonunda bozulmalar* Deri ve deri altı doku hastalıklarıYaygın olmayan: Döküntü, ürtikerSeyrek: Eritema nodozum, eritema multiforme Kloazma* Üreme sistemi ve meme hastalıklarıYaygın: Meme ağrısı, meme hassasiyeti Yaygın olmayan: Memede hipertrofiSeyrek: Vajinal akıntı, memede akıntı Azalmış menstrüasyon kanaması*, lekelenme*, ani kanama* ve atlanan çekilme kanaması*, hap sonrası amenore* AraştırmalarYaygın: Kiloda artış Seyrek: Kiloda azalma * Pazarlama sonrası bildirilen advers olaylar DIANE kullanan tüm kadınlarda tromboembolizm riski artmaktadır (bkz. Bölüm 4.4). 14/19 Seçilmiş advers reaksiyonların tanımı DIANE kullanan hastalarda pazarlama sonrası raporlarda şiddetli depresyon (çok nadir raporlarda dahil olan intihar düşüncesi veya davranışı) bildirilmiştir. Bununla birlikte, klinikdepresyon ve DIANE arasında nedensel bir ilişki kurulmamıştır. KHK kullanan kadınlarda miyokard enfarktüsü, inme, geçici iskemik atak, venöz tromboz ve pulmoner embolizm gibi arteriyel ve venöz trombotik ve tromboembolik olaylarda artmış birrisk gözlenmiştir (bkz. Bölüm 4.4). KHK kullanan kadınlarda aşağıdaki ciddi advers olaylar bildirilmiştir (bkz. Bölüm 4.4): Venöz tromboembolik bozukluklar Arteryel tromboembolik bozukluklar Hipertansiyon Karaciğer tümörleri KOK kullanımı ile ilişkinin kesin olmadığı durumların oluşması veya bozulması:Crohn hastalığı, ülseratif kolit, epilepsi, rahim miyomu, porfiri, sistemik lupuseritematozus, herpes gestasyon, Sydenham koresi, hemolitik üremik sendrom,kolestaza bağlı sarılık Kloazma Karaciğer fonksiyonunun akut veya kronik bozuklukları, karaciğer fonksiyonununbelirteçleri normale dönene kadar KOK kullanımının kesilmesini gerektirebilir. Kalıtsal anjiyoödemi olan kadınlarda, eksojen östrojenler anjiyoödem semptomlarınıuyarabilir ya da şiddetlendirebilir. Meme kanseri tanısının sıklığı KOK kullananlar arasında hafifçe artmıştır. 40 yaşın altındaki kadınlarda meme kanseri seyrek olduğundan, meme kanserinin total riski ile ilgili ek sayıdüşüktür. KOK kullanımının nedensellik ilişkisi bilinmemektedir. Daha fazla bilgi için bkz.Bölüm 4.3 ve Bölüm 4.4. Etkileşimler Diğer ilaçlarla (enzim indükleyici ilaçlar) oral kontraseptiflerin etkileşimi ara kanamalar ve/veya kontrasepsiyon başarısızlığı ile sonuçlanabilir (bkz. Bölüm 4.5). Şüpheli advers reaksiyonların raporlanmasıRuhsatlandırna sonrası şüpheli ilaç advers reaksiyonlarının raporlanması büyük önem taşımaktadır. Raporlama yapılması, ilacın yarar/risk dengesinin sürekli olarak izlenmesineolanak sağlar. Sağlık mesleği mensuplarının herhangi bir şüpheli advers reaksiyonu TürkiyeFarmakovijilans Merkezi (TÜFAM)'ne bildirmeleri gerekmektedir. (www.titck.gov.tr; e-posta: [email protected] ; tel: 0 800 314 00 08; faks: 0 312 218 35 99) 4.9. Doz aşımı ve tedavisiDoz aşımı bulantı, kusma ve çekilme kanamalarına neden olabilir. Çekilme kanaması, ilacı yanlışlıkla almaları halinde kız çocuklarında menarştan önce bile görülebilir. Spesifik birantidotu yoktur ve semptomatik tedavi uygulanmalıdır. 15/19 5. FARMAKOLOJİK ÖZELLİKLER5.1. Farmakodinamik özelliklerFarmakoterapötik grup : Seks hormonları ve genital sistem modülatörleri, antiandrojenler ve östrojenler ATC Kodu : G03HB01 DIANE androjen reseptörlerini bloke eder. Ayrıca androjen sentezini, hem hipotalamo-hipofiz-over sistemindeki negatif geri besleme etkisiyle; hem de androjen sentez enzimlerinin inhibisyonuyla azaltır. DIANE oral kontraseptif etkiye de sahip olmakla beraber, kadınlarda yalnız kontrasepsiyon amacıyla kullanılmamalı; androjene bağlı cilt bozukluklarının tanımlandığı tedavi gerektirendurumlar için saklanmalıdır. MenenjiyomBir Fransız epidemiyolojik kohort çalışmasından elde edilen sonuçlara dayanarak, siproteron asetat ve menenjiyom arasında kümülatif doza bağımlı bir ilişki gözlenmiştir. Bu çalışma,Fransız Sağlık Sigortasından (CNAM) alınan verilere dayanmaktadır ve 50-100 mg siproterontablet kullanan 253.777 kadından oluşan bir popülasyonu içermektedir. Cerrahi veyaradyoterapi ile tedavi edilen menenjiyom insidansı, yüksek doz siproteron asetata (kümülatifdoz >3 g) maruz kalan kadınlar ile siproteron asetata hafifçe (kümülatif doz <3 g) maruz kalankadınlar arasında karşılaştırılmıştır. Kümülatif bir doz-yanıt ilişkisi gösterilmiştir.
a Zamana bağlı değişken olarak yaş ve dahil olma aşamasındaki östrojen düzeyine göre ayarlanmıştır.Örneğin 12 g kümülatif doz, her ay 20 gün olacak şekilde 50 mg/gün dozunda bir yıllık tedaviye karşılık gelebilir. 5.2. Farmakokinetik özelliklerGenel özelliklerSiproteron asetatEmilim:Oral uygulanmasını takiben siproteron asetat geniş bir doz aralığında tamamen emilir. DIANE'in alımını takiben 1,6 saat sonra 15 ng siproteron asetat/ml'lik doruk serumkonsantrasyonuna ulaşır. Siproteron asetatın mutlak biyoyararlanımı neredeyse tamdır (dozun%88'i). DIANE ile ilgili rölatif siproteron asetat biyoyararlanımı sulu mikrokristalinsüspansiyonu ile karşılaştırıldığında %109'dur. Dağılım:Siproteron asetat hemen hemen tamamen serum albuminine bağlanır. Toplam serum ilaç konsantrasyonlarının sadece % 3,5-4,0'ü serbest olarak bulunur. Proteine bağlanma spesifikolmadığı için, seks hormonu bağlayıcı globulin (SHBG) seviyesindeki değişiklikler siproteronasetatın farmakokinetiğini etkilemez. 16/19 Biyotransformasyon:Plazmadan siproteron asetatın toplam klirensi 3,6 ml/dak/kg olarak belirlenmiştir. Siproteron asetat hidroksilasyonlar ve konjügasyonlar da dahil olduğu çeşitli yollarla metabolize olur. İnsan plazmasındaki ana metabolit 15 B -hidroksi türevidir. Eliminasyon:Siproteron asetat serum seviyeleri 0,8 saat ve 2,3 gün yarı ömür ile karakterize, iki fazlı düşüş gösterir. Alınan dozun bir kısmı safra sıvısıyla değişmeden atılır. Büyük bölümü isemetabolitler halinde 3:7 oranında idrar ve safra yoluyla atılır. Böbrek ve safra atılımı 1,9 günyarılanma ömrü ile ilerlemektedir. Plazma metabolitleri benzer oranla (yarılanma ömrü 1,7gün) atılır. Doğrusallık / Doğrusal olmayan durum:Plazmadan (serum) terminal dispozisyon fazının uzun yarılanma ömrü ve bir tedavi döngüsünce biriken günlük alınan siproteron asetat miktarlar göze alındığında, serumda ilaçmaksimum oranları 1.ve 3. tedavi dönemlerinin sonunda sırasıyla 15 ng/ml'den, (1.gün) 21ng/ml ve 24 ng/ml'ye yükselir. Zamana karşı konsantrasyon altındaki alan profili 2,2 kat(1.döngü sonunda) ve 2,4 kat (3. döngü sonunda) artmıştır. Kararlı durum şartları 16 günsonra yakalanmıştır. Uzun dönemli tedavide, siproteron asetat tedavi döngüsü boyunca faktör2 ile birikir. EtinilestradiolEmilim:Oral uygulanan etinilestradiol hızla ve tamamen emilir. DIANE alımını takiben 1,7 saatte, yaklaşık 80 pg/ml olan doruk ilaç serum düzeylerine erişilir. Plazmadan terminal dispozisyonfazının yarılanma ömrüne ve günlük alım miktarı göze alınınca, kararlı haldeki plazmaseviyelerine 3-4 gün içinde ulaşılır ve tek bir doz ile kıyaslandığında %30-40 daha yüksektir.Etinilestradiolün relatif biyoyararlanımı (referans:sulu mikrokristalin süspansiyonu) neredeyse tamdır. Etinilestradiolün sistemik biyoyararlanımı diğer ilaçlarca her iki tarafa da yönlendirilebilir. Bununla beraber C vitamininin yüksek dozlarıyla etkileşimi yoktur. Dağılım:Etinilestradiol için görünür dağılım hacmi yaklaşık 5 l/kg ve plazmadan metabolik klerens oranı yaklaşık 5 ml/dk/kg olarak tayin edilmiştir. Etinilestradiol serum albuminine yüksek oranda fakat non-spesifik olarak bağlanır. İlaç düzeyinin %2'si serbest olarak bulunur. Biyotransformasyon:Plazmadan metabolik klirens oranı yaklaşık 5 ml/dk/kg olarak belirlenmiştir. Emilim ve karaciğerden ilk geçiş esnasında etinilestradiol metabolize olur, bu da azalmış mutlak vedeğişken oral biyoyararlanıma neden olur. Eliminasyon:Etinilestradiol plazma değerleri yarılanma ömürleri 1-2 saat ve 20 saat olarak karakterize, iki fazlı düşüş gösterir. Analitik sebeplerden ötürü bu parametreler, yalnızca yüksek dozlar içinhesaplanabilir. Etinilestradiolün metabolitleri yaklaşık 1 gün yarılanma ömrüyle 4:6 oranındaidrar ve safra yoluyla atılır. 17/19 Doğrusallık / Doğrusal olmayan durum:Etinilestradiol SHBG ve globulin bağlayan kortikosteroidin (CBG) karaciğerde sentezini devamlı kullanıldığı sürece indükler. Bununla birlikte, SHBG indüksiyon boyutu, birlikteuygulanan progestinin kimyasal yapısına ve dozuna bağlıdır. DIANE tedavisi sırasında,serumdaki SHBG konsantrasyonları yaklaşık 100 nmol/l'den 300 nmol/l'ye ve serumdakiCBG konsantrasyonları yaklaşık 50 g/ml'den 95 g/ml'ye artmıştır. 5.3. Klinik öncesi güvenlilik verileriKÜB'ün diğer ilgili bölümlerine dahil edilmemiş olan ve ilacı reçeteleyen kişi açısından önemli herhangi bir klinik öncesi veri bulunmamaktadır. 6. FARMASÖTİK ÖZELLİKLER6.1. Yardımcı maddelerin listesiLaktoz monohidrat (sığır kaynaklı) Mısır nişastası Povidon 25Magnezyum stearatSukrozPovidon 90Makrogol 6000Kalsiyum karbonatTalk Gliserol %6.2. GeçimsizliklerYoktur. 6.3. Raf ömrü60 ay 6.4. Saklamaya yönelik özel tedbirler25°C altındaki oda sıcaklığında saklayınız. 6.5. Ambalajın niteliği ve içeriğiPVC/Al folyo, 21 tabletlik takvimli blister ambalajda. 6.6. Beşeri tıbbi üründen arta kalan maddelerin imhası ve diğer özel önlemlerKullanılmamış olan ürünler ya da atık materyaller, Tıbbi Atıkların Kontrolü Yönetmeliği ve Ambalaj ve Ambalaj Atıklarının Kontrolü Yönetmeliğine uygun olarak imha edilmelidir. 7. RUHSAT SAHİBİBayer Türk Kimya San. Ltd. Şti., Fatih Sultan Mehmet Mah. Balkan Cad. No:53 34770 Ümraniye/İstanbul Tel: 0216 528 36 00Faks: 0216 645 39 50 18 /19 8. RUHSAT NUMARASI2015/516 9. İLK RUHSAT TARİHİ / RUHSAT YENİLEME TARİHİİlk ruhsat tarihi : 24.06.2015 Ruhsat yenileme tarihi: 10. KÜB'ÜN YENİLENME TARİHİ
19/19 |
İlaç BilgileriDiane 2 Mg/ 35 Mcg Kaplı TabletEtken Maddesi: Siproteron Asetat, Etinil Estradiol Kullanma talimatı ve kısa ürün bilgileri
Google Reklamları
İlgili İlaçlar |
Ana Sayfa | Hakkımızda | İlaçlar | İlaç Ara | İlaç Firmaları | Gizlilik | Bize Ulaşın
Telif Hakkı 2008-2026 © İlaç Prospektüsü. Tüm Hakları Saklıdır.Uyarı: Sitemizde yayınladığımız ilaç bilgileri ile doktora danışmadan kesinlikle ilaç kullanmayınız!
Aksi halde doğabilecek sağlık sorunlarından ilacprospektusu.com sorumlu tutulamaz.