Relitrexed 100 Mg Iv İnfüzyonluk Çözelti Hazırlamada Kullanilacak Konsantre İçin Toz Kısa Ürün BilgisiKISA ÜRÜN BİLGİSİ1. BEŞERİ TIBBİ ÜRÜNÜN ADIRELİTREXED 100 mg i.v. infüzyonluk çözelti hazırlamada kullanılacak konsantre çözelti için toz Steril, sitotoksik.2. KALİTATİF VE KANTİTATİF BİLEŞİMEtkin madde:Her bir flakon 100 mg pemetrekset baza eşdeğer miktarda 110,3 mg pemetrekset disodyum içerir. Sulandırıldıktan sonra (Bkz. Bölüm 6.6. Beşeri tıbbi üründen arta kalan maddelerin imhası ve diğerözel önlemler) her bir flakon 25 mg/ml pemetrekset içerir. Yardımcı maddeler:Sodyum hidroksit (yeterli miktarda) Yardımcı maddeler için 6.1.'e bakınız. 3. FARMASÖTİK FORMİnfüzyonluk Çözelti Hazırlamada Kullanılacak Konsantre İçin Toz Beyaz ila açık sarı ya da sarı-yeşil liyofilize toz. %4. KLİNİK ÖZELLİKLER4.1. Terapötik endikasyonlarMalign plevral mezotelyomaRELİTREXED, daha önce kemoterapi almamış,rezeke edilemeyen malign plevral mezotelyoması olan hastaların tedavisinde platin ile kombine olarak endikedir. Non-skuamöz küçük hücreli dışı akciğer kanseri (KHDAK)RELİTREXED lokal ileri hastalık ya da metastatik evredeki küçük hücreli dışı akciğer kanserli hastaların, sadece non-skuamöz histolojik alt gruplarında olanlarında sisplatinle kombine olarakbaşlangıç tedavisinde endikedir (Bkz. Bölüm 5.1). RELİTREXED, birinci seri platin bazlı kemoterapiden sonra hastalığı progrese olmamış relaps veya metastatik küçük hücreli dışı akciğer kanserinin sadece non-skuamöz histolojik alt tiplerinde idametedavisinde tek başına endikedir (Bkz. Bölüm 5.1). RELİTREXED, daha önce pemetrekset bazlı tedavi kullanmamış relaps veya metastatik non-skuamöz küçük hücreli dışı akciğer kanseri hastalarının ikinci basamak tedavisinde endikedir (Bkz. Bölüm 5.1). 1 4.2. Pozoloji ve uygulama şekliPozolojiRELİTREXED sadece, antikanser kemoterapi uygulamasında deneyimli bir hekimin gözetimi altında uygulanmalıdır. Pozoloji/uygulama sıklığı ve süresi:RELİTREXED sisplatinle combine olarak:Önerilen RELİTREXED dozu, her 21 günlük kürün ilk gününde 10 dakikalık intravenöz infüzyon şeklinde uygulanmak üzere, 500 mg/m2'dir. (Vücut yüzey alanı VYA nın metre karesi başına500 mg). Önerilen sisplatin dozu, her 21 günlük kürün ilk gününde pemetrekset infüzyonununtamamlanmasından yaklaşık 30 dakika sonra, iki saatlik bir süreyle infüzyon ile uygulanmak üzere,75 mg/m2'dir. Hastalara sisplatin verilmeden önce ve/veya sonra yeterli antiemetik tedavi ve uygunhidrasyon uygulanmalıdır(özel dozlama için ayrıca sisplatin Kısa Ürün Bilgisi'ne bakınız).RELİTREXED tek ajan olarak:Önceden kemoterapi almış non-skuamöz küçük hücreli dışı akciğer kanseri için tedavi edilen hastalarda, önerilen RELİTREXED dozu her 21 günlük kürün ilk gününde 10 dakikalık intravenözinfüzyon şeklinde uygulanmak üzere 500 mg/m2'dir. Premedikasyon rejimi:Cilt reaksiyonlarının sıklık ve şiddetini azaltmak için, pemetrekset uygulamasından 1 gün önce, uygulama gününde ve uygulamadan sonraki günde kortikosteroid verilmelidir. Verilen kortikosteroidoral olarak günde iki kez uygulanan 4 mg deksametazona eşdeğer olmalıdır (Bkz. Bölüm 4.4). Toksisiteyi azaltmak için pemetrekset ile tedavi edilen hastalara vitamin desteği de verilmelidir (bkz. Bölüm 4.4). Hastalar günlük olarak, oral folik asit veya folik asit içeren (350-1000 mikrogram)multivitamin kullanmalıdırlar. İlk pemetrekset dozundan önceki 7 günde en az 5 doz folik asitalınmalı ve bu doz uygulaması tüm tedavi kürü boyunca ve son pemetrekset dozundan sonra da 21gün daha devam ettirilmelidir. Hastalara ilk pemetrekset dozundan önceki haftada ve bunun ardındanher üç kürde bir intramusküler B12 vitamini (1000 mikrogram) enjeksiyonu yapılmalıdır. Pemetreksetuygulaması ile aynı günde B12 vitamini enjeksiyonları da uygulanabilir. Monitorizasyon:Pemetrekset uygulanan hastalar, her dozdan önce diferansiyel lökosit ve trombosit sayımını da içeren, tam kan sayımı ile izlenmelidir. Her kemoterapi uygulamasından önce, renal ve hepatik fonksiyonlarıdeğerlendirmek için kan biyokimya testleri yapılmalıdır. Herhangi bir kemoterapi kürüne başlamadanönce hastanın aşağıdaki değerlere sahip olması gereklidir: Mutlak nötrofil sayısı (MNS) >1500 hücre/mm ve trombosit sayısı >100.000 hücre/mm olmalıdır. Kreatinin klerensi >45 ml/dak. olmalıdır. Toplam bilirubin, normal değer üst limitinin <1.5 katı olmalıdır. Alkalen fosfataz (AP), aspartat amino transferaz (AST veya SGOT) ve alanin amino transferaz (ALT veya SGPT) normal değer üstlimitinin <3 katı olmalıdır. Eğer karaciğerde tümör metastazı varsa, alkalen fosfataz, AST veyaALT'nin normal değer üst limitinin <5 katı olması kabul edilebilir. Doz ayarlaması:Bir sonraki kürün başlangıcındaki doz ayarlaması, bir önceki tedavi küründeki en düşük hematolojik sayımlara veya maksimum hematolojik olmayan toksisiteye dayanarak yapılmalıdır. Laboratuvarbulguları düzelene kadar tedavi ertelenebilir. Düzelme sağlandıktan sonra hastalar, RELİTREXED'intek ajan veya sisplatin ile kombinasyon halinde kullanımı için geçerli olan Tablo 1, 2 ve 3'tekikılavuzlara göre yeniden tedavi edilmelidir. TABLO 1 - RELİTREXED (tek ajan veya kombine olarak) ve sisplatin için doz ayarlama tablosu - Hematolojik toksisiteler
Eğer hastalarda (nörotoksisite hariç) >Grade 3 hematolojik olmayan toksisite gelişirse, hastanın tedavi öncesi değerlerinden daha düşük veya eşit değerlere geri dönülünceye dek RELİTREXEDuygulaması durdurulmalıdır. Tedavi, Tablo 2'deki kılavuzlara uygun olarak sürdürülmelidir. TABLO 2 - RELİTREXED (tek ajan veya kombine olarak) ve sisplatin için doz ayarlama tablosu - Hematolojik olmayan toksisitelera' b' b
Nörotoksisite gelişmesi halinde, RELİTREXED ve sisplatin için önerilen doz ayarlamaları Tablo 3'te verilmiştir. Eğer Grade 3 veya 4 nörotoksisite gözlenirse, hastalarda tedavi kesilmelidir. TABLO 3 - RELİTREXED (tek ajan veya kombinasyon olarak) ve sisplatin için doz ayarlama tablosu - Nörotoksisite
RELİTREXED tedavisi, hastanın iki doz azaltılması sonrasında herhangi bir hematolojik veya hematolojik olmayan Grade 3 veya 4 toksisite görülmesi halinde bırakılmalı veya Grade 3 veya 4nörotoksisite görülmesi halinde ise derhal kesilmelidir. Uygulama şekliRELİTREXED çözeltisi bölüm 6.6'da verilen talimatlara uygun olarak hazırlanmalıdır. RELİTREXED her 21 günlük periodun ilk gününde 10 dakikayı aşkın intravenöz infüzyon şeklinde uygulanır. Uygulamadan önce RELİTREXED'in sulandırılması ve seyreltme talimatlarıiçin bölüm 6.6'ya bakınız. Özel popülasyonlara ilişkin ek bilgiler:Böbrek yetmezliği:(Standard Cockcroft ve Gault formülü veya Tc99m-DPTA serum klerens metodu ile ölçülen Glomerüler Filtrasyon Oranı): Pemetrekset esas olarak değişmemiş halde böbrek yoluyla atılır. Klinikçalışmalarda, kreatinin klerensi > 45 ml/dak. olan hastalar, tüm hastalar için önerilenler dışında birdoz ayarlamasına gereksinim duymamışlardır. Kreatinin klerensi 45 ml/dak.'nın altında olanhastalarda pemetrekset kullanımı ile ilgili yeterli veri mevcut değildir; bu nedenle bu hastalardapemetrekset kullanılması önerilmemektedir (Bkz. Bölüm 4.4). Karaciğer yetmezliği:AST (SGOT), ALT (SGPT) veya toplam bilirubin ve pemetrekset farmakokinetiği arasında bir ilişki saptanmamıştır. Bununla beraber, bilirubin değeri normal değer üst limitinin > 1.5 katı ve/veyaaminotransferaz normal değer üst limitinin > 3.0 katı (hepatik metastazın olmadığı) veya normaldeğer üst limitinin > 5.0 katı (hepatik metastazın olduğu) olan karaciğer yetmezliği bulunan hastalarspesifik olarak araştırılmamıştır. Pediyatrik popülasyon:RELİTREXED'in malign plevral mezotelyoma ve küçük hücreli dışı akciğer kanserinde pediyatrik popülasyonda kullanımı yoktur. 18 yaş altındaki hastalarda önerilmemektedir. Geriyatrik popülasyon:Klinik çalışmalarda, 65 yaş veya üzerindeki hastaların 65 yaşın altındaki hastalarla karşılaştırıldığında artmış bir istenmeyen etki riski altında bulunduklarına dair bir bulgusaptanmamıştır. Genel olarak tüm hastalar için önerilenler dışında, doz azaltılması gerekli değildir. 4 / 24 4.3. KontrendikasyonlarPemetrekset veya ilacın bölüm 6.1'de içerdiği maddelerden herhangi birine karşı bilinen aşırı duyarlılığı bulunan hastalarda kontrendikedir. Pemetrekset ile tedavi sırasında emzirme kesilmelidir (Bkz. Bölüm 4.6). Sarıhumma aşısı ile birlikte kullanımı kontrendikedir (Bkz. Bölüm 4.5). 4.4. Özel kullanım uyarıları ve önlemleriPemetrekset, nötropeni, trombositopeni ve anemi (veya pansitopeni) ile kendini gösteren kemik iliği inhibisyonu yapabilir (Bkz. Bölüm 4.8). Miyelosupresyon genellikle doz kısıtlayıcı toksisitedir.Hastalar tedavi süresince miyelosupresyon açısından izlenmeli ve hastalara, mutlak nötrofil sayıları(MNS) > 1.500 hücre/mm3 ve trombosit sayısı > 100.000 hücre/mm3 düzeyine dönünceye kadarpemetrekset uygulanmamalıdır. Bir sonraki kürler için doz azaltılması bir önceki kürde gözlenen endüşük MNS, trombosit sayısı ve hematolojik olmayan maksimum toksisiteye dayanarak ayarlanır(Bkz. Bölüm 4.2). Folik asit ve B12 vitamini ile premedikasyon uygulandığında, daha az toksisite ve nötropeni, febril nötropeni ve Grade 3/4 nötropeni ile birlikte enfeksiyon gibi Grade 3/4 hematolojik ve hematolojikolmayan toksisitelerde azalma bildirilmiştir. Bu nedenle pemetrekset ile tedavi edilen tüm hastalar,tedaviyle ilişkili toksisiteyi azaltabilmek için profilaktik olarak folik asit ve B12 vitamini almalarıkonusunda bilgilendirilmelidir (bkz. Bölüm 4.2). Kortikosteroid ile premedikasyon görmemiş hastalarda cilt reaksiyonları bildirilmiştir. Deksametazon (veya eşdeğeri) ile premedikasyon cilt reaksiyonlarının sıklık ve şiddetini azaltabilir (Bkz. Bölüm4.2). Kreatinin klerensi 45 ml/dak.'nın altında olan araştırılmış hasta sayısı yeterli değildir. Bu nedenle, kreatinin klerensi 45 ml/dak.'nın altında olan hastalarda pemetreksetin kullanımı önerilmemektedir(Bkz. Bölüm 4.2). Hafif ile orta derecede böbrek yetmezliği bulunan hastalar (kreatinin klerensi 45-79 ml/dak.), pemetrekset uygulamasının 2 gün öncesinden itibaren, uygulama gününde ve uygulamadan sonra 2gün süreyle ibuprofen ve aspirin (günlük >1,3 g) gibi nonsteroidal antienflamatuar ilaçlar(NSAİİ) almaktan kaçınmalıdır (Bkz. Bölüm 4.5). Pemetrekset tedavisi için düşünülen orta ya da hafif böbrek yetmezliği olan hastalarda, eliminasyon yarılanma ömrü uzun olan NSAİİ'ler pemetrekset uygulamasının en az 5 gün öncesinden itibaren,uygulama gününde ve uygulama gününden sonra en az 2 gün süresince kesilmelidir (Bkz. Bölüm4.5). Pemetreksetin tek başına ya da diğer kemoterapötik ajanlarla birlikte kullanıldığında akut böbrek yetmezliği dahil ciddi böbrek bozuklukları bildirilmiştir. Bu hastaların çoğunda böbrekbozukluklarının gelişmesine neden olabilecek dehidrasyon, önceden var olan hipertansiyon veyadiyabet gibi risk faktörleri mevcuttur. Pazarlama sonrası dönemde tek başına pemetreksetle ya dadiğer kemoterapötik ajanlarla birlikte nefrojenik diyabetes insipidus ve renal tübüler nekrozbildirilmiştir. Bu olayların çoğu pemetreksetin bırakılmasından sonra çözülmüştür. Hastalar akut 5 / 24 tübüler nekroz, azalan böbrek fonksiyonu ve nefrojenik diyabetes insipidusun belirti ve semptomları (örn. hipernatremi) için düzenli olarak izlenmelidir. Plevral efüzyon veya asit gibi vücut boşluk sıvılarının pemetrekset üzerine olan etkileri tam olarak bilinmemektedir. Sıvı birikimi olan 31 solid tümör hastasında yapılan bir faz 2 çalışmada, sıvıbirikimi olmayan hastalarla kıyaslandığında pemetreksetin plazma konsantrasyonu ya da klerensi birfarklılık göstermemiştir. Bu nedenle pemetrekset tedavisi öncesinde toplanmış sıvı birikimlerinindrenajı değerlendirilmelidir ama gerekli olmayabilir. Pemetreksetin, sisplatin ile kombine olarak verildiğindeki gastrointestinal toksisitesine bağlı olarak şiddetli dehidrasyon gözlenmiştir. Bu nedenle, hastalara tedavi öncesinde ve/veya sonrasında yeterliantiemetik tedavi ve uygun hidrasyon uygulanmalıdır. Pemetrekset klinik çalışmalarında, genellikle diğer bir sitotoksik ajan ile kombine verildiği durumlarda, yaygın olmayan miyokardiyal enfarktüs ve serebrovasküler olaylar dahil ciddikardiyovasküler olaylar bildirilmiştir. Bu olayların gözlendiği hastaların çoğu önceden var olankardiyovasküler risk faktörlerine sahiptir (Bkz. Bölüm 4.8). Kanser hastalarında bağışıklık sistemi çoğunlukla baskılanmış durumdadır. Sonuç olarak, zayıflatılmış canlı aşılarla birlikte kullanılması önerilmez (bkz. Bölüm 4.3 ve 4.5). Pemetreksetin, genetik olarak hasar verici etkileri olabilir. Cinsel olgunluktaki erkeklere, tedavi sırasında ve sonraki 6 aya kadar çocuk sahibi olmamaları önerilir. Kontraseptif yöntemler veyailişkiden kaçınma tavsiye edilir. Pemetrekset tedavisinin geri dönüşümsüz infertiliteye sebep olabilmeihtimalinden dolayı erkeklere, tedaviye başlamadan önce sperm saklanması hakkında danışmanlıkalmaları önerilir. Doğum yapma potansiyeli olan kadınlarda pemetrekset ile tedavi sırasında etkin kontraseptif yöntemler kullanılmalıdır (Bkz. Bölüm 4.6). Pemetrekset tedavisi sırasında, tedavisini takiben veya tedaviden önce radyasyon tedavisi gören hastalarda radyasyon pnömönisi bildirilmiştir. Bu hastalarda ve diğer radyosensitif ajanlarınkullanımında özellikle dikkat edilmesi gerekir. Haftalar veya yıllar öncesi radyasyon tedavisi gören hastalarda radyasyon çağrışımı reaksiyonu (radyasyon recall) vakaları bildirilmiştir. Bu tıbbi ürün her flakonunda 1 mmol (23 mg)'dan daha az sodyum ihtiva eder; yani esasında sodyum içermez. Sodyuma bağlı herhangi bir uyarı gerekmemektedir. 4.5. Diğer tıbbi ürünler ile etkileşimler ve diğer etkileşim şekilleriPemetrekset büyük bir oranda değişmeden tübüler sekresyon ve daha az olarak da glomerüler filtrasyon ile böbrek yoluyla atılır. Nefrotoksik ilaçların (örn. aminoglikozid, kıvrım diüretikleri,platin bileşikleri, siklosporin) eş zamanlı olarak kullanılması, potansiyel olarak pemetreksetinklerensinin gecikmesine neden olabilir. Bu kombinasyon dikkatle kullanılmalıdır. Gerekiyorsa,kreatinin klerensi yakından izlenmelidir. 6 / 24 Pemetreksetin, tübüler olarak salınan maddeler (örn. probenesid, penisilin) ile de eş zamanlı olarak kullanılması potansiyel olarak klerensinin gecikmesine neden olabilir. Bu ilaçlar pemetrekset ilekombine kullanıldığında dikkatli olunmalıdır. Gerekiyorsa, kreatinin klerensi yakından izlenmelidir. Normal böbrek fonksiyonu olan hastalarda (kreatinin klerensi > 80 ml/dak), yüksek dozlarda nonsteroidal antienflamatuar ilaçlar (NSAİİ, örn. ibuprofen > 1.600 mg/gün) ve daha yüksekdozda asetilsalisilik asit (günde >1,3 g) pemetrekset atılımını azaltabilir ve sonuç olarakpemetrekset advers etkilerinin oluşumunu artırabilir. Bu nedenle, pemetrekset ile eş zamanlı olarakyüksek dozlarda NSAİİ ve asetilsali silik asit alan normal böbrek fonksiyonu olan hastalarda(kreatinin klerensi >80 ml/dak.) dikkatli olunmalıdır. Hafif ile orta derecede böbrek yetmezliği bulunan hastalarda (kreatinin klerensi 45-79 ml/dak.), pemetrekset uygulamasının 2 gün öncesinden itibaren, uygulama gününde ve uygulamadan sonra enaz 2 gün süreyle NSAİİ (örn. ibuprofen) veya yüksek dozlarda asetilsalisilik asit ile pemetreksetin eşzamanlı uygulamasından kaçınılmalıdır (Bkz. Bölüm 4.4). Pemetreksetin, piroksikam veya rofekoksib gibi uzun yarılanma ömürlü NSAİİ ile potansiyel etkileşimine ilişkin veri bulunmadığından hafif ya da orta derecede böbrek yetmezliği olan hastalardabunların, pemetreksetin uygulamasının en az 5 gün öncesinden itibaren, uygulama gününde veuygulamadan sonra en az 2 gün süreyle eş zamanlı kullanımı kesilmelidir (Bkz. Bölüm 4.4). EğerNSAİİ ile eş zamanlı kullanım gerekli ise hastalar özellikle miyelosupresyon ve gastrointestinaltoksisite nedeniyle yakından izlenmelidir. Pemetreksetin hepatik metabolizması sınırlıdır. İnsan karaciğer mikrozomlarında yapılan in vitroçalışmaların sonuçları, pemetreksetin CYP3A, CYP2D6, CYP2C9 ve CYP1A2 ile metabolize edilenilaçların metabolik klerenslerinde klinik olarak anlamlı bir inhibisyona neden olmasınınbeklenmediğine işaret etmektedir.Tüm sitotoksiklerde görülen etkileşimler: Kanserli hastalarda tromboz riskinin artmış olması nedeniyle, antikoagülan tedavisi kullanımı sıktır. Hastalık sırasında, koagülasyon durumunun bireysel olarak değişkenliğinin yüksek olması ve oralantikoagülanlar ile antikanser kemoterapisi arasındaki olası etkileşim, hastanın oral antikoagülanlar iletedavisine karar verilmesi halinde daha sık INR (Uluslararası Normalleştirilmiş Değer) izlenmesinigerektirir. Kontrendike eş zamanlı kullanım: Sarıhumma aşısı: Ölümcül jeneralize aşı hastalığı riski (Bkz. Bölüm 4.3). Önerilmeyen eş zamanlı kullanım: Zayıflatılmış canlı aşılar (eş zamanlı kullanımı kontrendike olan sarıhumma dışında): Sistemik, olasılıkla ölümcül hastalık riski. Altta yatan hastalıkları nedeniylebağışıklık sistemi baskılanmış bireylerde risk artmaktadır. Bulunabilirse bir inaktif aşı kullanılır(çocuk felci) (Bkz. Bölüm 4.4). Özel popülasyonlara ilişkin ek bilgiler:Pediyatrik popülasyon:Herhangi bir etkileşim çalışması yapılmamıştır. 7 / 24 4.6. Gebelik ve laktasyonGenel tavsiyeGebelik kategorisi: D Çocuk doğurma potansiyeli bulunan kadınlar/Doğum kontrolü (Kontrasepsiyon)Doğum yapma potansiyeli olan kadınlarda pemetrekset ile tedavi sırasında etkin kontraseptif yöntemler kullanılmalıdır. Pemetreksetin, genetik olarak zarar verici etkileri olabilir. Cinsel olgunluktaki erkeklere, tedavi sırasında ve sonraki 6 aya kadar çocuk sahibi olmamaları önerilir. Kontraseptif yöntemler veyailişkiden kaçınma tavsiye edilir. Gebelik dönemiPemetreksetin hamile kadınlarda kullanımına ait veri yoktur ancak pemetreksetin diğer anti-metabolitler gibi, gebelik döneminde uygulandığında ciddi doğum kusurlarına neden olmasından kuşkulanılmaktadır. Hayvanlar üzerinde yapılan araştırmalar üreme toksisitesinin bulunduğunugöstermiştir (Bkz. Bölüm 5.3). Pemetreksetin gebelik ve/veya fetus/yeni doğan üzerinde zararlıfarmakolojik etkileri bulunmaktadır. RELİTREXED, annenin ihtiyaçları ve fetus için riskin dikkatledeğerlendirmesinden sonra, belirgin şekilde gerekli olmadıkça gebelik döneminde kullanılmamalıdır(Bkz. Bölüm 4.4). Laktasyon dönemiPemetreksetin insan sütüyle atılıp atılmadığı bilinmemektedir ve emzirilen çocuk üstündeki istenmeyen etkileri göz ardı edilemez. RELİTREXED ile tedavi boyunca emzirmedurdurulmalıdır. (Bkz. Bölüm 4.3). Üreme yeteneği/FertilitePemetrekset tedavisinin geri dönüşümsüz infertiliteye sebep olabilme ihtimalinden dolayı erkeklere, tedaviye başlamadan önce sperm saklanması konusunda danışmanlık almaları önerilir. 4.7. Araç ve makine kullanımı üzerindeki etkilerPemetreksetin, araç ve makine kullanma yeteneği üzerine olan etkileri ile ilgili bir çalışma gerçekleştirilmemiştir. Bununla birlikte, yorgunluğa neden olabileceği bildirilmiştir. Bu etkininortaya çıkması durumunda, hastalar araç sürme veya makine kullanma konusunda uyarılmalıdır. 4.8. İstenmeyen etkilerGüvenlilik profili özetiPemetreksete ilişkin en yaygın bildirilen istenmeyen etkiler, ister monoterapi olarak ya da kombine olarak kullanılsın, kendini anemi, nötropeni, lökopeni, trombositopeni ile belli eden kemik iliğibaskılanması; ve kendini anoreksi, bulantı, kusma, diyare, konstipasyon, farenjit, mukozit ve stomatitile gösteren gastrointestinal toksisitelerdir.Diğer istenmeyen etkiler renal toksisiteler, aminotransferaz düzeylerinde artış, alopesi, yorgunluk, dehidrasyon, döküntü, enfeksiyon/sepsis ve nöropatiyi içerir. Seyrek olarak görülen olaylar Stevens-Johnson sendromu ve toksik epidermalnekrolizi içerir. 8 / 24 Advers reaksiyonların tablolanmış listesiMezotelyoma çalışması:Aşağıdaki tablo, sisplatin ve pemetrekset uygulanmak üzere randomize edilmiş mezotelyomalı 168 hasta ve tek ajan sisplatin uygulanmak üzere randomize edilmiş mezotelyomalı 163 hastanın %5'inden fazlasında bildirilmiş olan istenmeyen etkilerin sıklık ve şiddetlerini göstermektedir. Her ikitedavi grubunda da, daha önce kemoterapi almamış hastalara tam bir folik asit ve B12 vitaminitakviyesi verilmiştir.Advers reaksiyonlar: Sıklık derecesi: Çok yaygın (> 1/10); yaygın (> 1/100 ila <1/10); yaygın olmayan (> 1/1.000 ila <1/100); seyrek (>1 /10.000 ila <1/1.000); çok seyrek (<1/10.000), bilinmiyor (eldeki verilerdenhareketle tahmin edilemiyor). Her bir sıklık grubu içinde, istenmeyen etkiler ciddiyetindeki azalmaya göre sıralanmıştır.
9 / 24 Her toksisite grade'i için, kreatinin klerensinde azalma terimi dışındakiler için Ulusal Kanser Enstitüsü GTK 2.Baskı referans alınmıştır. ** renal/genitoüriner diğer teriminden türetilmiştir. *** Ulusal Kanser Enstitüsü Genel Toksisite Kriterlerine (GTK) (v2.0; NCl 1998) göre tat alma bozukluğu ve alopesi yalnız Grade 1 ve 2 olarak rapor edilmelidir. Bu tablonun amacı doğrultusunda, raportörün pemetrekset ve sisplatin ile olası bir ilişki olduğunu düşündüğü tüm olayların dahil edilmesi için %5'lik bir sınır değer kullanılmıştır.Sisplatin ve pemetrekset kullanmak üzere randomize olan hastaların > %%5'inde bildirilmiş olan klinik olarak anlamlı Genel Toksisite Kriterleri (GTK) toksisiteleri: Böbrek yetmezliği,enfeksiyon, yüksek ateş, febril nötropeni, artmış AST, ALT ve GGT, ürtiker ve göğüs ağrısınıiçermektedir.Sisplatin ve pemetrekset kullanmak üzere randomize olan hastaların <% 1'inde bildirilmiş olan klinik olarak anlamlı GTK toksisiteleri aritmi ve motor nöropatiyi içermektedir. Aşağıdaki tablo tek ajan olarak pemetrekset beraberinde folik asit ve B12 vitamini takviyesi uygulanmak üzere randomize edilmiş 265 hastanın % 5'inden fazlasında ve tek ajan dosetakseluygulanmak üzere randomize edilmiş 276 hastanın % 5'inden fazlasında bildirilmiş olan istenmeyenetkilerin sıklık ve şiddetlerini göstermektedir. Tüm hastalara lokal olarak ilerlemiş veya metastatikküçük hücreli dışı akciğer kanseri tanısı konmuş olup, daha önce kemoterapi almışlardır.
10 / 24 ** Ulusal kanser Enstitüsü Genel Toksisite Kriterlerine (GTK) (v2.0; NCI 1998) gore alopesi yalnız Grade 1 ve 2 olarak rapor edilmelidir. Pemetrekset kullanmak üzere randomize olan hastaların >% 1 ve <% 5'inde bildirilmiş olan klinik olarak anlamlı GTK toksisiteleri: Nötropeni olmaksızın enfeksiyon, febril nötropeni, alerjikreaksiyon/aşırı duyarlılık, artmış kreatinin, motor nöropati, sensoriyel nöropati, eritema multiformeve abdominal ağrıyı içermektedir. Pemetrekset kullanmak üzere randomize olan hastaların <% 1'inde bildirilmiş olan klinik olarak anlamlı GTK toksisiteleri supraventriküler aritmiyi içermektedir. Tek ajan olarak pemetrekset ile yapılan üç Faz 2 çalışmasının (n=164) birleştirilmiş sonuçları ve yukarıda tanımlanan tek ajan pemetrekset ile Faz 3 çalışması arasında nötropeni (sırasıyla %12.8'ekarşılık % 5.3) ve alanin aminotransferaz yükselmesi (sırasıyla % 15.2'ye karşılık % 1.9) dışındaklinik olarak anlamlı Grade 3 ve Grade 4 laboratuvar toksisiteleri benzer olmuştur. Bu farklılıklarhasta popülasyondaki farklılığa bağlı olarak ortaya çıkmış olabilir, çünkü Faz 2 çalışmaları hem dahaönce kemoterapi almamış hem de daha önce yoğun şekilde tedavi uygulanmış, önceden mevcutkaraciğer mestazları ve/veya anormal başlangıç karaciğer fonksiyon testleri bulunan meme kanserihastalarını içermiştir.Aşağıdaki tabloda, çalışmaya randomize edilen, sisplatin ile pemetrekset alan 839 küçük hücreli dışı akciğer kanseri hastasında ve sisplatin ile gemsitabin alan 830 küçük hücreli dışı akciğer kanserihastasında, % 5'den daha büyük sıklıkla bildirilen ve çalışma ilacı ile muhtemelen ilişkili olduğudüşünülen istenmeyen etkilerin sıklık ve şiddeti verilmektedir. Hastaların tümü lokal olarak ilerlemiş veya metastatik küçük hücreli dışı akciğer kanseri için başlangıç tedavisi olarak çalışma tedavisini almıştır ve her iki gruptaki hastalara tam bir folik asit ve vitamin B12desteği verilmiştir.
Bu tablonun amacı doğrultusunda, raportörün pemetrekset ile olası bir ilişki olduğunu düşündüğü tüm olayların dahil edilmesi için % 5'lik bir sınır değer kullanılmıştır. Sisplatin ve pemetrekset kullanmak üzere randomize olan hastaların >% 1 ve <% 5'inde bildirilmiş olan klinik olarak anlamlı toksisiteler: AST ve ALT düzeylerinde artış, enfeksiyon, febril nötropeni,böbrek yetmezliği, yüksek ateş, sıvı kaybı, konjunktivit ve kreatinin klerensinde azalmayıiçermektedir. Sisplatin ve pemetrekset kullanmak üzere randomize olan hastaların <% 1'inde (yaygın olmayan) bildirilmiş olan klinik olarak anlamlı toksisiteler: GGT düzeyinde artış, göğüs ağrısı, aritmi ve motornöropatiyi içermektedir. Pemetrekset ile birlikte sisplatin alan hastalarda, cinsiyete göre klinik açıdan önemli toksisiteler, genel hasta popülasyonuyla benzer olmuştur. Aşağıdaki tabloda, tek ajan pemetrekset idame tedavisi (JMEN: N=663) ve pemetrekset devam idame tedavisi (PARAMOUNT: N=539) çalışmalarında rastgele tek ajan pemetrekset alacak şekilderandomize edilen 800 hastanın ve rastgele plasebo alacak şekilde randomize edilen 402 hastanın >%5'inde bildirilen ve muhtemelen çalışma ilacıyla ilgili olduğu değerlendirilen istenmeyen etkilerinsıklığı ve şiddeti sunulmaktadır. Tüm hastalara Evre IIIB veya IV KHDAK tanısı konmuş ve tümhastalar daha önce platin bazlı kemoterapi görmüştür. Her iki çalışma kolundaki hastalar tam folik asitve B12 vitamini takviyesi almıştır.
Kısaltmalar: ALT: alanin aminotransferaz; AST: aspartat aminotransferaz; CTCAE: Advers Olay için Yaygın Terminoloji Kriteri; NCI: Ulusal Kanser Enstitüsü; SGOT: serum glutamik oksaloasektik aminotransferaz, SGPT: serum glutamikpiruvik aminotransferaz * Sıklık terimlerinin tanımı: Çok yaygın: >% 10; Yaygın: >% 5 ve <% 10. Bu tablonun amacı doğrultusunda, raportörün pemetrekset ile olası bir ilişki olduğunu düşündüğü tüm olayların dahil edilmesi için %5 'lik bir sınır değer kullanılmıştır. ** Her bir toksisite derecesi için NCI CTCAE Kriterlerine (Versiyon 3.0; NCI 2003) bakınız. Gösterilen rapor oranları CTCAE versiyon 3.0 doğrultusundadır. *** Birleştirilmiş advers reaksiyonlar tablosu JMEN pemetrekset idame tedavisi (N=663) ve PARAMOUNT pemetrekset devam idame tedavisi (N=539) çalışmalarının sonuçlarını birleştirmektedir. **** Birleştirilmiş terimler serum/kan kreatinin artışı, glomerüler filtrasyon hızında azalma, böbrek yetmezliği ve renal/genitoüriner - diğer olayları içermektedir. Rastgele pemetrekset verilen hastaların >% 1 ve <% 5'inde bildirilen herhangi bir grade klinik olarak ilgili Yaygın Terminoloji Kriteri (CTC) toksisitesi febril nötropeni, enfeksiyon, platelet sayısındaazalma, ishal, kabızlık, alopesi, prurit/kaşıntı, ateş (nötropeni olmadan), oküler yüzey hastalığı(konjonktivit dahil), gözyaşı salgılanmasında artış, baş dönmesi ve motor nöropatidir. Rastgele pemetrekset verilen hastaların <% 1'inde bildirilen herhangi bir dereceden klinik olarak ilgili CTC toksisitesi alerjik reaksiyon/hipersensitivite, eritema multiforme, supraventriküler aritmi vepulmoner embolizmi içermektedir. Pemetrekset almak üzere randomize edilen hastalarda (N=800) güvenlilik değerlendirilmiştir. Advers reaksiyon insidansı <6 siklus boyunca pemetrekset idame tedavisi alan hastalarda (N=519)değerlendirilmiş ve >6 siklus boyunca pemetrekset alan hastalarla (N=281) karşılaştırılmıştır. Dahauzun süre maruz kalmayla birlikte advers reaksiyonlarda (her gradede) artış gözlenmiştir.Pemetreksete daha uzun süre maruz kalındığında, muhtemelen ilaçla ilgili Grade 3/4 nötropeniinsidansında anlamlı bir artış gözlenmiştir (<6 siklus: %3.3, >6 siklus: %6.4; p=0,046). Dahauzun süre maruz kalma ile, başka herhangi bir bireysel Grade 3/4/5 advers reaksiyonda istatistikselolarak anlamlı bir fark görülmemiştir. Pemetreksetin genellikle diğer bir sitotoksik ajan ile kombine olarak verildiği klinik çalışmalarda, miyokard enfarktüsü, angina pektoris, serebrovasküler olay ve geçici iskemik atak dahil yaygın 13 / 24 olmayan ciddi kardiyovasküler ve serebrovasküler olaylar bildirilmiştir. Bu olayların gözlendiği hastaların çoğu önceden var olan kardiyovasküler risk faktörlerine sahiptir. Pemetrekset klinik çalışmalarında, potansiyel olarak ciddi hepatit vakaları seyrek olarak bildirilmiştir.Pemetrekset klinik çalışmalarında yaygın olmayan pansitopeni bildirilmiştir. Klinik çalışmalarda, pemetrekset ile tedavi edilen hastalarda (bazen ölümcül olan intestinal ve rektal kanama, intestinal perforasyon, intestinal nekroz ve tiflit dahil) yaygın olmayan kolit vakalarıbildirilmiştir. Klinik çalışmalarda, pemetrekset ile tedavi edilen hastalarda nadir olarak bazen ölümcül olan solunum yetmezliği ile seyreden interstisyel pnömoni vakaları bildirilmiştir. Pemetrekset ile tedavi edilen hastalarda yaygın olmayan ödem vakaları bildirilmiştir. Pemetrekset ile yapılan klinik çalışmalarda yaygın olmayan ösofajit/radyasyon ösofajiti bildirilmiştir. Pemetrekset ile yapılan klinik çalışmalarda bazen ölümcül olabilen sepsis yaygın olarak bildirilmiştir. Pazarlama sonrası araştırmalara göre pemetrekset ile tedavi edilen hastalarda aşağıdaki advers etkiler bildirilmiştir: Yaygın olarak hiperpigmentasyon bildirilmiştir. Pemetreksetin tek başına veya diğer kemoterapötik ajanlarla birlikte kullanıldığında yaygın olmayan akut böbrek yetmezliği vakaları bildirilmiştir (Bkz. Bölüm 4.4. Özel kullanım uyarıları ve önlemleri). Pemetrekset tedavisi sırasında, sonrasında veya tedaviden önce radyasyon tedavisi gören hastalarda yaygın olmayan radyasyon pnömonisi bildirilmiştir (Bkz. Bölüm 4.4. Özel kullanım uyarıları veönlemleri). Daha önce radyoterapi gören hastalarda seyrek olarak radyasyon anımsatma dermatiti (radyasyon recall) vakaları bildirilmiştir (Bkz. Bölüm 4.4. Özel kullanım uyarıları ve önlemleri). Bazen ekstremitede nekroza yol açan yaygın olmayan periferal iskemi vakaları rapor edilmiştir. Bazı vakalarda ölümcül olan toksik epidermal nekroliz ve Stevens-Johnson sendromunu içeren büllöz durumlar seyrek olarak bildirilmiştir. Pemetrekset ile tedavi edilen hastalarda immün yanıt sonucu gelişen hemolitik anemi seyrek olarak bildirilmiştir. Seyrek olarak anafilaktik şok bildirilmiştir. Şüpheli advers reaksiyonların raporlanmasıRuhsatlandırma sonrası şüpheli ilaç advers reaksiyonlarının raporlanması büyük önem taşımaktadır. Raporlama yapılması, ilacın yarar/risk dengesinin sürekli olarak izlenmesine olanak sağlar. Sağlık 14 / 24 mesleği mensuplarının herhangi bir şüpheli advers reaksiyonu Türkiye Farmakovijilans Merkezi (TÜFAM)'ne bildirmeleri gerekmektedir (www.titck.gov.tr;4.9. Doz aşımı ve tedavisiBildirilmiş doz aşımı semptomları nötropeni, anemi, trombositopeni, mukozit, sensoriyel polinöropati ve döküntüyü içermektedir. Doz aşımının beklenen komplikasyonları kendini nötropeni,trombositopeni ve anemi ile belli eden kemik iliği baskılanmasıdır. Ayrıca ateş ile birlikte veya ateşolmaksızın enfeksiyon, diyare ve/veya mukozit görülebilir. Doz aşımından şüphelenildiğinde,hastalar kan sayımı ile izlenmeli ve gereken destek tedaviler uygulanmalıdır. Pemetrekset dozaşımında kalsiyum folinat/folinik asit kullanımı düşünülmelidir. 5. FARMAKOLOJİK ÖZELLİKLER5.1. Farmakodinamik özelliklerFarmakoterapötik grubu : Folik asit analogları ATC kodu : L01BA04 RELİTREXED (pemetrekset) etkisini, hücre çoğalması için temel teşkil eden folata bağımlı metabolik süreçleri bozmak suretiyle gösteren çok hedefli, antikanser, antifolat bir ajandır. İn vitrode novobiyosentezi için folata bağımlı önemli enzimler olan timidilat sentaz (TS), dihidrofolat redüktaz (DHFR) veglisinamid ribonükleotid formiltransferazı (GARFT) inhibe etmek suretiyle çok-hedefli bir antifolatolduğunu göstermiştir. Pemetrekset, indirgenmiş folat taşıyıcı ve membran folat bağlayıcı proteintaşıma sistemlerinin her ikisi tarafından hücre içine taşınmaktadır. Hücre içine girdiğindepemetrekset, folilpoliglutamat sentetaz enzimi tarafından hızla ve etkin bir şekilde poliglutamatformlarına dönüştürülür. Poliglutamat formları hücre içinde tutulur ve daha da kuvvetli TS veGARFT inhibitörleridirler. Poliglutamasyon, tümör hücrelerinde ve daha az olarak da normaldokularda meydana gelen, zaman ve konsantrasyona bağımlı bir süreçtir. Poliglutamatadönüştürülmüş metabolitlerin hücre içi yarılanma ömrü artmış olup, bu da malign hücrelerde ilaçetkisinin daha uzun sürmesini sağlamaktadır.Klinik Etkililik: Mezotelyoma: Malign plevral mezotelyomalı, daha önce kemoterapi almamış hastalarda, pemetrekset ve sisplatin kombinasyonuna karşılık sisplatinin karşılaştırıldığı çok merkezli, randomize, tek kör, Faz 3çalışması (EMPHACIS), pemetrekset+sisplatin kombinasyonu ile tedavi edilen hastaların yalnızcasisplatin verilen hastalara kıyasla klinik olarak anlamlı 2.8 aylık bir medyan sağkalım avantajınasahip olduklarını göstermiştir. Çalışma sırasında toksisiteyi düşürmek için hastaların tedavisine düşük dozda folik asit ve B12 vitamini eklenmiştir. Bu çalışmanın primer analizi, randomize olarak bir tedavi grubuna ayrılan veçalışmailacı verilen (randomize olan ve tedavi edilen) tüm hasta popülasyonunda gerçekleştirilmiştir. Çalışma tedavisi süresince folik asit ve Bı2 vitamini desteği alan hastalarda alt grup analizi gerçekleştirilmiştir. Bu etkililik analizlerinin sonuçları aşağıdaki tabloda özetlenmiştir: 15 / 24 Malign plevral mezotelyomada pemetrekset - sisplatin kombinasyonuna karşılık sisplatin etkililiği
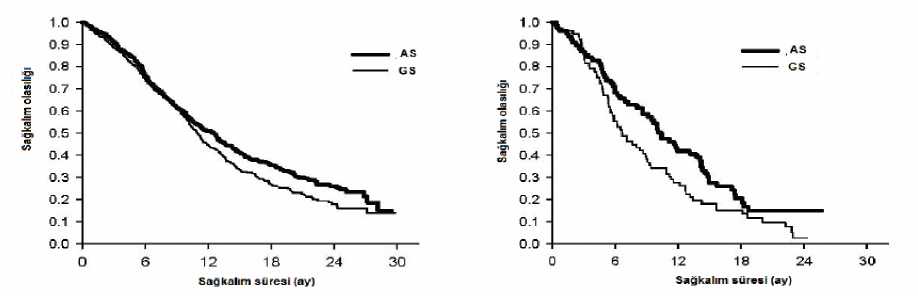
Tek başına sisplatin koluna (218 hasta) kı yasla pemetrekset/sisplatin kolunda (212 hasta) Akciğer Kanseri Semptom Ölçeği (Lung Cancer Symptom Scale) kullanılarak, malign plevral mezotelyomaile ilişkili klinik olarak önemli semptomlarda (ağrı ve dispne) istatistiksel olarak anlamlı bir iyileşmegözlenmiştir. Pulmoner fonksiyon testlerinde de istatistiksel olarak anlamlı iyileşmeler gözlenmiştir.Tedavi kolları arasındaki ayrım, pemetrekset/sisplatin kolunda akciğer fonksiyonunda iyileşme vekontrol kolunda ise zaman içinde akciğer fonksiyonunda kötüleşme ile gösterilmiştir. Yalnız pemetrekset ile tedavi edilen malign mezotelyomalı hastalara ait çok sınırlı veri bulunmaktadır. Pemetrekset 500 mg/m2 dozunda malign plevral mezotelyomalı 64 kemonaif hastadatek ajan olarak çalışılmıştır. Tüm cevap oranı %14,1'dir.İkinci basamak küçük hücreli dışı akciğer kanseri: Lokal olarak ilerlemiş veya metastatik küçük hücreli dışı akciğer kanseri hastalarında, daha önce alınan kemoterapi sonrasında, pemetrekset ile dosetakselin karşılaştırıldığı çok merkezli, randomize,açık etiketli faz 3 çalışma sonuçlarında medyan sağkalım süresi, pemetrekset ile tedavi edilenhastalarda 8,3 ay (tedavi denenen popülasyon (ITT) n=283), dosetaksel ile tedavi edilen hastalarda7,9 ay (ITT n=288)'dır. Önceki kemoterapiler pemetrekset içermemektedir. KHDAK histolojisinegöre tedavinin genel sağkalım üzerindeki etkisi ile ilgili bir analiz, baskın olarak skuamöz hücrelikarsinom histolojisine sahip olanlar dışındaki KHDAK hastalarında, dosetaksele karşı pemetreksetinistatistiksel olarak anlamlı düzeyde üstün olduğunu gösterirken (399 hasta, 9,3 aya karşılık, 8,0 ay 16 / 24 düzeltilmiş HR=0,78; % 95 GA =0,61-1,00, p=0,047), skuamöz hücreli karsinom histolojisine sahip hastalarda ise dosetaksel lehinedir (172 hasta, 7,4 aya karşılık 6,2 ay, düzeltilmiş HR=1,56; % 95 GA=1,08-2,26, p=0,018). Histolojik alt gruplar arasında pemetreksetin güvenlilik profili açısından klinikolarak önemli hiçbir fark gözlenmemiştir. Ayrı bir randomize, Faz 3, kontrollü çalışmadan elde edilen sınırlı klinik veriler pemetreksete yönelik etkililik verilerinin (genel sağkalım, progresyonsuz sağkalım) daha önce dosetaksel ile tedaviedilen hastalar (n=41) ve daha önce dosetaksel tedavisi almayan hastalar (n=540) arasında benzerolduğunu göstermektedir. KHDAK'inde pemetreksetin dosetaksele karşı etkililiği - ITT popülasyonu
Birinci basamak küçük hücreli dışı akciğer kanseri: Daha önce kemoterapi almamış, lokal olarak ilerlemiş veya metastatik (Evre IIIb veya IV) KHDAK hastalarında yapılan çok merkezli, randomize, açık etiketli bir Faz 3 çalışma pemetrekset artı sisplatintedavisini gemsitabin artı sisplatin tedavisi ile karşılaştırmış ve pemetrekset artı sisplatinin tedaviamacına yönelik [ITT] popülasyonunda (862 hasta) primer sonlanım noktasını karşılayarak genelsağkalım açısından gemsitabin artı sisplatin ile benzer klinik etkililik göstermiştir. Bu çalışmayaalınan tüm hastaların ECOG (The Eastern Cooperative Oncology Group-Doğu Kooperatif OnkolojiGrubu) performans durumu 0 veya 1'dir. Primer etkililik analizi, ITT popülasyonuna dayalıdır. Ayrıca ana etkililik sonlanım noktalarının duyarlılık analizleri Protokole Uygun (PQ) popülasyonda değerlendirilmiştir. PQ popülasyonukullanılarak yapılan etkililik analizleri ITT popülasyonuna yönelik analizlerle tutarlıdır vepemetrekset/sisplatin etkililiğinin gemsitabin/sisplatin etkililiğinden az olmadığını desteklemektedir. Progresyonsuz sağkalım (PFS) ve genel yanıt oranı tedavi gruplarında benzer olmuştur: Medyan PFS artı sisplatin için 4,8 ay iken gemsitabin artı sisplatin için 5,1 ay (düzeltilmiş HR 1,04; % 95 GA 0,941,15), genel yanıt oranı pemetrekset artı sisplatin için %30.6 (% 95 GA 27,3-33,9) iken gemsitabin artısisplatin için % 28.2 (% 95 GA 25,0-31,4). PFS verileri bağımsız bir değerlendirme ile kısmendoğrulanmıştır (1725 hastadan 400'ü değerlendirme için rastgele seçilmiştir). 17 / 24 KHDAK histolojisinin genel sağkalım üzerindeki etkisi ile ilgili analiz histolojiye göre klinik olarak farklılıklar göstermektedir, bakınız aşağıdaki tablo. KHDAK'nin Birinci Basamak Tedavisinde Pemetrekset + Sisplatin ile Gemsitabin + Sisplatinin Etkililiklerinin Karşılaştırması - ITT Popülasyonu ve Histolojik Alt Gruplar
Histolojiye Göre Genel Sağkalım İçin Kaplan Meier Eğrileri
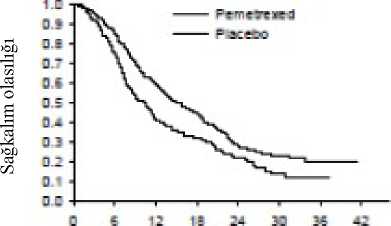
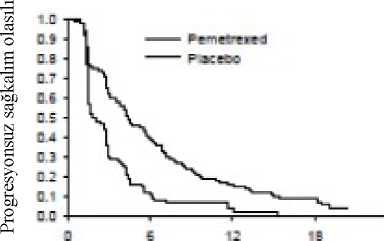
Histoloji alt gruplarında pemetrekset artı sisplatinin güvenlilik profilinde klinik olarak ilişkili bir farklılık gözlenmemiştir. Pemetrekset artı sisplatin ile tedavi edilen hastalarda daha az transfüzyon (% 28,9'a karşılık % 16,4, p< 0,001), eritrosit transfüzyonu (% 27,3'e karşılık % 16,1, p<0,001) vetrombosit transfüzyonu (% 4,5'e karşılık % 1,8, p=0.002) gerekmiştir. Ayrıca bu hastalara dahaaz eritropoietin/darbopoietin (% 18,1'e karşılık % 10,4, p<0,001), G-CSF/GM-CSF (% 6,1'ekarşılık % 3,1, p=0,004) ve demir preperatı (%7,0'a karşılık %4,3, p=0,021) verilmesigerekmiştir. 18 / 24 KHDAK, idame tedavisi:JMEN Gemsitabin, paklitaksel veya dosetaksel ile kombine sisplatin veya karboplatin içeren birinci basamak 4 kür ikili tedaviden sonra progrese olmayan lokal ileri (Evre IIIB) veya metastatik(Evre IV) KHDAK hastalarında pemetrekset artı en iyi destekleyici bakım (BSC) (n=441) ileplasebo artı BSC (n=222) idame tedavisinin etkililiğini ve güvenliliğini karşılaştıran çokmerkezli, randomize, çift kör, plasebo kontrollü Faz 3 çalışmadır (JMEN). Pemetrekset içerenbirinci basamak ikili tedavi çalışmaya dahil edilmemiştir. Bu çalışmaya dahil edilen tümhastaların ECOG performans durumu 0 veya 1'dir. Hastalar, hastalık ilerleyene kadar idametedavisi almıştır. Etkililik ve güvenlilik randomizasyon tarihinden birinci basamak (indüksiyon)tedavi tamamlanana kadar ölçülmüştür. Hastalar, pemetrekset ile medyan 5 kür, plasebo ilemedyan 3,5 kür idame tedavisi görmüştür. Toplam 213 hasta (% 48,3) >6 kür, toplam 103 hasta(% 23,4) >10 kür pemetrekset tedavisini tamamlamıştır. Çalışma primer sonlanım noktasını karşılamış ve pemetrekset kolunda plasebo koluna göre PFS açısından istatistiksel olarak anlamlı bir iyileşme göstermiştir (n=581, bağımsız olarak incelenenpopülasyon; sırasıyla medyan 4,0 ay ve 2,0 ay) (HR=0,60, % 95 GA=0,49-0,73, p <0,00001).Hasta taramalarının bağımsız incelemesi araştırmacının PFS değerlendirmesi bulgularınıdoğrulamıştır. Genel popülasyon için medyan OS (Overall Survival-Genel Sağkalım) (n=663),pemetrekset kolunda 13,4 ay ve plasebo kolunda 10,6 ay olmuştur; HR=0,79 (% 95 GA =0,65-0,95, p=0,01192). Diğer pemetrekset çalışmalarıyla tutarlı bir şekilde, JMEN'de de KHDAK histolojisine göre etkililik farkı gözlenmiştir. Ağırlıklı olarak skuamöz hücre histolojisi olanlar dışındaki KHDAKhastalarında (n=430, bağımsız olarak incelenen popülasyon) medyan PFS, pemetrekset koluiçin 4,4 ay ve plasebo kolu için 1,8 ay olmuştur; HR=0,47 (% 95 GA =0,37-0,60, p=0,00001).Ağırlıklı olarak skuamöz hücre histolojisi olanlar dışındaki KHDAK hastalarında medyan OS(n=481) pemetrekset kolu için 15,5 ay ve plasebo kolu için 10,3 ay olmuştur; HR=0,70 (% 95GA =0,56-0,88, p=0,002). Ağırlıklı olarak skuamöz hücre histolojisi olanlar dışındaki KHDAKhastalarında, indüksiyon fazı dahil medyan OS, pemetrekset kolu için 18,6 ay ve plasebokolu için 13,6 ay olmuştur; HR=0,71 (% 95 GA =0,56-0,88, p=0,002). Skuamöz hücre histolojisi olan hastalardaki PFS ve OS sonuçları pemetrekset için plaseboya göre herhangi bir avantaj göstermemiştir. Histoloji alt gruplarında pemetreksetin güvenlilik profili açısından klinik olarak anlamlı bir fark gözlenmemiştir. 19 / 24 JMEN: Ağırlıklı olarak skuamöz hücre histolojisi olanlar dışındaki KHDAK hastalarında plaseboya göre pemetrekset ile progresyonsuz sağkalım (PFS) ve genel sağkalım içinKaplan Meier grafikleri:Progresyonsuz sağkalım
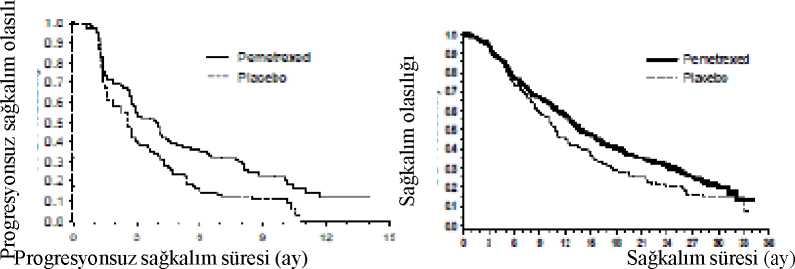
Progresyonsuz sağkalım süresi (ay) Sağkalım süresi (ay) PARAMOUNT Birinci basamak 4 kür pemetrekset/sisplatin ikili tedavisinden sonra progrese olmayan skuamöz hücre histolojisi olanlar dışındaki lokal ileri (Evre IIIB) veya metastatik (Evre IV) KHDAKhastalarında pemetrekset artı BSC (n=359) ve plasebo artı BSC (n=180) devam idametedavisinin etkililiğini ve güvenliliğini karşılaştıran çok merkezli, randomize, çift kör, plasebokontrollü Faz 3 çalışmadır (PARAMOUNT). Pemetrekset artı sisplatin indüksiyonu ile tedaviedilen 939 hastadan 539'u pemetrekset veya plasebo ile idame tedavisine randomize edilmiştir.Randomize edilen hastaların %44,9'u Pemetrekset artı sisplatin indüksiyonuna tam/kısmi yanıtverirken % 51,9'u stabil hastalık yanıtı vermiştir. İdame tedavisine randomize edilen hastalarınECOG performans durumu 0 veya 1 'dir. Pemetrekset artı sisplatin indüksiyon tedavisininbaşlangıcından idame tedavisinin başlangıcına kadar geçen medyan süre hem pemetrekset hemde plasebo kolunda 2,96 ay olmuştur. Randomize edilen hastalar, hastalık ilerleyene kadar idametedavisi almıştır. Etkililik ve güvenlilik randomizasyon tarihinden birinci basamak (indüksiyon)tedavi tamamlanana kadar ölçülmüştür. Hastalar, pemetrekset ve plasebo kolunda medyan 4 kürboyunca idame tedavisi görmüştür. Toplam 169 hasta (% 47,1) pemetrekset ile >6 kür idametedavisini tamamlamıştır, bu da pemetrekset için en az toplam 10 kürdür.Çalışma primer sonlanım noktasını karşılamış ve pemetrekset kolunda plasebo koluna göre PFS açısından istatistiksel olarak anlamlı bir iyileşme göstermiştir (n=472, bağımsız olarak incelenenpopülasyon; sırasıyla medyan 3,9 ay ve 2,6 ay) (HR=0,64, % 95 GA=0,51-0,81, p=0,0002).Hasta taramalarının bağımsız incelemesi araştırmacının PFS değerlendirmesi bulgularınıdoğrulamıştır. Randomize edilen hastalarda, pemetrekset artı sisplatin birinci basamakindüksiyon tedavisinin başlangıcında ölçülen, araştırmacı tarafından değerlendirilen medyanPFS, pemetrekset kolu için 6,9 ay ve plasebo kolu için 5,6 ay olmuştur (HR=0,59 % 95GA=0,47-0,74). Pemetrekset artı sisplatin indüksiyonunun ardından (4 kür), pemetrekset ile tedavi, OS açısından plaseboya göre istatistiksel olarak üstün olmuştur (medyan 13,9 ay ve 11,0 ay, HR=0,78, %95 GA=0,64-0,96, p=0,0195). Bu son sağkalım analizi sırasında, pemetrekset kolundakihastaların % 28,7'si hayattadır veya takip edilememiştir, bu oran plasebo kolunda % 21,7olmuştur. pemetreksetin rölatif tedavi etkisi, alt gruplar arasında (hastalık evresi, indüksiyonyanıtı, ECOG PS, sigara içme durumu, cinsiyet, histoloji ve yaş dahil) tutarlı olup, ayarlanmamış 20 / 24 OS ve PFS analizlerinde gözlenenlere benzer olmuştur. Pemetrekset grubundaki hastalarda 1 yıllık ve 2 yıllık sağkalım oranları sırasıyla %%32 olup, plasebo grubunda bu oranlarsırasıyla % 45 ve % 21 olmuştur. Pemetrekset artı sisplatin birinci basamak indüksiyontedavisinin başlangıcında, hastalardaki medyan OS, pemetrekset kolu için 16,9 ay ve plasebokolu için 14,0 ay olmuştur (HR=0,78 % 95 GA =0,64-0,96). Çalışma sonrası tedavi gören hastayüzdesi pemetrekset için % 64,3 ve plasebo için % 71,7'dir.PARAMOUNT: Skuamöz hücre histolojisi olanlar dışındaki KHDAK hastalarında plaseboya göre devam pemetrekset idamesi için PFS ve OS Kaplan Meier grafiği(randomizasyondan itibaren ölçülen)Progresyonsuz sağkalım Genel Sağkalım
Pemetrekset idame tedavisinin JMEN ve PARAMOUNT çalışmalarında elde edilen güvenlilik profilleri benzerdir. 5.2. Farmakokinetik özelliklerEmilim:Pemetreksetin farmakokinetik özellikleri, çeşitli solid tümörü bulunan 426 kanser hastasında tek ajan olarak 0,2-838 mg/m arası dozlarda, 10 dakikalık infüzyon sonrası değerlendirilmiştir.Pemetreksetin toplam eğri altı alanı (EAA) ve doruk plazma konsantrasyonu dozla doğru orantılıolarak artar. Pemetreksetin farmakokinetiği,tekrarlayan tedavi kürleri boyunca değişmemektedir. Dağılım:Pemetreksetin kararlılık durumundaki dağılım hacmi 9 L/m2'dir. İn vitroçalışmalar, pemetreksetin yaklaşık % 81 oranında plazma proteinlerine bağlandığını göstermiştir. Değişikevrelerdeki böbrek bozuklukları bu bağlanmayı anlamlı şekilde etkilememiştir.Biyotransformasyon:Pemetrekset sınırlı hepatik metabolizmaya maruz kalır. Eliminasyon:Pemetrekset esas olarak idrar ile atılmakta olup, uygulamayı takiben 24 saat içinde uygulanan dozun % 70 ile % 90 kadarı idrarda değişmemiş halde saptanmaktadır. İn vitroçalışmalarpemetreksetin organik anyon taşıyıcısı olan OAT3 tarafından aktif olarak sekrete edildiğinigöstermektedir. Pemetreksetin toplam sistemik klerensi 91,8 ml/dak. ve normal böbrek21 / 24 fonksiyonlarına (kreatinin klerensi 90 ml/dak) sahip olan hastalarda plazmadan atılım yarılanma ömrü 3,5 saattir. Klerensteki hastalar arası değişkenlik %19,3 ile orta düzeydedir.Doğrusallık/Doğrusalolmayan durum:Pemetreksetin toplam eğri altı alanı (EAA) ve doruk plazma konsantrasyonu dozla doğru orantılı olarak artar. Pemetreksetinfarmakokinetiği,tekrarlayan tedavi kürleri boyunca değişmemektedir. Farmakokinetik/farmakodinamik ilişkilerPemetreksetin farmakokinetik özellikleri, eş zamanlı uygulanan sisplatinden etkilenmemektedir. Oral folik asit ve intramüsküler B12 vitamini takviyesi pemetrekset farmakokinetiğinietkilememektedir. 5.3. Klinik öncesi güvenlilik verileriGebe farelere pemetrekset uygulanması, fötal yaşama kabiliyetinde düşüş, fötal ağırlıkta azalma, bazı iskelet yapılarının kemikleşmesinde tamamlanamama ve yarık damak oluşmasıylasonuçlanmıştır. Erkek farelere pemetrekset uygulanması, fertilite oranında azalma ve testiküler atrofi ile karakterize olan üreme toksisitesiyle sonuçlanmıştır. 9 ay boyunca intravenöz bolus enjeksiyonuyapılan av köpeklerinde gerçekleştirilen bir çalışmada testiküler bulgular (seminifer epitelyumundejenerasyonu/nekrozu) gözlenmiştir. Bu pemetreksetin erkek fertilitesini azaltabileceğinigöstermektedir. Dişi fertilitesi araştırılmamıştır. Çin hamsteri over hücrelerinde yapılan in vitroin vivomikronükleustestinde pemetreksetin klastojenik olduğu gösterilmiştir.Pemetreksetin karsinojenik potansiyelini değerlendiren çalışma yapılmamıştır. 6. FARMASÖTİK ÖZELLİKLER6.1. Yardımcı maddelerin listesiMannitol Hidroklorik asitSodyum hidroksitEnjeksiyonluk su 6.2. GeçimsizliklerPemetrekset, laktatlı Ringer enjeksiyonu ve Ringer enjeksiyonu dahil kalsiyum içeren tüm seyrelticileri ile fiziksel olarak geçimsizdir. Pemetreksetin diğer ilaçlar ve seyrelticiler ile diğergeçimlilik çalışmaları olmadığından, bu tıbbi ürün diğer tıbbi ürünler ile karıştırılmamalıdır. 22 / 24 6.3. Raf ömrüAçılmamış flakon: 24 ay Sulandırılmış infüzyon çözeltileri: Tarif edildiği şekilde seyreltilen RELİTREXED infüzyon çözeltileri antibakteriyel koruyucu içermemektedir. Pemetrekset infüzyon çözeltilerinin kullanım sırasındaki kimyasal ve fizikselstabilitesi 2°C-8°C sıcaklıkta 24 saattir. Mikrobiyolojik açıdan ürün hemen kullanılmalıdır. Eğerhemen kullanılmazsa, kullanmadan önceki saklama süresi ve koşulları kullanıcınınsorumluluğundadır ve 2°C-8°C arasında 24 saatten fazla olmamalıdır. 6.4. Saklamaya yönelik özel tedbirlerAçılmamış flakon: 25°C altındaki oda sıcaklığında saklayınız. Rekonstitüe edilmiş infüzyon çözeltileri: Rekonstitüe tıbbi ürünlerin saklama koşulları için Bkz. Bölüm 6.3. 6.5. Ambalajın niteliği ve içeriğiKauçuk tıpa ve flip-off aluminyum kapak ile kapatılmış renksiz 10 ml'lik Tip I cam flakonda 100 mg pemetrekset içeren liyofilize toz bulunur. 1 flakonluk ambalajda kullanma talimatı ile birlikte piyasaya sunulmaktadır. 6.6. Beşeri tıbbi üründen arta kalan maddelerin imhası ve diğer özel önlemler1. Pemetreksetin intravenöz infüzyon uygulaması için rekonstitüsyonu ve daha fazlaseyreltilmesi sırasında uygun aseptik teknikleri kullanınız. 2. Gerekli olan doz ve RELİTREXED flakon sayısını hesaplayınız. Her flakon, etikettebelirtilen miktarın rahatça çekilebilmesi için bir miktar fazla pemetrekset içermektedir. 3. Her bir 10 ml'lik flakon ise 4,2 ml 9 mg/ml (% 0,9'luk) koruyucusuz sodyum klorürenjeksiyonluk çözeltisi ile çözülerek 25 mg/ml pemetrekset içeren bir çözelti elde edilir. Toztamamen çözünene kadar flakonları hafifçe çalkalayınız. Elde edilen çözelti berrak ve ürünkalitesi üzerinde olumsuz etkisi olmaksızın renksiz-sarı veya yeşil-sarı arasında renklidir.Hazırlanmış çözeltinin pH'ı 6,6-7,8 arasındadır. Daha fazla seyreltme gereklidir.4. Hazırlanan pemetrekset çözeltisinin uygun hacmi, 9 mg/ml (% 0,9'luk) koruyucusuz sodyumklorür enjeksiyonluk çözeltisi ile 100 ml'ye seyreltilmelidir ve 10 dakika süreyle intravenözinfüzyon şeklinde uygulanmalıdır. 5. Yukarıda tarif edildiği şekilde hazırlanan pemetrekset infüzyon çözeltileri; infüzyon cam şişeleri, polivinil klorür ve poliolefin kaplı uygulama setleri ve infüzyon torbaları ileuyumludur. 6. Parenteral ilaç ürünleri uygulamadan önce partikül içeriği ve renk bozuklukları açısındangörsel olarak kontrol edilmelidir. Eğer partikül madde gözlenirse ürün kullanılmamalıdır. 7. Pemetrekset çözeltileri tek kullanım içindir. Kullanılmamış olan ürünler ya da atık materyaller, Tıbbi Atıkların Kontrol Yönetmeliği ve 'Ambalaj ve Ambalaj AtıklarınınKontrolü Yönetmelikleri'ne uygun olarak imha edilmelidir. 23 / 24 Hazırlama ve uygulama önlemleri:7. RUHSAT SAHİBİDem İlaç San. ve Tic. A.Ş. Dem Plaza İnönü Mah. Kayışdağı Cad. No: 172 34755 Ataşehir- İSTANBULTel: 0216 428 40 29Faks: 0216 428 40 86 8. RUHSAT NUMARASI2020/250 9. İLK RUHSAT TARİHİ / RUHSAT YENİLEME TARİHİ27.11.2020 10. KÜB'ÜN YENİLENME TARİHİ24 / 24 / 24 / 24 / 24 |
İlaç BilgileriRelitrexed 100 Mg Iv İnfüzyonluk Çözelti Hazırlamada Kullanilacak Konsantre İçin TozEtken Maddesi: Pemetrekset Disodyum Kullanma talimatı ve kısa ürün bilgileri
Google Reklamları
|
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
Ana Sayfa | Hakkımızda | İlaçlar | İlaç Ara | İlaç Firmaları | Gizlilik | Bize Ulaşın
Telif Hakkı 2008-2026 © İlaç Prospektüsü. Tüm Hakları Saklıdır.Uyarı: Sitemizde yayınladığımız ilaç bilgileri ile doktora danışmadan kesinlikle ilaç kullanmayınız!
Aksi halde doğabilecek sağlık sorunlarından ilacprospektusu.com sorumlu tutulamaz.