Tibersid 500 Mg/3 Ml İv İnfüzyon İçin Çözelti Kısa Ürün BilgisiKISA ÜRÜN BİLGİSİ1. BEŞERİ TIBBİ ÜRÜNÜN ADITİBERSİD 500 mg/3 ml IV infüzyon için enjeksiyonluk çözelti Steril 2. KALİTATİF VE KANTİTATİF BİLEŞİMEtkin madde:Her bir ampul (3 ml) 500 mg ornidazol içerir. Yardımcı madde(ler):Etanol (susuz) 900 mg Propilen glikol 1600 mg Yardımcı maddeler için 6.1.'e bakınız. 3. FARMASÖTİK FORMİnfüzyon için çözelti içeren ampul Şeffaf ampule doldurulmuş steril, berrak ve açık sarı renkli çözelti. 4. KLİNİK ÖZELLİKLER4.1. Terapötik endikasyonlar Anaerob bakterilere bağlı enfeksiyonlarda; septisemi, menenjit, peritonit, postoperatif yaraenfeksiyonları, doğum sonrası septisemi, septik abortus ve söz edilen bakterilerinispatlandığı veya varlığından şüphelenilen endometrit vakalarında, Özellikle kolon ve jinekolojik operasyon geçirecek vakalar başta olmak üzere, cerrahimüdahalelerde profilaksi amacıyla, Amebiyaz, amipli dizanteri dahil, Entamoeba histolytica'nın neden olduğu tüm intestinalenfeksiyonlarda, amebiyazın tüm ekstraintestinal formlarında, özellikle amebik karaciğerabsesi tedavisinde endikedir.4.2. Pozoloji ve uygulama şekliPozoloji/uygulama sıklığı ve süresi:Doktor tarafından başka şekilde tavsiye edilmediği taktirde; Önemli: Ampul içeriği kısa infüzyon şeklinde verilmeli, seyreltilmeden hiçbir şekilde enjekte edilmemelidir. 1. Anaerob bakterilere bağlı enfeksiyonlar a) Anerob bakterilere bağlı enfeksiyonların tedavisi: 500-1000 mg'lık (1-2 ampul)infüzyonla başlanır, daha sonra her 12 saatte bir 500 mg'lık (1 ampul) veya 5-10 günboyunca her 24 saatte bir 1 g'lık infüzyon yapılır. Hastanın durumu izin verdiği zamanparenteral tedavi yerini oral tedaviye bırakmalıdır. Örn. her 12 saatte bir 500 mg (2 tablet). b) Anaerob bakterilere bağlı enfeksiyonlarım profilaksisi: Ameliyattan yaklaşık yarımsaat önce 1000 mg (2 ampul) infüzyon şeklinde uygulanır. Karışık enfeksiyonlarınprofilaksisinde TİBERSİD bir aminoglikozit, bir penisilin veya bir sefalosporinle 1/7kombine edilerek kullanılmalıdır. İlaçlar ayrı ayrı uygulanmalıdır. Ancak 250 m l serum fizyolojik veya dekstroz çözeltisinde 1 g ornidazol ve 2 g seftriakson fiziksel ve kimyasalolarak geçimlidir. 2. Amebik karaciğer absesi ve ciddi amipli dizanteri; Başlangıçta 500-1000 mg IV infüzyonşeklinde (1-2 ampul) verilip her 12 saatte bir ortalama 3-4 gün boyunca 500 mg'lıkinfüzyonlar halinde uygulanır. Uygulama şekli:Kullanıma hazır infüzyon çözeltisinin hazırlanması:TİBERSİD'in kullanıma hazır çözeltisini hazırlamak için 500 mg'lık ampul aşağıdaki infüzyon çözeltilerinden birinin en az 100 ml'si ile seyreltilmelidir: %5 dekstroz, %10 dekstroz,Hartmann çözeltisi, Ringer çözeltisi, %0,9 sodyum klorür, %0,45 sodyum klorür + %2,5dekstroz. Çözelti kısa IV infüzyon şeklinde 15-30 dakikada uygulanır. Özel popülasyonlara ilişkin ek bilgiler:Böbrek yetmezliği:Böbrek yetmezliği hastalarında dozaj değişikliğine gerek yoktur. Karaciğer yetmezliği:Tavsiye edilen doz uygulandığında 3 ml'lik ampullerden 0,9 g etanol (susuz) alınmaktadır. Bu nedenle karaciğer hastalığında uygulanan özel doz aşıldığında sağlık riski oluşmaktadır.Ağır karaciğer yetmezliği olan hastalarda doz aralığı iki kat fazla olmalıdır. Pediyatrik popülasyon:Anaeroblara bağlı enfeksiyon endikasyonunda çocuklar için günlük doz 5-10 gün süreyle ikiye bölünmüş olarak 20 mg/kg vücut ağırlığıdır. Amibe bağlı karaciğer absesi ya da ciddi amip dizanterisinde çocuklar için günlük doz 2030 mg/kg vücut ağırlığıdır. Çocuklarda kullanımı ile ilgili uyarılar için bkz. Bölüm 4.4. Geriyatrik popülasyon:Yaşlılar için özel dozaj önerileri bulunmamaktadır. 4.3. KontrendikasyonlarOrnidazol, diğer nitroimidazol türevleri veya ilacın içerdiği yardımcı maddelerden herhangi birine karşı aşırı duyarlılığı olduğu bilinen hastalarda TİBERSİD kullanımı kontrendikedir. 4.4. Özel kullanım uyarıları ve önlemleriMerkezi sinir sistemi hastalığı (örn. epilepsi veya multipl skleroz) olan hastalarda ve ağır karaciğer hastalığı olanlarda dikkatli olmak gerekir. Ampuller etanol ve propilen glikol içermektedir. Propilen glikol içerdiği için alkol benzeri semptomlara neden olabilir. Bu tıbbi üründe (3 ml'lik çözelti) hacmin %38'i kadar etanol(alkol) vardır; örneğin, her dozda 22,5 ml biraya veya her dozda 9,36 ml şaraba eşdeğer 900 2/7mg etanol (alkol) içerir. Alkol bağımlılığı olanlar için zararlı olabilir. Hamile veya emziren kadınlar, çocuklar ve karaciğer hastalığı ya da epilepsi gibi yüksek risk grubundaki hastalardadikkate alınmalıdır. Diğer ilaçların etkisi artabilir veya azalabilir. Duyarlı kişilerde aşırı duyarlılık reaksiyonları gelişebilir. 4.5. Diğer tıbbi ürünler ile etkileşimler ve diğer etkileşim şekilleriOrnidazol kullanırken ve ilaç kesildikten sonra en az 3 gün boyunca alkol alınmamalıdır. Ornidazol, kumarin-tipi oral antikoagülanların etkisini potansiyelize eder. Antikoagülanın dozubu doğrultuda ayarlanmalıdır.Simetidin (antihistaminik), fenitoin ve fenobarbital gibi antiepileptik ilaçlar ve lityum ile birlikte kullanılırken dikkatli olunmalıdır. Ornidazol, vekuronyum bromürün adale gevşetici etkisini uzatır. Özel popülasyonlara ilişkin ek bilgilerÖzel popülasyonlara ilişkin etkileşim çalışması yapılmamıştır. Pediyatrik popülasyon:Pediyatrik popülasyonlar ile ilgili hiçbir etkileşim çalışması yapılmamıştır. 4.6. Gebelik ve laktasyonGenel tavsiyeGebelik kategorisi: C Çocuk doğurma potansiyeli bulunan kadınlar/Doğum kontrolü (Kontrasepsiyon)Ornidazol için, gebeliklerde maruz kalmaya ilişkin klinik veri mevcut değildir. Hayvanlar üzerinde yapılan çalışmalar, gebelik/embriyonal/fetal gelişim/doğum ya da doğum sonrasıgelişimileilgiliolarakdoğrudanyadadolaylızararlıetkilerolduğunu göstermemektedir. Ornidazolün çocuk doğurma potansiyeli bulunan kadınlara ve doğum kontrolü yöntemlerine etkisi bilinmemektedir. Gebelik dönemiOrnidazol için, gebeliklerde maruz kalmaya ilişkin klinik veri mevcut değildir. Hayvanlar üzerinde yapılan çalışmalar, gebelik/embriyonal/fetal gelişim/doğum ya da doğum sonrasıgelişimileilgiliolarakdoğrudanyadadolaylızararlıetkilerolduğunu göstermemektedir. Değişik türlerde yapılan yaygın çalışmalarda ilaç herhangi bir teratojenik veya fetotoksik etki göstermemiştir. Bununla beraber gebe kadınlarda kontrollü bir çalışma yapılmamıştır. Genelbir prensip olarak TİBERSİD gebeliğin erken dönemlerinde gerekli olmadıkça verilmemelidir. Laktasyon dönemiTİBERSİD genel bir prensip olarak emziren annelere gerekli olmadıkça verilmemelidir. 3/7Üreme yeteneği/FertiliteOrnidazol, erkek farelerde 400 mg/kg/gün gibi yüksek dozda uygulandığında, düşük sperm hızı bakımından epididimal sperm motilitesini inhibe ederek infertilite meydana getirmektedir.İnsanlar üzerinde yapılan çalışmalardan elde edilmiş veri bulunmamaktadır. 4.7. Araç ve makine kullanımı üzerindeki etkilerTİBERSİD alan hastalarda uyku hali, baş dönmesi, tremor, rijidite, koordinasyon bozuklukları, nöbet, vertigo veya geçici bilinç kaybı görülebilir. Bu gibi etkiler araç ve makine kullanımı gibidikkat gerektiren işleri etkileyebilir. 4.8. İstenmeyen etkilerOrnidazol ile yapılan klinik çalışmalarda görülen yan etkiler sistem organ sınıflarına ve sıklık gruplarına göre aşağıda verilmiştir: Çok yaygın (>1/10); yaygın (>1/100 ila <1/10); yaygın olmayan (> 1/1000 ila <1/100); seyrek (>1/10000 ila <1/1000); çok seyrek (<1/10000); bilinmiyor (eldeki verilerden hareketle tahminedilemiyor.) Kan ve lenf sistemi hastalıklarıSeyrek: Lökopeni Sinir sistemi hastalıklarıÇok seyrek: Uyku hali, baş ağrısı, baş dönmesi, tremor, rijidite, koordinasyon bozuklukları, nöbet, yorgunluk, vertigo, geçici bilinç kaybı ve duyusal veya kanşık periferal nöropati Gastrointestinal hastalıklarYaygın olmayan: Bulantı, kusma, ishal, epigastrik rahatsızlık, ağız kuruluğu ve iştahsızlık Seyrek: Tat alma bozukluğu Hepatobilier hastalıklarBilinmiyor: Sarılık, anormal karaciğer fonksiyon testleri Deri ve deri altı doku hastalıklarıSeyrek: Kaşıntı ve cilt reaksiyonları Genel bozukluklar ve uygulama bölgesine ilişkin hastalıklarBilinmiyor: İntravenöz infüzyon sırasında, aşırı duyarlılık ve lokal ağrı Şüpheli advers reaksiyonların raporlanmasıRuhsatlandırma sonrası şüpheli ilaç advers reaksiyonlarının raporlanması büyük önem taşımaktadır. Raporlama yapılması, ilacın yarar/risk dengesinin sürekli olarak izlenmesineolanak sağlar. Sağlık mesleği mensuplarının herhangi bir şüpheli advers reaksiyonu TürkiyeFarmakovijilans Merkezi (TÜFAM)'ne bildirmeleri gerekmektedir. (www.titck.gov.tr;[email protected]/74.9. Doz aşımı ve tedavisiDoz aşımında istenmeyen etkiler kısmında kayıtlı semptomlar daha ciddi olarak seyreder. Spesifik antidotu yoktur. Kramp oluştuğunda diazepam verilmesi tavsiye edilir. 5. FARMAKOLOJİK ÖZELLİKLER5.1. Farmakodinamik özelliklerFarmakoterapötik grup: Enfeksiyona karşı kullanılan ilaçlar ATC kodu: P01AB03 Ornidazol 5-nitroimidazol türevi antibakteriyel ve antiprotozoal bir ilaçtır. İnvazif nitelikteki amebiyazis olgularında güçlü etkinlik gösterir. TİBERSİD, BacteroidesClostridiumFusobacteriumEntomoeba hisyolytica'ya5.2. Farmakokinetik özelliklerGenel özelliklerEmilim:İntravenöz yolla parenteral uygulanmaktadır. Dağılım:IV uygulamadan sonra ortalama dağılım hacmi kg başına 1 litredir. Ornidazolün plazma proteinlerine bağlanma oranı %13'tür. TİBERSİD'in etkin maddesi serebrospinal sıvıya, vücutsıvılarına ve dokulara etkili konsantrasyonlarda geçer. Değişik endikasyonlara göre plazmakonsantrasyonlarının (6-36 mg/l) optimal aralıkta olduğu tahmin edilmektedir. Sağlıklıgönüllülerde 12 saatte bir tekrarlanan uygulamalardan sonra birikme faktörü 1,5-2,5 olarakhesaplanmıştır. Biyotransformasyon:Ornidazol karaciğerde başlıca 2-hidroksimetil ve a-hidroksimetil metabolitlerine metabolize olur. Değişmeyen ornidazole göre, bu iki metabolit Trichomonas vaginalisve anaerobikbakterilere karşı daha az etkilidir.Eliminasyon:Yarı ömrü yaklaşık 13 saattir. Alınan tek dozun, %85'i çoğu metabolize olarak ilk 5 gün içinde atılır. Dozun %4'ü değişmeyen bileşik olarak idrarla atılmaktadır. Doğrusallık/doğrusal olmayan durum5.3. Klinik öncesi güvenilirlik verileriGeçerli değildir. 5/76. FARMASÖTİK ÖZELLİKLER6.1. Yardımcı maddelerin listesiEtanol (susuz) Propilen glikol 6.2. Geçimsizlikler250 ml serum fizyolojik veya dekstroz solüsyonunda 1 g ornidazol ve 2 g seftriakson fiziksel ve kimyasal olarak geçimlidir. Ancak bu tıbbi ürün diğer tıbbi ürünlerle karıştırılmamalıdır. 6.3. Raf ömrü36 ay 6.4. Saklamaya yönelik özel tedbirler25°C altındaki oda sıcaklığında, ışıktan koruyarak saklayınız. Uygulama için hazırlanan seyreltilmiş çözeltilerin mümkün olan en kısa zamanda kullanılması önerilir. Bir defalık kullanım içindir. Kullanılmayan kısmı atınız. Son kullanma tarihiyle uyumlu olarak kullanınız. Ambalajdaki son kullanma tarihinden sonra TİBERSİD'i kullanmayınız. Eğer üründe ve/veya ambalajında bozukluklar fark ederseniz, TİBERSİD'i kullanmayınız. 6.5. Ambalajın niteliği ve içeriğiŞeffaf, Tip I cam ampullere doldurulmuş ürün, 3 ml'lik ladet ampul içeren karton kutu içinde ambalajlıdır. 6.6. Beşeri tıbbi üründen arta kalan maddelerin imhası ve diğer özel önlemler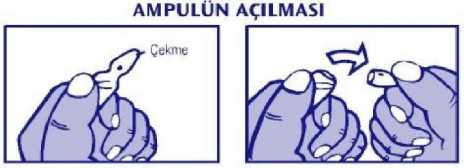
- Nokta yukarıda bulunacak şekilde tutulur. - Ampulün baş kısmı ok yönünde aşağıya doğru çekilir. - Testere kullanılmasına gerek yoktur. Kullanılmamış olan ürünler ya da atık materyaller Tıbbi Atıkların Kontrolü Yönetmeliği ve Ambalaj ve Ambalaj Atıklarının Kontrolü Yönetmeliklerine uygun olarak imha edilmelidir. 7. RUHSAT SAHİBİMenta Pharma İlaç Sanayi ve Ticaret Limited Şirketi Orta Mah. Üniversite Cad. No:35/1 Tuzla/İSTANBUL Tel: 0 216 594 59 36 Faks: 0 216 594 59 35 6/7e-posta:[email protected]8. RUHSAT NUMARASI2015/9219. İLK RUHSAT TARİHİ/RUHSAT YENİLEME TARİHİİlk ruhsat tarihi: 02.12.2015 Ruhsat yenileme tarihi: 20.01.201710. KÜB'ÜN YENİLENME TARİHİ7/7 |
İlaç BilgileriTibersid 500 Mg/3 Ml İv İnfüzyon İçin ÇözeltiEtken Maddesi: Ornidazol Kullanma talimatı ve kısa ürün bilgileri |
Ana Sayfa | Hakkımızda | İlaçlar | İlaç Ara | İlaç Firmaları | Gizlilik | Bize Ulaşın
Telif Hakkı 2008-2026 © İlaç Prospektüsü. Tüm Hakları Saklıdır.Uyarı: Sitemizde yayınladığımız ilaç bilgileri ile doktora danışmadan kesinlikle ilaç kullanmayınız!
Aksi halde doğabilecek sağlık sorunlarından ilacprospektusu.com sorumlu tutulamaz.