Ezetrol 10 Mg Tablet Kısa Ürün BilgisiKISA ÜRÜN BİLGİSİ1. BEŞERİ TIBBİ ÜRÜNÜN ADIEZETROL® 10 mg tablet 2. KALİTATİF VE KANTİTATİF BİLEŞİMEtkin madde:Ezetimib.................................10 mg Yardımcı maddeler:Laktoz monohidrat (ineklerden elde edilir)............55 mg Yardımcı maddeler için 6.1'e bakınız. 3. FARMASÖTİK FORMBir tarafında 414 işareti bulunan beyaz-beyazımtrak renkte, kapsül biçiminde tablet. 4. KLİNİK ÖZELLİKLER4.1. Terapötik endikasyonlarPrimer HiperkolesterolemiMonoterapiEZETROL tek başına uygulandığında primer hiperkolesterolemik (heterozigot ailesel ve ailesel olmayan) hastalarda diyete ek olarak yükselmiş total kolesterolün (toplam-K), düşükdansiteli lipoprotein kolesterol (LDL-K) ve apolipoprotein B (Apo B)'nin düşürülmesindeendikedir. HMG-CoA redüktaz inhibitörleri (statinler) ile kombinasyon tedavisiEZETROL, ile 3-hidroksi-3-metilglutaril-koenzim A (HMG-CoA) redüktaz inhibitörleri (statinler) birlikte uygulandığında primer (heterozigot ailesel ve ailesel olmayan)hiperkolesterolemik hastalarda diyete ek olarak yükselmiş toplam-K'nın, (LDL-K) ve ApoB'nin düşürülmesinde endikedir. Kardiyovasküler Hastalığın ÖnlenmesiEZETROL, devam eden statin tedavisine ilave edildiğinde veya tedaviye bir statin ile eş zamanlı başlatıldığında koroner kalp hastalığı (KKH) olan hastalarda kardiyovaskülerolayların riskini azaltmak için endikedir (bkz. Bölüm 5.1). Homozigot Ailevi Hiperkolesterolemi (HoFH)EZETROL bir statin ile birlikte verildiğinde HoFH'li hastalarda diğer lipid düşürücü tedavilere (örneğin LDL aferezis) ek olarak veya bu tedavilerin mevcut olmadığı durumlardayükselmiş toplam-K ve LDL-K seviyelerinin düşürülmesinde endikedir. Homozigot SitosterolemiEZETROL, homozigot ailevi sitosterolemili hastalarda yükselmiş sitosterol ve kampesterol düzeylerinin düşürülmesinde endikedir. 4.2. Pozoloji ve uygulama şekliHasta lipid düşürücü bir diyet uygulamalıdır ve EZETROL ile tedavi sırasında diyete devam etmelidir. Pozoloji:Tavsiye edilen doz günde 1 defa EZETROL 10 mg tablettir. EZETROL yiyeceklerle birlikte veya aç karnına günün herhangi bir saatinde alınabilir. EZETROL bir statin ile birlikte uygulanabilir (primer hiperlipidemili hastalarda) veya fenofibratlarla birlikte (karışık hiperlipidemili hastalarda) aşamalı etki için uygulanabilir.Daha güvenilir olması için ardışık kullanılan ilaçların doz önerilerine göre EZETROL'üngünlük dozu statinle eş zamanlı olarak alınmalıdır. EZETROL bir statine eklendiğinde, statinin endike olan olağan başlangıç dozuna veya daha önceden başlanan yüksek statin dozuna devam edilmelidir. Bu uygulamada, kullanılan belirlistatinin dozaj talimatlarına başvurulmalıdır. Koroner Kalp Hastalığı olan Hastalarda KullanımKoroner kalp hastalığı olan hastalarda artan kardiyovasküler olayları azaltmak amacıyla, EZETROL 10 mg, kardiyovasküler yararı kanıtlanmış bir statin ile birlikte uygulanabilir. Uygulama şekli:Oral yolla alınır. Özel popülasyonlara ilişkin ek bilgiler Böbrek yetmezliği:Böbrek bozukluğu olan hastalarda doz ayarlanması gerekmez (bkz. bölüm 5.2). Karaciğer yetmezliği:Hafif karaciğer yetmezliği olan hastalarda dozaj ayarlaması gerekmez (Child Pugh skoru 5-6). Orta ve şiddetli karaciğer yetmezliğinde (Child Pugh skoru 7-9 ve 9 un üstü) ezetimibe maruzkalmaya bağlı etkiler bilinmediğinden, EZETROL bu hastalara önerilmemektedir (bkz. bölüm4.4. ve 5.2). Pediyatrik popülasyon:Tedavinin başlatılması uzman incelemesi altında yürütülmelidir. Çocuklar ve ergenler > 6: Ezetimibin 6 ila 17 yaş arasındaki çocuklarda güvenlilik ve etkililiği kanıtlanmamıştır. Mevcut veriler 4.4, 4.8, 5.1 ve 5.2 bölümlerinde açıklanmaktadır,ancak pozoloji için bir tavsiye yapılamamaktadır. EZETROL bir statin ile birlikte uygulandığında, çocuklar için statin dozaj talimatlarına başvurulmalıdır. Çocuklar < 6: EZETROL'ün 6 yaşından küçük çocuklarda uygulanmasının güvenliliği ve etkililiği kanıtlanmamıştır. Geriyatrik popülasyon:Yaşlı hastalarda dozun ayarlanması gerekmez (bkz. bölüm 5.2). Diğer:Safra asidi sekestranları ile birlikte uygulama:EZETROL dozu bir safra asidi sekestranı uygulanmadan önce (> 2 saat geçmeli) veya > 4 saat sonra verilmelidir. 2/20 4.3. KontrendikasyonlarEZETROL, etkin maddeye veya bileşimindeki yardımcı maddelerden herhangi birine aşırı duyarlılığı olanlarda kontrendikedir. EZETROL ile bir statinin birlikte kullanıldığı durumlarda o ilacın KÜB'üne de bakılmalıdır. Gebelik ve emzirme dönemlerinde bir statin ile birlikte EZETROL uygulanması kontrendikedir. EZETROL ile bir statinin kombinasyonu aktif karaciğer hastalığı olan hastalarda ve serum transaminazlarında açıklanamayan, sürekli yükselmeler olan hastalarda kontrendikedir. EZETROL 6 yaşından küçük ÇOCUKLARDA KULLANILMAMALIDIR. Bu yaş grubu ile ilgili bilgi bulunmamamaktadır. 4.4. Özel kullanım uyarıları ve önlemleriEZETROL ile bir statinin birlikte kullanıldığı durumlarda o ilacın KÜB'üne de bakılmalıdır. Karaciğer enzimleri Bir statinle eş zamanlı olarak EZETROL uygulanan hastalarda yürütülen kontrollü çalışmalarda karaciğer transaminaz seviyelerinde ardışık yükselmeler (>3 X normal üst sınırın(NÜS) 3 katı ve daha yüksek), gözlenmiştir. EZETROL bir statin ile birlikte uygulanırken,tedaviye başlanmadan önce statinlerin uyarılarına uygun olarak karaciğer testleri yapılmalıdır(bkz. bölüm 4.8). Sonuçlarda Azalmanın İyileştirilmesi: Uluslararası Vytorin Etkinlik Çalışmasında (IMPROVE-IT), KKH ve AKS olay öyküsü olan 18144 hasta günde bir kez ezetimib/simvastatin 10/40 mg (n = 9067) veya günde bir kez simvastatin 40 mg (n= 9077 )almak üzere randomize edilmiştir. Medyan 6,0 yıllık takip döneminde, transaminazlardaardışık yükselmelerin (>3 X NÜS) insidansı, ezetimib/simvastatin için %2,5 ve simvastatiniçin %2,3 olmuştur (bkz. bölüm 4.8). Kronik böbrek hastalığına sahip 9000'den fazla hastanın günlük 20 mg simvastatin ile birlikte EZETROL 10 mg (n = 4650) veya plasebo (n = 4620) alacak şekilde randomize edildiğikontrollü bir klinik çalışmada (medyan takip süresi 4,9 yıl), ardışık transaminaz artışlarınıninsidansı (> 3 X NÜS) simvastatin ile birlikte EZETROL için %0,7 ve plasebo için %0,6olarak saptanmıştır (bkz. bölüm 4.8). İskelet kası EZETROL ile pazarlama sonrası deneyimde, miyopati ve rabdomiyoliz vakaları bildirilmiştir. Rabdomiyoliz gelişen hastaların çoğu EZETROL'e başlamadan önce birlikte bir statinalmıştır. Ancak rabdomiyoliz EZETROL monoterapisi ile çok seyrek olarak ve EZETROL ilerabdomiyoliz riskinde artışla ilişkili olduğu bilinen başka ajanların birlikte kullanımında daçok seyrek olarak bildirilmiştir. Kas semptomlarına dayanarak miyopatiden kuşkulanılırsaveya miyopati normalin üst sınırının 10 katı kreatin fosfokinaz (CPK) düzeyi ile doğrulanırsa,EZETROL, hastanın eş zamanlı aldığı statin veya rabdomiyoliz riskini arttıran bu ajanlardanherhangi biri derhal kesilmelidir. EZETROL tedavisine başlayan tüm hastalara miyopati riskikonusunda bilgi verilmeli ve kaslarda açıklanamayan ağrı, hassasiyet veya güçsüzlükolduğunda bunu derhal bildirmeleri söylenmelidir (bkz. bölüm 4.8). 3/20 IMPROVE-IT çalışmasında, KKH ve AKS olay öyküsü olan 18144 hasta günde bir kez ezetimib/simvastatin 10/40 mg (n = 9067) veya günde bir kez simvastatin 40 mg (n = 9077)almak üzere randomize edilmiştir. Medyan 6,0 yıllık takip döneminde, miyopati insidansıezetimib/simvastatin için %0,2 ve simvastatin için %0,1 olmuştur. Miyopati kaslardaaçıklanamayan güçsüzlük veya ağrı ile birlikte bir serum CK (kreatin kinaz) değerinde üstnormal sınırın > 10 katı yükselme veya peşpeşe iki ölçümde CK > 5 ve < 10 x NÜS yükselmegözlenmesi şeklinde tanımlanmıştır. Rabdomiyoliz insidansı ezetimib/simvastatin için %0,1ve simvastatin için %0,2 olarak saptanmıştır; rabdomiyoliz kaslarda açıklanamayan güçsüzlükveya ağrı ile birlikte bir serum CK değerinde > 10 x NÜS yükselmeye eşlik eden böbrekhasarı kanıtları veya CK > 10000 mU/mL olarak tanımlanmıştır (bkz. bölüm 4.8.). Kronik böbrek hastalığına sahip 9000'den fazla hastanın günlük 20 mg simvastatin ile birlikte EZETROL 10 mg (n= 4650 ) veya plasebo (n= 4620 ) alacak şekilde randomize edildiğikontrollü bir klinik çalışmada (medyan takip süresi 4,9 yıl), miyopati/rabdomiyoliz insidansısimvastatin ile birlikte EZETROL için %0,2 ve plasebo için %0,1 olarak belirlenmiştir (bkz.bölüm 4.8). Karaciğer yetmezliği Orta ve şiddetli karaciğer yetmezliğinde ezetimibe maruz kalmaya bağlı etkiler bilinmediğinden, EZETROL bu hastalara önerilmemektedir (bkz. bölüm 5.2). Pediyatrik popülasyon Heterozigot ailesel veya ailesel olmayan hiperkolesterolemisi olan 6 ila 10 yaşındaki hastalarda EZETROL'ün etkililik ve güvenliliği 12 haftalık plasebo-kontrollü klinik birçalışmada değerlendirilmiştir. 12 haftadan uzun tedavi sürelerinde ezetimibin etkileri bu yaşgrubunda incelenmemiştir (bkz. bölüm 4.2, 4.8, 5.1 ve 5.2). EZETROL 6 yaşından küçük hastalarda incelenmemiştir (bkz. bölüm 4.2 ve 4.8). Heterozigot ailevi hiperkolesterolemili 10-17 yaş arası hastalarda simvastatin ile birlikte EZETROL uygulanmasının etkililik ve güvenliliği adolesan erkekler (Tanner Evre II veyaüzeri) ve mensleri en az 1 yıl önce başlamış kızlarda yürütülen kontrollü bir klinik çalışmadadeğerlendirilmiştir. Bu sınırlı kontrollü çalışmada, adolesan erkeklerde veya kızlarda genel olarak büyüme veya cinsel olgunlaşma üzerinde ölçülebilir bir etki ve kızlarda menstrüel siklus uzunluğu üzerindeherhangi bir etki gözlenmemiştir. Ancak 33 haftadan uzun süren tedavi döneminde ezetimibinbüyüme ve cinsel olgunlaşma üzerindeki etkileri çalışılmamıştır (bkz. bölüm 4.2 ve 4.8). Günde 40 mg'dan yüksek simvastatin dozlarıyla birlikte uygulanan EZETROL'ün güvenlilik ve etkililiği 10-17 yaş arası pediyatrik hastalarda incelenmemiştir. Simvastatin ile birlikte uygulanan EZETROL'ün güvenlilik ve etkililiği 10 yaşından küçük pediyatrik hastalarda çalışılmamıştır (bkz. bölüm 4.2 ve 4.8). 17 yaşından küçük hastalarda EZETROL ile uzun süreli tedavinin erişkin çağda morbidite ve mortaliteyi azaltmadaki etkinliği incelenmemiştir. Fibratlar:Fibratlarla birlikte EZETROL uygulanmasının güvenliliği ve etkililiği kanıtlanmamıştır. 4/20 EZETROL ve fenofibrat alan hastada safra taşından kuşkulanılırsa safra kesesi tetkikleri gerekir ve bu tedavi kesilmelidir (bkz.bölüm 4.5 ve 4.8). Siklosporin:Siklosporin kullanımı sırasında hastaya EZETROL başlarken dikkatli olunmalıdır. EZETROL ve siklosporin alan hastalarda siklosporin konsantrasyonları izlenmelidir (bkz. bölüm 4.5). AntikoagülanlarEZETROL varfarin, diğer kumarin tipi antikoagülanlar veya fluindion ile birlikte kullanıldığında Uluslararası Normalize Oran (INR) uygun şekilde izlenmelidir (bkz. bölüm4.5). Yardımcı maddelerBu ürün 55 mg laktoz monohidrat içerir. Nadir kalıtımsal galaktoz intoleransı, Lapp laktaz eksikliği ya da glukoz-galaktoz malabsorpsiyon problemi olan hastaların bu ilacıkullanmamaları gerekir. EZETROL, her bir tablet başına 1 mmol (23 mg)'dan daha az sodyum ihtiva eder; yani aslında sodyum içermez. 4.5. Diğer tıbbi ürünlerle etkileşimler ve diğer etkileşim şekilleriKlinik öncesi çalışmalarda, ezetimibin sitokrom P450 ilaç metabolizma enzimlerini indüklemediği gösterilmiştir. Sitokrom P450 1A2, 2D6, 2C8, 2C9 ve 3A4 veya N-asetiltransferaz ile metabolize edildiği bilinen ilaçlar ile ezetimib arasında klinik yöndenanlamlı farmakokinetik etkileşimler gözlenmemiştir. Klinik etkileşim çalışmalarında ezetimib, birlikte uygulama sırasında dapson, dekstrometorfan, digoksin, oral kontraseptifler (etinil östradiol ve levonorgestrel), glipizid, tolbutamid veya midazolamın farmakokinetikleri üzerinde hiçbir etki göstermemiştir.Ezetimib ile birlikte uygulanan simetidinin ezetimibin biyoyararlanımı üzerinde hiçbir etkisiolmamıştır. AntasitlerEş zamanlı antasit uygulanması ezetimibin emilim hızını azaltmış ancak ezetimibin biyoyararlanımını etkilememiştir. Emilim hızındaki bu azalma klinik yönden anlamlı kabuledilmemektedir. KolestiraminEş zamanlı kolestiramin uygulanması total ezetimibin (ezetimib + ezetimib- glukuronidi) eğri altında kalan ortalama alanını (EAA) yaklaşık %55 azaltmıştır. Kolestiramine EZETROLeklenmesiyle düşük dansiteli lipoprotein kolesteroldeki (LDL-K) yüksek düşüş bu etkileşimnedeniyle azalabilir (bkz. bölüm 4.2). FibratlarFenofibrat ve EZETROL alan hastalarda, hekimler muhtemel kolelitiyazis ve safra kesesi hastalığı riskine karşı dikkatli olmalıdır (bkz. bölüm 4.4 ve 4.8). Fenofibrat ve EZETROL alan bir hastada kolelitiyazisden şüphelenilirse, safra kesesi tetkikleri gerekmekte ve bu tedavi kesilmelidir (bkz. bölüm 4.8). 5/20 Eş zamanlı fenofibrat veya gemfibrozil uygulanması total ezetimib konsantrasyonlarını hafifçe yükseltmiştir (sırasıyla yaklaşık 1,5 ve 1,7 kat). EZETROL'ün diğer fibratlarla kombine uygulanması incelenmemiştir. Fibratlar safraya kolesterol atılımını arttırarak kolelitiyazise neden olabilir. Hayvan çalışmalarında ezetimib tüm türlerde olmamakla birlikte safra kesesindeki kolesterol miktarınıbazen yükseltmiştir (bkz. bölüm 5.3). EZETROL'ün terapötik kullanımıyla ilişkili litojenik(taş oluşumu) risk dışlanamaz. StatinlerEzetimib atorvastatin, simvastatin, pravastatin, lovastatin, fluvastatin veya rosuvastatin ile birlikte uygulandığında klinik yönden anlamlı farmakokinetik etkileşimler görülmemiştir. SiklosporinSiklosporinin stabil bir dozunu alan ve kreatinin klerensi > 50 mL/dak olan böbrek transplantasyonu yapılmış sekiz hastadaki bir çalışmada, EZETROL'ün tekli 10 mg dozubaşka bir çalışmada (n = 17) tek başına ezetimib alan sağlıklı bir kontrol popülasyonuna göretotal ezetimibin ortalama EAA'sında 3.4 kat (aralık 2,3-7,9 kat) artışa yol açmıştır. Farklı birçalışmada, siklosporin ile birlikte başka birçok ilaç alan böbrek transplantasyonu yapılmış,ciddi böbrek yetmezliği olan bir hastanın total ezetimib maruz kalımında tek başına ezetimibalan benzer kontrollere göre 12 kat artış görülmüştür. Sağlıklı 12 gönüllüde yapılan ikidönemli, çapraz tasarımlı bir çalışmada, 8 gün süreyle günde 20 mg ezetimib ve 7. gündesiklosporinin tekli 100 mg dozunun uygulanması tek başına siklosporin 100 mg dozuna göresiklosporinin EAA'sında ortalama %15 artışa (aralık: %10 azalmadan %51 artışa kadar) yolaçmıştır. Böbrek transplantasyonu yapılmış hastalarda birlikte uygulanan ezetimibinsiklosporin maruz kalımına etkisini inceleyen kontrollü bir çalışma yapılmamıştır. Siklosporintedavisi sırasında EZETROL'e başlanırken dikkatli olunmalıdır. EZETROL ve siklosporinalan hastalarda siklosporin konsantrasyonları izlenmelidir (bkz. bölüm 4.4). AntikoagülanlarEş zamanlı ezetimib uygulanması (günde 10 mg) sağlıklı 12 erişkin erkekte yapılan bir çalışmada varfarinin biyoyararlanımını ve protrombin zamanını anlamlı olarak etkilememiştir.EZETROL'ün varfarin veya fluindiona eklendiği hastalarda INR'de artışa ilişkin pazarlamasonrası raporlar alınmıştır. EZETROL varfarin, diğer kumarin türevi antikoagülanlar veyafluindion ile birlikte kullanıldığında INR uygun şekilde izlenmelidir (bkz. bölüm 4.4). Özel popülasyonlara ilişkin ek bilgilerPediyatrik popülasyonEtkileşim çalışmaları yalnızca yetişkinlerde yapılmıştır. 4.6. Gebelik ve laktasyonGenel tavsiyeGebelik kategorisi:C Çocuk doğurma potansiyeli bulunan kadınlar/Doğum kontrolü(Kontrasepsiyon)Çocuk doğurma potansiyeli bulunan kadınlarda üreme etkilerini değerlendirmek için klinik çalışma yoktur. 6/20 Gebelik dönemiGebe kadınlara EZETROL yalnızca kesin bir gereklilik olduğunda verilmelidir. Gebelik döneminde EZETROL kullanımına ilişkin hiçbir klinik veri yoktur. Monoterapi şeklinde uygulanan ezetimib ile yürütülen hayvan çalışmaları gebelik, embriyofetal gelişim, doğum veya doğum sonrası gelişim üzerinde doğrudan veya dolaylızararlı etkilere dair bulgular göstermemiştir (bkz. bölüm 5.3). İnsanlara yönelik potansiyelrisk bilinmemektedir. Gebelik ve emzirme döneminde EZETROL ile bir statinin birlikte uygulanması kontrendikedir (bkz. bölüm 4.3); lütfen statinin Kısa Ürün Bilgisine bakınız. Laktasyon dönemi:EZETROL emzirme döneminde kullanılmamalıdır. Sıçanlarda yapılan çalışmalar ezetimibin anne sütüne geçtiğini göstermektedir. Ezetimibin insanlarda anne sütüne geçip geçmediğibilinmemektedir. Üreme yeteneği (fertilite)Ezetimibin insan fertilitesi üzerindeki etkisi hakkında klinik çalışma verisi bulunmamaktadır. Ezetimibin erkek veya dişi sıçanların fertilitesi üzerinde etkisi bulunmamaktadır (bkz. bölüm5.3). 4.7. Araç ve makine kullanımı üzerindeki etkilerEzetimibin araç ve makine kullanımına etkisi üzerine yapılmış çalışma yoktur. Ancak araç ve makine kullanırken, baş dönmesinin rapor edildiği göz önünde bulundurulmalıdır. 4.8. İstenmeyen etkilerİstenmeyen etkilerin listesi (klinik çalışmalar ve pazarlama sonrası deneyim) 112 haftaya kadar devam eden klinik çalışmalarda günde 10 mg EZETROL tek başına 2396 hastaya, bir statin ile birlikte 11308 hastaya veya fenofibrat ile birlikte 185 hastayauygulanmıştır. İstenmeyen reaksiyonlar genellikle hafif ve geçici olarak belirlenmiştir.EZETROL ile bildirilen istenmeyen olayların genel insidansı plaseboyla bildirilen ilebenzerdir. İstenmeyen olaylar nedeniyle tedaviyi bırakma oranı da EZETROL ve plasebo içinbenzer bulunmuştur. EZETROL tek başına veya bir statin ile birlikte uygulandığında: Aşağıdaki istenmeyen reaksiyonlar tek başına EZETROL alan hastalarda (n = 2396) plaseboya (n = 1159) veya bir statin ile birlikte EZETROL (n = 11308) alan hastalardabirlikte uygulanan statine (n = 9361) göre daha yüksek insidansla bildirilmiştir. EZETROL'ün(monoterapi olarak veya bir statin ile birlikte uygulanan) klinik çalışmalarında gözlenen veyapazarlama sonrası kullanımda EZETROL'ün tek başına veya bir statinle uygulanması sonucubildirilen advers reaksiyonlar Tablo 1'de listelenmiştir. Bu reaksiyonlar sistem organ sınıfınave görülme sıklığına göre sunulmaktadır. Sıklıklar şöyle tanımlanır: Çok yaygın ( >1/10); yaygın (> 1/100 ila <1/10); yaygın olmayan (>1/1.000 ila <1/100); seyrek (>1/10.000 ila <1/1,000), çok seyrek (<1/10.000) ve bilinmiyor(eldeki verilerden hareketle tahmin edilemiyor). Tablo 1 7/20
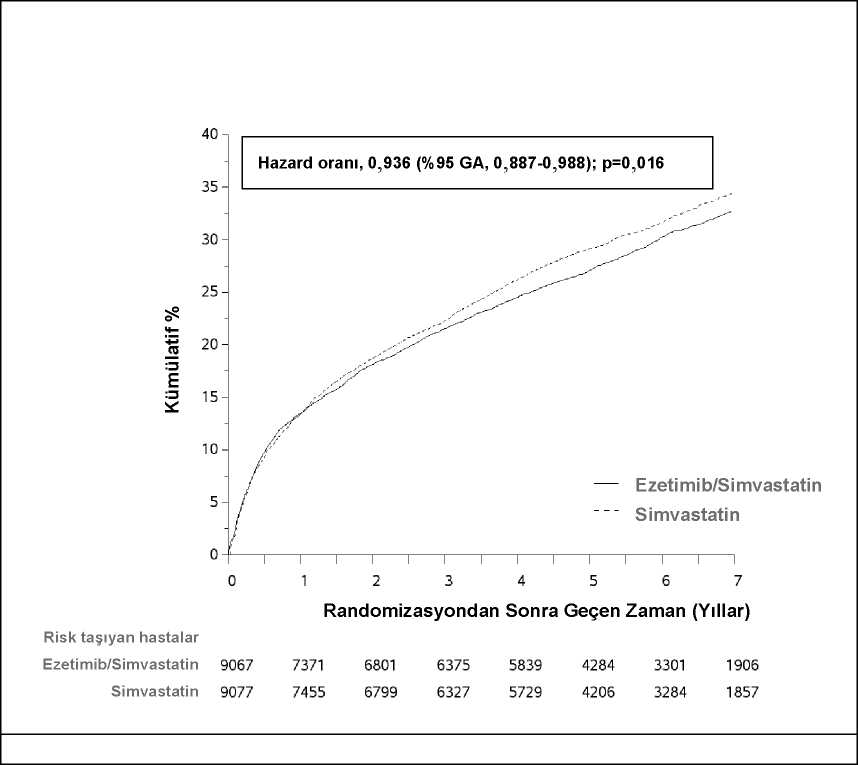
EZETROL ve fenofibrat birlikte uygulandığında:Gastrointestinal hastalıklar:Yaygın:Karın ağrısı8/20 Çok-merkezli, çift-kör, plasebo-kontrollü klinik bir çalışma, karışık hiperlipidemili hastalarda yapılmıştır. 625 hasta 12 haftaya kadar tedavi edilirken 576 hasta 1 yıla kadar tedavigörmüştür. Bu çalışmada 172 hasta EZETROL ve fenofibrat ile aldıkları tedaviyi 12 haftadatamamlamışlar ve 230 hasta EZETROL ve fenofibratla aldıkları tedaviyi (109 hasta tedavininilk 12 haftasında sadece EZETROL almıştır) 1 yılda tamamlamıştır. Bu çalışma tedavigrupları arasındaki sık görülmeyen durumları karşılaştırmak üzere tasarlanmamıştır. Serumtransaminazlarındaki klinik olarak önemli (>3 X NÜS, ardışık) yükselmelerin insidansı (%95GA (güven aralığı)) fenofibrat monoterapisi ve EZETROL ile birlikte fenofibrat tedavisinde%4,5 (1,9, 8,8) ve %2,7 (1,2, 5,4)'tür. Kolesistektomi için karşılık gelen insidansı, fenofibratmonoterapisi için ve EZETROL ile birlikte fenofibrat için sırasıyla %0,6 (0,0, 3,1) ve %1,7(0,6, 4,0)'dir (bkz. bölüm 4.4 ve 4.5). Pediyatrik (6-17 yaş arası) HastalarHeterozigot ailesel veya ailesel olmayan hiperkolesterolemisi olan pediyatrik (6 ila 10 yaş) hastaları kapsayan bir çalışmada (n = 138), ALT ve/veya AST artışları (> 3X NÜS, ardışık),plasebo grubundaki %0 ile karşılaştırıldığında ezetimib hastalarında %1,1 (1 hasta) olarakgözlenmiştir. CPK artışı (> 10X NÜS) söz konusu olmamıştır. Miyopati vakası raporedilmemiştir. Heterozigot ailevi hiperkolesterolemili adolesan (10-17 yaş arası) hastalarda (n =248) yürütülen bir çalışmada ALT ve/veya AST'de (>3 X NÜS, ardışık) yükselmelerezetimib/simvastatin alan hastaların %3'ünde (4 hasta) ve simvastatin monoterapi grubundakihastaların %2'sinde (2 hasta) gözlenmiştir; CPK'de (>10X NÜS) yükselme için rakamlarsırasıyla %2 (2 hasta) ve %0'dır. Hiçbir miyopati vakası bildirilmemiştir. Bu çalışma seyrek istenmeyen ilaç reaksiyonları karşılaştırılacak şekilde tasarlanmamıştır. Koroner Kalp Hastalığı ve AKS Olay Öyküsü olan HastalarEzetimib/simvastatin 10/40 mg (n=9067; bunlardan %6'sı ezetimib/simvastatin dozu 10/80 mg'ye titre edilmiştir) veya simvastatin 40 mg (n=9077; bunlardan %27'sinde simvastatindozu 80 mg'ye titre edilmiştir) ile tedavi edilen 18144 hastayı içeren IMPROVE-ITçalışmasında (bkz. bölüm 5.1), güvenlilik profillerinin medyan 6,0 yıllık takip dönemindebenzer olduğu saptanmıştır. İstenmeyen olaylar nedeniyle tedaviyi bırakma oranlarıezetimib/simvastatin tedavisi alan hastalarda %10,6 ve simvastatin ile tedavi edilen hastalarda%10,1'dir. Miyopati insidansı ezetimib/simvastatin için %0,2 ve simvastatin için %0,1'dir;miyopati kaslarda açıklanamayan güçsüzlük veya ağrı ile birlikte bir serum CK değerindenormal üst sınırın (NÜS) >10 katı yükselme veya peşpeşe iki ölçümde CK >5 ve <10 x NÜSyükselme gözlenmesi şeklinde tanımlanmıştır. Rabdomiyoliz insidansı ezetimib/simvastatiniçin %0,1 ve simvastatin için %0,2 olarak belirlenmiştir; rabdomiyoliz kaslardaaçıklanamayan güçsüzlük veya ağrı ile birlikte bir serum CK değerinde >10 x NÜSyükselmeye eşlik eden böbrek hasarı kanıtları veya CK >10000 mU/mL olaraktanımlanmıştır. Transaminazlarda ardışık yükselmelerin (>3 X NÜS) insidansıezetimib/simvastatin için %2,5 ve simvastatin için %2,3'dür (bkz. bölüm 4.4.) Safra kesesiyleilişkili istenmeyen etkiler ezetimib/simvastatin tedavisine yerleştirilen hastaların %3,1'inde vesimvastatin tedavisine yerleştirilen hastaların %3,5'inde bildirilmiştir. Kolesistektominedeniyle hospitalizasyonlarıninsidansı heriki tedavi grubunda %1,5'dir. Ezetimib/simvastatin veya simvastatin alan hastaların sırasıyla %9,4 ve %9,5'ine çalışma döneminde kanser (herhangi yeni malignite olarak tanımlanmıştır) tanısı konmuştur. 9/20 Kronik Böbrek Hastalığına Sahip HastalarGünlük EZETROL 10 mg ve simvastatin 20 mg sabit doz kombinasyonu (n = 4650) veya plasebo (n = 4620) ile tedavi edilen 9000'den fazla hastayı kapsayan Kalp ve Böbrek KorumaÇalışmasında (SHARP) güvenlilik profilleri 4,9 yıllık medyan takip süresincekarşılaştırılabilirdir. Bu klinik çalışmada, yalnızca ciddi advers olaylar ve herhangi bir adversolay nedeniyle tedavi kesintileri kaydedilmiştir. Advers olaylar nedeniyle tedavinin bırakılmaoranı benzerdir (simvastatin ile birlikte EZETROL ile tedavi edilen hastalarda %10,4, plaseboile tedavi edilen hastalarda %9,8). Miyopati/rabdomiyoliz insidansı, simvastatin ile birlikteEZETROL ile tedavi edilen hastalarda %0,2 ve plasebo ile tedavi edilen hastalarda %0,1'di.Transaminazların ardışık artışları (> 3X NÜS), simvastatin ile birlikte EZETROL ile tedaviedilen hastalarda %0,7 iken plasebo ile tedavi edilen hastalarda %0,6 olarak bulunmuştur(bkz. bölüm 4.4). Bu klinik çalışmada, kanser (simvastatin ile birlikte EZETROL için %9,4,plasebo için %9,5), hepatit, kolesistektomi veya safra taşı komplikasyonları veya pankreatitdahil olmak üzere önceden belirlenmiş advers olayların insidansında istatistiki olarak anlamlıartışlar olmamıştır. Laboratuvar değerleriKontrollü klinik monoterapi çalışmalarında serum transaminazlarında (ALT ve/veya AST >X3 NÜS) klinik olarak gözlenen önemli artışların insidansı, EZETROL (%0,5) ile plasebo(%0,3) arasında benzer bulunmuştur. Birlikte uygulama çalışmalarında statinle birlikteEZETROL uygulanan hastalarda insidans %1,3 iken, sadece statinle tedavi edilen hastalardainsidans %0,4'tür. Bu yükselişler genellikle asemptomatik, kolestazla ilişkisi olmayan vetedavinin sona erdirilmesiyle veya tedavinin devamında son bulan etkilerdir (bkz. bölüm 4.4). Klinik çalışmalarda CPK>10 X NÜS tek başına EZETROL uygulanan 1674 hastanın 4'ünde (%0,2) rapor edilmesine karşın plasebo uygulanan 786 hastanın 1'inde (%0,1) ve EZETROLile birlikte statin uygulanan 917 hastanın 1'inde (%0,1) ve yalnızca statin uygulanan 929hastanın 4'ünde (%0,4) rapor edilmiştir. İlgili kontrol kolu (plasebo veya yalnız statin) ilekarşılaştırıldığında EZETROL ile ilişkili miyopati ve rabdomiyolizde artış gözlemlenmemiştir(bkz. bölüm 4.4). Şüpheli advers reaksiyonların raporlanmasıRuhsatlandırma sonrası şüpheli ilaç advers reaksiyonlarının raporlanması büyük önem taşımaktadır. Raporlama yapılması, ilacın yarar/risk dengesinin sürekli olarak izlenmesineolanak sağlar. Sağlık mesleği mensuplarının herhangi bir şüpheli advers reaksiyonu TürkiyeFarmakovijilans Merkezi (TÜFAM)'ne bildirmeleri gerekmektedir (www.titck.gov.tr; e-posta: [email protected]; tel: 0 800 314 00 08; faks: 0312 218 35 99). 4.9. Doz aşımı ve tedavisiKlinik çalışmalarda günde 50 mg ezetimibin 15 sağlıklı bireye 14 güne kadar uygulanması veya günde 40 mg ezetimibin primer hiperkolesterolemili 18 hastaya 56 güne kadaruygulanması genel olarak iyi tolere edilmiştir. Hayvanlarda: sıçanlarda ve farelerdeezetimibin tekli oral 5000 mg/kg dozları ve 3000 mg/kg dozlarından sonra toksisitegözlenmemiştir. EZETROL ile çok az sayıda doz aşımı olgusu bildirilmiştir; bunların çoğu istenmeyen olaylar ile ilişkili olmamıştır. Bildirilen istenmeyen olaylar ciddi değildir. Doz aşımı halinde,semptomatik ve destekleyici önlemler alınmalıdır. 10/20 5. FARMAKOLOJİK ÖZELLİKLER5.1. Farmakodinamik özelliklerFarmasötik grubu: Diğer lipid düşürücü ajanlar ATC kodu: C10AX09 Etki mekanizmasıEZETROL kolesterol ve ilişkili bitki sterollerinin barsaktan emilimini seçici olarak inhibe eden yeni bir lipid düşürücü bileşik sınıfına mensuptur. Ezetimib oral olarak aktiftir ve diğerkolesterol düşürücü ilaçlardan (HMG-KoA redüktaz inhibitörleri (statinler), safra asidisekestranları [reçineler], fibrik asit türevleri ve bitki stenolleri) farklı bir etki mekanizmasınasahiptir. Ezetimibin molekül er hedefinin sterol taşıyıcısı Niemann- Pick C1-benzeri 1(NPC1L1) molekülü olduğu gösterilmiştir; NPC1L1 kolesterol ve fitosterollerin barsaktanuptake'inde rol oynar. Ezetimib ince barsağın fırçamsı kenarına lokalize olur ve kolesterol emilimini inhibe ederek karaciğere giden barsak kolesterolünü azaltır; statinler ise karaciğerde kolesterol senteziniazaltır. Birlikte bu iki mekanizma komplementer kolesterol azaltımı sağlar.Hiperkolesterolemili 18 hastada yapılan 2 haftalık klinik bir çalışmada EZETROL barsaktankolesterol emilimini plaseboya göre %54 inhibe etmiştir. Farmakodinamik etkilerEzetimibin kolesterol emilimini inhibe etmede seçiciliğini belirlemek amacıyla bir dizi klinik öncesi çalışma yapılmıştır. Ezetimib, [14C]-kolesterol emilimini inhibe ederken trigliseridler,yağ asitleri, safra asitleri, progesteron, etinil östradiol veya yağda çözünen vitaminlerin (A veD) emilimi üzerinde hiçbir etki göstermemiştir. Epidemiyolojik çalışmalar kardiyovasküler morbidite ve mortalitenin total-K ve LDL-K düzeyiyle doğru orantılı ve HDL-K düzeyiyle ters orantılı şekilde değiştiğini ortayakoymuştur. EZETROL'ün bir statin ile birlikte uygulanması KKH ve AKS olay öyküsü olan hastalarda kardiyovasküler olayların riskini azaltmada etkilidir. Klinik etkililik ve güvenlilikKontrollü klinik çalışmalarda, monoterapi şeklinde veya bir statin ile birlikte uygulanan EZETROL hiperkolesterolemili hastalarda total kolesterol (total-K), düşük dansitelilipoprotein kolesterol (LDL-K), apolipoprotein B (Apo B) ve trigliseridleri (TG) anlamlıolarak düşürmüş ve yüksek dansiteli lipoprotein kolesterolü (HDL-K) yükseltmiştir. Primer HiperkolesterolemiSekiz haftalık çift-kör, plasebo-kontrollü bir çalışmada, statin monoterapisi alan ve Ulusal Kolesterol Eğitim Programının (NCEP) LDL-K hedefinde olmayan (başlangıç özelliklerinebağlı olarak 2,6 - 4,1 mmol/L [100 - 160 mg/dL]) 769 hiperkolesterolemili hasta devam edenstatin tedavisine ek olarak EZETROL 10 mg veya plasebo almak üzere randomizeedilmişlerdir. Başlangıçta LDL-K hedefinde olmayan, statin tedavisi alan hastalarda (~%82), EZETROL'e randomize edilenlerde çalışmanın son noktasında LDL-K hedefine ulaşanların oranıplaseboya randomize edilenlere göre anlamlı olarak daha yüksektir (sırasıyla %72 ve %19).LDL-K azaltımları birbirinden anlamlı olarak farklıdır (EZETROL için %25, plasebo için 11/20 %4). Ayrıca, devam eden statin tedavisine eklenen EZETROL total-K, Apo B, TG'yi plaseboya göre anlamlı olarak düşürürken HDL-K'yı yükseltmiştir. Statin tedavisine eklenenEZETROL veya plasebo medyan C-reaktif proteini başlangıca göre sırasıyla %10 ve %0azaltmıştır. Primer hiperkolesterolemili 1719 hastada yürütülen iki çift-kör, randomize, plasebo-kontrollü, 12 haftalık çalışmada EZETROL 10 mg, total-K (%13), LDL-K (%19), Apo B (%14) veTG'yi (%8) plaseboya göre anlamlı olarak düşürmüş ve HDL-K'yı yükseltmiştir (%3).Ayrıca, EZETROL yağda eriyen vitaminlerin (A, D ve E) plazma konsantrasyonları veprotrombin zamanı üzerinde hiçbir etki göstermemiş ve diğer lipid düşürücü ajanlar gibiadrenokortikal steroid hormon üretimini bozmamıştır. Çok-merkezli, çift-kör, kontrollü bir klinik çalışmada (ENHANCE), heterozigot ailevi hiperkolesterolemili 720 hasta 2 yıl süreyle ezetimib 10 mg ile simvastatin 80 mgkombinasyonu (n = 357) veya sadece simvastatin 80 mg (n = 363) almak üzere randomizeedilmiştir. Çalışmanın birincil amacı, ezetimib/simvastatin kombinasyon tedavisinin karotidarter intima-media kalınlığı (İMK) üzerindeki etkisini simvastatin monoterapisiylekarşılaştırmaktır. Bu dolaylı markerin kardiyovasküler morbidite ve mortalite üzerindekietkisi henüz gösterilmemiştir. Birincil son nokta olan altı karotid segmentinin tümünde ortalama İMK değişimi B-mod ultrasonla ölçüldüğünde iki tedavi grubu arasında anlamlı olarak farklı bulunmamıştır(p=0,29). Ezetimib 10 mg ile simvastatin 80 mg kombinasyonu veya tek başına simvastatin80 mg ile intima-media kalınlığı çalışmanın 2 yılında sırasıyla 0,0111 mm ve 0,0058 mmartmıştır (başlangıçtaki ortalama karotid İMK sırasıyla 0,68 mm ve 0,69 mm). Ezetimib 10 mg ile simvastatin 80 mg kombinasyonu LDL-K, total-K, Apo B ve TG'yi simvastatin 80 mg'ye göre anlamlı olarak daha fazla düşürmüştür. HDL-K'de yüzde artış ikitedavi grubunda benzerdir. Ezetimib 10 mg ile simvastatin 80 mg kombinasyonu içinbildirilen istenmeyen olaylar onun bilinen güvenlilik profiliyle uyumludur. Pediyatrik popülasyonÇok merkezli, çift kör, kontrollü çalışmada, 6 ila 10 yaşında olan (ortalama yaş 8,3), heterozigot ailesel veya ailesel olmayan hiperkolesterolemisi (HeFH) olan ve başlangıç LDL-K düzeyleri 3,74 ila 9,92 mmol/l olan 138 hasta (59 erkek ve 79 kız), 12 hafta boyuncaEZETROL 10 mg veya plaseboya randomize edilmiştir. 12. haftada EZETROL, plasebo ile karşılaştırıldığında total-K (-%21 vs. %0), LDL-C (-%28 vs. -%1), Apo-B (-%22 vs. -%1) ve non-HDL-K'yı (-%26 vs. %0) anlamlı derecededüşürmüştür. İki tedavi grubuna yönelik sonuçlar TG ve HDL-K için benzerdir (sırasıyla -%6vs. +%8, +%2 vs. +%1). Çok-merkezli, çift-kör, kontrollü bir çalışmada, başlangıçtaki LDL-K düzeyleri 4,1 ile 10,4 mmol/L arasında olan, heterozigot ailevi hiperkolesterolemili (HeFH) 10-17 yaş arası(ortalama yaş 14,2) 142 erkek (Tanner evresi II ve üzeri) ve menarş sonrası 106 kız 6 haftaboyunca EZETROL 10 mg ile birlikte simvastatin (10, 20 veya 40 mg) ya da tek başınasimvastatin (10, 20 veya 40 mg); sonraki 27 haftada EZETROL ile birlikte 40 mg simvastatinveya tek başına 40 mg simvastatin ve sonraki 20 hafta boyunca açık etiketli olarak birlikteuygulanan EZETROL ve simvastatin (10 mg, 20 mg veya 40 mg) tedavisine randomizeedilmiştir. 12/20 Altıncı haftada, EZETROL ile birlikte simvastatin uygulanması (tüm dozlar) total-K (%38'e karşı %26), LDL-K (%49'a karşı %34), Apo B (%39'a karşı %27) ve non-HDL-K'yi (%47'yekarşı %33) tek başına simvastatine (tüm dozlar) göre anlamlı olarak düşürmüştür. İki tedavigrubunda TG ve HDL-K sonuçları benzerdir (-%17'ye karşı -%12 ve + %7'ye karşı +%6). 33.haftadaki sonuçlar 6. haftadakilerle benzerdir ve NCEP AAP'nin ideal LDL-K hedefine (< 2,8mmol/L [110 mg/dL]) ulaşanların sayısı EZETROL ile 40 mg simvastatin alan (%62)hastalarda 40 mg simvastatin (%25) alanlara kıyasla anlamlı olarak daha fazla bulunmuştur.Açık etiketli fazın sonu olan 53. haftada lipid parametreleri üzerindeki etkiler korunmuştur. Günde 40 mg'dan yüksek simvastatin dozlarıyla birlikte uygulanan EZETROL'ün güvenlilik ve etkililiği 10-17 yaş arası pediyatrik hastalarda çalışılmamıştır. Simvastatin ile birlikteuygulanan EZETROL'ün güvenliliği ve etkililiği 10 yaşından küçük pediyatrik hastalardaçalışılmamıştır. 17 yaşından küçük hastalarda EZETROL ile uzun süreli tedavinin erişkinçağda morbidite ve mortaliteyi azaltmadaki etkililiği incelenmemiştir. Kardiyovasküler Hastalığın ÖnlenmesiSonuçlarda Azaltımın İyileştirilmesi: Uluslararası Vytorin Etkinlik Çalışması (IMPROVE-IT) akut koroner sendrom (AKS; akut miyokard enfarktüsü [ME] veya kararsız angina [KA])nedeniyle hospitalizasyondan sonraki 10 gün içinde çalışmaya dahil edilen 18144 hastadayürütülen çok-merkezli, randomize, çift-kör, aktif-kontrollü bir çalışmadır. AKS ilebaşvurdukları tarihte hastaların LDL-K değeri eğer lipid düşürücü tedavi almamışlarsa <125 mg/dL (< 3,2 mmol/L) ve lipid düşürücü tedavi almışlarsa <100 mg/dL'dır(<2,6 mmol/L). Tüm hastalar ezetimib/simvastatin 10/40 mg (n=9067) veya simvastatin 40 mg(n=9077) almak üzere 1:1 oranında randomize edilmiş ve medyan 6,0 yıl boyunca takipedilmiştir. Hastaların ortalama yaşı 63,6'dır; %76'sı erkek, %84'ü beyaz ve %27'si diyabetiktir. Çalışmaya giriş için kriter olan olay tarihinde ortalama LDL-K değeri lipid düşürücü tedavi(n=6390) alanlarda 80 mg/dL (2,1 mmol/L) ve daha önce lipid düşürücü tedavi almamışolanlarda 101 mg/dL'dir (2,6 mmol/L) (n=11594). Çalışmaya giriş kriteri olan AKS olayı içinhospitalizasyondan önce, hastaların %34'ü statin tedavisi almaktadır. Birinci yılda, tedaviyedevam eden hastalarda ortalama LDL-K ezetimib/simvastatin grubunda 53,2 mg/dL(1,4 mmol/L) ve simvastatin monoterapisi alan grupta 69,9 mg/dL'dir (1,8 mmol/L). Lipiddeğerleri genellikle çalışma tedavisine devam eden hastalardan elde edilmiştir. Birincil son nokta, kardiyovasküler ölüm, majör koroner olaylar (MKO'lar; randomize tedaviye yerleşimden en az 30 gün sonra meydana gelen ölümcül olmayan miyokardenfarktüsü, hospitalizasyon gerektiren belgelenmiş kararsız angina veya herhangi bir koronerrevaskülarizasyon prosedürü olarak tanımlanmıştır) ve ölümcül olmayan inmenin bileşimidir.Çalışma, simvastatine eklenen ezetimib tedavisinin kardiyovasküler ölüm, MKO ve ölümcülolmayan inmeyi içeren birincil birleşik son noktayı tek başına simvastatine göre azaltmadailave yarar sağladığını göstermiştir (relatif risk azaltımı %6,4, p=0,016). Birincil son noktaezetimib/simvastatin grubunda yer alan 9067 hastadan 2572'sinde (7 yıllık Kaplan-Meier[KM] oranı %32,72) ve tek başına simvastatin grubundaki 9077 hastadan 2742'sinde ortayaçıkmıştır (7 yıllık KM oranı %34,67) (bkz. Şekil 1 ve Tablo 1) Bu ilave yararın,kardiyovasküler olayların riskini azaltmada etkin oldukları gösterilmiş diğer statinlerin eşzamanlı uygulanmasıyla benzer olması beklenmektedir (bkz. Tablo 1). 13/20 Ezetimib/simvastatinin tedavi etkisi cinsiyet, yaş, ırk, tıbbi öyküde diabetes mellitus varlığı, başlangıçtaki lipid düzeyleri, önceki statin tedavisi, geçirilmiş inme veya hipertansiyonuiçeren pek çok alt grupta tüm sonuçlarla genellikle uyumlu bulunmuştur.
14/20 Tablo 2 Kardiyovasküler Olaylar
Kronik Böbrek Hastalığında (KBH) Majör Vasküler Olayların ÖnlenmesiKalp ve Böbrek Koruma (SHARP) çalışması kronik böbrek hastalığı olan 9438 hastada (üçtebiri başlangıçta diyaliz tedavisi almaktaydı) yürütülen çok-uluslu, randomize, plasebo-kontrollü, çift-kör bir çalışmadır. Toplam 4650 hasta EZETROL 10 mg ile simvastatin 20mg'nin sabit dozlu bir kombinasyonunu ve 4620 hasta plasebo almak üzere randomizeedilmiş ve medyan 4,9 yıl izlenmiştir. Hastaların ortalama yaşı 62'dir, %63'ü erkek, %72'sibeyaz ve %23'ü diyabetiktir. Diyalize girmeyen hastalarda hesaplanmış ortalama glomerülerfiltrasyon hızı (eGFR) 26,5 mL/dak/1,73 m2'dir. Lipidler için hiçbir giriş kriteri yoktu.Başlangıçta ortalama LDL-K 108 mg/dL'dir. Bir yıl sonra, çalışma ilacını artık almayan15/20 hastalar dahil olmak üzere, tek başına simvastatin ile LDL-K plaseboya göre %26 azalırken, EZETROL 10 mg ve simvastatin 20 mg kombinasyonuyla %38 oranında azalmıştır. SHARP protokolünde tanımlanan birincil karşılaştırma sadece başlangıçta EZETROL ile kombine simvastatin grubuna (n = 4193) veya plasebo (n = 4191) grubuna randomize edilenhastalarda "majör vasküler olayların" (MVO; ölümcül olmayan miyokard enfarktüsü veyakardiyak ölüm, inme ya da herhangi bir revaskülarizasyon prosedürü şeklinde tanımlanmıştır)tedavi amaçlı analizidir. İkincil analizler EZETROL ile simvastatin kombinasyonuna (n =4650) veya plaseboya (n = 4620) randomize edilen (çalışmanın başlangıcında veya 1.yılda)tüm kohort için analiz edilen aynı birleşik son noktayı ve ayrıca bu birleşik son noktanınbileşenlerini içermiştir. Birincil son nokta analizi EZETROL ile simvastatin kombinasyonunun majör vasküler olayların riskini (plasebo grubunda olayların görüldüğü 749 hastaya karşılık EZETROL ilekombine simvastatin grubunda 639 hasta) relatif riskte %16 azalmayla birlikte anlamlıdüzeyde azalttığını göstermiştir (p = 0,001). Bununla birlikte, bu çalışma KKH hastalarında majör vasküler olayların riskini anlamlı düzeyde azaltmadaki etkinliğe tek bir bileşenin (ezetimib) katkısını ayrı olarak incelemekamacıyla tasarlanmamıştır. Tüm randomize edilmiş hastalarda majör vasküler olayların her bir bileşeni Tablo 2'de sunulmaktadır. EZETROL ile simvastatin kombinasyonu inme ve herhangi birrevaskülarizasyonun riskini anlamlı düzeyde azaltmış ve ölümcül olmayan ME ve kardiyakölüm açısından EZETROL ile simvastatin kombinasyonu lehine anlamlı olmayan rakamsalfarklar gözlenmiştir. Tablo 3 SHARP'da randomize edilen tüm hastalarda Tedavi Grubuna göre Majör Vasküler Olaylar a
16/20 b MAO; ölümcül olmayan miyokard enfarktüsü, koroner ölüm, hemorajik olmayan inme veya herhangi revaskülarizasyoun bileşimi olarak tanımlanmıştır. EZETROL ve simvastatin kombinasyonuyla LDL kolesterolde sağlanan mutlak azalma başlangıçta LDL-K değeri düşük olan hastalarda (<2,5 mmol/L) ve başlangıçta diyaliztedavisi almakta olan hastalarda diğer hastalara göre daha düşüktür ve bu iki grupta karşılıkgelen risk azaltımları zayıflamıştır. Homozigot Ailesel Hiperkolesterolemi (HoFH)Çift-kör, randomize, 12 haftalık bir çalışma klinik ve/veya genotipik HoFH tanısı koyulmuş, eş zamanlı LDL afereziyle birlikte veya aferez olmaksızın atorvastatin veya simvastatin (40mg) alan 50 hastayı incelemiştir. Atorvastatin (40 veya 80 mg) veya simvastatin (40 veya 80mg) ile birlikte uygulanan EZETROL LDL-K'yı simvastatin veya atorvastatin monoterapidozunun 40 mg'den 80 mg'ye yükseltilmesine göre %15 oranında anlamlı olarakdüşürmüştür. Homozigot Sitosterolemi (Fitosterolemi)Çift-kör, plasebo-kontrollü, 8 haftalık bir çalışmada homozigot sitosterolemili 37 hasta EZETROL 10 mg (n = 30) veya plasebo (n = 7) almak üzere randomize edilmiştir. Bazıhastalar başka tedaviler alıyorlardı (örn. statinler, reçineler). EZETROL iki önemli bitkisterolünü (sitosterol ve kampesterol) başlangıca göre sırasıyla % 21 ve % 24 oranındaazaltmıştır. Bu popülasyonda sitosterol düşürümünün morbidite ve mortalite üzerindekietkileri bilinmemektedir. Aort StenozuAort Stenozunda Simvastatin ve Ezetimib (SEAS) çalışması, Doppler ile ölçülen 2,5 - 4,0 m/s aralığında aort pik akış hızıyla belgelenen asemptomatik aort stenozu (AS) olan 1873 hastadaortalama 4,4 yıl yürütülen çok-merkezli, çift-kör, plasebo-kontrollü bir çalışmadır. Çalışmayasadece, statin tedavisinin aterosklerotik kardiyovasküler hastalık riskini azaltmak amacıylagerekli olduğu düşünülmeyen hastalar dahil edilmiştir. Hastalar plasebo veya ezetimib 10 mgile birlikte uygulanan simvastatin 40 mg/gün tedavisi almak üzere randomize edilmiştir. Birincil son nokta kardiyovasküler ölüm, aort kapağı değiştirme (AVR) cerrahisi, AS'nin ilerlemesine bağlı konjestif kalp yetmezliği (KKY), ölümcül olmayan miyokard enfarktüsü,koroner arter bypass graftı (CABG), perkutan koroner girişim (PCI), kararsız anginanedeniyle hospitalizasyon ve hemorajik olmayan inmeyi içeren majör kardiyovaskülerolayların bir bileşimidir. Önemli ikincil son noktalar, birincil son nokta olay kategorilerininalt kümelerinin bileşimleridir. Plaseboya kıyasla, ezetimib/simvastatin 10/40 mg majör kardiyovasküler olayların riskini anlamlı olarak azaltmamıştır. Birincil sonuç ezetimib / simvastatin grubunda 333 hastada(%35,3) ve plasebo grubunda 355 hastada (%28,3) görülmüştür (ezetimib / simvastatingrubunda risk oranı (HR), 0,96; %95 güven aralığı, 0,83 - 1,12; p = 0,59). Aort kapağıdeğişimi ezetimib / simvastatin grubunda 267 hastada (%28,3) ve plasebo grubunda 278hastada (%29,9) yapılmıştır (tehlike oranı, 1,00; %95 GA, 0,84 - 1,18; p = 0,97). Ezetimib /simvastatin grubunda iskemik kardiyovasküler olaylar (n=148) plasebo grubuna kıyasla (n =187) daha az hastada görülmüştür (tehlike oranı, 0,78; %95 GA, 0,63 - 0,97; p = 0,02); bununana nedeni, koroner arter bypass graftı yapılan hasta sayısının daha az olmasıdır. Ezetimib / simvastatin grubunda kanser daha sıklıkla görülmüştür (105'e karşı 70, p=0,01). Daha büyük SHARP çalışmasında herhangi bir kanser vakası olan toplam hasta sayısı (438 17/20 ezetimib/simvastatine göre 439 plasebo grup) farklı olmadığı için bu gözlemin klinik önemi bilinmemektedir. Ek olarak, IMPROVE-IT çalışmasında herhangi bir yeni malignitesi olan(853 ezetimib/simvastatin gruba göre 863 simvastatin grup) toplam hasta sayısı anlamlı olarakfarklılık yaratmamaktadır ve bu yüzden SEAS çalışmasının bulguları SHARP ya daIMPROVE-IT tarafından konfirme edilememiştir. 5.2. Farmakokinetik özelliklerEmilim:Oral uygulamadan sonra ezetimib hızla emilir ve farmakolojik yönden aktif bir fenolik glukuronata (ezetimib-glukuronat) kapsamlı biçimde konjuge olur. Ortalama pik plazmakonsantrasyonlarına (Cmaks) ezetimib ile 4-12 saatte ve ezetimib-glukuronat ile 1-2 saatteulaşılır. Ezetimibin mutlak biyoyararlanımı belirlenemez, çünkü bileşik enjeksiyon için uygunolan sulu ortamda neredeyse hiç çözünmemektedir. Ezetimib EZETROL 10 mg tabletler şeklinde uygulandığında eş zamanlı gıda alımı (yüksek oranda yağ içeren veya yağ içermeyen öğünler) ezetimibin emilim derecesini etkilememiştir.EZETROL gıdalarla birlikte veya ayrı alınabilir. Dağılım:Ezetimib ve ezetimib-glukuronat insan plazma proteinlerine sırasıyla %99,7 ve %88-92 oranında bağlanır. Biyotransformasyon:Ezetimib, ince barsakta ve karaciğerde glukuronik asit konjugasyonu (faz II reaksiyonu) ile metabolize olur; daha sonra safrayla atılır. İncelenen tüm türlerde minimal oksidatifmetabolizma (faz I reaksiyon) gözlemlenmiştir. Ezetimib ve ezetimib-glukuronat plazmadatotal ilacın sırayla %10 ila %20'si ve %80 ila %90'ını teşkil eder. Eliminasyon:Hem ezetimib hem de ezetimib-glukuronat anlamlı enterohepatik geridolaşım kanıtıyla plazmadan elimine edilirler. Ezetimib ve ezetimib- glukuronatın yarılanma ömrü 22 saattir. İnsan deneklere 14C-ezetimibin (20 mg) oral uygulanmasından sonra, total ezetimib plazmadaki toplam radyoaktivitenin yaklaşık %93'ünü oluşturmuştur. 10 günlük bir toplama periyodunun ardından, uygulanan radyoaktivitenin yaklaşık %78 ve %11'i, sırasıyla üre ve feçesten geri kazanılmıştır. 48 saat sonra plazmada radyoaktiviteölçülemeyecek düzeylerde bulunmuştur. Hastalardaki karakteristik özelliklerPediyatrik hastalar:6 yaşındaki ve daha büyük çocuklarda ezetimibin farmakokinetiği erişkinlerle benzerdir. 6 yaşından küçük pediyatrik popülasyonda farmakokinetik veri mevcut değildir. Pediyatrik veadolesan hastalarda klinik deneyim HoFH, HeFH ve sitosterolemili hastaları içerir. Geriyatrik hastalar:Total ezetimibin plazma konsantrasyonları yaşlı kişilerde (>65 yaş) genç kişilere (18- 45 yaş arası) göre yaklaşık 2 kat daha yüksektir. EZETROL ile tedavi edilen yaşlı ve gençgönüllülerde LDL-K düşürümü ve güvenlilik profili benzerdir. Dolayısıyla yaşlılarda dozayarlamasına gerek yoktur. 18/20 Karaciğer yetmezliği:Ezetimibin tekli 10 mg dozundan sonra, total ezetimibin eğri altında kalan ortalama alanı (EAA) hafif karaciğer yetmezliği olan hastalarda (Child-Pugh skoru 5 ila 6) sağlıklı bireyleregöre yaklaşık 1,7 kat artmıştır. Orta derecede karaciğer yetmezliği olan hastalarda(Child-Pugh skoru 7 ila 9) 14 gün süren bir çoklu-doz çalışmasında (günde 10 mg) totalezetimibin ortalama EAA değeri 1. günde ve 14. günde sağlıklı bireylere göre yaklaşık 4 katartmıştır. Orta derecede veya şiddetli (Child-Pugh skoru > 9) karaciğer yetmezliği olanhastalarda artmış ezetimib maruziyetinin etkileri bilinmediğinden, ezetimib bu hastalaraönerilmez (bkz. bölüm 4.4). Böbrek yetmezliği:Şiddetli böbrek yetmezliği olan hastalarda (n=8; ortalama kreatin klerensi < 30 mL/dak/1,73 m2) 10 mg lık tekli dozu sonrasında eğrinin altında kalan alanın (EAA) sağlıklı bireylere(n=9) oranla yaklaşık 1,5 kat arttığı görülmüştür. Bu sonuç klinik olarak anlamlı olmadığıiçin, böbrek yetersizliği olan hastalarda doz ayarlamasına gerek yoktur. Bu çalışmadaki başkabir hastada (böbrek transplantasyonu yapılmış, siklosporin dahil pek çok ilaç alan) totalezetimibe maruz kalım 12 kat daha yüksektir. Cinsiyet:Total ezetimibin plazma konsantrasyonları erkeklere göre kadınlarda biraz daha yüksektir (yaklaşık %20). EZETROL ile tedavi edilen erkekler ve kadınlarda LDL-K azaltımı vegüvenlilik profili benzerdir. Dolayısıyla cinsiyete göre doz ayarlaması gerekmez. 5.3. Klinik öncesi güvenlilik verileriEzetimibin kronik toksisitesini inceleyen hayvan çalışmaları toksik etkiler için hiçbir hedef organ ortaya koymamıştır. Dört hafta süreyle ezetimib (> 0,03 mg/kg/gün) ile tedavi edilenköpeklerde sistik kanaldaki kolesterol konsantrasyonu 2,5 - 3,5 kat yükselmiştir. Ancak günde300 mg/kg'a kadar dozların verildiği köpeklerle yapılan bir 1 yıllık çalışmada kolelitiyazisveya diğer hepatobiliyer etkilerin insidansında artış gözlenmemiştir. Bu verilerin insanlardakianlamı bilinmemektedir. EZETROL'ün terapötik kullanımıyla ilişkili litojenik (taş oluşumu)risk dışlanamaz. Ezetimib ve statinlerin kombine uygulandığı çalışmalarda gözlenen toksik etkiler statinler ile tipik olarak gözlenen etkilerdi. Toksik etkilerin bazıları tek başına statinlerle tedavi sırasındagözlenenlerden daha çarpıcıydı. Bu durum kombine tedavide farmakokinetik vefarmakodinamik etkileşimlere bağlanmaktadır. Bu tip etkileşimler klinik çalışmalarda ortayaçıkmamıştır. Miyopatiler sıçanlarda yalnızca insanlardaki terapötik dozun birkaç katüzerindeki dozlara (statinlerin EAA düzeyinin yaklaşık 20 katı ve aktif metabolitlerin EAAdüzeyinin 500-2000 katı) maruz kalımdan sonra gözlenmiştir. Bir dizi in vivoin vitroçalışmada, tek başına veya statinler ile birlikte uygulanan ezetimib genotoksik potansiyel sergilememiştir. Ezetimib ile yapılan uzun süreli karsinojenite testlerinegatiftir.Ezetimibin dişi veya erkek sıçanların üreme yeteneği üzerinde hiçbir etkisi bulunmamıştır; ayrıca ezetimib sıçanlarda veya tavşanlarda teratojenik değildir ve doğum öncesi ve sonrasıgelişimi etkilememiştir. Ezetimib günde 1000 mg/kg çoklu dozların verildiği gebe sıçanlardave tavşanlarda plasenta bariyerinden geçmiştir. Sıçanlarda ezetimib ve statinlerin birlikteuygulanması teratojenik değildir. Gebe tavşanlarda az sayıda iskelet deformitesi (toraks ve 19/20 kaudal omurlarda füzyon, kaudal omurların sayısında azalma) gözlenmiştir. Ezetimib ile lovastatinin birlikte uygulanması embriyo üzerinde ölümcül etkilere yol açmıştır. 6. FARMASÖTİK ÖZELLİKLER6.1. Yardımcı maddelerin listesiKroskarmeloz sodyum Laktoz monohidrat (ineklerden elde edilir) Magnezyum stearat Mikrokristalin selülozPovidon Sodyum laurilsülfat 6.2. GeçimsizliklerYeterli veri yoktur. 6.3. Raf ömrü36 ay 6.4. Saklamaya yönelik özel uyarılar25oC'nin altındaki oda sıcaklığında, çocukların göremeyeceği ve erişemeyeceği yerlerde ve ambalajında saklayınız. Blisterleri nemden korumak için orijinal ambalajında saklayınız. 6.5. Ambalajın niteliği ve içeriğiKutuda 28 tabletlik Poliklorotrifloroetilen/Al/PVC blister ambalajlarda. 6.6. Beşeri tıbbi üründen arta kalan maddelerin imhası ve diğer özel önlemlerKullanılmamış olan ürünler ya da atık materyaller Tıbbi Atıkların Kontrolü Yönetmeliği ve Ambalaj ve Ambalaj Atıkları Kontrolü Yönetmeliği'ne uygun olarak imha edilmelidir. 7. RUHSAT SAHİBİOrganon Turkey İlaçları Ltd. Şti. Esentepe Mah. Büyükdere Cad. Kanyon Blok No: 185 İç Kapı No: 271 Şişli - İstanbulTelefon : (212) 268 20 68Faks : (212) 319 76 00 8. RUHSAT NUMARASI2022/168 9. İLK RUHSAT TARİHİ / RUHSAT YENİLEME TARİHİİlk ruhsat tarihi: 30.03.2022 Ruhsat yenileme tarihi: 10. KÜB'ÜN YENİLENME TARİHİ20/20 |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
Ana Sayfa | Hakkımızda | İlaçlar | İlaç Ara | İlaç Firmaları | Gizlilik | Bize Ulaşın
Telif Hakkı 2008-2026 © İlaç Prospektüsü. Tüm Hakları Saklıdır.Uyarı: Sitemizde yayınladığımız ilaç bilgileri ile doktora danışmadan kesinlikle ilaç kullanmayınız!
Aksi halde doğabilecek sağlık sorunlarından ilacprospektusu.com sorumlu tutulamaz.