Humalog 100 IU/ml solüsyon içeren flakon Kısa Ürün BilgisiSindirim Sistemi ve Metabolizma » Diyabet (Şeker Hastalığı) İlaçları » İnsülinler ve Analogları » Insulins and analogues for injection, intermediate-acting » İnsülin Lispro KISA ÜRÜN BİLGİSİ1. BEŞERİ TIBBİ ÜRÜNÜN ADIHUMALOG 100 lU/ml 10 mİ solüsyon içeren flakon2. KALİTATİF VE KANTİTATİF BİLEŞİM Etkin madde:Her 1 ml'de, 100 ünite (3.5 mg' a eşdeğer) rekombinant DNA orijinli, E. coli'de üretilmiş insülin lispro içerir. Her flakonda 1000 ünite insülin lisproya eşdeğer 10 mİ çözelti bulunur.Yardımcı maddeler:Herml'de 3.15 mg metakrezol bulunur.Yardımcı maddeler için 6.1'e bakmız. 3. FARMASÖTİK FORMEnjeksiyonluk çözelti.HUMALOG, steril, berrak, renksiz stv( bir çözeltidir. 4. KLİNİK ÖZELLİKLER4.1 Terapötik endikasyonlarHUMALOG, normal glukoz homeostazmm korunması için insüline gereksinim duyan diabetes mellituslu hastaların tedavisinde endikedir. HUMALOG ayrıca, diabetes mellitusun başlangıç stabilizasyonu için de endikedir.4.2 Pozoloji ve uygulama şekli Pozoloji:Doz, hastanın gereksinimine göre doktor tarafından belirlenmelidir.Uygulama sıklığı ve süresi:HUMALOG yemeklerden 15 dakika önce uygulanabilir. Gerek duyulduğunda HUMALOG yemeklerden hemen sonra da uygulanabilir.Uygulama şekli:HUMALOG subkütan enjeksiyon şeklinde ya da sürekli subkütan infüzyon pompası ile uygulanmalıdır; tavsiye edilmemesine rağmen intramüsküler enjeksiyon da uygulanabilir. HUMALOG gerektiğinde (ketoasidozda kan glukoz seviyesinin kontrolü, akut hastalıkta, cerrahi operasyon sırasında ve sonrasında kullanım örnek gösterilebilir) intravenöz olarak da uygulanabilir.Subkütan uygulama kolun üst kısmı, uyluk, kalça ya da karma yapılmalıdır. Enjeksiyon yapılan bölgeler değiştirilerek aynı bölgenin ayda bir seferden fazla kullanılmaması sağlanmalıdır. HUMALOG, subkütan uygulandığı sırada bir kan damarına girilmediğinden emin olunmalıdır. Uygulamadan sonra, enjeksiyon bölgesine masaj yapılmamalıdır. Hastalar uygun enjeksiyon tekniğinin kullanılması konusunda eğitilmelidir. HUMALOG etkisini çabuk gösterir ve subkütan uygulamada regüler insüline kıyasla daha kısa bir etki süresine sahiptir (2 ila 5 saat). Etkinin hızlı başlaması, HUMALOG enjeksiyonunun (ya da sürekli subkütan infüzyon şeklindeki uygulamalarda HUMALOG bolus) Öğünlere çok yakın bir zamanda yapılmasına olanak verir. Herhangi bir insülinin etki süresi kişiden kişiye ya da aynı kişilerde farklı zamanlardaki uygulamalarda değişkenlik gösterebilir. Regüler insan insülinine kıyasla etkinin hızlı oluşması enjeksiyon bölgesinden bağımsızdır. Tüm insülin preparatlarında olduğu gibi HUMALOG'un etki süresi doz, enjeksiyon yeri, kanlanma, vücut sıcaklığı ve fiziksel aktiviteye bağlıdır. Doktor tarafmdan önerilmişse, HUMALOG daha uzun etkili insan insülinleri ile ya da oral sülfonilüre bileşikleri ile birlikte kullanılabilir. HUMALOG'un insülin infüzvon pompasıyla kullanımı:Yalnızca belirli CE-işaretli insülin infuzyon pompaları insülin lispro infuzyonunda kullanılabilir. İnsülin lisproyu infuze etmeden önce, uygunluğun belirlenmesi için üreticinin talimatları ya da özel pompa üzerinde çalışılmalıdır. Hastalar HUMALOG'u insülin infuzyon pompası ile birlikte kullanmadan önce insülin infüzyon pompası ile birlikte verilen talimatları ve HUMALOG'un Kullanma Talimatlarım dikkatlice okuyup uygulamalıdır ve yoğunlaştırılmış insülin tedavisi ve infüzyon pompası ve pompa aksesuarlarının fonksiyonları hakkında eğitilmelidir. Doktorlar, HUMALOG Kısa Ürün Bilgilerinde yer alan HUMALOG'un insülin infuzyon pompasıyla kullanımı bölümünü ve insülin infüzyon pompası İle birlikte verilen talimatları dikkatlice değerlendirmelidir. Pompa içİn doğru hazne ve katater kullanınız. İnfüzyon seti 48 saatte bir değiştirilmelidir. İnfuzyon seti yerleştirilirken aseptik teknik uygulanmalıdır. Açıklanamayan hipoglisemi atağı veya ketozis meydana gelirse, hızla fark edilmeli ve atak çözümleninceye kadar infüzyon durdurulmalıdır. Subkütan insülin enjeksiyonu ile ara tedavi gerekebilir. Eğer tekrarlanırsa ya da kan şekeri düzeyinizde ciddi düşüş olursa, doktorunuzu bilgilendirip insülin infüzyonunu azaltma veya durdurma gerekliliği değerlendirilmelidir. Pompadaki bozukluk veya infüzyon setindeki tıkanma glukoz seviyesinde hızlı artışa neden olabilir. İnsülin akışının kesilmesinden şüphelenilirse, ürüne aİt talimatları takİp edip; doktorunuzu bilgilendiriniz. İnsülin infüzyon pompası ile beraber kullanıldığında HUMALOG, seyreltilmemeli veya diğer insülinlerle karıştırılmamalıdır. HUMALOG, infuzyon pompası ile kullanıldığında 37°C'nin üzerindeki sıcaklıklara maruz bırakılmamalıdır. İnsülin infüzyon pompasıyla HUMALOG flakonlar 7 güne kadar kullanılabilir. İnsülinin İntravenöz uygulanımı:İnsülin lispronun intravenöz enjeksiyonu, intravenöz bolus ya da infüzyon sisteminde olduğu gibi intravenöz enjeksiyonlar için klinik uygulamalara göre yapılmalıdır. Kan şeker düzeyinin sık aralarla gözlenmesi gereklidir. İnsülin lispronun, %0.9 sodyum klorür ve %5 dekstroz içinde 0.1 U/ml ile 1.0 U/ml konsantrasyonlarındaki infuzyon sistemleri oda sıcaklığında 48 saat stabildir. Hastaya infiizyon uygulanımına başlamadan önce sistemin havasının alınması tavsiye edilir. Kullanım ile ilgili talimatlarFlakon uygun bir enjektör (100 ünite işaretli) ile kullanılmalıdır. A) Dozun hazırlanması:HUMALOG çözeltisini inceleyiniz. Berrak ve renksiz olması gerekmektedir. Eğer içeriği bulanık, koyulaşmış veya hafifçe renklenmiş görünüyorsa, ya da görülebilen katı parçacıklar varsa HUMALOG'u kuilanmaymız. i) HUMALOG 1. Ellerinizi yıkayınız. 2. Yeni bir flakon kullanılıyorsa, plastik koruyucu kapağı çıkartınız, ancak tıpayı çıkarmayınız,3. Eğer tedavi bazal insülin ve HUMALOG'un birlikte kulamimasım gerektiriyorsa her ikisi bir enjektörde karıştınlabilir. Eğer insülinler karıştınlacaksa, bölüm (ii) ve 6.2 de belirtilen şekilde karıştırmayı yapınız.4. Enjektörün içine, kullanacağınız HUMALOG dozuna eşit miktarda hava çekiniz. Flakonun üstünü alkollü pamukla siliniz. İğneyi HUMALOG flakonunun üstündeki lastik tıpaya batırınız ve havayı flakonun İçine enjekte ediniz. 5. Flakon ve enjektörü baş aşağı çeviriniz. Her ikisini de bir elinizle sıkıca tutunuz. 6. İğne ucunun HUMALOG flakonun içinde bulunduğundan emİn olarak, doğru miktarda dozu enjektöre çekiniz. 7. Kabarcık oluşumu çekilen HUMALOG miktarını azaltacağından İğneyi flakondan çıkarmadan önce, enjektörün içinde hava kabarcığı olup olmadığına bakınız. Kabarcık varsa, enjektörü dik tutunuz ve kabarcıklar üste çıkana kadar yan tarafına vurunuz. Enjektörün pistonunu iterek kabarcıkları dışarı çıkartınız ve doğru miktarda dozu enjektöre çekiniz. 8. İğneyi flakondan çıkartınız ve enjektörü bırakırken, iğnenin hiçbir yerle temas etmemesine dikkat ediniz, ii) HUMALOG'un daha uzun etkili insan insülinleri ile karıştırılması (bkz. bölüm 6.2^1. HUMALOG'u uzun etkili insan insülinleri ile ancak doktorunuzun önerdiği durumlarda karıştırınız. 2. Enjektörünüze, kullanacağınız uzun etkili insülin miktarına eşit miktarda hava çekiniz, İğneyi uzun etkili insülin flakonuna sokup havayı enjekte ediniz. İğneyi çekiniz. 3. Aynj şekilde HUMALOG flakonuna hava enjekte ediniz, ancak iğneyi çıkarmayınız. 4. Flakon ve enjektörü baş aşağı çeviriniz. 5. İğne ucunun HUMALOG flakonun içinde bulunduğundan emin olunuz. Doğru miktarda dozu enjektörün içine çekiniz. 6. Kabarcık oluşumu çekilen HUMALOG miktarını azaltacağından iğneyi flakondan çıkarmadan önce, enjektörün içinde hava kabarcığı olup olmadığına bakmız. Kabarcık varsa, enjektörü dik tutunuz ve kabarcıklar üste çıkana kadar yan tarafına vurunuz. Enjektörün pistonunu iterek kabarcıkları dışarı çıkartınız ve doğru miktarda dozu enjektöre çekiniz. 7. İğneyi HUMALOG flakonundan çıkartmtz ve daha uzun etkili insülin flakonuna sokunuz. Flakon ve enjektörü baş aşağı çeviriniz. Her ikisini tek elinizle sıkıca tutunuz ve hafifçe çalkalayınız. İğne ucunun insülin içerisinde bulunduğundan emin olarak, uzun etkili insülini enjektöre çekiniz. 8. İğneyi çıkartınız ve enjektörü bırakırken iğnenin hiçbir yerle temas etmemesine dikkat ediniz. B) Dozun enjeksiyonu 1. Enjeksiyon bölgesini seçiniz. 2. Enjeksiyon yapılacak bölgeyi uygun şekilde temizleyiniz. 3. Geniş bir alanı gererek ya da sıkıştırarak cildi sabitleştiriniz. İğneyi tarif edildiği şekilde batırınız. 4. Enjektör pistonunu sonuna kadar itiniz. İğneyi enjeksiyon yerinden çıkartınız ve enjeksiyon bölgesine birkaç saniye hafifçe basınç uygulayınız. Enjeksiyon bölgesini ovuşturmayınız. 5. Enjektör ve iğneyi emniyetli bir biçimde atınız. 6. Enjeksiyon yapılan bölgeler değiştirilerek aynı bölgenin ayda bir seferden fazla kullanılmaması sağlanmalıdır. C) İnsülinlerin karıştırılması Flakonlardaki insülinleri kartuşlardaki insülinlerle karıştırmayınız. Zirve etkisinde değişiklik olabileceğinden, insülinler karıştırılırken dikkatli olunmalıdır. Amerikan Diyabet Demeği'nin insülin uygulanımı konusundaki raporunda İnsülinler karıştırıldığında, karışımda fizikokimyasal değişimler olabilir (derhal veya zamanla). Sonuç olarak, insülİn karışımına karşı fizyolojik yanıt, ayrıca yapılan insülin enjeksiyonundan farklı olabilir. uyarısmda bulunmaktadır. HUMALOG'un Humulin N ile karıştırılması, HUMALOG'un absorpsiyon oranını veya toplam biyoyararlanımını azaltmaz. Tek başına veya Humulln N ile karıştırılarak verildiğinde HUMALOG, Humulin R'ye göre daha hızlı absorpsiyon ve glukoz düşürücü etkiye sahiptir. HUMALOG'un diğer üreticilerin ürettiği insüünlerle veya hayvan kökenli insülin preparatlarıyla karıştırılması hakkında herhangi bir çalışma yapılmamıştır (Bkz. bölüm 6.2). HUMALOG, Humulin N gibi daha uzun etkili bir insüiin ile karıştırıldığında uzun etkili insülinin HUMALOG ile bulanıklık oluşturmasını engellemek için enjektöre önce HUMALOG çekilmelidir. Enjeksiyon, karıştırma işleminden hemen sonra yapılmalıdır. Karışımlar intravenöz olarak uygulanmamalıdır. İnsülin inflizyon pompası ile beraber kullanıldığında HUMALOG, diğer insülinlerle kan şttrı İmamal ıd ır. Özel popülasyonlara ilişkin ek bilgilerBöbrek/Karaciğer yetmezliğiBöbrek yetmezliğinde insülin gereksinimi azalabilir.Karaciğer yetmezliği durumunda glukoneojenez kapasitesinin ve insülin yıkımmm azalmasına bağlı olarak insülin gereksinimi azalabilir. Bununla beraber, kronik karaciğer yetmezliği olan hastalarda insülin rezistansındaki artış, insülin gereksiniminin artmasına neden olabilir. Böbrek ve karaciğer işlev bozukluğu olan hastalarda glukoz düzeylerinin izlenmesi ve insülin dozunda ayarlama gerekebilir. Pediyatrik popülasyon:HUMALOG çocuklarda yalnızca hızlı etkili İnsülinin etkisi daha yararlı olacaksa regüler insüline tercih edilebilir (örneğin; enjeksiyon zamanlarının öğünlerle ilişkili olarak belirlenmesi gibi).Geriyatrik popülasyon:HUMALOG yaşlılarda kullanım için uygundur.4.3 Kontrendikasyonlarİnsülin lispro veya yardımcı maddelerden herhangi birine karşı aşın duyarlılık.Hipoglisemi sırasında. 4.4 Özel kullanım uyarılan ve önlemleri UyarılarBu insan insülin analogu regüler insan insülininden hızlı etki başlangıcı ve aktivitenin kısa olması açısından farklılık gösterir. Yemeklerle ilişkili olarak kullanıldığında, HUMALOG öğünlerden 15 dakika önce ve yemeklerden hemen sonra yapılmalıdır. HUMALOG'un kısa etki süresi nedeniyle, tip 1 diyabetli hastalar glukoz kontrolünü sağlamak için uzun etkili insüline de ihtiyaç duyarlar (dışarıdan insülin pompası kullanımı haricinde).HUMALOG da dahil olmak üzere insülinlerle ilgili görülen en yaygın advers etki hipoglisemidir. Tüm insülinlerie olduğu gibi, hipogliseminin zamanlaması değişik insülin formülasyonlarında farklılıklar gösterir. Diyabetli hastalarda glukoz monitorizasyonu tavsiye edilir.İnsülinde yapılan herhangi bir değişiklik dikkatle ve medikal gözlem altında yapılmalıdır.Doz, marka (üretici), tip (regüler, NPH, lente v.s.), tür (hayvan, insan, insan insülin analoğu) ve/veya üretim yöntemindeki (rekombinant DNA teknolojisiyle üretilen insüline karşı hayvan kökenli insülin) farklılıklar doz ayarlanmasını gerektirebilir.ÖnlemlerGenelHastalar, insülin ve diğer alternatif tedavilerin potansiyel riskleri hakkında bilgilendirilmelidir. Hastalar ayrıca, insülinin uygun saklama koşulları, enjeksiyon teknikleri, uygulama süresi, öğün planlamasına eklenmesi, düzenli fiziksel aktivite, düzenli kan glukoz seviyesi monitorizasyonu, periyodik hemoglobin A|c testi, hipoglisemi ve hipergliseminin fark edilmesi ve yönetilmesi ve diyabet komplikasyonlarının periyodik değerlendirilmesi konusunda da bilgilendirilmelidir. Tüm insülinlerin kullanımı ile ilişkili olarak görülen potansiyel klinik advers etkiler hipoglisemi ve hipokalemidir. Tedavi edilmeyen hipokalemi solunum felci, ventriküler aritmi ve ölüme neden olabilir. HUMALOG ve diğer insülinlerin etkİ farklılığı nedeniyle klinik olarak, ilgili potansiyel yan etkiler görülen hastalarda (örneğin oruç tutan, otonomik nöropatisi olan veya potasyum düşürücü ilaçlar kullanan ya da serum potasyum düzeylerine hassasiyet gösteren ilaç olan hastalar) dikkat edilmelidir. Lipodistrofı ve aşırı hassasiyet tüm insülinlerin kullanımı ile oluşan diğer potansiyel klinik advers etkilerdir. Tüm insülin preparatlarında olduğu gibi, HUMALOG'un etki süresi değişik bireylerde ya da aynı kişide değişik zamanlarda farklılıklar gösterir ve enjeksiyon bölgesi, kan desteği, sıcaklık ve fiziksel aktiviteye bağlıdır. Hasta fiziksel aktivİtesİni veya her zamanki yemek planını değiştirdiğinde hangi insülin olursa olsun doz ayarlaması yapılması gerekebilir. Hastalık, duygusal rahatsızlık veya stres sırasında insülin gereksinimleri değişebilir. Hipoglisemi Diğer insülin preparatlarında olduğu gibİ, hipoglisemİk reaksiyonlar HUMALOG uygulamasıyla ilişkili olabilir. Serum glukoz konsantrasyonlarındaki hızlı değişim diyabetli hastalarda glukoz değerinden bağımsız olarak hipoglisemi semptomlarını uyarabilir. Uzun süreli diyabet, yoğun İnsülin tedavisi, diyabetik nöropati ya da beta blokörler gibi ilaçlar hipogliseminin erken uyarı semptomlarını daha farklı ya da daha az belirgin hale getirebilir. Alerji Lokal Alerji_ Tüm insülin tedavilerinde olduğu gibi, hastalarda enjeksiyon bölgesinde kızarıklık, şişkinlik veya kaşıntı olabilir. Bu minör reaksiyonlar birkaç gün ile birkaç haftada düzelir. Bazen, bu reaksiyonlar cilt temizleme malzemeleri içindeki iritanlar veya uygun olmayan enjeksiyon teknikleri gibi insülinden başka faktörlerle de ilişkili olabilir. Sistem i k Alerji_ Sık olmayan ancak potansiyel olarak daha ciddi olan insüiine genel alerji tüm vücutta döküntüye (kaşmtı dahil), nefes kesilmesine, tansiyon düşmesi, hızlı nabız, hırıltılı solunum veya terlemeye neden olabilir. Anafllaktik reaksiyonun dahil olduğu ciddi sistemik alerji vakaları hayatı tehdit edebilir. Kontrollü klinik çalışmalarda, kaşıntı (döküntü olan veya olmayan) Humulin R (N-2969) kullanan 17 hastada ve HUMALOG (N=2944)(p=0.053) kullanan 30 hastada görülmüştür. Krezolün enjeksiyonluk preparatlarda yardımcı madde olarak kullanılması sonucu iokalize reaksiyonlar ve yaygın kas ağrısı bildirilmiştir. Antikor oluşumu. Büyük klinik araştırmalarda, insan insülini ve insülin lispro ile çapraz reaksiyon gösteren antikorlar Humulin R ve HUMALOG tedavi gruplarında gözlenmiştir. Beklendiği gibi 12 aylık klinik çalışmalar sırasında antikor düzeylerindeki en büyük artış insülin tedavisine yeni başlayan hastalarda gözlenmiştir. Hastanın, başka bir insülin tipi veya markasına geçirilmesi kesinlikle tıbbi gözetim altında gerçekleştirilmelidir. Doz, marka (üretici), tip (regüler, NPH, lente v.s.), tür (hayvan, insan, insan insülin analoğu) ve/veya üretim yöntemindeki (rekombinant DNA teknolojisiyle üretilen insüiine karşı hayvan kökenli insülin) farklılıklar doz ayarlanmasını gerektirebilir. Hızlı etkili insülinler için, bazal insülin kullananlar da dahil tüm hastalarda tüm gün boyunca Özellikle noktürnal/açlık glukoz kontrolünü sağlamak için her iki insülinin dozu optimize edilmelidir, Flakonun uzun etkili insülinle kontaminasyonunun Önlenmesi için enjektöre ilk Önce kısa etkili HUMALOG'un çekilmesi gerekir. insülinlerin önceden veya enjeksiyondan hemen önce karıştırılması doktorun tavsiyesine göre yapılmalıdır. Bu tavsiye aynı şekilde sürdürülmelidir. Hayvan kökenli insülinden insan kökenli insüiine geçen birkaç hastada uyarıcı nitelikteki erken hipoglisemi semptomlarının derecesinin önceki insüiine göre azaldığı ya da değişikliğe uğradığı bildirilmiştir. Düzeltilmemiş hipoglisemi ya da hiperglisemi reaksiyonları, bilinç kaybı, koma ya da ölüme neden olabilir. Yetersiz dozların kullanılması ya da tedavinin kesilmesi, özellikle insüiine bağımlı diyabetlilerde ölümcül potansiyeli bulunan hiperglisemiye ve diyabetik ketoasidoza yol açabilir. Böbrek yetmezliğinde İnsülin gereksinimi azalabilir. Glukoneojenez kapasitesinde ve insülin yıkımında azalmaya bağlı karaciğer yetmezliği olan hastalarda İnsülin gereksinimi azalabilir, ancak kronik karaciğer yetmezliği olan hastalarda insülin direncindeki artış insülin gereksinimlerinde artışa yol açabilir. Hastalık ya da duygusal bozukluklarda İnsülin gereksiniminde artış olabilir. Fiziksel aktivitesinde artış olan ya da alıştıkları beslenme tarzını değiştiren hastalarda da doz ayarlaması gerekebilir. Öğünden hemen sonra yapılan egzersiz hipoglisemi riskini artırabilir. Hızlı etkili insülin analoglarınm farmakodinamik özelliklerine bağlı olarak eğer hipoglisemi oluşursa, regüler insülinle karşılaştırıldığında enjeksiyondan sonra daha erken oluşabilir. HUMALOG çocuklarda yalnızca hızlı etkili insülinin etkisi daha yararlı olacaksa regüler insüiine tercih edilebilir. Örneğin; enjeksiyon zamanlarının öğünlerle ilişkili olarak belirlenmesi gibi. HUMALOG'un pioglitazon ile kombine kullanımı: özellikle kalp yetmezliği gelişimi riskini taşıyan hastalarda, pioglitazon insülin ile kombine olarak kullanıldığmda kalp yetmezliği vakaları bildirilmiştir. Eğer HUMALOG ve pioglitazonun kombine kullanımı düşünülüyorsa, bu göz önünde bulundurulmalıdır. Kombine tedavi uygulandığında hastalar kalp yetmezliğinin belirtileri ve semptomları, kilo artışı ve ödem bakımından gözetilmelidir. Kardiyak semptomlarda bozulma olduğu takdirde pioglitazon kesilmelidir. Bu tıbbi ürün alerjik reaksiyonlara sebep olabilecek metakrezol maddesini içermektedir. 4.5 Diğer tıbbi ürünlerle etkileşimler ve diğer etkileşim şekilleriOral kontraseptifler, kortikosteroidler, izoniazid, niasin gibi lipid düşürücü ilaçlar, östrojen, fenotiyazinler veya tiroid replasman tedavisinde kullanılan bileşikler, danazol, beta: stimülanları (ritodrin, saibutamol, terbutalin) gibi hiperglisemik aktivite gösteren ilaçlar insülin gereksiniminde artışa yol açabilir.Oral hipoglisemik ajanlar, salisilatlar (örneğin asetilsalisiHk asit), sülfa grubu antibiyotikler, bazı antidepresanlar (monoamin oksidaz inhibitörleri, selektif serotonin geri alım inhibitörleri), bazı anjiyotensin dönüştürücü enzim inhibitörleri (kaptopril, enalapril), anjiyotensin 11 reseptör blokörleri, beta blokörler, oktreotid ya da alkol gİbi hipoglisemik aktivite gösteren bileşikler kullanıldığında insülin dozunun azahılması gerekebilir. Beta-adrenerjik blokör ilaçlar, bazı hastalarda hipogliseminin semptomlarını maskeleyebilir. HUMALOG ile birlikte başka İlaçlar kullanılırken doktora danışılmalıdır (Bkz. bölüm 4.4). Özel popülasyonlara ilişkin ek bilgilerHiçbir etkileşim çalışması yapılmamıştır,Pediyatrik popülasyon:Hiçbir etkileşim çalışması yapılmamıştır.4.6 Gebelik ve laktasyonGenel tavsiyeGebelik Kategorisi: BÇocuk doğurma potansiyeli bulunan kadınlar/Doğum kontrolü (Kontrasepsiyon)Çok sayıda gebelikte maruz kalma olgularına ilişkin veriler insülin lispronun gebelik üzerinde ya da fetusun/yeni doğan çocuğun sağlığı üzerinde advers etkileri olduğunu göstermemektedir. Bugüne kadar herhangi önemli bir epidemiyolojik veri elde edilmemiştir.Gebe kadınlara verilirken tedbirli olunmalıdır. Oral kontraseptiflerin kullanımı insülin gereksiniminde artışa yol açabilir (Bkz. Bölüm 4.5). Diyabetli hastalara, gebe kaldıklarında ya da kalmayı düşündüklerinde durumu doktorlarına bildirmeleri tavsiye edilmelidir. Gebelik dönemiTeratojenik etkiler - Gebe sıçanlar ve tavşanlar üzerinde sırasıyla 4 ve 0.3 keze kadar parenteral dozlarda (vücut yüzey alanına bağlı olarak ortalama insan dozu ortalama 40 ünite/gün) üreme çalışmaları yapılmıştır. Sonuçlar, HUMALOG'un fertilitede azalmaya veya fetüste zarara yol açtığına dair herhangi bir belirti göstermemiştir. Ancak, HUMALOG'un gebe kadınlarda yapılmış yeterli sayıda kontrollü çalışması mevcut değildir. Hayvanlar üzerinde yapılan üreme çalışmaları her zaman insan üzerindeki etkilerini tahmin edebilmek için yeterli olmadığından, HUMALOG gebe kadınlara sadece kesinlikle gereksinim duyulduğunda verilmelidir.HUMALOG'un gebelik sırasında kullanımına dair kısıtlı klinik çalışma olmasına rağmen, insan insülinleri ile yapılan yayınlanmış çalışmalar, gebelik öncesi ve gebelik sırasında postprandiyal kontrolü de içeren genel glisemik kontrolü optimize etmenin bebeğin gelişimi ile ilgili sonuçları geliştirdiğini göstermektedir. Her ne kadar maternal hiperglisemiye bağlı fetal komplikasyonlar iyi dokümante edilmişse de, maternal hipoglisemiye bağlı maternal toksisite de raporlanmıştır. Gebelik sırasında insülin lispro kullanan çok sayıda gebe kadına ait veriler, insülin lispronun gebelik üzerinde ya da fetus ya da yenidoğanın sağlığı üzerinde herhangi bir advers etkisi olmadığını göstermiştir. Gebelik sırasında insülin tedavisi gören hastada (İnsüline bağımlı diyabet ya da gestasyonel diyabet) diyabet kontrolü büyük önem taşır. Genellikle, insülin gereksiniminde ilk trimesterde azalma, ikinci ve üçüncü trimesterlerde artış gözlenir. Diyabetli hastalara, gebe kaldıklarında ya da kalmayı düşündüklerinde durumu doktorlarına bildirmeleri tavsiye edilmelidir. Diyabetli hastaların gebeliği sırasında glukoz düzeylerinin ve genel sağlık durumlarının dikkatle izlenmesi gerekir. Laktasyon dönemiİnsülin lispronun insan ya da hayvan sütü ile atılmasına ilişkin yetersiz/sınırlı bilgi mevcuttur. Emzirilen çocuk açısından bir risk olduğu göz ardı edilemez. Emzirmenin durdurulup durdurulmayacağına ya da HUMALOG tedavisinin durdurulup/durdurulmayacağma/ tedaviden kaçınılıp kaçınılmayacağına İlişkin karar verilirken, emzirmenin çocuk açısından faydası ve HUMALOG tedavisinin emziren anne açısından faydası dikkate alınmalıdır.Emziren diyabetli annelerin HUMALOG dozunda, beslenme tarzında ya da her ikisinde değişiklik yapılması gerekebilir. Üreme yeteneği (fertilite)Üreme yeteneği üzerinde bir etkisi bulunmamaktadır.4.7 Araç ve makine kullanımı üzerindeki etkilerHastanın konsantre olabilme ve reaksiyon gösterme yetileri, hipoglisemi nedeniyle azalabilir. Bu durum, söz konusu yetilerin özellikle önemli olduğu durumlarda (Örn; araç sürme ya da makine kullanma gibi) risk yaratabilir.Hastalar araç kullanımı sırasında hipoglisemiyi engelleyecek önlemler almaları konusunda uyarılmalıdır. Bu özellikle uyarıcı hipoglisemi belirtileri azalmış ya da bunların farkma varmayan ya da sık sık hipoglisemi atağı geçiren hastalarda önemlidir. Bu gibi durumlarda hasta araç kullanımı konusunda uyarılmalıdır. 4.8 İstenmeyen etkilerİnsülin tedavisi gören bir diyabet hastasında en yaygın görülen yan etki hipoglisemidir. Ciddi hipoglisemi bilinç kaybına ve ileri vakalarda da ölüme neden olabilir. Hipoglisemi hem insülin dozu hem de hastanın diyeti ve egzersizi gibi diğer faktörlerin sonucu olduğundan hipoglisemi için spesifik bir sıklık belirlenmemiştir.Sıklıklar aşağıdaki şekilde tanımlanır: Çok yaygın (> 1/10); yaygın (> I/IOO ila < 1/10);yaygın olmayan (> 1/1,000 ila <1/100); seyrek (> 1/10,000 ila <1/1,000); çok seyrek (< 1/10,000), bilinmiyor (eldeki verilerden hareketle tahmin edilemiyor).İmmün sistem bozukluklarıYaygın:Lokal alerji. İnsülin enjeksiyon bölgesinde kızarıklık, şişme ve kaşıntı görülebilir. Bu durum genellikle birkaç gün ile birkaç hafta arasında ortadan kaybolur. Bazen alerji, insülinden çok, deriyi temizlemekte kullanılan tahriş edici maddelere ya da uygun olmayan enjeksiyon tekniğine bağlı olabilir. Seyrek: Sistemik alerji (insüline karşı genel bir alerji durumudur). Sİstemik alerji tüm vücutta döküntülere, solunum güçlüğüne, hırıltılı solunuma, kan basıncında azalmaya, kalp ritminde artışa ya da terlemeye yol açabilir Ciddi sistemik alerji vakaları hayatı tehdit edici özellikte olabilir. Deri ve deri altı dokusu bozukluklarıYaygın olmayan:Enjeksiyon bölgesi reaksiyonları, lipodistrofı, kaşıntı, döküntü Özellikle zayıf metabolik kontrolün yoğunlaştırılmış insülin tedavisi ile iyileştirildiği durumlar olmak üzere insülin tedavisi sırasında ödem vakaları bildirilmiştir. 4.9 Doz aşımı ve tedavisiSerum glukoz konsantrasyonları; insülİn düzeyleri, kullanılabilir glukoz miktarı ve diğer metabolik süreçler arasındaki karmaşık etkileşimlerin bir sonucu olduğundan, insülinlerin spesifik bir doz aşımı tanımlaması yoktur. Hipoglisemi insülinin alınan besinlere ya da enerji harcamalarına göreceli olarak fazla gelmesinin bİr sonucu olarak ortaya çıkabilir. Ürün dozunda ve öğün planında düzenleme veya egzersiz gerekebilir.Hipoglisemi ile birlikte dikkatsizlik, konfüzyon, çarpıntı, baş ağrısı, terleme ve kusma olabilir. Hafif hipoglisemi atakları, glukoz, şeker ya da şekerli ürünlerin oral yolla alınmasma yanıt verebilir. Orta düzeyde hipoglisemi intramüsküler ya da subkütan glukagon uygulanması ve hasta yeterince iyileştikten sonra oral karbonhidrat verilmesi ile düzeltilebilir. Glukagona yanıt vermeyen hastalara, intravenöz glukoz çözeltisi uygulanmalıdır. Hasta komada ise, intramüsküler ya da subkütan glukagon uygulanmalıdır. Ancak, glukagon mevcut olmadığmda ya da hasta glukagona yanıt vermediğinde intravenöz glukoz çözeltisi uygulanmalıdır. Bilinç kaybı düzeldikten hemen sonra hastaya yemek yedirilmelidir. Belirgin klinik iyileşme olduktan sonra da hipoglisemi tekrarlayabileceğinden, sürekli karbonhidratlı gıda ahmı sağlanmalı ve hasta gözlem altında bulundurulmahdır. 5. FARMAKOLOJİK ÖZELLİKLER5.1 Farmakodinamik özelliklerFarmakoterapötik grubu: Hızh etkili insan insülin analoğu.ATC kodu: AlOA B04 Etki mekanizması: insülin lispronun asıl etkisi, glukoz metabolizmasının regülasyonudur. Buna ilaveten insülin çeşitli dokularda bir takım anabolik ve anti-katabolik etkilere sahiptir. Bu etkiler, kas dokusunda glikojen, yağ asitleri, gliserol ve protein sentezi ile amino asit aliminin artışı, glikojenoliz, glikoneojenez, ketojenez, lipoliz, protein katabolizması ve amino asit açığa çıkışının azalmasj biçiminde gerçekleşir. İnsülin lispronun hızlı bir etki başlangıcına sahip olması (yaklaşık 15 dakika), regüler insüline göre öğünlere daha yakın uygulanmasına olanak verir; regüler insülin, öğünlerden 30 ila 45 dakika önce, insülin lispro ise öğüne başlamadan hemen önce ya da 15 dakika öncesine kadar uygulanabilir. Regüler insülin ile karşılaştırıldığında, etkisi daha hızlı ve daha kısa sürelidir (2-5 saat). Tip 1 ve tip 2 diyabetli hastalarda yapılan klinik çalışmalar insülin lispro ile postprandiyal hipergliseminin regüler insüline göre daha iyi kontrol edildiğini göstermiştir. Tüm insülin preparatlarında olduğu gibi İnsülin lispronun etkisi kişiden kişiye değiştiği gibi, aynı kişide farklı zamanlarda da değişkenlik gösterir. Etki süresi doz, enjeksiyon bölgesi, kanlanma, sıcaklık ve fiziksel aktİviteye bağlıdır. Subkütan enjeksiyondan sonra tipik aktivite profili aşağıda gösterilmiştir. 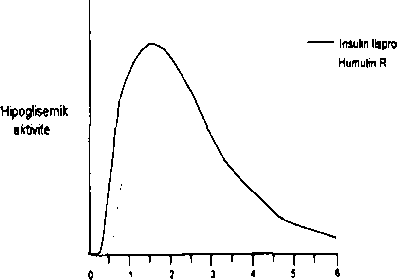 Zarran saat
Zarran saatYukarıdaki şekil, kişinin kan glukoz konsantrasyonlarını açlık kan şekerinin seviyesine yakın düzeylerde tutmak için gerekli glukoz miktarını yansıtmakta olup bu, insülinlerin zaman içinde glukoz metabolizması üzerindeki etkilerinin bir göstergesidir. Çocuklarda (2 ila 11 yaş arasındaki 61 hasta) ve çocuklar ile adolesanlarda (9 ila 19 yaş arasındaki 481 hasta) insülin lispro ile regüler insan insülinini karşılaştıran klinik çalışmalar yürütülmüştür. İnsülin lispronun çocuklardaki farmakodinamik profili yetişkinlerde gözlenen ile benzerdir. Subkütan inftizyon pompası ile kullanıldığında insülin lispro ile tedavinin, regüler insan insüiinine göre daha düşük bir glikozile hemoglobin düzeyi oluşturduğu görülmüştür. Bir çift kör, çapraz çalışmada 12 haftalık uygulama sonrasında glikozile hemoglobin düzeylerindeki düşme insülin lispro ile 0.37 yüzde puan ve regüler insülin için 0.03 yüzde puan olmuştur (p= 0,004). Çok yüksek dozlarda sülfonilüre alan tip 2 diyabetli hastalarda yapılan çalışmalar, sülfonilüre ile beraber insülin lispro kullanımının, tek başına sülfonilüre kullanımına göre, HbAic'yi belirgin oranda azalttığını göstermiştir. HbAic'deki bu azalma diğer insülin ürünleri (örn: regüler ve izofan insülin) ile de beklenir. Tip 1 ve tip 2 diyabetli hastalarda yapılan klinik çalışmalar, insülin lispro kullanan hastalarda regüler insüline göre gece hipoglisemisi epizodlarının azaldığını göstermiştir. Bazı çalışmalarda gece hipoglisemisindeki azalma gündüz hipoglisemisindeki artışla ilişkilidir. İnsülin lisproya gelen glukodinamİk cevap böbrek veya karaciğer fonksiyon bozukluğundan etkilenmez. Bir glukoz klamp çalışması sırasında insülin lİspro ile regüler insan insülini arasındaki glukodinamİk farklılıklar böbrek fonksiyonların derecesi farklı olan birçok hasta üzerinde ortaya konmuştur. İnsülin lispronun molar açıdan insan İnsülinİne eşdeğer olduğu belirlenmiştir ancak insülin lispro daha hızlı ve daha kısa süreli etkiye sahiptir. 5.2 Farmakokinetik özelliklerGenel ÖzelliklerEmilim:HUMALOG'un biyoyararlanımı regüler insan insülinİ İle aynı olup mutlak biyoyararlanımı, 0.1 ila 0.2 U/kg dozları arasında %55-%77 arasmdadır. Diyabetik olmayanlar ve tip I (insüline bağımlı) diyabetli hastalarda yapılan çalışmalarda HUMALOG'un regüler insan insülinininden (U-IOO) daha hızlı emildiği gösterilmiştir. Diyabetik olmayanlara 0.1-0.4 U/kg dozlarda subkütan olarak verilen Humalog ile doruk serum konsantrasyonu dozlama sonrası 30-90. dakikalarda gözlenmiştir. Diyabetik olmayanlar regüler insan insülini ile eşdeğer dozlar aldığında doruk serum konsantrasyonları dozlamadan 50-120. dakikalarda oluşmuştur. Benzer sonuçlar tip 1 diyabetli hastalarda görülmüştür. Diyabetik olmayanlara intravenöz yolla uygulandığında HUMALOG ve regüler insan insülininin farmakokinetik profilleri karşılaştırılabilir. Sağlıklı erkek gönüllülere 0.2 U/kg regüler insan insülini veya diyabetli hastalarca en çok kullanılan 3 bölge olan abdominal, deltoid veya femoral bölgelere subkütan yapıldığında HUMALOG regüler insan insülinine göre sürekli hızlı hızda emilir. HUMALOG'un abdominal uygulamasından sonra serum ilaç düzeyleri daha yüksek ve etki süresi deltoid ve kalçadan uygulama sonrası kısmen kısadır (bkz. Pozoloji ve uygulama şekli). HUMALOG regüler insan insülinine göre daha az hasta ve hastalar arası değişkenlik gösterir. 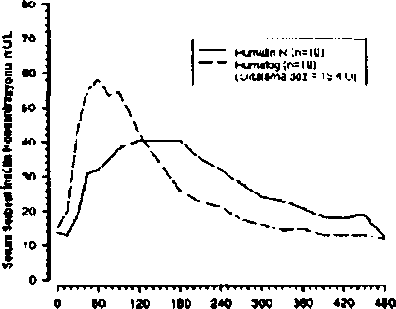
Regüler insan insülini veya HUMALOG'un tip 1 diyabetli 10 hastada yüksek karboohidratlt yemek öncesi yapılan subkiitan enjeksiyonu sonrası serum HUMALOG ve insülin düzeyleri** 0.2 mU/dak/kg insan insülin infüzyonu ile insülin konsantrasyonunun taban çizgisi sağlanmaktadır.Böbrek yetmezliği olan hastalarda, regüler İnsan insülini ile karşılaştırıldığında, insülin lispro daha hızlı emilir. Böbrek fonksiyonlannm derecesi farklı olan tip 2 diyabetli hastalarda insülin lispro ve regüler insan insülini arasındaki farmakokinetik farklılıkların böbrek fonksiyonundan bağımsız olduğu gösterilmiştir. Karaciğer yetmezliği olan hastalarda, regüler insan insülini ile karşılaştırıldığında, insülin lispro daha hızlı emilir ve atılır. Da&ılım:HUMALOG'un dağılım hacmİ insan regüler insülininki ile aynı olup 0.26 ila 0.36 L/kg aralığındadır. B i votransformasvon:İnsan metabolizma çalışmaları yürütülmemiştir. Ancak, hayvan çalışmaları HUMALOG metabolizmasının insan regüler insülininkiyle aynı olduğunu göstermektedir. Eliminasvon:Subkütan olarak verildiğinde HUMALOG'un yarılanma ömrü regüler insülİnİnkinden daha kısadır (sırasıyla, 1 saate karşılık 1.5 saat). İntravenöz olarak verildiğinde HUMALOG ve insan regüler insülini sırasıyla 0.1 ö/kg ve 0.2 U/kg dozlarında 26 ve 52 dakikalık yarılanma ömrü ile aynı bir doza-bağımlı elİminasyon sergilemiştir. Doğrusal!ık/doğrusal olmavan durum:Veri yoktur. Hastalardaki karakteristik özellilderVeri yoktur.Farmakokinetik/farmakodinamik özelliklerVeri yoktur.5.3 Klinik öncesi güvenlilik verileriİn vitrotestlerde insülin reseptör bölgelerine bağlanma ve büyüme hücreleri üzerine etkileri incelendiğinde insülin lispro insan insülinine benzerlik göstermiştir. Ayrıca yapılan çalışmalarda, insülin lispronun bağlanmış olduğu insülin reseptörlerinden ayrılma özelliğinin insan insülini ile aynı olduğu görülmüştür. Akut, 1 ay ve 12 ay süreli toksisite çalışmaları anlamlı toksisite bulgulan göstermemiştir.Yapılan hayvan çalışmalarında, insülin lispro fertilite bozulması, embriyotoksisite ya da teratojenite üzerinde bir etkide bulunmamıştır. 6. FARMASÖTİK ÖZELLİKLER6.1 Yardımcı maddelerin listesiMetakrezol (3.15 mg/ml)Gliserol Dibazik sodyum fosfat.THıO Çinko oksit Enjeksiyonluk su pH'ı 7.0 - 7.8'e ayarlamak için hidroklorik asit ve sodyum hidroksit kullanılabilir. 6.2 GeçimsizliklerHUMALOG diğer üreticilerin ürettiği insülinlerle veya hayvan kökenli insülin preparatlarıyla karıştırılmamalıdır. Bu tıbbi ürün, bölüm 4,2'de belirtilenler dışındaki tıbbi ürünlerle karıştırılmamalıdır.6.3 Raf ömrüKullanımdan önce:24 ay Kullanıma başladıktan sonra; 28 gün 6.4 Saklamaya yönelik özel uyanlarKullanımdan önce:Buzdolabında 2-8°C arasında saklayınız. Dondurmayınız. Donmuş ürünleri çözüp kullanmayınız. Aşın sıcak ve direkt güneş ışığı altında bırakmayınız. Kullanıma başladıktan sonra: Açılmış olan flakonlardaki çözelti 30°C'nin altındaki sıcaklıklarda saklanarak 28 gün boyunca kullanılabilir. Bu süreden sonra kullanılmamalıdır. Buzdolabında saklamayınız. 6.5 Ambalajın niteliği ve içeriğiÇözelti, butil veya halobutii tıpa ve aluminyum emniyet kapsülü ile kapatılmış tip I flint cam flakonlardadır. Flakon tıpası dimetikon veya silikon emülsiyonu ile muamele edilmiş olabilir.1 X 10 mİ HUMALOG 100 lU/ml 10 ml solüsyon içeren flakon 6.6 Beşeri tıbbi üründen arta kalan maddelerin imhası ve diğer özel önlemlerKullanılmamış olan ürünler ya da atık materyaller, 'Tıbbi atıkların kontrol yönetmeliği' ve 'Ambalaj ve Ambalaj Atıklarının Kontrolü yönetmelikleri'ne uygun olarak imha edilmelidir.7. RUHSAT SAHİBİLilly İlaç Ticaret Limited Şirketi Kuşbakışı Cad. Rainbovv Plaza No:4 Kat:3 34662 Altunizade - İstanbulTel : O 216 554 00 00 Faks : O 216 474 71 99 8. RUHSAT NUMARASI108/559. İLK RUHSAT TARİHİ / RUHSAT YENİLEME TARİHİİlk ruhsatlandırma tarihi: 26 Eylül 2000 Ruhsat yenileme tarihi: 08 Ağustos 200610. KÜB'ÜN YENİLENME TARİHİ15/15 |
İlaç BilgileriHumalog 100 IU/ml solüsyon içeren flakonEtken Maddesi: insülin lispro Atc Kodu: A10AC04 Kullanma talimatı ve kısa ürün bilgileri
Google Reklamları
İlgili İlaçlar |
Ana Sayfa | Hakkımızda | İlaçlar | İlaç Ara | İlaç Firmaları | Gizlilik | Bize Ulaşın
Telif Hakkı 2008-2026 © İlaç Prospektüsü. Tüm Hakları Saklıdır.Uyarı: Sitemizde yayınladığımız ilaç bilgileri ile doktora danışmadan kesinlikle ilaç kullanmayınız!
Aksi halde doğabilecek sağlık sorunlarından ilacprospektusu.com sorumlu tutulamaz.