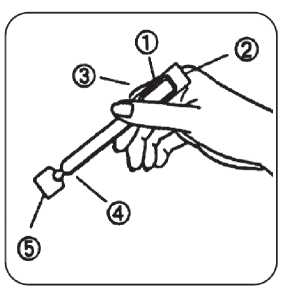
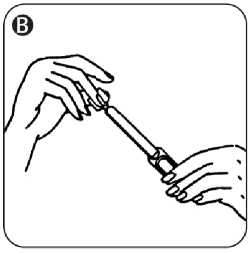
Crinone %8 Vaginal Jel Kısa Ürün BilgisiKISA ÜRÜN BİLGİSİ1. BEŞERİ TIBBİ ÜRÜNÜN ADICRINONE %8 vajinal jel 2. KALİTATİF VE KANTİTATİF BİLEŞİMEtkin madde:Her vajinal aplikatör etkin madde olarak 90 mg progesteron (%8 ağırlık/ağırlık) içerir.Yardımcı maddeler: 0,9 mg sorbik asitDiğer yardımcı maddeler için bölüm 6.1'e bakınız. 3. FARMASÖTİK FORMBeyaz polietilen vajinal aplikatör içerisinde beyaz ile beyazımsı vajinal jel 4. KLİNİK ÖZELLİKLER4.1 Terapötik endikasyonlar¦ Luteal faz yetmezliğine bağlı infertilite ¦ İnvitrofertilizasyon (IVF) uygulanan normal ovulatuar siklusları olan tubal, idiopatik,endometriozise bağlı infertilite 4.2 Pozoloji ve uygulama şekliPozoloji/ uygulama sıklığı ve süresi:CRINONE ile intravajinal tedavi, spesifik endikasyona ve her hastanın terapötik cevabına göre ayarlanmalıdır. En düşük etkin doz uygulanmalıdır. CRINONE'un, endometriyumda sekretuvar bir transformasyonu endüklemek üzere vajinal yoldan uygulanması ancak endometriyum endojen veya eksojen estrojen ile yeterli ölçüdehazırlanmışsa endikedir. Bu gibi vakalarda, gebelik meydana gelmemişse CRINONEtedavisinin kesilmesinden sonraki 3-7 gün içinde kesilme kanaması meydana gelir. CRINONE, intravajinal olarak uygulanır. CRINONE her gün aynı saatte uygulanmalıdır. Bir CRINONE dozu unutulduğunda hatırlar hatırlamaz, o doz hemen uygulanmalı ve öncekiprograma göre uygulamaya devam edilmelidir. Önerilen günlük dozdan fazlasıuygulanmamalıdır. Luteal faz yetmezliğine bağlı infertilite tedavisi:Dokümante edilmiş ovülasyonun ardından veya isteğe bağlı olarak, siklusun 18 ila 21. gününden başlayarak her gün bir uygulama (1.125 g %8 jel).İnvitro fertilizasyon (IVF) sırasında kullanım:Laboratuvar testleri ile gebelik gösterilmişse, 30 gün boyunca, günlük Crinone %8 Jel uygulaması sürdürülmelidir. 1 Uygulama şekli: Doktorunuz başka bir öneride bulunmadı ise günde tek doz, sabahları kullanımı önerilir. Kullandıktan sonra yatarak istirahate gerek yoktur. Aksine günlük aktiviteler ilacındağılımını olumlu etkileyeceğinden vajinada birikim ihtimali azalacaktır. Vajinal kullanım için özel tasarlanmış aplikatörü ile dokuya zarar vermeden uygulanır. CRINONE'u kendinize uygulamadan önce, lütfen aşağıdaki talimatları dikkatlice okuyunuz: Aplikatörünüzün görünüşü:1. Hava bölmesi 2. Kalın ucun düz tarafı 3. Kalın uç 4. İnce uç 5. Kapak Aplikatörünüzün kullanıma hazırlanışı: Aplikatörü kapalı paketinden çıkarınız. Büküp koparılarak açılan başlığı bu aşamadaçıkarmayınız. Dikkat:Yüksek irtifalarda (762 metre üzeri) uygulayabilmek için kalın uçtaki kabarıklığın düz kısmına iğne ile delik açınız. Bu yüksek irtifalarda aplikatörün içi ile dışı arasındaoluşan hava basıncı farkını düzenleyecektir. Alınacak doz miktarını etkilemeyecektir. Aplikatörü kalın ucundan sıkıca kavrayınız. İçindekilerin ince uçta birikmesini sağlamaküzere aşağı doğru tutarak termometre sallar gibi sallayınız. 2 Şimdi, aplikatörün ince ucundaki kapağı büküp kopararak açınız ve başlığı atınız. Jelin kullanmaya başlamadan öncedışarı akmasını önlemek için bu aşamada hava bölmesinisıkmayınız.
Aplikatörün yerleştirilmesi: Aplikatörü, oturma pozisyonunda veya dizleriniz bükülmüşolarak sırt üstü yatarken yerleştiriniz. Aplikatörün ince ucunuyavaşça, elleriniz vücudunuza değene kadar vajinayasokunuz. Jeli vajinanın içine doğru itmek üzere aplikatörün kalınucundaki hava bölmesini sıkınız. Dikkat:Yüksek irtifalarda uygulamak için baş parmağınızı veya parmağınızı kalın uçtaki kabarıklığın düz kısmınaaçtığınız deliğin üzerine koyunuz.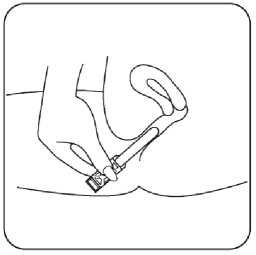 Aplikatörünüzü kullandıktan sonra: Aplikatörü çıkarınız ve atınız. Aplikatörde az bir miktar jel kalması önemli değildir. Yeterlidozu almış olursunuz. CRINONE jel vajinanızda birkaç gün kalabilir. Bu süre boyunca bej ila kahverengimsikümelenmiş şekilde veya bulanık beyaz akıntınız olabilir. Endişe edilecek bir durumdeğildir. Özel popülasyonlara ilişkin ek bilgiler:Böbrek/karaciğer yetmezliği:Karaciğer yetmezliğinde kullanılmamalıdır (bkz. bölüm 4.3). Böbrek bozukluğu olanlarda dikkatli kullanılmalıdır. Pediyatrik popülasyon:Uygulanabilir değildir. 3 Geriyatrik popülasyon:Uygulanabilir değildir. 4.3 Kontrendikasyonlar1. CRINONE formülasyonunun bileşenlerinden herhangi birine karşı bilinen hassasiyet. 2. Teşhis edilmemiş rahim kanaması. 3. Göğüste veya genital organlarda bilinen veya şüphelenilen progesteron-duyarlı malignansi. 4. Akut porfiri 5. Tromboflebit, tromboembolik bozukluklar, serebral apopleksi veya bu bozukluklara ilişkinhikayesi olan hastalar. 6. Atlanmış düşük 7. Karaciğer fonksiyon bozukluğu veya karaciğer hastalığı. 4.4 Özel kullanım uyarıları ve önlemleriCRINONE ile trombotik bozukluklar bildirilmemiştir. Bununla birlikte, bazı araştırmalarda, hormon replasman tedavisine bağlı olarak tromboflebit ve/veya tromboembolik bozukluklardabir artış riski bildirilmiştir. Hormon replasman tedavisi sırasında hekim, trombotik bozukluklar(tromboflebit, retinal tromboz, serebral embolizm ve pulmoner embolizm dahil) olasılığınakarşı dikkatli olmalı ve bunların erken belirtilerine karşı hazır bulunmalıdır. Bunlardanherhangi birinin meydana gelmesi veya şüphelenilmesi halinde hormon replasman tedavisihemen kesilmelidir. Trombotik bozukluklara ilişkin risk faktörü taşıyan hastalar dikkatlegözlenmelidir. Tromboembolizm riski estrojenler ile bağlantılı olmasına rağmen, progestinler ile bir bağlantı halen tartışmalıdır. Bu nedenle, kişisel veya aile öyküsü gibi tromboembolik olaylar için genelkabul görmüş risk faktörleri olan kadınlarda, Crinone tedavisi mevcut riski daha da artırabilir.Bu kadınlarda, Crinone uygulamasının yararlarının risklere karşı değerlendirilmesi gerekir.Ancak gebeliğin kendisinin de tromboembolik olay riski taşıdığı unutulmamalıdır. Tedavi öncesi ve sırasında periyodik muayenelerde tıbbi anamnez ve fiziki muayenede özellikle göğüsler ve pelvik organlar üzerinde durulmalı ve bir Papanicolaou smear (simir) alınmalıdır. CRINONE ciddi karaciğer yetmezliği olan hastalarda dikkatle kullanılmalıdır. Bütün düzensiz vajinal kanama vakalarında olduğu gibi ara kanama vakalarında işlevsel olmayan nedenler düşünülmelidir. Tanı konmamış vajinal kanama durumlarında, uygundiyagnostik incelemeler yapılmalıdır. Crinone düşük tehditlerinde endike değildir. Düşük durumunda tedavi durdurulmalıdır. Progestojenler bir ölçüde sıvı tutulmasına neden olabilecekleri için bu faktörden etkilenebilecekepilepsi, astım, migren ve kalp veya böbrek fonksiyon bozukluğu gibi hastalıkları olankadınların dikkatle gözlem altında tutulması gerekir. Depresyon geçmişi olan hastalar dikkatle gözlenmeli ve depresyon ciddi bir ölçüde tekrar ortaya çıkarsa CRINONE kesilmelidir. Azalan glukoz toleransı, estrojen-progestin kombine ilaçları kullanan hastalarda az sayıda görülmüştür. Bu düşüşün mekanizması bilinmemektedir. Bu nedenle, diyabetik hastalarprogestin tedavisi alırken dikkatli bir şekilde izlenmelidir. Progestojenlerle tedavi, postmenopozal semptomların ortaya çıkışını maskeleyebilir. Progestojenlerin endometriyum gibi organların yapısında ve patolojisindeki etkisi nedeniyle 4 ilgili numuneler verilen patologlara, progestojen tedavisi uygulandığı söylenmelidir. Progestojenler önceden mevcut porfiriya belirtilerini kötüleştirebilir. Bu nedenle, bu gibihastalarda CRINONE kullanılması önerilmez. Yardımcı madde olarak kullanılan sorbik asit lokal deri reaksiyonlarına (kontak dermatit gibi) ya da vajinal irritasyona sebebiyet olabilir. Mutajenez ve Karsinojenez:4.5 Diğer tıbbi ürünler ile etkileşimler ve diğer etkileşim şekilleriDiğer ilaçlarla hiç bir etkileşimi bildirilmemesine rağmen, CRINONE'un diğer intravajinal preparatlarla birlikte kullanılması önerilmemektedir. Eğer aynı anda başka bir antivajinal tedavikullanılacaksa, uygulamadan en az 6 saat önce ya da sonra olmalıdır. Kullanımdan birkaç günsonra bile, olası jel birikiminden ötürü, vajinal boşalma gibi küçük beyaz globüller görülebilir.Hastaya vajinal yolla antifungal bir tedavi uygulanıyorsa oral tedaviye geçilmesi önerilir. CYP3A4 indükleyiciler ile oral progesteronlar arasında serum progesteron seviyelerinin düşmesi ile sonuçlanan etkileşime ait bulgu olmasına rağmen CYP3A4 indükleyiciler iletekrarlayan CRINONE vaginal jel uygulaması sonucunda progesteron seviyelerinde anlamlıdeğişiklik beklenmemektedir. Laboratuvar testleri etkileşimleri:Özel popülasyonlara ilikin ek bilgilerPediyatrik popülasyonCRINONE çocuklarda kullanıma yönelik değildir. Geriyatrik popülasyonCRINONE yaşlılarda kullanıma yönelik değildir. 4.6 Gebelik ve laktasyonGenel tavsiye:Gebelikte kullanım kategorisi: B Çocuk doğurma potansiyeli bulunan kadınlar/Doğum kontrolü (Kontrasepsiyon):Geçerli değildir. Gebelik DönemiKorpus luteum eksikliğinde, CRINONE gebeliğin ilk haftasında kullanılabilir. Sınırlı sayıda maruz kalmış gebelik verileri, CRINONE'nun gebelik veya fetus / yeni doğan çocuk sağlığıüzerine herhangi bir advers etki göstermemiştir. Bugüne kadar ilgili başka herhangi birepidemiyolojik veri mevcut değildir. Hayvanlar üzerinde yapılan çalışmalar embriyonal/fetalgelişim ile ilgili olarak doğrudan ya da dolaylı zararlı etkiler olduğunu göstermemektedir (Bkz.Bölüm 5.3). Gebe kadınlara reçete edilirken dikkatli olunmalıdır. 5 CRINONE kullanımı, tekrarlayan düşük veya düşük tehlikesinde endike değildir. Laktasyon DönemiProgestojenler, bu ilaçları alan annelerin sütünde tespit edildikleri için laktasyonda kullanımları önerilmemelidir. Üreme yeteneği / fertiliteCRINONE infertilitede kullanım için endikedir (bkz. bölüm 4.1). 4.7 Araç ve makine kullanımı üzerindeki etkileriCRINONE'un araç ve makine kullanma yeteneği üzerine etkisi yoktur. 4.8 İstenmeyen etkilerCRINONE genellikle iyi tolere edilmektedir. Klinik araştırmalarda, CRINONE tedavisi sırasında aşağıdaki advers etkiler bildirilmiştir: İstenmeyen etkiler herbir sıklık grubu içinde, azalan ciddiyetine göre sunulmaktadır. Çok yaygın (>1/10); yaygın (>1/100 ila <1/10); yaygın olmayan (>1/1.000 ila <1/100); seyrek (>1/10.000 ila <1/1.000); çok seyrek (<1/10.000), bilinmiyor (eldeki verilerden hareketletahmin edilemiyor). İyi huylu ve kötü huylu neoplazmalarÇok seyrek: İyi huylu kist Kan ve lenf sistemi hastalıklarıYaygın olmayan: Purpura, anemi Bağışıklık sistemi hastalıklarıYaygın: İdrar yolu enfeksiyonu Yaygın olmayan: Enfeksiyon, farenjit, sinüzit, üst solunum yolu enfeksiyonları Metabolizma ve beslenme hastalıklarıYaygın olmayan: Susuzluk, ağız kuruluğu, terlemede artış Sinir sistemi hastalıklarıÇok yaygın: Baş ağrısı, depresyon, ruhsal durumda değişkenlik, sinirlilik, somnolans Yaygın: Unutkanlık, baş dönmesi Yaygın olmayan: Migren, tremor, insomnia, iritabilite Göz hastalıklarıYaygın olmayan: Göz kuruluğu, konjonktivit Kardiyak hastalıklarYaygın olmayan: Baygınlık Solunum, göğüs hastalıkları ve mediastinal hastalıklarYaygın olmayan: Astım, nefes darlığı, göğüslerin büyümesi, hiperventilasyon, rinit 6 Gastrointestinal hastalıklarYaygın: Kusma, kabızlık, diyare, şişkinlik, mide bulantısı Yaygın olmayan: Dispepsi, geğirti, diş ağrısı, mide ağrısı Deri ve deri altı doku hastalıklarıYaygın: Genital prüritis, genital moniliazis Yaygın olmayan: Döküntü, deride renk değişikliği, deri bozuklukları, ürtiker, kepeklenme, akne Kas-iskelet bozuklukları, bağ doku ve kemik hastalıklarıYaygın: Artralji, bacaklarda kramp, bacak ve eklem ağrısı Çok seyrek: Miyalji Böbrek ve idrar yolu hastalıklarıYaygın: Disparöni, noktüri, sistit Yaygın olmayan: Disüri, sık idrara çıkma, lökore Genel bozukluklar ve uygulama bölgesine ilişkin hastalıklarÇok yaygın: Yorgunluk, perineal ağrı, memelerde şişkinlik/hassasiyet Yaygın: Sırt ağrısı, karın ağrısı, vajinal akıntı, vajinalsekresyonda artma, alerji, cinsel arzunun azalması, vajinal kuruluk Yaygın olmayan: Alerjik reaksiyon, iştah azalması, asteni, ödem, yüz ödemi, sıcak basması, ateş, su tutulması, vajinal kanama/lekelenme, premenstürel sendrom, dismenore, laktasyon, grip benzeri semptomlar Pazarlama sonrası raporlarPazarlama sonrasında tespit edilen advers reaksiyonlarda sıklık bilinmemektedir (mevcut verilerle tahmin edilememektedir).Ayrıca, intermenstrüel kanama (lekelenme), vajinal irritasyon, genellikle deride kaşıntı gibi kendini gösteren aşırı hassasiyet reaksiyonları ve diğer hafif uygulama yeri reaksiyonlarıpazarlama sonrası rapor edilmiştir. Yukarıdaki bütün olaylarla CRINONE tedavisinin ilişkisi bilinmemektedir. Çoğu istenmeyen etki hafif ve geçicidir ve CRINONE tedavisinin sürdürülmesi ile ortadan kalkmaktadır. Şüpheli advers reaksiyonların raporlanmasıRuhsatlandırma sonrası şüpheli ilaç advers reaksiyonlarının raporlanması büyük önem taşımaktadır. Raporlama yapılması, ilacın yarar/risk dengesinin sürekli olarak izlenmesineolanak sağlar. Sağlık mesleği mensuplarının herhangi bir şüpheli advers reaksiyonu TürkiyeFarmakovilijans Merkezi (TÜFAM)'ne bildirmeleri gerekmektedir (www.titck.gov.tr;[email protected] Doz aşımı ve tedavisiCRINONE ile ilgili hiç bir doz aşımı raporu alınmamıştır. Progesteronun, vajinal epitelyumdan konsantrasyona bağımlı, sınırlı hızdaki absorpsiyonu ile formülasyonun kontrollü salınımözellikleri nedeniyle, bu üründe akut doz aşımı olası değildir. Bununla birlikte doz aşımı durumunda CRINONE'un kesilmesi ve hastanın semptomatik olarak tedavi edilmesi gerekir. 7 5. FARMAKOLOJİK ÖZELLİKLER5.1 Farmakodinamiik özelliklerFarmakoterapötik grup: Ürogenital sistem ve cinsiyet hormonları, cinsiyet hormonları ve genital sistem modülatörleri, progestogenler, pregnen (4) türevleri, progesteronATC kodu: G03DA04 Progesteron, estrojenle uyarılmış endometriyumun, döllenmiş yumurtayı kabul edebilir sekretuvar endometriyum haline dönüşmesinde ve daha sonra embriyonun gelişiminin ilkaşamalarında emplantasyonun sürdürülmesinde önemli bir rol oynar. Corpus luteum, doğalprogestojen olan progesteronun primer kaynağıdır; plasenta, gebeliğin sürdürülmesinisağlamak üzere progesteron salgılamayı sürdürür. Progesteron, memenin glandüleroluşumlarını stimüle eder, servikal mukusu kalınlaştırır ve vücut sıcaklığını yükseltir.Aldosteron salgısında bir artışa yol açacak şekilde mineralo kortikoidlerin sodyum tutmaetkilerini antagonize eder. Menopozdan sonra ovarian estradiol salgısının kaybı; uyku bozukluğu ve aşırı terleme, ürogenital atrofi, disparoni ve üriner inkontinans ile birlikte sıcak basmalarına neden olantermoregülasyon instabilitesi ile sonuçlanabilir. Estrojen replasman tedavisi, menopozdevresindeki kadında estradiol eksikliğine bağlı birçok semptomu giderir. Progestojenlerin, estrojen replasman tedavisiyle birlikte devresel kullanımı, estrojenlerin, endometriyumun sekretuvar dönüşümüne neden olan uyarıyı önler ve progesteronun kesilmesi,endometrial tabakanın parçalanarak atılmasına ve vajinal kanamaya neden olur. Progestojentedavisi, endometrial kanser riskinde bir azalmayla sonuçlanır. Estrojen replasman tedavisine oral bir progestojenin eklenmesi, estrojen tedavisinin lipidler üzerindeki faydalı etkilerini azaltabilir. Bu nedenle, bu değişiklikleri en aza indirmek içinprogestojen seçimi önemli olabilir. Doğal progesteron, HDL-C veya alt-fraksiyonlarınıetkilememektedir. İntravajinal olarak uygulanan progesteron, estrojenin rahim arterlerinde endüklediği vasküler direnç azalmasını sadece minimal ölçüde tersine dönüştürmektedir. Disfonksiyonel rahim kanaması veya sekonder amenoreye neden olabilecek hormon dengesizliği, eksojen progesteron ile düzeltilebilir. 5.2 Farmakokinetik özelliklerEmilim: Progesteron vajinal jel, vajinal mukozaya bağlanan ve en az üç gün uzatılmış progesteron salınımı sağlayan bir polikarbofil uygulama sisteminden oluşmaktadır.Ortalama yarı ömrü (t/) (25-50 saat), CRINONE'un farmakokinetiğinin, CRINONE'dan progesteron absorpsiyonunun nispeten yavaş olduğunu yansıtmaktadır. Dağılım: Vajinal uygulama ile, transvajinal yoldan uterusa öncelikli dağılım ve karaciğerde ilk-geçiş metabolizasyonu aşamasının olmaması sonucunda, ilacın etki bölgesi olan uterus dokularında progesteronun yüksek biyoyararlanımına yol açabilir (Uterusda İlk Geçiş Etkisi).Biyotransformasyon: Progesteron esas olarak karaciğerde metabolize olur.8 Eliminasyon5.3 Klinik öncesi güvenlilik verileriTavşanlarda CRINONE'un deri değil, göz tahriş edici etkisi saptanmıştır. 5 gün süreyle günde 2 ml %8 jel uygulama sonrası tavşanlarda orta derecede vajinal irritasyon oluşmuştur.Hayvanlarda yürütülen teratojenisite/embriyotoksisite çalışmaları doğal progesteron tedavisinden sonra konjenital bozukluk riski olduğunu göstermemiştir 6. FARMASÖTİK ÖZELLİKLERİ6.1 Yardımcı maddelerin listesiGliserin, Hafif sıvı parafin, Hidrojene hurma yağı gliseridi, Karbopol 974P, Sorbik asit, Polikarbofil Sodyum hidroksitSaf su 6.2 GeçimsizliklerBilinen kontraseptif aletlerle geçimsizliği bulunmadı. 6.3 Raf-ömrü36 ay. 6.4 Saklamaya yönelik özel tedbirler25°C'nin altındaki oda sıcaklıklarında ve ambalajında saklayınız. 6.5 Ambalajın niteliği ve içeriğiİntravajinal uygulama için dizayn edilmiş, tek kullanımlık, bir parça, ucu bükülebilir beyaz polietilen aplikatör. Her bir aplikatör 1.45 g jel içerir ve 1.125 g jel taşır. Her biri sarılmış ve kağıt / aluminyum / polietilen folyo ile kapatılmıştır. Her bir CRINONE %8 vajinal jel ambalajı 15 aplikatör içerir. 6.6 Beşeri tıbbi üründen arta kalan maddelerin imhası ve diğer özel önlemler9 Kullanılmamış olan ürünler ya da atık materyaller "Tıbbi Ürünlerin Kontrolü Yönetmeliği" ve "Ambalaj Atıklarının Kontrolü Yönetmeliği"ne uygun olarak imha edilmelidir. 7. RUHSAT SAHİBİMerck İlaç Ecza ve Kimya Tic.A.Ş. Atatürk Mh. Ertuğrul Gazi Sk. Metropol İstanbul Sit. C2 Apt. No: 2A/20 Ataşehir/İstanbul Tel: 0 216 578 66 00 Fax: 0 216 469 09 22 8. RUHSAT NUMARASI109/16 9. İLK RUHSAT TARİHİ / RUHSAT YENİLEME TARİHİİlk ruhsat tarihi: 10/11/2000 Ruhsat yenileme tarihi: 10/11/2005 10. KÜB'ÜN YENİLEME TARİHİ10 |
İlaç BilgileriCrinone %8 Vaginal JelEtken Maddesi: Progesteron
Google Reklamları
İlgili İlaçlar |
Ana Sayfa | Hakkımızda | İlaçlar | İlaç Ara | İlaç Firmaları | Gizlilik | Bize Ulaşın
Telif Hakkı 2008-2026 © İlaç Prospektüsü. Tüm Hakları Saklıdır.Uyarı: Sitemizde yayınladığımız ilaç bilgileri ile doktora danışmadan kesinlikle ilaç kullanmayınız!
Aksi halde doğabilecek sağlık sorunlarından ilacprospektusu.com sorumlu tutulamaz.