Lievo 500mg/100ml Iv Perfüzyonluk Çözelti İçeren Flakon Kısa Ürün BilgisiKISA ÜRÜN BİLGİSİUYARI: TENDİNİT VE TENDON YIRTILMASI, PERİFERAL NÖROPATİ, SANTRAL SİNİR SİSTEMİ ETKİLERİ VE MYASTENİA GRAVİS'İNŞİDDETLENMESİNİ DE İÇEREN CİDDİ ADVERS REAKSİYONLAR LİEVO da dahil olmak üzere florokinolonlar aşağıdaki gibi sakatlığa yol açan ve geridönüşümüz advers reaksiyonlara neden olabilir: o Tendinit ve tendon yırtılması o Periferal nöropatio Santral sinir sistemi etkileri Bu reaksiyonlardan herhangi birinin gözlendiği hastalarda LİEVO kullanımı derhal bırakılmalı ve florokinolon kullanımından kaçınılmalıdır. LİEVO da dahil olmak üzere florokinolonlar, myastenia gravisli hastalarda kas güçsüzlüğünü şiddetlendirebilir. Bilinen myastenia gravis öyküsü olanlarda LİEVO kullanımından kaçınılmalıdır. 1. BEŞERİ TIBBİ ÜRÜNÜN ADILİEVO 500 mg/100 ml İ.V. perfüzyonluk çözelti içeren flakon Steril2. KALİTATİF VE KANTİTATİF BİLEŞİMEtkin madde:100 mL perfüzyon çözeltisinde: Levofloksasin :500 mg (5 mg/ml) (500 mg levofloksasine eşdeğer 512,46 mg levofloksasin hemihidrat içerir) Yardımcı maddeler:Sodyum klorür : 900 mg Diğer yardımcı maddeler için 6.1'e bakınız. 3. FARMASÖTİK FORMİ.V. perfüzyonluk çözelti Temiz, yabancı partikül içermeyen yeşilimsi-sarı çözelti. 4. KLİNİK ÖZELLİKLER4.1 Terapötik endikasyonlarLİEVO, levofloksasine duyarlı mikroorganizmaların etken olduğu aşağıda belirtilen erişkinlerdeki enfeksiyonların tedavisinde endikedir: Toplumda edinilmiş pnömoni Staphylococcus aureus, Streptococcus pneumoniae (penisilin için MİK değeri > 2 g/ml olan penisiline dirençli suşlar dahil), Haemophilus influenzae, Haemophilus parainfluenzae,Klebsiella pneumoniae, Moraxella catarrhalis, Chlamydia pneumoniae, Legionellapneumophila veya Mycoplasma pneumoniae 'nin neden olduğuPiyelonefrit dahil, komplikasyonlu üriner sistem enfeksiyonlarıEscherichiaEnterococcus faecalis, Enterobacter cloacae, Escherichia coli, Klebsiella pneumoniae, Proteus mirabilis veya Pseudomonasaeruginosa'nin neden olduğuProstatit:Escherichia coli, Enterococcus faecalis ya da Stapylococcus epidermidis 'inneden olduğu Deri ve yumuşak doku enfeksiyonları Metisiline duyarlı Staphylococcus aureus, Enterococcus faecalis, Streptococcus pyogenes veya Proteus mirabilis 'inStaphylococcus aureusStreptococcus pyogenes'inneden olduğu apse, selülit,furonkül, impetigo, piyoderma, yara enfeksiyonlarının dahil olduğu komplikasyonsuz derive deri ekleri enfeksiyonları Hastanede edinilmiş pnömoni Staphylococcus aureus, Pseudomonas aeruginosa, Serratia marcescens, Escherichia coli, Klebsiella pneumoniae, Enterobacter aerogenes, Haemophilus influenzaeStreptococcus pneumoniae.Pseudomonasaeruginosaolması halinde bir anti-psödomonal P-laktam ile kombine tedavi önerilir. Şarbon inhalasyonu Havaya karışmış Bacillus antracis 'e4.2 Pozoloji ve uygulama şekliLİEVO I.V. perfüzyon çözeltisi yavaş intravenöz infüzyon şeklinde (en az 60 dakika süren infüzyon) günde tek doz veya iki kez uygulanabilir. Dozaj, enfeksiyonun tipine, şiddetine veolası etken patojenin duyarlılığına bağlı olarak ayarlanır. Hastanın durumuna bağlı olarak,başlangıçtaki iv uygulamadan birkaç gün sonra oral uygulamaya LİEVO 250 veya 500 mg filmkaplı tablet ile geçilmesi mümkün olabilmektedir. Oral ve parenteral formlar biyoeşdeğerolduğundan, her iki formda da aynı dozajın uygulanması mümkündür. Pozoloji:LİEVO'nun aşağıda belirtilen dozlarda erişkinler için uygulanması önerilir:
Uygulama şekli:LİEVO perfüzyon çözeltisi, sadece yavaş intravenöz infüzyon ile uygulanır. Uygulama günde tek doz veya günde iki kez yapılabilir. İnfüzyon süresi 500 mg LİEVO çözeltisi için 60 dakika 2/17
olmalıdır (Bkz. bölüm 4.4). Hastanın durumuna bağlı olarak, birkaç gün içinde aynı dozajla, başlangıçtaki intravenöz uygulamadan oral uygulamaya geçilmesi mümkün olabilmektedir.Geçimsizlikler için, bölüm 6.2. ye bakınız. Tedavinin süresiTedavinin süresi hastalığın seyrine bağlıdır (Yukarıdaki tabloya bakınız). Genel olarak bütün antibiyotik tedavilerinde olduğu gibi, LİEVO kullanımı hastanın ateşi düştükten ve bakteriyeleradikasyon elde edildiğine dair kanıt sağlandıktan sonra, en az 48-72 saat daha sürdürülmelidir. Özel popülasyonlara ilişkin ek bilgiler:Böbrek yetmezliği :Aşağıdaki tabloda belirtilen şekilde kullanılır.K reatinin klirensi <50 ml/dakika olan hastalarda dozaj (Enfeksiyonun şiddetine göre)_
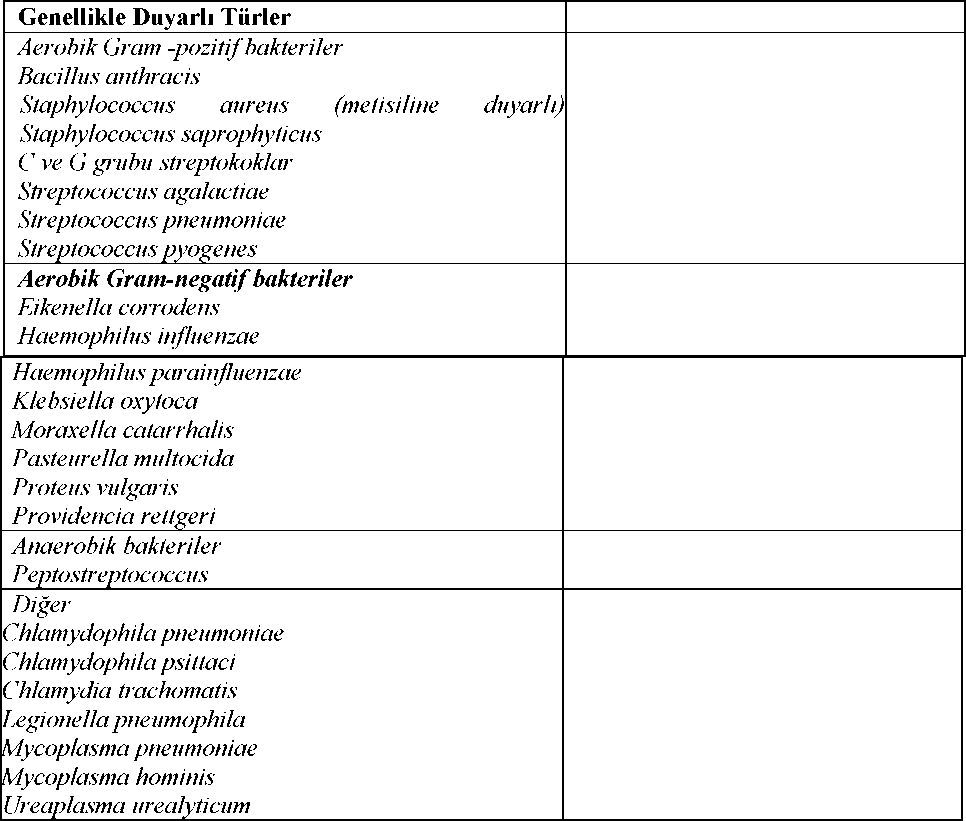
Karaciğer yetmezliği:Levofloksasin karaciğerde çok düşük miktarlarda metabolize olduğu ve esas olarak böbrekler yoluyla atıldığı için karaciğer yetmezliğinde doz ayarlamasına gerek yoktur. Pediyatrik popülasyon:LİEVO çocuklarda ve büyümesi devam eden ergenlerde kontrendikedir. (Bkz. bölüm 4.3). Geriyatrik popülasyon:Yaşlı hastalarda böbrek fonksiyonları yeterli düzeyde ise dozaj ayarlamasına gerek yoktur. (Bkz. Bölüm 4.4, QT aralığının uzaması) 4.3 KontrendikasyonlarAşağıda belirtilen durumlarda LİEVO (levofloksasin) kullanılmamalıdır: Levofloksasine veya LİEVO perfüzyon çözeltisi bileşiminde bulunan maddelerdenherhangi birine veya florokinolon grubu bir diğer antibakteriyel ilaca karşı aşırı duyarlılığıolduğu bilinen hastalar Epilepsisi olan hastalar Florokinolon grubu bir antibakteriyelin kullanımına bağlı geliştiği bilinen tendonrahatsızlığı öyküsü olan hastalar Çocuklar ve büyümesi devam eden ergenler Hamilelik sırasında Emziren kadınlarda 3/17Çocuklarda, büyümesi devam eden ergenlerde, hamilelik sırasında ve emziren kadınlarda kullanımı kontrendikedir çünkü -hayvan çalışmalarına dayanılarak- gelişmekte olanorganizmanın gelişen kıkırdak dokusuna zarar verme riski tamamen göz ardı edilemez. 4.4 Özel kullanım uyarıları ve önlemleriGenel uyarılar Edinilmiş direnç prevalansı, bazı bakteri türleri için ülkeden ülkeye ve zaman içinde değişiklik gösterebilir. Bu nedenle dirençle ilgili yerel verilere gereksinim vardır; özellikle ağırenfeksiyonlarda veya tedaviye yanıt alınamadığında, patojen izole edilerek mikrobiyolojik tanıkonmalı ve patojenin duyarlılığına dair kanıt aranmalıdır. Çok ciddi pnömokoksik pnömoni olguları için LİEVO en uygun tedavi olmayabilir. P. aeruginosa'nınetken olduğu nozokomiyal enfeksiyonlarda kombine tedaviye ihtiyaç olabilir.İdrar yolu enfeksiyonlarında en yaygın patojen olan E.colfnin,E.colfninflorokinolonlara karşı direncinin lokal prevelansını dikkate almaları tavsiye edilmektedir.Metisiline dirençli S. aureus:(MDSA):Metisiline dirençli S.Tendinit ve tendon rüptürü, periferal nöropati ve merkezi sinir sistemi etkileri dâhil sakatlığa sebep olan ve potansiyel geri dönüşümsüz ciddi advers reaksiyonlarLİEVO dâhil florokinolonlar, sakatlığa sebep olabilen ve potansiyel geri dönüşümsüz ciddi advers reaksiyonlarla ilişkilendirilmiştir. Yaygın olarak görülen advers reaksiyonlar kas- iskeletve periferal sinir sistemi (tendinit, tendon rüptürü, tendonlarda şişme veya enflamasyon,karıncalanma veya uyuşma, kol ve bacaklarda uyuşukluk, kas ağrısı, kas güçsüzlüğü, eklemağrısı, eklemlerde şişme gibi) artralji, miyalji, periferal nöropati ve merkezi sinir sistemietkileridir (halüsinasyon, anksiyete, depresyon, intihar eğilimi, insomnia, şiddetli baş ağrısı vekonfüzyon) (bkz. bölüm 4.8). Bu reaksiyonlar, LİEVO başladıktan sonra saatler ya da haftalar içinde görülebilir. Her yaş grubundan veya önceden mevcut risk faktörleri olmayan hastalar, bu advers reaksiyonlarıyaşamıştır. Herhangi bir ciddi advers reaksiyonun ilk bulgularının veya semptomlarının ortaya çıkması durumunda LİEVO derhal kesilmelidir. Ayrıca, florokinolonlarla bağlantılı olarak bu ciddiadvers reaksiyonlardan herhangi birini yaşayan hastalarda LİEVO dâhil florokinolonlarınkullanımından kaçınılmalıdır. Konvülsiyona eğilimli hastalar: Kinolonlar nöbet eşiğini düşürebilir ve nöbetleri tetikleyebilir. Diğer kinolonlarla olduğu gibi LİEVO, epilepsisi olan hastalarda kontrendikedir (Bkz. Bölüm 4.3) ve diğer kinolonlarda olduğugibi, epileptik nöbetlere yatkın olan veya teofilin gibi nöbet eşiğini düşüren ilaçlarla eşzamanlıtedavi gören hastalarda son derece dikkatle kullanılmalıdır (Bkz. Bölüm 4.5). Konvülsiyon tipinöbet oluşması durumunda (Bkz. Bölüm 4.8) levofloksasin tedavisinin kesilmesi gerekir. 4/17Clostridium difficileile ilişkili hastalık (Psödomembranöz kolit)LİEVO perfuzyon çözeltisi tedavisi sırasında veya sonrasında (tedaviden birkaç hafta sonrası dahil olmak üzere) şiddetli, ısrarlı ve/veya kanlı diyare görülürse, bu Clostridium difficile ileilişkili psödomembranöz kolitin belirtisi olabilir. Bu hastalığın şiddeti, en şiddetlisipsödomembranöz kolit olmak üzere, orta seviyeden hayatı tehdit edici boyuta kadar değişebilir(Bkz. Bölüm 4.8). Dolayısıyla, levofloksasin ile tedavi sırasında ve sonrasında ciddi ishal gelişenhastalarda bu tanının dikkate alınması önemlidir. Bu psödomembranöz enterokolitin en ciddiformudur. Eğer psödomembranöz enterokolitten şüpheleniliyorsa, LİEVO tedavisi hemensonlandırılmalı ve gecikmeden uygun bir tedaviye başlanmalıdır. Bu klinik durumda, bağırsakhareketlerini engelleyen ilaçlar kontrendikedir. Tendinit ve tendon rüptürü: Nadiren tendinit meydana gelebilir. En çok aşil tendonunu etkiler ve tendon rüptürüne yol açabilir. Tendinit ve tendon rüptürü (bazen bilateral olmak üzere) tedavinin başlangıcındansonraki 48 saat içinde oluşabilir; tedavinin bitmesinden sonraki birkaç aya kadar tendinit vetendon rüptürü vakaları bildirilmiştir. 60 yaş üzerindeki hastalarda, günlük 1000 mg'lık doz alanhastalarda kortikosteroid kullanan hastalarda, tendinit ve tendon rüptürü riski artar. Ayrıca, nakilyapılan hastalar artan tendinit riski altında olduğundan, bu popülasyonda florokinolonlarkullanıldığında dikkatli olunması önerilir. Yaşlı hastalarda günlük doz, kreatinin klirensine göreayarlanmalıdır (Bkz. Bölüm 4.2). Bu hastalara LİEVO reçete edildiyse, yakından takip edilmelerigerekir. Tendinit belirtileri yaşayan bütün hastalar doktorlarına danışmalıdırlar. Eğer tendinittenşüpheleniliyorsa LİEVO tedavisi derhal kesilmeli ve etkilenmiş tendonun hareketsiz tutulması(immobilizasyon) şeklinde uygun tedavi başlatılmalıdır. (Bkz. Bölüm 4.3 ve 4.8). Aşırı duyarlılık reaksiyonları:Levofloksasin, ilk dozunu takiben nadiren, öldürücü potansiyeli olan ciddi aşırı duyarlılık reaksiyonlarına (örn. anjiyoödem, anafilaktik şok) neden olabilir (Bkz. bölüm 4.8). Hastalarderhal tedaviyi kesmeli ve acil önlem alınması için doktora başvurmalıdır. Ağır bülloz reaksiyonlar:Levofloksasin ile Stevens Johnson sendromu veya toksik epidermal nekroliz gibi ağır büllöz deri reaksiyonları bildirilmiştir (bkz. Bölüm 4.8). Herhangi bir deri ve/veya mukoza bozukluğu ortayaçıkması halinde, hastaların tedaviye devam etmeden önce hemen doktorlarına başvurmalarıgerekir. Hepato-biliyer bozukluklar:Sepsis gibi altta yatan çok ciddi hastalıkları bulunan kişilerde, levofloksasin uygulanması ile karaciğer nekrozundan yaşamı tehdit eden karaciğer yetmezliğine kadar gidebilen olgular raporedilmiştir (Bkz. bölüm 4.8). İştahsızlık, sarılık, koyu renkte idrar, kaşıntı veya karında hassasiyetgibi karaciğer hastalığıyla ilgili semptom ve işaretler gelişirse, hastanın tedaviyi durdurması vederhal doktoruyla temas kurması gerekir. QTaralığında uzama:Levofloksasin de dâhil olmak üzere florokinolon kullanan hastalarda, aşağıdaki gibi QT aralığının uzaması açısından risk faktörleri varsa dikkatli olunması gerekir: - Düzeltilmemiş elektrolit dengesizliği (örn. hipokalemi, hipomagnezemi) - Konjenital uzun QT sendromu - Kardiyak hastalık (örn. kalp yetmezliği, miyokard enfarktüsü, bradikardi) - QT aralığını uzattığı bilinen ilaçların birlikte kullanılması (örn. Sınıf IA ve III antiaritmikler,trisiklik antidepresanlar, makrolidler, antipsikotikler) 5/17İleri yaştaki hastalar ve kadınlar QTc aralığını uzatan ilaçlara karşı daha duyarlı olabilirler. Bu nedenle, bu hasta grubunda levofloksasin de dahil olmak üzere florokinolonlar kullanıldığındadikkatli olunmalıdır. (Bkz. Bölüm 4.2, 4.5, 4.8 ve 4.9). Disglisemi:Diğer tüm kinolonlarla olduğu gibi, genellikle oral hipoglisemik ajan (örn. glibenklamid) veya insülin ile tedavi gören diyabetli hastalarda hiperglisemi ve hipoglisemiyi içeren kan glukozdüzeyi bozuklukları görüldüğü bildirilmiştir. Hipoglisemik koma olguları bildirilmiştir. Diyabetlihastalarda kan glukozunun dikkatle takip edilmesi tavsiye edilmektedir (Bkz. bölüm 4.8). Miyastenia Gravis'in şiddetlenmesi:Levofloksasinin de dahil olduğu florokinolonlar nöromüsküler blokaj aktivitesine sahiptirler ve myastenia gravisli hastalarda kas güçsüzlüğünü şiddetlendirebilirler. Florokinolon kullananmyastenia gravisli hastalarda, ventilatör desteği gerektiren akciğer yetmezliği ve ölümü dekapsayan pazarlama sonrası ciddi advers olaylar, florokinolonla ilişkilendirilmiştir. Öyküsündemyastenia gravis bulunan hastalar florokinolon kullanımından kaçınılmalıdır. Böbrek yetmezliği olan hastalar:Levofloksasin temel olarak böbrekler yoluyla atıldığından, böbrek yetmezliği olan hastalarda LİEVO perfüzyon çözeltisinin dozunun ayarlanması gerekir (Bkz. bölüm 4.2). Işığa karşı duyarlılık gelişmesi (fotosensitizasyon):Levofloksasine bağlı fotosensitizasyon çok nadiren görülmekle birlikte, fotosensitizasyonun önlenmesi için hastaların tedavi süresince ve tedavi sonlandırıldıktan sonra 48 saat boyuncakuvvetli güneş ışığına çıkmamaları veya solaryum gibi yapay ultraviyole ışınlarına maruzkalmamaları önerilir. Süperenfeksiyon:Diğer antibiyotiklerde olduğu gibi, levofloksasinin uzun süreli kullanımı, dirençli olmayan organizmaların aşırı çoğalmasına sebep olabilir. Hastanın durumunun tekrarlayandeğerlendirmeleri önemlidir. Eğer süperenfeksiyon oluşursa uygun tedavi yöntemleriuygulanmalıdır. Glikoz-6-fosfat dehidrogenaz eksikliği olan hastalar:Glikoz-6-fosfat dehidrogenaz aktivitesinde latent veya aktüel defekt bulunan hastalar kinolon grubu antibakteriyellerle tedavi edildiğinde hemolitik reaksiyonlara eğilimi artabilir, bu yüzdenlevofloksasin bu tip hastalarda kullanılacaksa hemoliz gelişme potansiyeli yakından takipedilmelidir. Periferik nöropatiLevofloksasin de dahil olmak üzere florokinolon kullanan hastalarda, başlangıcı hızlı olabilen duyusal veya duyusal-motor periferik nöropati bildirilmiştir. (Bkz. Bölüm 4.8). Geri dönüşümsüzbozuklukların gelişmesini önlemek için, eğer hasta nöropati semptomları yaşarsa, levofloksasinkullanımına son verilmesi gerekir. Şarbon inhalasyonuİnsanlarda kullanım, in vitro Bacillus anthrasisduyarlılığı verilerini, hayvanlardaki deneysel verileri ve insanlardaki sınırlı verileri temel almaktadır. Tedaviyi uygulayan doktor, şarbontedavisi ile ilgili ulusal ve/veya uluslararası uzlaşı belgelerine başvurmalıdır.Enfüzyon süresi 6/17LİEVO 500 mg iv perfuzyon çözeltisi için önerilen infüzyon süresi en az 60 dakikadır. Bu süre boyunca hasta gözlenmelidir. LİEVO perfüzyonu ile taşikardi ve kan basıncında geçici düşme,nadir vakalarda kan basıncının belirgin şekilde düşmesi ile dolaşım kollapsı gelişebilmektedir.Levofloksasin (ofloksasin'in l-izomeri) infüzyonu sırasında kan basıncında dikkati çekecek kadarbir düşme gözlenirse, infüzyon hemen kesilmelidir. K vitamini antagonistleriyle tedavi edilen hastalar K vitamini antagonisti (örn. varfarin) ile tedavi edilen hastalarda birlikte LİEVO kullanılması durumunda koagülasyon testlerinde (PT/INR) yükselme ve/veya kanamada artış ihtimaline karşı,bu ilaçların birlikte kullanılması durumunda, koagülasyon testleriyle takip yapılması gereklidir(Bkz. bölüm 4.5). Psikotik reaksiyonlar Levofloksasin dahil, kinolon alan hastalarda psikotik reaksiyonlar geliştiği bildirilmiştir. Çok nadir olgularda, bazen tek bir levofloksasin dozunu takiben intihar düşüncelerine kapılma vekendini tehlikeye atan davranışlar görülmüştür (Bkz. bölüm 4.8). Hastada bu gibi reaksiyonlargelişirse, levofloksasin kesilmeli ve uygun önlemler alınmalıdır. Psikotik bozukluğu olan veyapsikiyatrik hastalık öyküsü bulunan hastalarda levofloksasin kullanılması gerekiyorsa, dikkatliolunmalıdır. Görme bozukluklarıGörme bozukluğu ya da gözlerde herhangi bir etki ortaya çıktığında hemen göz hastalıkları uzmanı tarafından muayene yapılmalıdır (Bkz. Bölüm 4.7 ve 4.8). Laboratuvar testleri ile etkileşimLevofloksasin ile tedavi edilen hastalarda idrarda opiyat saptanması sırasında yalancı pozitif sonuç alınabilir. Bu sonucun daha özgün metotlar kullanılarak doğrulanması gerekebilir. Levofloksasin Mucobacterium tuberculosis çoğalmasını baskılayabilir ve bu nedenle tüberkülozun bakteriyolojik tanısında yalancı negatif sonuca yol açabilir. Aort anevrizması ve diseksiyonuEpidemiyolojik çalışmalar, florokinolon kullanımından sonra özellikle yaşlı popülasyonda aort anevrizması ve diseksiyonu riskinde artış olduğunu bildirmektedir. Bu nedenle florokinolonlar, aile öyküsünde anevrizma hastalığı pozitif olan hastalarda, önceden aort anevrizması ve/veya aort diseksiyonu teşhisi konulan hastalarda, aort anevrizması vediseksiyonu için diğer risk faktörlerini ya da predispozan durumları içeren hastalarda (örn.Marfan sendromu, vasküler Ehlers-Danlos sendromu, Takayasu arteriti, dev hücreli arterit,Behçet hastalığı, hipertansiyon, bilinen ateroskleroz) sadece dikkatli bir yarar/riskdeğerlendirmesi yapıldıktan sonra ve diğer terapötik seçenekler göz önüne alındıktan sonrakullanılmalıdır. Ani karın, göğüs veya sırt ağrısı durumunda, hastalara acil servise derhal başvurmaları tavsiye edilmelidir. LİEVO, litresinde 154 mmol sodyum ihtiva eder. Bu durum, kontrollü sodyum diyetinde olan hastalar için göz önünde bulundurulmalıdır. 4.5 Diğer tıbbi ürünler ile etkileşimler ve diğer etkileşim şekilleriTeofilin, fenbufen veya benzeri diğer nonsteroidal antienflamatuvar ilaçlarYapılan bir klinik çalışmada levofloksasin ile teofilin arasında herhangi bir farmakokinetik etkileşim bulunmamıştır. Fakat konvülsiyon eşiğini düşüren ilaçlar, teofilin veya nonsteroidal 7/17antienflamatuvar ilaçların, kinolon grubu bir antibiyotik ile birlikte kullanılması halinde, beyin konvülsiyon eşiğinde belirgin bir düşme görülebilir. Tek başına uygulanmasına kıyasla, fenbufen ile birlikte kullanıldığında levofloksasinin konsantrasyonu yaklaşık olarak %13 oranında daha yüksek bulunmaktadır.Probenesid ve simetidinLevofloksasin, probenesid ve simetidin gibi levofloksasinin tübüler böbrek sekresyonunu azaltan ilaçlarla birlikte uygulandığında, özellikle böbrek yetmezliği olan hastalarda dikkatli olunmalıdır. Probenesid ve simetidin, levofloksasinin eliminasyonu üstünde istatistiksel olarak önemli ölçüde etki yapmaktadır. Levofloksasinin renal klirensi, simetidin ile % 24 oranında probenesid ile % 34oranında azalmaktadır. Bunun nedeni her iki ilacın da levofloksasinin renal tübüler sekresyonunubloke etmesidir. Ancak yapılan çalışmada incelenen dozlarda, istatistiksel olarak anlamlı görülenkinetik farklılıkların, klinik açıdan anlamlılık taşıması ihtimali yoktur. SiklosporinSiklosporinin yarı-ömrü, levofloksasin ile birlikte uygulandığında % 33 oranında artmaktadır. Bu durum klinik açıdan önemli olmadığı için, doz ayarlamasına gerek yoktur. K vitamini antagonistleriLevofloksasin ile birlikte, bir K vitamini antagonisti (örneğin varfarin) ile tedavi edilen hastalardaki pıhtılaşma testleri (PT/INR) ve/veya kanamada şiddetli olabilen artışlarbildirildiğinden, K vitamini antagonistleri ile tedavi edilen hastalarda pıhtılaşma testleri yakındantakip edilmelidir. Hastalar kanama belirtisi yönünden de dikkatli bir şekilde takip edilmelidir (Bkz. bölüm 4.4). QT aralığını uzattığı bilinen ilaçlarLevofloksasin diğer florokinolonlarda olduğu gibi, QT aralığını uzattığı bilinen ilaçları (örneğin Sınıf IA ve III antiaritmikler, trisiklik antidepresanlar, makrolidler, antipsikotikler) alanhastalarda dikkatli kullanılmalıdır (Bkz. bölüm 4.4, QT aralığının uzaması). Diğer klinik farmakoloji çalışmalarında, digoksin, glibenklamid, ranitidin, kalsiyum karbonat ile birlikte uygulanması halinde levofloksasinin farmakokinetiğinde klinikte önemi olabilecekherhangi bir değişiklik olmadığı gösterilmiştir. Bir farmakokinetik etkileşim çalışmasında levofloksasin teofilin (bir CYP1A2 substratı) farmakokinetiğini etkilememiştir; bu nedenle levofloksasin bir CYP1A2 inhibitörü değildir. 4.6 Gebelik ve laktasyonGenel tavsiyeGebelik kategorisi C'dir. Çocuk doğurma potansiyeli bulunan kadınlar/Doğum kontrolü (Kontrasepsiyon)Çocuk doğurma potansiyeli bulunan kadınlarda levofloksasinin kullanımıyla ilgili herhangi bir veri yoktur. Gebelik dönemiLevofloksasinin gebe kadınlarda kullanımına ilişkin yeterli veri mevcut değildir. LİEVO gebelik döneminde kontrendikedir. Hayvanlar üzerinde yapılan çalışmalar, gebelik ve/veya embriyonal/fetal gelişim ve/veya/doğum ve/veya doğum sonrası gelişim üzerindeki etkiler bakımından yetersizdir. (Bkz. bölüm 4.3 ve5.3). İnsanlara yönelik potansiyel risk bilinmemektedir. İnsanlarla ilgili verilerin yeterli olmaması 8/17ve florokinolonlarla yapılan deneysel çalışmalarda büyüyen organizmalarda ağırlık taşıyan kıkırdağa zarar verme riskinin gösterilmesi nedeniyle, LİEVO perfüzyon çözeltisi gebelikdöneminde kullanılmamalıdır. Laktasyon dönemiLİEVO emzirme döneminde kontrendikedir. Levofloksasinin insan ya da hayvan sütü ile atıldığına ilişkin yetersiz/sınırlı bilgi mevcuttur. Levofloksasinin süt ile atılmasına yönelik fizikokimyasal ve eldeki farmakodinamik/toksikolojikveriler nedeniyle emzirilen çocuk açısından bir risk olduğu göz ardı edilemez. Florokinolonlarlayapılan deneysel çalışmalarda büyüyen organizmalarda ağırlık taşıyan kıkırdağa zarar vermeriskinin gösterilmesi nedeniyle, LİEVO perfüzyon çözeltisi emzirme dönemindekullanılmamalıdır. (Bkz. bölüm 4.3 ve 5.3). Üreme yeteneği/FertiliteLİEVO'nun insanlar üzerindeki üreme yeteneğine ilişkin yeterli veri mevcut değildir. 4.7 Araç ve makine kullanımı üzerindeki etkilerLİEVO kullanımı, hastanın konsantrasyon ve tepki verme yeteneğini bozabilecek sersemlik/baş dönmesi, görme bozuklukları, uyuklama gibi bazı istenmeyen yan etkilere yol açabilir. Araç vemakine kullanımı gibi özel dikkat isteyen durumlarda bu yeteneklerdeki azalma bir risk teşkiledebilir. LİEVO kullanırken bu gibi yan etkiler yaşayan hastaların araç ve makine kullanmamasıgerekir. 4.8 İstenmeyen etkilerAşağıda verilen bilgiler 8300'den fazla hastanın katıldığı klinik araştırmalardan ve pazarlama sonrası deneyimlerden elde edilen verileri temel almaktadır. Çok yaygın (> 1/10); yaygın (> 1/100 ila < 1/10); yaygın olmayan (> 1/1.000 ila < 1/100); seyrek(> 1/10.000 ila < 1/1.000); çok seyrek (<1/10.000), bilinmiyor (eldeki verilerden hareketletahmin edilemiyor). Enfeksiyonlar ve enfestasyonlarYaygın olmayan: Kandida enfeksiyonu dahil mantar enfeksiyonları, patojen direnci Kan ve lenf sistemi hastalıklarıYaygın olmayan: Lökopeni, eozinofili Seyrek: Nötropeni, trombositopeni Bilinmiyor (pazarlama sonrası veriler): Pansitopeni, agranülositoz, hemolitik anemi Bağışıklık sistemi hastalıklarıSeyrek: Anjiyoödem, aşırı duyarlılık Bilinmiyor (pazarlama sonrası verileri): Anafilaktik şok, anafilaktoid şok. İlk dozdan sonra bile bazen anafilaktik ve anafilaksi benzeri reaksiyonlar meydana gelebilir (bkz. Bölüm 4.4). Metabolizma ve beslenme hastalıklarıYaygın olmayan: Anoreksi Seyrek: Özellikle diyabetli hastalarda hipoglisemi (bkz. Bölüm 4.4) Bilinmiyor: Hiperglisemi, hipoglisemik koma (bkz. Bölüm 4.4) Psikiyatrik hastalıklarYaygın: İnsomnia 9/17Yaygın olmayan: Anksiyete, konfüzyon durumu, sinirlilik Seyrek: Psikotik bozukluk (örn. halüsinasyon ve paranoya ile birlikte), depresyon, ajitasyon, anormal rüyalar, kabuslar Bilinmiyor (pazarlama sonrası veriler): İntihar düşünceleri ve intihar girişimi de dahil, kendine zarar verici davranışlarla birlikte psikotik reaksiyonlar Sinir sistemi hastalıklarıYaygın: Baş ağrısı, sersemlik Yaygın olmayan: Somnolans, tremor, tat duyusunda bozukluk (disguzi) Seyrek: Parestezi, konvülsiyonlar (bkz. Bölüm 4.4), Bilinmiyor (pazarlama sonrası veriler): Duyusal ve duyusal-motor periferik nöropati (bkz. Bölüm 4.4), diskinezi, ekstrapiramidal bozukluk, tat duyusu kaybı (aguzi), koku duyusu kaybı (anosmi)dahil koku alma bozuklukları (parosmi), senkop, benign intrakranial hipertansiyon Göz hastalıklarıSeyrek: Bulanık görüş dahil görme yeteneğinde bozulma Bilinmiyor: Geçici görme kaybı, üveit (Bkz. Bölüm 4.4) Kulak ve iç kulak hastalıklarıYaygın olmayan: Vertigo Seyrek: Kulak çınlaması Bilinmiyor: İşitme yeteneğinde bozulma, işitme kaybı Kardiyak hastalıklarSeyrek: Taşikardi, palpitasyon Bilinmiyor (pazarlama sonrası veriler): Kalp durmasıyla sonuçlanabilen Torsade de pointes, ventriküler aritmi, ventriküler taşikardi, elektrokardiyogramda QT aralığının uzaması (Bkz.bölüm 4.4, QT aralığı uzaması ve Bölüm 4.9). Vasküler hastalıklarYaygın: Flebit Seyrek: Hipotansiyon Solunum, göğüs bozuklukları ve mediastinal hastalıklarYaygın olmayan:Dispne Bilinmiyor (pazarlama sonrası veriler): Bronkospazm, alerjik pnömoni Gastrointestinal hastalıklarYaygın: Diyare, kusma, bulantı Yaygın olmayan: Karın ağrısı, dispepsi, flatulans, konstipasyon Bilinmiyor (pazarlama sonrası veriler): Hemorajik diyare -çok seyrek olgularda psödomembranöz kolit (Bkz. Bölüm 4.4) dahil, enterokolite işaret edebilir, pankreatit Hepato-biliyer hastalıklarYaygın: Karaciğer enzimlerinde artış (ALT/AST, alkalin fosfataz, GGT) Yaygın olmayan: Kanda bilirubin artışı Bilinmiyor (pazarlama sonrası veriler): Ağır karaciğer hasarı, sarılık Primer olarak altta yatan ciddi hastalığı bulunan hastalarda, levofloksasin ile bazen ölümcül olabilen akut karaciğer yetmezliği gelişen olgular rapor edilmiştir (Bkz. Bölüm 4.4), hepatit. Deri ve derialtı dokusu hastalıklarıYaygın olmayan: Kaşıntı, kızarıklık, ürtiker, hiperhidroz 10/17Bilinmiyor: Toksik epidermal nekroliz, Stevens-Johnson sendromu (Bkz. Bölüm 4.4), eritema multiforme, fotosensitivite reaksiyonu (Bkz. Bölüm 4.4), lökositoklastik vaskülit, stomatit.Bazen ilk dozu takiben bile mukokütanöz reaksiyonlar meydana gelebilir. Kas-iskelet bozuklukları, bağ dokusu ve kemik hastalıklarıYaygın olmayan: Artralji, miyalji Seyrek: Tendinit dahil tendon bozukluğu (Bkz. bölüm 4.4) (örneğin Aşil tendonunda gelişebilir), Myastenia Gravis'li hastalarda özel önem taşıyan kas güçsüzlüğü (Bkz. bölüm 4.4 MyasteniaGravis'in şiddetlenmesi) Bilinmiyor (pazarlama sonrası veriler): Rabdomiyoliz, tendon rüptürü (örn. Aşil tendonu) (Bkz. bölüm 4.4), ligament rüptürü, kas rüptürü, artrit Böbrek ve idrar yolu hastalıklarıYaygın olmayan: Kan kreatinin düzeyinin artması Seyrek: Akut böbrek yetmezliği (örn. interstisyel nefrite bağlı) Genel bozukluklar ve uygulama bölgesine ilişkin hastalıklarYaygın: Enfüzyon yapılan bölgede reaksiyon (ağrı, kızarıklık) Yaygın olmayan: Asteni Seyrek: Ateş Bilinmiyor: Ağrı (sırt, göğüs ve ekstremiteler) Florokinolon uygulanmasıyla ilişkili diğer istenmeyen etkiler:Çok seyrek: Porfiri hastalığı bulunanlarda porfiri atakları Şüpheli advers reaksiyonların raporlanması:Ruhsatlandırma sonrası şüpheli ilaç advers reaksiyonların raporlanması büyük önem taşımaktadır. Raporlama yapılması, ilacın yarar / risk dengesinin sürekli olarak izlenmesineolanak sağlar. Sağlık mesleği mensuplarının herhangi bir şüpheli advers reaksiyonu TürkiyeFarmakovijilans Merkezi (TUFAM)'ne bildirmeleri gerekmektedir (www.titck.gov.tr[email protected];4.9 Doz aşımı ve tedavisiBelirtiler: Hayvanlarda yapılan toksisite çalışmalarına göre LİEVO perfüzyon çözeltisinin akut aşırı dozu durumunda beklenmesi gereken en önemli işaretler konfüzyon, sersemlik, bilinç bozukluğu vekonvülsif nöbetlerdir. Konfüzyon durumu, konvülzsiyon, halüsinasyon ve tremoru da içerenmerkezi sinir sistemi etkileri, pazarlama sonrası deneyimlerde gözlenmiştir. Gastrointestinalsistemle ilgili reaksiyonlar bulantı ve mukoza erozyonlarıdır. Supra terapötik dozlarla yapılanklinik farmakoloji çalışmalarında QT aralığında uzama görülmüştür. Tedavi: Aşırı doz durumunda hasta dikkatle izlenmeli, QT aralığında uzama ihtimali olduğundan EKG takibi yapılmalı ve semptomatik tedavi uygulanmalıdır. Mide mukozasının korunması içinantasidler uygulanabilir. Hemodiyaliz, peritoneal diyaliz veya sürekli ambulatuvar peritoneal diyaliz, levofloksasinin vücuttan uzaklaştırılmasında etkili değildir. Spesifik bir antidotu yoktur. 11/175. FARMAKOLOJİK ÖZELLİKLER5.1 Farmakodinamik özelliklerFarmakoterapötik grup: Kinolon antibakteriyeller, florokinolonlar ATC Kodu: J01MA12 Levofloksasin florokinolon sınıfından sentetik bir antibakteriyel ilaçtır. Rasemik ilaç maddesi olan ofloksasin'in, (s) - enantiomeridir. Etki mekanizması Bir florokinolon antibakteriyel ilaç olarak levofloksasin, DNA giraz kompleksi ve topoizomeraz IV üzerine etki yapar. Antibakteriyel spektrumu Direnç oranları coğrafik olarak ve seçilen suş için zamana bağlı olarak değişebilir ve direnç paternleri için lokal bilgiler, özellikle şiddetli enfeksiyonların tedavisinde göz önündebulundurulmalıdır. Aşağıdaki bilgiler Ağustos 2012 itibariyle Avrupa harmonizasyon verilerini yansıtmaktadır. 12/17
DirençLevofloksasine direnç, tip II topoizomeraz, DNA giraz ve topoizomeraz IV hedef bölge mutasyonlarıyla, aşamalı bir süreç sonucunda kazanılır. Permeasyon bariyeri (Pseudomonas aeruginosa'dasıktır) ve pompa mekanizmaları gibi diğer direnç mekanizmaları da levofloksasineduyarlılığı etkileyebilir.Levofloksasin ve diğer florokinolonlar arasında çapraz direnç gözlenmiştir. Etki mekanizması nedeniyle genel olarak levofloksasin ve diğer antibakteriyal ilaç sınıfları ile arasında çaprazdirenç yoktur. Sınır değeriAvrupa Antimikrobik Duyarlılık Testleri Komitesi (EUCAST) tarafından çok duyarlı ile duyarlı ve orta derecede duyarlı ile dirençli organizmaları ayırmak amacıyla levofloksasin için önerilenMİK sınır değerleri aşağıdaki tabloda sunulmaktadır (MİK testi -mg/l). Levofloksasin için EUCAST klinik MİK sınır değerleri (versiyon 2.0, 2012-01-01):
13/171. Levofloksasin sınır değerleri yüksek doz tedavi ile ilişkilidir. 2. Düşük düzeyli florokinolon direnci (siprofloksasin MİK 0.12-0,5 mg/l) ortaya çıkabilir fakatbu direncin H. influenzae.ile gelişen solunum yolu enfeksiyonlarında klinik önemine ilişkinkanıt bulunmamaktadır3. Duyarlı sınır değerleri üzerinde MİK değerine sahip suşlar çok nadirdir ya dabildirilmemiştir. Bu izolatlardan herhangi birinde yapılan tanıma ya da antimikrobiyalduyarlılık testleri tekrarlanmalıdır ve sonuç doğrulanırsa izolat referans laboratuvarınagönderilmelidir. Güncel direnç sınır değeri üzerindeki MİK değerine sahip olduğudoğrulanmış izolatların klinik yanıt ile ilişkili kanıtı ortaya çıkana dek dirençli olarakbildirilmelidir. 4. Sınır değerleri oral 500 mg x 1 - 500 mg x 2 ve intravenöz 500 mg x 1 - 500 mg x 2 dozları için geçerlidir._Direnç prevalansı coğrafik olarak ve seçilmiş türlerin zamanına göre değişebilir. Özellikle şiddetli enfeksiyonların tedavisinde lokal direnç bilgisi gereklidir. Gerektiğinde, ilacınkullanımının en azından bazı enfeksiyonlarda sorgulandığı durumlarda lokal direnç prevalansıiçin uzman görüşü alınmalıdır. 5.2 Farmakokinetik özelliklerGenel özelliklerEmilim:Oral yoldan verilen levofloksasin 1-2 saat içinde pik plazma konsantrasyonlarının elde edilmesiyle hızla ve neredeyse tamamen absorbe olur (Tek doz 500 mg levofloksasinin ardındanCmax: 5.2+/-1,2 mcg/ml'dir). Mutlak biyoyararlanımı %99-100'dür. Levofloksasin 50 ila 1000mg aralığında doğrusal farmakokinetik özellik gösterir. Günde tek veya iki doz 500 mg'ın alınmasından 48 saat sonra sabit duruma ulaşır. Günde veya iki günde bir uygulanan multipl oral veya IV 500 mg doz uygulamasının 10. gündeki doruk ve çukur plazma konsantrasyonlarını gösteren tablo aşağıdadır:
Levofloksasinin emilimi üzerinde gıdaların küçük bir etkisi vardır. Dağılım:Tek doz ve tekrarlayan 500 mg ve 750 mg dozlarının uygulanmasından sonra, vücut dokularına yaygın dağılım gösteren levofloksasinin ortalama dağılım hacmi yaklaşık 100 l'dir.Levofloksasinin yaklaşık %30-40'ı serum proteinlerine bağlanmış durumdadır. 14/17Dokulara ve vücut sıvılarına geçiş: Bronşial Mukoza, Epitelyal Mukus Sıvısına ve Alveaolar Makrofajlara PenetrasyonTek doz 500 mg p.o. dozdan sonra bronşial mukozada ve epitelyal mukus sıvısında maksimum levofloksasin konsantrasyonları sırasıyla 8,3 gg/g ve 10,9 gg/ml olup mukozadan ve epitelmukus sıvısından seruma penetrasyon oranları sırasıyla 1,1- 1,8 ve 0,8- 3'tür. Bu düzeylere,sırasıyla, verildikten yaklaşık 1 saat veya 4 saat sonra ulaşılmıştır. 5 gün boyunca 500 mg ve 750 mg oral uygulamanın ardından, son uygulamadan 4 saat sonraki epitelyal mukus sıvısında ortalama konsantrasyonlar sırasıyla 9,94 mcg/ml ve 22,12 mcg/ml'dir.Alveolar makrofajda sırasıyla 97,9 mcg/ml ve 105,1 mcg/ml'dir. Akciğer Dokusuna Penetrasyon500 mg p.o. dozdan sonra akciğer dokusundaki maksimum levofloksasin konsantrasyonları 11,3 |ig/g'dır ve bu düzeylere, verildikten yaklaşık 4-6 saat sonra ulaşılmış olup akciğer dokusundanplazmaya dağılım oranı 2-5'tir. Bül Sıvısına Penetrasyon3 gün boyunca 500 mg'lık dozun günde bir veya iki kez verilmesinden 2-4 saat sonra, bül sıvısı içinde sırasıyla 4,0 ve 6,7 Ag/ml'lik maksimum levofloksasin konsantrasyonlarına ulaşılmış olupbül sıvısı/plazma oranı yaklaşık 1'dir. Kemik Dokusuna DağılımLevofloksasin proksimal ve distal femurdaki kortikal ve süngerimsi dokuya penetrasyon oranları 0,1'den 3'e olmak üzere iyi şekilde penetre olur. 500 mg p.o.'nun ardından spongios proksimalfemurdaki maksimum levofloksasin konsantrasyonu uygulamadan 2 saat sonra yaklaşık 15,1mcg/g'dır. Serebro-Spinal Sıvıya PenetrasyonLevofloksasinin serebro-spinal sıvıya geçişi düşüktür.Prostat dokusuna dağılımGünde 3 kez oral 500 mg levofloksasin uygulanmasından sonra prostat dokusundaki konsantrasyonu ortalama 2 saatten sonra 8,7 gg/g ve ortalama prostat/plazma konsantrasyonu1,84'dür. İdrardaki Konsantrasyonu150 mg, 300 mg veya 500 mg'lık oral tek dozdan sonra levofloksasinin ortalama idrar konsantrasyonları sırasıyla 44 mg/L, 91 mg/L ve 200 mg/L'dir. Biyotransformasyon:Levofloksasin çok az düzeyde metabolize olur, metabolitleri desmetil-levofloksasin ve levofloksasin N-oksittir. Metabolitler, idrarda atılırlar ve dozun <%5'ini oluştururlar.Levofoksasin stereokimyasal olarak stabildir ve izomerik dönüşüme uğramaz. Eliminasyon:Levofloksasin oral ve intravenöz verilmesini takiben, plazmadan göreceli olarak yavaş elimine olur (t1/2: 6 - 8 saat). Ekskresyonu esas olarak renal yoldandır (verilen dozun >%85'i). 500 mgtek dozu takiben levofloksasinin ortalama total vücut klirensi 175 +/- 29,2 ml/dak.'dır. 750 mg tek dozu takiben levofloksasinin ortalama total vücut klirensi 143 +/- 29,1 ml/dak.'dır. 15/17Levofloksasinin intravenöz ve oral uygulanmasında temel farmakokinetik farklılık yoktur, bu oral ve intravenöz yolların birbirinin yerine geçebileceğini düşündürmektedir. Doğrusallık/Doğrusal olmayan durum:150-600 mg doz aralığında, levofloksasin doğrusal bir farmakokinetik izler. Hastalardaki karakteristik özelliklerBöbrek yetmezliği olan hastalar:Böbrek yetmezliğinde levofloksasinin farmakokinetik özellikleri etkilenir. Böbrek fonksiyonlarının azalmasıyla birlikte, böbreklerden eliminasyonu ve klirensi düşer ve aşağıdakitabloda gösterildiği gibi, eliminasyon yarı ömrü uzar:
Yaşlı hastalar:Levofloksasinin farmakokinetik özellikleri, kreatinin klirensindeki farklılıklarla alakalı olanlar dışında, yaşlılarla gençler arasında önemli değişiklikler göstermez. Cinsiyet farklılıkları:Kadın ve erkeklerde yapılan ayrı analizler neticesinde levofloksasinin farmakokinetik özelliklerinde cinsiyetler arasında çok küçük marjinal farklılıklar olduğu gösterilmiştir. Bufarkların klinik açıdan anlamlı olduğuna dair herhangi bir kanıt yoktur. 5.3. Klinik öncesi güvenlilik verileriKlinik öncesi veriler tek doz toksisitesi, tekrarlayan doz toksisitesi, karsinojenik potansiyel ve üreme/gelişme toksisitesini içeren geleneksel çalışmalar temelinde insanlar için özel bir zararsaptamamıştır. Levofloksasin sıçanlarda fertilite ya da üreme performansında bozukluğa yol açmamıştır ve fetüs üzerindeki tek etkisi maternal toksisiteye bağlı olan gelişme geriliğidir. Levofloksasin bakteri ya da memeli hücrelerinde gen mutasyonuna yol açmamıştır fakat Çinli hamster akciğer hücrelerinde in vitroİn vivotestlerde (mikronükleus, kardeş kromatiddeğişimi, plansız DNA sentezi, dominant letal testler) genotoksik potansiyel göstermemiştir.Farelerde yürütülen çalışmalar levofloksasinin yalnızca çok yüksek dozlarda fototoksik aktiviteye sahip olduğunu göstermiştir. Levofloksasin fotomutajenite tayininde genotoksikpotansiyel göstermemiştir ve bir fotokarsinojenite çalışmasında tümör gelişimini azaltmıştır. Diğer florokinolonlar gibi levofloksasin sıçan ve köpeklerde kıkırdak üzerinde etki (soyulma ve boşluk oluşumu) göstermiştir. Bu etkiler genç hayvanlarda daha belirgin olmuştur. 6. FARMASÖTİK ÖZELLİKLER6.1 Yardımcı maddelerin listesiSodyum klorür Hidroklorik asitEnjeksiyonluk su 16/176.2 GeçimsizliklerLİEVO iv, aşağıdaki infüzyon solüsyonları ile uyumludur: %0,9 sodyum klorür çözeltisi%5 dekstroz çözeltisi% 2,5 dekstroz, Ringer çözeltisi içinde parenteral beslenme için hazırlanmış kombinasyon çözeltileri (amino asitler, karbonhidratlar, elektrolitler) LİEVO, heparin veya alkali çözeltilerle (örn. sodyum hidrojen karbonat) karıştırılmamalıdır. 6.3 Raf ömrü24 ay 6.4 Saklamaya yönelik özel tedbirler25oC'nin altındaki oda sıcaklığında ve ambalajında saklayınız. Işıktan koruyunuz. Ambalajından çıkarıldıktan sonra oda ışığında dayanma Süresi 3 gündür. LİEVO, %0.9 NaCl, %5 dekstroz,%2.5 ringer solüsyonu ve parenteral beslenme solüsyonları (amino asit, karbonhidrat, elektrolit)içinde 24 saat stabildir. 6.5 Ambalajın niteliği ve içeriği100 ml steril çözelti içeren, bromobütil lastik tıpa ve alüminyum flip-off kapak ile kapatılan, tip I renksiz cam flakonlarda, 1 flakonluk ambalaj boyutu ile piyasaya sunulmaktadır 6.6 Beşeri tıbbi üründen arta kalan maddelerin imhası ve diğer özel önlemlerKullanılmamış olan ürünler ya da atık materyaller Tıbbi Atıkların Kontrolü Yönetmeliği ve Ambalaj ve Ambalaj Atıklarının Kontrolü Yönetmeliklerine uygun olarak imha edilmelidir. 7. RUHSAT SAHİBİNinova Ecza Deposu İthalat İhracat Ltd. Şti. Bahçelievler Mah. Taşkent Cad. No: 58/A Çankaya-ANKARA Tel: 0 312 214 10 69 Fax: 0 312 214 10 69 8. RUHSAT NUMARASI2022/283 9. İLK RUHSAT TARİHİ/RUHSAT YENİLEME TARİHİİlk ruhsat tarihi: 24/05/2022 Ruhsat yenileme tarihi: - 10. KÜB'ÜN YENİLENME TARİHİ17/17 |
İlaç BilgileriLievo 500mg/100ml Iv Perfüzyonluk Çözelti İçeren FlakonEtken Maddesi: Levofloksasin Hemihidrat Kullanma talimatı ve kısa ürün bilgileri
Google Reklamları
İlgili İlaçlar |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
Ana Sayfa | Hakkımızda | İlaçlar | İlaç Ara | İlaç Firmaları | Gizlilik | Bize Ulaşın
Telif Hakkı 2008-2026 © İlaç Prospektüsü. Tüm Hakları Saklıdır.Uyarı: Sitemizde yayınladığımız ilaç bilgileri ile doktora danışmadan kesinlikle ilaç kullanmayınız!
Aksi halde doğabilecek sağlık sorunlarından ilacprospektusu.com sorumlu tutulamaz.