Fludalt Duo 50 Mcg/ 500 Mcg İnhalasyon İçin Toz İçeren Kapsül Kısa Ürün BilgisiKISA ÜRÜN BİLGİSİ1. BEŞERİ TIBBİ URUNUN ADIFLUDALT DUO 50 mcg / 500 mcg İnhalasyon için Toz İçeren Kapsül 2. KALİTATİF VE KANTİTATİF BİLEŞİMEtkin madde :72.5 mcg 500 mcg Her bir inhalasyon kapsülü içinde Salmeterol ksinafoat * Flutikazon propiyonat *50 mcg salmeterole eşdeğer Yardımcı maddelerLaktoz............................................11,9275 mg (inek sütünden elde edilir.) Yardımcı maddeler için Bölüm 6.1' e bakınız. 3. FARMASÖTİK FORMİnhalasyon için Toz İçeren Kapsül Renksiz kapsül içinde beyaz ya da beyazımsı toz 4. KLİNİK ÖZELLİKLER4.1 Terapötik endikasyonlarAstım semptomlarının düzeltilmesi ve kontrol altına alınması amacıyla kullanılır. Astım hastalığının basamaklı tedavisinde 3.basamaktan itibaren verilir. Orta ve ağır KOAH olgularında semptomları veatak sıklığını azaltır. 4.2 Pozoloij ve uygulama şekliPozoloji/uygulama sıklığı ve süresi :FLUDALT DUO sadece inhalasyon yolu ile uygulanır. Hastalar, belirtileri olmasa dahi optimum fayda için FLUDALT DUO'yu düzenli olarak kullanmaları gerektiği konusunda uyarılmalıdır. Hastaların düzenli doktor kontrolünde bulundurularak aldıkları FLUDALT DUO dozunun optimum düzeyde kalması sağlanmalı ve sadece doktor önerisi ile değiştirilmelidir. Alternatif olarak, uzun süre etkili beta2 agonist kullanması gereken hastalarda FLUDALT DUO, reçete eden hekimin görüşüne göre hastalık kontrolünün sağlanmasında yeterli olacağıdüşünülüyorsa günde bir kez olacak şekilde de titre edilebilir. Hastada gece görülen semptomöyküsü varsa ve günde bir kez dozlam uygulanıyorsa doz geceleri verilmeli; hastada genellikle Belg e Doğrulama Kodu: lZW56aklUQ3NRZl AxZl AxZmxXZmxXS3kO 1 Belge Takip Adresi:https://www.turkiye.gov.tr/saglik-titck-ebys gündüz görülen semptom öyküsü varsa doz sabahları verilmelidir. AstımDoz, belirtileri etkili olarak kontrol eden en düşük doza ayarlanmalıdır. Günde 2 kez uygulanan FLUDALT DUO ile belirtilerin kontrolü sağlandığında, etkili en düşük doz açısından, günde 1 kezuygulanan FLUDALT DUO' da değerlendirmeye dahil edilebilir. Hastalara hastalıklarının şiddetine göre uygun flutikazon propiyonat dozu içeren FLUDALT DUO verilmelidir. Eğer hasta yalnız inhale kortikosteroid tedavisi ile yeterli derecede kontrol edilemiyorsa tedavinin terapötik olarak eşdeğer kortikosteroid dozunda FLUDALT DUO ile değiştirilmesi astımkontrolünde düzelme sağlayabilir. Astımı yalnız inhale kortikosteroid tedavisi ile yeterli derecedekontrol edilebilen hastalarda tedavinin FLUDALT DUO ile değiştirilmesi astım kontrolünüsürdürürken kortikosteroid dozunun azaltılmasını sağlayabilir. Daha ayrıntılı bilgi için lütfenFarmakodinamik özellikler bölümüne bakınız. Tavsiye edilen dozlarYetişkinler, 12 yaş ve üzeri adolesanlar:Günde 2 kez 1 inhalasyon (50 mikrogram salmeterol ve 100 mikrogram flutikazon propiyonat) veya günde 2 kez 1 inhalasyon (50 mikrogram salmeterol ve 250 mikrogram flutikazon propiyonat) veyagünde 2 kez 1 inhalasyon (50 mikrogram salmeterol ve 500 mikrogram flutikazon propiyonat) Hızlı şekilde kontrol edilmesi gereken, orta dereceli inatçı astımı olan erişkin veya adolesan hastalarda (hastanın günlük semptomlarına, günlük kurtarma ilacı kullanımına ve orta ila şiddetlihavayolu sınırlamasına göre tanımlanır) kısa süreli FLUDALT DUO uygulaması başlangıç tedavisiolarak kabul edilebilir. Bu durumlarda, önerilen başlangıç dozu günde iki kez iki inhalasyon olarak50 mikrogram salmeterol ve 100 mikrogram flutikazon propiyonattır. Astım kontrolü sağlandığında,tedavi tekrar gözden geçirilmeli ve hastaların, tek başına inhale kortikosteroid alacak şekilde dozunazaltılması düşünülmelidir. Tedavide doz azaltılırken hastaların düzenli olarak takip edilmesiönemlidir. Bir veya iki hastalık şiddeti kriteri eksik olduğunda, başlangıç tedavisi olarak tek başına inhale flutikazon propiyonat kullanımına kıyasla net bir yarar gösterilmemiştir. Genel olarak inhalekortikosteroidler hastaların büyük çoğunluğunda birinci basamak tedavi olmaya devam etmektedir.FLUDALT DUO'nun hafif astımın ilk tedavisinde kullanımı amaçlanmamaktadır. FLUDALT DUO50 mikrogram /100 mikrogram dozları, şiddetli astımı olan çocuklarda ve erişkinlerde kullanımauygun değildir; şiddetli astım hastalarında herhangi bir sabit kombinasyonun kullanılmasından önceuygun inhale kortikosteroid dozunun gösterilmesi önemlidir. Kronik Obstrüktif Akciğer Hastalığı (KOAH)Yetişkin hastalar için tavsiye edilen doz günde 2 kez 1 inhalasyon 50/250 mikrogram-50/500 mikrogram salmeterol/flutikazon propiyonattır. Uygulama şekli :FLUDALT DUO sadece inhalasyon yoluyla kullanılır. Bu belge Belge Do Hastalara inhalerlerini doğru şekilde kullanmaları için bilgi verilmelidir. İnhalasyon sırasında, hastanın tercihen ayakta veya dik oturur konumda olması gerekir. Özel popülasyonlara ilişkin ek bilgiler:Böbrek yetmezliği :Böbrek yetmezliği olan hastalarda dozun ayarlanmasına gerek yoktur. Karaciğer yetmezliği:Karaciğer yetmezliği olan hastalarda FLUDALT DUO kullanımına ilişkin bilgi yoktur. Pediyatrik popülasyon :4 -12 yaş arası çocuklarda: Günde 2 kez 1 inhalasyon (50 mikrogram salmeterol ve 100 mikrogram flutikazon propiyonat). 4 yaşından küçük çocuklarda FLUDALT DUO kullanımı ile ilgili bilgi yoktur. Geriyatrik popülasyon :Yaşlı hastalarda doz ayarlanmasına gerek yoktur. 4.3 KontrendikasyonlarFLUDALT DUO, etkin madde veya yardımcı maddelerden herhangi birine karşı aşırı duyarlılığı olan hastalarda kontrendikedir (bkz. Bölüm 6.1) 4.4 Özel kullanım uyarıları ve önlemleriEtkin maddelerden salmeterol, astımlı hastalarda tek başına monoterapi olarak kullanılmamalıdır. FLUDALT DUO astım hastalığının başlangıç tedavisi için önerilmez. Hastalığın kötüleşmesiFLUDALT DUO'nun içeriğinde bulunan salmeterol gibi uzun etkili P 2agonistler kullanılırken, özellikle astım ile ilgili advers olaylar bakımından, bu ilaç başlandıktan sonra ilk üç ay hastalaryakından takip edilmelidir.FLUDALT DUO hızlı ve kısa etkili bir bronkodilatörün (örneğin salbutamol) kullanımını gerektiren akut belirtileri rahatlatmak için kullanılmamalıdır. Hastalara akut astım ataklarında rahatlamak içinkullanmaları gereken ilaçları her zaman yanlarında bulundurmaları tavsiye edilmelidir. Hastalar alevlenme dönemlerinde ise ya da önemli ölçüde veya akut olarak kötüye giden astım şikayetleri varsa, uzun etkili beta agonistlerle tedaviye başlanmamalıdır. FLUDALT DUO ile tedavi sırasında astımla ilişki ciddi adves etkiler veya alevlenmeler gerçekleşebilir. Hastalara, FLUDALT DUO tedavisine başladıktan sonra astım semptomları kontrolaltına alınamaz veya kötüleşirse tedaviye devam etmeleri, ancak yine de hekimlerine danışmaları Bu belge Belg e Doğrulama Kodu: lZW56aklUQ3NRZl AxZl AxZmxXZmxXS3kO 3 Belge Takip Adresi:https://www.turkiye.gov.tr/saglik-titck-ebys gerektiği anlatılmalıdır. Rahatlatıcı ilaç (kısa etkili bronkodilatörler) kullanımı gereksinimlerinde artış veya rahatlatıcı ilaçlara yanıtta azalma astım kontrolünde bozulmaya işaret eder ve hastalar bir hekim tarafındandeğerlendirilmelidir. Uzun etkili beta agonist preparatlarına bağlı olarak nadiren, ciddi ve bazen ölümcül olabilen astım ile ilgili solunum problemleri meydana gelebilir. İnhale kortikosteroide ek olarak uzun etkili beta agonist kullanan pediatrik ve adolesan hastalarda, her iki ilaca uyumu garanti altına almak için, hem inhale kortikosteroid hem de uzun etkili betaagonist içeren bir kombinasyon preparatı kullanılması önerilir. Uzun etkili beta agonistler astım semptom kontrolünü sağlayan en kısa süre boyunca kullanılmalı ve astım kontrolüne ulaşıldığında eğer mümkünse kullanımları durdurulmalıdır. Sonrasında hastalarınkontrol edici bir tedaviyle idamesi sağlanmalıdır. Astım kontrolünün ani ve ilerleyen şekilde kötüleşmesi hayatı tehdit eden bir durumdur ve hastanın hekim tarafından tekrar muayene edilmesi gereklidir. Kortikosteroid dozunun artırılmasıdüşünülmelidir. Astım semptomları kontrol altına alındığında, FLUDALT DUO dozunun kademeli olarak azaltılması değerlendirilebilir. Tedavi kademeli olarak azaltılırken hastaların düzenli olarak kontrol edilmesiönemlidir. FLUDALT DUO'nun etkili en düşük dozu kullanılmalıdır (bkz. Bölüm 4.2). Alevlenme yaşayan KOAH hastalarında genellikle sistemik kortikosteroid kullanımı endikedir, bu nedenle FLUDALT DUO ile semptomlar kötüleşirse hastaların hekimlerine danışmaları gerektiğianlatılmalıdır. Astımlı hastalarda alevlenme riski nedeniyle FLUDALT DUO tedavisi ani olarak kesilmemelidir, tedavi dozu hekim gözetiminde kademeli olarak azaltılmalıdır. KOAH'lı hastalarda tedavininkesilmesine semptomatik dekompanzasyon eşlik edebilir ve tedavinin kesilmesi bir hekimgözetiminde yapılmalıdır. Kortikosteroid içeren tüm inhale ilaçlarla olduğu gibi, aktif veya sessiz akciğer tüberkülozu olan hastalarda ve mantar, virüs ya da diğer solunum yolu enfeksiyonları olan hastalarda FLUDALT DUOdikkatli kullanılmalıdır. Gerekli olduğu takdirde uygun tedavi derhal başlatılmalıdır. Kardiyovasküler etkilerYüksek terapötik dozlarda FLUDALT DUO, seyrek olarak kardiyak aritmilere (örn. supraventriküler taşikardi, esktrasistoli ve atriyal fibrilasyon) ve serum potasyum seviyesinde geçici hafif azalmalaraneden olabilir. Ciddi kardiyovasküler bozuklukları veya kalp ritm bozuklukları olan hastalarda vediabetes mellitus, tirotoksikozis, tedavi edilmemiş hipokalemi veya düşük serum potasyumseviyesine predispoze hastalarda FLUDALT DUO dikkatli kullanılmalıdır. HiperglisemiÇok seyrek olarak kan glukoz düzeylerinde artış rapor edilmiştir (bkz. Bölüm 4.8) ve diabetes mellitus öyküsü olan hastalara reçete edilirken bu husus göz önünde bulundurulmalıdır. Bu belge Belge Do Paradoksal bronkospazmDiğer inhalasyon tedavilerinde olduğu gibi, doz uygulamasından hemen sonra başlayan hırıltı artışı ve nefes darlığı ile birlikte paradoksal bronkospazm ortaya çıkabilir. Paradoksal bronkospazm, hızlıetkili bronkodilatöre yanıt verir ve hemen tedavi edilmelidir. FLUDALT DUO derhal kesilmeli, hastadeğerlendirilmeli ve gerekli ise alternatif tedaviye başlanmalıdır. P 2agonist tedavisinin tremor, çarpıntılar ve baş ağrısı gibi farmakolojik yan etkileri bildirilmiştir fakat bunlar geçici olma ve düzenli tedaviyle birlikte azalma eğilimindedir.Sistemik kortikosteroid etkilerHerhangi bir inhale kortikosteroid özellikle yüksek dozlarda, uzun süre kullanıldığında sistemik etkiler oluşabilir. Oral kortikosteroid uygulamasına göre bu etkilerin oluşma olasılığı çok daha azdır(bkz. Bölüm 4,9). Olası sistemik etkiler; Cushing sendromu, Cushing benzeri belirtiler, adrenalsupresyon, çocukların ve adolesanların büyümesinde gecikme, kemik mineral dansitesinde azalma,katarakt ve glokom ile daha seyrek olarak psikomotor hiperaktivite, uyku bozukluğu, anksiyete,depresyon ve agresyon (özellikle çocuklarda) gibi psikolojik ve davranışsal etkileri içerir. Bunedenle, astımı olanlarda inhale kortikosteroid dozunun, etkili kontrolü sağlayan en düşük dozaayarlanması önemlidir. Hastaların yüksek dozlarda inhale kortikosteroidlerle uzun süreli tedavisi adrenal supresyon ve akut adrenal krize neden olabilir. 500 ila 1000 mikrogram flutikazon propiyonat dozlarında çok seyrekolarak adrenal supresyon ve akut adrenal krizler ile ilgili bildirimler bulunmaktadır. Potansiyel olarakakut adrenal krizi tetikleyebilecek durumlar travma, cerrahi girişim, enfeksiyon veya dozda aniazalmalardır. Gözlenen semptomlar genellikle belirsiz olmakla birlikte anoreksi, karın ağrısı, kilokaybı, yorgunluk, baş ağrısı, bulantı, kusma, hipotansiyon, bilinç seviyesinde azalma, hipoglisemi venöbettir. Stres veya elektif cerrahi girişim sırasında ilave sistemik koritkosteroid tedavisidüşünülmelidir. İnhale flutikazon propiyonat tedavisinin oral steroid ihtiyacını minimize etmesi beklenir, ancak oral steroidlerden transfer edilen hastalarda önemli bir süre adrenal yetmezlik riski olabilir. Bu nedenlebu tip hastaların yakından takip edilmesi ve adrenokortikol fonksiyonun izlenmesi gereklidir.Geçmişinde acil durum yüksek doz kortikosteroid tedavisi gereken hastalarda da bu risk mevcutolabilir. Stres yaratması muhtemel acil ve elektif durumlarda adrenal yanıt bozukluğu olasılığıdaima akılda tutulmalıdır ve uygun kortikosteroid tedavisi düşünülmelidir. Adrenal yetmezliğinderecesi elektif girişimlerden önce uzman değerlendirmesi gerektirebilir. Ritonavir, plazmadaki flutikazon propiyonat konsantrasyonunu büyük ölçüde artırabilir. Bu nedenle hastaya potansiyel yararı sistemik kortikosteroid yan etkilerinden fazla olmadığı sürece birliktekullanımdan kaçınılmalıdır. Flutikazon propiyonat'ın diğer güçlü CYP3A inhibitörleriyle birliktekullanımında da sistemik yan etki riski artar. KOAH hastalarında pnömoniKortikosteroid içeren inhale ilaçları alan KOAH hastalarında, hastaneye yatış gerektiren pnömoni dahil pnömoni insidansında artış gözlemlenmiştir. Artan steroid dozu ile pnömoni riskinde artışkanıtları bulunmaktadır, ancak bu durum çalışmaların tamamında kesin olarak gösterilmemiştir. Kortikosteroid içeren inhale ilaçların pnömoni riskinin büyüklüğü konusunda sınıf içi farklılık için y Bu oelge, güvenli eleKtronık imza ne imzalanmıştır. 0JJBelg e Doğrulama Kodu: lZW56aklUQ3NRZl AxZl AxZmxXZmxXS3kO 5 Belge Takip Adresi:https://www.turkiye.gov.tr/saglik-titck-ebys kesin klinik kanıt bulunmamaktadır. Hekimler, KOAH hastalarında olası pnömoni gelişimine karşı, enfeksiyonların klinik özellikleri ile KOAH semptomlarının alevlenme durumunun karışması ihtimali dolayısıyla dikkatliolmalıdırlar. KOAH hastalarındaki pnömoni risk faktörleri arasında; sigara içimi, ileri yaş, düşük vücut kitle indeksi ve şiddetli KOAH bulunmaktadır. CYP3A4 inhibitörleriyle etkileşimSistemik ketokonazol ile birlikte kullanımı salmetorol'ün sistemik maruziyetini ciddi ölçüde artırmaktadır. Bu durum sistemik etkilerin (örn. QTc aralığının uzaması ve palpitasyonlar)insidansında artışa neden olabilir. Bu nedenle hastaya olan potansiyel yararı sistemik salmeterol yanetkileri riskinden fazla olmadıkça CYP3A4 inhibitörleriyle birlikte kullanımından kaçınılmalıdır. Görme bozukluklarıSistemik ve topikal kortikosteroid kullanımında görme bozuklukları rapor edilebilir. Bir hastada bulanık görüş veya diğer görme bozukluğu şikayetleri varsa hasta, sistemik ve topikal kortikosteroidkullanımı sonrası bildirilen katarakt, glokom veya santral seröz korioretinopati (CSCR) gibi olasınedenlerin değerlendirilmesi için oftalmoloji uzmanına yönlendirilmelidir. Pediyatrik popülasyonYüksek doz flutikazon propiyonat (genellikle 1000mikrogram/gün veya daha fazla) alan 16 yaşın altındaki çocuklar ve ergenler risk altında olabilir. Özellikle yüksek dozlarda uzun süreli tedavidesistemik etkiler gerçekleşebilir. Olası sistemik etkiler; Cushing sendromu, Cushing benzeri belirtiler,adrenal supresyon, akut adrenal kriz, çocukların ve adolesanların büyümesinde gecikme ile dahaseyrek olarak psikomotor hiperaktivite, uyku bozukluğu, anksiyete, depresyon ve agresyondur.Çocuk veya ergen hastanın pediyatrik solunum uzmanına sevk edilmesi düşünülmelidir. Uzun süre inhale kortikosteroid tedavisi alan çocukların boyunun düzenli olarak izlenmesi tavsiye edilmektedir.İnhale kortikosteroid astım kontrolünü sağlayan en düşük dozda kullanılmalıdır. Yardımcı madde: FLUDALT DUO'nun her bir dozu 11,9275 miligrama kadar laktoz monohidrat içerir. Bu miktar, laktoz intoleransı olan kişilerde normalde bir probleme neden olmamaktadır. Laktoz yardımcımaddesi küçük miktarlarda süt proteini içerir ve bu alerjik reaksiyonlara neden olabilir. 4.5 Diğer tıbbi ürünlerle etkileşimler ve diğer etkileşim şekilleriP adrenerjik blokörler salmeterolün etkisini zayıflatabilir veya antagonize edebilir. Astımlı hastalarda kullanımları için gerekli nedenler olmadığı sürece hem selektif olmayan hem de selektif P blokörlerinkullanımından kaçınılmalıdır. P2 agonist tedavisiyle potansiyel olarak ciddi hipokalemigerçekleşebilir. Akut şiddetli astımda, bu etki ksantin türevleri, steroidler ve diüretikler ile eşzamanlıtedavi ile artabileceğinden özel dikkat tavsiye edilir. Diğer P adrenerjik içeren ilaçların eşzamanlı kullanımı potansiyel aditif etkiye sahip olabilir. Flutikazon Propiyonat Bu belge Belge Do Normal şartlar altında, inhalasyon yolu ile uygulanmasından sonra, geniş ilk geçiş metabolizması ve karaciğer ve bağırsakta sitokrom P450 3A4'ün aracılık ettiği yüksek sistemik klerens sonucu,flutikazon propiyonatın plazma konsantrasyonu düşüktür. Bu nedenle, flutikazon propiyonatınaracılık ettiği klinik olarak anlamlı ilaç etkileşimi olası değildir. Sağlıklı gönüllüler üzerinde yapılan bir ilaç etkileşim çalışması, günde 2 defa 100 mg ritonavirin (oldukça güçlü sitokrom CYP3A4 inhibitörü), flutikazon propiyonatın plazma konsantrasyonlarınıbirkaç yüz kat artırabildiğini ve serum kortizol konsantrasyonlarında anlamlı azalmaya yol açtığınıgöstermiştir. İnhale flutikazon propiyonat için bu etkileşime dair bilgi bulunmamaktadır, ancakflutikazon propiyonat plazma seviyeslerinde anlamlı artış beklenmektedir. Cushing sendromu veadrenal supresyon vakaları bildirilmiştir. Bu nedenle, hastaya olan potansiyel yararı sistemikkortikosteroid yan etkileri riskinden fazla olmadıkça ritonavir ve flutikazon propiyonatın birliktekullanımından kaçınılmalıdır. Sağlıklı gönüllülerde yapılan küçük ölçekli bir çalışmada daha düşük potense sahip bir CYP3A inhibitörü olan ketokonazol tek inhalasyondan sonra flutikazon propiyonat maruziyetini % 150artırmıştır. Bu etki tek başına flutikazon propiyonata kıyasla plazma kortizol düzeyinde daha fazladüşüşe neden olmuştur. İtrakonazol ve kobisistat içeren ilaçlar gibi diğer potent CYP3A inhibitörlerive eritromisin gibi orta kuvvetli CYP3A inhibitörleri ile birlikte tedavinin de sistemik flutikazonpropiyonat maruziyetini ve sistemik yan etki riskini artırması beklenmektedir. Hastaya olanpotansiyel yararı sistemik kortikosteroid yan etkileri riskinden fazla olmadıkça, birlikte kullanımdankaçınılmalıdır. Birlikte kullanımda hastalar sistemik kortikosteroid yan etkileri açısından takipedilmelidir. Salmeterol Kuvvetli CYP3A4 inhibitörleri 15 sağlıklı gönüllüde 7 gün süreyle yürütülen bir ilaç etkileşim çalışmasında eşzamanlı sistemik ketokonazol (günde bir kez 400 mg) ve salmeterol (günde iki kez inhale 50 mikrogram)kullanımının plazma salmeterol maruziyetini anlamlı derecede artırdığı gözlenmiştir (Cmaks 1.4 katve EAA 15 kat). Bu durum, salmeterol tedavisinin diğer sistemik etkilerinin (örn. QTc aralığınınuzama ve palpitasyonlar) insidansının tek başına salmeterol veya ketokonazole tedavisi ilekarşılaştırıldığında artmasına neden olabilir. Kan basıncı, kalp hızı, kan glukoz ve kan potasyum düzeylerinde klinik açıdan anlamlı etkiler görülmemiştir. Ketokonazol ile birlikte uygulanımı salmeterol eliminasyon yarı ömrünü veyatekrarlı dozlamla salmeterol birikimini artırmamıştır. Tedavinin yararları salmeterolün artan sistemik yan etkiler riskinden yüksek olmadığı sürece ketokonazol ile eş zamanlı kullanımından kaçınılmalıdır. Diğer potent CYP3A4 inhibitörleri ile benzer bir etkileşimriskinin olması muhtemeldir (örn. itrakonazol, telitromisin, ritonavir). Orta düzeyde CYP 3A4inhibitörleri 15 sağlıklı gönüllüde 6 gün süreyle birlikte salmeterol (inhalasyon yoluyla günde iki kez 50 mikrogram) ve eritromisin (oral yolla günde bir kez 500 mg) uygulanımı salmeterol maruziyetindeküçük ancak istatistiksel açıdan anlamlı olmayan bir artışa neden olmuştur (Cmaks 1.4 kat ve EAA1.2 kat). Eritromisinin birlikte uygulanımı herhangi bir ciddi yan etki ile ilişkilendirilmemiştir. Özel popülasyonlara ilişkin ek bilgilerYaşlı hastalarda veya böbrek veya karaciğer yetmezliği olan hastalarda etkileşim çalışmaları yapılmamıştır (bkz. Bölüm 5.2). Bu belge Belge Do Pediyatrik popülasyon:Pediyatrik hastalarda etkileşim çalışmaları yapılmamıştır (bkz. Bölüm 5.2). 4.6 Gebelik ve laktasyonGenel tavsiyeGebelik kategorisi : C Çocuk doğurma potansiyeli bulunan kadınlar/Doğum kontrolü (Kontrasepsiyon)FLUDALT DUO'nun doğum kontrol yöntemleri üzerine etkisi olup olmadığına dair herhangi bir bilgi bulunmamaktadır. Gebelik dönemiFLUDALT DUO'nun gebe kadınlarda kullanımına ilişkin yeterli veri mevcut değildir. Hayvanlar üzerinde yapılan çalışmalar, gebelik ve/veya embriyonal/fetal gelişim ve/veya doğum ve/veya doğum sonrası gelişim üzerindeki etkiler bakımından yetersizdir (bkz Bölüm 5.3). İnsanlarayönelik potansiyel risk bilinmemektedir. Gebe kadınlardan elde edilen veriler (1000'den fazla gebe vakası) salmeterol ve flutikazon propiyonat malformasyon veya feto/neonatal toksisitesi göstermemektedir. Hayvan çalışmaları P 2adrenoreseptör agonistleri ve glukokortikosteroidlerin uygulamasından sonra üreme toksisitesigöstermiştir.İlaç kullanımı ancak anneye sağlaması beklenen yararı fetusa olan olası bir riskten fazla ise düşünülmelidir. Gebe kadınlarda flutikazon propiyonatın astım kontrolünü sağlayan etkili en düşük dozu kullanılmalıdır. Laktasyon dönemiSalmeterol ve flutikazon propiyonat/metabolitlerinin insan sütüne geçip geçmediği bilinmemektedir. Çalışmalar salmeterol ve flutikazon propiyonat ve metabolitlerinin emziren sıçanların sütüne geçtiğini göstermiştir. Emziren yenidoğan/bebeklerde risk göz ardı edilemez. Çocuğun emzirmesi ile tedavinin anneye faydaları değerlendirilerek FLUDALT DUO tedavisinin emzirmenin veya tedavinin bırakılmasınakarar verilmelidir. Üreme yeteneği / Fertiliteİnsanlarda kullanımına dair veri bulunmamaktadır. Ancak, hayvan çalışmaları salmeterol veya flutikazon tedavisinin fertilite üzerinde etkisi olmadığını göstermiştir. 4.7 Araç ve makine kullanımı üzerindeki etkilerFLUDALT DUO'nun araç ve makine kullanımı üzerinde etkisi yoktur veya göz ardı edilebilir düzeydedir. Belge Do 4.8 İstenmeyen etkilerFLUDALT DUO, salmeterol ve flutikazon propiyonat içerdiğinden her iki bileşenle de ilişkili olan tipte ve şiddette advers reaksiyonlar görülebilir. Bu iki bileşiğin birlikte verilmesiyle ilave advers etkibildirilmemiştir. Salmeterol/flutikazon propiyonat ile ilgili advers olaylar sistem organ sınıfına göre aşağıdaki sıklıklarda verilmiştir: Çok yaygın ( > 1/10 ), Yaygın ( > 1/100 ve < 1/10),Yaygın olmayan (> 1/1000 ve < 1/100) Seyrek (> 1/10000 ve < 1/1000) ve İzole raporlar dahil çok seyrek ( < 1/10000), bilinmiyor (eldekiverilerden hareketle tahmin edilemiyor) Enfeksiyonlar ve enfestasyonlarYaygın : Ağız ve boğazda kandidiyazis, pnömoni (KOAH hastalarında)1, 3 5 , bronşit1, 3 Seyrek : Özofajiyal kandidiyaz Bağışıklık sistemi hastalıklarıYaygın olmayan : Kütanöz duyarlılık reaksiyonları, solunum semptomları (dispne) Seyrek : Anjiyoödem (temelde yüzde ve orofarinksde ödem), solunum semptomları (bronkospazm), anafilaktik şok dahil, anafilaktik reaksiyonlar Endokrin hastalıklarıSeyrek4 : Cushing sendromu, Cushing benzeri özellikleri, adrenal süpresyonu, çocuklar ve adolesanlarda gelişim geriliği, azalan kemik mineral yoğunluğu Metabolizma ve beslenme hastalıklarıYaygın :Hipokalemi3 Yaygın olmayan : Hiperglisemi4 Psikiyatrik hastalıklarYaygın olmayan : Anksiyete, uyku bozuklukları Seyrek :Psikomotor hiperaktivite ve iritabilite dahil davranış değişiklikleri (çoğunlukla çocuklarda ) Bilinmiyor :Depresyon, huzursuzluk (çoğunlukla çocuklarda) Sinir sistemi hastalıklarıÇok yaygın : Baş ağrısı1 Yaygın olmayan : Tremor Göz hastalıklarıYaygın olmayanSeyrek Bilinmiyor :Katarakt :Glokom4:Bulanık görme4 Kardiyak hastalıklarYaygın olmayan : Palpitasyon, taşikardi, atrial fibrilasyon, anjina pektoris Bu belge Belge Do: Kardiyak aritmi ( supraventriküler taşikardi ve ekstrasistol dahil)
Seyrek Solunum, göğüs bozuklukları ve mediastinal hastalıklarÇok yaygın :Nazofarenjit2, 3 Yaygın :Boğaz irritasyonu, ses kısıklığı/disfoni, sinüzit1, 3 Seyrek :Paradoksal bronkospazm4 Deri ve deri altı doku hastalıklarıYaygın :Kontüzyonlar1, 3 Kas-iskelet bozuklukları, bağ doku ve kemik hastalıklarıYaygın : Kas krampları,travmatik kırıklar1, 3, artralji, miyalji 1Plaseboda yaygın olarak raporlanmıştır. 2Plaseboda çok yaygın olarak raporlanmıştır. 3Bir KOAH çalışmasında 3 yıldan fazla raporlanmıştır. 4Bölüm 4.4'e bakınız. 5Bölüm 5.1'e bakınız. Seçili advers olayların tanımıP 2agonist tedavisinin tremor, çarpıntılar ve baş ağrısı gibi farmakolojik yan etkileri bildirilmiştir fakat bunlar geçici olma ve düzenli tedaviyle birlikte azalma eğilimindedir.Diğer inhalasyon tedavilerinde olduğu gibi, doz uygulamasından hemen sonra başlayan hırıltı artışı ve nefes darlığı ile birlikte paradoksal bronkospazm ortaya çıkabilir. Paradoksal bronkospazm, hızlıetkili bronkodilatöre yanıt verir ve hemen tedavi edilmelidir. FLUDALT DUO derhal kesilmeli,hasta değerlendirilmeli ve gerekli ise alternatif tedaviye başlanmalıdır. Flutikazon propionat içeriği nedeniyle bazı hastalarda ses kısıklığı ağız ve boğaz ve seyrek vakalarda özofagus kandidiyazı (pamukçuk) görülebilir. Gerek ses kısıklığı gerekse ağız ve boğazkandidiyazı insidansı, ürün kullanıldıktan sonra ağız yıkanarak ve/veya dişler fırçalanarakgiderilebilir. Semptomatik ağız ve boğaz kandidiyazı, FLUDALT DUO tedavisi devam ederkentopikal anti-fungal terapi ile tedavi edilebilir. Özel popülasyonlara ilişkin ek bilgiler:Pediyatrik popülasyonOlası sistemik etkiler; Cushing sendromu, Cushing benzeri belirtiler, adrenal supresyon, çocukların ve adolesanların büyümesinde gecikmedir (bkz. Bölüm 4.4). Çocuklarda ayrıca anksiyete, uykubozukluğu ve hiperaktiviteyle iritabilite gibi davranışsal değişiklikler görülebilir. Şüpheli advers reaksiyonların raporlanmasıRuhsatlandırma sonrası şüpheli ilaç advers reasksiyonlarının raporlanması büyük önem taşımaktadır. Raporlama yapılması, ilacın yarar/risk dengesinin sürekli olarak izlenmesine olanak sağlar. Sağlıkmesleği mensuplarının herhangi bir şüpheli advers reaksiyonu Türkiye Farmakovijilans Merkezi(TÜFAM)'ne bildirmeleri gerekmektedir. (www.titck.gov.tr[email protected];4.9 Doz aşımı ve tedavisiBu belge Belge Do Semptomlar ve bulgularFLUDALT DUO için doz aşımına dair klinik çalışma verisi bulunmamaktadır, ancak salmeterol ve/veya flutikazon propiyonat ile ilgili doz aşımı bilgileri aşağıda verilmiştir: Salmeterol doz aşımının belirti ve semptomları sersemlik hali, sistolik kan basıncında artış, tremor, baş ağrısı ve taşikardidir. FLUDALT DUO doz aşımı için spesifik bir tedavi bulunmamaktadır. Dozaşımı durumunda hastaya, gerektiği şekilde uygun gözlem ile birlikte destekleyici tedaviuygulanmalıdır. Buna ek olarak hipokalemi meydana gelebilir bu nedenle serum potasyum düzeyleriizlenmelidir. Potasyum replasmanı göz önünde bulundurulmalıdır. Akut: Önerilenden yüksek flutikazon propiyonat dozlarının akut inhalasyonu adrenal fonksiyonunda geçici süpresyona neden olabilir. Adrenal fonksiyonu plazma kortizol ölçümleri ile doğrulandığıüzere birkaç günde normale döndüğünden bu doz acil tedavi gerektirmemektedir. İnhale flutikazon propiyonat ile kronik doz aşımı: Adrenal rezerv izlenmelidir. Sistemik kortikosteroidler ile tedavi gerekli olabilir. Stabilizasyon sağlandığında önerilden dozda inhale kortikosteroid ile tedaviye devam edilmelidir. Adrenalsupresyon için bkz. Bölüm 4.4. Gerek akut gerekse kronik flutikazon propionat doz aşımı durumunda FLUDALT DUO tedavisine, semptom kontrolü için uygun dozajda devam edilmelidir. 5. FARMAKOLOJİK ÖZELLİKLER5.1 Farmakodinamik özelliklerFarmakoterapötik grubu : Kortikosteroidler ve Diğer İlaçlar ile Kombine Adrenerjikler (Antikolinerjik Kombinasyonları Hariç) ATC Kodu : R03AK06 Etki mekanizmasıFLUDALT DUO farklı etki şekline sahip salmeterol ve flutikazon propiyonat içermektedir. . İki etkin maddenin ilgili etki mekanizmaları aşağıda tartışılmaktadır. SalmeterolSalmeterol, reseptörün sekonder bağlanma bölgesine bağlanan bir uzun yan zinciri olan, selektif uzun etkili (12 saat) bir beta-2 adrenoreseptör agonistidir. Salmeterol klasik kısa etkili beta2-agonistlerin önerilen dozlarına göre en az 12 saat süren, daha uzun süreli bronkodilatasyonsağlamaktadır. Flutikazon propiyonatÖnerilen dozlarda inhalasyon yoluyla verilen flutikazon propiyonat akciğerlerde bir glukokortikoid antienflamatuvar etkiye sahiptir ve bu etki kortikosteroidler sistemik yolla uygulandığında Belg e Doğrulama Kodu: lZW56aklUQ3NRZl AxZl AxZmxXZmxXS3kO HBelge Takip Adresi:https://www.turkiye.gov.tr/saglik-titck-ebys görülenden daha az yan etkiyle semptomlarda ve astım alevlenmelerinde azalma sağlamaktadır. Klinik etkililik ve güvenlilikFlutikazon propiyonat/Salmeterol astım klinik çalışmaları Uzun süreli astımlı 3416 erişkin ve adolesanda 12 aylık bir çalışmada (Optimal Astım Kontrolünü Sağlanması, GOAL) astım tedavisi hedeflerinin erişilebilir olup olmadığının belirlenmesi için tekbaşına inhale kortikosteroidler (Flutikazon Propiyonat) ile Flutikazon propiyonat/Salmeterol'ünetkinlik ve güvenilirliği karşılatırılmıştır. Tedavi dozu **Toplam kontrol sağlanana veya çalışmailacının en yüksek dozuna erişilene kadar 12 haftada bir artırılmıştır. GOAL, Flutikazonpropiyonat/Salmeterol verilen hastadan tek başına inhale kortikosteroid (IKS) verilen hastalarakıyasla daha fazla hastalarda astım kontrolü sağlandığı ve bu kontrolün daha düşük kortikosteroiddozunda elde edildiğini göstermiştir. *İyi kontrol altına alınmış astım, tek başına IKS'ye kıyasla Flutikazon propiyonat/Salmeterol ile daha hızlı şekilde elde edilmiştir. Bireysel olarak iyi kontrolün sağlandığı haftanın elde edilmesi içinhastaların %50'sindeki tedavi süresi Flutikazon propiyonat/Salmeterol için 16 gün ve IKS grubunda37 gündü. Daha önce steroid tedavisi alamayan bir hasta alt grubunda bireysel iyi kontrol altınaalınmış haftaya kadar geçen süre Flutikazon propiyonat/Salmeterol ile 16 gün olurken IKS ile 23gündü.
*Yeterli düzeyde kontrol altına alınan astım; >1 semptom skoru ile < 2 gün (semptom skoru 1, 'gün içinde bir kısa süreli semptom' şeklinde tanımlanır), <2 gün ve haftada <4 SABA kullanımı, > %80öngörülen sabah pik ekspiratuar akımı, gece uyanmalarının olmaması, alevlenmelerin olmaması vetedavi değişikliği gerektiren yan etkilerin olmaması **Tam kontrol altına alınan astım; semptomların olmaması, SABA kullanımının olmaması, > %80 öngörülen sabah pik ekspiratuar akışı, gece uyanmalarının olmaması, alevlenmelerin olmaması vetedavi değişikliği gerektiren yan etkilerin olmaması Bu çalışmadaki bulgular günde iki kez Salmeterol/Flutikazon 50/100 mikrogram dozunun, hızlı astım kontrolünün gerekli olduğu düşünülen orta şiddette dirençli astım hastalarında ilk idametedavisi olarak değerlendirilebileceğini düşündürmektedir. >18 yaşındaki dirençli astım hastası 318 kişide yapılan bir çift kör, randomize, paralel gruplu çalışmada iki haftalık sürede günde iki kez iki inhalasyonla (çift doz) Flutikazonpropiyonat/Salmeterol kullanımının güvenilirlik ve tolerabilitesi değerlendirilmiştir. Bu çalışma 14güne kadar her Flutikazon propiyonat/Salmeterol dozu inhalasyonunun iki katına çıkarılmasının Belg e Doğrulama Kodu: lZW56aklUQ3NRZlAxZlAxZmxXZmxXS3kO 123elge Takip Adresi:https://www.turkiye.gov.tr/saglik-titck-ebys günde iki kez tek inhalasyona kıyasla beta agonist ile ilişkili yan etkilerde küçük bir artışa (tremor; 0'a karşı 1 hasta [%1], palpitasyon; 1 hastaya [<%1] karşı 6 [%3], kas krampları; 1 [<%1] hastayakarşı 6 [%3] ) ve inhale kortikosteroid ile ilişkili yan etkilerde benzer bir insidansa neden olduğunugöstermiştir (örn, oral kandidiyazis; 16 hastaya [%8] karşı 6 [%6], ses kısıklığı; 4 hastaya [%2]karşı 2 [%2] ). Flutikazon propiyonat/Salmeterol dozunun ek kısa süreli (14 güne kadar) inhalekortikosteroid tedavisine ihtiyaç duyulan erişkin hastalarda iki katına çıkarılması düşünülürse betaagonist ile ilişkili yan etkilerdeki küçük artış dikkate alınmalıdır. AstımÇok Merkezli Salmeterol Astım Araştırma Çalışması Çok Merkezli Salmeterol Astım Araştırma Çalışması, yetişkin ve ergen gönüllülerde olağan tedaviye salmeterol veya plasebo eklenmesinin güvenliliğini karşılaştıran 28 haftalık bir ABDçalışmasıydı. Solunum ile ilişkili ölüm ve solunum ile ilişkili yaşamı tehdit eden olayların kombinesayısı olan primer sonlanım noktası açısından anlamlı farklılık olmasa da, çalışma salmeterol alanhastalarda astımla ilişkili ölüm sayısında anlamlı artış göstermiştir (salmeterol ile tedavi edilen13.176 hastada 13 ölüme kıyasla plasebo alan 13.179 hastada 3 ölüm). Çalışma eşzamanlı inhalekortikosteroid kullanımının etkisi değerlendirmek için tasarlanmamıştır ve gönüllülerin yalnızca%47'si başlangıçta İKS kullanımını bildirmiştir. Astımda salmeterol+flutikazon propiyonat ile tek başına flutikazon propiyonat'ın güvenliliği ve etkililiği Salmeterol+flutikazon propiyonat ile tek başına flutikazon propiyonat'ın güvenliliği ve etkililiğini karşılaştırmak için biri yetişkin ve ergen gönüllülerde (AUSTRI çalışması), diğeri 4-11 yaşlarındapediyatrik gönüllülerde (VESTRI çalışması) olmak üzere iki tane çok merkezli 26 haftalık çalışmayürütülmüştür. Her iki çalışmaya dahil edilen gönüllülerin bir önceki yılda astımla ilişkili hastaneyeyatış veya astım alevlenmesi ile birlikte orta ile şiddetli inatçı astımı vardı. İki çalışmanın da primerhedefi tek başına İKS'ye (flutikazon propiyonat) kıyasla İKS tedavisine LABA eklenmesinin(salmeterol+flutikazon propiyonat) astımla ilişkili olaylar (astımla ilişkili hastaneye yatış,endotrakeyal entübasyon ve ölüm) açısından non- inferioriteyi değerlendirmekti. Çalışmanın ikincilhedefi ciddi astım alevlenmesi (astımın kötüye gitmesi nedeniyle en az 3 gün sistemikkortikosteroid kullanımına gerek olması veya sistemik kortikosteroid kullanımı gerektiren astımnedenli hastaneye veya acile yatış olarak tanımlanmıştır) açısından İKS+LABA'nın(salmeterol+flutikazon propiyonat) tek başına İKS tedavisine (flutikazon propiyonat) üstünlüğünüdeğerlendirmekti. AUSTRI ve VESTRI çalışmalarına sırasıyla 11.679 ve 6.208 hasta randomize edilmiş ve tedavi görmüştür. Primer sonlanma noktası güvenlilik için, her iki çalışmada da non- inferioritegösterilmiştir (bkz. aşağıda tablo)
verilmiştir b Göreceli risk için %95 GA üst sonucu 2.675'ten azsa, non-inferiorite sonucuna karar verilmiştir İkincil etkililik sonlanma noktası için, flutikazon propiyonat'la karşılaştırıldığında salmeterol+flutikazon propiyonat'ta ilk astım alevlenmesine kadar geçen sürede azalma her ikiçalışmada da görülmüştür, ancak yalnızca AUSTRI'de istatistiksel olarak anlamlı fark sağlanmıştır:
KOAHKısa etkili beta 2-agonistlerine % 10 reversibilite kısıtlaması olmayan semptomatik KOAH hastaları: Altı ay boyunca yürütülen plasebo kontrollü klinik çalışmalar, 50/250 mikrogram ve 50/500mikrogram'lık Flutikazon propiyonat/Salmeterol'ın düzenli kullanımının akciğer fonksiyonunuhızlı ve anlamlı derecede düzelttiğini, nefes darlığını ve rahatlatıcı ilaç kullanımını anlamlıderecede azalttığını göstermiştir. Aynı zamanda hastaların sağlık durumunda da anlamlı derecededüzelme olmuştur.Kısa etkili beta 2-agonistlerine % 10'dan daha az reversibilite gösteren semptomatik KOAH hastaları:6 ve 12 ay boyunca yürütülen plasebo kontrollü klinik çalışmalar, 50/500 mikrogram Flutikazon propiyonat/Salmeterol'ün düzenli kullanımının akciğer fonksiyonunu hızlı ve anlamlı derecededüzelttiğini, nefes darlığını ve rahatlatıcı ilaç kullanımını anlamlı derecede azalttığını göstermiştir.12 aylık periyod boyunca KOAH alevlenme riski ve ilave oral kortikosteroid ihtiyacı anlamlıderecede azalmıştır. Aynı zamanda hastaların sağlık durumunda da anlamlı derecede düzelmeolmuştur. Bu belge Belg e Doğrulama Kodu: lZW56aklUQ3NRZlAxZlAxZmxXZmxXS3kO 14elge Takip Adresi:https://www.turkiye.gov.tr/saglik-titck-ebys Flutikazon propiyonat/Salmeterol 50/500 mikrogram hem tedavi sırasında sigara içen, hem de sigarayı bırakmış hastalarda akciğer fonksiyonunu ve sağlık durumunu düzeltmede ve KOAHalevlenme riskini azaltmada etkili bulunmuştur. TORCH çalışması (TOwards a Revolution in COPD Health; KOAH'ta devrime doğru):TORCH, KOAH hastalarında, günde 2 kez 50/500 mikrogram Flutikazon propiyonat/Salmeterol, günde 2 kez 50 mikrogram salmeterol, günde 2 kez 500 mikrogram FP (flutikazon propiyonat) veyaplasebo ile yapılan tedavinin tüm nedenlere bağlı ölümler üzerindeki etkisini değerlendirmek içinyapılan 3 yıllık bir çalışmadır. Başlangıç (bronkodilatatörden önce) FEWi beklenen normaldeğerin %60'ından az olan orta-şiddetli ve şiddetli KOAH hastaları çift-kör tedavi almak üzererandomize edilmiştir. Çalışma boyunca, diğer inhale kortikosteroidler, uzun etkili bronkodilatörlerve uzun süre sistemik kortikosteroidler dışında, her zamanki KOAH tedavilerini almalarına izinverilmiştir. Üç yıllık sağkalım durumu, çalışmadan çıkıp çıkmadıklarına bakılmaksızın hastalarıntümü için tespit edilmiştir. Primer sonlanma noktası, plaseboya kıyasla Flutikazonpropiyonat/Salmeterol için 3 yılda tüm nedenlere bağlı ölümlerin azaltılmasıdır. (Tablo 1)
Flutikazon propiyonat/Salmeterol'ün, plaseboya kıyasla 3 yıl içinde herhangi bir zamanda ölüm riskini % 17,5 oranında azalttığı görülmüştür. (Risk Oranı 0,825 (% 95 GA 0,68, 1,00, p = 0,052;tümü ara analizler için ayarlanmıştır). Plaseboya kıyasla, üç yıllık süre içinde herhangi bir zamandaherhangi bir nedenden dolayı gerçekleşen ölümlerde, salmeterol ile % 12 azalma (p = 0,180) ve FPile % 6 artış (p = 0,525) olmuştur. (Tablo 1) Cox'un Orantısal Risk modelinin kullanıldığı destekleyici bir analiz, plaseboya kıyasla 3 yıl içinde herhangi bir zamanda ölüm riskinde % 19 azalma gösteren Flutikazon propiyonat/Salmeterol için0,811'lik (% 95 GA 0,670, 0,982, p = 0,031) bir risk oranı olduğunu göstermiştir. Model önemlifaktörler (sigara içme durumu, yaş, cinsiyet, bölge, başlangıç FEV 1ve Vücut Kitle İndeksi) içinayarlanmıştır. Tedavi etkilerimn bu fiiktöriere göre teğjştigjra dair kanıt ydcto. (Tabl° 1)Belge Do Üç yıl içinde KOAH'a bağlı nedenlerden dolayı ölen hastaların yüzdesi plasebo için % 6.0,salmeterol için % 6,1, FP için % 6.9 ve Flutikazon propiyonat/Salmeterol için % 4,7'dir. (Tablo 1)Plaseboya kıyasla Flutikazon propiyonat/Salmeterol, orta şiddetli ve şiddetli alevlenmeleri % 25 (% 95 GA: % 19 ve % 31 arasında; p < 0.001) oranında azaltmıştır Flutikazon propiyonat/Salmeterolalevlenme oranını, salmeterol ile karşılaştırıldığında % 12 (% 95 GA: % 5 ve % 19 arasında; p =0.002), FP ile karşılaştırıldığında da % 9 (% 95 GA: % 1 ve % 16 arasında; p = 0.024) oranındaazaltmıştır. Plaseboya kıyasla salmeterol ve FP alevlenme oranını anlamlı derecede sırasıyla % 15(% 95 GA: % 7 ve % 22 arasında; p < 0,001) ve % 18 (% 95 GA: % 11 ve % 24 arasında; p <0,001) oranında azaltmıştır. St George Solunum Anketi (SGSA) ile ölçülen Sağlıkla İlişkili Yaşam Kalitesi, plaseboya kıyasla tüm aktif tedavi yöntemleri ile düzelmiştir. Üç yıl boyunca Flutikazon propiyonat/Salmeterol ilesağlanan ortalama düzelme plaseboya kıyasla - 3,1 birim (% 95 GA: - 4,1 ve - 2,1 arasında; p <0,001), salmeterole kıyasla - 2.2 birim (p < 0,001) ve FP'ye kıyasla - 1.2 birimdir (p = 0,017). Üç yıllık tedavi süresi boyunca, FEV 11üzerinde Flutikazon propiyonat/Salmeterol salmeteroldenveya FP'den daha etkilidir (salmeterol için ortalama fark 50 mL, p < 0,001 ve FP için 44 mL'dir, p< 0.001).Advers olay olarak bildirilen pnömoninin 3 yıllık tahmini olasılığı plasebo için % 12.3, salmeterol için % 13.3, FP için % 18.3 ve Flutikazon propiyonat/Salmeterol için % 19,6'dır (Flutikazonpropiyonat/Salmeterol'ün plaseboya karşı risk oranı: 1,64, % 95 GA: 1,33 ve 2,01 arasında, p <0,001). Pnömoni ile ilişkili ölümlerde artış olmamıştır; tedavi sırasında birincil olarak pnömoniyebağlı oldukları düşünülen ölümler plasebo için 7, salmeterol için 9, FP için 13 ve Flutikazonpropiyonat/Salmeterol için 8 olarak tespit edilmiştir. Kemik kırılma olasılığında anlamlı farklılıkyoktur (plasebo % 5,1, salmeterol % 5,1, FP % 5,4 ve Flutikazon propiyonat/Salmeterol % 6,3;plaseboya karşı Flutikazon propiyonat/Salmeterol için risk oranı: 1,22, % 95 GA: 0,87 ve 1,72arasında, p = 0.248). Göz bozuklukları, kemik bozuklukları ve hipotalamus-hipofiz-adrenal eksenbozuklukları ile ilgili advers olayların insidansı düşüktür ve tedaviler arasında farklılıkgözlenmemiştir. Salmeterol alan tedavi gruplarında kardiyak advers olaylarında artış olduğuna dairkanıt yoktur. Pediyatrik popülasyon: SAM101667 çalışmasında, 6 ila 16 yaşlarında semptomatik astımı olan 158 çocukta, semptom kontrolü ve akciğer fonksiyonu açısından salmeterol/flutikazon propiyonat kombinasyonuflutikazon propiyonat dozunun ikiye katlanmasıyla eşit etkililikte bulunmuştur. Bu çalışmaalevlenme üzerine etkileri araştırmak için tasarlanmamıştır. 4 ila 11 yaşlarında çocukların (n=257), her ikisi de günde iki defa olmak üzere salmeterol/flutikazon propiyonat 50/100 veya salmeterol 50mcg + flutikazon propiyonat 100mcg iletedavi edildiği 12 haftalık bir çalışmada, her iki tedavi kolunda pik ekspiratuar akımda %14'lük birgelişme ile semptom skoru ve kurtarıcı salbutamol kullanımında iyileşmeler görülmüştür. İki tedavikolu arasında farklılık bulunmamıştır. İki tedavi kolu arasında güvenlilik parametreleri açısındanfarklılık bulunmamıştır. Bu belge Belge Do 4 ila 11 yaşlarında persistan astımı olan ve inhale kortikosteroid tedavisindeyken semptomatik olan çocukların (n=203) dahil edildiği randomize paralel grup çalışmasında güvenlilik primer hedefolmuştur. Çocuklara günde iki defa tek başına salmeterol/flutikazon propiyonat (50/100mcg) veyatek başına flutikazon propiyonat (100mcg) tedavisi verilmiştir. Salmeterol/flutikazon propiyonatalan iki çocuk ve flutikazon propiyonat alan beş çocuk astımın kötüleşmesi nedeniyle çalışmadanayrılmıştır. 12 hafta sonunda çalışmanın her iki kolunda da 24 saatlik üriner kortizol atılımı anormalolan çocuk bulunmamıştır. Çalışma kolları arasında güvenlilik profili açısından fark bulunmamıştır. Gebelik sırasında astımda flutikazon propiyonat içeren ilaçların kullanımı Majör konjenital malformasyon (MKM) riskini değerlendirmek için, Birleşik Krallık elektronik sağlık kayıtları kullanılarak birinci trimesterde tek başına inhale flutikazon propiyonat vesalmeterol+flutikazon propiyonat ile flutikazon propiyonat içermeyen İKS maruziyetininkarşılaştırıldığı, gözlemsel retrospektif epidemiyolojik kohort çalışması yürütülmüştür. Buçalışmaya karşılaştırma amaçlı plasebo dahil edilmemiştir. Birinci trimesterde İKS-maruziyeti olan 5362 gebeden oluşan astım kohortunda, 131 tanı konmuş MKM belirlenmiştir; flutikazon propiyonat veya salmeterol+flutikazon propiyonat maruziyeti olan1612'sinden (%30) 42'sinde MKM tanısı konulduğu belirlenmiştir. 1. yılda flutikazon propiyonatile flutikazon propiyonat olmayan İKS maruziyeti karşılaştırıldığında kadınlarda tanı konulmuşMKM'ler için ayarlanmış olasılık oranı orta şiddette astımlılarda 1,.1 (%95 GA: 0.5 - 2,3) veşiddetli astımlılarda 1,2 (%95 GA: 0,7 - 2,0) olmuştur. İlk trimesterde tek başına flutikazonpropiyonat ile salmeterol+flutikazon propiyonat maruziyeti karşılaştırıldığında MKM riskindefarklılık görülmemiştir. Astım şiddet basamaklarında mutlak MKM riskleri flutikazon propiyonatmaruziyeti olan 100 gebelikte 2,0 ila 2,9 arasında değişmektedir. Bu da Pratisyen HekimlikAraştırma Veritabanında astım tedavisine maruziyeti olmayan 15,840 gebelikte yürütülençalışmanın sonuçlarıyla karşılaştırılabilir olmuştur (100 gebelikte 2,8 MKM). 5.2 Farmakokinetik özelliklerGenel ÖzelliklerHayvanlarda veya insanlarda inhalasyon yoluyla birlikte uygulanan salmeterol ve flutikazon propiyonatın birbirlerinin farmakokinetiğini etkilediğine dair herhangi bir bulgu yoktur. Bu nedenle farmakokinetik açıdan her iki bileşen ayrı ayrı düşünülebilir. SalmeterolSalmeterol akciğerlerde lokal olarak etki eder, bu nedenle plazma seviyeleri terapötik etkinin belirleyicisi değildir. Terapötik dozlarda inhalasyondan sonra çok düşük plazma konsantrasyonlarıgösterdiği için (yaklaşık 200 pg/ml veya daha az) plazmadaki ilaç miktarının tayini teknik olarak zorolduğundan salmeterolün farmakokinetiği ile ilgili sadece sınırlı veriler bulunmaktadır. Flutikazon propiyonatEmilim:Sağlıklı gönüllülerde inhalasyon yoluyla alınan tek doz flutikazon propiyonatın mutlak biyoyararlanımı, kullanılan inhalasyon cihazına göre nominal dozun yaklaşık %5-11'i arasındadeğişmektedir. Astımlı hastalarda inhale flutikazon propiyonata sistemik maruziyetin daha düşük Bu belge Belge Do düzeyde gözlenmiştir. Sistemik emilim temelde akciğerlerde meydana gelmekte olup ilk başta hızlı ve sonrasında uzun sürelidir. İnhale dozun kalanı yutulabilir ancak düşük suda çözünürlük vepresistemik metabolizma nedeniyle sistemik maruziyete minimum katkıda bulunur ve oralbiyoyararlanımının %1'den az olmasını sağlar. Sistemik maruziyet, inhale dozun artışıyla lineerşekilde artar. Dağılım:Flutikazon propiyonatın dispozisyonu, yüksek plazma klerensi (1150 ml/dak), kararlı durumda yüksek dağılım hacmi (300 L) ve yaklaşık 8 saat olan terminal yarılanma ömrü ile karakterizedir. Flutikazon propiyonatın plazma proteinlerine bağlanma oranı % 91'dir. Biyotransformasyon:Flutikazon propiyonat başlıca sitokrom P450 enzimi CYP3A4 tarafından inaktif karboksilik asite metabolize edilir. Eliminasyon:Flutikazon propiyonat sistemik dolaşımdan çok hızlı temizlenir. Flutikazon propiyonatın renal klirensi önemsiz düzeydedir. Dozun %5'inden daha azı idrarda temelde metabolitler olarakatılmaktadır. Dozun büyük bir bölümü feçeste metabolitler ve değişmemiş olarak atılmaktadır. Hastalardaki karakteristik özelliklerBöbrek/Karaciğer yetmezliği:Veri bulunmamaktadır. Değişik yaş grupları:Pediatrik popülasyon4 ila 77 yaş arası 350 hastayı (hastaların 174'ü 4-11 yaş) içeren, farklı cihazların (DISKUS, ölçülü inhalasyon cihazı) kullanıldığı, kontrol gruplarına yer verilen 9 çalışmadan bildirilen verilerinkullanıldığı bir popülasyon farmakokinetiği analizinde, flutikazon propionat 100 ilekarşılaştırıldığında Flutikazon propiyonat/salmeterol 50/100 ile tedavi sonrasında daha yüksekflutikazon propionat sistemik maruziyeti görülmüştür. Çocuklarda ve Adölesan/Erişkin Popülasyonlarda flutikazon propionat karşısında Salmeterol/flutikazon propionat karşılaştırması için Geometrik Ortalama Oranı [%90 GA]
Bu belge Belg e Doğrulama Kodu: lZW56aklUQ3NRZl AxZl AxZmxXZmxXS3kO 18Belge Takip Adresi:https://www.turkiye.gov.tr/saglik-titck-ebys
21 günlük Flutikazon propiyonat/salmeterol inhaler 25/50 mikrogram (spacer ile birlikte veya spacer olmaksızın günde iki kez 2 inhalasyon) veya Flutikazon propiyonat/salmeterol US 50/100mikgrogram (günde iki kez 1 inhalasyon) tedavilerinin etkisi 4 ila 11 yaşlarında hafif astımlı 31çocukta değerlendirilmiştir. Flutikazon propiyonat/salmeterol inhaler, spacer ile birlikte Flutikazonpropiyonat/salmeterol inhaler ve Flutikazon propiyonat/salmeterol için salmeterol sistemikmaruziyeti benzer olmuştur (sırasıyla 126pg sa/mL [%95 GA: 70, 225], 103pg sa/mL [%95 GA: 54,200] ve 110 pg sa/mL [%95 GA: 55, 219]). Flutikazon propiyonat sistemik maruziyeti spacer ilebirlikte kullanılan Flutikazon propiyonat/salmeterol inhaler ile (107pg sa/mL [%95 GA: 45.7,252.2]) ve Flutikazon propiyonat/salmeterol'de (138pg sa/mL [%95 GA: 69.3, 273.2]) benzerolmştur, ancak Flutikazon propiyonat/salmeterol inhaler için daha düşüktür (24pg sa/mL [%95 GA:9.6, 60.2]). 5.3 Klinik öncesi güvenlilik verileriAyrı şekilde verilen salmeterol ve flutikazon propiyonatın hayvan çalışmalarına göre insanlarda kullanıma yönelik güvenlilikle ilişkili tek endişe farmakolojik etkilerin artmasıyla ilişkili etkilerolmuştur. Hayvan üreme çalışmalarında glukokortikoidlerin, malformasyonlara (yarık damak, iskelet bozuklukları) neden olduğu gösterilmiştir. Bununla birlikte bu hayvan deneylerinin önerilendozların verildiği insanlar için anlamlı olduğu düşünülmemektedir. Salmeterol ksinafoat ile yapılanhayvan çalışmaları sadece yüksek maruziyet düzeylerinde embriyofetal toksisite göstermiştir.Birlikte uygulanımı takiben bilinen glukokortikoid kaynaklı anomalilerle ilişkilendirilen dozlardasıçanlarda artan transpoze umblikal arter ve ossipital kemikte eksik osifikasyon insidansı tespitedilmiştir. Salmeterol ksinafoat veya flutikazon propionat genetik toksisite potansiyeligöstermemiştir. 6. FARMASÖTİK ÖZELLİKLER6.1 Yardımcı maddelerin listesiLaktoz monohidrat (inek sütü kaynaklıdır.) 6.2 Geçimsizlikler6.3 Raf ömrü24 ay 6.4 Saklamaya yönelik özel tedbirler25°C altındaki oda sıcaklığında saklanmalıdır. Kuru bir yerde saklanmalıdır. Bu belge Belge Do Çocukların göremeyeceği, erişemeyeceği yerlerde ve ambalajında saklayınız. 6.5 Ambalajın niteliği ve içeriğiBlister ambalajda 60 kapsül ve inhalasyon cihazı içeren karton kutularda satılmaktadır. 6.6 Beşeri tıbbi üründen arta kalan maddenin imhası ve diğer özel önlemlerTüm kullanılmayan ürün ve artık maddeler Tıbbi Atıkların Kontrolü Yönetmeliği ve Ambalaj ve Ambalaj Atıklarının Kontrolü Yönetmeliğine uygun olarak imha edilmelidir. FLUDALT DUO akciğerlere inhale edilen toz salıvermektedir. İnhalasyon cihazının kullanımı doktor ve eczacı tarafından hastaya gösterilmelidir. Kapsüllerin kesinlikle ağız içine alınarak yutulmaması ve kesinlikle inhaler içine yerleştirildikten sonra solukalma yolu ile kullanılması gerektiği konusunda hasta bilgilendirilmelidir. Jelatin kapsülünparçalanabileceği ve inhalasyondan sonra ağız ve boğaza küçük jelatin parçacıklarının ulaşabileceğihastaya anlatılmalıdır. Bu olasılık kapsülün birden fazla delinmemesi ile en aza indirilir. Cihaz, koruma kapağı çıkarılarak açılır ve kullanıma hazırlanır. Ağızlık ağıza yerleştirilir ve dudaklar etrafını saracak şekilde kapatılır. Bundan sonra doz inhale edilebilir ve koruma kapağıtekrar kapatılabilir. FLUDALT DUO'nun kullanım talimatları
3. Bir kapsülü cihazın içindeki boşluğa yerleştirin. Kapsülü ambalajından kullanmadan hemen önce çıkartın. 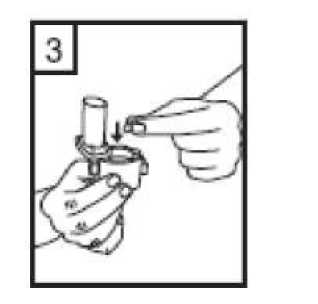
4.
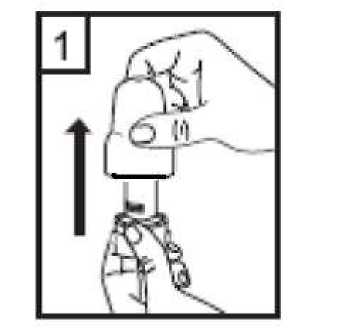
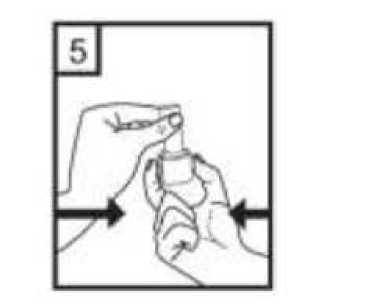
Ağızlık kısmını çevirerek kapatın. 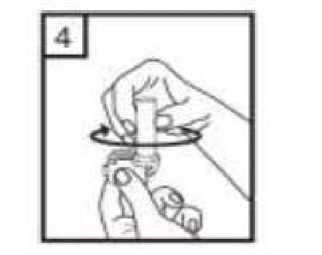 5. Cihazı dik tutun, kenardaki düğmelere sadece bir kez tam olarak basın ve bırakın. Kapsül her iki ucundan delinecektir. Nefes almanız sırasında küçük jelatin kapsül parçaları ağzınıza gelebilir. Jelatin parçaları zararsızdır ve yutulduktan sonra sindirileceklerdir. Küçük jelatin parçalarının oluşma riskikapsülün ambalajından çıkarılır çıkarılmaz hemen kullanılması ve düğmelere sadece bir kezbasılması ile azalır.
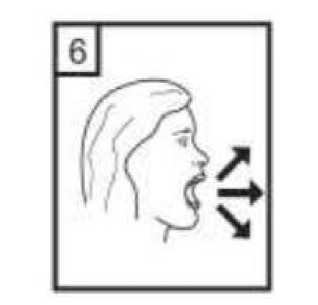
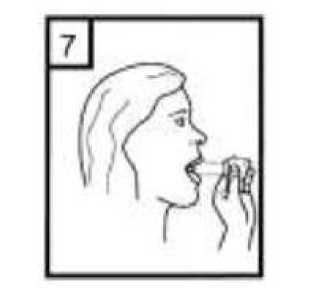
Bu belge Belg e Doğrulama Kodu: lZW56aklUQ3NRZl AxZl AxZmxXZmxXS3kO 2Pelge Takip Adresi:https://www.turkiye.gov.tr/saglik-titck-ebys 7. Ağız parçasını ağzınıza yerleştirin ve başınızı hafifçe arkaya doğru eğin. Ağızlık etrafındadudaklarınızı sıkıca kapatın ve olabildiğince hızlı ve derin nefesalın. 8. Cihazı ağzınızdan çıkarın ve rahatsız olmadan olabildiğince uzun süre nefesinizi tutun. Sonranormal şekilde soluk alıp verin. Cihazı tekrar açın ve kapsül içerisinde toz kalıp kalmadığınabakın. Kapsül içerisinde toz kalmış ise 6,7 ve 8 numaralı basamakları tekraredin. 9. Kullanımdan sonra, boş kapsülü atın ve ağızlık kısmını kapatın. 10. Sonrasında, ağzınızı su ile çalkalayınız tükürünüz. UNUTMAYINIZ ! Cihazınızı kuru tutunuz. Kullanılmadığı zaman kapalı tutunuz. Cihazın içine asla nefes vermeyiniz. Hareket kolunu sadece ilacı almaya hazır olduğunuzda itiniz. Söylenen dozdan daha fazla almayınız. 7. RUHSAT SAHİBİ Bu belge Belg e Doğrulama Kodu: lZW56aklUQ3NRZl AxZl AxZmxXZmxXS3kO 223elge Takip Adresi:https://www.turkiye.gov.tr/saglik-titck-ebys Arımed İlaç San. ve Tic. A.Ş. Kağıthane/İstanbul 8. RUHSAT NUMARASI2016/365 9. İLK RUHSAT TARİHİ/RUHSAT YENİLEME TARİHİİlk ruhsat tarihi: 28.04.2016 Ruhsat yenileme tarihi: 06.05.2021 10. KÜB'ÜNYENİLENMETARİHİBu belge Belg e Doğrulama Kodu: lZW56aklUQ3NRZl AxZl AxZmxXZmxXS3kO 23^elge Takip Adresi:https://www.turkiye.gov.tr/saglik-titck-ebys |
İlaç BilgileriFludalt Duo 50 Mcg/ 500 Mcg İnhalasyon İçin Toz İçeren KapsülEtken Maddesi: Salmeterol Ksinafoat + Flutikazon Propiyonat Kullanma talimatı ve kısa ürün bilgileri
Google Reklamları
İlgili İlaçlar |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
Ana Sayfa | Hakkımızda | İlaçlar | İlaç Ara | İlaç Firmaları | Gizlilik | Bize Ulaşın
Telif Hakkı 2008-2026 © İlaç Prospektüsü. Tüm Hakları Saklıdır.Uyarı: Sitemizde yayınladığımız ilaç bilgileri ile doktora danışmadan kesinlikle ilaç kullanmayınız!
Aksi halde doğabilecek sağlık sorunlarından ilacprospektusu.com sorumlu tutulamaz.