Tilanta 90 Mg Film Kaplı Tablet Kısa Ürün BilgisiKISA URUN BILGISI1. BEŞERI TIBBI URUNUN ADITİLANTA 90 mg film kaplı tablet 2. KALİTATİF VE KANTİTATİF BİLEŞİMEtkin madde:
90 mg
Tikagrelor Yardımcı maddeler:Yardımcı maddeler için 6.1'e bakınız. 3. FARMASÖTİK FORMFilm kaplı tablet. Bir tarafında 9 baskılı diğer tarafı düz olan; açık sarı renkli, yuvarlak, bikonveks film kaplı tablettir. 4. KLİNİK ÖZELLİKLER4.1. Terapötik endikasyonlarAsetilsalisilik asit (ASA) ile birlikte uygulanan TİLANTA, tıbbi gözetimdeki hastalar ve perkütan koroner girişim (PKG) veya koroner arter bypass grefti (KABG) ile tedavi edilen hastalar da dahilolmak üzere, akut koroner sendromlu (stabil olmayan anjina, ST yükselmesiz miyokardenfarktüsü [NSTEMI] veya ST yükselmeli miyokard enfarktüsü [STEMI] olan) hastalardatrombotik olayların (kardiyovasküler ölüm, miyokard enfarktüsü ve inme) önlenmesindeendikedir. Daha fazla bilgi için bölüm 5.1'e bakınız. 4.2. Pozoloji ve uygulama şekliPozoloji/uygulama sıklığı ve süresi:TİLANTA tedavisi, tek dozluk 180 mg yükleme dozu (iki tane 90 mg'lık tablet) ile başlatılır ve günde iki kez 90 mg ile devam edilir. TİLANTA kullanan hastalar ayrıca, spesifik olarak kontrendike olmadıkça, günde bir doz ASA kullanmalıdır. ASA'nın başlangıç dozunu takiben TİLANTA, ASA'nın 75-150 mg'lık idamedozu ile birlikte kullanılmalıdır (Bkz. Bölüm 5.1). Tedavide kesintilerden kaçınılmalıdır. Bir doz TİLANTA almayı unutan hastalar, planlanmış olan zamanda yalnızca bir adet 90 mg tablet (bir sonraki doz) almalıdır. Akut koroner sendrom (AKS) tanısı konmuş hastalarda ihtiyaç halinde klopidogrelden TİLANTA'ya direkt geçiş yapılabilir (Bkz. Bölüm 5.1). Prasugrelden TİLANTA'ya geçişaraştırılmamıştır. Klinik açıdan tedavinin kesilmesi gerekmediği sürece, en az 12 ay TİLANTA ile tedavi önerilmektedir (Bkz. Bölüm 5.1). AKS hastalarında, TİLANTA da dahil olmak üzere herhangi bir antitrombositik ile tedavinin erken kesilmesi, hastanın altta yatan hastalığından dolayı kardiyovasküler ölüm veya miyokardenfarktüsü risk artışı ile sonuçlanabilir (Bkz. Bölüm 4.4). Bu nedenle, tedavinin erkenkesilmesinden kaçınılmalıdır. Uygulama şekli:Oral kullanım içindir. TİLANTA gıdalarla birlikte veya ayrı alınabilir. Tableti bir bütün olarak yutamayan hastalar için, TİLANTA tabletleri ince toz haline gelecek şekilde ezilip yarım bardak suda karıştırılarak hemen içilebilir. Dibinde ilaç kalmadığından eminolmak için, boş bardağı yarım bardak su ile daha çalkalayıp içilmelidir. Karışım ayrıca nazogastriktüp (CH8 veya daha büyüğü) ile uygulanabilir. Karışımın uygulanmasından sonra nazogastrik tüpiçerisinde ilaç kalmadığından emin olmak için su ile durulamak önemlidir. Özel popülasyonlara ilişkin ek bilgiler:Böbrek yetmezliğiBöbrek yetmezliği olan hastalarda doz ayarlamasına gerek yoktur (bkz. Bölüm 5.2) Karaciğer yetmezliğiAğır derecede karaciğer yetmezliği olan hastalarda tikagrelor çalışılmamıştır ve tikagrelorun bu hastalarda kullanılması kontrendikedir (bkz. Bölüm 4.3). Orta derecede karaciğer yetmezliği olanhastaların tedavisinde sınırlı bilgi mevcuttur. Doz ayarlamasına gerek yoktur, ancak tikagrelordikkatli kullanılmalıdır (bkz. Bölüm 4.4 ve 5.2) Hafif karaciğer yetmezliği olan hastalarda dozayarlaması gerekli değildir (bkz. Bölüm 4.4 ve Bölüm 5.2). Pediyatrik popülasyonTikagrelorun 18 yaşın altındaki çocuklarda etkililiği ve güvenliliği belirlenmemiştir. Orak hücre hastalığı olan çocuklarda tikagrelorun ilgili kullanımı yoktur (Bkz. Bölüm 5.1 ve 5.2). Geriyatrik popülasyonYaşlılarda doz ayarlamasına gerek yoktur (bkz. Bölüm 5.2). 4.3. KontrendikasyonlarEtkin madde veya diğer yardımcı maddelere aşırı duyarlılık (bkz. Bölüm 4.8) Aktif patolojik kanama İntrakraniyal hemoraji öyküsü (bkz. Bölüm 4.8) Ağır derecede karaciğer yetmezliği (bkz. Bölüm 4.2, 4.4 ve 5.2) Eşzamanlı uygulama tikagrelora maruziyette belirgin bir artışa neden olabileceği için, güçlü CYP3A4 inhibitörleri (örn.; ketokonazol, klaritromisin, nefazodon, ritonavir ve atazanavir)ile tikagrelorun birlikte kullanımı (bkz. Bölüm 4.5). 4.4. Özel kullanım uyarıları ve önlemleriKanama riskiBilinen kanama riski artmış olan hastalarda tikagrelor kullanımı, aterotrombotik olayların önlenmesinden elde edilecek yarara karşı dengelenmelidir (bkz. Bölüm 4.8 ve Bölüm 5.1). Eğerklinik olarak endike ise, tikagrelor aşağıdaki hasta gruplarında dikkatli kullanılmalıdır: Kanama eğilimi olan hastalar (örn.; yeni travma, yeni ameliyat, koagülasyon hastalıkları,aktif veya yeni gastrointestinal kanama) veya travma riski yüksek olan hastalar. Aktifpatolojik kanaması olan hastalarda ve intrakraniyal hemoraji öyküsü ve ağır derecedekaraciğer yetmezliği olanlarda tikagrelor kullanımı kontrendikedir (bkz. Bölüm 4.3). Kanama riskini artıran ilaçları (örn.; nonsteroidal antiinflamatuvar ilaçlar (N SAİİ'ler), oralantikoagülanlar ve/veya fibrinolitikler) tikagrelor dozundan sonra 24 saat içinde eşzamanlıkullanan hastalar. Trombosit transfüzyonu sağlıklı gönüllülerde tikagrelorun antitrombosit etkisini tersine çevirmez ve kanaması bulunan hastalarda klinik yarar sağlaması mümkün değildir. Tikagrelorundesmopressin ile eşzamanlı olarak uygulanması temel kanama süresini kısaltmadığından,desmopressinin klinik kanama olaylarının tedavisinde etkili olması beklenmez (bkz. Bölüm 4.5). Antifibrinolitik tedavi (aminokaproik asit veya traneksamik asit) ve/veya rekombinant faktör VIIa tedavisi hemostazı artırabilir. Kanamanın sebebi tanımlanıp kontrol altına alındıktan sonratikagrelor tedavisi yeniden başlatılabilir. CerrahiHastalar herhangi bir cerrahi girişim öncesinde ve herhangi bir yeni tıbbi ürün kullanmadan önce, hekimlerini ve diş hekimlerini tikagrelor aldıkları ile ilgili bilgilendirmeleri konusundaeğitilmelidirler. Koroner arter bypass greft (KABG) ameliyatı geçiren PLATO çalışmasındaki hastalarda, ameliyattan 1 gün önce kesilen tikagrelor, klopidogrel ile karşılaştırıldığında, daha fazla kanamaolmuş fakat ameliyattan 2 gün veya daha öncesinde tedavi kesildiğinde majör kanama oranlarıklopidogrel ile benzer bulunmuştur (bkz. Bölüm 4.8). Eğer hasta elektif cerrahi müdahale geçirecekse ve antitrombositik etki istenmiyorsa, tikagrelor ameliyattan 5 gün önce kesilmelidir (bkz. Bölüm 5.1). Daha önce iskemik inme geçirmiş hastalarDaha önce iskemik inme geçirmiş AKS hastaları, 12 aya kadar tikagrelor ile tedavi edilebilir (PLATO çalışması). PEGASUS çalışmasına daha önce iskemik inme geçirmiş Mİ öyküsü olan hastalar dahil edilmemiştir. Bu nedenle, veri yokluğu nedeniyle bu hastalarda bir yılı aşan tedaviönerilmemektedir. Karaciğer yetmezliğiTikagrelor kullanımı ağır derecede karaciğer yetmezliği olan hastalarda kontrendikedir (bkz. Bölüm 4.2 ve Bölüm 4.3). Orta derecede karaciğer yetmezliği olan hastalarda tikagrelor iledeneyim sınırlı olduğundan bu hastalarda dikkatli olunması tavsiye edilmektedir (bkz. Bölüm 4.2ve Bölüm 5.2). Bradikardik olaylar için risk altında olan hastalarHolter EKG takibi klopidogrele kıyasla tikagrelor ile uygulanan tedavi sırasında genellikle asemptomatik olan ventriküler duraklamaların sıklığında artış olduğunu göstermiştir. Bradikardikolay riski artan hastalar (örn.; hasta sinus sendromu, 2. veya 3. derece AV blok veya bradikardiyebağlı senkop gözlenen pacemaker olmayan hastalar) tikagrelorun etkililiği ve güvenliliğinindeğerlendirildiği ana çalışmalardan hariç tutulmuştur. Bu sebeple, bu hastalardaki sınırlı klinikdeneyimden dolayı, tedbirli olunmalıdır (Bkz. Bölüm 5.1). Ayrıca tikagrelor, bradikardiyi uyardığı bilinen tıbbi ürünlerle eşzamanlı olarak uygulandığında dikkatli olunmalıdır. Bununla birlikte, PLATO çalışmasında bradikardiyi uyardığı bilinen bir yada daha fazla tıbbi ürünün eşzamanlı uygulamasının ardından (örn.; %96 beta blokörler, %33kalsiyum kanal blokörleri diltiazem ve verapamil ve %4 digoksin) klinik açıdan önemli adversreaksiyon kanıtı gözlenmemiştir (Bkz. Bölüm 4.5). PLATO'daki Holter alt-çalışması sırasında AKS'nin akut fazı süresince klopidogrele kıyasla tikagrelor ile daha fazla hastada >3 saniyelik ventriküler duraklamalar ortaya çıkmıştır. AKS'ninakut fazı sırasında, tikagrelor ile Holter tarafından saptanan ventriküler duraklamalardaki artışgenel popülasyona kıyasla kronik kalp yetmezliği (KKY) bulunan hastalarda daha fazla olmuş,ancak bu durum tikagrelor ile birinci ayda ya da klopidogrel ile karşılaştırıldığındagözlenmemiştir. Bu hasta popülasyonunda bu dengesizlik ile ilişkili advers klinik sonuçlarsaptanmamıştır (senkop ya da pacemaker uygulaması dahil) (Bkz. Bölüm 5.1). Özellikle kardiyak iskemi ve kalp hızını azaltan veya kardiyak iletimi etkileyen ilaçların potansiyel karıştırıcı olduğu, tikagrelor alan AKS'li hastalarda, pazarlama sonrasında bradiaritmikolaylar ve AV blokları bildirilmiştir (Bkz. Bölüm 4.8). Hastanın klinik durumu ve birliktekullandığı ilaçlar potansiyel karıştırıcı nedenler olarak tedaviyi ayarlamadan öncedeğerlendirilmelidir. DispneDispne, tikagrelor ile tedavi edilen hastalarda bildirilmiştir. Şiddeti genellikle hafiften ortaya değişmiş ve sıklıkla tedavinin bırakılmasını gerektirmeden düzelmiştir. Astım/Kronik ObstrüktifAkciğer Hastalığı (KOAH) bulunan hastalarda tikagrelor ile dispne olayının meydanagelmesindeki mutlak risk artmış olabilir (Bkz. Bölüm 4.8). Tikagrelor, astım ve/veya KOAHöyküsü bulunan hastalarda dikkatli kullanılmalıdır. Mekanizma henüz aydınlatılmamıştır. Eğerbir hasta yeni, uzayan ya da kötüleşen bir dispne bildirirse bu durum ayrıntılı olarak incelenmelive tolere edilemezse tikagrelor tedavisi kesilmelidir. Daha fazla bilgi için Bölüm 4.8'e bakınız. Merkezi uyku apnesiTikagrelor alan hastalarda pazarlama sonrası ortamda Cheyne-Stokes solunumu dahil merkezi uyku apnesi bildirilmiştir. Merkezi uyku apnesinden şüpheleniliyorsa, daha ileri klinikdeğerlendirme düşünülmelidir. Kreatinin yükselmeleriTikagrelor ile tedavi sırasında kreatinin düzeyleri yükselebilir. Mekanizma henüz açıklığa kavuşturulmamıştır. Böbrek fonksiyonları rutin tıbbi uygulamalara göre kontrol edilmelidir. AKShastalarında böbrek fonksiyonlarının, tikagrelor ile tedaviye başlandıktan bir ay sonra da kontroledilmesi, > 75 yaş hastalarda, orta şiddette veya şiddetli böbrek yetmezliği olan hastalarda ve biranjiyotensin reseptör blokörü (ARB) ile eşzamanlı tedavi alan hastalarda özellikle dikkatliolunması önerilir. Ürik asit artışıTikagrelor ile tedavi sırasında hiperürisemi oluşabilir (bkz. Bölüm 4.8). Hiperürisemi ya da gut artriti öyküsü olan hastalarda dikkat edilmesi önerilir. İhtiyati önlem olarak ürik asit nefropatisiolan hastalarda tikagrelor kullanımı önerilmemektedir. Trombotik Trombositopenik Purpura (TTP)Tikagrelor kullanımıyla ilgili olarak çok nadiren Trombotik Trombositopenik Purpura (TTP) bildirilmiştir. Nörolojik bulgular, böbrek disfonksiyonu ya da ateş ile ilişkili olabilentrombositopeni ve mikroanjiyopatik hemolitik anemi ile karakterizedir. TTP, plazmaferez de dahilacil tedavi gerektiren potansiyel olarak ölümcül bir durumdur. Heparin ile indüklenen trombositopeni (HIT) tanısı koymak için kullanılan trombosit fonksiyon testleri ile enterferansHIT tanısı koymak için kullanılan heparin ile indüklenen trombosit aktivasyonu (HIPA) testinde, hastanın serumunda bulunan anti-trombosit faktör 4/heparin antikorları, heparin varlığındasağlıklı donörlerin trombositlerini aktive eder. Tikagrelor uygulanan hastalarda, HIT için kullanılan trombosit fonksiyon testlerinde (HIPA testi dahildir, ancak bununla sınırlı olmayabilir) yanlış negatif sonuçlar bildirilmiştir. Bu durum, testiniçerdiği sağlıklı donörlere ait trombositler üzerindeki P 212reseptörünün hastanınserumundaki/plazmasındaki tikagrelor tarafından inhibe edilmesi ile ilgilidir. HIT trombositfonksiyon testlerinin yorumlanması için, tikagrelor ile eşzamanlı tedavi hakkında bilgi sağlanmasıgereklidir.HIT gelişen hastalarda, tikagrelor ile tedaviye devam edilmesinin yarar-risk değerlendirmesi, hem HIT'nin protrombotik durumu, hem de eşzamanlı antikoagülan ve tikagrelor tedavisinde artankanama riski dikkate alınarak yapılmalıdır. Diğerİdame ASA dozu ve klopidogrele kıyasla tikagrelorun bağıl etkililiğinin araştırıldığı PLATO çalışmasında gözlenmiş olan bir ilişki temel alınarak, tikagrelor ve 300 mg üzerindeki ASA'nınyüksek idame dozunun eşzamanlı uygulanması önerilmemektedir (bkz. Bölüm 5.1). Tedavinin erken kesilmesiTİLANTA dahil herhangi bir antitrombositik tedavinin erken kesilmesi, hastanın altta yatan hastalığına bağlı olarak kardiyovasküler (KV) ölüm, Mİ veya inme riskinde artışa neden olabilir.Bu nedenle tedavinin erken kesilmesinden kaçınılmalıdır. Bu tıbbi ürün her dozunda 1 mmol (23 mg)'dan daha az sodyum ihtiva eder; yani aslında sodyum içermez. 4.5. Diğer tıbbi ürünler ile etkileşimler ve diğer etkileşim şekilleriTikagrelor öncelikle bir CYP3A4 substratıdır ve zayıf bir CYP3A4 inhibitörüdür. Tikagrelor aynı zamanda bir P-glikoprotein (P-gp) substratı ve zayıf bir P-gp inhibitörüdür ve bu nedenle P-gpsubstratlarına maruziyeti artırabilir. Tıbbi ve diğer ürünlerin tikagrelor üzerindeki etkisiCYP3A4 i^nhibit^^leriGüçlü CYP3A4 inhibitörleri - Ketokonazolün tikagrelor ile birlikte uygulanmasıtikagrelorun Cmaks ve EAA değerlerini sırasıyla 2,4 kat ve 7,3 kat arttırmış, aktifmetabolitin Cmaks ve EAA değerleri sırasıyla %89 ve %56 azalmıştır. Diğer güçlü CYP3A4inhibitörlerinin (klaritromisin, nefazadon, ritonavir ve atanazavir) benzer etki göstermesibeklenir ve bu nedenle güçlü CYP3A4 inhibitörlerinin tikagrelor ile eş zamanlıkullanımları kontrendikedir (bkz. Bölüm 4.3). Orta dereceli CYP3A4 inhibitörleri - Diltiazemin tikagrelor ile birlikte uygulanmasıtikagrelorun Cmaks değerini %69, EAA değerini 2,7 kat artırmış ve aktif metabolitin Cmaksdeğerini %38 azaltmış, EAA değerini değiştirmemiştir. Tikagrelorun diltiazem plazmadüzeyleri üzerinde etkisi yoktur. Diğer orta dereceli CYP3A4 inhibitörlerinin de (örn.;amprenavir, aprepitant, eritromisin ve flukonazol) benzer bir etki göstermesi beklenir vebunlar tikagrelor ile aynı anda uygulanabilir. Her gün yüksek miktarlarda (3x200 ml) greyfurt suyu tüketimlerinin ardından tikagrelormaruziyetinde 2 kat artış gözlenmiştir. Bu boyutta bir maruziyet artışının çoğu hastadaklinik anlama sahip olması beklenmemektedir. CYP3A4 indükleyicileriRifampisinin tikagrelor ile birlikte uygulanması, tikagrelorun Cmaks ve EAA değerlerini sırasıyla %73 ve %86 azaltmıştır. Aktif metabolitin Cmaks değeri değişmemiş ve EAA değeri %46azalmıştır. Diğer CYP3A4 indükleyicilerinin (örn.; fenitoin, karbamazepin ve fenobarbital)tikagrelora maruziyeti azaltması beklenir. Tikagrelorun güçlü CYP3A indükleyicileri ile birlikteuygulanması, tikagrelor maruziyetini ve etkililiğini azaltabilir; bu nedenle tikagrelor ile eşzamanlıolarak uygulanmaları tercih edilmez. Siklosporin (P-gp ve CYP3A inhibitörü)Tikagrelor ile eş zamanlı olarak siklosporin (600 mg) uygulanması, tikagrelorun Cmaks ve EAA değerlerini sırasıyla 2,3 ve 2,8 kat artırmıştır. Siklosporin varlığında aktif metabolitin EAA değeri%32 artarken, Cmaks %15 azalmıştır. Tikagrelorun, güçlü P-glikoprotein (P-gp) inhibitörleri ve orta düzeyde CYP3A4 inhibitörleri (örn.; verapamil, kinidin) olan ve tikagrelor maruziyetini de artırabilecek diğer etkin maddelerleeşzamanlı kullanımına ilişkin veri mevcut değildir. Eğer bu ilişkiden kaçınılamıyorsa eşzamanlıkullanımda dikkatli olunmalıdır. DiğerleriKlinik farmakoloji etkileşim çalışmaları, tikagrelorun heparin, enoksaparin ve ASA veya desmopresin ile birlikte uygulanmasının, tek başına tikagrelor uygulanmasına kıyasla tikagrelorya da aktif metabolit farmakokinetiği ya da ADP'nin indüklediği trombosit agregasyonu üzerindeetkisi olmadığını göstermiştir. Klinik olarak endike olduğu takdirde, hemostazı değiştiren tıbbiürünler tikagrelor ile kombinasyon halinde uygulanırken dikkatle kullanılmalıdır. Morfinle tedavi uygulanan AKS'li hastalarda tikagrelor ve aktif metabolitinin de aralarında olduğu oral P 212212inhibisyonunun gerekligörüldüğü AKS'li hastalarda parenteral bir P2Yi2 inhibitörünün kullanılması düşünülebilir. Tikagrelorun diğer tıbbi ürünler üzerinde etkisiCYP3A4 ile metabolize olan tıbbi ürünler Sim-yastatin- Tikagrelor ve simvastatinin birlikte uygulanması, simvastatin Cmaks değerini%81, EAA değerini %56 artırmıştır ve bazı bireysel 2-3 kat artışlarla birlikte simvastatinasit Cmaks değerini %64 ve EAA değerini %52 artırmıştır. Tikagrelorun günde 40 mg'ı aşansimvastatin dozlarıyla birlikte uygulanması, simvastatinin advers etkilerinin meydanagelmesine neden olabilir ve böyle uygulamalara potansiyel yararlarla karşılaştırmayapılarak karar verilmelidir. Simvastatinin tikagrelor plazma düzeyi üzerinde etkisiyoktur. Tikagrelor lovastatin üzerinde de benzer etki gösterebilir. Tikagrelorun 40 mg'ınüzerindeki simvastatin veya lovastatin dozlarıyla eşzamanlı olarak uygulanması tavsiyeedilmemektedir. At^^astatin- Atorvastatin ve tikagrelorun birlikte uygulanması, atorvastatin asit Cmaksdeğerini %23 ve EAA değerini %36 artırmıştır. Tüm atorvastatin asit metabolitleri içinEAA ve Cmaks'ta benzer artışlar gözlenmiştir. Bu artışların klinik açıdan anlamlı olmadığıdüşünülmektedir. CYP3A4 ile metabolize olan diğer statinler üzerinde benzer bir etki çıkması dışlanamaz.PLATO çalışmasında yer alan ve tikagrelor alan hastalar çeşitli statinler kullanmışlar, butıbbi ürünleri alan PLATO kohort grubunun %93'ünde statin güvenliliği ile ilişkili birendişe yaşanmamıştır. Tikagrelor hafif bir CYP3A4 inhibitörüdür. Tikagrelor ile dar terapötik indekse sahip CYP3A4 substratlarının (örn.; sisaprid ya da ergot alkaloidleri) eşzamanlı uygulaması önerilmez; çünkütikagrelor bu tıbbi ürünlere maruziyeti artırabilir. P-slikoyrotein (P-gp) substratları (dişoksin, siklosporin dahil)Eşzamanlı tikagrelor uygulaması, digoksin Cmaks değerini %75, EAA değerini %28 artırmıştır. Tikagrelor ile eşzamanlı uygulanmasıyla ortalama taban digoksin düzeyleri yaklaşık olarak %30artmış, bazı kişilerdeki artış maksimum 2 kata kadar ulaşmıştır. Digoksin varlığında tikagrelorunve aktif metabolitinin Cmaks ve EAA değerleri etkilenmemiştir. Bu sebeple, digoksin gibi darterapötik indeksli ve P-gp bağımlı ilaçlar tikagrelor ile aynı anda verildiğinde uygun klinik ve/veyalaboratuvar takibinin yapılması önerilir. Tikagrelorun, siklosporin kan düzeyleri üzerinde etkisi olmamıştır. Tikagrelorun diğer P-gp substratları üzerindeki etkileri çalışılmamıştır. CYP2C9 ile metabolize olan tıbbi ürünlerTikagrelorun tolbutamid ile birlikte uygulanması, her iki tıbbi ürünün de plazma düzeylerini değiştirmemiş, bu da tikagrelorun CYP2C9 inhibitörü olmadığı ve varfarin ve tolbutamid gibiCYP2C9 bağımlı metabolize olan tıbbi ürünlerin metabolizmasını değiştirmeyeceği izleniminivermiştir. RosuvastatinTikagrelor, rosuvastatinin renal atılımını etkileyerek rosuvastatin birikimi riskini artırabilir. Kesin mekanizması bilinmese de, bazı durumlarda tikagrelor ve rosuvastatinin eş zamanlı kullanımırenal fonksiyonun azalmasına, CPK düzeyi ve rabdomiyolizin artmasına yol açmaktadır. Oral kontraseptiflerTikagrelorun levonorgestrel ve etinil estradiol ile birlikte uygulanması etinil estradiol maruziyetini yaklaşık %20 artırmış; fakat levonorgestrelin farmakokinetiğini değiştirmemiştir. Levonorgestrelve etinil estradiol tikagrelor ile birlikte uygulandığında oral kontraseptifin etkililiği üzerinde klinikolarak ilişkili bir etki beklenmemektedir. Bradikardi oluşturduğu bilinen tıbbi ürünlerÇoğunlukla asemptomatik olan ventriküler duraklamalar ve bradikardi gözlemleri nedeniyle, tikagrelorun bradikardiyi uyardığı bilinen ilaçlarla eşzamanlı uygulaması sırasında dikkatliolunmalıdır (bkz. Bölüm 4.4). Bununla birlikte, PLATO çalışmasında bradikardiyi uyardığıbilinen bir ya da daha fazla tıbbi ürünün (örn.; %96 beta blokörler, %33 kalsiyum kanal blokörleridiltiazem ve verapamil ve %4 digoksin) eşzamanlı uygulamasının ardından klinik açıdan anlamlıadvers reaksiyon kanıtı gözlenmemiştir. Diğer eşlik eden tedaviKlinik çalışmalarda birlikte uygulama koşulları için gerektiğinde tikagrelor, yaygın olarak ASA, proton pompası inhibitörleri, statinler, beta blokörler, anjiyotensin dönüştürücü enzim (ADE)inhibitörleri ve anjiyotensin reseptör blokörleri ile birlikte uzun dönemli olarak uygulanmış, ayrıcaheparin, düşük molekül ağırlıklı heparin ve intravenöz GpIIb/IIIa inhibitörleri ile birlikte kısasürelerle uygulanmıştır (bkz. Bölüm 5.1). Bu tıbbi ürünlerle klinik olarak anlamlı adversetkileşimlere dair herhangi bir kanıt gözlenmemiştir. Tikagrelorun, heparin, enoksaparin ya da desmopressin ile eşzamanlı uygulamasının aktive parsiyel tromboplastin zamanı (aPTz), aktif pıhtılaşma zamanı (APZ) ya da faktör Xa miktartestleri üzerinde etkisi olmamıştır. Bununla birlikte, potansiyel farmakodinamik etkileşimlernedeniyle, tikagrelorun hemostazı değiştirdiği bilinen tıbbi ürünlerle eş zamanlı uygulamasısırasında dikkatli olunmalıdır. Selektif serotonin geri alım inhibitörleri (SSRI) (örn.; paroksetin, sertralin ve sitalopram) ile kutanöz kanama anomalilerini içeren raporlar nedeniyle, kanama riskini artırabileceğindentikagrelor ile SSRI'lar uygulanırken dikkatli olunması önerilmektedir. 4.6. Gebelik ve laktasyonGenel tavsiyeGebelik kategorisi: C Çocuk doğurma potansiyeli bulunan kadınlar/Doğum kontrolü (Kontrasepsiyon)Tikagrelor ile tedavi gören çocuk doğurma potansiyeli olan kadınlar, gebe kalmamak için uygun bir doğum kontrol yöntemi kullanmalıdır. Gebelik dönemiTikagrelorun gebe kadınlarda kullanımına ilişkin veri yoktur veya sınırlıdır. Hayvanlarda yapılan çalışmalar üreme toksisitesini göstermiştir (Bkz. Bölüm 5.3). Tikagrelor hamilelik s l ras l ndaönerilmemektedir. Laktasyon dönemiHayvanlardan elde edilen farmakodinamik/toksikolojik veriler, tikagrelorun ve aktif metabolitlerinin süte geçtiğini göstermiştir (bkz. Bölüm 5.3). Yeni doğanlar/bebekler için risk gözardı edilememektedir. Çocuk için emzirmenin yararları ve kadın için tedavinin yararları dikkatealınarak, emzirmenin kesilmesine ya da tikagrelor tedavisinin kesilmesine/bu tedavidenkaçınılmasına karar verilmelidir. Üreme yeteneği/FertiliteTikagrelorun deney hayvanlarında dişi veya erkek fertilitesi üzerinde etkisi yoktur (bkz. Bölüm 5.3). 4.7. Araç ve makine kullanımı üzerindeki etkilerTikagrelorun araç ve makine kullanma yetisi üzerinde etkisi yoktur ya da göz ardı edilebilir etkilere sahiptir. Tikagrelor ile tedavi süresince sersemlik ve konfüzyon bildirilmiştir. Bu nedenle,bu semptomların görüldüğü hastalar araç veya makine kullanırken dikkatli olmalıdır. 4.8. İstenmeyen etkilerGüvenlilik profili özetiTikagrelorun güvenlilik profili 39,000'in üzerinde hastayı içeren iki büyük faz 3 sonuç çalışmasında (PLATO ve PEGASUS) değerlendirilmiştir (bkz. Bölüm 5.1). PLATO çalışmasında tikagrelor tedavisi alan hastalarda advers olaylar sebebiyle tedaviyi bırakma insidansı, klopidogrel kullanan hastalara göre daha yüksek olmuştur (%7,4'e karşın %5,4).PEGASUS çalışmasında tikagrelor tedavisi alan hastalarda advers olaylar sebebiyle tedaviyibırakma insidansı, tek başına ASA tedavisi ile karşılaştırıldığında daha yüksektir (tikagrelor 60mg + ASA için %16,1'e karşın tek başına ASA tedavisi için %8,5). Tikagrelor ile tedavi edilenhastalarda en yaygın bildirilen advers reaksiyonlar kanama ve dispnedir (bkz. Bölüm 4.4). Advers reaksiyonların tablolanmış özetiAşağıdaki advers reaksiyonlar, tikagrelor ile yapılan çalışmaları takiben ya da pazarlama sonrası deneyimde bildirilmiş olanlara göre tanımlanmıştır. Advers reaksiyonlar MedDRA Sistem Organ Sınıfına (SOC) göre listelenmiştir. Advers reaksiyonlar, her bir SOC içinde sıklık kategorilerine göre sıralanmıştır ve azalan ciddiyet sırasınagöre sunulmaktadır. Sıklıklar şu şekilde tanımlanır: Çok yaygın (>1/10); yaygın (>1/100 ila<1/10); yaygın olmayan (>1/1.000 ila <1/100); seyrek (>1/10.000 ila <1/1.000); çok seyrek(<1/10.000); bilinmiyor (eldeki verilerden hareketle tahmin edilemiyor). İyi huylu, kötü huylu ve belirtilmemiş neoplazmalar (Kist ve polipler de dahil olmak üzere)Yaygın olmayan: Tümör kanamalarıa Kan ve lenf sistemi hastalıklarıÇok yaygın: Kan hastalığı kanamalarıb Bilinmiyor: Trombotik Trombositopenik Purpurac Bağışıklık sistemi hastalıklarıYaygın olmayan: Anjiyoödem dahil aşırı duyarlılık reaksiyonlarıc Metabolizma ve beslenme hastalıklarıÇok yaygın: Hiperürisemid Yaygın: Gut/Gut artriti Psikiyatrik hastalıklarYaygın olmayan: Konfüzyon Sinir sistemi hastalıklarıYaygın: Sersemlik, senkop, baş ağrısı Yaygın olmayan: İntrakraniyal hemoraji Göz hastalıklarıYaygın olmayan: Göz hemorajisi® Kulak ve iç kulak hastalıklarıYaygın: VertigoYaygın olmayan: Kulak hemorajisi Kardiyak hastalıklarıBilinmiyor: Bradiaritmi, AV bloklama c Vasküler hastalıklarYaygın: Hipotansiyon Solunum, göğüs bozuklukları ve mediastinal hastalıklarÇok yaygın: DispneYaygın: Solunum sistemi kanamaları^ Gastrointestinal hastalıklarYaygın: Gastrointestinal hemorajig, diyare, bulantı, dispepsi, konstipasyon Yaygın olmayan: Retroperitoneal hemoraji Deri ve deri altı doku hastalıklarıYaygın: Deri altı veya deride kanamah, kaşıntı, döküntü Kas-iskelet bozuklukları, bağ doku ve kemik hastalıklarıYaygın olmayan: Kasta kanamalari Böbrek ve idrar yolu hastalıklarıYaygın: İdrar yolunda kanamaj Üreme sistemi ve meme hastalıklarıYaygın olmayan: Üreme sistemi kanamalarık AraştırmalarYaygın: Kan kreatinin düzeyinde artışd Yaralanma ve zehirlenme ve prosedüre ait komplikasyonlarYaygın: Post-prosedürel hemoraji, travmatik kanamalarl a örn.; mesane kanseri, gastrik kanser, kolon kanseri nedeniyle kanama. b örn.; morarmaya, spontan hematoma, hemorajik diatez eğilimde artış.c Pazarlama sonrası teşhis edilmiş deneyim 1 örn.; kontüzyon, travmatik hematom, travmatik hemoraji. m örn., spontan, prosedürle ilgili veya travmatik intrakranial hemoraji. Seçilen advers reaksiyonların tanımıKanamaPLATO çalışmasındaki kanama bulgularıPLATO çalışmasındaki kanama oranlarının genel sonucu Tablo 1'de gösterilmiştir. Tablo 1 - Genel kanama olaylarının analizi, 12 ayda Kaplan-Meier tahminleri (PLATO)
Kanama kategorilerinin tanımları:Majör Ölümcül/Yaşamı Tehdit Edici Kanama:veyaveyaveyaveyapressörler ya da cerrahi gerektiren şiddetli hipotansiyon veyahipovolemik şok.Majör Diğer:veyaanlamlı derecede engelleyici.TIMI Minör Kanama:Hemoglobinde 30-50 g/L azalma ile klinik olarak belirgin. |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
Tablo 2 - Genel kanama olaylarının analizi, 36 ayda Kaplan-Meier tahminleri (PEGASUS) | ||||||||||||||||||||||||||||||
| ||||||||||||||||||||||||||||||
|
Diğer TIMI majör |
1,6 |
3,61 (2,31, 5,65) |
0,5 |
<0,0001 |
|
TIMI Majör veya Minör |
3,4 |
2,54 (1,93, 3,35) |
1,4 |
<0,0001 |
|
TIMI Majör veya Minör veya Tıbbi müdahale gerektiren |
16,6 |
2,64 (2,35, 2,97) |
7,0 |
<0,0001 |
Güvenlilik sonlanım noktaları |
%KM |
Tehlike oranı (%95 GA) |
%KM |
^-değeri |
|
TIMI Majör veya Minör veya Tıbbi müdahale gerektiren |
16,6 |
2,64 (2,35, 2,97) |
7,0 |
<0,0001 |
PLATO tanımlı kanama kategorileri | ||||
|
PLATO Majör |
3,5 |
2,57 (1,95, 3,37) |
1,4 |
<0,0001 |
|
Ölümcüm/Yaşamı tehdit edici |
2,4 |
2,38 (1,73, 3,26) |
1,1 |
<0,0001 |
|
Diğer PLATO Majör |
1,1 |
3,37 (1,95, 5,83) |
0,3 |
<0,0001 |
|
PLATO Majör veya Minör |
15,2 |
2,71 (2,40, 3,08) |
6,2 |
<0,0001 |
Kanama kategorisi tanımları:
TIMI Majör:
Ölümcül kanama VEYA herhangi bir intrakraniyal kanama VEYA hemoglobinde (Hgb) >50 g/L'lik düşme veya Hgb mevcut olmadığında hemotokritte (Hct) %15'lik düşme ileilişkili klinik olarak belirgin hemoraji bulguları.Ölümcül:
7 gün içinde doğrudan ölüme yol açan bir kanama olayı.İK:
İntrakraniyal Kanama (İntrakraniyal hemoraji).Diğer TIMI Majör:
Ölümcül olmayan İK dışı TIMI Majör kanama.TIMI Minör:
Hemoglobinde 30-50 g/L azalma ile klinik olarak belirgin.Tıbbi müdahale gerektiren TIMI:
Müdahale gerektiren VEYA hastaneye yatışa yol açan VEYA değerlendirme gerektiren.PLATO Majör Ölümcül/Yaşamı tehdit edici:
Ölümcül kanama VEYA herhangi bir intrakraniyal kanama VEYA kardiyak tamponad ile intraperikardiyal VEYA presör/inotrop veyaameliyat gerektiren hipovolemik şok veya şiddetli hipotansiyon ile VEYA hemoglobinde >50 g/Lazalma ile klinik olarak belirgin VEYA > 4 ünite eritrosit transfüzyonu.PLATO Majör Diğer:
Anlamlı derecede engelleyici VEYA hemoglobinde 30-50 g/L azalma ile klinik olarak belirgin VEYA 2-3 ünite eritrosit transfüzyonu.PLATO Minör:
Kanamayı durdurmak veya tedavi etmek için tıbbi girişim gerektiren.PEGASUS çalışmasında, TIMI Majör kanamanın günde iki defa uygulanan tikagrelor 60 mg için tek başına ASA için olandan daha yüksek olduğu görülmüştür. Tek başına ASA tedavisiylekarşılaştırıldığında ölümcül kanama için kanama riskinde artış görülmemiş ve sadece intrakraniyalhemorajilerde küçük bir artış gözlenmiştir. tikagrelor 60 mg için 11 (%0,3), tek başına ASAtedavisi içinse 12 (%0,3) olmak üzere, az sayıda ölümcül kanama olayı ortaya çıkmıştır.Tikagrelor 60 mg ile TIMI Majör kanama riskinde gözlenen artışın nedeni, başlıca gastrointestinalsistem organ sınıfındaki olaylardan kaynaklanan diğer TIMI Majör kanama sıklığının daha yüksekolmasıdır.
TIMI Majöre benzer kanama paternlerinde artış, TIMI Majör veya Minör ve PLATO Majör ve PLATO Majör veya Minör kanama kategorileri için görülmüştür (bkz. Tablo 2). Kanamanedeniyle tedavinin kesilmesi tek başına ASA tedavisine kıyasla tikagrelor 60 mg ile dahayaygındır (sırasıyla %6,2 ve %1,5). Bu kanamaların büyük çoğunluğu burun kanaması, morarmave hematomlar gibi daha düşük ciddiyette (TIMI tıbbi müdahale gerektiren olarak sınıflandırılmış)kanamalardır.
Tikagrelor 60 mg'ın kanama profili TIMI Majör, TIMI Majör veya Minör ve PLATO Majör kanama olayları için çoklu önceden tanımlanmış alt gruplar arasında (örn.; yaş, cinsiyet, kilo, ırk,coğrafik bölge, eşzamanlı rahatsızlıklar, eşzamanlı tedavi ve tıbbi öykü) tutarlı bulunmuştur.
İntrakraniyal kanama:
Spontan intrakraniyal hemorajiler tikagrelor 60 mg ve tek başına ASA tedavisi için benzer oranlarda bildirilmiştir (her iki tedavi grubunda da n=13, %0,2). Travmatik ve prosedürle ilişkiliintrakraniyal hemorajiler tek başına ASA tedavisine (n=10, %0,1) kıyasla tikagrelor 60 mgtedavisi ile küçük bir artış göstermiştir (n=15, %0,2). Tikagrelor 60 mg ile 6 ölümcül intrakraniyalkanama ve tek başına ASA tedavisi ile 5 ölümcül intrakraniyal kanama meydana gelmiştir.İntrakraniyal kanama insidansı, araştırma altındaki popülasyonun anlamlı komorbidite vekardiyovasküler risk faktörleri dikkate alındığında her iki tedavi grubunda da düşük olmuştur.
Dispne
Tikagrelor ile tedavi edilen hastalarda bir tür nefessizlik hissi olan dispne bildirilmiştir. PLATO çalışmasında dispne advers olayları (AO'lar) (dispne, dinlenme sırasında dispne, efor dispnesi,paroksimal nokturnal dispne ve nokturnal dispne), kombine edildiğinde, tikagrelor alan hastaların%13,8'inde, klopidogrel alan hastaların %7,8'inde rapor edilmiştir. Tikagrelor alan hastaların%2,2'sinde ve klopidogrel alan hastaların %0,6'sında araştırmacılar dispnenin PLATOçalışmasındaki tedaviyle nedensel olarak bağlantılı olduğunu düşünmüştür ve yalnızca birkaçıciddi olarak değerlendirilmiştir (%0,14 tikagrelor; %0,02 klopidogrel) (bkz. Bölüm 4.4).Bildirilen dispne semptomlarının çoğu hafif ila orta şiddette olmuş ve çoğu, tedaviyebaşlanmasından sonraki erken dönemle tek bir epizot olarak bildirilmiştir.
Klopidogrel ile karşılaştırıldığında, tikagrelor ile tedavi edilen astım/KOAH hastalarında ciddi olmayan dispne (tikagrelor ile %3,29'a karşın klopidogrel ile %0,53) ve ciddi dispne (tikagrelorile %0,38'e karşın klopidogrel ile %0,00) yaşama riski artabilir. Mutlak terimler açısından risk,genel PLATO popülasyonundan daha yüksek olabilir. Tikagrelor, astım ve/veya KOAH öyküsübulunan hastalarda dikkatli kullanılmalıdır (bkz. Bölüm 4.4).
Epizotların yaklaşık %30'u 7 gün içinde düzelmiştir. PLATO çalışmasına başlangıçta konjestif kalp yetmezliği, KOAH ya da astımı olan hastalar dahil edilmiştir; bu hastalar ve yaşlıların dispnebildirme olasılıkları daha fazla olmuştur. Tikagrelor için hastaların %0,9'u dispne nedeniyleçalışmayı bırakırken, klopidogrel alanlarda bu oran %0,1 olmuştur. Tikagrelor ile ortaya çıkandaha yüksek dispne insidansı, yeni ya da kötüleşen kalp ya da akciğer hastalığı ile ilişkili değildir(bkz. Bölüm 4.4). Tikagrelor akciğer fonksiyonu testlerini etkilememektedir.
PEGASUS çalışmasında dispne, günde iki kez tikagrelor 60 mg alan hastaların %14,2'sinde ve tek başına ASA alan hastaların %5,5'inde bildirilmiştir. PLATO çalışmasında en çok bildirilendispne olayları hafif ila orta şiddete olmuştur (bkz. Bölüm 4.4). Dispne bildiren hastalar daha yaşlıolma ve daha sık olarak da temelde dispne, KOAH veya astım hastası olma eğilimindedir.
Araştırmalar
Ürik asit yükselmeleri: PLATO çalışmasında, klopidogrel alan hastalar ile %13 olan oran ile kıyaslandığında tikagrelor alan hastaların %22'sinde serum ürik asit, normalin üst sınırından dahafazla yükselmiştir. PEGASUS çalışmasında karşılık gelen değerler tikagrelor 90 mg, 60 mg veplasebo için sırasıyla %9,1, %8,8 ve %5,5 olmuştur. Ortalama serum ürik asit klopidogrel ileyaklaşık %7,5 olan oran ile karşılaştırıldığında tikagrelor ile yaklaşık %15 artmış ve tedavidurdurulduktan sonra tikagrelor tedavisinde yaklaşık %7'ye düşmüştür; ancak klopidogrel ile birazalma gözlenmemiştir. PEGASUS çalışmasında tikagrelor 90 mg ve 60 mg için ortalama serumürik asit düzeylerinde sırasıyla %6,3 ve %5,6'lık geri dönüşlü yükselmeler bulunmuş, plasebogrubunda ise %1,5'lik bir azalma yaşanmıştır. PLATO çalışmasında gut artriti sıklığı tikagreloriçin %0,2'ye karşın klopidogrel için %0,1 bulunmuştur. PEGASUS çalışmasında gut/gut artritiiçin karşılık gelen değerler tikagrelor 90 mg, 60 mg ve plasebo için sırasıyla %1,6, %1,5 ve%1,1'dir.
Şüpheli advers reaksiyonların raporlanması
Ruhsatlandırma sonrası şüpheli ilaç advers reaksiyonlarının raporlanması büyük önem taşımaktadır. Raporlama yapılması, ilacın yarar/risk dengesinin sürekli olarak izlenmesine olanaksağlar. Sağlık mesleği mensuplarının herhangi bir şüpheli advers reaksiyonu TürkiyeFarmakovijilans Merkezi (TÜFAM)'ne bildirmeleri gerekmektedir
(www.titck.gov.tr:[email protected]:4.9. Doz aşımı ve tedavisi
Tikagrelor 900 mg'a kadar olan tekli dozlarda iyi tolere edilir. Gastrointestinal toksisitenin, tekli yükselen doz çalışmasında doz sınırlayıcı olduğu belirlenmiştir. Doz aşımı ile ortaya çıkabilecekdiğer klinik olarak anlamlı advers etkiler arasında dispne ve ventriküler bradikardiler mevcuttur(bkz. Bölüm 4.8).
Doz aşımı durumunda yukarıdaki potansiyel advers reaksiyonlar meydana gelebilir ve bu durumda EKG takibi düşünülmelidir.
Henüz tikagrelorun etkilerini tersine çevirecek bilinen bir antidot yoktur ve tikagrelorun diyalizle temizlenebilir değildir (bkz. Bölüm 5.2). Doz aşımı tedavisinde yerel standart tıbbi tedbirleralınmalıdır. Aşırı tikagrelor dozunda, beklenen etki platelet inhibisyonuna bağlı olarak kanamariski süresinin uzamasıdır. Platelet transfüzyonunun kanama bulunan hastalarda klinik yararsağlaması mümkün değildir (bkz. Bölüm 4.4). Eğer kanama gözlenirse, uygun destekleyicitedbirler alınmalıdır.
5. FARMAKOLOJİK ÖZELLİKLER5.1. Farmakodinamik özellikler
Farmakoterapötik grup: Trombosit agregasyon inhibitörleri (Heparin hariç)
ATC kodu: B01AC24
Etki mekanizması
TİLANTA, oral, doğrudan etkili, selektif ve geri dönüşümlü olarak bağlanan bir P2Yi2 reseptör antagonisti olan ve ADP-aracılı P2Yi2'ye bağımlı trombosit aktivasyonunu ve agregasyonunuinhibe eden, siklopentiltriazolopirimidin (SPTP) kimyasal sınıfının bir üyesi olan tikagreloriçermektedir. Tikagrelor ADP'nin reseptöre bağlanmasını engellemez ancak P2Yi2 reseptörünebağlandığı zaman ADP-uyarılı sinyal iletimini engeller. Trombositler aterosklerotik hastalığıntrombotik komplikasyonlarının başlaması ve/veya gelişmesine katıldıkları için, trombositfonksiyonu inhibisyonunun ölüm, Mİ veya inme gibi KV olay riskini azalttıkları gösterilmiştir.Tikagrelor, aynı zamanda dengeleyici nükleozid taşıyıcısı-1 (ENT-l)'i inhibe ederek lokalendojen adenozin düzeylerini de arttırır.
Tikagrelorun, sağlıklı kişilerde ve AKS hastalarında aşağıdaki adenozin-uyarılı etkileri arttırdığı belgelenmiştir: vazodilatasyon (sağlıklı gönüllüler ve AKS hastalarında koroner kan akışıartışlarıyla ölçülür; baş ağrısı), trombosit fonksiyonu inhibisyonu
(in vitro
olarak insanda tamkanda) ve dispne. Bununla birlikte, gözlemlenen adenozin artışları ve klinik sonuçlar (örn.;morbidite-mortalite) arasındaki bağlantı açıkça ortaya konmamıştır.Farmakodinamik etkiler
Etkinin başlaması
ASA tedavisi görmekte olan stabil koroner arter hastalığı (KAH) olan hastalarda, tikagrelor, 0,5 saatte 180 mg yükleme dozundan sonra yaklaşık %41'lik ortalama trombosit agregasyoninhibisyonu (TAİ) değeri ile hızlı farmakolojik etki başlangıcı göstermiştir; %89'luk maksimumTAİ etkisi dozdan 2-4 saat sonra ortaya çıkmış ve 2-8 saat arasında sürmüştür. Dozdan 2 saatsonra hastaların %90'ında nihai kapsamlı TAİ > %70'dir.
Etkinin sonlanması
Eğer KABG prosedürü planlanıyorsa, tikagrelorun prosedürden önce 96 saatten daha kısa bir süre içerisinde kesilmesi durumunda tikagrelor kanama riski klopidogrele göre artmaktadır.
Geçiş verileri
Klopidogrel 75 mg'dan günde iki kez tikagrelor 90 mg'a geçiş, %26,4 mutlak TAİ artışı ile sonuçlanır ve tikagrelordan klopidogrele geçiş %24,5 mutlak TAİ azalması ile sonuçlanır.Hastalar antitrombositik etkide herhangi bir kesinti olmaksızın klopidogrelden tikagreloregeçebilir (bkz. Bölüm 4.2).
Klinik etkililik ve güvenlilik
Tikagrelorun etkililiği ve güvenliliği için klinik bulgular iki faz 3 çalışmasından elde edilmiştir:
PLATO
[PLAT
elet Inhibition and Patient Outcomes] çalışması, her ikisi de ASA ve diğerstandart tedavi ile kombinasyon halinde verilen tikagrelorun klopidogrel ilekarşılaştırılması PEGASUS TIMI-54 [PrEvention with TicaGrelor of SecondAry Thrombotic Events inHigh-RiSk AcUte Coronary Syndrome Patients] çalışması, ASA ile kombinasyon halindetikagrelor tedavisinin tek başına ASA tedavisi ile karşılaştırılması
PLATO çalışması (Akut Koroner Sendromlar)
PLATO çalışması, stabil olmayan anjina (UA), ST yükselmesiz miyokard enfarktüsü (NSTEMI) veya ST yükselmeli miyokard enfarktüsü (STEMI) semptomlarının başlangıçlarının 24 saatiiçinde bulunan ve öncelikle tıbbi olarak veya perkutan koroner girişim (PKG) veya KABG iletedavi edilen 18.624 hastayı kapsamaktadır.
Klinik etkililik
Günde bir defa ASA uygulanan arka plan tedavisinde, günde iki defa 90 mg tikagrelorun KV ölüm, Mİ veya inmeden oluşan kompozit sonlanım noktasını önleme açısından günde bir defa 75mg klopidogrelden üstün olduğu görülmüş olup, farka KV ölüm ve Mİ neden olmuştur. Hastalara300 mg klopidogrel yükleme dozu (PKG uygulanacaksa 600 mg da verilebilir) veya 180 mgtikagrelor verilmiştir.
Bu sonuç erken dönemde ortaya çıkmış (30 günde mutlak risk azalması [MRA] %0,6 ve nispi risk azalması [NRA] %12), 12 aylık dönem süresince istikrarlı bir tedavi etkisi söz konusu olmuş,%16'lık NRA ile senede %1,9'luk MRA sağlanmıştır. Bu sonuçlar, hastaların 12 ay süreyle gündeiki kez tikagrelor 90 mg ile tedavi edilmesinin uygun olduğunu göstermektedir (bkz. Bölüm 4.2).54 AKS hastasının klopidogrel yerine tikagrelor ile tedavi edilmesi, 1 aterotrombotik vakayıönleyecek; 91 hastanın tedavi edilmesi ise 1 KV ölümü önleyecektir (bkz. Şekil 1 ve Tablo 3).
Tikagrelorun klopidogrele kıyasla tedavi etkisi; kilo, cinsiyet, diyabet tıbbi öyküsü, geçici iskemik atak veya hemorajik olmayan inme veya revaskülarizasyon; heparinler, GpIIb/IIIa inhibitörleri veproton pompası inhibitörleri içeren eşzamanlı tedaviler (bkz. Bölüm 4.5); nihai indeks olgu tanısı(STEMI, NSTEMI veya UA) ve randomizasyonda hedeflenen tedavi yolağı (invazif veya tıbbi)dahil olmak üzere pek çok alt grup arasında tutarlıdır.
Birincil sonlanım noktasına ait tehlike oranının (TO) Kuzey Amerika'da klopidogreli desteklediği; ancak dünyanın geri kalanında tikagreloru desteklediği düşük düzeyde anlamlı birtedavi etkileşimi gözlenmiş olup, bu etkileşimin incelenen genel popülasyonun yaklaşık %10'unutemsil ettiği görülmüştür (etkileşim p-değeri = 0,045). Araştırmaya yönelik analizler, ASAdozunun artmasıyla birlikte tikagrelor ile etkililiğinin azaldığı gözlendiği için ASA dozuyla olasıbir ilişki olduğunu ortaya koymaktadır. Tikagrelor ile birlikte verilecek olan kronik günlük ASAdozları 75 - 150 mg olmalıdır (Bkz. Bölüm 4.2 ve 4.4).
Şekil 1'de bileşik etkililik sonlanım noktasında herhangi bir olayın tahmini ilk görülme riski gösterilmektedir.
Şekil 1 - KV ölüm, Mİ ve inmenin birincil klinik bileşik sonlanım noktası analizi (PLATO)
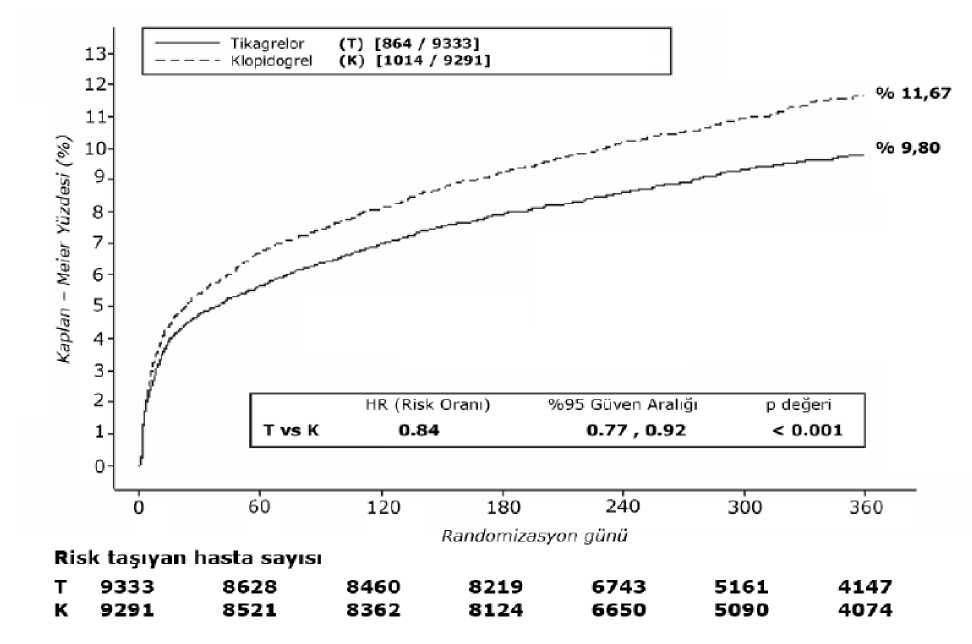
Tikagrelor, klopidogrel ile kıyaslandığında hem UA/NSTEMI hem de STEMI popülasyonunda birincil bileşik sonlanım noktasının ortaya çıkmasını azaltır (Tablo 3). Dolayısıyla, medikal tedavigören hastalar ve perkutan koroner girişim (PKG) ya da koroner bypass grefti (KABG) ile tedaviedilen hastalar dahil olmak üzere AKS hastalarında (stabil olmayan anjina, ST yükselmesizMiyokart İnfarktüsü [NSTEMI] ve ST yükselmeli Miyokart İnfarktüsü [STEMI]) düşük doz ASAile birlikte günde iki kez TİLANTA 90 mg kullanılabilir.
Tablo 3- Birincil ve ikincil etkililik sonlanım noktalarının analizi (PLATO)
|
|
Günde iki kez tikagrelor90 mg (olayyaşayan hasta%'si)N=9333 |
Günde bir kez klopidogrel 75 mg (olayyaşayanhasta %'si)N=9291 |
MRAa(%/yıl) |
NRAa (%) (%95 GA) |
p-değeri |
|
KV ölüm, Mİ (sessiz Mİhariç) ya dainme |
9,3 |
10,9 |
1,9 |
16 (8, 23) |
0,0003 |
|
İnvazif müdahale |
8,5 |
10,0 |
1,7 |
16 (6, 25) |
0,0025 |
|
Medikal müdahale |
11,3 |
13,2 |
2,3 |
15 (0,3, 27) |
0.0444d |
|
KV ölüm |
3,8 |
4,8 |
1,1 |
21 (9, 31) |
0,0013 |
|
Mİ (sessiz Mİ hariç)b |
5,4 |
6,4 |
1,1 |
16 ( 525) |
0,0045 |
|
İnme |
1,3 |
1,1 |
-0,2 |
-17 (-52, 9) |
0,2249 |
|
Tüm nedenlere bağlı mortalite, Mİ (sessiz Mİhariç) ya dainme |
9,7 |
11,5 |
2,1 |
16 (8, 23) |
0,0001 |
|
KV ölüm, toplam Mİ,inme, CRİ,RI, GİA yada diğerATOc |
13,8 |
15,7 |
2,1 |
12 (5, 19) |
0,0006 |
|
Tüm nedenlere bağlı mortalite |
4,3 |
5,4 |
1,4 |
22 (11, 31) |
0.0003d |
|
Belirli stent trombozu |
1,2 |
1,7 |
0,6 |
32 (8, 49) |
0,0123d |
aMRA = mutlak risk azalması; NRA = nispi risk azalması = (1-Tehlike oranı) x %100. Negatif NRA nispi risk artışını göstermektedir.bSessiz Mİ hariç.
cCRİ = Ciddi reküren iskemi; RI = Reküren iskemi; GİA = Geçici iskemik atak; ATO = Arteriyel trombotik olay. Toplam Mİ, sessiz Mİ'yi içerir ve olayın tarihi, keşfedildiği tarih olarak belirlenir.dNominal anlamlılık değeri; tüm diğerleri önceden tanımlanmış hiyerarşi testine göre resmi olarakve istatistiksel açıdan anlamlıdır.
PLATO genetik alt çalışması
PLATO çalışmasında 10.285 hastanın CYP2C19 ve ABCB1 genotiplerinin belirlenmesi, genotip gruplarının PLATO sonuçlarıyla ilişkilerini ortaya koymuştur. Tikagrelorun klopidogrele göremajör KV olayları azaltmadaki üstünlüğü, hastanın CYP2C19 ya da ABCB1 genotipinden anlamlıoranda etkilenmemiştir. Genel PLATO çalışmasına benzer şekilde, toplam PLATO majörkanama, CYP2C19 ya da ABCB 1 genotipinden bağımsız olarak tikagrelor ve klopidogrel arasındafarklılık göstermemiştir. KABG olmayan PLATO majör kanama, bir ya da daha fazla CYP2C19fonksiyon kaybı alleli olan hastalarda klopidogrel ile karşılaştırıldığında tikagrelor ile artışgöstermiştir; fakat fonksiyon kaybı alleli olmayan hastalarda klopidogrele benzerdir.
Kombine etkililik ve güvenlilik bileşimi
Kombine etkililik ve güvenlilik bileşimi (KV ölüm, Mİ, inme veya PLATO tanımlı toplam majör kanama) klopidogrel ile karşılaştırıldığında tikagrelorun etkililiğindeki faydanın,AKS'den sonraki 12 ayda majör kanama olayları ile dengelenmediğini göstermektedir (MRA%1,4, NRA %8, TO 0,92; p=0,0257).
Klinik güvenlilik
Holter alt çalışması:
PLATO çalışması sırasında ventriküler duraklamaların ve diğer aritmik epizotların ortaya çıkışını incelemek üzere araştırmacılar yaklaşık 3000 hastadan oluşan bir alt grupta Holter izlemiyapmıştır; bu hastaların yaklaşık 2000'nininde hem AKS'lerinin akut fazında hem de bir aysonrasında kayıtlar mevcuttur. İncelenen primer değişken, > 3 saniyelik ventrikülerduraklamaların ortaya çıkmasıdır. Akut fazda klopidogrele (%3,5) göre tikagrelor (%6,0) ile dahafazla hastada ventriküler duraksamalar olmuştur, 1 ay sonra bu oranlar sırasıyla %2,2 ve %1,6'dır(Bkz. Bölüm 4.4). AKS'nin akut fazında ventriküler duraklamalardaki artış, KKY öyküsü olantikagrelor hastalarında daha belirgin olmuştur (KKY öyküsü olmayan hastalarda %9,2'ye karşı%5,4; klopidogrel hastalarında, KKY öyküsü olmayanlarda %3,6'ya karşı %4,0). Bu dengesizlikbir ayda ortaya çıkmamıştır: KKY öyküsü olan ve olmayan tikagrelor hastaları için sırasıyla%2,0'a karşı %2,1 ve klopidogrel ile %3,8'e karşı %1,4'tür. Bu hasta popülasyonunda budengesizlik ile ilişkili advers klinik sonuçlar söz konusu olmamıştır (pacemaker yerleştirilmesidurumları dahil).
PEGASUS Çalışması (Miyokart İnfarktüsü Öyküsü)
PEGASUS TIMI-54 çalışması, Mİ öyküsü ve aterotromboz açısından ek risk faktörleri olan hastalarda tek başına ASA tedavisi ile karşılaştırıldığında düşük doz ASA (75-150 mg) ilekombinasyon halinde 2 doz şeklinde (ya günde iki kez 90 mg ya da günde iki kez 60 mg) verilentikagrelor ile aterotrombotik olayların önlenmesini değerlendiren 21.162 hastalı, olayların yönverdiği, randomize, çift kör, plasebo kontrollü, paralel gruplu, uluslararası çok merkezli birçalışmadır.
50 yaş veya üzeri, Mİ öyküsü (randomizasyondan 1 ila 3 yıl önce) ve aşağıdaki aterotromboz risk faktörlerinden en azından birine sahip hastalar çalışmaya katılım açısından uygun bulunmuştur:>65 yaş, ilaç tedavisi gerektiren diabetes mellitus, önceden geçirilmiş ikinci bir Mİ, çoklu damarKAH bulgusu veya son evre olmayan kronik böbrek fonksiyon bozukluğu.
Hastalar şu durumlarda çalışmaya katılım açısından uygunsuz bulunmuştur: Çalışma süresince P2Y12 reseptör antagonisti, dipiridamol, silostazol veya antikoagülan tedavisi planlanmışsa;pıhtılaşma bozukluğu varsa veya iskemik inme veya intrakraniyal kanama öyküsü varsa, santralsinir sistemi tümörü veya bir intrakraniyal vasküler anomali varsa; önceki 6 ay içindegastrointestinal kanamaları olmuşsa veya önceki 30 gün içinde majör ameliyat geçirmişlerse.
Klinik etkililikŞekil 2 - KV ölüm, MI ve inmenin birincil klinik bileşik sonlanım noktası analizi (PEGASUS)
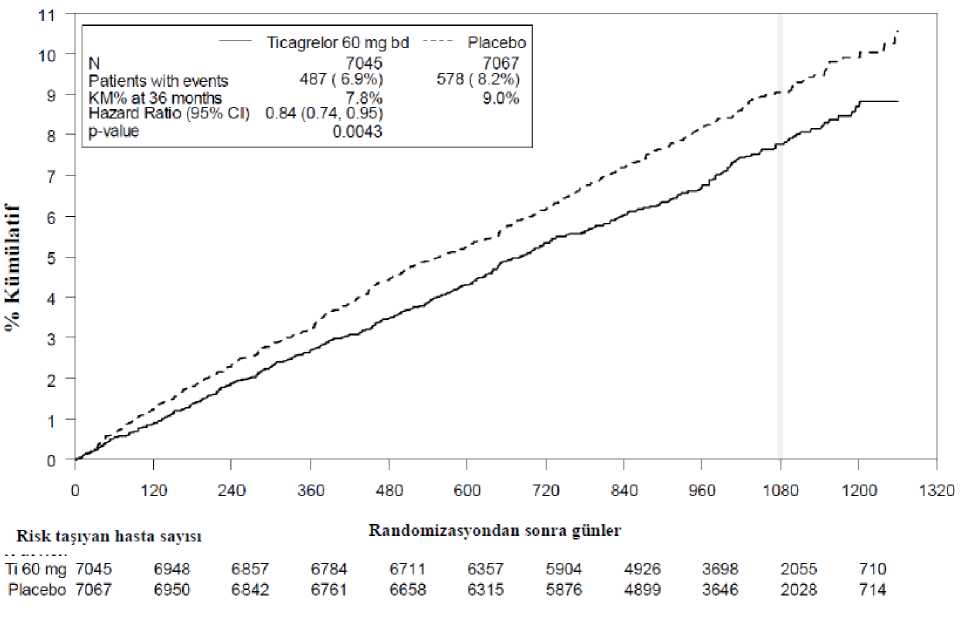
Tablo 4 - Birincil ve İkincil Etkililik Sonlanım Noktalarının Analizi (PEGASUS) | |||||||||||||||||||||||||||
| |||||||||||||||||||||||||||
|
KV ölüm |
174 (%2,5) |
%2,9 |
0,83 (0,68, 1,01) |
210 (%3,0) |
%3,4 |
0,0676 |
|
Mİ |
285 (%4,0) |
%4,5 |
0,84 (0,72, 0,98) |
338 (%4,8) |
%5,2 |
0,0314 |
|
İnme |
91 (%1,3) |
%1,5 |
0,75 (0,57, 0,98) |
122 (%1,7) |
%1,9 |
0,0337 |
|
İkincil sonlanım noktası | ||||||
|
KV ölüm |
174 (%2,5) |
%2,9 |
0,83 (0,68, 1,01) |
210 (%3,0) |
%3,4 |
- |
|
Tüm nedenlere bağlı mortalite |
289 (%4,1) |
%4,7 |
0,89 (0,76, 1,04) |
326 (%4,6) |
%5,2 |
|
Tehlike oranı ve ^-değerleri, tek açıklayıcı değişken olarak tedavi grubu ile Cox orantılı tehlikeler modelinden hareketle tek başına ASA tedavisine karşın tikagrelor için ayrı ayrı hesaplanır.
36 ayda hesaplanan Kaplan-Meier yüzdesi.
Not: KV ölüm, Mİ ve İnme bileşenleri için ilk olayların sayısı her bir bileşen için ilk olayların gerçek sayısı olup, bileşik sonlanım noktasındaki olay sayısına ilave edilmez.
(s) İstatistiksel anlamı belirtir.
GA=Güven aralığı; KV=Kardiyovasküler; TO=Tehlike oranı; KM=Kaplan-Meier;
Mİ=Miyokard infarktüsü.
ASA ile kombinasyon halinde hem günde iki kez 60 mg hem de günde iki kez 90 mg tikagrelor rejimleri çalışma periyodu boyunca tutarlı bir tedavi etkisi ile aterotrombotik olaylarınönlenmesinde (bileşik sonlanım noktası: KV ölüm, Mİ ve inme) tek başına ASA'dan üstün olup,tikagrelor 60 mg için %16 nispi risk azalması (NRA) ve %1,27 mutlak risk azalması (MRA) vetikagrelor 90 mg için %15 NRA ve %1,19 MRA değerlerini vermektedir.
90 mg ve 60 mg'ın etkililik profili benzer olmasına rağmen, daha düşük dozun kanama ve dispne riski ile ilişkili olarak daha iyi güvenlilik profiline ve tolerabiliteye sahip olduğuna dair kanıtlarbulunmaktadır. Bu nedenle, ASA ile birlikte yalnızca günde iki kez uygulanan tikagrelor 60 mgMİ öyküsü olan ve aterotrombotik olay gelişimi açısından yüksek risk taşıyan hastalardaaterotrombotik olayların (KV ölüm, Mİ ve inme) önlenmesi için önerilmektedir.
Tek başına ASA'ya göre günde iki kez tikagrelor 60 mg KV ölüm, Mİ ve inme birincil bileşik sonlanım noktasını anlamlı olarak azaltır. Bileşenlerin her biri birincil bileşik sonlanım noktasındaazalmaya katkıda bulunmuştur (KV ölüm %17 NRA, Mİ %16 NRA ve inme %25 NRA).
Birinci günden 360. güne kadar (%17 NRA) ve 361 gün ve sonrasındaki (%16 NRA) bileşik sonlanım noktası NRA'ları benzerdir. Uzatılmış tedaviden 3 yıl sonrasında tikagrelore ait etkililikve güvenlilik verileri sınırlıdır.
Mİ'den 2 yıldan fazla bir sürede klinik olarak stabil olan hastalarda veya önceki ADP reseptör inhibitörü tedavisi bırakıldıktan sonra bir yıldan fazla süre geçtiğinde günde iki kere tikagrelor 60mg uygulandığında fayda olduğu yönünde kanıt söz konusu olmamıştır (KV ölüm, Mİ ve inmedebirincil bileşik sonlanım noktasında azalma yoktur; ancak majör kanamada artış vardır) (ayrıcaBkz. Bölüm 4.2).
Klinik güvenlilik
Kanama ve dispne nedeniyle tikagrelor 60 mg ile tedaviyi kesme oranı, >75 yaş hastalarda (%42), daha genç hastalar ile karşılaştırıldığında daha yüksek olmuş (%23 - %31 aralığında), >75 yaşhastalarda plaseboya karşın fark %10'dan yüksek bulunmuştur (%42'ye karşın %29).
Pediyatrik popülasyon
Randomize, çift kör, paralel gruplu bir Faz III çalışmasında (HESTIA 3), orak hücre hastalığı olan 193 pediyatrik hasta (2 ila 18 yaş altı), vücut ağırlığına bağlı olarak günde iki kez 15 mg ila 45mg dozlarında plasebo veya tikagrelor alacak şekilde randomize edilmiştir. Tikagrelor, kararlıdurumda doz öncesi %35 ve dozdan 2 saat sonra %56 medyan trombosit inhibisyonu ilesonuçlanmıştır.
Plasebo ile karşılaştırıldığında, tikagrelorun vazo-okluzif krizlerin oranı üzerinde faydalı bir tedavi edici etkisi olmamıştır.
Avrupa İlaç Ajansı, akut koroner sendromlar (AKS) ve miyokard enfarktüsü (Mİ) öyküsüne sahip pediyatrik popülasyonun tüm alt kümelerinde tikagrelor ile çalışma sonuçlarını sunmazorunluluğunu iptal etmiştir (pediyatrik kullanım hakkında bilgi için Bkz. Bölüm 4.2).
5.2. Farmakokinetik özelliklerGenel özellikler
Emilim
Tikagrelorun emilimi, ortalama tmaks değeri 1,5 saat olup hızlıdır. Tikagrelorun dolaşımdaki başlıca metaboliti AR-C124910XX'in (aynı zamanda aktif metaboliti) oluşumu yaklaşık 2,5 saatortalama tmaks değeri ile hızlıdır. 90 mg tikagrelorun sağlıklı gönüllülerde açlık koşulları altındaoral olarak uygulanmasının ardından Cmaks değeri 529 ng/ml ve EAA değeri 3451 ng*s/ml'dir.Ana metabolit oranları Cmaks için 0,28 ve EAA için 0,42'dir. Mİ öyküsü olan hastalarda tikagrelorve AR-C124910XX'in farmakokinetiği, AKS popülasyondaki ile genel olarak benzer olmuştur.PEGASUS çalışmasının popülasyon farmakokinetik analizine dayalı olarak, medyan tikagrelorCmaks değeri 391 ng/mL ve tikagrelor 60 mg için kararlı durumda EAA değeri 3801 ng*s/mL'dir.Tikagrelor 90 mg için kararlı durumda Cmaks 627 ng/mL ve EAA 6255 ng*s/mL'dir.
Tikagrelorun ortalama mutlak biyoyararlanımının %36 olması tahmin edilmektedir. Yüksek yağlı beslenmenin tikagrelorun Cmaks değerinde ve aktif metabolitin EAA değerinde herhangi bir etkisiyoktur, fakat tikagrelorun EAA değerinde %21'lik artışa ve aktif metabolitin Cmaks değerinde%22'lik azalmaya neden olmuştur. Bu küçük değişikliklerin minimal klinik öneme sahip olduğudeğerlendirilmektedir, bu sebeple tikagrelor yemeklerle birlikte veya ayrı olarak alınabilir.Tikagrelor ve aktif metabolit, P-gp substratlarıdır.
Ezilmiş ve suyla karıştırılmış tikagrelor tabletler, oral olarak ya da bir nazogastrik tüp aracılığıyla mideye uygulandığında, tikagrelor ve aktif metabolitin EAA ve Cmaks değerleri açısından, tamtabletlerle benzer bir biyoyararlanıma sahiptir. Ezilmiş ve suyla karıştırılmış tikagrelortabletlerden başlangıç maruziyeti (dozdan 0,5 ve 1 saat sonra) tam tabletlere kıyasla daha yüksekolmuş, daha sonra (2 ila 48 saat) genellikle benzer bir konsantrasyon profili ortaya çıkmıştır.
Dağılım
Tikagrelorun kararlı durum dağılım hacmi 87,5 litredir. Tikagrelor ve aktif metaboliti insan plazma proteinine büyük ölçüde bağlanır (> %99,0).
Biyotransformasyon
CYP3A4, tikagrelorun metabolizmasından ve aktif metabolitin oluşumundan sorumlu majör enzimdir ve diğer CYP3A substratları ile etkileşimleri aktivasyondan inhibisyona kadardeğişebilir.
Tikagrelorun majör metaboliti AR-C124910XX olup, aynı zamanda trombosit P2Yi2 ADP-reseptörüne
in vitro
bağlanması değerlendirildiğinde etkili olduğu da bulunmuştur. Aktif metabolite sistemik maruziyet, tikagrelor için elde edilenin yaklaşık %30-40'ıdır.Eliminasyon
Tikagrelor eliminasyonunun primer yolu hepatik metabolizmadır. Radyoizotopla işaretli tikagrelor uygulandığında, radyoaktivitenin ortalama geri eldesi yaklaşık olarak %84'tür (feçeste%57,8, idrarda %26,5). Tikagrelor ve aktif metabolitinin idrarda geri eldesi dozun %1'indenazdır. Aktif metabolit için primer eliminasyon yolu ağırlıklı olarak safra ile atılımdır. Ortalamat1/2 tikagrelor için yaklaşık 7 saat ve aktif metabolit için 8,5 saattir.
Doğrusallık/doğrusal olmayan durum
Tikagrelor doğrusal farmakokinetik gösterir ve tikagrelore ve aktif metabolite (AR-C124910XX) maruziyet 1260 mg'a kadar yaklaşık olarak dozla orantılıdır.
Özel popülasyonlar:
Geriyatrik yoyülasyon
Popülasyon farmakokinetik analizi ile yaşlı (> 75 yaş) AKS hastalarında, daha genç hastalara oranla tikagrelor ve aktif metabolitine daha yüksek maruziyetler (Cmaks ve EAA için yaklaşık %25)gözlenmiştir. Bu farklılıkların klinik olarak anlamlı olduğu düşünülmemektedir (bkz. Bölüm 4.2).
Pediyatrik ^ popülasyon
Orak hücre hastalığı olan çocuklarla ilgili sınırlı veri mevcuttur.
HESTIA 3 çalışmasında, 2 ila 18 yaşından küçük, > 12 ila < 24 kg, >24 ila < 48 kg ve >48 kg olan hastalara, pediyatrik dağılabilir 15 mg tabletler olarak sırasıyla günde iki kez 15, 30 ve 45 mgdozlarında tikagrelor verilmiştir. Popülasyon farmakokinetik analizi ışığında, kararlı durumdaortalama EAA 1095 ng*sa/mL ile 1458 ng*sa/mL arasında ve ortalama C maks 143 ng/mL ile206 ng/mL arasında değişmiştir
Cinsiyet
Erkekler ile kıyaslandığında kadınlarda tikagrelor ve aktif metabolite daha yüksek maruziyet gözlenmiştir. Bu farklılıkların klinik olarak anlamlı olduğu düşünülmemektedir.
Böbrek yetmezliği
Normal böbrek fonksiyonlu gönüllülerle kıyaslandığında şiddetli böbrek yetmezliği (kreatinin klerensi < 30 mL/dak) olan hastalarda tikagrelora maruziyet yaklaşık %20 daha düşüktür ve aktifmetabolite maruziyet yaklaşık %17 daha yüksektir.
Hemodiyaliz uygulanmakta olan terminal evre böbrek hastalığına sahip hastalarda diyaliz uygulanmayan bir günde uygulanan tikagrelor 90 mg'ın EAA ve Cmaks değerinin normal böbrekfonksiyonuna sahip gönüllülerdekine kıyasla %38 ve %51 daha yüksek olduğu görülmüştür.Tikagrelorun diyalizle temizlenebilir olmadığını gösterir şekilde, tikagrelor diyalizden hemenönce uygulandığında maruziyette benzer bir artış gözlenmiştir (sırasıyla %49 ve %61). Aktifmetabolite maruziyet daha düşük boyutta artış sergilemiştir (EAA %13-14, Cmaks %17-36).Terminal evre böbrek hastalığı bulunan hastalarda tikagrelorun trombosit agregasyonuinhibisyonu (IPA) etkisinin diyalizden bağımsız olduğu ve normal böbrek fonksiyonuna sahipgönüllülerdekiyle benzer olduğu görülmüştür (Bkz. Bölüm 4.2).
Karaciğer yetmezliği
Eşlenmiş sağlıklı gönüllülerle karşılaştırıldığında hafif karaciğer yetmezliği olan hastalarda tikagrelor için Cmaks ve EAA değerleri sırasıyla %12 ve %23 daha yüksektir; bununla birliktetikagrelorun TAİ etkisi iki grup arasında benzerdir. Hafif derecede karaciğer yetmezliği olanhastalarda doz ayarlaması gerekli değildir. Tikagrelor, ağır derecede karaciğer yetmezliği olanhastalarda çalışılmamış olup, orta derecede karaciğer yetmezliği olan hastalarla ilgilifarmakokinetik bilgi bulunmamaktadır. Başlangıçta bir veya daha fazla karaciğer fonksiyonutestinde orta veya şiddetli yükselmesi olan hastalarda tikagrelor plazma konsantrasyonları,başlangıçta yükselmeleri olmayan hastalar ile karşılaştırıldığında ortalama olarak benzer veyahafif şekilde daha yüksek olmuştur. Orta derecede karaciğer yetmezliği olan hastalarda herhangibir doz ayarlaması önerilmemektedir (bkz. Bölüm 4.2 ve Bölüm 4.4).
Irk
Beyaz ırktan hastalarla kıyaslandığında Asya kökenli hastalarda ortalama biyoyararlanım %39 daha yüksektir. Beyaz ırktan hastalarla kıyaslandığında tikagrelorun biyoyararlanımı siyah ırktanhastalarda %18 daha düşüktür. Klinik farmakoloji çalışmalarında, beyaz ırkla kıyaslandığındaJapon hastalarda tikagrelora maruziyet (Cmaks ve EAA) yaklaşık %40 (vücut ağırlığı içinayarlandıktan sonra %20) daha yüksektir.
5.3. Klinik öncesi güvenlilik verileri
Güvenlilik farmakolojisi, tek ve tekrarlanan doz toksisitesi ve genotoksik potansiyel klasik çalışmaları baz alındığında, tikagrelor ve majör metaboliti için klinik öncesi verileri insanlar içinadvers olaylar açısından kabul edilemez bir risk göstermemiştir.
Çeşitli hayvan türlerinde, klinik açıdan anlamlı maruziyet düzeylerinde gastrointestinal irritasyon gözlenmiştir (bkz. Bölüm 4.8).
Dişi sıçanlarda, yüksek dozdaki tikagrelor rahim tümörleri (adenokarsinomlar) ve hepatik adenomlar için artmış insidans göstermiştir. Rahim tümörlerinin mekanizması olasılıklasıçanlarda tümörlere neden olabilen hormon dengesizliğidir. Hepatik adenomların mekanizmasıise olasılıkla karaciğerde kemirgenlere özgü enzim indüksiyonuna bağlıdır. Bu nedenlerle,karsinojenisite bulgularının insanlarla ilişkili olabileceği düşünülmektedir.
Sıçanlarda, maternal toksik dozda (güvenlilik sınırı 5.1) minör gelişim anomalileri görülmüştür. Tavşanlarda, yüksek dozda dişilerin fetüslerinde, maternal toksisite göstermeksizin (güvenliliksınırı 4.5) hepatik matüritede ve iskelet gelişiminde hafif bir gecikme görülmüştür.
Sıçan ve tavşanlardaki çalışmalar, anne vücut ağırlığı artışında hafif düşüş ve yeni doğan viyabilitesinde ve büyümede gecikme ile doğum ağırlığında azalmayla üreme toksisitesigöstermiştir. Tikagrelor dişi sıçanlarda düzensiz siklüslere (çoğunlukla uzamış siklüsler) nedenolmuş ancak erkek ve dişi sıçanlarda genel fertiliteyi etkilememiştir. Radyoaktif işaretli tikagrelorile yürütülen farmakokinetik çalışmalar, ana bileşenin ve metabolitlerinin sıçanların sütü ileatıldığını göstermiştir (Bkz. bölüm 4.6).
6. FARMASOTIK ÖZELLİKLER6.1. Yardımcı maddelerin listesi
Mannitol (E421)
Kalsiyum Hidrojen Fosfat Dihidrat Kroskarmelloz SodyumHidroksipropil SelülozMannitol GranülKolloidal Silikon DioksitMagnezyum StearatOpadry 03B220055 Yellow*
*HPMC 2910/Hipromelloz, titanyum dioksit, talk, makrogol, sarı demir oksit
6.2. Geçimsizlikler6.3. Raf ömrü
24 ay
6.4. Saklamaya yönelik özel tedbirler
25°C altındaki oda sıcaklığında saklayınız.
6.5. Ambalajın niteliği ve içeriği
Karton kutu içinde 56 veya 168 tabletlik PVC/PE/PVDC-Alüminyum takvimli blister (güneş/ay sembolleri ile birlikte) ambalajlarda sunulmaktadır.
6.6. Beşeri tıbbi üründen arta kalan maddelerin imhası ve diğer özel önlemler
Kullanılmamış olan ürünler ya da atık materyaller Tıbbi Atıkların Kontrolü Yönetmeliği ve Ambalaj Atıklarının Kontrolü Yönetmeliklerine uygun olarak imha edilmelidir.
7. RUHSAT SAHİBİ
Abdi İbrahim İlaç San. ve Tic. A.Ş.
Reşitpaşa Mahallesi, Eski Büyükdere Caddesi No:4 34467 Maslak/S arıyer/İstanbulTel: 0212 366 84 00Faks: 0212 276 20 20
8. RUHSAT NUMARASI
2020/689. ILK RUHSAT TARIHI/RUHSAT YENILEME TARIHI
İlk ruhsat tarihi: 02.04.2020 Ruhsat yenileme tarihi:
10. KÜB'ÜN YENILENME TARIHI
1Tek açıklayıcı değişken olarak tedavi grubu ile Cox orantısal tehlike modelinden hesaplanan
p-
değeri.İlaç Bilgileri
Tilanta 90 Mg Film Kaplı Tablet
Etken Maddesi: Tikagrelor
Kullanma talimatı ve kısa ürün bilgileri
Ana Sayfa | Hakkımızda | İlaçlar | İlaç Ara | İlaç Firmaları | Gizlilik | Bize Ulaşın
Telif Hakkı 2008-2026 © İlaç Prospektüsü. Tüm Hakları Saklıdır.Uyarı: Sitemizde yayınladığımız ilaç bilgileri ile doktora danışmadan kesinlikle ilaç kullanmayınız!
Aksi halde doğabilecek sağlık sorunlarından ilacprospektusu.com sorumlu tutulamaz.