Yervoy 200mg/40ml Iv İnfüzyonluk Çözelti Konsantresi İçeren Flakon Kısa Ürün BilgisiKISA URUN BILGISI¡ Bu ilaç ek izlemeye tabidir. Bu üçgen yeni güvenlilik bilgisinin hızlı olarak belirlenmesini sağlayacaktır. Sağlık mesleği mensuplarının şüpheli advers reaksiyonları TÜFAM'a bildirmeleribeklenmektedir. Bakınız Bölüm 4.8 Advers reaksiyonlar nasıl raporlanır? 1. BEŞERİ TIBBİ ÜRÜNÜN ADIYERVOY 200 mg/40 mL IV infüzyonluk çözelti konsantresi içeren flakon Steril 2. KALİTATİF VE KANTİTATİF BİLEŞİMEtkin madde:İpilimumab 5 mg/mL 40 mL'lik bir flakon 200 mg ipilimumab içerir.İpilimumab rekombinant DNA teknolojisi ile Çin hamsteri over hücrelerinde üretilen tamamen insana özgü bir anti-CTLA-4 monoklonal antikordur (IgGİK). Yardımcı madde(ler):Çözeltinin her mL'si 0.1 mmol sodyum, yani 2,30 mg sodyum içerir. Yardımcı maddeler için 6.1'e bakınız. 3. FARMASÖTİK FORMİnfüzyonluk çözelti konsantresi (steril konsantre) Berrak ilâ hafif opalesan, renksiz ilâ açık sarı sıvıdır, içinde az miktarda partikül olabilir ve pH değeri 7 osmolaritesi ise 260-300 mOsm/kg'dır. 4. KLİNİK ÖZELLİKLER4.1 Terapötik endikasyonlarıMelanom YERVOY, daha önce en az bir seri sistemik tedavi kullanmış ve sonrasında progresyon göstermiş rezeke edilemeyen relaps veya metastatik erişkin malign melanom hastalarının tedavisinde endikedir.YERVOY, nivolumab ile kombinasyon halinde, ECOG performans durumu 0-1 olan yetişkinlerdeileri evre (rezeke edilemeyen veya metastatik) melanom tedavisinde endikedir. Renal Hücreli Karsinom (RHK) YERVOY, nivolumab ile kombinasyon halinde IMDC risk kategorisi orta/kötü riskli, Karnofsky Performans Durumu 70 ve üzerinde olan ve 65 yaş ve altındaki ileri evre renal hücreli karsinomluyetişkin hastaların birinci basamak tedavisinde endikedir (bkz. Bölüm 5.1). Küçük Hücreli Dışı Akciğer Kanseri (KHDAK) YERVOY, nivolumab ve 2 kür platin bazlı kemoterapi ile kombinasyon halinde, EGFR mutasyonu veya ALK translokasyonu bulunmayan metastatik küçük hücreli dışı akciğer kanserli ECOGPerformans Skoru 0-1 olan yetişkin hastaların birinci basamak tedavisinde endikedir. Malign Plevral Mezotelyoma (MPM) YERVOY, nivolumab ile kombinasyon halinde, rezeke edilemeyen malign plevral mezotelyoması olan yetişkin hastaların birinci basamak tedavisinde endikedir. 4.2 Pozoloji ve uygulama şekliTedavi, kanser tedavisinde deneyimli uzman doktorlar tarafından başlatılmalı ve kontrol edilmelidir Pozoloji/uygulama sıklığı ve süresi:YERVOY MonoterapisiMelanomYetişkinlerdeYERVOY'un önerilen indüksiyon rejimi 3 haftada bir 30 dakikalık bir sürede intravenöz yoldan uygulanan 3 mg/kg olmak üzere toplam 4 dozdur. Yeni lezyonların ortaya çıkmasına ya da var olanlezyonların büyümesine bakılmaksızın, hastalar tolere ettikleri sürece, bütün indüksiyon rejimini (4doz) almalıdırlar. Tümörün verdiği yanıtı, ancak indüksiyon tedavisi tamamlandıktan sonradeğerlendirmek gerekir. Nivolumab ile kombinasyon halinde YERVOYMelanomÖnerilen doz; ilk 4 doz boyunca her 3 haftada bir intravenöz yoldan uygulanan 1 mg/kg ipilimumab nivolumab ile kombinasyon halinde 3 mg/kg YERVOY şeklindedir. Tablo 1'de gösterildiği üzere,bunu her 2 haftada bir 240 mg veya her 4 haftada bir 480 mg dozunda intravenöz yoldan uygulanannivolumab monoterapisi fazı takip eder. Monoterapi fazında, ilk nivolumab dozu aşağıda gösterilenşekillerde uygulanmalıdır; ¦ Her iki haftada bir 240 mg uygulanıyor ise, nivolumab ve YERVOY kombinasyonunun sondozundan 3 hafta sonra; veya ¦ Her 4 haftada bir 480 mg uygulanıyor ise, nivolumab ve YERVOY kombinasyonunun sondozundan 6 hafta sonra. Tablo 1:Nivolumab ile kombinasyon halinde intravenöz YERVOY uygulaması için önerilen dozlar ve infüzyon süreleri
Renal Hücreli Karsinom (RHK)Önerilen doz; ilk 4 doz boyunca her 3 haftada bir intravenöz yoldan uygulanan 1 mg/kg ipilimumab ile kombinasyon halinde 3 mg/kg nivolumab şeklindedir. Tablo 2'de gösterildiği üzere, bunu her 2haftada bir 240 mg veyaher 4 haftada bir 480 mg dozunda intravenöz yoldan uygulanan nivolumabmonoterapisi fazı takip eder. Monoterapi fazında, ilk nivolumab dozu aşağıda gösterilen şekillerdeuygulanmalıdır;¦ Her iki haftada bir 240 mg uygulanıyor ise, YERVOY ve nivolumab kombinasyonunun sondozundan 3 hafta sonra; veya ¦ Her 4 haftada bir 480 mg uygulanıyor ise, YERVOY ve nivolumab kombinasyonunun sondozundan 6 hafta sonra. Tablo 2: Nivolumab ile kombinasyon halinde intravenöz YERVOY uygulaması için önerilen dozlar ve infüzyon süreleri
Malign plevral mezotelyomaÖnerilen doz, 6 haftada bir 30 dakika boyunca intravenöz yoldan uygulanan 1 mg/kg ipilimumab ile kombinasyon halinde her 3 haftada bir 30 dakika boyunca intravenöz yoldan uygulanan 360 mgnivolumab veya 2 haftada bir 30 dakikalık intravenöz infüzyonla verilen 3 mg/kg nivolumabdır.Hastalık progresyonuna, kabul edilemez toksisiteye veya hastalık progresyonu olmayan hastalarda24 aya kadar tedavi önerilir. Nivolumab ve kemoterapi ile kombinasyon halinde YERVOYKüçük hücreli dışı akciğer kanseriÖnerilen doz, 6 haftada bir 30 dakika boyunca intravenöz yoldan uygulanan 1 mg/kg ipilimumab ve her 3 haftada bir uygulanan platin bazlı kemoterapi ile kombinasyon halinde her 3 haftada bir 30dakika boyunca intravenöz yoldan uygulanan 360 mg nivolumabtır. 2 kür kemoterapitamamlandıktan sonra tedaviye 6 haftada bir 1 mg/kg ipilimumab ile kombinasyon halinde 3 haftadabir intravenöz yoldan uygulanan 360 mg nivolumab ile devam edilir. Hastalık progresyonuna, kabuledilemez toksisiteye veya hastalık progresyonu olmayan hastalarda 24 aya kadar tedavi önerilir. Tedavi süresi Nivolumab ile kombinasyon halinde YERVOY tedavisi, klinik yarar gözlendiği sürece ya da hasta artık tedaviyi tolere edemeyene dek ya da belirli bir endikasyon için belirtilmişse maksimum tedavisüresine kadar kullanılmaya devam edilmelidir. Atipik yanıtlar (yani ilk birkaç ay içinde tümörünboyutunda başlangıca göre geçici bir artış veya küçük yeni lezyonlar ve ardından tümörün küçülmesi)gözlenmiştir. Klinik açıdan stabil hastalarda hastalığın ilerlediğine ilişkin ilk kanıtın ardından,hastalığın ilerlediği doğrulanana kadar, nivolumab ile kombinasyon halinde YERVOY tedavisinedevam edilmesi önerilir. Karaciğer fonksiyon testleri (KCFT) ve tiroid fonksiyon testleri, başlangıçta ve de her bir YERVOY dozunun uygulanmasından önce değerlendirilmelidir. Buna ek olarak, diyare ve kolit dahil olmaküzere immün ilişkili advers reaksiyonlara ilişkin her bir belirti veya semptom, YERVOY tedavisisırasında değerlendirilmelidir (bkz. Tablo 3A, 3B ve bölüm 4.4). Tedavinin tamamen bırakılması ya da dozların atlanmasıİmmünite ile ilişkili advers reaksiyonları tedavi etmek için bir dozun atlanması ya da YERVOY tedavisinin tamamen kesilerek yüksek dozda sistemik kortikosteroid başlanması gerekebilir. Bazıvakalarda ek bir immünosüpressif tedavinin başlatılması düşünülebilir (bkz. bölüm 4.4). Dozun yükseltilmesi veya azaltılması önerilmez. Bireysel güvenlilik ve tolerabiliteye dayanarak dozun ertelenmesi veya kesilmesi gerekebilir. Tablo 3A'da ve 3B'de monoterapi olarak YERVOY için, Tablo 3C'de ise nivolumab ile kombinasyon halinde verilen YERVOY için ya da kombinasyon tedavisini takiben tedavinin ikincifazı (nivolumab monoterapisi) için dozların sonlandırılmasına ya da dozlara ara verilmesine yönelikrehber yer almaktadır. İmmünite ile ilişkili advers reaksiyonların yönetimi için rehber Bölüm 4.4'teyer almaktadır.
a Toksisite dereceleri Advers Olaylar için Ulusal Kanser Enstitüsü Ortak Terminoloji Kriterlerine uygundur. Versiyon 4.0 (NCI-CTCAE v4). b İmmun sistem ile ilgili olduğu kanıtlanan veya olduğundan şüphelenilen herhangi diğer advers reaksiyonları CTCAE'ye göre derecelendirilmelidir.YERVOY'u kesme kararı olayın şiddetine göre alınmalıdır.c Hormon replasman tedavisi ile kontrol edilen şiddetli (Derece 3 veya 4) endokrinopatisi olan hastalar, tedaviyedevam edebilir. Monoterapi olarak kullanıldığında, YERVOY dozlarının atlanması gereken durumlarTablo 3BAşağıdaki immünite ile ilişkili advers reaksiyonların görüldüğü hastaların YERVOY dozlarıa atlanır. Detaylı tedavi bilgisi bölüm 4.4'te verilmiştir. atlanır. Detaylı tedavi bilgisi bölüm 4.4'te verilmiştir.
Aksiyon Advers Reaksiyonlar1. Advers reaksiyon düzelip Derece 1veya Derece 0'a (ya da başlangıçtakidurumuna) gelene kadar doza araverilir. 2. Eğer düzelirse, tedaviye devam edilir Gastrointestinal:Tıbbi tedavi ile kontrol edilemeyen, uzun süren (5-7 gün) veya nükseden orta şiddette diyare veya kolit Hepatik: Derece 2 AST, ALT ya da total bilirubinde artış
d 3. Eğer düzelmezse, düzelene kadardozlar atlanır ve tedaviye kaldığıyerden devam edilir d. 4. Derece 1 ya da Derece 0'a gelmezveya başlangıç seviyesine geridönmez ise YERVOY kesilir. Deri:Orta ile ciddi seviyede (Derece 3)b cilt kızarıklıkları veya etiyolojisine bakmaksızın (Derece 2) yaygın/yoğun kaşıntı Endokrin: Endokrin bezlerinde, hormon replasman tedavisi veya yüksek dozda immünosüpressif tedavi ile yeterince kontrolaltına alınamayan hipofizit ve tiroidit gibi şiddetli adversreaksiyonlar Derece 3 diyabet_Nörolojik: Orta şiddette (Derece 2)b açıklanamayan motor nöropati, kas zayıflığı veya duyusal nöropati (4 günden uzun süren)Orta şiddetteki diğer advers reaksiyonlarca YERVOY dozunun azaltılması önerilmez. b Toksisite dereceleri Advers Olaylar için Ulusal Kanser Enstitüsü Ortak Terminoloji Kriterlerine uygundur. Versiyon 4.0 (NCI-CTCAE v4). Tablo 3C: Nivolumab ile kombinasyon halinde YERVOY için önerilen tedavi değişiklikleri veya kombinasyon tedavisinden sonra tedavinin ikinci fazının (nivolumab monoterapisi)uygulanması
YERVOY nivolumab ile kombinasyon halinde aşağıdaki durumlarda kalıcı olarak kesilmelidir: Derece 4 ya da tekrarlayan Derece 3 advers reaksiyonlar; Tedaviye rağmen devam eden dirençli Derece 2 ya da 3 advers reaksiyonlar. YERVOY nivolumab ile kombinasyon halinde uygulandığında, ajanlardan birinin kesilmesi halinde, diğer ajan da kesilmelidir. Doz atlanması halinde doza yeniden başlandığı takdirde, hastanın bireyseldeğerlendirmesi temel alınarak kombinasyon tedavisi veya nivolumab monoterapisine yenidenbaşlatılabilir. Uygulama şekli:YERVOY intravenöz kullanım içindir. Önerilen infüzyon süresi 30 dakikadır. YERVOY dilue edilmeden intravenöz yolla uygulanabildiği gibi enjeksiyonluk 9 mg/ml (%0,9) sodyum klorür çözeltisi veya enjeksiyonluk 50 mg/ml (%5) glukoz çözeltisinde 1 ila 4 mg/ml arasıkonsantrasyonlara seyreltilebilmektedir. YERVOY, intravenöz puşe veya bolus enjeksiyon yoluyla uygulanmamalıdır. Nivolumab ile kombinasyon halinde veya nivolumab ve kemoterapi ile kombinasyon halinde uygulandığında, aynı gün içerisinde önce nivolumab ve ardından YERVOY ve sonrasında kemoterapiverilmelidir. Her bir infüzyon için ayrı infüzyon torbaları ve filtreleri kullanılmalıdır. Tıbbi ürünün uygulanmadan önceki hazırlama ve kullanım talimatları bölüm 6.6'da verilmiştir. Özel popülasyonlara ilişkin ek bilgiler Pediyatrik popülasyon:18 yaşından küçük çocuklarda YERVOY'un güvenliliği ve etkililiği belirlenmemiştir. Veri bulunmamaktadır. YERVOY 18 yaşın altındaki çocuklarda kullanılmamalıdır. Geriyatrik popülasyon:Yaşlı (> 65 yaşında) ve daha genç (<65 yaşında) hastalar arasında genel güvenlilik ya da etkililik farklılıkları rapor edilmemiştir. 75 yaş ve üstü RHK hastalarının birinci basamak tedavisinden gelenveriler bu popülasyon açısından bir sonuca varmak için son derece kısıtlıdır (Bkz. Bölüm 5.1). Bupopülasyonda spesifik doz ayarı gerekmez. Böbrek yetmezliği:Böbrek yetmezliği olan hastalarda YERVOY'un güvenliliği ve etkililiği çalışılmamıştır. Popülasyon farmakokinetik sonuçlarına dayanarak, hafif ilâ orta şiddette renal disfonksiyonu olan hastalardaspesifik bir doz ayarı yapmak gerekmez (bkz. bölüm 5.2). Karaciğer yetmezliği:Karaciğer yetmezliği olan hastalarda ^RVOY'un güvenliliği ve etkililiği çalışılmamıştır. Popülasyon farmakokinetik sonuçlarına dayanarak, hafif karaciğer yetmezliği olan hastalarda spesifikbir doz ayarı yapmak gerekmez (bkz. bölüm 5.2). Başlangıçta transaminaz düzeyleri > 5 x ÜNL yada bilirubin düzeyleri > 3 x UNL olan hastalarda YERVOY dikkatli uygulanmalıdır (bkz bölüm 5.1). 4.3 KontrendikasyonlarEtkin maddeye veya bölüm 6.1'de listelenen yardımcı maddelerden herhangi birine karşı aşırı duyarlılığı olanlarda kontrendikedir. 4.4 Özel kullanım uyarıları ve önlemleriİzlenebilirlik Biyoteknolojik tıbbi ürünlerin izlenebilirliğini iyileştirmek için uygulanan ürünün ticari ismi ve seri numarası mutlaka hasta dosyasına kaydedilmelidir. PD-L1 durumunun değerlendirilmesi Tümörün PD-L1 durumunu değerlendirirken, iyi valide edilmiş ve güçlü bir metodolojinin kullanılması önemlidir. Nivolumab ile kombinasyon halinde YERVOY YERVOY, kombinasyon halinde uygulandığında, tedavinin başlangıcından önce nivolumabın Kısa Ürün Bilgisi'ne bakınız. Nivolumab tedavisi ile ilişkili uyarılar ve önlemler hakkında ayrıntılı bilgialmak için lütfen nivolumab KÜB'e bakınız. İmmünite ile ilişkili advers reaksiyonların birçoğukortikosteroid tedavisinin başlatılması ve tedavi değişiklikleri dahil olmak üzere uygun yönetimadımları ile iyileşmiş ya da çözülmüştür (bkz. Bölüm 4.2). Monoterapi olarak uygulanan nivolumabile karşılaştırıldığında nivolumabın, YERVOY ile kombinasyon şeklinde uygulanması durumundaimmünite ile ilişkili advers reaksiyonlar daha yüksek sıklıklarda oluşmuştur. Kombinasyon tedavisinde pulmoner emboli dahil olmak üzere kardiyak ve pulmoner advers olaylar da bildirilmiştir. Hastalar kardiyak ve pulmoner advers reaksiyonlar ayrıca tedavi öncesinde ve tedavisırasında periyodik olarak elektrolit bozukluklarının ve dehidratasyonun göstergesi olan klinikbulgular, semptomlar ve laboratuvar anormallikleri için sürekli izlenmelidir. Nivolumab ilekombinasyon halinde YERVOY uygulaması yaşamı tehdit eden ya da tekrarlayan şiddetli kardiyakve pulmoner advers reaksiyonların meydana gelmesi halinde kesilmelidir (bkz. Bölüm 4.2). Nivolumab ile kombinasyon halinde YERVOY tedavisi sırasında veya tedaviden sonraki herhangi bir zamanda bir advers reaksiyon meydana gelebileceğinden, hastalar sürekli olarak (son dozu takibenen az 5 ay) izlenmelidir. İmmünite ile ilişkili reaksiyonlar YERVOY, etki mekanizmasına bağlı olabilen artmış veya aşırı immün aktivite sonucu ortaya çıkan enflamatuvar advers reaksiyonlar ile ilişkili bulunmuştur (immünite ile ilişkili advers reaksiyonlar).Ciddi veya yaşamı tehdit edici olabilen immünite ile ilişkili advers reaksiyonlar, gastrointestinal,karaciğer, deri, sinir, endokrin veya diğer organ sistemlerini içerebilmektedir. Çoğu immünite ileilişkili advers reaksiyonlar indüksiyon döneminde görülmüş olsa bile, son YERVOY dozuuygulandıktan aylar sonra ortaya çıkanlar da bildirilmiştir. Farklı bir etiyoloji saptanmadıkça, diyare,artan dışkı sıklığı, kanlı dışkı, KCFT değerlerinde artış, deri döküntüsü ve endokrinopati,enflamatuvar ve YERVOY ile ilişkili olarak düşünülmelidir. Yaşamı tehdit eden komplikasyonlarıminimize etmek için erken teşhis ve uygun yönetim gereklidir. İmmünite ile ilişkili ciddi advers reaksiyonların tedavisi için ilave immünosüpresif tedavi ile birlikte veya bu tedaviler olmaksızın yüksek dozda sistemik kortikosteroid gerekli olabilir. İmmünite ileilişkili advers reaksiyonların yönetimi için monoterapi olarak ya da nivolumab ile kombinasyonhalinde YERVOY'a özel kılavuz aşağıda yer almaktadır. Şüpheli immünite ile ilişkili advers reaksiyonlar için, etiyolojiyi doğrulamak veya diğer nedenleri dışlamak için uygun değerlendirmeler yapılmalıdır. Advers reaksiyonun şiddetine dayanarak,YERVOY veya nivolumab ile kombinasyon halinde YERVOY tedavisine ara verilmeli vekortikosteroidler uygulanmalıdır. Kombinasyon tedavisinin sonucu olarak meydana gelen bir adversreaksiyonu tedavi etmek üzere kortikosteroidlerle immünsüpresyon olması durumunda, iyileşmesonrasında en az 1 aylık süre içerisinde azaltılarak kesilmelidir. Dozun kısa sürede kesilmesi adversreaksiyonun kötüleşmesine veya tekrarlamasına yol açabilir. Kortikosteroid kullanımına rağmenkötüleşme görülen veya iyileşme görülmeyen hastalarda kortikosteroid dışında bir immünosüpresiftedavi eklenmelidir. Hasta, immünosüpresif kortikosteroid dozlarını ya da diğer immünosüpresif tedavileri alırken nivolumab ile kombinasyon halinde YERVOY tedavisi sürdürülmemelidir. İmmünosüpresif tedavialan hastalarda fırsatçı enfeksiyonların önlenmesi için profilaktik antibiyotikler kullanılmalıdır. Herhangi bir şiddette immünite ile ilişkili advers reaksiyonun tekrarlaması veya yaşamı tehdit eden herhangi bir immünite ile ilişkili advers reaksiyon görülmesi durumunda nivolumab ile kombinasyonhalinde YERVOY tedavisi kalıcı olarak kesilmelidir. İmmünite ile ilişkili gastrointestinal reaksiyonlar YERVOY monoterapisiYERVOY immünite ile ilişkili ciddi gastrointestinal reaksiyonlar ile ilişkilendirilmiştir. Klinik çalışmalarda gastrointestinal perforasyon nedeni ile ölümler bildirilmiştir (bkz. Bölüm 4.8). Bir Faz 3 ileri evre (rezeke edilemeyen veya metastatik) melanom çalışmasında (MDX010-20, bkz. Bölüm 5.1) 3 mg/kg dozunda YERVOY monoterapisi alan hastalarda şiddetli ya da fatal (Derece 35) immünite ile ilişkili gastrointestinal reaksiyonlar, tedaviye başlandıktan sonra ortanca 8 haftada(aralık: 5 ilâ 13 hafta) görülmüştür. Protokolde belirtilen yönetim kılavuzlarıyla, vakaların büyük birbölümünde (%90) düzelme (hafif [Derece 1] veya daha düşük şiddete veya başlangıçtaki şiddetegerileme olarak tanımlanır) görülmüş olup, olayın ortaya çıkması ile düzelmesi arasında geçenortanca süre 4 haftadır (aralık: 0,6 ilâ 22 hafta). Hastalar immünite ile ilişkili kolit, diyare ya dagastrointestinal perforasyonu akla getiren gastrointestinal belirti ve semptomlar açısındangözlenmelidir. Klinik durum diyare, bağırsak hareketlerinde artış, karın ağrısı veya ateşli ya da ateşsizhematoşezi içerebilir. Klinik çalışmalarda immünite ile ilişkili kolit ülserasyon ile birlikte veyaülserasyon olmadan mukoza enflamasyonu ve lenfositik ve nötrofilik infiltrasyon ileilişkilendirilmiştir. Pazarlama sonrası, kortikosteroidlere dirençli immünite ile ilişkili kolithastalarında sitomegalovirüs (CMV) enfeksiyonu/reaktivasyonu olguları bildirilmiştir. Diyarenin yada kolitin ortaya çıkması durumunda enfeksiyöz ya da farklı etiyolojilerinin dışlanması amacıyladışkıda enfeksiyon araştırılmalıdır. Diyare ile kolitin yönetim önerileri semptomların şiddetine göre belirlenir (NCI-CTCAE v4'e göre şiddet derecelendirme sınıflandırması). Hafif ilâ orta şiddette (Derece 1 ya da 2) diyaresi (günde 6defaya kadar dışkılama) olan veya hafif ila orta şiddette kolitten şüphelenilen (ör, karın ağrısı veyadışkıda kan) hastalar YERVOY'a devam edebilirler. Semptomatik tedavi (ör, loperamid, sıvıreplasmanı) ve yakın gözlem önerilir. Eğer hafif ilâ orta şiddetteki semptomlar tekrarlar veya 5-7 günsürerse planlanan YERVOY dozuna ara verilmelidir ve kortikosteroid tedavisine (ör. günde bir defa1 mg/kg oral prednison ya da eşdeğeri) başlanmalıdır. Derece 0-1 veya başlangıç düzeyine geridönerse, YERVOY'a kalınan yerden devam edilebilir (bkz. Bölüm 4.2). Ciddi (Derece 3 veya 4) diyare ya da kolitin geliştiği hastalarda YERVOY tamamen kesilmelidir (bkz. Bölüm 4.2) ve sistemik yüksek dozda intravenöz kortikosteroid tedavisine derhal başlanmalıdır(Klinik çalışmalarda 2 mg/kg/gün metilprednisolon kullanılmıştır). Diyare ve diğer semptomlarkontrol edildikten sonra, klinik değerlendirme doğrultusunda kortikosteroid yavaş yavaşazaltılmalıdır. Klinik çalışmalarda hızla azaltınca (<1 aylık sürelerde) bazı hastalarda diyare veyakolit nüksetmiştir. Hastalarda gastrointestinal perforasyon ya da peritonit belirtilerideğerlendirilmelidir. Klinik çalışmalarda elde edilen kortikosteroid-refrakter diyare ya da kolit tedavisi deneyimi sınırlıdır. Diğer nedenlerin dışarıda bırakılması durumunda (biyopside viral PCR ve diğer viral, bakteriyel veparazitik etiyoloji ile değerlendirilen Sitomegalovirüs (CMV) enfeksiyonu/reaktivasyonu dahil)kortikosteroide dirençli immünite ile ilişkili kolitte kortikosteroid rejimine alternatif birimmünosüpresif ajan eklenmesi düşünülmelidir. Klinik çalışmalarda kontrendike olmadığı sürece 5mg/kg'lık tek bir infliksimab dozu eklenmiştir. Gastrointestinal perforasyondan veya sepsistenşüpheleniliyorsa infliksimab kullanılmamalıdır (İnfliksimab Kısa Ürün Bilgisi'ne bakınız). İmmünite ile ilişkili kolit Nivolumab ile kombinasyon halinde YERVOYNivolumab ile kombinasyon halinde YERVOY ile şiddetli diyare ya da kolit gözlenmiştir (bkz. Bölüm 4.8). Hastalar diyare ya da karın ağrısı ve dışkıda mukus veya kan gibi ilave kolit semptomlarıiçin izlenmelidir. Enfeksiyöz ve hastalıkla ilişkili etiyolojiler dışlanmalıdır. Derece 4 diyare ya da kolit için nivolumab ile kombinasyon halinde YERVOY kalıcı olarak kesilmeli ve 1 ila 2 mg/kg/gün metilprednizolon eşdeğer dozda kortikosteroid başlanmalıdır. Nivolumab ile kombinasyon halinde YERVOY ile gözlenen Derece 3 diyare veya kolit, tedavinin kalıcı olarak kesilmesini ve 1 ila 2 mg/kg/gün metilprednizolon eşdeğer dozda kortikosteroidlerinbaşlatılmasını gerektirir. Derece 2 diyare ya da kolit için nivolumab ile kombinasyon halinde YERVOY'a ara verilmelidir. Dirençli diyare veya kolit için, 0,5 ila 1 mg/kg/gün metilprednizolon eşdeğer dozda kortikosteroid ileyönetilmelidir. İyileşmeden sonra, kortikosteroid tedavisinin kademeli olarak kesilmesini takibengerekirse nivolumab ile kombinasyon halinde YERVOY tedavisi yeniden başlatılabilir. Kortikosteroid başlanmasına rağmen kötüleşme olursa veya iyileşme görülmezse kortikosteroid dozu 1 ila 2 mg/kg/gün metilprednizolon eşdeğerine yükseltilmeli ve nivolumab ile kombinasyon halindeYERVOY kalıcı olarak kesilmelidir. İmmünite ile ilişkili pnömonit Nivolumab ile kombinasyon halinde YERVOYNivolumab ile kombinasyon halinde YERVOY sırasında şiddetli pnömonit veya ölümcül vakalar dahil olmak üzere interstisyel akciğer hastalığı gözlenmiştir (bkz. Bölüm 4.8). Hastalar radyografikdeğişiklikler (ör., fokal buzlu cam opasiteleri ve yama tarzında filtratlar), dispne ve hipoksi gibipnömonit işaretleri ve semptomları açısından izlenmelidir. Enfeksiyöz ve hastalıkla ilişkilietiyolojiler dışlanmalıdır. Derece 3 veya 4 pnömonit için nivolumab ile kombinasyon halinde YERVOY kalıcı olarak kesilmeli ve 2 ila 4 mg/kg/gün metilprednizolon eşdeğer dozda kortikosteroide başlanmalıdır. Derece 2 (semptomatik) pnömonit için nivolumab ile kombinasyon halinde YERVOY'a ara verilmeli ve 1 mg/kg/gün metilprednizolon eşdeğeri kortikosteroide başlanmalıdır. İyileşmeden sonra,kortikosteroidin kademeli olarak kesilmesini takiben YERVOY ile kombinasyon halinde nivolumabyeniden başlatılabilir. Kortikosteroide başlanmasına rağmen kötüleşme olursa veya iyileşmegörülmezse kortikosteroid dozu 2 ila 4 mg/kg/gün metilprednizolon eşdeğerine yükseltilmeli venivolumab ile kombinasyon halinde YERVOY kalıcı olarak kesilmelidir. İmmünite ile ilişkili hepatotoksisite YERVOY monoterapisiYERVOY ciddi immünite ile ilişkili hepatotoksisite ile ilişkilendirilmiştir. Klinik çalışmalarda ölümcül hepatik yetmezlik rapor edilmiştir (bkz. Bölüm 4.8). MDX010-20'de 3 mg/kg YERVOY monoterapisi alan hastalarda orta ilâ ciddi şiddette ya da fatal (Derece 2-5) İmmünite ile ilişkili hepatotoksisite, tedaviye başlandıktan sonra 3 ilâ 9 hafta içindeortaya çıkmıştır. Protokolde belirtilen yönetim kılavuzları ile, iyileşme süresi 0,7 ilâ 2 hafta arasındadeğişmiştir. Erken laboratuvar değişiklikleri immünite ile ilişkili hepatitin göstergesi olabileceği için her YERVOY dozundan önce hepatik transaminaz ve bilirubin değerlendirilmelidir (bkz. Bölüm 4.2).Klinik semptom görülmeyen durumlarda KCFT yükselmeleri olabilir. Enfeksiyonlar, tümörprogresyonu veya birlikte kullanılan ilaçlar dahil diğer hepatik yaralanma nedenlerini bertaraf etmekiçin AST ve ALT ya da total bilirubin artışları değerlendirilip düzelene kadar gözlemlenmelidir.İmmünite ile ilişkili hepatotoksisitesi olan hastaların karaciğer biyopsilerinde akut enflamasyonbelirtilerine rastlanmıştır (nötrofiller, lenfositler ve makrofajlar). Derece 2 transaminaz ya da total bilirubin yükselmesi olan hastalarda planlanan YERVOY dozuna ara verilmeli ve KCFT düzelene kadar gözlenmelidir. İyileşme olduktan sonra YERVOY'a devamedilebilir (bkz. Bölüm 4.2). Derece 3 veya 4 transaminaz ya da total bilirubin yükselmesi görülen hastaların tedavileri tamamen kesilmelidir (bkz. Bölüm 4.2); bu hastalara sistemik yüksek doz intravenöz kortikosteroid tedavisine(ör. günde 2 mg/kg metilprednisolon ya da eşdeğeri) derhal başlanmalıdır. Bu hastalarda KCFT,normalleşene kadar gözlemlenmelidir. Semptomlar düzelip KCFT'de sürekli gelişme gözleninceveya KCFT başlangıç seviyesine dönünce klinik değerlendirmeye göre kortikosteroid yavaş yavaşazaltılmaya başlanmalıdır. Azaltma en az 1 ay sürmelidir. Azaltma dönemindeki KCFT yükselmelerikortikosteroid dozu arttırılıp azaltma yavaşlatılarak tedavi edilebilir. KCFT yükselmeleri ciddi ve kortikosteroid tedavisine refrakter olan hastalarda kortikosteroid rejimine alternatif olarak bir immünosüpresif ajan ilavesi düşünülebilir. Klinik çalışmalarda,kortikosteroid tedavisine yanıt vermeyen veya kortikosteroid dozunun azaltıldığı dönemdekortikosteroid dozu arttırılarak düşürülemeyen KCFT yükselmeleri olan hastalarda mikofenolatmofetil kullanılmıştır (mikofenolat mofetilin Kısa Ürün Bilgisi'ne bakınız). Nivolumab ile kombinasyon halinde YERVOYNivolumab ve YERVOY kombinasyonu ile ciddi hepatit gözlenmiştir (bkz. Bölüm 4.8). Hastalar transaminaz ve total bilirubin seviyelerinde yükselmeler gibi hepatit belirti ve semptomları açısındanizlenmelidir. Enfeksiyöz ve hastalıkla ilgili etiyolojiler dışlanmalıdır. Derece 3 ve 4 transaminaz ya da total bilirubin yükselmeleri için nivolumab ile YERVOY kombinasyonu kalıcı olarak kesilmeli, 1-2 mg/kg/gün metilprednizolon eşdeğer dozundakortikosteroid başlanmalıdır. Derece 2 transaminaz ya da total bilirubin yükselmeleri için nivolumab ile YERVOY kombinasyonuna ara verilmelidir. Laboratuvar değerlerinde inatçı yükselmeler 0,5-1 mg/kg/günmetilprednizolon eşdeğer dozunda kortikosteroidlerle yönetilmelidir. İyileşme sağlandığındakortikosteroidler azaltılarak kesildikten sonra gerekiyorsa nivolumab ile YERVOY kombinasyonuyeniden başlanabilir. Kortikosteroidlerin başlanmasına rağmen kötüleşme olursa ya da iyileşmeolmazsa kortikosteroid dozu 1-2 mg/kg/gün metilprednizolon eşdeğer dozuna çıkartılmalı venivolumab ile YERVOY kombinasyonu kalıcı olarak kesilmelidir. İmmünite ile ilişkili advers deri reaksiyonları Önceki immün uyarıcı kanser tedavisi sırasında ağır ya da yaşamı tehdit eden advers deri reaksiyonları öyküsü olan hastalarda YERVOY veya nivolumab ile kombinasyon halinde YERVOYkullanımı düşünüldüğünde dikkatli olunmalıdır. YERVOY monoterapisiYERVOY immünite ile ilişkili olabilecek ciddi advers deri reaksiyonu ile ilişkilendirilmiştir. Bazılarında ölümcül sonuçlar görülen ender toksik epidermal nekroliz (TEN) vakaları (Stevens-Johnson Sendromu dahil) gözlenmiştir, Klinik çalışmalarda ve pazarlama sonrası kullanımdaEozinofili ve Sistemik Semptomların Eşlik Ettiği İlaç Reaksiyonları (DRESS) rapor edilmiştir (bkz.Bölüm 4.8). DRESS şu özelliklerden bir veya daha fazlasıyla ilişkili eozinofilinin eşlik ettiği döküntüler olarak ortaya çıkar: ateş, lenfadenopati, yüzde ödem ve iç organ tutulumu (hepatik, renal, pulmoner).DRESS, tıbbi ürüne maruziyet ile hastalığın başlangıcı arasında uzun latent bir dönemle (iki ila sekizhafta) karakterize olabilir. YERVOY'un indüklediği kızarıklık ve kaşıntı çoğunlukla hafif veya orta şiddetteydi (Derece 1 ya da 2) ve semptomatik tedaviye cevap vermekteydi. MDX010-20'de 3 mg/kg YERVOY monoterapisialan hastalarda orta ilâ ciddi şiddette veya fatal (Derece 2-5) advers deri reaksiyonlarının ortancaortaya çıkış süresi tedaviye başlandıktan sonra 3 hafta (aralık: 0,9-16 hafta) olmuştur. Protokoldebelirtilen yönetim rehberinde çoğu vaka (%87) düzelmiş, olayın ortaya çıkması ile düzelmesi arasındaortanca 5 hafta geçmiştir (aralık: 0,6 - 29 hafta). YERVOY'un indüklediği kızarıklık ve kaşıntı şiddetine göre yönetilmelidir. Hafif ilâ orta şiddette (Derece 1 veya 2) kızarıklık görülen hastalar YERVOY'a devam edip semptomatik tedavi görebilirler(ör. antihistaminikler). 1 ilâ 2 hafta süren ve lokal kortikosteroidler ile iyileşmeyen hafif ilâ ortaşiddette kızarıklık veya kaşıntı vakalarında oral kortikosteroid tedavisi başlatılmalıdır (ör. günde birkere 1 mg/kg prednison ya da eşdeğeri). Ciddi (Derece 3) kızarıklık görülen hastalarda planlanan YERVOY dozuna ara verilmelidir. Eğer başlangıçtaki semptomlar hafif dereceye (Derece 1) gerilerse ya da ortadan tamamen kalkarsaYERVOY tedavisine devam edilebilir (bkz. Bölüm 4.2). Çok ciddi (Derece 4) kızarıklık veya ciddi (Derece 3) kaşıntı görülen hastalarda YERVOY tamamen kesilmeli (bkz. Bölüm 4.2) ve derhal yüksek dozda sistemik intravenöz kortikosteroid tedavisi (ör. 2mg/kg/gün dozunda metilprednisolon) başlatılmalıdır. Kızarıklık ya da kaşıntı kontrol altınaalındıktan sonra, klinik değerlendirmeye göre kortikosteroidinin azaltılmasına başlanmalıdır.Azaltma süresi en az 1 ay olmalıdır. Nivolumab ile kombinasyon halinde YERVOYNivolumab ile kombinasyon halinde YERVOY'da şiddetli döküntü gözlenmiştir (bkz. Bölüm 4.8). Nivolumab ile kombinasyon halinde YERVOY tedavisinde Derece 3 döküntü görülürse tedaviye araverilmeli, Derece 4 döküntüde ise kesilmelidir. Şiddetli döküntü için, 1 ila 2 mg/kg/günmetilprednizolon eşdeğer dozda yüksek doz kortikosteroid ile yönetilmelidir. Bazıları fatal sonuç gösteren seyrek SJS ve TEN olguları gözlenmiştir. SJS veya TEN belirtileri veya bulguları gelişirse, nivolumab ile kombinasyon halinde YERVOY tedavisi kesilmelidir ve hastadeğerlendirme ve tedavi için uzman bir üniteye yönlendirilmelidir. Hastada nivolumab ilekombinasyon halinde YERVOY kullanımına bağlı SJS veya TEN gelişmişse, tedavinin kalıcı olarakkesilmesi önerilir (bkz. Bölüm 4.2). İmmünite ile ilişkili nörolojik reaksiyonlar YERVOY monoterapisiYERVOY İmmünite ile ilişkili ciddi nörolojik advers reaksiyonlar ile ilişkilendirilmiştir. Klinik çalışmalarda fatal Guillain-Barre sendromu rapor edilmiştir. Myastenia gravis benzeri semptomlar dabildirilmiştir (bkz. Bölüm 4.8). Hastalar kas zayıflığından şikayet edebilir. Duyusal nöropati deolabilir. 4 günden fazla süren açıklanamayan motor nöropati, kas zayıflığı ya da duyusal nöropati değerlendirilmeli ve hastalığın progresyonu, enfeksiyonlar, metabolik sendromlar ve eşzamanlı ilaçtedavileri gibi enflamatuvar olmayan nedenler bertaraf edilmelidir. Muhtemelen YERVOY'a bağlıorta şiddette (Derece 2) nöropatisi olan hastalarda (duyusal ya da duyusal olmayan motor) planlanandoza ara verilmelidir. Eğer nörolojik semptomlar başlangıç seviyesine geri gelirse, hasta YERVOY'adevam edebilir (bkz. Bölüm 4.2). YERVOY'a bağlı olduğundan şüphelenilen ciddi (Derece 3 ya da 4) duyusal nöropatisi olan hastalarda YERVOY kalıcı olarak kesilmelidir (bkz. Bölüm 4.2). Hastalar kurumun duyusalnöropatiye yönelik yönetim rehberleri doğrultusunda tedavi edilmeli ve derhal intravenözkortikosteroidlere (ör. 2 mg/kg/gün metilprednisolon) başlanmalıdır. Progresif motor nöropati bulguları immünite ile ilişkili olarak değerlendirilmeli ve buna göre yönetilmelidir. Nedeni ne olursa olsun şiddetli (Derece 3 ya da 4) motor nöropati geliştiren hastalardaYERVOY tamamen kesilmelidir (bkz. Bölüm 4.2). İmmünite ile ilişkili nefrit ve renal fonksiyon bozukluğu Nivolumab ile kombinasyon halinde YERVOYNivolumab ile kombinasyon halinde YERVOY ile şiddetli nefrit veya böbrek fonksiyon bozukluğu gözlenmiştir (bkz. Bölüm 4.8). Hastalar, nefrit ve böbrek fonksiyon bozukluğu belirti ve semptomlarıiçin izlenmelidir. Hastaların çoğunda herhangi bir semptom olmadan serum kreatininde artışgözlenmiştir. Hastalıkla ilişkili etiyolojiler dışlanmalıdır. Derece 4 serum kreatinin artışları için nivolumab ile kombinasyon halinde YERVOY kalıcı olarak kesilmeli ve 1 ila 2 mg/kg/gün metilprednizolon eşdeğer dozunda kortikosteroidlere başlanmalıdır. Derece 2 veya 3 serum kreatinin artışı için, nivolumab ile kombinasyon halinde YERVOY'a ara verilmeli ve 0,5 ila 1 mg/kg/gün metilprednizolon eşdeğer dozda kortikosteroidlere başlanmalıdır.İyileşmeden sonra, kortikosteroid dozunun kademeli olarak kesilmesini takiben nivolumab ilekombinasyon halinde YERVOY yeniden başlatılabilir. Kortikosteroide başlanmasına rağmenkötüleşme olursa veya iyileşme görülmezse kortikosteroid dozu 1 ila 2 mg/kg/gün metilprednizoloneşdeğerine yükseltilmeli ve nivolumab ile kombinasyon halinde YERVOY kalıcı olarak kesilmelidir. İmmünite ile ilişkili endokrinopati YERVOY monoterapisiYERVOY endokrin sistem organlarında enflamasyona neden olabilir; hipofizit, hipopituitarizm, adrenal yetmezlik, hipotiroidizm, Tip 1 diyabetis mellitus ve diyabetik ketoasidoz (bkz. Bölüm 4.2ve 4.8) görülebilir ve hastalar beyin metastazı ya da altta yatan hastalık gibi başka nedenlere benzeyenspesifik olmayan semptomlar gösterebilirler. En sık görülen klinik tablo baş ağrısı ve yorgunluktur.Semptomlar arasında görüş alanı bozuklukları, davranış değişiklikleri, elektrolit bozuklukları vehipotansiyon da olabilir. Adrenal krizin hastanın semptomlarından biri olup olmadığı anlaşılmalıdır.YERVOY ile ilişkilendirilen endokrinopati ile klinik deneyim sınırlıdır. MDX010-20'de 3 mg/kg dozunda YERVOY monoterapisi uygulanan hastalar için orta ilâ çok şiddetli (Derece 2-4) immünite ile ilişkili endokrinopatinin görülmesi tedaviye başlandıktan 7 ilâyaklaşık 20 hafta sonrasında olmuştur. Klinik çalışmalarda gözlenen immünite ile ilişkiliendokrinopati genellikle immünosüpresif ilaç tedavisi ve hormon replasman tedavisi ile kontroledilmiştir. Eğer, ciddi dehidratasyon, hipotansiyon veya şok gibi adrenal kriz bulguları varsa derhal mineralokortikoid aktivitesi olan intravenöz kortikosteroidlerin uygulanması önerilir ve hasta sepsisveya enfeksiyon açısından değerlendirilmelidir. Eğer adrenal yetmezlik bulguları varsa fakat hastaadrenal krizde değilse laboratuvar ve görüntüleme değerlendirmeleri dahil daha fazla araştırmayapmak gerekir. Kortikosteroid tedavisine başlamadan önce endokrin fonksiyonu değerlendirmekiçin laboratuvar sonuçlarına bakılabilir. Eğer pituiter görüntüleme ya da endokrin fonksiyonlaboratuvar testleri anormalse, etkilenen bezin enflamasyonunu tedavi etmek amacıyla kısa bir süreiçin yüksek dozda kortikosteroid tedavisi (ör. 6 saatte bir 4 mg deksametason veya eşdeğeri)uygulanması ve planlanan YERVOY dozuna ara verilmesi önerilir (bkz. Bölüm 4.2). Kortikosteroidtedavisinin bezin fonksiyon bozukluğunu düzeltip düzeltmediği halen bilinmemektedir. Uygunhormon replasmanına da başlanmalıdır. Uzun süreli hormon replasman tedavisi gerekebilir. Semptomatik diyabet için, YERVOY verilmemeli ve gerektiğinde insülin replasmanı başlatılmalıdır. Uygun insülin replasmanının kullanıldığından emin olmak için kan şekerinin izlenmesi devametmelidir. Hayatı tehdit eden diyabet için YERVOY kalıcı olarak kesilmelidir. Semptomlar veya laboratuvar anomalileri kontrol altına alınıp hastanın genel olarak iyiye gittiği kesinleşince, YERVOY tedavisi devam edebilir ve klinik değerlendirmeye göre kortikosteroiddozunun yavaş yavaş düşürülmesine başlanabilir. Doz düşürme, en az 1 aylık periyotlarla olmalıdır. Nivolumab ile kombinasyon halinde YERVOYNivolumab ile kombinasyon halinde YERVOY tedavisi ile hipotiroidizm, hipertiroidizm, adrenal yetmezlik (sekonder adrenokortikal yetmezlik dahil), hipofizit (hipopitüitarizm dahil), diabetesmellitus ve diyabetik ketoasidoz dahil şiddetli endokrinopatiler gözlenmiştir (bkz. Bölüm 4.8). Hastalar endokrinopatilerin klinik belirti ve semptomları, hiperglisemi ve tiroid fonksiyonundaki değişiklikler açısından dikkatli şekilde izlenmelidir (tedavinin başında, tedavi sırasında periyodikolarak ve klinik değerlendirmeye dayanarak gerekli olduğunda). Hastalarda yorgunluk, baş ağrısı,mental durum değişiklikleri, karın ağrısı, olağandışı bağırsak alışkanlıkları ve hipotansiyon veyabeyin metastazları ya da altta yatan hastalık gibi diğer nedenlere benzeyen, spesifik olmayansemptomlar görülebilir. Alternatif etiyoloji belirlenene dek, endokrinopati belirti ve semptomlarınınimmünite ile ilişkili olduğu kabul edilmelidir. Semptomatik hipotiroidizm için nivolumab ile kombinasyon halinde YERVOY'a ara verilmeli ve gerektiği şekilde tiroid hormon replasmanına başlanmalıdır. Semptomatik hipertiroidizm içinnivolumab ile kombinasyon halinde YERVOY'a ara verilmeli ve gerektiği şekilde antitiroid ilaçtedavisine başlanmalıdır. Tiroidin akut enflamasyonundan şüpheleniliyorsa, 1 ila 2 mg/kg/günmetilprednizolon eşdeğeri dozda kortikosteroidlere başlanmalıdır. İyileşmeden sonra, kortikosteroiddozunun kademeli olarak kesilmesini takiben gerekirse nivolumab ile kombinasyon halindeYERVOY'a yeniden başlatılabilir. Uygun hormon replasmanının kullanıldığından emin olmak içintiroid fonksiyonu sürekli şekilde izlenmelidir. Yaşamı tehdit eden hipertiroidizm veya hipotiroidizmdurumunda nivolumab ile kombinasyon halinde YERVOY kalıcı olarak kesilmelidir. Semptomatik Derece 2 adrenal yetmezlik için nivolumab ile kombinasyon halinde YERVOY'a ara verilmeli ve gerektiği şekilde fizyolojik kortikosteroid replasmanına başlanmalıdır. Ciddi (Derece 3)veya yaşamı tehdit eden (Derece 4) adrenal yetmezlik durumunda nivolumab ile kombinasyonhalinde YERVOY kalıcı olarak kesilmelidir. Uygun kortikosteroid replasmanının kullanıldığındanemin olmak için adrenal fonksiyon ve hormon düzeyleri sürekli şekilde izlenmelidir. Semptomatik Derece 2 veya 3 hipofizit için nivolumab ile kombinasyon halinde YERVOY'a ara verilmeli ve gerektiği şekilde hormon replasmanına başlanmalıdır. Akut hipofiz bezienflamasyonundan şüpheleniliyorsa, 1 ila 2 mg/kg/gün metilprednizolon eşdeğeri dozdakortikosteroidlere başlanmalıdır. İyileşmeden sonra, kortikosteroid dozunun kademeli olarakkesilmesini takiben gerekirse nivolumab ile kombinasyon halinde YERVOY yeniden başlatılabilir.Yaşamı tehdit eden (Derece 4) hipofizit durumunda nivolumab ile kombinasyon YERVOY kalıcıolarak kesilmelidir. Uygun hormon replasmanının kullanıldığından emin olmak için hipofizfonksiyonu ve hormon düzeyleri sürekli şekilde izlenmelidir. Semptomatik diyabet için nivolumab ile kombinasyon halinde YERVOY'a ara verilmeli ve gerektiği şekilde insülin replasmanına başlanmalıdır. Uygun insülin replasmanının kullanıldığından eminolmak için kan şekeri sürekli şekilde izlenmelidir. Yaşamı tehdit eden diyabet durumunda nivolumabile kombinasyon halinde YERVOY kalıcı olarak kesilmelidir. İnfüzyon reaksiyonu Monoterapi olarak ya da nivolumab ile kombinasyon halinde YERVOYYERVOY ya da nivolumab ile kombinasyon halinde YERVOY ile yapılan klinik çalışmalarda ciddi infüzyon reaksiyonları bildirilmiştir (bkz. Bölüm 4.8). Ciddi ya da yaşamı tehdit eden infüzyonreaksiyonu durumunda YERVOY ya da nivolumab ile kombinasyon halinde YERVOY infüzyonukesilmeli ve uygun tıbbi tedavi uygulanmalıdır. Hafif ya da orta şiddetteki infüzyon reaksiyonlarıgelişen hastalara yakın izlem ve infüzyon reaksiyonları profilaksisi için yerel tedavi rehberlerine göreverilen premedikasyon ile YERVOY ya da nivolumab ile kombinasyon halinde YERVOY verilebilir.İmmünite ile ilişkili diğer advers reaksiyonlar YERVOY monoterapisiMDX010-20'de 3 mg/kg YERVOY monoterapisi alan hastalarda immünite ile ilişkiliolduğundan şüphe edilen aşağıdaki advers reaksiyonlar da rapor edilmiştir: uveit, eozinofili, lipaz yükselmesi veglomerulonefrit. MDX010-20'de bundan başka 3 mg/kg YERVOY + gp100 peptid aşısı ile tedaviedilen hastalarda iritis, hemolitik anemi, amilaz yükselmeleri, çoklu organ yetmezliği ve pnömonitde bildirilmiştir. Pazarlama sonrasında Vogt-Koyanagi-Harada sendromu vakaları ve seröz retinadekolmanı ve infektif olmayan sistit vakaları bildirilmiştir (bkz. Bölüm 4.8). Ciddi (Derece 3 ya da 4) seyretmeleri halinde, bu reaksiyonlar derhal yüksek dozda sistemik kortikosteroid tedavisinin başlanmasını ve YERVOY'un kesilmesini gerektirebilir (bkz. Bölüm 4.2).YERVOY ilişkili uveit, iritis, seröz retina dekolmanı veya episklerit için topikal kortikosteroid gözdamlalarının tıbben endike olduğu varsayılabilir. YERVOY ilişkili oküler enflamasyonları olanhastalarda geçici görme kaybı bildirilmiştir. Pazarlama sonrası YERVOY ile tedavi edilen hastalarda solid organ nakli reddi bildirilmiştir. YERVOY tedavisi solid organ nakli alıcılarının ret riskini arttırabilir. Bu hastalarda YERVOY'lauygulanan tedavinin olası organ transplantasyonu sonrasında organ reddi riski karşısındaki faydasıdeğerlendirilmelidir. YERVOY monoterapisi ya da PD-1 veya PD-L1 inhibitörü ile kombinasyon halinde YERVOYYERVOY monoterapisi ve PD-1 veya PD-L1 inhibitörü (nivolumab dahil) ile kombinasyon halindekullanılan YERVOY'la birlikte hemofagositik lenfohistiyositoz (HLH) gözlenmiştir. YERVOY,monoterapi olarak veya PD-1 veya PD-L1 inhibitörü ile kombinasyon halinde uygulanırken dikkatliolunmalıdır. HLH doğrulandığı takdirde YERVOY veya PD-1 veya PD-L1 inhibitörü ilekombinasyon halinde YERVOY uygulaması kesilmelidir ve HLH tedavisi başlatılmalıdır.Nivolumab ile kombinasyon halinde YERVOYAşağıdaki immünite ile ilişkili advers reaksiyonlar çeşitli dozlarda ve tümör tiplerinde yapılan klinik çalışmalarda nivolumab ile kombinasyon halinde YERVOY ile tedavi edilen hastaların %1'indenazında bildirilmiştir: pankreatit, üveit, demiyelinizasyon, otoimmün nöropati (fasiyal ve abdusenssinir parezisi dahil), Guillain-Barre sendromu, myastenia gravis, miyastenik sendrom, aseptikmenenjit, ensefalit, gastrit, sarkoidoz, duodenit, miyozit, miyokardit ve rabdomiyoliz. Pazarlamasonrasında Vogt-Koyanagi-Harada sendromu ve seröz retina dekolmanı vakaları bildirilmiştir (bkz.Bölüm 4.8). YERVOY ilişkili oküler enflamasyonları olan hastalarda geçici görme kaybıbildirilmiştir. Şüpheli immünite ile ilişkili advers reaksiyonlar için etiyolojiyi doğrulamak veya diğer nedenleri dışlamak için uygun değerlendirmeler yapılmalıdır. Advers reaksiyonun şiddetine dayanaraknivolumab ile kombinasyon halinde YERVOY'a ara verilmeli ve kortikosteroidler uygulanmalıdır.İyileşmeden sonra, kortikosteroid dozunun kademeli olarak kesilmesini takiben nivolumab ilekombinasyon halinde YERVOY yeniden başlatılabilir. Herhangi bir şiddetli immünite ile ilişkiliadvers reaksiyonun tekrarlaması veya yaşamı tehdit eden herhangi bir immünite ile ilişkili reaksiyongörülmesi durumunda nivolumab ile kombinasyon halinde YERVOY kalıcı olarak kesilmelidir. Nivolumab ile kombinasyon halinde YERVOY tedavisi ile bazıları ölümcül olan nadir miyotoksisite (miyozit, miyokardit ve rabdomiyoliz) vakaları bildirilmiştir. Hastada miyotoksisite belirtileri vesemptomları geliştiği takdirde yakın takip uygulanmalıdır ve gecikmeden değerlendirme ve tedaviuygulanması için bir uzmana sevk edilmelidir. Miyotoksisitenin şiddetine bağlı olarak, nivolumab ilekombinasyon halinde YERVOY'a ara verilmeli veya kesilmelidir (bkz. Bölüm 4.2) ve uygun tedavibaşlatılmalıdır. Miyokardit tanısı için yüksek şüphe indeksi gereklidir. Kardiyak ya da kardiyo-pulmoner semptomları olan hastalar potansiyel miyokardit açısından değerlendirilmelidir. Miyokardit şüphesivarsa, derhal yüksek dozda steroidlere (1 ila 2 mg/kg/gün prednizon veya 1 ila 2 mg/kg/günmetilprednizolon) başlanmalı ve mevcut klinik rehberlere göre teşhis çalışması ile hızlı kardiyolojikonsültasyonu başlatılmalıdır. Miyokardit tanısı konduktan sonra nivolumab ile kombinasyonhalindeki YERVOY'a ara verilmeli ya da kalıcı olarak kesilmelidir (bkz. Bölüm 4.2). Hastalığa özgü önlemler MelanomOküler melanom, primer Merkezi Sinir Sistemi (MSS) melanomu ve aktif beyin metastazları görülen hastalar MDX010-20 çalışmasına dahil edilmemiştir (bkz. Bölüm 5.1). Oküler melanomu olan hastalar CA184-169 klinik çalışmasına dahil edilmemiştir. Bununla birlikte, beyin metastazları bulunan hastalar, metastatik beyin lezyonları ile ilişkili nörolojik semptomlarıyoksa ve YERVOY tedavisine başlanmasından önceki 10 gün içerisinde sistemik kortikosteroidtedavisine gerek duymamış ya da bu tedaviyi görmemişlerse bu çalışmaya dahil edilmişlerdir (bkz.Bölüm 5.1). Oküler melanomu, aktif beyin metastazları olan ve daha önce YERVOY tedavisi görmüş olan hastalar pediyatrik çalışma CA184070'a dahil edilmemiştir (bkz. Bölüm 5.1). Oküler melanomu, aktif beyin metastazları olan ve daha önce CTLA-4, PD-1, PD-L1 ya da CD137 hedefli ajanlarla tedavi görmüş olan hastalar pediyatrik çalışma CA184178'e dahil edilmemiştir (bkz.Bölüm 5.1). Başlangıç performans skoru 2 ve 2'den büyük olan, aktif beyin metastazları veya otoimmün hastalığı bulunan hastalar ile çalışmaya giriş öncesinde sistemik immünosüpresanlar almakta olan hastalarnivolumab ile kombinasyon halinde YERVOY'un klinik çalışmalarından çıkarılmıştır. Oküler/uvealmelanomu bulunan hastalar klinik melanom çalışmalarının dışında tutulmuştur. Veribulunmadığında, nivolumab bu popülasyonlarda potansiyel fayda/risk değerlendirmesi bireyselolarak yapıldıktan sonra dikkatli kullanılmalıdır. Nivolumab monoterapisine kıyasla, YERVOY'un nivolumab ile kombinasyonu için PFS'de bir artış, yalnızca tümör PD-L1 ekspresyonu düşük olan hastalarda tespit edilmiştir. Tümör PD-L1ekspresyonu yüksek olan hastalarda (PD-L1 >%1) YERVOY ile nivolumab ve nivolumabmonoterapisi arasında OS'deki iyileşme benzerdi. Kombinasyon tedavisine başlamadan öncedoktorlara her bir hastayı ve tümör karakteristiklerini, gözlemlenen faydaları ve nivolumabmonoterapisine kıyasla kombinasyonun toksisitesini dikkate alarak dikkatle değerlendirmeleriönerilir (bkz. Bölüm 4.8 ve 5.1). Hastalıkları hızla ilerleyen melanom hastalarında nivolumab ile kombinasyon halinde YERVOY'un kullanımı.Doktorlar, hastalığı hızla ilerleyen hastalarda tedaviye başlamadan önce nivolumab ile kombinasyon halindeki YERVOY etkisinin geciken başlangıcını değerlendirmelidir (bkz. Bölüm 5.1). Renal Hücreli KarsinomNivolumab ile kombinasyon halinde YERVOY çalışmalarına eş zamanlı beyin metastazı ya da beyin metastazı öyküsü olan, aktif otoimmün hastalığı ya da sistemik immünosüpresyon tedavisi gerektirenmedikal durumu olan hastalar dahil edilmemiştir (bkz. Bölüm 4.5 ve 5.1). Verilerin olmadığıdurumlarda nivolumab ile kombinasyon halinde YERVOY, bu popülasyonlarda her hasta içinbireysel olarak potansiyel risk-yararın dikkatli değerlendirilmesinden sonra dikkatle kullanılmalıdır. Küçük Hücreli Dışı Akciğer KanseriKHDAK'nin birinci basamak tedavisiAktif otoimmün hastalığı, semptomatik interstisyel akciğer hastalığı, sistemik immünosupresyon gerektiren tıbbi koşulları, aktif (tedavi edilmemiş) beyin metastazı olan, lokal ileri hastalık için dahaönce sistemik tedavi görmüş veya duyarlı EGFR mutasyonları veya ALK translokasyonları olanhastalar, KHDAK'nin birinci basamak tedavisini araştıran kılavuz çalışmalara dahil edilmemiştir(bkz. Bölüm 4.5 ve 5.1). Yaşlı hastalarda (>75 yaş) sınırlı veri mevcuttur (bkz. Bölüm 5.1). Buhastalarda, nivolumab ve kemoterapi ile kombinasyon halinde ipilimumab, bireysel bazda potansiyelfayda/risk dikkatli bir şekilde değerlendirildikten sonra dikkatle kullanılmalıdır. Malign plevral mezotelyomaPrimitif peritoneal, perikardiyal, testis veya tunika vajinalis mezotelyoması, interstisyel akciğer hastalığı, aktif otoimmün hastalığı, sistemik immünosupresyon gerektiren tıbbi koşulları ve beyinmetastazı olan hastalar (cerrahi olarak rezeke edilmedikçe veya stereotaksik radyoterapi ile tedaviedilmedikçe ve tedaviye dahil edilmeden önceki 3 ay içinde herhangi bir gelişme olmadıkça)MPM'nin birinci basamak tedavisini araştıran kılavuz çalışmalara dahil edilmemiştir (bkz. bölüm 4.5ve 5.1). Veri bulunmadığından, nivolumab ile kombinasyon halinde ipilimumab bu popülasyonlardakişi bazında potansiyel yarar/risk değerlendirmesi yapılmasının ardından dikkatli şekildekullanılmalıdır. Otoimmün hastalığı olan hastalar Aktif otoimmün hastalığı ya da organ nakli greft devamlılığı için sistemik immünosüpresif tedaviye ihtiyacı olanlar dahil olmak üzere geçmişte otoimmün hastalığı olan hastalar (vitiligo vehipotiroidizm gibi yeterli derecede kontrol altında tutulan endokrin yetersizlikler dışında), klinikçalışmalarda değerlendirilmemiştir. YERVOY immün yanıtı sağlayan (bkz. Bölüm 5.1) bir T-hücresipotansiyalize edicisidir ve immünosüpresif tedaviye müdahale edebilir; sonuçta altta yatan hastalıkalevlenebilir ya da greftin reddedilmesi riski artabilir. Daha sonraki immün aktivasyonunun yaşamıtehdit etme potansiyelinin bulunduğu şiddetli aktif otoimmün hastalığı olan hastalarda YERVOY'dankaçınılmalıdır. YERVOY otoimmün hastalık geçmişi olan diğer hastalarda potansiyel risk yararprofili bireysel olarak dikkatlice ele alındıktan sonra dikkatli kullanılmalıdır. Kontrollü sodyum diyetinde olan hastalarBu tıbbi ürün, DSÖ'nün bir yetişkin için önerdiği günlük maksimum 2 g sodyum alımının sırasıyla %1,15'ine ve %4,60'ına eşdeğer gelen her 10 mL'lik flakonda 23 mg sodyum ve her 40 mL'likflakonda 92 mg sodyum ihtiva eder. Bu durum, kontrollü sodyum diyetinde olan hastalar için gözönünde bulundurulmalıdır. Vemurafenib ile eşzamanlı uygulamaBir Faz 1 çalışmada, YERVOY (3 mg/kg) ve vemurafenibin (960 mg BID veya 720 mg BID) eş zamanlı kullanımı ile asemptomatik Derece 3 transaminaz (ALT/AST> 5 x UNL) ve bilirubin (totalbilirubin>3 x UNL) artışları bildirilmiştir. Bu ön verilere dayanarak, YERVOY ve vemurafenibin eşzamanlı kullanımı tavsiye edilmez. Vemurafenib ile sıralı uygulamaFaz 2 çalışmasında, BRAF mutasyonu olan metastatik melanomlu hastalarda vemurafenib ile sıralı tedavi ve ardından 10 mg/kg YERVOY tedavisi, tek başına YERVOY ile karşılaştırıldığında Derece3+ deri advers reaksiyonlarında daha yüksek insidans göstermiştir. Vemurafenib sonrasındaYERVOY uygulandığında dikkatli olunmalıdır. Pediyatrik popülasyonYERVOY 18 yaşından küçük çocuklarda kullanılmamalıdır. 4.5 Diğer tıbbi ürünler ile etkileşimler ve diğer etkileşim şekilleriYERVOY, sitokrom P450 enzimleri (CYP) veya ilaçları metabolize eden diğer enzimlerce metabolize edilmeyen bir insan monoklonal antikorudur. Daha önce tedavi almamış ileri evre melanom hastalarında tek başına ve kemoterapi (dakarbazin ya da paklitaksel/karboplatin) ile kombinasyon halindeYERVOY uygulanan yetişkinlerde bir ilaçetkileşim çalışması yapılmış ve CYP izoenzimleri (özellikle CYP1A2, CYP2E1, CYP2C8 veCYP3A4) ile etkileşimi değerlendirilmiştir. YERVOY ve paklitaksel/karboplatin, dakarbazin veyaonun metaboliti, 5-aminoimidazol-4-karboksamid (AIC) arasında klinik olarak ilgili hiçbirfarmakokinetik ilaç-ilaç etkileşimi gözlenmemiştir. Diğer etkileşim formlarıKortikosteroidlerYERVOY'un farmakodinamik aktivitesi ve etkililiği ile olası etkileşimi nedeniyle, YERVOY'a başlamadan önce; başlangıçta sistemik kortikosteroidlerin kullanımından kaçınılmalıdır. Yine deimmünite ile ilişkili advers reaksiyonların tedavi edilmesi için YERVOY'a başlandıktan sonrasistemik kortikosteroidler veya diğer immünosüpresanlar kullanılabilir. YERVOY tedavisinebaşlandıktan sonra sistemik kortikosteroidlerin kullanımının YERVOY'un etkililiğini bozmadığıgörülmektedir. AntikoagülanlarAntikoagülanların kullanımının gastrointestinal hemoraji riskini artırdığı bilinmektedir. Gastrointestinal hemoraji, YERVOY ile görülebilir bir advers reaksiyon olduğundan (bkz. Bölüm4.8) eşzamanlı antikoagülan tedavisine ihtiyaç duyan hastalar yakından izlenmelidir. Özel popülasyonlara ilişkin ek bilgiler:Yaşlılarda, böbrek ve karaciğer yetmezliği olanlarda hiçbir ilaç etkileşim çalışması yapılmamıştır. Pediyatrik Popülasyon:Pediyatrik hastalar için klinik veri bulunmamaktadır. 4.6 Gebelik ve laktasyonGenel tavsiyeGebelik kategorisi: C Çocuk doğurma potansiyeli bulunan kadınlar/Doğum kontrolü (Kontrasepsiyon):Çocuk doğurma potansiyeli bulunan kadınlarda etkili kontraseptif metotlar kullanılmalıdır. Gebelik dönemiYERVOY'un gebe kadınlarda kullanımına ilişkin veri mevcut değildir. Hayvan üreme çalışmaları üreme toksisitesinin bulunduğunu göstermiştir (bkz. Bölüm 5.3). İnsan IgG1, plasenta bariyerinigeçmektedir. Tedavinin gelişmekte olan fetusa yönelik potansiyel riski bilinmemektedir. Klinikyararı potansiyel riskinden fazla olmadığı sürece, YERVOY'un gebelik döneminde veya etkili birdoğum kontrol yöntemi kullanmayan çocuk doğurma potansiyeline sahip kadınlarda kullanılmasıönerilmemektedir. Laktasyon dönemiHamilelik sırasında tedavi gören cynomolgus maymunlarında YERVOY sütte çok düşük seviyelerde görülmüştür. YERVOY'un insanlarda anne sütüne geçip geçmediği bilinmemektedir. IgG'lerin annesütüne geçişi genellikle sınırlıdır ve IgG'ler düşük bir oral biyoyararlanıma sahiptir. İnfantlardasistemik anlamlı bir maruziyet beklenilmemektedir ve emzirilen yeni doğan/infant üzerinde herhangibir etki meydana gelmesi beklenmemektedir. Ancak emzirilen infantlarda advers reaksiyonpotansiyelinden dolayı, çocuk için emzirmenin yararı ve kadın için YERVOY tedavisinin yararı gözönünde bulundurularak emzirmeye devam edilip edilmemesi veya YERVOY tedavisinin kesilipkesilmemesi konusunda karar verilmelidir. Üreme yeteneği/FertiliteYERVOY'un fertilite üzerindeki etkisini değerlendiren çalışmalar yapılmamıştır. Bu durumda YERVOY'un erkek ve dişi fertilitesi üzerindeki etkisi bilinmemektedir. 4.7 Araç ve makine kullanımı üzerindeki etkilerYERVOY'un araç ve makine kullanımı üzerine etkisi düşüktür. Yorgunluk gibi potansiyel advers reaksiyonlara yol açabilmesi nedeniyle (bkz. Bölüm 4.8) hastalara YERVOY'un kendilerini ters bir şekilde etkilemediğinden emin olana dek araç ve makinekullanmaları konusunda dikkatli olmaları önerilmelidir. 4.8 İstenmeyen etkilerYERVOY monoterapisi (bkz. Bölüm 4.2)a) Güvenlilik profili özeti YERVOY farklı dozlarda ve tümör tiplerinde kullanımının değerlendirildiği bir klinik programda yaklaşık 10.000 hastaya uygulanmıştır. Aksi belirtilmediği sürece, aşağıda belirtilen veriler, klinikmelanom çalışmalarında 3 mg/kg'da YERVOY maruziyetini yansıtmaktadır. Faz 3 çalışmasında(MDX010-20. bkz. Bölüm 5.1) hastaların aldığı ortanca doz sayısı 4'tür (aralık 1-4). YERVOY en çok immün aktivitedeki artış veya aşırı immün aktivite sonucu ortaya çıkan advers reaksiyonlar ile ilişkilendirilmiştir. Ciddi reaksiyonlar dahil bunların çoğu uygun medikal tedaviyebaşlandıktan ya da YERVOY kesildikten sonra düzelmiştir (immünite ile ilişkili adversreaksiyonların yönetimi ile ilgili bilgiler Bölüm 4.4'te bulunmaktadır). MDX010-20'de 3 mg/kg YERVOY monotereapisi alan hastalarda en sık bildirilen advers reaksiyonlar (hastaların > %10'u) diyare, kızarıklık, kaşıntı, yorgunluk, bulantı, kusma, iştahazalması ve karın ağrısıdır. Çoğunluğu hafif ilâ orta şiddette seyretmiştir (Derece 1 veya 2).Hastaların %10'unda advers reaksiyonlar nedeni ile YERVOY tedavisi kesilmiştir. b) Advers reaksiyonların tablo halinde listesi Klinik çalışmalarda (n=767) 3 mg/kg YERVOY ile tedavi edilen ileri evre melanom hastalarında ve pazarlama sonrası gözetimde rapor edilen advers reaksiyonlar Tablo 4'te gösterilmiştir. Bu reaksiyonlar sistem organ sınıfı ve sıklık ile sunulmaktadır. Sıklıklar şu şekilde tanımlanmaktadır: çok yaygın (>1/10); yaygın (>1/100 ila <1/10); yaygın olmayan (>1/1.000 ila <1/100); seyrek(>1/10.000 ila <1/1.000); çok seyrek (<1/10.000); bilinmiyor (eldeki verilerle tahmin edilemiyor).Her bir sıklık grubunda advers reaksiyonlar azalan şiddete göre yazılmıştır. MDX010-20'de YERVOYalan HLA-A2*0201 pozitif hastalarda immünite ile ilişkili advers reaksiyon oranları genel klinikprogramda gözlenenlere benzer olmuştur. Birleştirilmiş Faz 2 ve 3 klinik çalışmalarda daha önce kemoterapi görmemiş olan hastalarda (n=75: tedavi edilmiş), iki retrospektif gözlem çalışmasında (n=273 ve n=157) ve CA184-169'da (N= 362)daha önce tedavi edilmemiş hastalarda YERVOY 3 mg/kg'ın güvenlilik profili, daha önce tedaviedilmiş ileri evre melanomlu hastalarda gözlenenle benzerdi. Rezeke edilemeyen veya metastatik melanom bulunan, YERVOY ile tedavi edilmiş (3 mg/kg, en az 3 yıllık takip dönemi ile) ve çok uluslu, prospektif gözlem çalışması CA184143'e kaydolmuş(N=1151) hastalar için güvenlilik verileri, ileri evre melanom için YERVOY klinik çalışmalarındabildirilenlere benzerdi.
Tablo 4'te sunulan advers reaksiyon frekansları tamamen ipilimumaba atfedilemez, ancak altta yatan hastalıklar nedeniyle katkılar içerebilir. a) Sıklıklar, melanomda YERVOY 3 mg/kg dozunun araştırıldığı 9 klinik çalışmadan toplanan verilere dayanmaktadır. b) Ölümcül sonuç dahil c) Bu potansiyel olarak enflamatuvar advers reaksiyonlar ile ilgili ilave bilgiler seçilen advers reaksiyonlar tanımı veBölüm 4.4'te sunulmaktadır. Bu bölümlerde sunulan veriler öncelikli olarak Faz 3 çalışması MDX010-20'den elde edilendeneyimi yansıtmaktadır. d) Melanomda tamamlanan 9 klinik çalışma dışında veriler sıklık tespitlerine dahil edilmiştir. e) Pazarlama sonrası olay (ayrıca bkz. Bölüm 4.4.). f) Kas ve iskelet ağrısı; sırt ağrısı, kemik ağrısı, kas-iskelet göğüs ağrısı, kas iskelet rahatsızlığı, miyalji, boyun ağrısı,ekstremitelerde ağrı, spinal ağrıyı içeren kompozit bir terimdir. g) Raporlanmış klinik çalışma ve pazarlama sonrası ayarlamalar. h) Tip 1 diyabetis mellitus diyabetik ketoasidoz ile ilişkili olabilir. Klinik melanom çalışmalarında farklı dozlarda YERVOY (<veya>3 mg/kg) alan hastalarda Tablo 4'te listelenmeyen ilave advers reaksiyonlar bildirilmiştir. Aksi belirtilmedikçe %1'den az sıklıktameydana gelen bu ilave reaksiyonlar şöyledir: meningizm, miyokardit, perikardiyal effüzyon,kardiyomiyopati, otoimmün hepatit, eritema nodozum, otoimmün pankreatit, hiperpituitarizm,hipoparatiroidizm, enfeksiyöz peritonit, episklerit, sklerit, Raynaud fenomeni, palmar-plantareritrodizestezi sendromu, sitokin salınımı sendromu, sarkoidoz, kanda gonadotropinin azalması,lökopeni, polisitemi, lenfositoz, oküler miyozit ve nörosensoriyel hipoakuzi. CA184-169 (N=362) klinik çalışmasında 3 mg/kg dozunda YERVOY'un genel güvenlilik profili ileri evre melanom tedavisi gören hastalarda YERVOY için belirlenen güvenlilik profili ile uyumludur. Nivolumab ile kombinasyon halinde YERVOY (kemoterapi ile ya da kemoterapisiz) (bkz. Bölüm 4.2)a) Güvenlilik profilinin özeti YERVOY, kombinasyon halinde uygulandığında, tedavinin başlangıcından önce diğer terapötik ajanların Kısa Ürün Bilgileri'ne bakınız. YERVOY ile kombinasyon halinde kullanılan diğerterapötik ajanların güvenlik profili ilee ilgili ek bilgiler için lütfen KÜB'e bakınız. Nivolumab ile kombinasyon halinde (kemoterapi ile ya da kemoterapisiz) YERVOY için (n = 2094) birleştirilmiş veri setinde minimum takip süresi 6 ay ila 47 ay arasında değişmekte olup, en yaygın(>%10) advers reaksiyonlar yorgunluk (%50), döküntü (%38), diyare (%37), bulantı (%31), kaşıntı(%29), kas ve iskelet ağrısı (%28), pireksi (%25), öksürük (%24), iştah kaybı (%23), kusma (%20),dispne (%19), konstipasyon (%19), artralji (%19), karın ağrısı (%18), hipotiroidizm (%16), baş ağrısı(%16), üst solunum yolu enfeksiyonları (%15) , ödem (%13) ve baş dönmesi (%11) olmuştur.YERVOY ile kombinasyon halinde nivolumab (kemoterapi ile ya da kemoterapisiz) için derece 3-5advers reaksiyonların insidansı, %67 olup %0.7'si ölümcül advers reaksiyonlar nedeniyle çalışmailacıyla ilişkilendirildi. Nivolumab 1 mg/kg ile kombinasyon halinde YERVOY 3 mg/kg ile tedaviedilen hastalarda, yorgunluk (%62), döküntü (%57), ishal (%52), bulantı (%42), kaşıntı (%40), ateş(%36) ve baş ağrısı (%26) görülmüştür; bu yan etkiler nivolumab ile kombinasyon halinde(kemoterapi ile ya da kemoterapisiz) YERVOY'un birleştrilmiş veri setinden >%10 daha yüksekoranda raporlanmıştır. YERVOY 1 mg/kg ile kombinasyon halinde nivolumab 360 mg ve kemoterapiile tedavi edilen hastalar arasında, anemi (% 32) ve nötropeni (% 15) görülmüştür; bu yan etkilernivolumab (kemoterapili veya kemoterapisiz) ile kombinasyon halinde YERVOY'un birleştirilmişveri setinde bildirilen oranlardan% 10 > daha yüksek bir insidansta bildirilmiştir. b) Advers reaksiyonların tablo halinde özeti Nivolumab ile kombinasyon halinde YERVOY ile tedavi edilen hastalar (kemoterapi ile ya da kemoterapisiz) (n=2094), birleştirilmiş veri setinde pazarlama sonrası bildirilen advers reaksiyonlarTablo 5'te sunulmaktadır. Bu reaksiyonlar sistem organ sınıfı ve sıklığa göre sunulmaktadır. Sıklıklaraşağıdaki şekilde tanımlanmıştır: çok yaygın (>1/10); yaygın (>1/100 ila <1/10); yaygın olmayan(>1/1.000 ila <1/100); seyrek (>1/10.000 ila <1/1.000); çok seyrek (<1/10.000), bilinmiyor (mevcutpazarlama sonrası verilerden hesaplanamıyor). Her bir sıklık grubunda, advers reaksiyonlar azalanşiddet derecesine göre listelenmiştir.
a Tamamlanmış ya da devam etmekte olan klinik çalışmalarda ölümcül vakalar bildirilmiştir. b Laboratuvar terimlerinin sıklık dereceleri laboratuvar ölçümlerinde başlangıca kıyasla kötüleşme yaşayanhastaların oranını temsil eder. Aşağıda Seçilen yan etkilerin açıklaması; laboratuvar anomalileri bölümünebakınız. c Döküntü; makulopapuler döküntü, eritematöz döküntü, pruritik döküntü, foliküler döküntü, makuler döküntü, morbiliform döküntü, papüler döküntü, püstüler döküntü, papüloskuamöz döküntü, veziküler döküntü, yaygındöküntü, eksfoliatif döküntü, dermatit, akneli dermatit, alerjik dermatit, atopik dermatit, büllöz dermatit,eksfolyatif dermatit, sedefli dermatit, ilaç döküntüsü, nodüler döküntü ve pemfigoid. i Anemi, diğer sebeplerin yanı sıra, demir eksikliği anemisi, kırmızı kan hücresi sayısı azalması, ve hemoglobin düşüşü,, hemolitik anemi ve otoimmün anemi kapsayan birleşik bir terimdir. Seçilen yan etkilerin açıklaması; Belirtilenlerin dışında, YERVOY monoterapisine ilişkin veriler, ileri evre (rezeke edilemeyen veya metastatik) melanoma ilişkin bir Faz 3 çalışmada (MDX010-20, bkz. Bölüm 5.1) 3 mg/kg YERVOYmonoterapisi (n=131) veya gp100 ile kombine 3 mg/kg YERVOY (n=380) alan hastalaradayanmaktadır. Kombinasyon halinde YERVOY tedavisi, immünite ile ilişkili advers reaksiyonlarla ilişkilendirilmiştir. İmmünite ile ilişkili advers reaksiyonlar çoğu vakada uygun tıbbi tedaviyleçözülmüştür. Nivolumab monoterapisi alanlara kıyasla nivolumab ile kombinasyon halindeYERVOY alan hastaların daha yüksek bölümünde tedavinin kalıcı olarak kesilmesi gerekmiştir.Tablo 6'da nivolumab ile kombinasyon halinde YERVOY tedavisi kalıcı olarak kesilen immünite ileilişkili advers reaksiyonlar görülen hastaların yüzdesi sunulmaktadır. Ek olarak, advers reaksiyondeneyimleyen hastalar için, Tablo 6'da yüksek dozda kortikosteroid gereken (en az 40 mg günlükprednizon eşdeğeri) hastaların yüzdesi sunulmaktadır. Bu advers reaksiyonlara yönelik tedaviuygulamaları Bölüm 4.4'te belirtilmektedir.
YERVOY, ciddi immünite ile ilişkili gastrointestinal reaksiyonlar ile ilişkilendirilmiştir. gp 100 ile kombinasyon halinde 3 mg/kg YERVOY uygulanan hastaların <%1'inde gastrointestinalperforasyona bağlı ölümler bildirilmiştir. 3 mg/kg YERVOY monoterapi grubunda, sırasıyla hastaların %27 ve %8'inde herhangi bir şiddette diyare ve kolit bildirilmiştir. Ciddi (Derece 3 veya 4) diyare ve şiddetli (Derece 3 veya 4) kolit sıklığıher ikisi için %5'ti. Ciddi veya ölümcül (Derece 3-5) immünite ile ilişkiligastrointestinalreaksiyonların başlamasına kadar geçen ortanca süre, tedavinin başlangıcından itibaren 8 haftaydı(aralık: 5 - 13 hafta). Protokolde belirtilen yönetim rehberleri ile vakaların büyük bir bölümünde(%90) iyileşme [hafif (Derece 1) veya daha düşük veya başlangıçtaki şiddete gerileme olaraktanımlanmıştır] meydana gelmiş olup başlangıçtan iyileşme görülene kadar geçen ortanca süre 4haftaydı (aralık; 0,6 - 22 hafta). Klinik çalışmalarda immünite ile ilişkili kolit, ülserasyon ile veyaolmaksızın mukozal enflamasyon ve lenfositik ve nötrofilik infiltrasyon bulgusu ileilişkilendirilmiştir. İmmünite ile ilişkili kolitNivolumab (kemoterapi ya da kemoterapisiz) ile kombinasyon halindeki YERVOY ile tedavi edilen hastalarda, diyare ya da kolit insidansı %27,7 (580/2094) olmuştur. Hastaların sırasıyla %8,8(184/2094), %6,8 (142/2094) ve %0,1'inde (3/2094) Derece 2, Derece 3, Derece 4 ve Derece 5vakalar bildirilmiştir. Bir hasta (<%0,1) ölüm ile sonuçlandı. Başlangıca kadar geçen medyan süre1,4 aydı (aralık: 0,0-48,9). 577 hastada (%90,8) iyileşme gözlenmiştir ve iyileşme ortaya çıkana kadargeçen medyan süre 2,7 hafta olduğu belirlenmiştir (aralık: 0,1-159,4+). Nivolumab 1mg/kg ile kombinasyon halindeki YERVOY 3m/kg ile tedavi edilen hastalar arasında, diyare ya da kolit insidansı %46,7, Derece 2 (%13,6), Derece 3 (%15,8) ve Derece 4 (%0,4) oluşmuştur. İmmünite ile ilişkili pnömonitNivolumab (kemoterapi ya da kemoterapisiz) ile kombinasyon halindeki YERVOY ile tedavi edilen hastalarda, interstisyel akciğer hastalığı dahil pnömonit insidansı %6,9 (145/2094) olmuştur.Hastalarda sırasıyla %3,5 (73/2094), %1,1 (24/2094) ve %0,4'ünde (8/2094) Derece 2, Derece 3 veDerece 4 vakalar bildirilmiştir. Dört hastada (%0,2) ölüm ile sonuçlandı. Başlangıca kadar geçenmedyan süre 2,7 aydı (aralık: 0,1-56,8). 119 hastada (%82,1) iyileşme gözlenmiştir ve iyileşme ortayaçıkana kadar geçen medyan süre 6,1 hafta olduğu belirlenmiştir (aralık: 0,3-149,3+). İmmünite ile ilişkili hepatotoksisiteYERVOY, ciddi immünite ile ilişkili hepatotoksisite ile ilişkilendirilmiştir. 3 mg/kg YERVOY monoterapisi uygulanan hastaların %1'inden azında ölümcül karaciğer yetmezliği bildirilmiştir. Sırasıyla hastaların %1 ve %2'sinde AST ve ALT değerlerinde herhangi bir şiddette yükselme bildirilmiştir. Ciddi (Derece 3 veya 4) AST veya ALT yükselmesi bildirilmemiştir. Orta ila şiddetliveya ölümcül (Derece 2 - 5) immünite ile ilişkili hepatotoksisitenin başlamasına kadar geçen süre,tedavinin başlangıcından itibaren 3 ila 9 hafta arasında değişmiştir. Protokolde belirtilen yönetimrehberlerinde iyileşme görülene kadar geçen süre 0,7 ila 2 hafta arasında değişmektedir. Klinikçalışmalarda, immünite ile ilişkili hepatotoksisite görülen hastalarda karaciğer biyopsileri, akutenflamasyon (nötrofiller, lenfositler ve makrofajlar) olduğuna dair kanıtlar göstermiştir. Dakarbazin ile kombinasyon halinde tavsiye edilen dozun üzerinde YERVOY alan hastalarda, immünite ile ilişkilihepatoksisite, 3 mg/kg YERVOY monoterapisi alan hastalara kıyasla daha sıkolarak meydana gelmiştir. Nivolumab (kemoterapi ya da kemoterapisiz) ile kombinasyon halindeki YERVOY ile tedavi edilen hastalarda, karaciğer fonksiyon testi anomalilerinin insidansı %19,2 (402/2094) olmuştur. Hastalarınsırasıyla %4,2 (88/2094), %7,8 (163/2094) ve %1,2'sinde (25/2094) Derece 2, Derece 3 ve Derece 4vakalar bildirilmiştir. Başlangıca kadar geçen medyan süre 1,9 aydı (aralık: 0,0-36,6). 351 hastada(%87,8) iyileşme gözlenmiştir ve iyileşme ortaya çıkana kadar geçen medyan süre 5,3 hafta olduğubelirlenmiştir (aralık: 0,1-175,9+). Nivolumab 1mg/kg ile kombinasyon halindeki YERVOY 3m/kgile tedavi edilen hastalar arasında, karaciğer fonksiyon testi anomalilerinin insidansı Derece 2 (%6,9),Derece 3 (%15,8) ve Derece 4 (%1,8) dahil olmak üzere toplamda %30,1 olmuştur. İmmünite ile ilişkili advers deri reaksiyonlarıYERVOY, immünite ile ilişkili olması muhtemel olan, ciddi advers deri reaksiyonları ile ilişkilendirilmiştir. gp100 ile kombinasyon halinde YERVOY alanhastaların %1'inden azındaölümcül toksik epidermal nekroliz (SJS dahil) bildirilmiştir (bkz. Bölüm 5.1). Klinik çalışmalarda vepazarlama sonrası kullanımda YERVOY ile Eozinofili ve Sistemik Semptomların Eşlik Ettiği İlaçReaksiyonları (DRESS) nadir olarak bildirilmiştir. Pazarlama sonrası kullanım sırasında tesadüfipemfigoid vakaları bildirilmiştir. 3 mg/kg YERVOY monoterapi grubunda hastaların %26'sında herhangi bir şiddette döküntü ve kaşıntı bildirilmiştir. YERVOY kaynaklı döküntü ve kaşıntı, ağırlıklı olarak hafif (Derece 1) veyaorta şiddette (Derece 2) olup semptomatik tedaviye yanıt vermekteydi. Orta ila şiddetli veya ölümcül(Derece 2 - 5) advers deri reaksiyonlarının başlamasına kadar geçen ortanca süre, tedavininbaşlangıcından itibaren 3 haftaydı (aralık 0,9 - 16 hafta). Protokolde belirtilen yöntem rehberlerinde,vakaların büyük bir bölümünde (%87) iyileşme görülürken başlangıçtan itibaren iyileşme görülenekadar geçen ortanca süre 5 haftaydı (aralık 0,6 - 29 hafta). Nivolumab (kemoterapi ya da kemoterapisiz) ile kombinasyon halindeki YERVOY ile tedavi edilen hastalarda, döküntü insidansı %46,2 (968/2094) olmuştur. Hastaların sırasıyla %14,1(296/2094), %4,6 (97/2094) ve %<0,1'sinde (2/2094) Derece 2, Derece 3 ve Derece 4 vakalarbildirilmiştir. Başlangıca kadar geçen medyan süre 0,7 aydı (aralık: 0,0-33,8). 671 hastada (%69,6)iyileşme gözlenmiştir ve iyileşme ortaya çıkana kadar geçen medyan süre 11,1 hafta olduğubelirlenmiştir (aralık: 0,1-268,7+). Nivolumab 1mg/kg ile kombinasyon halindeki YERVOY 3mg/kgile tedavi edilen hastalar arasında, Derece 2 (%20,3) ve Derece 3 (%7,8) dahil olmak üzere döküntüinsidansı %65,2 olmuştur. İmmünite ile ilişkilinörolojik reaksiyonlarYERVOY, ciddi immünite ile ilişkili nörolojik reaksiyonlar ile ilişkilendirilmiştir. gp100 ile kombinasyon halinde 3 mg/kg YERVOY alan hastaların %1'inden azında ölümcül Guillain-Barresendromu bildirilmiştir. Klinik çalışmalarda daha yüksek dozda YERVOY uygulanan hastaların%1'inden azında myastenia gravis benzeri semptomlar da bildirilmiştir. İmmünite ile ilişkili nefrit ve renal fonksiyon bozukluğuNivolumab (kemoterapi ya da kemoterapisiz) ile kombinasyon halindeki YERVOY ile tedavi edilen hastalarda, nefrit ya da renal fonksiyon bozukluğu insidansı %6,1 (128/2094) olmuştur. Hastalarınsırasıyla %2,3 (49/2094), %1,0 (20/2094) ve %0,5'inde (10/2094) Derece 2, Derece 3 ve Derece 4vakalar bildirilmiştir. İki hasta (<% 01) ölümle sonuçlanmıştır. Başlangıca kadar geçen medyan süre2,5 aydı (aralık: 0,0-34,8). 97 hastada (%75,8) iyileşme gözlenmiştir ve iyileşme ortaya çıkana kadargeçen medyan süre 6,3 hafta olduğu belirlenmiştir (aralık: 0,1-172,1+). İmmünite ile ilişkili endokrinopati3 mg/kg YERVOY monoterapi grubunda hastaların %4'ünde herhangi bir şiddette hipopitüitarizm bildirilmiştir. Hastaların %2'sinde herhangi bir şiddette adrenal yetmezlik, hipertiroidizm vehipotiroidizm bildirilmiştir. Ciddi (Derece 3 veya 4) hipopitütiarizm sıklığı hastaların %3'ü olarakkaydedilmiştir. Çok ciddi (Derece 3 veya 4) adrenal yetmezlik, hipertiroidizm veya hipotiroidizmbildirimi yapılmamıştır. Orta ila çok şiddetli (Derece 2 - 4) immünite ile ilişkili endokrinopatininbaşlamasına kadar geçen süre, tedavinin başlangıcından itibaren 7 ila yaklaşık 20 hafta arasındaydı.Klinik çalışmalarda gözlemlenen immünite ile ilişkili endokroinopati genelde hormon replasmantedavisi ile kontrol edilmiştir. Nivolumab (kemoterapi ya da kemoterapisiz) ile kombinasyon halindeki YERVOY ile tedavi edilen hastalarda, tiroid bozukluklarının insidansı %22,9 (479/2094) olmuştur. Hastaların sırasıyla %12,5(261/2094) ve %1,0'inde (21/2094) Derece 2 ve Derece 3 tiroid bozukluk bildirilmiştir. Hastaların sırasıyla %2,0 (42/2094) ve %1,6'sında (33/2094) Derece 2 ve Derece 3 hipofizit (lenfositik hipofizit dahil) meydana gelmiştir. Hastaların sırasıyla %0,8 (16/2094) ve %0,5'inde(11/2094) Derece 2 ve Derece 3 hipopitüitarizm meydana gelmiştir. Hastaların sırasıyla %2,3(49/2094), %1,5 (32/2094) ve %0,2'sinde (4/2094) Derece 2, Derece 3 ve Derece 4 adrenal yetersizlik(ikincil adrenokortikal yetmezlik dahil) meydana gelmiştir Hastaların sırasıyla %0,1 (1/2094), %0,2(4/2094), <%0,1'sinde (1/2094) ve 0,1 (3/2094) Derece 1, Derece 2, Derece 3 ve Derece 4 şekerhastalığı meydana gelmiştir. Hastaların <% 0,1 (2/2094)'inde Derece 4 diyabetik ketoasidozraporlanmıştır. Bu endokrinopatilerin başlangıcına kadar geçen medyan süre 2,1 aydı (aralık: 0,0-28,1). 201 hastada (%40,7) iyileşme gözlenmiştir ve iyileşmeye kadar geçen süresi 0,3 ile 257,1+hafta arasında değişmiştir. İnfüzyon reaksiyonlarıNivolumab (kemoterapi ya da kemoterapisiz) ile kombinasyon halindeki YERVOY ile tedavi edilen hastalarda, aşırı duyarlılık/infüzyon reaksiyonlarının insidansı %4,9 (103/2094) olmuştur. Hastalarınsırasıyla %2,1 (44/2094), %2,5'inde (53/2094), %0,2(5/2094) ve <%0,1(1/2094)'ünde Derece 1,Derece 2, Derece 3 ve Derece 4 vakalar bildirilmiştir. MPM'de, nivolumab 3 mg/kg ile kombinasyonhalindeki YERVOY 1 mg/kg ile tedavi edilen hastalarda, aşırı duyarlılık/infüzyon reaksiyonlarınıninsidansı %12 idi. İmmünoj^^isiteFaz 2 ve 3 klinik çalışmalarda YERVOY alan ileri evre melanomlu hastaların %2'sinden daha azında YERVOY'a karşı antikor gelişmiştir. Bu hastaların hiçbirinde infüzyonla ilgili ya da infüzyonsırasında aşırı duyarlılık ya da anafilaktik reaksiyonlar gözlenmemiştir. YERVOY'a karşı nötralizeedici antikorlar tespit edilmemiştir. Genel olarak, antikor gelişimi ile yan etkiler arasında belirgin birilişki gözlenmemiştir. Nivolumab ile kombinasyon halinde YERVOY ile tedavi edilen ve anti-ipilimumab antikorlarının varlığı açısından değerlendirilebilen hastaların anti-ipilimumab antikorları insidansı %6,3 ila %8,4arasındaydı. Anti-nivolumab antikorlarının varlığı açısından değerlendirilebilen hastalarda, anti-nivolumab antikorlarının insidansı, 3 haftada bir nivolumab 3 mg/kg ve YERVOY 1 mg/kg ile %26,3 haftada bir nivolumab 1 mg/kg ve YERVOY 3 mg/kg ile %37,8 olmuştur. Nivolumaba karşınötralize edici antikorların insidansı, 3 haftada bir nivolumab 3 mg/kg ve YERVOY 1 mg/kg ile %0,5,3 haftada bir nivolumab 1 mg/kg ve YERVOY 3 mg/kg ile %4,6 olmuştur. Nivolumab ile kombinasyon halinde uygulandığında, YERVOY'un CL'si anti-ipilimumab antikorlarının varlığında değişmemiştir ve toksisite profilinin değiştiğine ilişkin kanıt bulunmamıştır. Laboratuvar değerlerindeki bozukluklarNivolumab (kemoterapi ya da kemoterapisiz) ile kombinasyon halindeki YERVOY ile tedavi edilen hastalarda, başlangıçtan itibaren laboratuvar değerlerinde Derece 3 veya 4 düzeyinde bozuklukgözlenen hastaların oranı: Anemi için %4,9, trombositopeni için %1,5, lökopeni için %2,3, lenfopeniiçin %7,3, nötropeni için %3,4, alkalen fosfataz yükselmesi için %2,9, AST artışı için %7,3, ALTartışı için %8,4, toplam bilirubin yükselmesi için %1,2, kreatinin yükselmesi için %1,6, hiperglisemiiçin %5,8, amilaz yükselmesi için %8,4, lipaz yükselmesi için %16,7, hipokalsemi için %0,8,hipernatremi için %0,2, hiperkalsemi için %1,0, hiperkalemi için %1,9, hipermagnezemi için %0,5,hipokalemi için %3,4 ve hiponatremi için %9,8. Nivolumab 1 mg/kg ile kombinasyon halindekiYERVOY 3 mg/kg ile tedavi edilen hastalar arasında, başlangıçtan Derece 3 veya 4'e kötüleşenyüksek oranda hastada ALT artışı (%15,3)gözlemlenmiştir. Pediyatrik PopülasyonYERVOY 18 yaşın altındaki çocuklarda kullanılmamalıdır. Yaşlı HastalarMPM hastalarında, nivolumab ile kombinasyon halinde ipilimumab alan tüm hastalara (sırasıyla %54 ve %28) kıyasla 75 yaş ve üzeri hastalarda (sırasıyla %68 ve %35) ciddi advers reaksiyonların veadvers reaksiyonlara bağlı tedaviyi bırakma oranı daha yüksekti. Şüpheli advers reaksiyonların raporlanmasıRuhsatlandırma sonrası şüpheli ilaç advers reaksiyonlarının raporlanması büyük önem taşımaktadır. Raporlama yapılması, ilacın yarar / risk dengesinin sürekli olarak izlenmesine olanak sağlar. Sağlıkmesleği mensuplarının herhangi bir şüpheli advers reaksiyonu Türkiye Farmakovijilans Merkezi(TÜFAM)'ne bildirmeleri gerekmektedir. (www.titck.gov.tr; e- posta: [email protected]; tel: 0 800 31400 08; faks: 0 312 218 35 99) 4.9 Doz aşımı ve tedavisiYERVOY'un tolere edilen maksimum dozu belirlenmemiştir. Klinik çalışmalarda hastalar bariz bir toksik etki görülmeden 20 mg/kg'a kadar dozlar almıştır. Doz aşımı olursa, hastalar advers reaksiyon bulguları ya da semptomları açısından yakından gözlenmeli ve uygun semptomatik tedavi başlatılmalıdır. 5. FARMAKOLOJİK ÖZELLİKLERİ5.1 Farmakodinamik ÖzellikleriFarmakoterapötik grup: Antineoplastik ajanlar, monoklonal antikorlar, ATC kodu: L01FX04. Etki mekanizmasıSitotoksik T-lenfosit antijeni (CTLA-4) T-hücresi aktivasyonunun önemli bir regülatörüdür. YERVOY, CTLA-4 yolağıyla indüklenen T hücresi inhibe edici sinyalleri bloke eden bir CTLA-4immün kontrol noktası inhibitörüdür ve tümör hücrelerine karşı doğrudan bir T hücresi immünsaldırısına geçmek için harekete geçen reaktif T efektör hücrelerin sayısını arttırmaktadır. CTLA-4blokajı, düzenleyici T hücrelerinin işlevini de azaltabilir ve bu durum bir anti-tümör immün yanıtınakatkıda bulunabilir. YERVOY tümör bölgesindeki düzenleyici T hücrelerini seçici olarak tüketebilirve bu da tümör içi efektör T/düzenleyici T hücre oranının artmasına yol açarak tümör hücrelerininölümünü tetikleyebilir. Farmakodinamik etkileri YERVOY alan melanom hastalarında periferal kandaki mutlak lenfosit sayımı (ALC) indüksiyon dozu süreci boyunca artmıştır. Faz 2 çalışmalarda bu artış doza bağlıdır. MDX010-20'de (bkz. Bölüm5.1), gp100 ile birlikte ya da tek başına uygulanan 3 mg/kg YERVOY, indüksiyon dozu sürecindeALC'yi yükseltmiş, ancak araştırma amaçlı tek başına gp 100 peptid aşısı alan kontrol grubuhastalarında anlamlı bir ALC değişikliği görülmemiştir. Melanom hastalarının periferal kanındaYERVOY tedavisinden sonra aktive HLA-DR+ CD4+ ve CD8+T hücrelerinin yüzdesinde ortalamabir artış gözlenmiştir: bu gözlemler etki mekanizması ile uyumludur. YERVOY tedavisinden sonramerkezi hafıza (CCR7+ CD45RA-) CD4+ ve CD8+ T hücrelerinin yüzdesinde ortalama bir yükselmeve efektör hafıza (CCR7- CD45RA-) CD8+ T hücrelerinin yüzdesinde ise daha az ancak anlamlı birortalama yükselme de gözlenmiştir. Klinik etkililik ve güvenlilik Nivolumab ile kombinasyon halinde YERVOYYERVOY ile kombinasyon tedavisini takiben monoterapi olarak verilen nivolumab için doz önerileri ile ilişkili klinik etkililik ve güvenlilik hakkında daha fazla bilgi için lütfen nivolumab KÜB'ünebakınız. Doz/maruziyet etkililik ve güvenlilik ilişkilerinin modellenmesine dayanarak, her 2 haftada bir 240 mg veya her 2 haftada bir 3 mg/kg nivolumab arasında etkililik ve güvenlilik açısından klinik olarakanlamlı bir fark bulunmamaktadır. Ek olarak, bu ilişkilere dayanarak, ileri evre melanom ve RHK'de4 haftada bir 480 mg veya her 2 haftada bir 3 mg/kg nivolumab dozu arasında klinik olarak anlamlıbir fark görülmemiştir. YERVOY monoterapisi ile Klinik Çalışmalar MelanomDaha önce tedavi edilmiş ve ileri evre (rezeke edilemeyen veya metastatik) melanom hastalarında önerilen 3 mg/kg YERVOY dozunda genel sağkalım (OS) avantajı bir Faz 3 çalışmada (MDX010-20) kanıtlanmıştır. Oküler melanom, primer MSS melanomu, aktif beyin metastazları, insan immünyetmezlik virüsü (HIV), hepatit B ve hepatit C görülen hastalar, MDX010-20 klinik çalışmasına dahiledilmemiştir. Klinik çalışmaya ECOG (The Eastern Cooperative Oncology Group - Doğu KooperatifOnkoloji Grubu) performans durumu >1 olan ve mukozal melanom görülen hastalar dahiledilmemiştir. Karaciğer metastazı görülmeyen ve başlangıçta AST değeri >2,5 x UNL olan hastalar,karaciğer metastazı görülen ve başlangıçta AST değeri >5 x UNL olan hastalar ve başlangıçta totalbilirubin değeri > 3 x ÜNL olan hastalar da çalışmaya dahil edilmemiştir. Otoimmün hastalık geçmişi olan hastalar için bkz. Bölüm 4.4. MDX010-20Aşağıdakilerden birini ya da daha fazlasını içeren rejimler ile önceden tedavi görmüş olan ileri evre (rezeke edilemeyen veya metastatik) melanom hastalarının kaydolduğu çift kör, bir Faz 3çalışmasıdır: IL-2, dekarbazin, temozolomid, fotemustin, veya karboplatin. Hastalar 3:1:1 oranındarandomize edilmiş ve 3 mg/kg YERVOY + araştırma amaçlı gp 100 peptid aşısı (gp100), 3 mg/kgYERVOY monoterapisi ya da sadece gp100 almışlardır. Hastaların tamamı HLA-A2*0201tipindedir; bu HLA tipi immün gp100 varlığını destekler. Hastalar, başlangıç BRAF mutasyondurumundan bağımsız olarak kaydedilmiştir. Hastalar, toleranslarına göre, 4 doz YERVOY'u 3haftada bir almışlardır (indüksiyon tedavisi). İndüksiyon dönemi bitmeden tümör yüklerindeki artışbelirgin olan hastalar performans durumlarının uygun olması şartıyla, tolere ettikleri sürece,indüksiyon tedavisine devam etmişlerdir. YERVOY'a verilen tümör yanıtı indüksiyon tedavisitamamlandıktan sonra yaklaşık 12. haftada değerlendirilmiştir. Tümörün ilk değerlendirmesinden >3 ay sonra, başlangıçtaki klinik yanıtın (PR veya CR) ardından veya stabil hastalık (SD) (modifiye DSÖ kriterlerine göre) ardından progresif hastalık (PD) geliştirenkişilere YERVOY ile ilave tedavi (tekrar tedavi) önerilmiştir. Primer sonlandırma kriteri gp100grubuna karşı YERVOY + gp100 grubunda genel sağkalımdı (OS). Başlıca sekonder sonlandırmakriterleri YERVOY monoterapi grubuna karşı YERVOY+gp100 grubunda ve gp100 grubuna karşıYERVOY monoterapi grubunda OS idi. Toplam 676 hasta randomize edilmiştir: 137'si YERVOY monoterapi grubuna, 403'ü YERVOY + gp100 grubuna, 136'sı da sadece gp100 grubuna. Büyük bir bölümü, indüksiyon sırasında 4 dozunhepsini de almıştır. Otuz iki hasta bir tekrar tedavi almıştır: bunların 8'i YERVOY monoterapigrubunda, 23'ü YERVOY + gp100 grubunda ve 1'i de gp100 grubundadır. Takip süresi 55 ay devametmiştir. Başlangıç karakteristikleri gruplar arasında iyi dengelenmişti. Ortanca yaş 57'ydi. Hastalarınçoğunluğunun (%71-73) M1c evresinde hastalığı vardı ve hastaların %37-40'ının başlangıç laktatdehidrojenazı (LDH) yüksekti. Toplam 77 hastanın daha önce tedavi edilmiş beyin metastazı hikayesivardı. YERVOY içeren rejimler gp100 kontrol grubuna karşı istatistiksel olarak anlamlı bir OS avantajı elde etmiştir. OS karşılaştırmasında YERVOY monoterapisi ile gp100 arasındaki risk oranı (HR)0, 66 (%95 GA: 0,51, 0,87; p = 0,0026) olmuştur. Alt grup analizinde, genel sağkalım (OS) yararının hasta alt gruplarının büyük bir kısmının içerisinde tutarlıydı (M [metastaz]-evre, önceki interlökin-2, başlangıçtaki LDH, yaş, cinsiyet ve önceki tedavitipi ve sayısı). Ancak, 50 yaşın üzerindeki kadınlarda YERVOY tedavisinin OS yararını destekleyenveriler sınırlıdır. Alt grup analizi az sayıda hastayı içerdiğinden, bu verilerden kesin sonuçlarçıkartılamamaktadır. 1 ve 2 yıldaki ortanca ve tahmin edilen OS oranları Tablo 7'de verilmiştir.
3 mg/kg YERVOY monoterapi grubunda ortanca OS, sırasıyla SD olan hastalarda 22 ay ve PD olanlarda 8 ay olmuştur. Bu analiz yapılırken CR ya da PR geliştiren hastaların ortancalarınaulaşılmamıştı. Tekrar tedavi gereken hastalar için BORR, YERVOY monoterapi grubunda %o38 (3/8 hasta) ve gp100 grubunda %0 olmuştur. Hastalık kontrol oranı (DCR, CR+PR+SD olarak tanımlanır) sırasıyla %75(6/8 hasta) ve %0 olmuştur. Bu analizlerde hasta sayısının sınırlı olmasından dolayı YERVOY'untekrar tedavi etkisi tam olarak bilinmemektedir. YERVOY tedavisini takiben sistemik kortikosteroid kullanılarak veya kullanılmadan klinik aktivite benzer şekilde gelişmiş veya korunmuştur. CA184-169Bir çift kör, Faz 3 çalışmaya daha önce tedavi görmüş ya da tedavi görmemiş rezeke edilemeyen Evre III ya da Evre IV melanom hastaları kaydolmuştur. Toplam 727 hasta, 4 doza kadar her 3 haftada bir362'si YERVOY 3 mg/kg ve 365'i YERVOY 10 mg/kg alacak şekilde randomize edilmiştir.YERVOY 10 mg/kg grubunda ortanca OS (%95 GA) 16 ay (11,63, 17,84) ve YERVOY 3 mg/kggrubunda ortanca OS (%95 GA) 12 aydı (9,86, 13,27). YERVOY 10 mg/kg ve 3 mg/kg gruplarıarasında karşılaştırılan genel sağkalım HR = 0,84 (%95 GA: 0,70, 0,99; P-değeri = 0,04) göstermiştir.10 mg/kg ve 3 mg/kg grupları arasında progresyonsuz sağkalımda (PFS) istatistiksel açıdan anlamlıfark gözlemlenmemiştir. (HR 0,89, %95 GA 0,76, 1,04 ve log-sıra testi P-değeri = 0,1548). BORR,10 mg/kg ve 3 mg/kg gruplarında benzerdi. BORR, 10 mg/kg grubunda %15,3 (%95 GA: 11,8, 19,5)ve 3 mg/kg grubunda %12,2 (%95 GA: 9, 16) idi. YERVOY 10 mg/kg, 3 mg/kg doz ilekarşılaştırıldığında daha yüksek advers olay oranları ile ilişkilendirilmiştir. 10 mg/kg ve 3 mg/kggruplarındaki ciddi advers reaksiyon sıklıkları %37% ve %18 olup, en yaygın 3 advers reaksiyondiyare (%10,7'ye %5,5), kolit (%8'e %3) ve hipofizitti (%4,4'e %1,9). 10 mg/kg ve 3 mg/kggruplarında tedavinin kesilmesine neden olan advers olaylar sırasıyla hastaların %31'i ve %19'undameydana gelmiş olup, 4 ve 2 hastada ölüme neden olan AO'lar meydana gelmiştir. Önerilen 3 mg/kg dozunda, ortanca OS, genel popülasyona kıyasla 50 yaşındaki ve üstündeki kadınların alt grubunda benzerdi: (11,40 aya 11,53). Başlangıçta beyin metastazları olan alt gruptakiortanca OS önerilen 3 mg/kg dozunda 5,67 aydı. YERVOY monoterapisi ile diğer çalışmalar Melanom CA184332CA184338Birleştirilmiş Faz 2 ve 3 klinik çalışmalarda daha önce kemoterapi görmemiş olan hastalarda (N=78: randomize edilen) ve iki retrospektif gözlem çalışmasındaki daha önce tedavi edilmemiş hastalarda(N=273 ve N=157) YERVOY 3 mg/kg monoterapisi ile elde edilen OS, genel olarak tutarlıdır. İkigözlem çalışmasında, hastaların %12,1 ve 33,1'inde ileri evre melanom teşhisi sırasında beyinmetastazı mevcuttu. Ortanca OS ve tahmini 1 yıllık, 2 yıllık, 3 yıllık ve 4 yıllık sağkalım oranlarıTablo 8'de sunulmaktadır. Birleştirilmiş Faz 2 ve 3 klinik çalışmalarda daha önce kemoterapigörmemiş olan hastalarda (N=78) tahmini 1 yıllık, 2 yıllık ve 3 yıllık sağkalım oranları, sırasıyla%54,1 (%95 GA: 42,5 - 65,6), %31,6 (%95 GA: 20,7 - 42,9) ve %23,7 (%95 GA: 14,3 - 34,4) idi.
CA184332 çalışmasında beyin metastazı olan hastalarda ortanca genel sağkalım 7 ay (%95 GA: 5,06 - 12,81) ve beyin metastazı olmayan hastalarda ortanca genel sağkalım 14,1 ay (%95 GA: 9,96-tahmin edilemiyor) bulunmuştur. CA184338 çalışmasında beyin metastazı olan hastalarda ortanca genel sağkalım 6,3 ay (%95 GA: 3,2 - 12) ve beyin metastazı olmayan hastalarda ortanca genel sağkalım 17,7 ay (%95 GA: 13,6 - 12,1)bulunmuştur. YERVOY (3mg/kg'da) tedavisinin uzun dönemli sağkalım yararı önceden tedavi görmüş ve hiç tedavi görmemiş ileri melanomlu hastalarda (N = 965) yapılan klinik çalışmalardan alınan OSverilerinin birleştirilmiş analiziyle gösterilmektedir. Kaplan-Meier OS eğrisi yaklaşık 3. yıldabaşlayan ve bazı hastalarda 10 yıla kadar uzayan bir platoyu ortaya koymuştur (OS oranı = %21 [%95GA: 17-24]) (bkz. Şekil 1). Şekil 1: Birleştirilmiş analizde YERVOY 3 mg/kg ile Genel Sağkalım 1.0-K3.0 mg/kg 0.8 H l
aö Ü 0.0-
Nivolumab ile kombinasyon halinde YERVOY ile klinik çalışmalar MelanomYERVOY monoterapisine karşı nivolumab ile kombinasyon halinde YERVOY veya nivolumab monoterapisi alınan randomize Faz 3 çalışma (CA209067)İleri evre (rezeke edilemeyen veya metastatik) melanom tedavisi için YERVOY 3 mg/kg monoterapisine karşı 1 mg/kg nivolumab ile kombinasyon halindeki 3 mg/kg YERVOY'un ve 3mg/kg nivolumabın güvenliliği ve etkililiği faz 3, randomize, çift kör çalışmada (CA209067)değerlendirilmiştir. Nivolumab içeren iki grup arasındaki farklılıklar tanımlayıcı şekildedeğerlendirilmiştir. Çalışmaya rezeke edilemeyen Evre III ya da Evre IV melanomun doğrulandığıyetişkin hastalar dahil edilmiştir. Hastaların ECOG performans durumunun 0 ya da 1 olmasıgerekmiştir. Rezeke edilemeyen ya da metastatik melanom için daha önce sistemik kanser tedavisigörmemiş olan hastalar kaydolmuştur. Randomizasyondan en az 6 hafta önce tamamlanmış olmasıkaydıyla önceki adjuvan/neoadjuvan tedavisine izin verilmiştir. Aktif otoimmün hastalığı,oküler/üveal melonomu veya aktif beyin ya da leptomeningeal metastazları bulunan hastalarçalışmaya dahil edilmemiştir. Toplam 945 hasta, nivolumab ile kombinasyon halinde YERVOY (n=314), nivolumab monoterapisi (n=316) veya YERVOY monoterapisi (n=315) alacak şekilde randomize edilmiştir. Kombinasyonkolundaki hastalar ilk 4 doz için her 3 haftada bir intravenöz yoldan 60 dakika boyunca 1 mg/kgnivolumab ve 90 dakika boyunca 3 mg/kg YERVOY ardından her 2 haftada bir 3 mg/kg nivolumabmonoterapisi almıştır. Nivolumab monoterapisi kolundaki hastalar her 2 haftada bir 3 mg/kgnivolumab almıştır. Karşılaştırma ilacı kolundaki hastalar 4 doz için her 3 haftada bir intravenözyoldan 3 mg/kg YERVOY ve nivolumab eşleşmeli plasebo ardından her 2 haftada bir plaseboalmıştır. Randomizasyon, PD-L1 ekspresyonu (<%5'e > %5 tümör hücresi membran ekspresyonu),BRAF durumu ve Amerika Kanser Komitesi (AJCC) Evreleme Sistemi uyarınca M evresine görekatmanlandırılmıştır. Tedavi, klinik yarar gözlendiği sürece veya tedavi hasta tarafından artık tolereedilmeyinceye kadar sürdürülmüştür. Tümör değerlendirmeleri randomizasyondan 12 hafta sonra ve ardından ilk yıl için her 6 haftada bir ve daha sonra 12 haftada bir gerçekleştirilmiştir. Primer sonlanım noktaları progresyonsuz sağkalım ve OS idi. ORR ve yanıt süresi de değerlendirilmiştir. Başlangıç karakteristikleri üç tedavi grubu arasında dengeliydi. Hastaların ortanca yaşı 61 olup (aralık: 18 ila 90 yaş) hastaların %65'i erkek ve %97'si beyazdı. ECOG performans durumu 0 (%73)veya 1 (%27) idi. Hastaların büyük çoğunluğunda AJCC Evre IV hastalık (%93) vardı; %58'indeçalışmaya giriş sırasında M1c hastalık vardı. Hastaların yüzde yirmi üçü daha önce adjuvan tedavisigörmüştü. Hastaların yüzde otuz ikisinde BRAF mutasyon pozitif melanom vardı; hastaların%26,5'inde PD-L1 > %5 tümör hücresi membran ekspresyonu vardı. Hastaların yüzde dördündebeyin metastazı öyküsü vardı ve hastaların %36'sında başlangıç LDH düzeyi çalışma başlangıcındakiUNL'ten yüksekti. Ölçülebilir tümör PD-L1 ekspresyonu olan hastalar arasında, hastaların dağılımıüç tedavi grubunda dengeliydi. Tümör PD-L1 ekspresyonu, PD-L1 IHC 28-8 pharmDx miktar tayinikullanılarak belirlenmiştir. Birincil analizde (minimum takip 9 ay) ortanca PFS, nivolumab grubunda 6,9 ay iken YERVOY grubunda 2,9 aydı (HR = 0,57, %99,5 GA: 0,43, 0,76; p <0,0001). Ortanca PFS, YERVOYgrubundaki 2,9 aya kıyasla nivolumab grubuyla kombinasyon halinde YERVOY'da 11,5 aydı (HR =0,42, %99,5 GA: 0,31, 0,57; p <0,0001). Tanımlayıcı analizden PFS sonuçları (en az 90 ay takip süresi ile) Şekil 2'de (tamamı randomize edilmiş popülasyon), Şekil 3 (tümör PD-L1 %5 kesmede) ve Şekil 4'te (tümör PD-L1 %1 kesmede)gösterilmiştir. Şekil 2: Progresyonsuz Sağkalım (CA209067)
YERVOY 3157846 343128211816151211109971- - -*---- Nivolumab+YERVOY (olaylar: 189/314), ortanca ve %95 GA: 11,50 (8,90, 20,04).12 ayda PFS oram ve %95 GA: %49 (44, 55), 60 ayda PFS oram ve %95 GA: %36 (32, 42), , 90 ayda PFS oram % 95 GA: %33 (27,39)-A-Nivolumab (olaylar: 203/316), ortanca ve %95 GA: 6,93 (5,13, 10,18).12 ayda PFS oranı ve %95 GA: %42 (36, 47), 60 ayda PFS oranı ve %95 GA: %29 (24, 35), 90 ayda PFS oranı %95 GA: %27 (22,33)- - -O- - - YERVOY (olaylar: 245/315), ortanca ve %95 GA: 2,86 (2,79, 3,15).12 ayda PFS oranı ve %95 GA: %18 (14, 23), 60 ayda PFS oranı ve %95 GA: %8 (5, 12), 90 ayda PFS oranı ve %95 GA: %7 (4,11)Nivolumab+YERVOY'a karşı YERVOY - risk oranı ve %95 GA: 0,42 (0,35, 0,51);Nivolumab'a karşı YERVOY - risk oranı ve %95 GA: 0,53 (0,44, 0,64);Nivolumab+ YERvOY'a karşı nivolumab - risk oranı ve %95 GA: 0,79 (0,65, 0,97)Şekil 3: PD-L1 ekspresyonuna göre progresyonsuz sağkalım: %5 kesme (CA209067)PD-L1 ekspresyonu <%5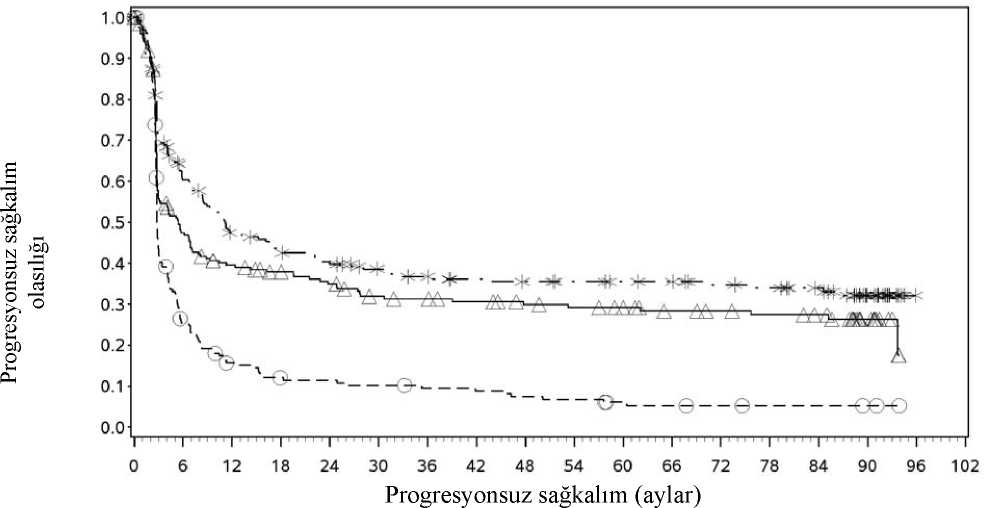
Risk altındaki gönüllülerin sayısı Nivolumab + YERVOY210113- - -*----Nivolumab+YERVOY (olaylar: 127/210), ortanca ve %95 GA: 11,17 (7,98, 17,51)-A-Nivolumab (olaylar: 139/208), ortanca ve %95 GA: 5,39 (2,96, 7,13)- - -O- - - YERVOY (olaylar: 171/202), ortanca ve %95 GA: 2,79 (2,76, 3,02)Nivolumab+YERVOY'a karşı YERVOY - risk oranı ve %95 GA: 0,42 (0,33, 0,53) Nivolumab'a karşı YERVOY - risk oranı ve %95 GA: 0,54 (0,43, 0,68)Nivolumab+ YERVOY'a karşı nivolumab - risk oranı ve %95 GA: 0,77 (0,61, 0,98)#
İH"o13)bX5NS c o 2i bC p- - -*----Nivolumab+YERVOY (olaylar: 36/68), ortanca ve %95 GA: 22.11 (9,72, 82,07)-A-Nivolumab (olaylar: 46/80), ortanca ve %95 GA: 22,34 (9,46, 39,13.)- - -O- - - YERVOY (olaylar: 60/75), ortanca ve %95 GA: 3,94 (2,79, 4,21)Nivolumab+ YERVOY'a karşı YERVOY risk oranı ve %95 GA: 0,38 (0,25, 0,58) Nivolumab'a karşı YERVOY - risk oranı ve %95 GA: 0,43 (0,29, 0,64)Nivolumab+ YERvOY'a karşı nivolumab - risk oranı ve %95 GA:0,89 (0,58, 1,35)Şekil 4: PD-L1 ekspresyonuna göre progresyonsuz sağkalım: %1 kesme (CA209067)PD-L1 ekspresyonu <%1
Risk Altındaki Hasta Sayısı Nivolumab + YERVOY12365514641
Nivolumab 117YERVOY 113- - -*----Nivolumab+YERVOY (olaylar: 76/123), ortanca ve %95 GA: 11,17 (6,93, 22,18)-A- Nivolumab (olaylar: 85/117), ortanca ve %95 GA: 2,83 (2,76, 5,62)- - -O- - - YERVOY (olaylar: 94/113), ortanca ve %95 GA: 2,73 (2,66, 2,83)Nivolumab+ YERVOY'a karşı YERVOY risk oranı ve %95 GA: 0,39 (0,28, 0,53) Nivolumab'a karşı YERVOY - risk oranı ve %95 GA: 0,59 (0,44, 0,79)Nivolumab+ YERvOY'a karşı nivolumab - risk oranı ve %95 GA:0,66 (0,48, 0,90)PD-L1 ekspresyonu > %1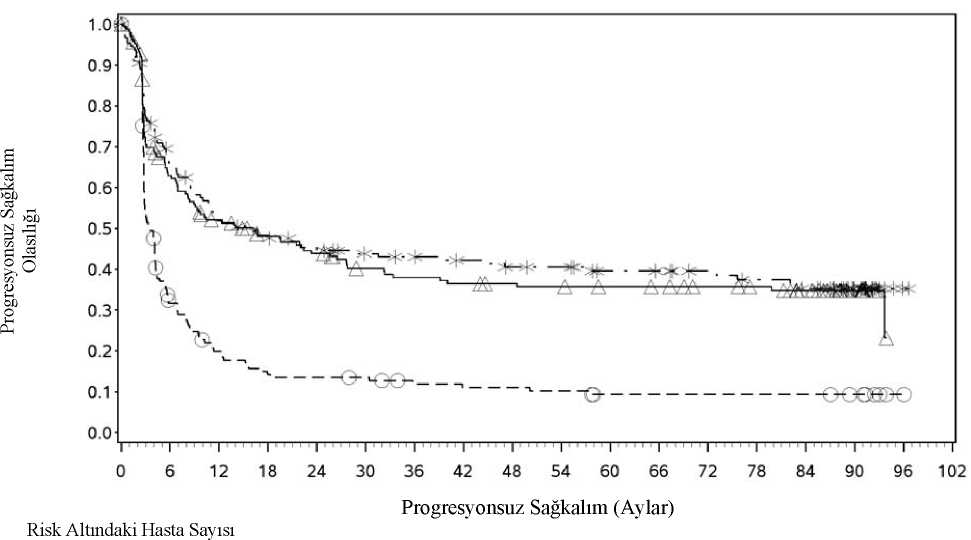
- - -*----Nivolumab+YERVOY (olaylar: 90/155), ortanca ve %95 GA: 16,13 (8,90, 45,08)-A-Nivolumab (olaylar: 102/171), ortanca ve %95 GA: 16,20 (8,11, 27,66)- - -O- - - YERVOY (olaylar: 137/164), ortanca ve %95 GA: 3,48 (2,83, 4,17)Nivolumab+ YERVOY'a karşı YERVOY risk oranı ve %95 GA: 0,42 (0,32, 0,55)Nivolumab'a karşı YERVOY - risk oranı ve %95 GA: 0,45 (0,35, 0,59)Nivolumab+ YERVOY'a karşı nivolumab - risk oranı ve %95 GA: 0,92 (0,69, 1,22)Nihai OS analizi tüm hastalar için en az 28 aylık takip süresi olduğunda meydana gelmiştir. 28 ayda, YERVOY grubundaki 19,98 aya (HR=0,63, %98 GA: 0,48, 0,81; p-değeri: <0,0001) karşı nivolumabgrubunda medyan OS'ye ulaşılmamıştır. YERVOY grubuyla (HR=0,55; %98 GA: 0,42, 0,72; p-değeri: <0,0001) kıyaslandığında nivolumab ile kombinasyon halindeki YERVOY grubunda medyanOS'ye ulaşılmamıştır. En az 90 aylık takip döneminde yapılan ek tanımlayıcı analizin OS sonuçları orijinal primer analizle tutarlı sonuçlar göstermektedir. Bu takip dönemi analizinin OS sonuçları Şekil 5 (tümü randomize),Şekil 6 ve Şekil 7'de (tümör PD-Ll'de %5 ve %1 kesme) gösterilmektedir. OS analizi alınan sonraki tedavileri de hesaplayacak şekilde ayarlanmamıştır. Sırasıyla kombinasyon, nivolumab monoterapisi ve YERVOY kollarındaki hastaların %36,0, %49,1 ve %66,3'ü daha sonrasistemik tedavi görmüştür. Sırasıyla kombinasyon, nivolumab monoterapisi ve YERVOYkollarındaki hastaların %19,1, %34,2 ve %48,3'ü daha sonra immünoterapi (anti-PD1 tedavisi, anti-CTLA-4 antikoru veya başka bir immünoterapi dahil) almıştır. Şekil 5 Genel Sağkalım (CA209067) - Minimum 90 aylık takip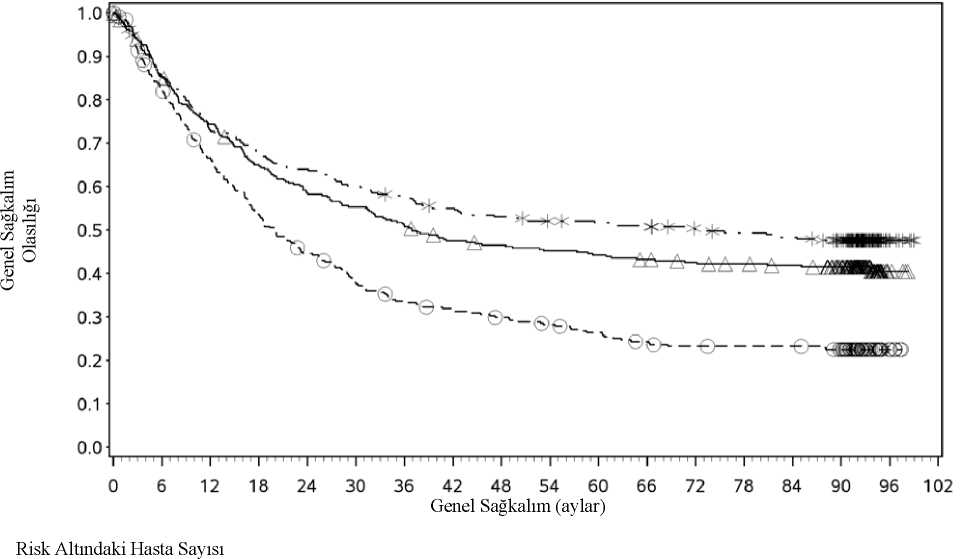 Nivolumab+YERVOY314 265227210199187179169163158Nivolumab316 266231201181171158145141137YERVOY315 253203163135113100948781-*---- Nivolumab+YERVOY (olaylar: 162/314), ortanca ve % 95 GA: 72,08. (38,18, Belirlenemedi)OS oranı ve %95 GA: 12 ayda %73 (68, 78), 24 ayda: %64 (59, 69), 36 ayda: %58 (52, 63), 60 ayda: %52 (46, 57) ve 90 ayda: %48 (42,53)-A-Nivolumab (olaylar: 176/316), ortanca ve %95 GA: 36,93 ay (28,25, 58,71)OS oranı ve %95 GA: 12 ayda %74 (69, 79), 24 ayda: %59 (53, 64), 36 ayda: %52 (46, 57), 60 ayda: %44 (39, 50) ve 90 ayda: %42 (36.47)-O-- YERVOY (olaylar: 230/315), ortanca ve % 95 GA: 19,94 ay (16,85, 24,61)OS oranı ve %95 GA: 12 ayda %67 (61, 72), 24 ayda: %45 (39, 50), 36 ayda: %34 (29, 39), 60 ayda: %26 (22, 31) ve 90 ayda: %22 (18,27)Nivolumab+ YERVOY'a karşı YERVOY - HR (%95 GA): 0,53 (0,44, 0,65); Nivolumab'a karşı YERVOY - HR (%95 GA): 0.63 (0,52, 0,77);Nivolumab+ YERVOY'a karşı nivolumab - HR (%95 GA): 0,84 (0,68, 1,04)PD-L1 ekspresyonu <%5
---*----Nivolumab+YERVOY (olaylar: 109/210), ortanca ve % 95 GA: 65,94 (32,72, Belirlenemedi)-A-Nivolumab (olaylar: 121/208), ortanca ve %95 GA: 35,94 ay (23,06, 60,91)- - -o----YERVOY (olaylar: 157/202), ortanca ve %95 GA: 18,40 ay (13,70, 22,51)Nivolumab+ YERVOY'a karşı YERVOY - HR (%95 GA): 0,50 (0,39, 0,65)Nivolumab'a karşı YERVOY - HR (%95 GA): 0,62 (0,49, 0,79)Nivolumab+ YERVOY'a karşı nivolumab - HR (%95 GA): 0,81 (0,62, 1,06)
Nivolumab 8076YERVOY 7566---*----Nivolumab+YERVOY (olaylar: 33/68, ortanca ve %95 GA: Belirlenemedi (39,06, Belirlenemedi)-A-Nivolumab (olaylar: 41/80), ortanca ve %95 GA: 64,28 (36,64, Belirlenemedi)... ----YERVOY (olaylar: 50/75), ortanca ve %95 GA: 28,88 ay (18,10, 44,16)Nivolumab+ YERVOY'a karşı YERVOY - HR (%95 GA): 0,61 (0,39, 0,94)Nivolumab'a karşı YERVOY - HR (%95 GA): 0,61 (0,41, 0,93)Nivolumab+ YERVOY'a karşı nivolumab - HR (%95 GA): 0,99 (0,63, 1,57)
---*----Nivolumab+YERVOY (olaylar: 66/123), ortanca ve % 95 GA: 61,44 (26,45, Belirlenemedi)-A-Nivolumab (olaylar: 76/117), ortanca ve %95 GA: 23,46 ay (13,01, 36,53)- - -o----YERVOY (olaylar: 87/113), ortanca ve %95 GA: 18,56 ay (13,67, 23,20)Nivolumab+ YERVOY'a karşı YERVOY - HR (%95 GA): 0,55 (0,40, 0,76)Nivolumab'a karşı YERVOY - HR (%95 GA): 0,77 (0,57, 1,05)Nivolumab+ YERVOY'a karşı nivolumab - HR (%95 GA): 0,71 (0,51, 0,99)
Risk Altındaki Hasta Sayısı Nivolumab + YERVOY155 13211610510196948784797977747270652Nivolumab171 1591401221121081009390878683818078702YERVOY164 137113887667585449464139363535334---*----Nivolumab+YERVOY (olaylar: 76/155), ortanca ve % 95 GA: 82,30 (39,06, Belirlenemedi)-A-Nivolumab (olaylar: 86/171), ortanca ve %95 GA: 85,09 (39, Belirlenemedi)- - -I----YERVOY (olaylar: 121/164), ortanca ve %95 GA: 21,49 ay (16,85, 29,08)Nivolumab+ YERVOY'a karşı YERVOY - HR (%95 GA): 0,52 (0,39, 0,70)Nivolumab'a karşı YERVOY - HR (%95 GA): 0,52 (0,39, 0,69)Nivolumab+ YERVOY'a karşı nivolumab - HR (%95 GA): 1,01 (0,74, 1,37)Objektif Yanıt Oranı (ORR) analizi için minimum takip süresi 90 aydı. Yanıtlar Tablo 9'da özetlenmiştir. 9:Objektif yanıt (CA209067)
Nivolumab içeren her iki kol, tek başına YERVOY ile kıyaslandığında anlamlı PFS ve OS faydası ile daha yüksek ORR sergilemiştir. 18 aylık takip süresinde gözlemlenen PFS sonuçları ile 28 aylıktakipte ORR ve OS sonuçları başlangıç ECOG performans durumu, BRAF durumu, M evresi, yaş,beyin metastaz öyküsü ve başlangıç LDH düzeyi dahil hasta alt gruplarında tutarlı şekildegösterilmiştir. Bu gözlem minimum 90 aylık takipte OS sonuçlarında korunmuştur. 28 aylık takip süresinden sonra advers reaksiyon nedeniyle kombinasyon tedavisi kesilen 131 hasta arasında ORR %71 olup (93/131), %20'si (26/131) tam yanıtı sağlamış ve ortanca OS'yeulaşılamamıştır. Nivolumab içeren her iki kol, PD-L1 ekspresyon seviyelerine bakılmaksızın YERVOY'dan daha yüksek objektif yanıt oranları sergilemiştir. ORR'ler, 90 aylık takip sonrasında tümör PD-L1ekspresyon seviyeleri genelinde (Tablo 11) nivolumab monoterapisine göre nivolumab ve YERVOYkombinasyonu için daha yüksek olup, tam yanıtın en iyi genel yanıtı iyileşen sağkalım oranıylailişkilendirilmiştir. 90 aylık takip sonrasında, tümör PD-L1 ekspresyon seviyesi >%5 olan hastalar için ortanca yanıt sürelerine kombinasyon kolunda 78,19 ay (aralık: 18,07 - Belirlenemedi), nivolumab monoterapisikolunda 77,21 ay (aralık: 26,25 - Belirlenemedi) ve YERVOY kolunda 31,28 aydı (aralık: 6,08 -Belirlenemedi). Tümör PD-L1 ekspresyonu <%5'te, ortanca yanıt sürelerine kombinasyon kolundaulaşılmamış (aralık: 61,93 - Belirlenemedi), nivolumab monoterapisi kolunda 90,84 (aralık: 50,43 -Belirlenemedi) ve YERVOY monoterapisi kolunda 19,25 aydı (aralık: 5,32 - 47,44). Tümör yanıtı ile PFS ve OS'nin ilgili sonlanım noktalarını değerlendirirken PD-L1 ekspresyonu için net bir kesme değeri güvenli şekilde belirlenememektedir. Keşifsel çok değişkenli analizlere aitsonuçlar, sağkalım sonucuna katkıda bulunabilecek hasta ve tümör karakteristiklerini (ECOGperformans durumu, M evresi, başlangıçtaki LDH, BRAF mutasyon durumu, PD-L1 durumu vecinsiyet) tanımlamıştır. BRAF durumuna göre etkililik: 90 aylık takip süresinden sonra, nivolumab ile kombinasyon halinde YERVOY koluna randomize edilen BRAF [V600] mutasyonu pozitif ve BRAF negatif tip hastalar için ortanca PFS sırasıyla 16,76ay (%95 GA: 8,28-32) ve 11,17 ay (%95 GA: 7-19,32) iken, nivolumab monoterapisi kolundakihastalar için ortanca PFS sırasıyla 5,62 ay (%95 GA: 2,79- 9,46) ve 8,18 ay (%95 GA: 5,13-19,55)olmuştur. YERVOY monoterapisine randomize edilen BRAF [V600] mutasyonu pozitif ve BRAFnegatif tip hastalarda ortanca PFS sırasıyla 3,09 ay (%95 GA: 2,79; 5,19) ve 2,83 aydı (%95 GA:2,76; 3,06) olmuştur. 90 aylık takip süresinden sonra, nivolumab ile kombinasyon halinde YERVOY koluna randomize edilen BRAF [V600] mutasyonu pozitif ve BRAF negatif tip hastalar için ortanca ORR %67 (%95GA: 57, 75,9; n = 103) ve %54 (%95 GA: 47,1, 60,9; n = 211) iken, nivolumab monoterapisikolundaki hastalar için ortanca ORR sırasıyla %37,87 (%95 GA: 28,2, 48,1; n = 98) ve %48,2 (%95GA: 41.4, 55,0; n = 218) olmuştur. YERVOY monoterapisine randomize edilen BRAF [V600]mutasyonu pozitif ve BRAF negatif tip hastalarda ortanca ORR sırasıyla %23 (%95 CI: 15,2, 32,5; n= 100) and %17,2 (%95 GA: 12,4, 22,9; n = 215). 90 aylık takip sonrasında, BRAF[V600] mutasyonu pozitif hastalarda, kombinasyon kolunda ortanca OS'ye ulaşılmamıştı ve nivolumab monoterapisi kolunda 45,5 aydı. YERVOY tedavi kolundakiBRAF[V600] mutasyonu pozitif hastalarda ortanca OS 24,6 aydı. BRAF negatif tip hastalardaortanca OS kombinasyon kolunda 39,06 ay, nivolumab monoterapisi kolunda 34,37 ay ve YERVOYmonoterapisi kolunda 18,5 aydı. YERVOY ile kombinasyon halinde nivolumaba karşı nivolumabmonoterapisi için OS HR değerleri, BRAF[V600] mutasyonu pozitif hastalar için 0,66 (%95 GA:0,44, 0,98) ve BRAF mutasyonu negatif hastalar için 0,95 (%95 GA: 0,74, 1,22) olarak belirlenmiştir. Nivolumab ile kombinasyon halinde YERVOY ve YERVOY'un randomize faz 2 çalışması (CA209069)Çalışma CA209069, ileri evre (rezeke edilemeyen veya metastatik) melonomu olan, CA209067çalışmasının ve BRAF-negatif tip melanomu olan hastalardaki (hastaların %77'si) primer analizebenzer dahil etme kriterlerine sahip 142 hastada nivolumab ve YERVOY kombinasyonunu tek başınaYERVOY ile karşılaştıran randomize, çift kör, Faz 2 çalışmasıydı. Araştırmacı tarafındandeğerlendirilen ORR kombinasyon kolunda %61 (%95 GA: 48,9, 72,4) iken YERVOY kolunda%11'di (%95 GA: 3, 25,4). Tahmini 2 yıllık ve 3 yıllık OS oranları kombinasyon (n=73) için sırasıyla68 (%95 GA: 56, 78) ve %61 (%95 GA: 49, 71) ve YERVOY (n = 37) için sırasıyla %53 (%95 GA:36, 68) ve %44'tü (%95 GA: 28, 60).Renal Hücreli Karsinom (RHK) Nivolumab ile kombinasyon halinde YERVOY tedavisi^^^ Sunitinib ile karşılaştırıldığı randomize faz 3 çalışma (CA209214)İleri evre/metastatik RHK tedavisi için nivolumab 3 mg/kg ile kombinasyon halinde YERVOY 1 mg/kg'nin güvenliliği ve etkililiği faz 3, randomize, açık etiketli bir çalışmada (CA209214)değerlendirilmiştir. Çalışmaya, daha önce tedavi edilmemiş, berrak hücreli komponenti olan ileri evreveya metastatik renal hücreli karsinom hastaları (18 yaş ve üzeri) dahil edilmiştir. Primer etkililikpopülasyonu, Uluslararası Metastatik RHK Veri Tabanı Konsorsiyumu (IMDC) kriterlerine göre 6prognostik risk faktöründen en az 1 veya daha fazla olan orta/kötü riskli hastaları içermiştir (ilk renalhücreli karsinom teşhisi zamanından randomizasyona kadar bir yıldan az, Karnofsky performansdurumu <%80, normal alt sınırdan daha düşük hemoglobin, 10 mg/dL'den daha yüksek düzeltilmişkalsiyum, normal üst sınırdan daha yüksek trombosit sayımı ve normal üst sınırdan daha yüksekmutlak nötrofil sayımı). Hastalar bu çalışmaya tümör PD-L1 durumlarından bağımsız olarak dahiledilmiştir. Karnofsky performans durumunun <%70 olduğu ve herhangi bir geçmiş veya mevcutbeyin metastazı olan, aktif otoimmün hastalığa sahip veya sistemik immünosüpresyon gerektiren tıbbikoşulları olan hastalar çalışmaya dahil edilmemiştir. Hastalar IMDC prognostik skoru ve bölgeyegöre katmanlandırılmıştır. Çalışmaya toplam 1096 hasta randomize edilmiş olup, bunlardan 847'si orta/kötü riskli RHK'ye sahipti ve 4 doza kadar her 3 haftada bir 60 dakika boyunca intravenöz yoldan uygulanan nivolumabile kombinasyon halinde 30 dakika boyunca intravenöz yoldan uygulanan 1 mg/kg YERVOY(n=425) ve bunu takiben 2 haftada bir 3 mg/kg nivolumab monoterapisi almış veya her kürde 4 haftaboyunca oral yoldan günde 50 mg sunitinib (n=422) almış ve bunu 2 haftalık tedavisiz dönemizlemiştir. Tedaviye klinik yarar gözlendiği sürece veya hasta tedaviyi artık tolere edemeyene dekdevam edilmiştir. İlk tümör değerlendirmesi randomizasyondan 12 hafta sonra yapılmış vedeğerlendirmeler, ilk yıl için 6 haftada bir ve daha sonra progresyona veya tedavinin kesilmesinekadar, hangisi sonra meydana gelirse, her 12 haftada bir devam etmiştir. Araştırmacı tarafındandeğerlendirilen RECIST, versiyon 1.1'de tanımlı ilk progresyondan sonra tedaviye, araştırmacıtarafından belirlenen şekilde hastanın klinik yarar elde etmesi ve çalışma ilacını tolere etmesidurumunda izin verilmiştir. Primer sonlanım noktaları, orta/kötü riskli hastalarda KörlenmişBağımsız Merkezi İnceleme (BICR) ile belirlenen OS, ORR ve PFS idi. Başlangıç karakteristikleri iki grup arasında genellikle dengeli olmuştur. Ortanca yaş 61 (aralık: 21 -85) olup, %38'i > 65 yaşında ve %8'i > 75 yaşındaydı. Hastaların çoğunluğu erkek (%73) ve beyazdı (%87) ve hastaların %31 ve %69'unda başlangıç KPS değeri sırasıyla %70 ila 80 ve %90 ila 100olarak belirlenmiştir. İlk tanıdan randomizasyona kadar geçen ortanca süre hem nivolumab 3 mg/kgile kombinasyon halindeki YERVOY 1 mg/kg hem de sunitinib gruplarında 0,4 yıldı. Ortanca tedavisüresi nivolumab ve YERVOY ile tedavi edilen hastalarda 7,9 ay (aralık: 1 gün-21,4+ ay) ve sunitinibile tedavi edilen hastalarda 7,8 ay (aralık: 1 gün-20,2+ ay) olmuştur. Nivolumab ile YERVOY,hastaların %29'unda progresyondan sonra da devam etmiştir. Orta/kötü riskli hastalardan elde edilen etkililik sonuçları Tablo 11'de (minimum 17,5 aylık takip ve minimum 60 aylık takiple primer analiz) ve Şekil 7'de (minimum 60 aylık takip) gösterilmektedir. Minimum 60 aylık takiple yapılan tanımlayıcı analizden elde edilen OS sonuçları, orijinal primer analizden elde edilen sonuçlarla uyumlu idi. Şekil 8: Orta/kötü riskli hastalarda OS'ye ilişkin Kaplan-Meier eğrileri (CA209214) -Minimum 60 aylık takip
Risk Altındaki Hasta Sayısı Nivolumab + YERVOY425 3723323062702412202071961811637920Sunitinib422 3532912372061841691511371251125830-A-Nivolumab + YERVOY (olaylar: 166/425), ortanca ve %95 GA: 46,95 (35,35-57,43)-I----Sunitinib (olaylar: 282/422), ortanca ve %95 GA: 26,64 (22,08-33,54)Orta/kötü riskli hastalarda, tümör PD-L1 ekspresyonundan bağımsız olarak sunitinibe karşı nivolumab ile kombinasyon halinde YERVOY kolunda OS yararı gözlemlenmiştir. Tümör PD-L1ekspresyonu >%1 olan hastalarda ortanca OS değerine nivolumab ile kombinasyon halinde YERVOYkolunda ulaşılamazken, sunitinib kolunda bu değer 19,61 ay olmuştur (HR = 0,52; %95 GA: 0,34,0,78). Tümör PD-L1 ekspresyonu <%1 olan hastalar için, ortanca OS nivolumab ile kombinasyonhalinde YERVOY kolunda 34,7 ay ve sunitinib kolunda 32,2 ay olmuştur (HR = 0,70; %95 GA: 0,54,0,92). CA209214 çalışmasında ayrıca IMDC kriterlerine göre iyi riskli 249 hasta nivolumab artı YERVOY (n=125) veya sunitinib (n=124) kollarına randomize edilmiştir. Bu hastalar primer etkililikpopülasyonunun bir parçası olarak değerlendirilmemiştir. Sunitinibe kıyasla nivolumab artıYERVOY alan iyi riskli hastalarda OS için risk oranı 1,13 (%95 GA: 0,64, 1,99; p = 0,6710) idi. Birinci basamak RHK'de sadece berrak olmayan hücre histolojisine sahip hastalarda nivolumab ile kombinasyon halinde YERVOY'un kullanımına ilişkin veri mevcut değildir. Orta/kötü riskli hastalar için etkililik sonuçları Tablo 10'da gösterilmektedir.
Tüm hastalar minimum 24 ay takip edildiğinde güncellenmiş bir tanımlayıcı OS analizi yapılmıştır (bkz. Şekil 8). Bu analiz sırasında, kombinasyon kolunda 166/425 olay ve sunitinib kolunda 209/422olay ile risk oranı 0,66 (%99,8 GA 0,48-0,91) idi. Orta/kötü riskli hastalarda, OS oranı tümör PD-L1ekspresyonundan bağımsız şekilde sunitinib koluna kıyasla nivolumab ile kombinasyon halindeYERVOY için OS yararı gözlenmiştir. Tümör PD-L1 ekspresyonu >%1 olan hastalarda, nivolumabile kombinasyon halinde YERVOY için medyan OS'ye erişilmemiş ve sunitinib için 19,61 ayolmuştur (HR=0,52; %95 GA: 0,34-0,78). Tümör PD L1 ekpsresyonu <%1 olan hastalarda, medyan OS nivolumab ile kombinasyon halinde YERVOY için 34,7 ay iken sunitinib kolunda 32,2 ay olmuştur (HR=0,70; %95 GA: 0,54-0,92). CA209214 çalışmasında ayrıca IMDC kriterlerine göre iyi riskli 249 hasta nivolumab artı YERVOY (n = 125) veya sunitinib (n = 124) kollarına randomize edilmiştir. Bu hastalar primer etkililikpopülasyonunun bir parçası olarak değerlendirilmemiştir. 24 aylık takipte sunitinibe kıyaslanivolumab artı YERVOY alan iyi riskli hastalarda OS için risk oranı 1,13 (%95 GA: 0,64-1,99; p =0,6710) idi. 60 aylık takipte OS için HR 0,94 idi (%95 GA: 0,65-1,37). Birinci basamak RHK'de berrak hücreli olmayan histolojiye sahip hastalarda nivolumab ile kombinasyon halinde ipilimumabın kullanımına ilişkin veri mevcut değildir. 75 yaşında ve daha büyük hastalar CA209214'teki tüm orta/kötü riskli hastaların %8'ini temsil etmiştir ve nivolumab ile YERVOY kombinasyonu, minimum 17,5 aylık takiple bu alt grupta genelpopülasyona kıyasla OS sonuçları sayısal olarak daha az etki göstermiştir (HR 0,97, %95 GA: 0,48,1,95). Bu alt grubun küçük olmasından dolayı, bu verilerden kesin bir sonuç çıkarılamamaktadır. Küçük hücreli dışı akciğer kanserinin birinci basamak tedavisi4 kür platin bazlı kemoterapiye karşı ipilimumabın nivolumab ve 2 kür platin bazlı kemoterapi ile kombinasyonun araştırıldığı randomize faz 3 çalışma (CA2099LA)3 haftada bir nivolumab 360 mg ve 2 kür platin bazlı kemoterapi ile kombinasyon halinde 6 haftada bir ipilimumab 1 mg/kg'ın güvenliliği ve etkililiği, bir faz 3, randomize, açık etiketli çalışmada(CA2099LA) değerlendirilmiştir. Çalışmaya histolojik olarak teyit edilmiş skuamöz olmayan veyaskuamöz Evre IV veya rekürren KHDAK (7 inci Uluslararası Akciğer Kanseri Çalışmaları Derneğininsınıflandırmasına göre), ECOG performans durumu 0 veya 1 olan ve daha önce hiçbir kanser tedavisigörmemiş (EGFR ve ALK inhibitörleri dahil) hastalar (18 yaş ve üzeri) dahiledilmiştir. Hastalar tümör PD-L1 durumlarına bakılmaksızın çalışmaya kaydedilmiştir. EGFR mutasyonları veya ALK translokasyonları, aktif (tedavi edilmemiş) beyin metastazları, karsinomatöz menenjit, aktif otoimmün hastalık veya sistemik immünosüpresyon gerektiren tıbbikoşullara sahip hastalar çalışmaya dahil edilmemiştir. Tedavi edilen beyin metastazları olanhastalar, kayıttan en az 2 hafta önce nörolojik olarak başlangıç seviyesine dönmüşlerse vekortikosteroidleri kesmişlerse veya günde <10 mg prednizon eşdeğeri olan stabil veya azalan bir dozalıyorsa çalışmaya alınmıştır. Randomizasyon histolojiye (skuamöze karşı skuamöz olmayan), tümörPD-L1 ekspresyon düzeyine (>%1'e karşı <%1) ve cinsiyete (erkek ve kadın) görebasamaklandırılmıştır. Toplam 719 hasta, nivolumab ve platin bazlı kemoterapi ile kombinasyon halinde ipilimumab (n= 361) veya platin bazlı kemoterapi (n= 358) alacak şekilde randomizeedilmiştir. Nivolumab ve platin bazlı kemoterapi ile kombinasyon halinde ipilimumab kolundakihastalar, her 3 haftada bir 30 dakika boyunca intravenöz yoldan uygulanan 360 mg nivolumab ve 2kür için her 3 haftada bir uygulanan platin bazlı kemoterapi ile kombinasyon halinde 6 haftada bir 30dakika boyunca intravenöz yoldan uygulanan 1 mg/kg ipilimumab almıştır. Kemoterapi kolundakihastalara 4 kür boyunca her 3 haftada bir platin bazlı kemoterapi uygulanmıştır; skuamöz olmayanhastaların isteğe bağlı pemetrekset idame tedavisi almasına izin verilmiştir. Platin bazlı kemoterapi skuamöz olmayan KHDAK için karboplatin (EAA 5 ya da 6) ve pemetrekset 500 mg/m2 ya da sisplatin 75 mg/m2 ve pemetrekset 500 mg/mm2 veya skuamöz KHDAK içinkarboplatin (EAA 6) ve paklitaksel 200 mg/m2 içermiştir. Tedavi, hastalık progresyonuna, kabul edilemez toksisiteye veya 24 aya kadar devam etmiştir. Hasta klinik olarak stabilse ve araştırmacı tarafından klinik fayda sağladığı kabul edilirse, hastalığınilerlemesinden sonra devam eden tedaviye izin verilmiştir. İpilimumab'a atfedilen bir advers olaynedeniyle kombinasyon tedavisini bırakan hastaların nivolumab monoterapisine devam etmelerineizin verilmiştir. Tümör değerlendirmeleri, çalışma tedavisinin ilk dozundan sonra ilk 12 ayboyunca 6 haftada bir, daha sonra hastalık progresyonuna veya çalışma tedavisi kesilene kadar her12 haftada bir yapılmıştır. CA2099LA başlangıç özellikleri genel olarak tüm tedavi gruplarında dengelenmişti. Medyan yaş 65 (aralık: 26-86) olup, %51'i > 65 yaşında ve %10'u > 75 yaşındaydı. Hastaların çoğunluğu beyaz(%89) ve erkekti (%70). Başlangıç ECOG performans durumu 0 (%31) veya 1 (%68) iken hastaların%57'sinde PD-L1> %1 ve %37'sinde PD-L1 < %1 idi, % 31'inde skuamöz ve %69'unda skuamözolmayan histoloji vardı, %17'sinde beyin metastazı vardı ve %86'sı daha önce/halen sigaraiçiyordu. Hiçbir hasta daha önce immünoterapi almamıştır. CA2099LA çalışmasının primer etkililik sonuç ölçümü OS idi. İlave etkililik sonlanım noktaları, BICR ile belirlenen ORR, PFS ve yanıt süresi idi. Çalışma, 351 olay gözlemlendiğinde önceden belirlenmiş ara analizde tek başına platin bazlı kemoterapiye kıyasla nivolumab ve platin bazlı kemoterapi ile kombinasyon halinde ipilimumabkoluna randomize edilen hastalarda OS, PFS ve ORR'de istatistiksel olarak anlamlı bir yararolduğunu göstermiştir (son analiz için planlanan olay sayısının %87'si). OS için minimum takipsüresi 8,1 aydı. Etkililik sonuçları Şekil 9'da (minimum 12,7 aylık takip ile güncellenmiş OS analizi) ve Tablo 12'de (minimum 8.1 aylık takip ile birincil analiz) gösterilmektedir. Tüm hastalar en az 12,5 ay takipedildikten sonra güncellenmiş bir etkililik analizi yapılmıştır (Bkz. Şekil 9). Bu analiz sırasında, OSiçin risk oranı 0,66 (%95 GA: 0,55-0,80) ve PFS için risk oranı 0,68 (%95 GA: 0,57-0,82) idi.
Genel Sağkalım (Ay) Risk Altındaki Hasta SayısıNivolumab + ipilimumab + kemoterapi 36132629225022715386331010Kemoterapi358 31926011260671161662080-A-Nivolumab + ipilimumab + kemoterapi (olaylar: 190/361), medyan ve %95 GA: 15,64 (13,93-19,98)------Kemoterapi (olaylar: 242/358), medyan ve %95 GA: 10,91 (9,46 - 12,55)
Kombinasyon ve kemoterapi kollarındaki hastaların sırasıyla %28,8'i ve %41,1'i sistemik tedavi almıştır. Kombinasyon ve kemoterapi kollarındaki hastaların sırasıyla %3,9 ve %27,9'u daha sonraimmünoterapi (anti-PD-1, anti-PD-L1 ve anti-CTLA4 dahil) almıştır. CA2099LA çalışmasında, kemoterapiye göre bir tanımlayıcı alt grup analizinde, nivolumab ve kemoterapi ile kombinasyon halinde ipilimumab ile tedavi edilen skuamöz histolojiyesahip hastalarda (HR [%95 GA] 0,65 [0,46-0,93], n = 227) ve skuamöz olmayan histolojiye sahiphastalarda (HR [%95 Ga] 0,72 [0,55-0,93], n = 492) OS yararı gösterilmiştir. Tablo 12'de, önceden tanımlanmış alt grup analizlerinde tümör PD-L1 ekspresyonuna göre OS, PFS ve ORR etkililik sonuçları özetlenmektedir.
CA2099LA çalışmasına > 75 yaşında toplam 70 KHDAK hastası dahil edilmiştir (nivolumab ve kemoterapi ile kombinasyon halinde ipilimumab kolundaki 37 hasta ve kemoterapi kolundaki33 hasta). Bu çalışma alt grubunda kemoterapiye kıyasla nivolumab ve kemoterapi ile kombinasyonhalinde ipilimumab için OS'de 1,36 HR (%95 GA: 0,74-2,52) ve PFS'de 1,12 HR (%95 GA: 0,641,96) gözlenmiştir. ORR, nivolumab ve kemoterapi ile kombinasyon halinde ipilimumab kolunda% 27 ve kemoterapi kolunda %15,2 idi. Yetmiş beş yaş ve üzeri hastaların %43'ü, nivolumab vekemoterapi ile kombinasyon halinde ipilimumab tedavisini bırakmıştır . Bu hasta popülasyonundanivolumab ve kemoterapi ile kombinasyon halinde ipilimumabın etkililik ve güvenlilikverileri sınırlıdır. Bir alt grup analizinde, daha önce hiç sigara içmemiş olan hastalarda kemoterapiye kıyasla nivolumab ve kemoterapi ile kombinasyon halinde ipilimumab alan hastalarda azalan sağkalım yararıgözlenmiştir. Ancak düşük hasta sayısından dolayı bu verilerden kesin bir sonuç çıkarılamaz. Malign plevral mezotelyomaKemoterapiye karşı n^^olumab ile kombinasyon halinde ipilimumabın araştırıldığı randomize faz 3 çalışla (CA209743)Her 2 haftada bir 3 mg/kg nivolumab ile kombinasyon halinde 6 haftada bir 1 mg/kg ipilimumabın güvenliliği ve etkililiği bir faz 3, randomize, açık etiketli çalışmada değerlendirilmiştir(CA209743). Çalışma, histolojik olarak teyit edilmiş ve daha önce tedavi edilmemiş epiteloid veyaepiteloid olmayan histolojiye sahip malign plevral mezotelyoma bulunan, ECOG performansdurumu 0 veya 1 olan ve ilk çalışma tedavisinden önceki 14 gün içinde palyatifradyoterapi uygulanmamış hastaları (18 yaş veya üzeri) içermiştir. Hastalar, tümör pD-L1durumlarına bakılmaksızın çalışmaya kaydedilmiştir. Primitif peritoneal, perikardiyal, testis veya tunika vajinalis mezotelyoması, interstisyel akciğer hastalığı, aktif otoimmün hastalığı, sistemik immünosüpresyon gerektiren tıbbi koşullar ve beyinmetastazı olan hastalar (cerrahi olarak rezeke edilmedikçe veya stereotaksik radyoterapi ile tedaviedilmedikçe ve çalışmaya dahil edilmeden önceki 3 ay içinde herhangi bir gelişme olmadıkça) çalışmaya dahil edilmemiştir. Randomizasyon, histolojiye (epitelioide karşı sarkomatoid veya karışık histoloji alt tipleri) ve cinsiyete (erkek ve kadın) göre basamaklandırılmıştır. Toplam 605 hasta, nivolumab ile kombinasyon halinde ipilimumab (n = 303) veya kemoterapi (n = 302) almak üzere randomize edilmiştir. Nivolumab ile kombinasyon halinde ipilimumabkolundaki hastalar, 2 yıla kadar 2 haftada bir 30 dakika boyunca intravenöz yoldan uygulanan 3mg/kgnivolumab ile kombinasyon halinde 6 haftada bir 30 dakika boyunca intravenöz yoldan uygulanan 1mg/kg ipilimumab almıştır. Kemoterapi kolundaki hastalar 6 küre kadar kemoterapi almıştır (her kür21 gündü). Kemoterapi sisplatin 75 mg/m2 ve pemetrekset 500 mg/m2 veya karboplatin 5 EAA vepemetrekset 500 mg/m2 terapilerini içermiştir. Tedavi, hastalık progresyonuna, kabul edilemez toksisiteye veya 24 aya kadar devam etmiştir. Hasta klinik olarak stabilse ve araştırmacı tarafından klinik fayda sağladığı kabul edilirse, hastalığınilerlemesinden sonra tedaviye izin verilmiştir. İpilimumaba atfedilen bir advers reaksiyon nedeniylekombinasyon tedavisini bırakan hastaların nivolumab monoterapisine devam etmesine izinverilmiştir. Tümör değerlendirmeleri, çalışma tedavisinin ilk dozundan sonra ilk 12 ayboyunca 6 haftada bir, daha sonra hastalık progresyonuna veya çalışma tedavisi kesilene kadar her12 haftada bir yapılmıştır. CA209743 başlangıç özellikleri genel olarak tüm tedavi gruplarında dengeliydi. Medyan yaş 69 (aralık: 25-89) olup, hastaların %72'si>65ve %26'sı>75 yaşındaydı. Hastaların çoğunluğubeyaz (%85) ve erkekti (%77). Başlangıç ECOG performans durumu 0 (%40) veya 1 (%60),hastaların %80'inde PD-Ll > %1 ve hastaların %20'sinde PD-Ll < %1 idi, % 75'inde epiteloid ve%25'inde epiteloid olmayan histoloji mevcuttu. CA209743 primer etkililik sonuç ölçümü OS idi. Kilit ikincil etkililik sonlanım noktaları, plevral mezotelyoma için modifıye RECIST kriterleri kullanılarak BICR ile belirlenen PFS, ORR ve yanıtsüresiydi. Bu ikincil sonlanım noktaları için tanımlayıcı analizler Tablo 14'de sunulmuştur. Çalışma, 419 olay gözlemlendiğinde (nihai analiz için planlanan olay sayısının %89'u) önceden belirlenmiş ara analizde kemoterapiye kıyasla nivolumab ile kombinasyon halinde ipilimumabkoluna randomize edilen hastalarda OS'de istatistiksel olarak anlamlı bir iyileşme göstermiştir. OSiçin minimum takip süresi 22 aydı. Şekil 10: OS'ye ilişkin Kaplan-Meier eğrileri (CA209743)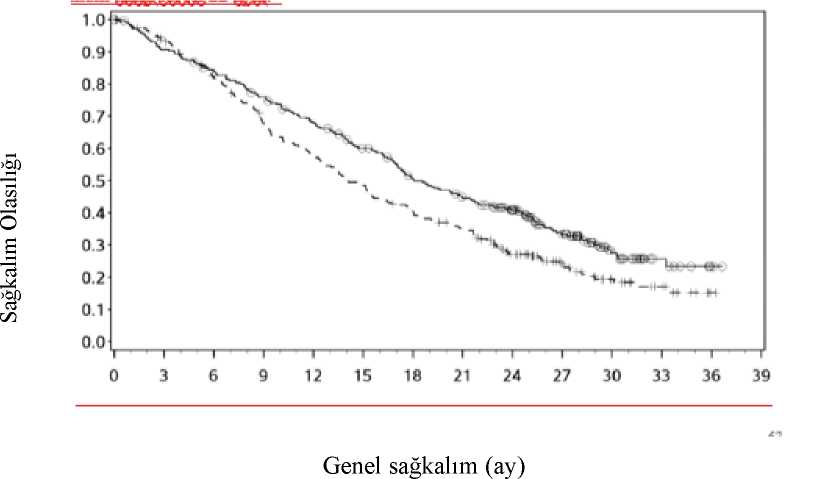
- -0-- Nivolumab + ipilimumab (olaylar: 200/303), medyan ve %95 GA: 18,07 (16,82-21,45) +-- Kemoterapi (olaylar: 219/302), medyan ve %95 GA: 14,09 (12,45-16,23)
Kombinasyon ve kemoterapi kollarındaki hastaların sırasıyla %44,2 ve %40,7'si daha sonra sistemik tedavi almıştır. Kombinasyon ve kemoterapi kollarındaki hastaların sırasıyla %3,3 ve %20,2'si dahasonra immünoterapi (anti-PD-1, anti-PD-L1 ve anti - CTLA - 4 dahil) almıştır. Tablo 14'de, önceden belirlenmiş alt grup analizlerinde histolojiye göre OS, PFS ve ORR etkililik sonuçları özetlenmektedir.
Tablo 15'de, önceden belirlenmiş alt grup analizlerinde başlangıç tümör PD-L1 ekspresyonuna göre OS, PFS ve ORR etkililik sonuçları özetlenmektedir.
CA209743 çalışmasına 75 yaş ve üzeri toplam 157 MPM hastası kaydedilmiştir (nivolumab ile kombinasyon halinde ipilimumab kolunda 78 ve kemoterapi kolunda 79). Bu çalışma alt grubundakemoterapiye kıyasla nivolumab ile kombinasyon halinde ipilimumab kolunda OS'de 1,02'lik riskoranı (% 95 GA: 0,70-1,48) gözlenmiştir. Nivolumab ile kombinasyon halinde ipilimumab alan tümhastalara kıyasla 75 yaş ve üstü hastalarda daha yüksek ciddi advers reaksiyon ve adversreaksiyonlara bağlı olarak tedaviyi bırakma oranı görülmüştür (bkz. bölüm 4.8). Ancak, bu alt grupanalizinin keşifsel doğası nedeniyle, kesin sonuçlara varılamaz. 5.2 Farmakokinetik özellikleriGenel özelliklerEmilim:YERVOY terapötik bir protein olup, sadece intravenöz bir infüzyon olarak melanomun tedavisi için uygulanır. Dolayısıyla, YERVOY için emilim ve biyoyararlanım değerlendirmesi geçerli değildir. Dağılım:Popülasyon farmakokinetik analizine dayanarak, YERVOY için aşağıdaki ortalama (yüzde varyasyon katsayısı) parametreler elde edilmiştir: kararlı durumdaki dağılım hacmi 7,47 L (%10,1)olmuştur. 3 mg/kg indüksiyon rejimi ile kararlı durumda elde edilen ortalama (yüzde varyasyonkatsayısı) YERVOY Cmin 19,4 mikrogram/mL (%74,6) olmuştur. Biyotransformasyon:YERVOY'un insanlarda metabolizmasını ve metabolik yolaklarını değerlendirmek üzere klinik farmakoloji çalışmaları yapılmamıştır. Terapötik proteinlerin çoğu gibi, ipilimumab, karaciğersitokromu P-450 (CYP) veya diğer metabolize edici enzimlerle metabolize olmaz ve inhibisyon veindüksiyon bakımından CYP'ler veya diğer metabolize edici enzimler üzerinde herhangi bir etkiyesahip olma olasılığı yoktur. Dolayısıyla, YERVOY'un anlamlı metabolizma bazlı ilaç-ilaçetkileşimleri olması olasılığı yoktur. YERVOY gibi monoklonal antikorlar, CYP'lerin veya taşıyıcıların aşağı regülasyonu ile CYP450 substratları olan ilaçların sistemik konsantrasyonlarındaki değişimler ve sitokinlerin salınımı yoluylaküçük moleküllerin farmakokinetiği ile etkileşime girebilir. CYP izozimleri (özellikle CYP2C8,CYP3A4, CYP1A2 ve CYP2E1) substratları (paklitaksel [175 mg/m2] ve DTIC [850 mg/m2]) ilepotansiyel etkileşimi değerlendiren bir klinik çalışma (CA184078) yapılmıştır (bkz. Bölüm 4.5). Eliminasyon:Popülasyon farmakokinetik analizine dayanarak, YERVOY için aşağıdaki ortalama (yüzde varyasyon katsayısı) parametreler elde edilmiştir: sistemik CL 16,8mL/sa (%38,1) ve terminalyarılanma ömrü 15,4 gün (%34,4) olmuştur ve bunlar, insan monoklonal antikorlarının eliminasyonuile uyumludur. YERVOY CL'si, başlangıçta vücut ağırlığındaki artış ve laktat dehidrojenaz (LDH) arttıkça yükselmiştir; ancak, mg/kg bazında uygulama sonrasında, yükselmiş LDH veya vücut ağırlığı içindoz ayarlaması gerekmez. CL yaş (aralık: 23-88 yaş), cinsiyet, eşzamanlı budesonid veya dakarbazinkullanımı, performans durumu, HLA-A2*0201 durumu, hafif karaciğer yetmezliği, böbrekyetmezliği, immünojenisite ve önceki anti-kanser tedavilerinden etkilenmemiştir. Doğrusallık/ Doğrusal olmayan durum:YERVOY'un farmakokinetiği 0,3 ilâ 10 mg/kg arasında değişen indüksiyon dozlarını alan 3 haftada bir 4 doz uygulanmış 785 ileri evre melanom hastasında araştırılmıştır. YERVOY'un Cmaks, Cmin veEAA incelenen doz aralığında doz ile orantılı bulunmuştur. Her 3 haftada bir tekrarlanan YERVOYdozlarında, klirens (CL) zamana göre değişmemiş olarak bulunmuş ve akümülasyon indeksi 1,5 katveya daha düşük olmak üzere belirgin olarak minimal bir sistemik akümülasyon gözlenmiştir. Üçüncüdoz ile YERVOY kararlı duruma ulaşmıştır. Hastalardaki karakteristik özelliklerİleri evre melanomlu 497 hastada yapılan maruziyet-yanıt analizine göre, OS önceki sistemik anti kanser tedavilerinden bağımsızdı ve daha yüksek YERVOY Cminss plazma konsantrasyonları ilebirlikte artmıştır. Irk: Beyaz ırka ait olmayan etnik gruplarda yeterli veri bulunmadığından ırkın etkisi incelenmemiştir. Böbrek yetmezliği:YERVOY'un böbrek yetmezliği olan hastalardaki farmakokinetiğinin değerlendirilmesi için hiçbir kontrollü çalışma yapılmamıştır. Metastatik melanomlu hastalarla yapılan klinik çalışmalardan elde edilen verilerin popülasyon farmakokinetik analizinde, önceden mevcut hafif ve orta şiddetli böbrek yetmezliği, YERVOYCL'sini etkilememiştir. Önceden mevcut ciddi böbrek yetmezliği ile klinik ve farmakokinetik verilersınırlıdır; doz ayarlamasının gerekli olup olmadığı belirlenememektedir. Metastatik melanomlu hastalarla yapılan klinik çalışmalardan elde edilen verilerin popülasyon farmakokinetik analizinde, önceden mevcut hafif karaciğer yetmezliği, YERVOY CL'sinietkilememiştir. Önceden mevcut hafif karaciğer yetmezliği ile klinik ve farmakokinetik verilersınırlıdır; doz ayarlamasının gerekli olup olmadığı belirlenememektedir. Klinik çalışmalarda öncedenmevcut ciddi karaciğer yetmezliği olan hastalar tanımlanmamıştır. Pediyatrik popülasyon:Faz 4, 2 yetişkin çalışmasından (N=521) ve 2 pediyatrik çalışmadan (N=44) 565 hastadan elde edilen mevcut birleştirilmiş verileri kullanan bir popülasyon FK analizine göre, artan başlangıç vücut ağırlığıile YERVOY'un CL'si artmıştır. Yaş (2-87 yaş) YERVOY'un CL'si üzerinde klinik olarak önemlibir etkiye sahip değildi. Tahmini geometrik ortalama CL, 12 yaşında ve daha büyük ila 18 yaşındanküçük yaş arası adolesan hastalarda 8,72 mL/sa'dır. Adolesanlardaki maruziyet, aynı mg/kg dozunualan yetişkinlerdeki maruziyetlerle karşılaştırılabilirdir. Yetişkinlerde ve pediyatrik popülasyondakisimülasyona göre, yetişkinlerde ve pediyatrik popülasyonda her 3 haftada bir önerilen 3 mg/kgdozunda karşılaştırılabilir maruziyet elde edilmiştir. Farmakokinetik/farmakodinamik ilişkilerNivolumab ile kombinasyon halinde YERVOY:.YERVOY 1 mg/kg, nivolumab 3 mg/kg ile kombinasyon halinde uygulandığında, YERVOY CL'si %1,5 azalmış ve nivolumab CL'si %1 artmışolup, klinik açıdan ilgili kabul edilmemiştir. YERVOY 3 mg/kg, nivolumab 1 mg/kg ile kombinasyonhalinde uygulandığında, YERVOY CL'si %9 artmış ve nivolumab CL'si %29 artmış olup, klinikaçıdan ilgili kabul edilmemiştir.Nivolumab ile kombinasyon halinde uygulandığında, YERVOY CL'si anti-YERVOY antikorlarının varlığında %5,7 artmış ve nivolumab CL'si anti-nivolumab antikorlarının varlığında %20 artmıştır.Bu değişiklikler klinik olarak ilgili kabul edilmemiştir. Nivolumab ve kemoterapi ile kombinasyon halinde YERVOY.6 haftada bir YERVOY 1 mg/kg 3 haftada bir nivolumab 360 mg ve 2 kür kemoterapi ile kombinasyon halinde uygulandığında, ipilimumab CL değeri yaklaşık %22 artmış ve nivolumab CLdeğeri yaklaşık %10 düşmüş ve bu düşüş klinik olarak anlamlı kabul edilmemiştir. 5.3 Klinik öncesi güvenlilik verileriMaymunlarda yapılan intravenöz dozların tekrarlandığı toksikoloji çalışmalarında YERVOY genelde iyi tolere edilmiştir. İmmünite ile ilişkili advers reaksiyonlar nadiren (~3%) gözlemlenmiş ve kolit(tek bir ölüm vakası ile sonuçlanmıştır), dermatit ve infüzyon reaksiyonunu (muhtemelen yüksekenjeksiyon hızından kaynaklanan akut sitokin salımı nedeniyle) içermiştir. Bir çalışmada eşlik edenhistopatolojik bulgular olmaksızın tiroid ve testislerin ağırlığında düşüş olduğu görülmüştür ve bubulgunun klinik ilgisi bilinmemektedir. YERVOY'un prenatal ve postnatal gelişimdeki etkileri sinomolgus maymunlarında yapılan bir çalışmada araştırılmıştır. Hamile maymunlar, doğuma kadar ilk trimesterde organogenezinbaşlangıcından itibaren 3 haftada bir, klinik 3 mg/kg YERVOY dozu ile ilişkili olanlara benzer veyaonlardan yüksek maruziyet (EAA) düzeylerinde YERVOY almışlardır. Hamileliğin ilk iki trimesterısırasında üreme üzerinde tedavi ilişkili hiçbir yan etki tespit edilmemiştir. Üçüncü trimesterdanbaşlayarak, her iki YERVOY grubundaki kürtaj, ölü doğum, prematüre doğum (ve bununla ilişkiliolarak düşük doğum ağırlığı) ve bebek mortalitesi insidansı kontrol hayvanlarına göre daha yüksek olmuştur; bu bulguların doza bağlı olduğu tespit edilmiştir. Ayrıca, ana rahminde YERVOY'a maruz kalan 2 bebeğin ürogenital sisteminde harici ve viseral gelişimsel anomaliler tespit edilmiştir. Bir dişibebekte sol böbrekte ve üreterde tek taraflı böbrek agenezisi ve bir erkek bebekte imperforat üretrave bununla ilişkili üriner obstrüksiyon ve subkütan skrotal ödem görülmüştür. Bu malformasyonlarıntedavi ile ilişkisi açık değildir. YERVOY'un mutajenik ve karsinojenik potansiyelini değerlendirecek çalışma yapılmamıştır. Fertilite çalışmaları yapılmamıştır. 6. FARMASÖTİK ÖZELLİKLER6.1 Yardımcı maddelerin listesiTris hidroklorür (2-amino-2-hidroksimetil-1,3-propanediol hidroklorür) Sodyum klorür Mannitol (E421) Pentetik asit (dietilenetriaminepentaasetik asit) Polisorbat 80 Sodyum hidroksit (pH ayarı için) Hidroklorik asit (pH ayarı için) Enjeksiyonluk su 6.2 GeçimsizliklerGeçimlilik çalışmaları bulunmadığından bu tıbbi ürün diğer tıbbi ürünler ile karıştırılmamalıdır. 6.3 Raf ömrüAçılmamış flakon: 36 ay Açıldıktan sonra: İnfüzyon solüsyonu: mikrobiyolojik bakış açısından, bir kere açıldıktan sonra, tıbbi ürünün infüzyonu ya da dilüsyonu ve infüzyonu hemen yapılmalıdır. İnfüzyon solüsyonu (dilüe edilmiş ya daedilmemiş) açıldıktan sonra hemen kullanılmazsa 2°-8°C'de buzdolabında ya da 25'nin altındaki odasıcaklığında 24 saate kadar saklanabilir. 6.4 Saklamaya yönelik özel tedbirler2 -8°C arasında (buzdolabında) saklayınız. Dondurmayınız. Işıktan korumak için orijinal ambalajında saklayınız. Tıbbi ürünün ilk açılışından veya dilüe edilmesinden sonraki saklama şartları için bkz. Bölüm 6.3. 6.5 Ambalaj niteliği ve içeriğiTıpalı (butil lastik kaplanmış) ve flip off' mühürlü (alüminyum) bir flakonda (Tip I cam) 40 mL konsantre. 1'lik ambalaj. 6.6 Beşeri tıbbi üründen arta kalan maddelerin imhası ve diğer özel önlemlerHazırlama aşaması, özellikle asepsi ile ilgili olarak iyi uygulamalara ilişkin kurallara uygun olarak eğitimli personel tarafından gerçekleştirilmelidir. Dozun hesaplanması: YERVOY monoterapisi veya nivolumab ile kombinasyon halinde YERVOY: Hasta için reçete edilen doz mg/kg cinsinden verilir. Reçete edilen bu doza dayanılarak uygulanacak toplam doz hesaplanır. Hastaya tam doz uygulanabilmesi için birden fazla YERVOY konsantresiflakonu gerekli olabilir. ¦ Her bir 10 mL'lik YERVOY konsantresi flakonu 50 mg ipilimumab, her bir 40 mL'likflakon ise 200 mg ipilimumab içermektedir. ¦ mg olarak toplam ipilimumab dozu = kg olarak hastanın ağırlığı x mg/kg olarak reçeteedilen doz. ¦ Dozun hazırlanması için YERVOY konsantresinin hacmi (mL) = 5'e bölünmüş olarak,toplam doz (mg) (YERVOY konsantresinin dozu 5 mg/mL'dir). İnfüzyonun hazırlanması: İnfüzyon hazırlanırken aseptik koşullar sağlanmalıdır. YERVOY, aşağıda belirtildiği şekliyle intravenöz uygulama için kullanılabilir: ¦ Seyreltme yapılmaksızın uygun bir steril enjektör kullanılarak bir infüzyon kabınaaktarıldıktan sonra; veya ¦ Orijinal konsantre hacminin 5 katına kadar seyreltme yapıldıktan sonra (1 hacimkonsantreye 4 hacim seyreltici). Nihai konsantrasyon 1 ila 4 mg/mL arasında olmalıdır.YERVOY konsantresinin seyreltilmesi için aşağıdakiler kullanılabilir: ¦ 9 mg/mL (%0,9) enjeksiyonluk sodyum klorür çözeltisi veya, ¦ 50 mg/mL (%5) enjeksiyonluk glukoz çözeltisi AŞAMA 1: ¦ Uygun sayıda YERVOY flakonu yaklaşık 5 dakika kadar oda sıcaklığında bekletilir. ¦ YERVOY konsantresi partikül veya renk bozukluğu bakımından incelenir. YERVOYkonsantresi, hafif (az miktarda) partikül içerebilen, berrak ila hafif opak renksiz ila açık sarıbir sıvıdır. Alışılmadık miktarda partikül veya renk bozukluğu belirtisi varsa konsantrekullanılmamalıdır. ¦ Uygun steril bir enjektör kullanılarak gerekli hacimde YERVOY konsantresi alınır. AŞAMA 2: ¦ Konsantre, steril, havası alınmış cam bir şişeye ya da intravenöz torbaya (PVC veya PVColmayan) aktarılır. ¦ Uygun durumda, gerekli hacimde 9 mg/mL (%0,9) enjeksiyonluk sodyum klorür çözeltisiveya 50 mg/mL (%5) enjeksiyonluk glukoz çözeltisi ile seyreltilir. Hazırlama kolaylığı için,konsantre ayrıca uygun hacimde sodyum klorür 9 mg/mL (%0,9) enjeksiyonluk çözelti veya50 mg/mL (%5) enjeksiyonluk glukoz çözeltisi içeren kullanıma hazır torbaya doğrudanaktarılabilir. Elinizde döndürülerek infüzyon hafifçe karıştırılır. Uygulama: YERVOY infüzyonu, 30 dakikalık bir periyotta intravenöz yoldan uygulanır. YERVOY infüzyonu, diğer ajanlarla aynı intravenöz hatta aynı zamanda infüze edilmemelidir İnfüzyon için ayrı bir infüzyon hattı kullanılır. Bir infüzyon seti ve in-line, steril, pirojenik olmayan, proteinlere bağlanma oranı düşük bir filtre kullanılır (por boyutu 0,2 mikrometre ila 1,2 mikrometre). YERVOY infüzyonu aşağıdakiler ile geçimlidir: PVC infüzyon setleri Polietersülfon (0,2 mikrometre ila 1,2 mikrometre) ve naylon (0,2 mikrometre) in-linefiltreler İnfüzyon sonunda 9 mg/mL (%0,9) enjeksiyonluk sodyum klorür çözeltisi veya 50 mg/mL (%5) enjeksiyonluk glukoz çözeltisi ile hat yıkanır. Kullanılmamış olan ürünler ya da atık materyaller Tıbbi Atıkların Kontrolü Yönetmeliği ve Ambalaj Atıklarının Kontrolü Yönetmeliklerine uygun olarak imha edilmelidir. 7. RUHSAT SAHİBİ Bristol-Myers Squibb İlaçları Inc. İstanbul Şubesi Sarıyer - İstanbul Tel: (0212) 335 89 00 Faks: (0212) 286 2496 e-mail: [email protected] 8. RUHSAT NUMARASI(LARI) 2014/481 9. İLK RUHSAT TARİHİ/RUHSAT YENİLEME TARİHİ İlk Ruhsat Tarihi: 05.06.2014 Ruhsat Yenileme Tarihi: 21.06.2019 10. KÜB'ÜN YENİLENME TARİHİ |
İlaç BilgileriYervoy 200mg/40ml Iv İnfüzyonluk Çözelti Konsantresi İçeren FlakonEtken Maddesi: İpilimumab Kullanma talimatı ve kısa ürün bilgileri
Google Reklamları
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
Ana Sayfa | Hakkımızda | İlaçlar | İlaç Ara | İlaç Firmaları | Gizlilik | Bize Ulaşın
Telif Hakkı 2008-2026 © İlaç Prospektüsü. Tüm Hakları Saklıdır.Uyarı: Sitemizde yayınladığımız ilaç bilgileri ile doktora danışmadan kesinlikle ilaç kullanmayınız!
Aksi halde doğabilecek sağlık sorunlarından ilacprospektusu.com sorumlu tutulamaz.