Rudista 85 Mg/500 Mg Film Kaplı Tablet Kısa Ürün BilgisiKISA URUN BILGISI1. BEŞERI TIBBI URUNUN ADIRUDİSTA 85 mg/500 mg film kaplı tablet 2. KALITATIF VE KANTİTATIF BILEŞIMEtkin maddeler:Her bir film kaplı tablet etkin madde olarak 85 mg sumatriptan'a eşdeğer 119 mg sumatriptan süksinat ve 500 mg naproksen sodyum içerir.Yardımcı maddeler:Her bir film kaplı tablet; Sodyum hidrojen karbonat..............42 mg Kroskarmelloz sodyum..............151,4 mg Sodyum klorür..........................100 mg Yardımcı maddeler için 6.1'e bakınız. 3. FARMASÖTIK FORMFilm kaplı tablet. Mavi renkli, oblong, bikonveks film kaplı tablettir. 4. KLİNIK ÖZELLIKLER4.1. Terapötik endikasyonlarRUDİSTA, yetişkinlerde ve 12 yaş ve üzeri pediyatrik hastalarda auralı veya aurasız akut migren tedavisi için endikedir. Kullanım Sınırlamaları: Yalnızca açık olarak migren tanısı konulmuşsa kullanılmalıdır. Bir hasta RUDİSTA iletedavi edilen ilk migren atağına yanıt vermiyorsa, sonraki atakları tedavi etmek içinRUDİSTA uygulanmadan önce migren tanısını yeniden değerlendirin. RUDİSTA, migren atak profilaksisi için endike değildir. RUDİSTA'nın küme tipi baş ağrısı için güvenliliği ve etkililiği belirlenmemiştir. 4.2. Pozoloji ve uygulama şekliPozoloji/uygulama sıklığı ve süresi:Yetişkinlerde dozaj:Yetişkinler için önerilen doz 1 tablet RUDİSTA 85 mg/500 mg'dır. RUDİSTA 85 mg/500 mg, en düşük etkili dozdan daha yüksek bir sumatriptan dozu içerir. Sumatriptan dozunun seçimive RUDİSTA 85 mg/500 fflgıgibiv^sabifctfeifkkomıbiflâsyanuP kullanılması, daha yüksek bir  esumatriptan dozunun olası faydasını tartarak, daha büyük advers reaksiyon risk potansiyeli ile bireysel olarak yapılmalıdır. 24 saatlik bir süre içinde önerilen maksimum doz, en az 2 saat arayla alınan 2 tablettir. Yetişkinlerde 30 günlük bir dönemde ortalama 5'ten fazla migren baş ağrısının tedavi edilmesinin güvenliliği belirlenmemiştir. Bireysel hasta tedavi hedefleriyle tutarlı en kısa süre için en düşük etkili doz kullanılmalıdır. 12 ila 17 yaş arası pediyatrik hastalarda dozaj24 saatlik sürede önerilen maksimum doz 1 tablet RUDİSTA 85 mg/500 mg'dır.Pediyatrik hastalarda 30 günlük bir dönemde ortalama 2'den fazla migren baş ağrısının tedavi edilmesinin güvenliliği belirlenmemiştir. Bireysel hasta tedavi hedefleriyle tutarlı en kısa süre için en düşük etkili doz kullanılmalıdır. Uygulama şekli:Ağızdan alınır. RUDİSTA aç karnına veya yiyeceklerle birlikte alınabilir. Tabletler su veya diğer sıvılarla bütün olarak alınmalıdır. Tabletler bölünmemeli, ezilmemeli veya çiğnenmemelidir. Özel popülasyonlara ilişkin ek bilgiler:Böbrek yetmezliği:RUDİSTA'nın kreatinin klirensi 30 mL/dak'dan az olan hastalarda kullanılması tavsiye edilmez. Hafif (CrCl=60 ila 89 mL/dak) veya orta (CrCl=30 ila 59 mL/dak) dereceli böbrekyetmezliği, önceden mevcut böbrek hastalığı veya dehidratasyonu olan hastalarda serumkreatinin ya da kreatinin klirensi izlenmelidir. Karaciğer yetmezliği:RUDİSTA şiddetli karaciğer yetmezliği olan hastalarda kontrendikedir. Hafif veya orta dereceli karaciğer yetmezliği olan hastalar için RUDİSTA dozu azaltılmalıdır. Hafif ila orta şiddette karaciğer yetmezliği olan hastalarda 85mg/500mg RUDİSTA kullanımı önerilmemektedir. Pediyatrik popülasyon:12 yaşın altındaki pediyatrik hastalarda RUDİSTA'nın güvenliliği ve etkililiği belirlenmemiştir. RUDİSTA'nın 12 ila 17 yaşındaki pediyatrik hastalarda akut migren tedavisi için güvenliliği ve etkililiği, çift kör, plasebo kontrollü bir çalışmada belirlenmiştir. Geriyatrik popülasyon:Genç hastalara kıyasla yaşlı hastalar NSAİİ ile ilişkili ciddi kardiyovasküler, gastrointestinal ve/veya renal advers reaksiyonlar açısından daha fazla risk altındadır. RUDİSTA'nın böbrekfonksiyonu azalmış, tanınmamış KAH için riski yüksek olan, yüksek kan basıncı olan yaşlılardabu durum daha belirgindir. Yaşlı hastalarda kullanılması tavsiye edilmez. RUDİSTA'yı almadan önce diğer kardiyovasküler risk faktörlerine (örn. diyabet, hipertansiyon, sigara içme, obezite, ailede güçlü KAH öyküsü) sahip geriyatrik hastalar için birkardiyovasküler değerlendirmesi önerilir. 4.3. KontrendikasyonlarRUDİSTA aşağıdaki hastalarda kontrendikedir: İskemik koroner arter hastalığı (KAH) (anjina pektoris, miyokardiyal enfarktüs öyküsüveya belgelenmiş asemptomatik miyokard iskemisi) veya Prinzmetal anjina dahil koroner artervazospazmı. Koroner arter by-pass grefti (CABG) ameliyatı durumunda. Wolff-Parkinson-White sendromu veya diğer kardiyak aksesuar iletim yolu bozuklukları ileilişkili aritmiler. İnme veya geçici iskemik atak (TIA) öyküsü veya hemiplejik veya baziler migren öyküsü,çünkü bu hastalar daha yüksek inme riski altındadır. Periferik vasküler hastalık. İskemik bağırsak hastalığı. Kontrolsüz hipertansiyon. Son zamanlarda (24 saat içinde) ergotamin içeren ilaçların, ergot tipi ilaçların(dihidroergotamin veya metiserjid gibi) veya başka bir 5-hidroksitriptaminı (5-HT ı) agonistininkullanımı. Bir monoamin oksidaz (MAO)-A inhibitörünün eşzamanlı uygulaması veya yakın zamanda(2 hafta içinde) bir MAO-A inhibitörünün kullanımı. Aspirin veya diğer NSAİİ'leri aldıktan sonra astım, ürtiker veya alerjik tip reaksiyonöyküsü. Bu tür hastalarda NSAİİ'lere karşı şiddetli, bazen ölümcül, anafilaktik reaksiyonlarbildirilmiştir. Sumatriptan, naproksen veya RUDİSTA'nın herhangi bir bileşenine karşı bilinen aşırıduyarlılık (örn. anafilaktik reaksiyonlar, anjiyoödem ve ciddi deri reaksiyonları ). Gebeliğin üçüncü trimesteri. Şiddetli karaciğer yetmezliği. 4.4. Özel kullanım uyarıları ve önlemleriKardiyovasküler Trombotik OlaylarRUDİSTA'nın kullanımı, sumatriptan ve NSAİİ ile ciddi kardiyovasküler olay riskinin artması nedeniyle iskemik veya vazospastik koroner arter hastalığı (KAH) olan hastalarda ve koronerarter by-pass grefti (CABG) cerrahisi durumunda kontrendikedir (bkz. Bölüm 4.3). Sumatriptan ile Kardiyovasküler OlaylarSumatriptan uygulamasından sonraki birkaç saat içinde meydana gelen, akut miyokard enfarktüsü dahil ciddi kardiyak advers reaksiyonlara dair nadir raporlar bildirilmiştir. Bureaksiyonlardan bazıları, bilinen KAH'ı olmayan hastalarda meydana gelmiştir. RUDİSTA,KAH geçmişi olmayan hastalarda bile koroner arter vazospazmına (Prinzmetal anjina) nedenolabilir. Nonsteroid Antiinflamatuvar İlaçlarla Kardiyovasküler Trombotik OlaylarÜç yıla kadar süren çeşitli COX-2 seçici ve seçici olmayan NSAİİ'lerin klinik çalışmaları,ölümcül olabilen miyokard enfarktüsü (Mİ) ve inme dahil olmak üzere ciddi kardiyovasküler(KV) trombotik olay riskinde artış olduğunu göstermiştir. Mevcut verilere dayanarak, KVtrombotik olay riskinin tüm NSAİİ'ler için benzer olduğu belirsizdir. Ciddi KV trombotikolaylarda NSAİİ kullanımının sağladığı başlangıç düzeyine göre göreceli artış, bilinen KVhastalığı veya KV hastalığı için risk faktörleri olan ve olmayanlarda benzer görülmektedir.Ancak, bilinen KV hastalığı veya risk faktörleri olan hastalarda, artan başlangıç oranlarınedeniyle, aşırı ciddi KV trombotik olayların mutlak insidansı daha yüksektir. Bazı gözlemselçalışmalar, bu ciddi KV trombotik olay risk artışınıtedavinin ilk haftaları kadar erkenbaşladığını bulmuştur. KV trombotik risk artışı, daha yüksek dozlarda en tutarlı şekildegözlenmektedir.NSAİİ ile tedavi edilen hastalarda potansiyel KV riskinin en aza indirilmesi için, en düşük etkili doz olası en kısa süreyle kullanılmalıdır. Hekimler ve hastalar daha önceden KV semptomlarolmasa dahi bu tür semptomlara karşı hazırlıklı olmalıdır. Hastalar ciddi KV belirti ve/veyabulgular ve bunlar ortaya çıktığı takdirde yapılacaklar hakkında bilgilendirilmelidirler. Birlikteaspirin kullanımının, NSAİİ kullanımı ile ilişkili ciddi KV trombotik olay riskindeki artışıazalttığına dair tutarlı kanıtlar yoktur. Aspirin ve NSAİİ'lerin birlikte kullanımı ciddigastrointestinal (Gİ) olayların gelişme riskini artırmaktadır. Koroner Arter By-pass Greft (CABG) Cerrahisi Sonrası Durumİki büyük, kontrollü klinik çalışmada, CABG cerrahisini izleyen ilk 10-14 gün içerisinde ağrı tedavisi için COX-2 selektif NSAİİ kullanımının miyokardiyal enfarktüs ve felç insidansındaartışa neden olduğu ortaya konmuştur. NSAİİ'ler, CABG durumunda kontrendikedir (bkz.Bölüm 4.3). Mİ Sonrası HastalarDanimarka Ulusal Kayıtları'nda yürütülen gözlemsel çalışmalar, Mİ sonrası dönemde NSAİİ'lerle tedavi edilen hastaların, tedavinin ilk haftasından itibaren yeniden enfarktüs, KVile ilişkili ölüm ve tüm nedenlere bağlı ölüm riskinde artış olduğunu göstermiştir. Aynıkohortta, Mİ sonrası ilk yıldaki ölüm insidansı NSAİİ ile tedavi edilen hastalarda 100 kişi yılda20 iken, NSAİİ tedavisi almayan hastalarda 100 kişi yılda 12 idi. Mutlak ölüm oranı, Mİ sonrasıilk yıldan sonra bir miktar düşmesine rağmen, NSAİİ kullanıcılarında artan göreceli ölüm riski,en azından sonraki dört yıllık takiplerde de devam etmiştir. RUDİSTA'yı almadan önce birden çok kardiyovasküler risk faktörüne (örn. ileri yaş, diyabet, hipertansiyon, sigara içme, obezite, güçlü aile KAH öyküsü) sahip hastalarda kardiyovaskülerdeğerlendirme yapılmalıdır. KAH veya koroner arter vazospazmına dair kanıt olmasıdurumunda RUDİSTA kontrendikedir. Kardiyovasküler değerlendirmesi negatif olan birdençok kardiyovasküler risk faktörüne sahip hastalar için, ilk RUDİSTA dozunun tıbbi gözleminolduğu bir ortamda uygulanması ve RUDİSTA uygulamasının hemen ardından birelektrokardiyogram (EKG) yapılması dikkate alınmalıdır. Bu tür hastalar için, aralıklı uzunsüreli RUDİSTA kullanıcılarında periyodik kardiyovasküler değerlendirme yapılması dikkatealınmalıdır. Hekimler ve hastalar daha önceden KV semptomlar olmasa dahi bu tür semptomlara karşı hazırlıklı olmalıdır. Hastalar ciddi KV belirti ve/veya bulgular ve bunlar ortaya çıktığı takdirdeyapılacaklar hakkında bilgilendirilmelidirler. Gastrointestinal Kanama, Ülserasyon ve PerforasyonRUDİSTA'nın bir bileşeni olan naproksen de dahil olmak üzere NSAİİ'ler, mide, ince bağırsak veya kalın bağırsakta ölümcül olabilen inflamasyon, kanama, ülserasyon ve delinme gibi ciddigastrointestinal yan etkilere neden olur. Bu ciddi advers olaylar, NSAİİ'lerle tedavi edilenhastalarda herhangi bir zamanda uyarı semptomları vererek veya vermeksizin ortaya çıkabilir.NSAİİ tedavisinde ciddi bir üst gastrointestinal yan etki geliştiren 5 hastadan sadece 1'isemptomatiktir. NSAİİ'lerin neden olduğu üst gastrointestinal ülserler, büyük kanama veyaperforasyon, 3 ila 6 ay boyunca her gün tedavi edilen hastaların yaklaşık %1'inde ve 1 yıl tedavigören hastaların yaklaşık %2 ila %4'ünde ortaya çıkmaktadır. Bununla birlikte, kısa sürelitedavi bile risksiz değildir. Kontrollü ve kontrolsüz klinik çalışmalarda RUDİSTA alan 3.302 yetişkin migren hastası arasında, 1 hasta 3 hafta boyunca 8 doz aldıktan sonra mide ülseri nüksü yaşamıştır ve 1 hasta7 ayda ortalama 8 atağı tedavi edildikten sonra mide ülseri geliştirmiştir. Gİ Kanama, Ülserasyon ve Perforasyon için Risk FaktörleriÖnceden peptik ülser ve/veya gastrointestinal kanama öyküsü olan ve NSAİİ kullanan hastalarda, Gİ kanama riski bu risk faktörleri olmayan hastalara göre 10 kat artmıştır. NSAİİile tedavi edilen hastalarda, Gİ kanama riskini artıran diğer faktörler, beraberinde oralkortikosteroid, anti-koagülan, aspirin veya seçici serotonin geri alım inhibitörlerinin(SSRI'ların) kullanılması, uzun süreli NSAİİ kullanımı, sigara içilmesi, alkol kullanımı, ileriyaş ve genel durum bozukluğudur Ölümcül Gİ olaylara ait spontan bildirimlerin çoğu, yaşlıveya genel sağlık durumu kötü hastalara aittir, dolayısıyla bu hasta gruplarının tedavisindedikkatli olunmalıdır. Ek olarak, ilerlemiş karaciğer hastalığı ve/veya koagülopatisi olanhastalar, Gİ kanama açısından yüksek risk altındadır. NSAİİ ile tedavi edilen hastalarda Gİ riskleri en aza indirmeye yönelik stratejiler: En düşük etkili doz mümkün olan en kısa süre için kullanılmalıdır. Aynı anda birden fazla NSAİİ uygulamasından kaçınılmalıdır. Faydaların artan kanama riskinden daha ağır basması beklenmedikçe yüksek risk altındaki hastalarda kullanılmasından kaçınılmalıdır. Aktif Gİ kanaması olanların yanı sıra yüksek riskli hastalar için NSAİİ'ler dışında alternatif tedaviler düşünülmelidir. Doktorlar ve hastalar NSAİİ kullanımı sırasında gelişebilecek Gİ kanama ve ülserasyonbelirti ve semptomlarına karşı hazırlıklı olmalıdırlar. Ciddi bir Gİ advers olaydan şüpheleniliyorsa, derhal ek değerlendirmeye ve tedaviyebaşlanmalıdır ve ciddi bir Gİ advers olay ortadan kalkana kadar RUDİSTA kullanımıdurdurulmalıdır. Kardiyak profilaksi için düşük doz aspirinin eşzamanlı kullanılması durumunda, hastalarGİ kanama belirti ve semptomları açısından daha yakından izlenmelidir. Aritmiler5-HTı agonistlerinin uygulanmasını takiben birkaç saat içinde ventriküler taşikardi ve ölüme yol açan ventriküler fibrilasyon dahil olmak üzere yaşamı tehdit eden kardiyak ritimbozuklukları bildirilmiştir. Bu rahatsızlıklar meydana gelirse RUDİSTA kullanımıdurdurulmalıdır. RUDİSTA, Wolff-Parkinson-White sendromu veya diğer kardiyak aksesuar iletim yolu bozuklukları ile ilişkili aritmileri olan hastalarda kontrendikedir. Göğüs, Boğaz, Boyun ve/veya Çene Ağrısı/Sıkışması/BasmcıSumatriptan ile tedaviden sonra prekordiyum, boğaz, boyun ve çenede; sıkılık, ağrı, basınç ve ağırlık hissi sıklıkla ortaya çıkar ve genellikle köken olarak kalp dışıdır. Bununla birlikte, buhastalar yüksek kardiyak risk altındaysa kardiyak değerlendirme yapılmalıdır. RUDİSTA'nınkullanımı, KAH ve Prinzmetal varyant anjinası olan hastalarda kontrendikedir. Serebrovasküler Olaylar5-HTı agonistleri ile tedavi edilen hastalarda serebral hemoraji, subaraknoid kanama ve inme meydana gelmiş ve bazıları ölümle sonuçlanmıştır. Bazı vakalarda, serebrovasküler olaylarınprimer olmasının mümkün gözükmektedir, bu semptomların migrenden kaynaklanmamasınarağmen migren kaynaklı gibi yanlış bir inançla bu hastalara 5-HT ı agonistleri uygulanmaktadır.Ayrıca, migren hastaları belirli serebrovasküler olaylar (örn. inme, kanama, TIA) açısındanyüksek risk altında olabilir. Serebrovasküler bir olay meydana gelmesi durumunda RUDİSTAkullanımı durdurulmalıdır. Daha önce migren tanısı konmamış hastalarda ve atipik semptomlar gösteren migrenlilerde baş ağrılarını tedavi etmeden önce, potansiyel olarak ciddi nörolojik durumlar dışlanmalıdır.RUDİSTA, inme veya TIA öyküsü olan hastalarda kontrendikedir (bkz. Bölüm 4.3). Diğer Vazospazm ReaksiyonlarıSumatriptan, periferik vasküler iskemi, gastrointestinal vasküler iskemi ve enfarktüs (karın ağrısı ve kanlı ishal ile kendini gösterir), dalak enfarktüsü ve Raynaud sendromu gibi koronerolmayan vazospastik reaksiyonlara neden olabilir. Herhangi bir 5-HTı agonistinin kullanımını
takiben koroner olmayan vazospazm reaksiyonunu düşündüren semptomlar veya bulgular yaşayan hastalarda, ek RUDİSTA almadan önce vazospastik reaksiyon dışlanmalıdır. 5-HTı agonistlerinin kullanımı ile geçici ve kalıcı körlük ve önemli kısmi görme kaybı raporları bildirilmiştir. Görsel bozukluklar bir migren atağının parçası olabileceğinden, bu olaylar ve 5-HTı agonistlerinin kullanımı arasında nedensel ilişki net bir şekilde kurulmamıştır. HepatotoksisiteRUDİSTA'nın bir bileşeni olan naproksen dahil NSAİİ'leri alan hastaların %15'inde 1 veya daha fazla karaciğer testinde sınırda yükselmeler meydana gelebilir. Karaciğer anomalileri,doğrudan toksisiteden çok aşırı duyarlılığın sonucu olabilir. Bu anomaliler ilerleyebilir,değişmeden kalabilir veya devam eden tedavide geçici olabilir. NSAİİ'lerle yapılan klinikçalışmalarda hastaların yaklaşık %1'inde SGPT (ALT) veya SGOT (AST)'da dikkate değer(normalin üst sınırının 3 katı) yükselmeler bildirilmiştir. Ek olarak, NSAİİ'lerle sarılık veölümcül fulminan hepatit, karaciğer nekrozu ve karaciğer yetmezliği dahil olmak üzere, nadir,bazen ölümcül ciddi karaciğer hasarı vakaları bildirilmiştir. RUDİSTA şiddetli karaciğer yetmezliği olan hastalarda kontrendikedir. RUDİSTA ile tedavi sırasında, bir hastada karaciğer disfonksiyonu geliştiğine dair belirti ve/veya bulgular ortayaçıktığında veya anormal karaciğer testleri olanlarda, daha ciddi karaciğer reaksiyonlarınıngelişimine ait kanıtlar incelenmelidir. Karaciğer hastalığı ile uyumlu klinik belirti vesemptomlar gelişirse, sistemik belirtiler ortaya çıkarsa (örn. eozinofili, döküntü) veya anormalkaraciğer testleri devam ederse veya kötüleşirse RUDİSTA kullanımı durdurulmalıdır. Hastaları hepatotoksisitenin uyarı belirtileri ve semptomları hakkında bilgilendiriniz (örn. mide bulantısı, yorgunluk, uyuşukluk, ishal, kaşıntı, sarılık, sağ üst kadran hassasiyeti ve "gripbenzeri" semptomlar). Karaciğer hastalığı ile uyumlu klinik belirti ve semptomlar gelişirse veyasistemik belirtiler ortaya çıkarsa (örn. eozinofili, döküntü vb.) RUDİSTA kullanımı derhaldurdurulmalıdır ve hastanın klinik değerlendirmesi yapılmalıdır. HipertansiyonRUDİSTA'nın bir bileşeni olan sumatriptan da dahil olmak üzere 5-HTı agonistleri ile tedavi edilen hastalarda nadir durumlarda organ sistemlerinde akut bozuklukla birlikte hipertansif krizdahil olmak üzere kan basıncında önemli artış bildirilmiştir. Bu durum, hipertansiyon öyküsüolmayan hastaları da içermektedir. RUDİSTA'nın bir bileşeni olan naproksen de dahil olmak üzere NSAİİ'ler ayrıca yeni hipertansiyonun başlamasına veya önceden var olan hipertansiyonun kötüleşmesine yol açabilirve her ikisi de kardiyovasküler olayların artmış insidansına katkıda bulunabilir. Anjiyotensindönüştürücü enzim (ADE) inhibitörleri, anjiyotensin reseptör blokerleri (ARB'ler), betablokerleri, tiyazid diüretikleri veya loop diüretikleri alan hastalarda, NSAİİ'leri alırken butedavilere verilen yanıtta bozulma olabilir. RUDİSTA ile tedavi edilen hastalarda kan basıncım izleyiniz. RUDİSTA, kontrol altında olmayan hipertansiyon hastalarında kontrendikedir (bkz. Bölüm 4.3). Kalp Yetmezliği ve ÖdemSelektif COX-2 inhibitörlerin ve geleneksel NSAİİ'lerin randomize kontrollü çalışmalarının meta-analizi, selektif COX-2 inhibitörleri ile ve seçici olmayan NSAİİ ile tedavi edilenhastalarda kalp yetmezliği nedeniyle hastaneye yatışlarda plasebo ile tedavi edilen hastalarakıyasla yaklaşık iki kat artış olduğunu göstermiştir. Danimarka Ulusal Kayıt çalışmasında, kalpyetmezliği olan hastalarda NSAİİ kullanımı Mİ riskini, kalp yetmezliği nedeniyle hastaneyeyatışı ve ölümü artırmıştır. Ek olarak, NSAİİ'lerle tedavi edilen bazı hastalarda sıvı tutulumu ve ödem gözlenmiştir. Naproksen kullanımı, bu tıbbi durumları tedavi etmek için kullanılan çeşitli terapötik ajanlarınKV etkilerini azaltabilir (örn. diüretikler, ADE inhibitörleri veya anjiyotensin reseptörblokerleri [ARB'ler]). Faydaların kalp yetmezliğini kötüleştirme riskinden daha ağır basması beklenmedikçe, şiddetli kalp yetmezliği olan hastalarda RUDİSTA kullanımından kaçınınız. RUDİSTA şiddetli kalpyetmezliği olan hastalarda kullanılıyorsa, hastaları kalp yetmezliğinin kötüleşme belirtileriaçısından izleyiniz. Her RUDİSTA 85 mg/500 mg film kaplı tablet yaklaşık 64 mg sodyum içerdiğinden, genel sodyum alımının ciddi şekilde kısıtlanması gereken hastalarda bu durum dikkate alınmalıdır. ilaç Aşırı Kullanımına Bağlı Baş AğrısıAkut migren ilaçlarının aşırı kullanımı (örn. ergotamin, triptanlar, opioidler veya bu ilaçların kombinasyonunun ayda 10 gün veya daha fazla) baş ağrısının şiddetlenmesine (ilaç aşırıkullanım baş ağrısı) yol açabilir. İlaç aşırı kullanımbaş ağrısı, migren benzeri günlük baş ağrılarıolarak veya migren ataklarının sıklığında belirgin bir artış olarak ortaya çıkabilir. Aşırıkullanılan ilaçların kesilmesi dahil olmak üzere hastaların detoksifikasyonu ve yoksunluksemptomlarının (genellikle baş ağrısının geçici olarak kötüleşmesini içerir) tedavisi gerekliolabilir. Serotonin SendromuSerotonin sendromu, RUDİSTA ile, özellikle seçici serotonin geri alım inhibitörleri (SSRI'lar), serotonin norepinefrin geri alım inhibitörleri (SNRI'lar), trisiklik antidepresanlar (TCA'lar) veMAO inhibitörleri ile birlikte uygulama sırasında ortaya çıkabilir. Serotonin sendromusemptomları arasında zihinsel durum değişiklikleri (örn. ajitasyon, halüsinasyonlar, koma),otonomik dengesizlik (örn. taşikardi, değişken kan basıncı, hipertermi), nöromüsküleranormallikler (örn. hiperrefleksi, koordinasyon bozukluğu) ve/veya gastrointestinalsemptomlar (örn. bulantı, kusma, ishal) bulunmaktadır. Semptomların başlangıcı genellikleyeni veya daha yüksek dozda serotonerjik bir ilaç aldıktan sonraki dakikalar ila saatler arasında
ortaya çıkar. Serotonin sendromundan şüphelenilmesi durumunda RUDİSTA kullanımı durdurulmalıdır. Renal Toksisite ve HiperkalemiRenal ToksisiteNSAİİ'lerin uzun süre kullanımı renal papiller nekroza ve diğer böbrek hasarlarına neden olur. Böbrek perfüzyonunun sağlanmasında prostaglandinlerin kompansatuar etkinliği olanhastalarda da renal toksisite gözlenmiştir. Bu hastalarda non-steroid anti-inflamatuar ilaçkullanımı, doza bağımlı olarak prostaglandinlerin yapımında azalmaya ve ikincil olarak böbrekkan akımını azaltarak böbrek dekompansasyonunun açıkça hızlanmasına neden olabilir. Böbrekfonksiyon bozukluğu, kalp yetmezliği, karaciğer yetmezliği, dehidrasyon, hipovolemi, tuzeksikliği olanlarda, diüretik ve ADE inhibitörleri alanlarda ve yaşlı hastalarda bu reaksiyonunriski daha fazladır. NSAİİ tedavinin kesilmesiyle, genellikle tedavi öncesi duruma geri dönülür.Böbrek hastalığı ile uyumlu klinik belirti ve semptomlar gelişirse veya sistemik belirtiler ortayaçıkarsa RUDİSTA kullanımı durdurulmalıdır. RUDİSTA'nın, faydalarının böbrek fonksiyonunun kötüleşme riskinden daha ağır basması beklenmedikçe şiddetli böbrek yetmezliği (kreatinin klirensi [CrCl] <30 mL/dak) olanhastalarda kullanılması önerilmez. İlerlemiş böbrek hastalığı olan hastalarda RUDİSTAkullanılıyorsa, böbrek fonksiyonlarında kötüleşme belirtileri açısından hastaları izleyiniz. Hafif(CrCl=60 ila 89 mL/dak) veya orta (CrCl=30 ila 59 mL/dak) böbrek yetmezliği, öncedenmevcut böbrek hastalığı veya dehidratasyonu olan hastalarda böbrek fonksiyonunu izleyiniz. RUDİSTA'nın renal etkileri, önceden böbrek hastalığı olan hastalarda böbrek fonksiyon bozukluğunun ilerlemesini hızlandırabilir. RUDİSTA'yı başlatmadan önce dehidrate veya hipovolemik hastalarda hacim durumunu düzeltiniz. RUDİSTA kullanımı sırasında böbrek veya karaciğer yetmezliği, kalp yetmezliği,dehidratasyon veya hipovolemisi olan hastalarda böbrek fonksiyonunu izleyiniz. Faydalarınböbrek fonksiyonunun kötüleşme riskinden daha ağır basması beklenmedikçe, ilerlemiş böbrekhastalığı olan hastalarda RUDİSTA kullanımından kaçınınız. İlerlemiş böbrek hastalığı olanhastalarda RUDİSTA kullanılıyorsa, böbrek fonksiyonlarında kötüleşme belirtileri açısındanhastaları izleyiniz. HiperkalemiNSAİİ'lerin kullanımı ile, böbrek yetmezliği olmayan bazı hastalarda bile, hiperkalemi dahil serum potasyum konsantrasyonunda artışlar bildirilmiştir. Normal böbrek fonksiyonu olanhastalarda, bu etkiler hiporeninemik-hipoaldosteronizm durumuna atfedilmiştir. Anafilaktik ReaksiyonlarRUDİSTA'nın herhangi bir bileşenine önceden maruz kalmadığı bilinen hastalarda anafilaktik reaksiyonlar meydana gelebilir. Bu tür reaksiyonlar yaşamı tehdit edici veya ölümcül olabilir.Genel olarak, ilaçlara karşıBanafilaktik (Biaksâyı 0nJarifizbifd§&. fazla alerjene duyarlılık öyküsüolan kişilerde görülme olasılığı daha yüksektir, ancak naproksene aşırı duyarlılığı olmayan
hastalarda veya aspirine duyarlı astımı olan hastalarda naproksen ile anafilaktik reaksiyonlar meydana gelmiştir (bkz. Bölüm 4.3). RUDİSTA, aspirin triadı olan hastalara verilmemelidir.Bu semptom kompleksi tipik olarak nazal polipi olan veya olmayan, rinit geçiren astımhastalarında veya aspirin veya diğer NSAİİ alımı sonrasında potansiyel olarak ölümcül, ciddibronkospazm sergileyen hastalarda gelişir (bkz. Bölüm 4.3). RUDİSTA, sumatriptan, naproksen veya RUDİSTA'nın herhangi başka bir bileşenine aşırı duyarlılık reaksiyonu öyküsü olan hastalarda kontrendikedir. Naproksen, naproksene aşırıduyarlılığı bilinmeyen hastalarda ve aspirine duyarlı astımı olan hastalarda anafilaktikreaksiyonlarla ilişkilendirilmiştir (bkz. Bölüm 4.3). Anafilaktoid reaksiyon gelişen vakalardaacil müdahale düşünülmelidir. Ciddi deri reaksiyonlarıNSAİİ içeren ürünler, ölümcül olabilen eksfolyatif dermatit, Stevens-Johnson sendromu (SJS) ve toksik epidermal nekroliz (TEN) gibi ciddi deri advers reaksiyonlarına neden olabilir. Buciddi olaylar, uyarı olmadan gerçekleşebilir. Hastaları ciddi deri reaksiyonlarının belirti vesemptomları hakkında bilgilendiriniz ve deri döküntüsü veya herhangi bir başka aşırı duyarlılıkbelirtisi görüldüğünde RUDİSTA kullanımını durdurunuz. RUDİSTA, NSAİİ'lere karşı dahaönce ciddi deri reaksiyonları olan hastalarda kontrendikedir (bkz. Bölüm 4.3). Duktus Arteriozus Erken KapanmasıRUDİSTA, duktus arteriozusun erken kapanmasına neden olabilir. 30. gebelik haftasından (üçüncü trimester) itibaren gebe kadınlarda RUDİSTA dahil NSAİİ'lerin kullanımındankaçınınız (bkz. Bölüm 4.3). Hematolojik ToksisiteRUDİSTA dahil olmak üzere, NSAİİ alan hastalarda bazen anemi gözlenebilir. Bunun nedeni sıvı retansiyonu, gizli veya aşikar Gİ kan kaybı veya eritropoez üzerindeki tam olaraktanımlanmamış etkilerdir. RUDİSTA dahil olmak üzere, uzun süreli NSAİİ alan hastalarda,herhangi bir anemi belirti veya bulgusu gözlenirse hemoglobin ve hematokrit değerleri kontroledilmelidir. NSAİİ'ler trombosit agregasyonunu inhibe eder ve bazı hastalarda kanamazamanının uzadığı gösterilmiştir. Aspirinden farklı olarak, trombosit fonksiyonları üzerindekietkileri kantitatif olarak daha az, kısa süreli ve geri dönüşümlüdür. Pıhtılaşma bozuklukları olanveya antikoagülan alan hastalarda olduğu gibi, trombosit fonksiyonundaki değişikliklerdenolumsuz şekilde etkilenen ve RUDİSTA alan hastalar, dikkatlice takip edilmelidir. Koagülasyon bozuklukları gibi eşlik eden hastalık durumları veya varfarin, diğer antikoagülanlar, antitrombosit ajanlar (örn. aspirin), serotonin geri alım inhibitörleri (SSRI'lar)ve serotonin norepinefrin geri alım inhibitörlerinin (SNRI'ler) eşzamanlı kullanılması bu riskiartırabilir. Bu hastaları kanama belirtileri açısından dikkatlice takip edilmelidir (bkz. Bölüm4.5). Aspirin Duyarlılığına Bağlı Astım AlevlenmesiAstımlı hastaların bir alt popülasyonunda, nazal poliplerle komplike hale gelen kronik rinosinüzit, şiddetli, potansiyel olarak ölümcül bronkospazm ve/veya aspirin ve diğerNSAİİ'lere karşı intolerans gösteren, aspirine duyarlı astım olabilir. Aspirin ile diğer NSAİİ'lerarasında çapraz reaktivite bu tür aspirine duyarlı hastalarda bildirildiğinden, RUDİSTA bu türaspirin duyarlılığı olan hastalarda kontrendikedir ve önceden astımı olan hastalarda dikkatlikullanılmalıdır (bkz. Bölüm 4.3). RUDİSTA önceden astımı olan hastalarda (bilinen aspirin duyarlılığı olmayan) kullanıldığında, hastaları astım belirti ve semptomlarındaki değişiklikler açısından takip ediniz. NöbetlerSumatriptan uygulamasının ardından nöbetler bildirilmiştir. Bazıları, nöbet öyküsü olan veya nöbetlere yatkınlık yaratan eşzamanlı koşulları olan hastalarda meydana gelmiştir. Hastalardabu tür predispozan faktörlerin belirgin olmadığı raporlar da vardır. RUDİSTA, epilepsi öyküsüolan veya düşmüş nöbet eşiği ile ilişkili durumları olan hastalarda dikkatli kullanılmalıdır. inflamasyon ve Ateşin MaskelenmesiRUDİSTA'nın inflamasyonu ve muhtemelen ateşi azaltmadaki farmakolojik aktivitesi, enfeksiyonların teşhis edilmesindeki tanısal işaretlerin kullanılabilirliğini azaltabilir. Laboratuvar İzlemiCiddi Gİ kanaması, hepatotoksisite ve böbrek hasarı, uyarı semptomları veya belirtileri olmadan ortaya çıkabileceğinden, uzun süreli NSAİİ tedavisi gören hastaların tam kan sayımıve biyokimya profilini periyodik olarak izlemeyi düşününüz. Bu tıbbi ürün her dozunda 64 mg sodyum ihtiva eder. Bu durum, kontrollü sodyum diyetinde olan hastalar için göz önünde bulundurulmalıdır. 4.5. Diğer tıbbi ürünler ile etkileşimler ve diğer etkileşim şekilleriRUDİSTA ile Klinik Olarak Önemli İlaç EtkileşimleriNSAİİ'ler veya Sumatriptan ile klinik olarak önemli ilaç etkileşimleri için Tablo 1'e bakınız. Tablo 1. Naproksen veya sumatriptan ile Klinik Olarak Önemli İlaç Etkileşimleri
 Monoamin oksidaz-A inhibitörleriKlinik Etki:MAO-A inhibitörleri, oral yoldan uygulanan sumatriptanın sistemik maruziyetini 7 kat arttırır. Girişim:MAO-A inhibitörleri alan hastalarda RUDİSTA kullanımı kontrendikedir. Diğer 5-HTı AgonistleriKlinik Etki:
5-HTı agonisti ilaçlar vazospastik etkilere neden olabilir. Girişim:Bu etkiler aditif olabileceğinden, RUDİSTA ve diğer 5 HTı agonistlerinin (örn. triptanlar) 24 saat içinde birlikte uygulanmasıkontrendikedir. Hemostazı Etkileyen İlaçlarKlinik Etki: Naproksen ve varfarin gibi antikoagülanların kanama üzerindesinerjistik etkisi vardır. Naproksen ve antikoagülanların eşzamanlıkullanımı, her iki ilacın tek başına kullanımına kıyasla ciddikanama riskinde artışa sahiptir. Trombositler tarafından salınan serotonin, hemostazda önemli bir rol oynar. Vaka kontrolü ve kohort epidemiyolojik çalışmalar, serotonin geri alımına müdahale eden ilaçların ve bir NSAİİ'nineşzamanlı kullanımının kanama riskini tek başına bir NSAİİ kullanımından daha fazla artırabileceğini göstermiştir._Girişim:RUDİSTA'yı antikoagülanlar (örn. varfarin), antitrombosit ajanlar (örn. aspirin), seçici serotonin geri alım inhibitörleri (SSRI'lar) veserotonin norepinefrin geri alım inhibitörleri (SNRI'lar) ile eşzamanlıolarak kullanan hastaları kanama belirtileri açısından izleyiniz (bkz. Bölüm 4.4).AspirinKlinik Etki:Bir farmakodinamik (PD) çalışma, daha düşük dozda naproksenin (220 mg/gün veya günde iki kez 220 mg), düşük dozda hızlı salımlı aspirininantiplatelet etkisine müdahale ettiği bir etkileşimi göstermiştir veetkileşim en çok naproksenin arınma döneminde belirgindir. Reçetelinaproksen dozları veya enterik kaplı düşük doz aspirin ile etkileşimoluşmasının beklenmesi için nedenler vardır; bununla birlikte, aspirinfonksiyonu ile pik etkileşim, daha uzun arınma döneminden dolayı PDçalışmasında gözlemlenenden daha geç olabilir. Kontrollü klinikçalışmalar, NSAİİ'lerin ve aspirin analjezik dozlarının eşzamanlıkullanımının, tek başına NSAİİ'lerin kullanımından daha büyük birterapötik etki yaratmadığını göstermiştir. Bir klinik çalışmada, NSAİİve aspirinin eşzamanlı kullanımı, tek başına NSAİİ kullanımınakıyasla önemli ölçüde artmış Gİ advers reaksiyon insidansı ileilişkilendirilmiştir (bkz. Bölüm 4.4). Girişim:doğrulama Kodu: 1ZW56Q3NRRG8:müdahale'setmesU snedeniyte Tanapr0kSeftfn"'^feeSrtmg8İtfinglftrdffedaBmüdahale'setmesU snedeniyte Tanapr0kSeftfn"'^feeSrtmg8İtfinglftrdffedaB
 
İlaç/Laboratuvar Test EtkileşimleriKan testleriNaproksen, trombosit agregasyonunu azaltabilir ve kanama süresini uzatabilir. Kanama süreleri belirlenirken bu etki göz önünde bulundurulmalıdır. İdrar TestleriNaproksen sodyumun uygulanması, ilaç ve/veya metabolitleri ile bu testte kullanılan m-di-nitrobenzen arasındaki etkileşim nedeniyle 17-ketojenik steroidlerin idrar değerlerinde artışa neden olabilir. 17-hidroksi-kortikosteroid ölçümleri (Porter-Silber testi) yapay olarakdeğişmiş gibi görünmesede, Porter-Silber testi kullanılacaksa, naproksen tedavisinin adrenalfonksiyon testleri yapılmadan 72 saat önce geçici olarak kesilmesi önerilmektedir. Naproksen, 5-hidroksi indolasetik asitin (5HIAA) idrarda tayinini hatalı olarak etkileyebilmektedir. Özel popülasyonlara ilişkin ek bilgiler Pediyatrik popülasyon:Pediyatrik popülasyona ilişkin herhangi bir etkileşim çalışması tespit edilmemiştir. 4.6. Gebelik ve laktasyonGenel tavsiyeÇocuk doğurma potansiyeli bulunan kadınlar / Doğum kontrolü (kontrasepsiyon)RUDİSTA ve etken madddelerden bir olan sumatriptan için yeterli veri mevcut değildir. Naproksen etken maddesi ise hamile kalmayı planlayan kadınlarda kullanılmamalıdır. Gebelik dönemiGebe kadınlarda yeterli ve iyi kontrollü çalışmalar yoktur. RUDİSTA (sumatriptan ve naproksen), gebeliğin birinci ve ikinci trimesterinde, yalnızca potansiyel yararın fetüsünpotansiyel riskinden fazla olması halinde kullanılmalıdır. RUDİSTA, gebeliğin üçüncütrimesterinde kullanılmamalıdır çünkü prostaglandin sentezi inhibitörlerinin (naproksen dahil)insanlarda duktus arteriyozusun erken kapanmasına neden olduğu bilinmektedir. Hayvançalışmalarında, sumatriptan ve naproksenin gebelik sırasında tek başına veya kombinasyonhalinde uygulanması, klinik olarak ilgili dozlarda gelişim toksisitesine (fetal malformasyonvakalarında artış, embriyofetal ve yavru ölümleri, azalmış embriyofetal büyüme) nedenolmuştur. Organogenez süresi boyunca hamile tavşanlara sumatriptanın naproksen sodyum ile birlikte (5/9, 25/45 veya 50/90 mg/kg/gün sumatriptan/naproksen sodyum) veya her bir ilacın tek başına(50/0 veya 0/90 mg/kg/gün sumatriptan/naproksen sodyum) oral yoldan uygulanması, tümdozlarda toplam fetal anormallik vakalarında artışa ve tek başına veya kombinasyon halinde enyüksek sumatriptan ve naproksen dozunda spesifik malformasyon (50/90 mg/kg/gün grubundakardiyak interventriküler septal defekt, 50/0 ve 0/90 mg/kg/gün gruplarında kaynaşmış kaudalvertebra) ve varyasyon vakalarında (akciğerin ara lobunun yokluğu, kafatasının düzensizossifikasyonu, yetersiz kemikleşmiş sternum) artışa neden olmuştur. Tavşanlarda gelişimseltoksisite için etkisiz bir doz belirlenmemiştir. En düşük etkili doz, maksimum insan günlükdozu (MHDD) olan 170 mg sumatriptan ve 1000 mg naproksen sodyumda (24 saatlik dönemdeiki tablet RUDİSTA 85 mg/500 mg) elde edilenlerden daha az olan sumatriptan ve naproksenplazma maruziyetleri (EAA) ile ilişkili olan 5/9 mg/kg/gün sumatriptan/naproksen sodyumdu. Sumatriptanın önceki gelişimsel toksisite çalışmalarında, organogenez periyodu sırasında hamile sıçanlara 250 mg/kg/gün veya daha yüksek dozlarda oral uygulama, fetal kan damarıanormalliklerinin insidansında artış ve yavru sağkalımında azalma ile sonuçlanmıştır. Etkisizen yüksek doz, mg/m2 bazında 170 mg sumatriptanın MHDD'sinin yaklaşık 3 katı olan 60mg/kg/gün olmuştur. Sumatriptanın organogenez periyodu sırasında hamile tavşanlara oralyoldan uygulanması, 50 mg/kg/gün dozda vasküler ve iskelet anormalliklerinde ve 100mg/kg/gün dozda embriyoletalite vakalarında artışa neden olmuştur. Tavşanlarda gelişimseltoksisite için en yüksek etkisiz sumatriptan dozu 15 mg/kg/gün veya mg/m2 bazında 170 mgsumatriptanın MHDD'sinin yaklaşık 2 katıdır. Naproksen içeren ürünler sancı sırasında ve doğumda tavsiye edilmez çünkü prostaglandin sentezini inhibe edici etkisiyle naproksen fetal dolaşımı olumsuz etkileyebilir ve uteruskasılmalarını engelleyerek uterus kanaması riskini arttırabilir. NSAİİ'lerle yapılan sıçançalışmalarında, prostaglandin sentezini inhibe ettiği bilinen diğer ilaçlarda olduğu gibi, distosi Belge DcvegebfRteişdoğumffisidaös^a^âif^ yavru'sağka^ında iseaza3maffleydan&°ğetffiiştiri'"-"''y^Laktasyon dönemiRUDİSTA'nın her iki aktif bileşeninin, sumatriptan ve naproksenin insan sütüne geçtiği rapor edilmiştir. RUDİSTA'nın emzirilen bebeklerde ciddi advers reaksiyon potansiyeli olmasınedeniyle, ilacın anne için önemi göz önünde bulundurularak, emzirmenin mi yoksa ilacın mıbırakılacağına karar verilmelidir. Üreme yeteneği / FertiliteRUDİSTA ve etken maddelerinden bir olan sumatriptan için veri yoktur. Ancak diğer bir etken madde olan naproksen kullanımı için siklooksijenaz/prostaglandin sentezini inhibe ettiğibilinen herhangi bir ilaç ile olduğu gibi, fertiliteyi bozabilir ve hamile kalmayı planlayankadınlarda kullanılmamalıdır. Gebe kalma güçlüğü olan veya kısırlık incelemeleri yapılankadınlarda, naproksenin kesilmesi düşünülmelidir. 4.7. Araç ve makine kullanımı üzerindeki etkilerRUDİSTA baş dönmesine, halsizliğe veya uyuşukluğa neden olabilir. Bu semptomlar varsa araba sürülmemeli, makine kullanılmamalı veya uyanık olunması gereken herhangi bir işyapılmamalıdır. 4.8. İstenmeyen etkilerSistem organ sınıfına göre aşağıda listelenen istenmeyen olayların sıklık dereceleri şu şekilde tanımlanmıştır: Çok yaygın (>1/10); yaygın (>1/100 ila <1/10); yaygın olmayan (>1/1.000 ila <1/100); seyrek (>1/10.000 ila <1/1.000); çok seyrek (<1/10.000); bilinmiyor (eldeki verilerden hareketletahmin edilemiyor) Enfeksiyonlar ve enfestasyonlarBilinmiyor: Aseptik menenjitKan ve lenf sistemi hastalıklarıBilinmiyor: Hematolojik toksisiteBağışıklık sistemi hastalıklarıBilinmiyor: Anaflaktoid reaksiyonlarMetabolizma ve beslenme hastalıklarıBilinmiyor: HiperkalemiPsikiyatrik hastalıklarBilinmiyor: Depresyon, uyku bozukluğu, uykusuzluk, konfüzyon, halüsinasyon Sinir sistemi hastalıklarıÇok yaygın: Baş dönmesi, zayıf, uykulu veya yorgun hissetme, el veya ayak parmaklarınızda karıncalanma veya uyuşma Bilinmiyor: Serebrovasküler olaylar, ilaç aşırı kullanımına bağlı baş ağrısı, nöbetler Kardiyak hastalıklarÇok yaygın: Palpitasyon, boyun, boğaz, çene veya göğsünüzde ağrı, rahatsızlık veya sertlik Bilinmiyor: Kardiyovasküler trombotik olaylar, aritmiler, kalp yetmezliği ve ödem, vazospazmreaksiyonları, hipertansiyon Solunum, göğüs bozuklukları ve mediastinal hastalıklarBilinmiyor: Aspirin duyarlılığına bağlı astım alevlenmesiGastrointestinal hastalıklarÇok yaygın: Mide yanması, mide bulantısı, ağız kuruluğu Bilinmiyor: Gİ kanama, ülserasyon ve perforasyon Hepato-bilier hastalıklarBilinmiyor: HepatotoksisiteDeri ve derialtı doku hastalıklarıBilinmiyor: Ciddi deri reaksiyonlarıKas-iskelet bozukluklar, bağ doku ve kemik hastalıklarıÇok yaygın: Kas gerginliğiBöbrek ve idrar yolu hastalıklarıBilinmiyor: Böbrek toksisitesiGenel bozukluklar ve uygulama bölgesine ilişkin hastalıklarKlinik Çalışma DeneyimleriKlinik araştırmalar çok çeşitli koşullar altında yürütüldüğünden, bir ilacın klinik araştırmalarında gözlemlenen advers reaksiyon oranları, başka bir ilacın klinikaraştırmalarındaki oranlarla doğrudan karşılaştırılamaz ve pratikte gözlemlenen oranlarıyansıtmayabilir. YetişkinlerAşağıda bildirilen advers reaksiyonlar, sumatriptan + naproksen sodyum 85 mg/500 mg ile yapılan klinik araştırmalara özgüdür. Naproksen ve sumatriptan ürünleri için tam reçete Tablo 2, 2 plasebo kontrollü klinik çalışmada (Çalışma 1 ve 2) 1 doz çalışma ilacı alan yetişkin hastalarda meydana gelen advers reaksiyonları listelemektedir. Yalnızca sumatriptan +naproksen sodyum 85 mg/500 mg ile tedavi edilen herhangi bir grupta %2 veya daha fazlasıklıkta meydana gelen ve plasebo grubundan daha sık görülen advers reaksiyonlar Tablo 2'yedahil edilmiştir. Tablo 2. Migrenli Yetişkin Hastalarda Havuzlanmış Plasebo Kontrollü Çalışmalardaki Advers Reaksiyonlar
Kontrollü klinik çalışmalardaki advers reaksiyon insidansı, hastaların cinsiyetinden veya yaşından etkilenmemiştir. Irkın advers reaksiyon insidansı üzerindeki etkisini değerlendirmekiçin yeterli veri yoktu. 12 ila 17 yaş arası pediyatrik hastalar1 doz sumatriptan + naproksen sodyum 10 mg/60 mg, 30 mg/180 mg veya 85 mg/500 mg alan 12-17 yaş arası pediyatrik hastaları değerlendiren plasebo kontrollü bir klinik araştırmada, 10mg/60 mg alan hastaların %13'ünde, 30 mg/180 mg alan hastaların %9'unda, 85 mg/500 mgalanların %13'ünde ve plasebo alanların %8'inde yan etkiler meydana gelmiştir. Sumatriptan +naproksen sodyum alan hiçbir hasta, denemeden çekilmeye neden olan advers reaksiyonlaryaşamamıştır. 12 ila 17 yaş arası pediyatrik hastalarda advers reaksiyon insidansı, plasebo ilekarşılaştırıldığında 3 dozun tamamında karşılaştırılabilir olmuştur. Tablo 3, sumatriptan +naproksen sodyum ile 12 ila 17 yaş arasındaki pediyatrik hastalarda plasebo kontrollü bir
çalışmada %2 veya daha fazla sıklıkta meydana gelen ve plasebo grubundan daha sık görülen advers reaksiyonları listelemektedir. Tablo 3. 12 ila 17 Yaş Arası Migrenli Pediyatrik Hastalarda Plasebo Kontrollü Bir Çalışmadaki Advers Reaksiyonlar
Şüpheli advers reaksiyonların raporlanmasıRuhsatlandırma sonrası şüpheli ilaç advers reaksiyonlarının raporlanması büyük önem taşımaktadır. Raporlama yapılması, ilacın yarar/risk dengesinin sürekli olarak izlenmesineolanak sağlar. Sağlık mesleği mensuplarının herhangi bir şüpheli advers reaksiyonu TürkiyeFarmakovijilans Merkezi (TÜFAM)'ne bildirmeleri gerekmektedir (www.titck.gov.tr:[email protected]. Doz aşımı ve tedavisiHastalar (N=670), önemli advers etkiler olmadan 140 ila 300 mg sumatriptan içeren tek oral dozlar almıştır. Gönüllüler (N=174), ciddi advers etkiler olmadan 140 ila 400 mg'lık tek oraldozlar almıştır. Hayvanlarda sumatriptan aşırı dozu ölümcül olmuştur ve konvülsiyonlar, titreme, felç, hareketsizlik, pitoz, ekstremitelerde eritem, anormal solunum, siyanoz, ataksi, midriyazis,salivasyon ve lakrimasyon ile kendini göstermiştir. Akut NSAİİ aşırı dozlarını takip eden semptomlar tipik olarak uyuklama, uyuşukluk, mide bulantısı, kusma ve epigastrik ağrı ile sınırlıdır. Gastrointestinal kanama meydana gelmiştir.Hipertansiyon, akut böbrek yetmezliği, solunum depresyonu ve koma meydana gelmiştir, ancakbunlar nadirdir (bkz. Bölüm 4.4). NSAİİ doz aşımının ardından hastalara semptomatik ve destekleyici bakım veriniz. Spesifik bir , ,Ru belge, güveııli elektronik imza ile imzalanıjjıştjr..-i ı ı j Belge D<afttidotudy:oktur<2U&SBlamadan 5İ°lrâkiAdörİ6saat igindPaigpÂülefttsemRt?ffl&tik(hasialarda-vıeya
fazla doz aşımı olan hastalarda (önerilen dozun 5 ila 10 katı) kusturma ve/veya aktif kömür (kg başına, yetişkinlerde 60 ila 100 gram, pediyatrik hastalarda 1 ila 2 gram) ve/veya ozmotikkatartik düşününüz. Hemodiyaliz, proteine yüksek oranda bağlanması nedeniyle naprokseninplazma konsantrasyonunu azaltmaz. Hemodiyaliz veya periton diyalizinin sumatriptanın serumkonsantrasyonları üzerinde ne gibi bir etkisi olduğu bilinmemektedir. Zorlu diürez, idrarınalkalileşmesi, hemodiyaliz veya hemoperfüzyon, yüksek protein bağlanması nedeniyle yararlıolmayabilir. Doz aşımı tedavisi hakkında ek bilgi için bir zehir kontrol merkezine başvurunuz. 5. FARMAKOLOJİK ÖZELLİKLER5.1. Farmakodinamik özelliklerFarmakoterapötik grup: Selektif serotonin (5HT1) agonistleri ATC kodu: N02CC Etki MekanizmasıRUDİSTA, sumatriptan ve naproksen içerir. Sumatriptan, klonlanmış 5-HT 1B/1DIB/IDreseptörlerinde agonist etkiler yoluylagösterir, bu da kraniyal damar daralmasına ve nöropeptit salımının inhibisyonuna neden olur.RUDİSTA'nın analjezik, antiinflamatuar ve antipiretik özellikleri vardır. Diğer NSAİİ'lerinki gibi RUDİSTA'nın etki mekanizması tam olarak anlaşılmamıştır, ancak siklooksijenazın(COX-1 ve C0X-2) inhibisyonunu içerir. Naproksen, in vitroin vivoFarmakodinamikBir sağlıklı gönüllü çalışmasında, günde bir kez 220 mg naproksen ile düşük dozda hızlı salımlı aspirinin (81 mg) birlikte 10 günlük eşzamanlı uygulamasında, 10. gündeki dozun ardından 24saatte serum tromboksan B2 inhibisyonu ile ölçülen aspirinin antiplatelet aktivitesi ile biretkileşim göstermiştir [%98,7 (tek başına aspirin) vs. %93,1 (naproksen ve aspirin)]. Etkileşim,11. günde naproksenin kesilmesinden sonra bile gözlemlenmiştir (aspirin dozu devam ederken)ancak 13. günde normale ^önmüştürni eAya^ikşalışmadajnıfiıtkileşim, naproksen aspirinden 30 Belge Takip Adresi:https://www.turkiye.gov.tr/saglik-titck-ebysBelge Do dakika önce uygulandığında daha yüksek [%98,7'ye karşı %87,7] ve naproksenden 30 dakika önce aspirin uygulandığında minimumdur [%98,7'ye karşı %95,4]. Düşük dozda hızlı salımlı aspirin ile günde iki kez 220 mg naproksen uygulamasının ardından (aspirinden 30 dakika önce verilen ilk naproksen dozu), etkileşim 10. gün dozunu takip eden24 saatte minimal olmuştur [%98,7'ye karşı %95,7]. Bununla birlikte, etkileşim 11. gündenaproksenin (arınma) kesilmesinden sonra daha belirgindir [%98,7'ye karşı %84,3] ve 13.günde tamamen normale dönmemiştir [%98,5'e karşı %90,7] (bkz. Bölüm 4.5). Kan basıncıRandomize, çift kör, paralel grup, aktif kontrol denemesinde 6 ay boyunca aralıklı olarak uygulanan sumatriptan + naproksen sodyum 85 mg/500 mg, normotansif yetişkin popülasyonda(n=122) kan basıncını artırmamıştır. Bununla birlikte, hipertansiyon öyküsü olan ve olmayanhastalarda 5-HTı agonistleri ve NSAİİ'ler ile kan basıncında önemli yükselmeler bildirilmiştir. Klinik ÇalışmalarYetişkinlerSumatriptan + naproksen sodyumun yetişkinlerde auralı veya aurasız akut migren tedavisinde etkililiği, karşılaştırma tedavileri olarak plasebo ve sumatriptan + naproksen sodyum 85 mg/500mg'ın her bir aktif bileşenini kullanan (sumatriptan ve naproksen sodyum) 2 randomize, çiftkör, çok merkezli, paralel grup denemesinde gösterilmiştir (Çalışma 1 ve Çalışma 2). Bu 2denemeye kaydedilen hastalar ağırlıklı olarak kadın (%87) ve beyaz (%88) olup, ortalama yaş40'tır (aralık: 18 ila 65 yaş). Hastalara, orta ila şiddetli ağrılı migreni 1 tablet ile tedavi etmeleritalimatı verilmiştir. Dozdan sonraki 2 saat içinde hiçbir kurtarma ilacına izin verilmemiştir.Hastalar, 1 doz çalışma ilacını aldıktan 2 saat sonra baş ağrılarını değerlendirmişlerdir; başağrısı rahatlaması, baş ağrısı şiddetinde orta veya şiddetli ağrıdan hafif veya ağrısız duruma birazalma olarak tanımlanmıştır. Mide bulantısı, fotofobi ve fonofobi ile ilişkili semptomlar dadeğerlendirilmiştir. Baş ağrısı şiddetinde orta veya şiddetli ağrıdan, hafif, orta veya şiddetli ağrıgeri dönüşü olmadan ve doz sonrası 24 saat boyunca kurtarma ilacı kullanılmadan dozdan 2saat sonra baş ağrısı şiddetinde orta veya şiddetli ağrıdan ağrısız duruma azalma, sürekli ağrısızdurum olarak tanımlanmıştır. Çalışma 1 ve 2'nin sonuçları Tablo 4'te özetlenmiştir. Her ikiçalışmada da, tedaviden 2 saat sonra baş ağrısı hafifleyen hastaların yüzdesi, sumatriptan +naproksen sodyum 85 mg/500 mg (%65 ve %57) alan hastalarda plasebo alanlara (%28 ve %29)kıyasla önemli ölçüde daha yüksektir. Ayrıca, doz sonrası 24 saat boyunca diğer ilaçları kullanmadan ağrısız kalan hastaların yüzdesi tek doz sumatriptan + naproksen sodyum 85 mg/500 mg (%25 ve %23) alan hastalar arasındaplasebo (%8 ve %7) veya tek başına sumatriptan (%16 ve %14) veya naproksen sodyum (%10)alanlara kıyasla anlamlı derecede daha yüksek olmuştur.
Tablo 4. Tedaviden sonra 2 saatlik ağrı rahatlaması yaşayan ve sürekli ağrısız durumda olan yetişkin hastaların yüzdesia
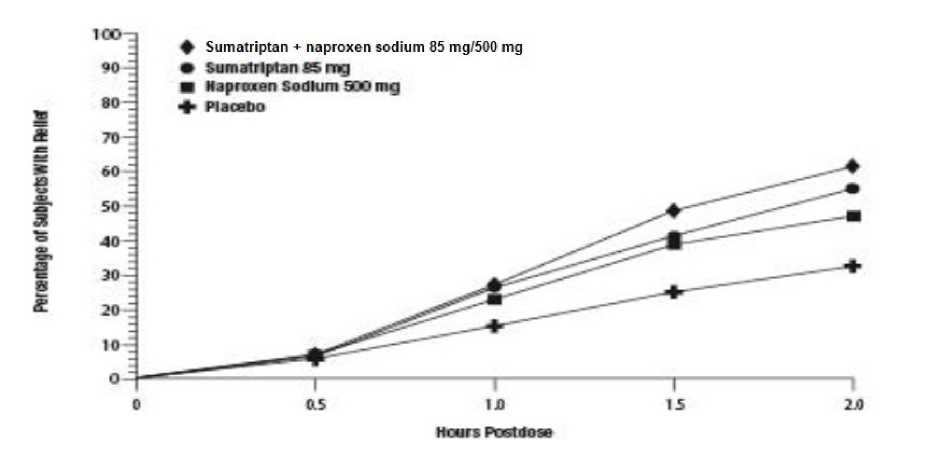
aPcPP<0,01 vs. plasebo, sumatriptan ve naproksen sodyum.Sumatriptan + naproksen sodyum 85 mg/500 mg ile tedaviyi izleyen 2 saat içinde ilk baş ağrısı hafifleyen hastaların yüzdesi Şekil 1'de gösterilmektedir. Şekil 1. 2 saat içerisinde ilk baş ağrısı hafifleyen yetişkin hastaların yüzdesi

Plasebo ile karşılaştırıldığında, sumatriptan + naproksen sodyum 85 mg/500 mg uygulamasından 2 saat sonra fotofobi, fonofobi ve bulantı insidansında azalma olmuştur. İlk 24saatte bir kurtarma ilacı alma olasılığının tahmini Şekil 2'de gösterilmektedir. Şekil 2. İlk dozu takip eden 24 saat içinde bir kurtarma ilacı alan yetişkinlerin tahmini olasılığı^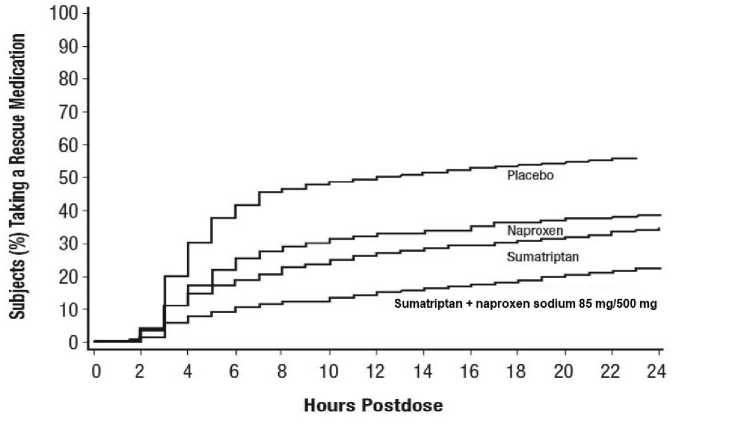 a Kaplan-Meier grafiği, 24 saate kadar sansürlenmiş ek tedavileri kullanmayan hastalarla etkililik kanıtı sağlayan 2 klinik kontrollü çalışmada elde edilen verilere dayanmaktadır. Grafikayrıca ilk doza yanıt vermeyen hastaları da içermektedir. Dozdan sonraki 2 saat içinde hiçbirkurtarma ilacına izin verilmemiştir. Sumatriptan + naproksen sodyum 85 mg/500 mg, auranın varlığına, tedaviden önceki baş ağrısının süresine, deneğin cinsiyeti, yaşı veya kilosuna veya oral kontraseptiflerin veya yaygınmigren profilaktik ilaçlarının (örn. beta blokerler, anti-epileptik ilaçlar, trisiklikantidepresanlar) birlikte kullanımına bakılmaksızın plasebodan daha etkili olmuştur. 12 ila 17 yaş arası pediyatrik hastalarSumatriptan + naproksen sodyumun 12 ila 17 yaşındaki pediyatrik hastalarda auralı veya aurasız akut migren tedavisinde etkililiği, 3 doz sumatriptan + naproksen sodyum ve plaseboyukarşılaştıran randomize, çift kör, çok merkezli, paralel grup, plasebo kontrollü, çok merkezlibir çalışmada gösterilmiştir (Çalışma 3). Bu denemeye kaydedilen hastalar çoğunlukla kadın(%59) ve beyaz (%81) olup, ortalama yaşları 15'tir. Hastaların, tedavi edilmedikleri dönemde genellikle 3 saat veya daha uzun süren auralı veya aurasız en az 6 aylık migren atakları öyküsü olması gerekmektedir. Tek kör, plasebo çalışmaaşamasını takiben, plaseboya yanıt vermeyenler, tek bir sumatriptan + naproksen sodyum 10mg/60 mg, 30 mg/180 mg, 85 mg/500 mg veya plasebo dozu alacak şekilde randomizeedilmiştir. Hastalara orta ile şiddetli derecede baş ağrısı olan tek bir migren atağını tedavietmeleri talimatı verilmiştiin.beDpzdaai esaH^ıfcinz2iiesaıa^aıişi^de hiçbir kurtarma ilacına izin Belge Takip Adresi:https://www.turkiye.gov.tr/saglik-titck-ebysBelge Do verilmemiştir. Hastalar, 1 doz çalışma ilacını aldıktan 2 saat sonra baş ağrılarım değerlendirmişlerdir. Dozdan 2 saat sonra baş ağrısı şiddetinde orta veya şiddetli ağrıdan ağrısızduruma bir azalma iki saatlik ağrısız dönem olarak tanımlanmıştır. Sonuçlar Tablo 5'te özetlenmiştir. Dozdan 2 saat sonra ağrısız olan hastaların yüzdesi, 3 sumatriptan + naproksen sodyum dozundan herhangi birini alan hastalar arasında, plaseboyakıyasla önemli ölçüde daha yüksek olmuştur. Tablo 5. Çalışma 3'te Tedaviden Sonra 2 Saatte Ağrısız Yanıtı olan 12 ila 17 Yaş Arası Pediyatrik Hastaların Yüzdesia
Dozdan 2 ila 24 saat sonra diğer ilaçları kullanmadan ağrısız kalan pediyatrik hastaların yüzdesi, tek doz sumatriptan + naproksen sodyum 85 mg/500 mg uygulamasından sonraplaseboya kıyasla anlamlı ölçüde daha yüksek olmuştur. Tek doz 10 mg/60 mg veya 30 mg/180mg alan pediyatrik hastaların daha büyük bir yüzdesi, plaseboya kıyasla dozdan 2 ila 24 saatsonra ağrısız durumda kalmıştır. Plasebo ile karşılaştırıldığında, 85 mg/500 mg'lık tek bir doz uygulamasından 2 saat sonra fotofobi ve fonofobi insidansı önemli ölçüde azalırken, mide bulantısı insidansı benzerolmuştur. Plaseboya kıyasla 10 mg/60 mg veya 30 mg/180 mg tek doz uygulamasından 2 saatsonra fotofobi, fonofobi ve bulantı insidansında azalma olmuştur. 5.2. Farmakokinetik özelliklerGenel özelliklerEmilim:Sumatriptan, sumatriptan + naproksen sodyum 85 mg/500 mg olarak verildiğinde, tek başına sumatriptan süksinat 100 mg tabletlere benzer bir ortalama Cmax değerine sahiptir. Sumatriptan+ naproksen sodyum 85 mg/500 mg olarak verildiğinde sumatriptanın medyan Tmax değeri,sumatriptan süksinat 100 mg tabletlerden (medyan Tmax 1,5 saat) biraz farklı olarak 1 saattir(aralık: 0,3 ila 4 saat). Sumatriptan + naproksen sodyum 85 mg/500 mg olarak verildiğindenaproksen, naproksen sody&mei550mg etabt©fli®pdefe yakâıaş^r%o36 daha düşük bir C max a ve 5
saatlik bir medyan Tmax'a sahiptir (aralık: 0,3 ila 12 saat), bu da, naproksen sodyum tablet 550 mg'dan yaklaşık 4 saat sonraya denk gelmektedir. Sumatriptan ve naproksen için EAA değerlerisumatriptan + naproksen sodyum 85 mg/500 mg için sumatriptan süksinat 100 mg tablet veyanaproksen sodyum 550 mg tabletle karşılaştırıldığında benzerdir. 16 denekte yapılan çaprazgeçişli bir denemede, sumatriptan + naproksen sodyum 85 mg/500 mg olarak uygulanan her ikibileşenin farmakokinetiği, bir migren atağı sırasında ve migrensiz bir dönemde benzerolmuştur. Sumatriptanın biyoyararlanımı, temel olarak presistemik eliminasyona (ilk geçiş etkisi) ve kısmen de eksik absorpsiyona bağlı olarak yaklaşık %15'tir. Naproksen, %95 in vivobiyoyararlanımı ile gastrointestinal sistemden absorbe edilir.Yiyeceklerin, sumatriptan + naproksen sodyum olarak uygulanan sumatriptan veya naproksenin biyoyararlanımı üzerinde önemli bir etkisi olmamıştır, ancak sumatriptanınTmax'ını yaklaşık 0,6 saat geciktirmiştir. Dağılım:Plazma proteinlerine bağlanma %14 ila %21'dir. Sumatriptanın diğer ilaçların protein bağlanması üzerindeki etkisi değerlendirilmemiştir. Sumatriptanın dağılım hacmi 2,7 L/kg'dır. Naproksenin dağılım hacmi 0,16 L/kg'dır. Tedavi dozlarında naproksenin %99'dan fazlası plazma proteinlerine bağlanır. 500 mg/gün'den daha yüksek naproksen dozlarında, yüksekdozlarda plazma protein bağlanmasının doygunluğundan kaynaklanan klirensteki artışa bağlıolarak plazma seviyelerinde orantısaldan daha az bir artış vardır (ortalama dip değer Css=36,5, 49,2, ve 56,4 mg/L [sırasıyla 500-; 1.000-; ve 1.500-mg'lık günlük naproksen dozları ile]).Bununla birlikte, bağlanmamış naproksen konsantrasyonu, dozla orantılı olarak artmaya devametmektedir. Biyotransformasyon:İnsan mikrozomlarıyla yapılan in vitroçalışmalar, sumatriptanın monoamin oksidaz (MAO), ağırlıklı olarak A izoenzimi tarafından metabolize edildiğini göstermektedir. Bir MAO-Binhibitörü ile önemli bir etki görülmemiştir.Naproksen, büyük ölçüde 6-0-desmetil naproksene metabolize olur ve hem ana hem de metabolitler metabolize edici enzimleri indüklemez. Eliminasyon:Sumatriptanın eliminasyon yarılanma ömrü yaklaşık 2 saattir. Ağızdan uygulanan radyoaktif işaretli 14C-sumatriptan büyük ölçüde renal yoldan atılır (yaklaşık %60), yaklaşık %40'ıdışkıda bulunur. İdrarda atılan radyoaktif işaretli sumatriptan dozunun çoğu, her ikisi de inaktifolan majör metabolit indol asetik asit (IAA) veya IAA glukuroniddir. Dozun yüzde üçü değişmemiş sumatriptan olarakl gefi'fcâzaftllaMlİrza ile imzalanmıştır. Belge Takip Adresi:https://www.turkiye.gov.tr/saglik-titck-ebysBelge Do Naproksen klirensi 0,13 mL/dak/kg'dır. Herhangi bir dozdan alınan naproksenin yaklaşık %95'i idrarla, başlıca naproksen (%1'den az), 6-0-desmetil naproksen (%1'den az) veya bunlarınkonjugatları (%66 ila %92) olarak atılır. İnsanlarda naproksen anyonunun plazma yarılanmaömrü yaklaşık 19 saattir. Naproksenin hem metabolitlerinin hem de konjugatlarmın karşılıkgelen yarılanma ömürleri 12 saatten daha kısadır ve bunların atılma hızlarının, naprokseninplazmadan kaybolma hızıyla yakından tutarlı olduğu bulunmuştur. Böbrek yetmezliği olanhastalarda metabolitler birikebilir. Doğrusallık/doğrusal olmayan durum:Veri bulunmamaktadır. Hastalardaki karakteristik özelliklerYaşlılarGeriatrik hastalarda sumatriptan + naproksen sodyumun farmakokinetiği çalışılmamıştır. Yaşlı hastaların karaciğer fonksiyonlarında azalma ve böbrek fonksiyonlarında azalma olma olasılığıdaha yüksektir. Yaşlılarda (ortalama yaş: 72 yıl, 2 erkek ve 4 kadın) ve migren hastalarında (ortalama yaş: 38 yıl, 25 erkek ve 155 kadın) oral sumatriptanın farmakokinetiği sağlıklı erkek deneklerdekine(ortalama yaş: 30 yıl) benzer olmuştur. Çalışmalar, naproksenin toplam plazma konsantrasyonunun değişmemiş olmasına rağmen, toplam konsantrasyonun <%1'ini temsil eden bağlanmamış plazma fraksiyonunun yaşlılardaarttığını göstermektedir (dip değer naproksen ile bağlanmama aralığı, yaşlı kişilerde %0,12ila %0,19 iken, genç kişilerde %0,05 ila %0,075'tir). PediatriBir farmakokinetik çalışma, 12-17 yaş arası (n=24) pediyatrik hastalarda 3 doz sumatriptan + naproksen sodyumu yetişkinlerle (n=26) karşılaştırmıştır. Sumatriptanın EAA ve Cmax'ı,yetişkin deneklere (n=8) kıyasla 12-17 yaş arası pediyatrik hastalarda (n=7) tek bir sumatriptan+ naproksen sodyum 10 mg/60 mg dozunu takiben %50-60 daha yüksektir ve pediyatrideyetişkinlere göre tek bir sumatriptan + naproksen sodyum 30 mg/180 mg veya 85 mg/500 mgdozunu takiben %6-26 daha yüksektir. Naproksenin farmakokinetik parametreleri pediatri veyetişkinler arasında benzerdir. Böbrek yetmezliğiBöbrek yetmezliğinin sumatriptan + naproksen sodyumun farmakokinetiği üzerindeki etkisi araştırılmamıştır. Naproksen ve metabolitleri ve konjugatları birincil olarak böbrek tarafındanatıldığından, naproksen metabolitlerinin böbrek yetmezliği varlığında birikme potansiyelivardır. Şiddetli böbrek yetmezliği olan hastalarda naproksen eliminasyonu azalır (bkz. Bölüm4.4).
Karaciğer yetmezliğiKaraciğer yetmezliğinin sumatriptan + naproksen sodyumun farmakokinetiği üzerindeki etkisi araştırılmamıştır. Sağlıklı deneklerle (n=8) cinsiyet, yaş ve kilo açısından eşleştirilen ortaderecede karaciğer yetmezliği olan hastalarda (n=8) yapılan bir çalışmada, karaciğer yetmezliğiolan hastalarda sumatriptanın EAA ve Cmax değerlerinde yaklaşık %70 artış görülürken, Tmax,sağlıklı deneklere kıyasla 40 dakika erken olarak kaydedilmiştir. Sumatriptanın şiddetlikaraciğer yetmezliği olan hastalarda farmakokinetiği çalışılmamıştır. Cinsiyet5 farmakokinetik çalışmanın havuzlanmış bir analizinde, sumatriptan + naproksen sodyumun sistemik maruziyeti üzerinde cinsiyetin bir etkisi olmamıştır. IrkIrkın sumatriptan + naproksen sodyumun farmakokinetiği üzerindeki etkisi araştırılmamıştır. Sumatriptanın sistemik klirensi ve Cmax'ı siyah (n=34) ve beyaz (n=38) sağlıklı erkekdeneklerde benzer olmuştur. İlaç Etkileşim ÇalışmalarıAspirinNaproksen, aspirin (>1 gram/gün) ile birlikte uygulandığında, naproksenin proteinlere bağlanması azalmıştır, ancak serbest naproksenin klirensi değişmemiştir. Bir NSAİİ olannaproksenin aspirin ile klinik olarak önemli ilaç etkileşimleri için Tablo 1'e bakınız (bkz. Bölüm4.5). PropranololGünde iki kez verilen propranolol 80 mg, sumatriptan farmakokinetiği üzerinde anlamlı bir etkiye sahip değildir. Bir beta bloker olan propranololün sumatriptan + naproksen sodyum ileklinik olarak önemli ilaç etkileşimleri için Tablo 1'e bakınız (bkz. Bölüm 4.5). 5.3. Klinik öncesi güvenlilik verileriKarsinojenez, Mutajenez, Fertilite BozukluğuKarsinojenezSumatriptan + naproksen sodyumun karsinojenik potansiyeli araştırılmamıştır. Fare ve sıçanlarda yapılan karsinojenisite çalışmalarında, sumatriptan, 160 mg/kg/gün'e kadar olan dozlarda sırasıyla 78 ve 104 hafta süreyle oral olarak uygulanmıştır. Test edilen en yüksekdozlar, mg/m2 bazında 170 mg sumatriptanın maksimum insan günlük dozunun (MHDD)yaklaşık 5 (fare) ve 9 (sıçan) katıdır (24 saatlik periyotta iki tablet sumatriptan + naproksensodyum 85 mg/500 mg). Naproksenin karsinojenik potansiyeli, sıçanlarda 8, 16 ve 24 mg/kg/gün dozlarında 2 yıllık bir oral karsinojenite çalışmasındag,veJırag/tkJi/ıaüna4ozuanadâşs}çanlarda başka bir 2 yıllık oral Belge DtkaırsTnöjeniıevçal^işmasi^da 6^e§e¥fesdi^imiştir. He^ Trkb 4şaiıişmadawd&i'ktümöfijeriiteteikamtı bulunamamıştır. Test edilen en yüksek doz mg/m2 bazında MHDD (1.000 mg) naproksenden daha azdır. MutajenezSumatriptan ve naproksen sodyum tek başına ve kombinasyon halinde test edilmiştir ve in vitroin vivomikronükleus testinde negatif çıkmıştır.Sumatriptan ve naproksen sodyum kombinasyonu, metabolik aktivasyon varlığında ve yokluğunda bir in vitroinvitrofare lenfoma timidin kinaz testi, naproksen sodyum tek başına metabolik aktivasyonvarlığında tekrarlanabilir şekilde pozitif gelmiştir.Tek başına ve sumatriptan ile kombinasyon halinde naproksen sodyum, metabolik aktivasyon varlığında ve yokluğunda memeli hücrelerinde bir in vitroklastojenite testi pozitif çıkmıştır.Kombinasyon için klastojenik etki bu deneyde tekrarlanabilir olmuştur ve tek başına naproksensodyum ile gözlemlenenden daha büyüktür. Sumatriptan tek başına bu testlerde negatiftir.Gönüllü insanlarda sumatriptan + naproksen sodyum ile 7 gün boyunca günde iki kez dozlamanın ardından periferik kan lenfositlerinde kromozomal anormalliklerindüklenmemiştir. Önceki çalışmalarda, sumatriptan tek başına in vitroin vivo(sıçan mikronükleusu) deneylerde negatif gelmiştir.Fertilite BozukluğuSumatriptan + naproksen sodyumun hayvanlarda doğurganlık üzerindeki etkisi araştırılmamıştır. Sumatriptan (5, 50, 500 mg/kg/gün) erkek ve dişi sıçanlara çiftleşme döneminden önce ve bu süre boyunca oral yoldan uygulandığında, 5 mg/kg/gün'den (mg/m2 bazında 170 mgMHDD'den daha az) daha yüksek dozlarla tedavi edilen hayvanlarda çiftleşmedeki azalmayasekonder olarak doğurganlıkta ilaca bağlı bir azalma olmuştur. Bu bulgunun erkek veya kadınüzerindeki bir etkiden mi yoksa her ikisinden mi kaynaklandığı net değildir. Hayvan Toksikolojisi ve/veya FarmakolojisiKornea OpasiteleriOral sumatriptan alan köpekler, kornea epitelinde kornea opasiteleri ve kusurlar geliştirmiştir. Kornea opasiteleri, test edilen en düşük doz olan 2 mg/kg/gün'de görülmüştür ve 1 aylıktedaviden sonra mevcuttur. Kornea epitelindeki kusurlar 60 haftalık bir çalışmadakaydedilmiştir. Bu toksisiteler için daha önceki incelemeler yapılmamıştır ve etkisiz dozlarbelirlenmemiştir. Test edilen en düşük doz, mg/m2 bazında sumatriptanın MHDD'sinden (170mg) daha azdır. Belge Do Belge Takip Adresi:https://www.turkiye.gov.tr/saglik-titck-ebys6. FARMASOTIK ÖZELLİKLER6.1. Yardımcı maddelerin listesiTablet çekirdeğiKalsiyum Hidrojen Fosfat (Susuz) Sodyum Hidrojen Karbonat Mikrokristalin Selüloz (Tip 101) Mikrokristalin Selüloz (Tip 102) Kroskarmelloz Sodyum Povidon (K30) Sodyum Klorür Talk Magnezyum Stearat Film kaplama (Aguarius Preferred HSP BPP317114 Blue)Hidroksipropil Metilselüloz Kopovidon Titanyum Dioksit Polidekstroz Polietilen glikol FD&C Blue 2 Lake (35-42%) FD&C Blue 2 Lake (12-14%) Kaprilik Kaprik Trigliserit 6.2. GeçimsizliklerGeçerli değildir. 6.3. Raf ömrü24 ay 6.4. Saklamaya yönelik özel tedbirler25°C altındaki oda sıcaklığında saklayınız. 6.5. Ambalajın niteliği ve içeriği6 ve 9 film kaplı tablet içeren Alüminyum folyo/Alüminyum folyo blister ambalaj.  6.6. Beşeri tıbbi üründen arta kalan maddelerin imhası ve diğer özel önlemlerKullanılmamış olan ürünler ya da atık materyaller Tıbbi Atıkların Kontrolü Yönetmeliği ve Ambalaj Atıklarının Kontrolü Yönetmeliğine uygun olarak imha edilmelidir. 7. RUHSAT SAHİBİAbdi İbrahim İlaç San. ve Tic. A.Ş. Reşitpaşa Mah. Eski Büyükdere Cad. No:4 34467 Maslak / Sarıyer / İstanbulTel: 0212 366 84 00Faks: 0212 276 20 20 8. RUHSAT NUMARASI2023/361 9. İLK RUHSAT TARİHİ / RUHSAT YENİLEME TARİHİİlk ruhsat tarihi: 10.09.2023 Ruhsat yenileme tarihi: 10. KÜB'ÜN YENİLENME TARİHİ
|
İlaç BilgileriRudista 85 Mg/500 Mg Film Kaplı TabletEtken Maddesi: Sumatriptan, Naproksen Sodyum Kullanma talimatı ve kısa ürün bilgileri
Google Reklamları
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
Ana Sayfa | Hakkımızda | İlaçlar | İlaç Ara | İlaç Firmaları | Gizlilik | Bize Ulaşın
Telif Hakkı 2008-2026 © İlaç Prospektüsü. Tüm Hakları Saklıdır.Uyarı: Sitemizde yayınladığımız ilaç bilgileri ile doktora danışmadan kesinlikle ilaç kullanmayınız!
Aksi halde doğabilecek sağlık sorunlarından ilacprospektusu.com sorumlu tutulamaz.