Augmentin Es 600 Mg+42.9mg/5 Ml Oral Süspansiyon Hazırlamak İçin Kuru Toz Kısa Ürün BilgisiKISA URUN BILGISI1. BEŞERI TIBBİ ÜRÜNÜN ADIAUGMENTİN ES 600 mg+42,9 mg/5 mL oral süspansiyon hazırlamak için kuru toz 2. KALİTATİF VE KANTİTATİF BİLEŞİMEtkin madde:Her 5 ml'de: Amoksisilin..............................600 mg (688,75 mg Amoksisilin trihidrata eşdeğer) Klavulanik asit.........................42,9 mg (51,1 mg Potasyum klavulanata1 eşdeğer) Potasyum klavulanat üretiminde inek sütünden elde edilen hammadde kullanılmaktadır. Yardımcı maddeler:Her 5 ml'de: Aspartam.............................................12,5 mg Çilek kreması aroması (maltodekstrin içermektedir).........................26 mg Yardımcı maddeler için Bölüm 6.1'e bakınız. 3. FARMASÖTİK FORMOral süspansiyon hazırlamak için kuru toz. Serbestçe akabilen, karakteristik çilek kokulu kırık beyaz toz. 4. KLİNİK ÖZELLİKLER4.1. Terapötik endikasyonlarAUGMENTİN ES, lokal resmi antibiyotik reçeteleme kılavuzları ve duyarlılık verilerine uygun olarak kullanılmalıdır. AUGMENTİN ES, pediyatrik hastalarda AUGMENTİN ES'e duyarlı organizmaların yol açtığı bakteriyel enfeksiyonların kısa süreli tedavisinde endikedir. Tipik olarak Staphylococcus aureus*Streptococcuspyogenes'ınneden olduğu deri ve yumuşak doku enfeksiyonları.#Bubakteri türlerinin bazı üyeleri, amoksisiline duyarsız hale gelmelerini sağlayan beta-laktamaz üretirler (bkz. Bölüm 5.1).AUGMENTİN ES'e duyarlılık, coğrafya ve zamana göre değişecektir. Mevcut ise lokal duyarlılık verilerine danışılmalı ve gerektiğinde mikrobiyolojik örnekleme ve duyarlılıktestleri yapılmalıdır. 4.2 Pozoloji ve uygulama şekli Pozoloji/uygulama sıklığı ve süresi:Önerilen AUGMENTİN ES dozu, 10 gün boyunca, 12 saat arayla, ikiye bölünmüş doz halinde verilen 90/6,4 mg/kg/gün'dür (aşağıdaki tabloya bakınız). Ağırlığı 40 kg'ın üzerindeolan pediyatrik hastalar veya yetişkinler üzerinde herhangi bir deneyim yoktur. 3 aylıktanküçük çocuklarda AUGMENTİN ES ile ilgili klinik veri bulunmamaktadır.
AUGMENTİN ES 600+42,9 mg/5 mL oral süspansiyon hazırlamak için kuru toz diğer amoksisilin-klavulanat süspansiyonlarıyla aynı miktarda klavulanik asit (potasyum tuzuolarak) içermez. AUGMENTİN ES 600+42,9 mg/5 mL oral süspansiyon hazırlamak için kurutoz, her 5 ml'de 42,9 mg klavulanik asit içerirken, AUGMENTİN-BID 200/28 mg/5 mL oralsüspansiyon hazırlamak için kuru toz her 5 ml'de 28,5 mg klavulanik asit, AUGMENTİN-BID 400+57 mg/5 mL Fort oral süspansiyon hazırlamak için kuru toz ise her 5 ml'de 57 mgklavulanik asit içerir. Bu nedenle, AUGMENTİN-BID 200+28 mg/5 mL oral süspansiyonhazırlamak için kuru toz ve AUGMENTİN-BID 400+57 mg/5 mL Fort oral süspansiyonhazırlamak için kuru toz, AUGMENTİN ES 600+42,9 mg/5 mL oral süspansiyon hazırlamakiçin kuru toz yerine kullanılmamalıdır çünkü bu ürünler birbirlerinin yerine kullanılamaz. Uygulama şekli:Gastrointestinal intoleransı en aza indirmek için AUGMENTİN ES yemekle birlikte alınmalıdır. Tedavi, gözden geçirilmeden 14 günden fazla uzatılmamalıdır. Tedavi parenteral olarak başlatılıp bir oral preparat ile sürdürülebilir. Kullanmadan önce oral süspansiyon iyice çalkalanmalıdır. Özel popülasyonlara ilişkin ek bilgiler:Böbrek/Karaciğer yetmezliği:Kreatinin klerensi 30 ml/dak veya üzerinde olan çocuklarda doz ayarlamasına gerek yoktur. Kreatinin klerensi 30 ml/dak altında olan çocuklardaAUGMENTİN ES kullanımı tavsiye edilmemektedir.Karaciğer yetmezliğinde doz dikkatli bir şekilde ayarlanmalıdır; karaciğer fonksiyonları düzenli aralıklarla izlenmelidir. Doz önerisinde bulunmaya temel teşkil edecek yeterli veribulunmamaktadır. Pediyatrik popülasyon:Yukarıda belirtilen pozoloji/uygulama sıklığı ve süresi bilgileri pediyatrik popülasyon için geçerlidir. Geriyatrik popülasyon:Uygulanabilir değildir. 4.3. KontrendikasyonlarEtkin maddelere, penisilinlerden herhangi birine ya da bölüm 6.1'de listelenen yardımcı maddelerin herhangi birine aşırı duyarlılığı olanlarda kontrendikedir. AUGMENTİN ES, diğer beta-laktam ajanlara karşı (örn. sefalosporin, karbapenem veya monobaktam) aşırı duyarlılık hikayesi (örn. anafilaksi) olan hastalarda kontrendikedir. AUGMENTİN ES, amoksisilin/klavulanik asit ile ilişkili sarılık/karaciğer fonksiyon bozukluğu geçmişi olan hastalarda kontrendikedir (bkz. Bölüm 4.8). 4.4. Özel kullanım uyarıları ve önlemleriAUGMENTİN ES ile tedaviye başlanmadan önce geçmişinde penisilin, sefalosporin ve diğer beta-laktam ajanlara karşı aşırı duyarlılık hikayesinin varlığı dikkatlice sorgulanmalıdır (bkz.Bölüm 4.3 ve 4.8). Penisilin tedavisi alan hastalarda ciddi ve bazen ölümcül aşırı duyarlılık reaksiyonları (anafilaktoid ve şiddetli kutanöz advers reaksiyonlar dahil) bildirilmiştir. Aşırı duyarlılıkreaksiyonları, miyokard enfarktüsü ile sonuçlanabilecek ciddi bir alerjik reaksiyon olanKounis sendromuna da ilerleyebilir (bkz. Bölüm 4.8). Bu reaksiyonların geçmişinde penisilinekarşı aşırı duyarlılık hikayesi olan ve atopik bireylerde görülmesi daha olasıdır. . İlaca bağlıenterokolit sendromu (DIES) çoğunlukla amoksisilin/klavulanik asit alan çocuklardabildirilmiştir (bkz. Bölüm 4.8). DIES, alerjik deri veya solunum semptomlarının yokluğunda,başlıca semptomu uzun süreli kusma (ilaç uygulamasından 1 -4 saat sonra) olan alerjik birreaksiyondur. Diğer semptomlar karın ağrısı, diyare, hipotansiyon veya nötrofili ile birliktelökositozdan oluşabilir. Şoka kadar ilerleyen ciddi vakalar görülmüştür. Alerjik bir reaksiyonmeydana gelmesi halinde, AUGMENTİN ES tedavisi kesilmeli ve uygun alternatif tedaviyebaşlanmalıdır. Bir enfeksiyonunun amoksisiline duyarlı organizma/organizmalara bağlı olduğu kanıtlanırsa, resmi kılavuzlara göre amoksisilin/klavulanik asitten amoksisiline geçiş göz önündebulundurulmalıdır. Böbrek fonksiyonunda bozukluk olan veya yüksek dozlar alan hastalarda konvülsiyonlar görülebilir (bkz. Bölüm 4.8). Amoksisilin kullanımını takiben görülen kızamık benzeri döküntü enfeksiyöz mononükleoz ile ilişkili olabileceğinden eğer enfeksiyöz mononükleoza ilişkin bir şüphe var iseAUGMENTİN ES tedavisinden kaçınılmalıdır. Amoksisilin ile tedavi sırasında eşzamanlı allopurinol kullanımı alerjik deri reaksiyonları olasılığını artırabilir. Uzun süreli kullanım bazen duyarlı olmayan organizmaların aşırı üremesi ile sonuçlanabilir. Tedavinin başında püstüllerle birlikte ateşli bir genel eritemin oluşması akut jeneralize eksantematöz püstülozun (AGEP) bir semptomu olabilir (bkz. Bölüm 4.8). Bu reaksiyonAUGMENTİN ES'in bırakılmasını gerektirir ve daha sonraki amoksisilin kullanımıkontrendike hale gelir. Amoksisilin/klavulanik asit karaciğer fonksiyon bozukluğu bulgusu olan hastalarda dikkatle kullanılmalıdır (bkz. Bölüm 4.2, 4.3 ve 4.8). Karaciğer olayları daha çok erkeklerde ve yaşlı hastalarda bildirilmiştir ve uzun süreli tedaviyle ilişkili olabilir. Bu olaylar çocuklarda nadiren bildirilmiştir. Tüm popülasyonlardabelirti ve semptomlar, genellikle tedavi sırasında ya da tedaviden kısa süre sonra ortaya çıkarancak bazı olgularda tedavinin kesilmesinin ardından birkaç haftaya kadar belirgin halegelmeyebilir. Bunlar genellikle geri dönüşlüdür. Hepatik olaylar ciddi olabilir ve son derecenadir koşullarda ölümler bildirilmiştir. Bunlar hemen her zaman altta yatan ciddi hastalığıolanlarda ya da eşzamanlı olarak karaciğer üzerinde etkili olma potansiyeli bilinen ilaçlarıkullananlarda meydana gelmiştir (bkz. Bölüm 4.8). Amoksisilin dahil neredeyse tüm antibakteriyel ajanlarla, antibiyotiğe bağlı kolit bildirilmiştir ve şiddeti, hafiften yaşamı tehdit edici boyuta kadar uzanabilir (bkz. Bölüm 4.8). Bu sebeple,herhangi bir antibiyotik tedavisi sırasında veya sonrasında ishal olan hastalarda bu teşhisindeğerlendirilmesi önemlidir. Antibiyotiğe bağlı kolit gözlendiğinde, amoksisilin/klavulanikasit tedavisi derhal kesilmeli, bir doktor tarafından değerlendirilmeli ve uygun tedavibaşlatılmalıdır. Bu durumda anti-peristaltik ilaçlar kontrendikedir. Uzun süreli tedavi sırasında böbrek, karaciğer fonksiyonları ve hematopoetik fonksiyonlar dahil olmak üzere organ sistemi fonksiyonlarının periyodik olarak değerlendirilmesi tavsiyeedilir. Amoksisilin/klavulanik asit alan hastalarda protrombin zamanında uzama nadiren bildirilmiştir. Antikoagülanlar ile birlikte reçete edildiğinde uygun şekilde izlenmesi gerekir.İstenilen antikoagülasyon düzeyini sürdürebilmek için oral antikoagülan dozunda ayarlamayapılması gerekebilir (bkz. Bölüm 4.5 ve 4.8). Azalmış idrar çıkışı olan hastalarda, özellikle parenteral tedavide çok seyrek olarak kristalüri (akut renal hasarı da içeren) görülmüştür. Yüksek doz amoksisilin tedavisi sırasında,amoksisilin kristalüri olasılığını azaltmak için uygun miktarda sıvı alınması ve idrarmiktarının düzenlenmesi tavsiye edilebilir. Mesane kateterleri olan hastalarda düzenli açıklıkkontrolü sürdürülmelidir (bkz. Bölüm 4.8 ve 4.9). Amoksisilinle tedavi sırasında idrarda glukozun arandığı testler yapıldığında, enzimatik glukoz oksidaz yöntemleri kullanılmalıdır, çünkü enzimatik olmayan yöntemlerde yalancı pozitifsonuçlar görülebilir. AUGMENTİN ES içindeki klavulanik asit varlığı, kırmızı hücre membranlarınca IgG ve albüminin spesifik olmayan bağlanmasına neden olarak yalancı pozitif Coombs testine yolaçabilir. Amoksisilin/klavulanik asit alan ve daha sonra AspergillusAspergillusAspergillusAspergillus-dışıpolisakkaridler ve polifuranozlar arasında çapraz reaksiyonlar bildirilmiştir.Bu nedenle amoksisilin/klavulanik asit alan hastalardaki pozitif test sonuçları dikkatliyorumlanmalı ve başka tanı yöntemleriyle doğrulanmalıdır.AUGMENTİN ES aspartam içerir. Fenilketonürisi olan insanlar için zararlı olabilir. AUGMENTİN ES formülasyonunda yer alan tatlandırıcılar maltodekstrin (glukoz) içerir. Nadir glukoz-galaktoz malabsorpsiyon hastalığı olan hastaların bu ilacı kullanmamaları gerekir. 4.5. Diğer tıbbi ürünler ile etkileşim ve diğer etkileşim şekilleriOral antikoagülanlarOral antikoagülanlar ve penisilin antibiyotikleri etkileşim raporları alınmaksızın uygulamada yaygın olarak kullanılmıştır. Bununla birlikte literatürde asenokumarol veya varfarinle idameettirilen ve bir amoksisilin kürü reçete edilen hastalarda artmış uluslararası normalize oran(INR) vakaları mevcuttur. Eşzamanlı uygulama gerekli ise, protrombin zamanı veyauluslararası normalize oran (INR) amoksisilin ilavesi veya kesilmesi durumunda dikkatliceizlenmelidir. Ayrıca, oral antikoagülanların dozunda ayarlamalar da gerekli olabilir (bkz.Bölüm 4.4 ve 4.8). MetotreksatPenisilinler metotreksatın atılımını azaltabilir ve bu da toksisitede potansiyel bir artışa neden olur. ProbenesidProbenesid ile birlikte kullanımı önerilmemektedir. Probenesid amoksisilinin renal tübüler sekresyonunu azaltır. Probenesidin AUGMENTİN ES ile birlikte kullanımı amoksisilinin kanseviyelerinin artışına ve kanda bulunma süresinin uzamasına neden olabilirken, klavulanatı etkilemez. Mikofenolat mofetilMikofenolat mofetil alan hastalarda, oral amoksisilin artı klavulanik asit başlatılmasını takiben aktif metabolit mikofenolik asidin doz öncesi konsantrasyonunda yaklaşık %50'lik birazalma bildirilmiştir. Doz öncesi düzeydeki değişim, genel mikofenolik asit maruziyetindekideğişimleri doğru şekilde temsil etmeyebilir. Bu nedenle, mikofenolat mofetil dozunda birdeğişiklik normalde klinik greft fonksiyon bozukluğu kanıtı yokluğunda gerekli olmayacaktır.Öte yandan, kombinasyon sırasında ve antibiyotik tedavisinden kısa süre sonra yakın kliniktakip yürütülmelidir. AllopurinolAmoksisilin tedavisi sırasında allopurinol kullanımı alerjik cilt reaksiyonları olasılığını artırabilir. Allopurinol ve AUGMENTİN ES'in birlikte kullanımına ait veri yoktur. Oral kontraseptiflerDiğer antibiyotiklerde de olduğu gibi AUGMENTİN ES, bağırsak florasını etkileyebilir, östrojen reabsorpsiyonunun azalmasına yol açar ve kombine oral kontraseptiflerin etkililiğiniazaltır. Özel popülasyonlara ilişkin ek bilgilerEtkileşim çalışması yapılmamıştır. Veri bulunmamaktadır. Pediyatrik popülasyon:Etkileşim çalışması yapılmamıştır. Yukarıda verilen bilgiler pediyatrik popülasyon için geçerlidir. 4.6. Gebelik ve laktasyonGenel tavsiyeGebelik Kategorisi: B Çocuk doğurma potansiyeli bulunan kadınlar/Doğum kontrolü (Kontrasepsiyon)Diğer antibiyotiklerde de olduğu gibi AUGMENTİN ES, bağırsak florasını etkileyebilir, östrojen reabsorpsiyonunun azalmasına yol açar ve kombine oral kontraseptiflerin etkililiğiniazaltır. Bu nedenle tedavi süresince alternatif, etkili ve güvenilir bir doğum kontrol yöntemiuygulanmalıdır. Gebelik dönemiHayvan çalışmaları gebelik, embriyonal/fetal gelişim, doğum veya postnatal gelişim açısından doğrudan ya da dolaylı zararlı etkilere işaret etmemektedir (bkz. Bölüm 5.3). İnsanlardagebelik sırasında amoksisilin/klavulanik asit kullanımına ilişkin kısıtlı veriler artmışkonjenital malformasyonlar riskine işaret etmemektedir. Preterm, prematüre fetal membranrüptürü görülen kadınlarda yürütülen tekli bir çalışmada, amoksisilin/klavulanik asit ileprofilaktik tedavinin neonatlarda artmış nekrotizan enterokolit riski ile ilişkili olabileceğibildirilmiştir. Hekim tarafından zorunlu bulunmadıkça gebelik sırasında kullanımdankaçınılmalıdır. Gebe kadınlara verilirken dikkatli olunmalıdır. Oral ve parenteral yolla verildiği hayvanlar (fare ve sıçanlara insanlarda uygulanan dozun 10 katı dozda) üzerinde yapılan reprodüktif çalışmalarda, AUGMENTİN ES teratojenik etkigöstermemiştir. Tüm ilaçlarda olduğu gibi, doktor tarafından gerekli görülmedikçe gebelik esnasında özellikle gebeliğin ilk üç ayında kullanılmamalıdır. LaktasyonAUGMENTİN ES'in iki etkin maddesi de anne sütüne geçer (klavulanik asitin anne sütü alan süt çocukları üzerindeki etkisi ile ilgili herhangi bir bilgi yoktur). Dolayısıyla anne sütüylebeslenen süt çocuklarında ishal ve mukoz mebranlarda mantar enfeksiyonu olasılığı vardır,bu nedenle emzirmenin kesilmesi gerekebilir. Sensitizasyon olasılığı göz önüne alınmalıdır.Emzirme döneminde amoksisilin/klavulanik asit sadece tedaviyi uygulayan hekiminfayda/risk değerlendirmesinden sonra kullanılmalıdır. Üreme yeteneği/Fertilite1,200 mg/kg/güne varan oral dozlarda (vücut yüzey alanı temelinde maksimum yetişkin insan dozunun 5.7 katı) AUGMENTİN ES'in, 2:1 oranında amoksisilin:klavulanat formülasyonu iledozlanmış sıçanlarda fertilite ve üreme performansı üzerinde etkisi olmadığı tespit edilmiştir. 4.7. Araç ve makine kullanımı üzerindeki etkilerAUGMENTİN ES'in araç ve makine kullanımı üzerindeki etkileriyle ilgili bir çalışma gerçekleştirilmemiştir. Ancak, hastalar araç ve makine kullanımını etkileyebilecek istenmeyenetkiler (örn. alerjik reaksiyonlar, sersemlik hali, konvülsiyonlar) oluşabileceği ile ilgilibilgilendirilmelidir (bkz. Bölüm 4.8). 4.8. İstenmeyen etkilerEn çok raporlanan istenmeyen etkiler diyare, bulantı ve kusmadır. AUGMENTİN ile yapılan klinik çalışmalardan ve pazarlama sonrası gözetimden elde edilen ve MedDRA sistem organ sınıfına göre ayrılan advers ilaç reaksiyonları aşağıdalistelenmektedir. İstenmeyen etkilerin meydana gelme sıklıklarına göre sınıflandırılması için aşağıdaki terminolojiler kullanılmıştır: Çok yaygın > 1/10 Yaygın > 1/100 ila < 1/10 Yaygın olmayan > 1.000 ila < 1/100 Seyrek > 1/10.000 ila < 1/1.000 Çok seyrek < 1/10.000 Bilinmiyor (mevcut verilerden hareketle tahmin edilemiyor) Enfeksiyonlar ve enfestasyonlarYaygın: Mukokutanöz kandidiazis Bilinmiyor: Duyarlı olmayan organizmaların aşırı çoğalması Kan ve lenf sistemi hastalıklarıSeyrek: Geri dönüşümlü lökopeni (nötropeni dahil) ve trombositopeni. Bilinmiyor: Geri dönüşümlü agranülositoz, hemolitik anemi, kanama ve protrombin zamanında uzama1 Bağışıklık sistemi hastalıklarıBilinmiyor: Anjiyonörotik ödem9, anafilaksi9, serum hastalığı benzeri sendrom9, aşırı duyarlılık vasküliti9, Sinir sistemi hastalıklarıYaygın olmayan: Baş ağrısı, baş dönmesi Bilinmiyor: Geri dönüşümlü hiperaktivite, konvülsiyonlar1, aseptik menenjit. Kalp hastalıkları
Kounis sendromu
Bilinmiyor: Gastrointestinal hastalıklarYaygın: Diyare, bulantı2, kusma. Yaygın olmayan: Sindirim güçlüğü Bilinmiyor: Antibiyotiğe bağlı kolit3, ilaca bağlı enterokolit sendromu, akut pankreatit siyah tüylü dil (dildeki papillaların belirginleşip siyah renk alması), dişte renk değişikliği4 Hepato-bilier hastalıklarYaygın olmayan:AST ve/veya ALT5'da artış Bilinmiyor: Hepatit6 ve kolestatik sarılık6 Hepatik olaylar daha çok erkeklerde ve yaşlı hastalarda bildirilmiştir ve uzun süreli tedaviyle ilişkili olabilir. Bu olaylar çocuklarda nadiren bildirilmiştir. Tüm popülasyonlarda belirti vesemptomlar, genellikle tedavi sırasında ya da tedaviden kısa süre sonra ortaya çıkar ancakbazı olgularda tedavinin kesilmesinin ardından birkaç haftaya kadar belirgin halegelmeyebilir. Bunlar genellikle geri dönüşlüdür. Hepatik olaylar ciddi olabilir ve son derecenadir koşullarda ölümler bildirilmiştir. Bunlar hemen her zaman altta yatan ciddi hastalığıolanlarda ya da eşzamanlı olarak karaciğer üzerinde etkili olma potansiyeli bilinen ilaçlarıkullananlarda meydana gelmiştir. Deri ve deri altı doku hastalıkları7Yaygın olmayan: Deride döküntü, kaşıntı, ürtiker Seyrek: Eritema multiforme Bilinmiyor: Stevens-Johnson sendromu, toksik epidermal nekrolizis, bülloz döküntülü dermatit, akut generalize ekzantemöz püstüller (AGEP)1, eozinofili ve sistemik semptomlarıneşlik ettiği ilaç reaksiyonu (DRESS), linear IgA rahatsızlığı . Böbrek ve idrar yolu hastalıkları:Bilinmiyor: İnterstisyel nefrit, kristalüri (akul renal hasarı da içeren)8 (bkz. Bölüm 4.9). 1 bkz. Bölüm 4.4 4Çocuklarda çok nadir olarak yüzeysel dişte renk değişikliği bildirilmiştir. Genellikle fırçalama ile giderilebildiğinden, iyi bir ağız hijyeni dişte renk değişimini önlemeye yardımcıolabilir. 6Bu olaylar diğer penisilinler ve sefalosporinler ile not edilmiştir (bkz. Bölüm 4.4). 8bkz. Bölüm 4.9 9bkz. Bölüm 4.3 ve 4.4 Şüpheli advers reaksiyonların raporlanmasıRuhsatlandırma sonrası şüpheli ilaç advers reaksiyonlarının raporlanması büyük önem taşımaktadır. Raporlama yapılması, ilacın yarar / risk dengesinin sürekli olarak izlenmesineolanak sağlar. Sağlık mesleği mensuplarının herhangi bir şüpheli advers reaksiyonu TürkiyeFarmakovijilans Merkezi (TÜFAM)'ne bildirmeleri gerekmektedir. (www.titck.gov.tr; e-posta: [email protected]; tel: 0 800 314 00 08; faks: 0 312 218 35 99) 4.9. Doz aşımı ve tedavisiDoz aşımı semptomları ve belirtileriGastrointestinal semptomlar ve sıvı ve elektronik dengesi bozuklukları belirgin olabilir. Bazı durumlarda böbrek yetmezliğine yol açan amoksisilin kristalürisi gözlenmiştir (bkz. Bölüm 4.4) . Böbrek fonksiyonu bozulmuş hastalarda ve yüksek dozları alanlarda konvülsiyonlar meydana gelebilir. Amoksisilinin ağırlıklı olarak büyük dozlarının intravenöz uygulanmasından sonra mesane kateterlerinde çöktüğü bildirilmiştir. Düzenli açıklık kontrolü sürdürülmelidir (bkz. Bölüm 4.4) . İntoksikasyon tedavisiGastrointestinal semptomlar su/elektrolit dengesine dikkat edilerek semptomatik olarak tedavi edilebilir. Amoksisilin/klavulanik asit dolaşımdan hemodiyaliz ile uzaklaştırılabilir. 5. FARMAKOLOJIK ÖZELLIKLER5.1. Farmakodinamik özelliklerFarmakoterapötik grup: Beta laktamaz inhibitörlerini de içeren penisilin kombinasyonları ATC kodu: J01CR02 Etki mekanizmasıAmoksisilin bakteriyel hücre duvarının bütünleyici bir yapısal bileşeni olan biyosentetik bakteriyel peptidoglikan yolağındaki bir ya da daha fazla enzimi (sıklıkla penisilin bağlayanproteinler, PBP'ler olarak adlandırılan) inhibe eden yarı sentetik bir penisilindir (beta-laktamantibiyotik). Peptidoglikan sentezinin inhibisyonu genellikle hücre duvarının zayıflamasınayol açar ki bunu genellikle hücre lizisi ve ölüm izler. Amoksisilin dirençli bakterilerin ürettiği beta-laktamazlarla parçalanmaya duyarlıdır ve bu nedenle tek başına amoksisilinin aktivite spektrumu bu enzimleri üreten organizmalarıiçermez. Klavulanik asit yapısal olarak penisilinlerle ilişkili bir beta-laktamdır. Bazı beta-laktamaz enzimlerini inaktive ederek amoksisilinin inaktivasyonunu önler. Tek başına klavulanik asitklinik açıdan faydalı antibakteriyel etki göstermez. Farmakokinetik/farmakodinamik ilişkisiMinimum inhibe edici konsantrasyon üzerindeki süre (T>MİK) amoksisilin için ana etkililik belirleyici etken olarak kabul edilir. Direnç mekanizmalarıAmoksisilin/klavulanik aside direnç için başlıca iki mekanizma mevcuttur: Sınıf B, C ve D dahil kendileri klavulanik asit ile inhibe olmayan bakteriyelbeta-laktamazlar ile inaktivasyon. Hedef için antibakteriyel ajanın afinitesini azaltan, PBP'lerde değişiklik Bakterilerin veya atım pompası mekanizmalarının geçirmezliği özellikle Gram-negatif bakterilerde bakteriyel dirence neden olabilir veya katkıda bulunabilir. Kesim noktalarıAmoksisilin/klavulanik asit için MİK kesim noktaları, Avrupa Antimikrobiyal Duyarlılık Testi (EUCAST) kesim noktalarıdır.
Moraxella catarrhalis
1
1
1 Pasteurella multocida
11
1 Burkholderia pseudomallei
0.0011
8
21
8
Türlerle ilişkili olmayan kesim noktaları 1 Duyarlılık testi amacına yönelik olarak, klavulanik asit konsantrasyonu 2 mg/L'ye sabitlenmiştir. 2 Çoğu S. aureuspenisilinaz üretir ve bazıları metisiline dirençlidir. Her iki mekanizma da onlarıbenzilpenisilin, fenoksimetilpenisilin, ampisilin, amoksisilin, piperasilin ve tikarsilin'e dirençli kılar.Testte benzilpenisilin ve sefoksitine duyarlı bulunan stafilokoklar, tüm penisilinlere duyarlı olarakbildirilebilir. Benzilpenisiline dirençli ancak sefoksitine duyarlı olan stafilokoklar, beta-laktamazinhibitörü kombinasyonlarına, izoksazolilpenisilinlere (oksasilin, kloksasilin, dikloksasilin veflukloksasilin) ve nafsiline duyarlıdır. Oral olarak verilen ajanlar için, enfeksiyon bölgesinde yeterlimaruziyetin sağlanmasına özen gösterilmelidir. Sefoksitine dirençli olan izolatlar tüm penisilinleredirençlidir.3 Stafilokokların çoğu penisilinaz üretirler ve bazıları metisiline dirençlidir. Her iki mekanizma daonları benzilpenisilin, fenoksimetilpenisilin, ampisilin, amoksisilin, piperasilin ve tikarsilin'e dirençlikılar. Güncel olarak hiçbir yöntem, tüm stafilokok türlerinde penisilinaz üretimini güvenilir birşekilde saptayamamaktadır, ancak yukarıda söz edildiği üzere gibi sefoksitin ile metisilin direncisaptanabilir. 4 Ampisiline duyarlı S. saprophyticusmecA-negatiftir ve ampisilin, amoksisilin ve piperasilineduyarlıdırlar (beta-laktamaz inhibitörlü veya bir beta-laktamaz inhibitörü olmadan).5 Enterokoklardaki aminopenisilin kesim noktaları, intravenöz uygulamaya dayanmaktadır. Oraluygulama sadece üriner sistem enfeksiyonlarında geçerlidir 6 Ampisilin, amoksisilin ve piperasilin duyarlılığı (beta-laktamaz inhibitörlü veya bir beta-laktamazinhibitörü olmadan) çıkarımı ampisilin temel alınarak yapılabilir. Ampisiline direnç E. faecalis'teE. faecium'dayaygındır.7Beta-laktamaz inhibitörü eklenmesi ek klinik yarar sağlamaz. 8 Streptokok grup A, B, C ve G'nin penisiline duyarlılığı çıkarımında, benzilpenisiline duyarlılıktemel alınmaktadır (menenjit dışındaki endikasyonlarda) ancak streptokok grup B içinfenoksimetilpenisilin ve izoksazolpenisilin buna istisnadır. 9 Benzilpenisilin (MİK veya disk difüzyon), viridans grubu streptokoklarda beta-laktam direncinitaramak için kullanılabilir. Tarama negatif olarak kategorize edilen izolatların, klinik kesimnoktalarının listelendiği beta-laktam ajanlara duyarlı olduğu bildirilebilir (Not ile bildirilenlerdahil). Tarama pozitif olarak sınıflandırılan izolatlar, her bir ajana duyarlılık açısından testedilmelidir. 10 Benzilpenisilin taraması negatif izolatlar için (inhibisyon zonu >18 mm ya da MİK <0.25 mg/L), benzilpenisilin veya ampisilin temel alınarak duyarlılık çıkarımı yapılabilir. Benzilpenisilin taraması pozitif izolatlar için (inhibisyon zonu <18 mm ya da MİK >0.25 mg/L), duyarlılık çıkarımı için ampisilin temel alınır._Direnç prevalansı seçili türler için coğrafik açıdan ve zamanla çeşitlilik gösterebilir ve dirence ilişkin yerel bilgiler özellikle şiddetli enfeksiyonlar tedavi edilirken arzu edilir. Gerektiğindeyerel direnç prevalansı enfeksiyonların en azından bazı tiplerinde ajanın faydasından şüpheedilmesine yol açacak şekilde olduğunda uzman tavsiyesi alınmalıdır. Genellikle duyarlı türlerAerobik Gram-pozitif mikroorganizmalarStaphylococcus aureus(metisiline duyarlı)$Streptococcus pneumoniae^Streptococcuspyogenesve diğer beta hemolitik streptokoklarAerobik Gram-negatif mikroorganizmalarHaemophilus influenzae2Moraxella catarrhalisMoraxella catarrhalisEdinilmiş direncin bir sorun oluşturabileceği türlerAerobik Gram-negatif mikroorganizmalarKlebsiella pneumoniaeDoğası gereği dirençli organizmalarAerobik Gram-negatif mikroorganizmalarLegionella pneumophilaDiğer mikroorganizmalarChlamydophila pneumoniaeChlamydophila psittaciCoxiella burnetiiMycoplasma pneumoniae
$ Metisiline dirençli tüm stafilokoklar amoksisilin/klavulanik asite dirençlidir. 1 Yalnızca onaylı endikasyonlarda penisiline dirençli olan Streptococcus pneumoniae 'ninamoksisilin/klavulanik asitin bu sunumuyla tedavisi uygundur (bkz. Bölüm 4.1).2Bazı AB ülkelerinde duyarlılığı azalmış suşlar, %10'dan daha yüksek bir sıklıkta bildirilmiştir. 5.2. Farmakokinetik özelliklerGenel özelliklerEmilim:AUGMENTİN ES'in her iki bileşeni, hem amoksisilin hem de klavulanik asit, fizyolojik pH'da sulu çözeltilerde tamamen ayrışırlar. İki bileşen de oral uygulama sonrası hızla ve iyiabsorbe olur. Oral uygulamayı takiben amoksisilin ve klavulanik asit yaklaşık %70 oranındaserumda serbest halde bulunur. Her iki bileşenin plazma profilleri benzer olmakla birlikte, pikplazma konsantrasyonlarına ulaşma süresi (Tmaks) her durumda yaklaşık bir saattir. Aşağıda, pediyatrik hastalara her 12 saatte bir 45 mg/3,2 mg/kg olarak uygulanan AUGMENTİN ES için farmakokinetik parametreler yer almaktadır.
Amoksisilin/klavulanik asit ile elde edilen amoksisilin ve klavulanik asit serum konsantrasyonları, amoksisilin ve klavulanik asitin tek başlarına oral yolla verilişi ile eldeedilen konsantrasyonlarla benzerlik göstermektedir. Dağılım:Toplam plazma klavulanik asitinin %25 ve toplam plazma amoksisilinin %18 kadarı proteine bağlanır. Görünürdeki dağılım hacmi amoksisilinde 0,3-0,4 L/kg ve klavulanik asitte0,2/ L/kg dolayındadır. İntravenöz uygulamadan sonra safra kesesinde, abdominal dokularda, deri, yağ, kas dokularında, sinoviyal ve peritoneal sıvılarda, safra ve iltihapta hem amoksisilin hem deklavulanik asit bulunmuştur. Amoksisilinin beyin omurilik sıvısına dağılımı yeterli değildir. Hayvan çalışmalarında, bileşenlerden herhangi biri için ilaçtan kaynaklanan materyallerle önemli doku tutulumuna ilişkin kanıt yoktur. Penisilinlerin çoğu gibi amoksisilin de annesütünde saptanabilir. Anne sütünde eser miktarda klavulanik asit de saptanabilmektedir (bkz.Bölüm 4.6). Hem amoksisilin hem de klavulanik asitin plasenta bariyerini geçtiği gösterilmiştir (bkz. Bölüm 4.6). Biyotransformasyon:Amoksisilin kısmen idrarla, başlangıç dozunun yaklaşık %10-25'i oranında inaktif penisiloik asit şeklinde atılır. Klavulanik asit insanda büyük oranda metabolize olur, idrar ve feçes içindeve karbondioksit şeklinde hava ile atılır. Eliminasyon:Amoksisilinin başlıca eliminasyon yolu böbreklerdir, buna karşılık klavulanik asit hem renal hem de renal olmayan mekanizmalarla atılır. Amoksisilin/klavulanik asitin ortalama eliminasyon yarılanma ömrü yaklaşık bir saattir ve ortalama total klerens sağlıklı kişilerde yaklaşık 25 L/saattir. 250 mg/125 mg ya da 500mg/125 mg'lık tek bir AUGMENTİN tabletinin uygulanmasından sonraki ilk 6 saatteamoksisilinin yaklaşık %60-70'i ve klavulanik asitin yaklaşık %40-65'i idrarla değişikliğeuğramadan atılır. Çeşitli çalışmalarda, 24 saatlik bir dönemde amoksisilinin idrarla atılımmiktarının %50-85 ve klavulanik asitin %27-60 arasında olduğu bulunmuştur. Klavulanikasitte, ilacın en büyük miktarı uygulamadan sonraki ilk 2 saatte atılmaktadır. Eşzamanlı probenesid kullanılması, amoksisilin atılmasını geciktirmekle birlikte klavulanik asitin böbreklerden atılmasını geciktirmez (bkz. Bölüm 4.5). Hastalardaki karakteristik özelliklerBöbrek yetmezliği:Böbrek işlevinin azalmasıyla doğru orantılı olarak amoksisilin/klavulanik asitin total serum klerensi de azalır. İlaç klerensindeki azalma, amoksisilinin daha büyük bir bölümünün böbrekyoluyla atılması nedeniyle, amoksisilinde klavulanik asitten daha belirgindir. Bu yüzden,böbrek yetmezliğinde dozlar, amoksisilinin fazla birikmesini önlerken, yeterli klavulanik asitdüzeylerinin sürdürülmesini sağlamalıdır (bkz. Bölüm 4.2). Karaciğer yetmezliği:Karaciğer yetmezliği bulunan hastalarda doz dikkatle belirlenmeli ve karaciğer işlevleri düzenli aralıklarla izlenmelidir. Yaş:Amoksisilinin eliminasyon yarılanma ömrü 3 aylıktan 2 yaşına kadar olan çoçuklarda ve daha büyük çocuklarda aynıdır. Yaşamın ilk haftasındaki çok küçük çocuklar için (preterm yenidoğanlar dahil) uygulama aralığı renal eliminasyon yolağının gelişmemiş olmasından dolayıgünde iki kez uygulamayı aşmamalıdır. Yaşlı hastalarda böbrek işlevlerinde azalma olasılığıdaha fazla olduğundan, doz seçiminde dikkatli olunmalıdır ve böbrek işlevinin izlenmesiyararlı olabilir. Cinsiyet:Sağlıklı erkek ve kadınlara oral yoldan amoksisilin/klavulanik asit uygulanmasından sonra cinsiyetin amoksisilin ya da klavulanik asitin farmakokinetikleri üzerinde önemli bir etkisigörülmemiştir. Doğrusallık/Doğrusal olmayan durum:Amoksisilin, terapötik doz aralığında doğrusal farmakokinetiğe sahiptir. 5.3. Klinik öncesi güvenlilik verileriKlinik öncesi veriler, farmakoloji, genotoksisite ve üreme toksisitesi güvenliliğine yönelik çalışmalar temelinde insanlar açısından özel bir tehlike ortaya koymamıştır. Köpeklerde amoksisilin/klavulanik asitle yapılan tekrarlanan doz toksisitesi çalışmalarında, gastrik tahriş, kusma ve dilde renk bozukluğu görülmüştür. Amoksisilin/klavulanik asit ile karsinojenisite çalışmaları yapılmamıştır. 6. FARMASÖTİK ÖZELLİKLER6.1. Yardımcı maddelerin listesiKolloidal silikon dioksit Sodyum karboksimetilselüloz Çilek kreması aroması (içeriğinde maltodekstrin bulunmaktadır) Ksantan sakızı AspartamSilikon dioksit 6.2. GeçimsizliklerBilinen herhangi bir geçimsizliği bulunmamaktadır. 6.3. Raf ömrü24 ay 6.4. Saklamaya yönelik özel tedbirlerOral süspansiyon tozu iyice kapatılmış ambalajı içinde, 25 °C'nin altındaki oda sıcaklığında ve kuru bir yerde saklanmalıdır. Kullanıma hazırlanan süspansiyon buzdolabında (2-8 °C)saklanmalı ve 7-10 gün içinde kullanılmalıdır. 6.5. Ambalajın niteliği ve içeriğiAUGMENTİN ES 600+42,9 mg/5 mL oral süspansiyon hazırlamak için kuru toz, 5 ml'lik 1 adet plastik kaşık ile birlikte 100 ml'lik çocuk korumalı kapak içeren, çıkarılabilir emniyetbandı ile kapatılmış şeffaf cam şişelerde bulunmaktadır. 6.6 Beşeri tıbbi üründen arta kalan maddelerin imhası ve diğer özel önlemler
ve
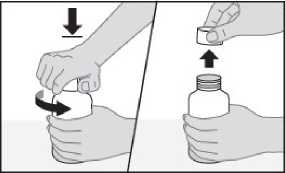
Tüm kullanılmayan ürün ve atık maddeler Tıbbi Atıkların Kontrolü Yönetmeliği" Ambalaj Atıklarının Kontrolü Yönetmeliği" ne uygun olarak imha edilmelidir. AUGMENTİN ES süspansiyonun hazırlanması:AUGMENTİN ES toz halindedir, bu yüzden ilk önce sulandırmak gerekir. AUGMENTİN ES'i sulandırmak için aşağıdaki yönlendirmeleri takip ediniz: Şişe ağzında yer alan emniyet bandının bozulmamış olduğuna emin olunuz. 1) Tüm toz dağılıp serbestçe akana kadar şişeyi sallayınız. 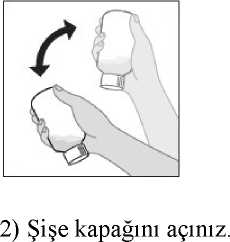
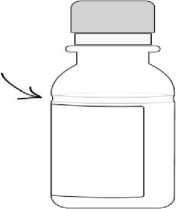
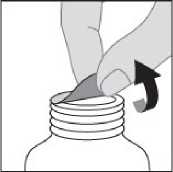 AUGMENTİN ES için sulandırma çizgisi, şişesinin etrafını çevreleyen şeffaf bir girinti şeklinde gösterilmiştir.
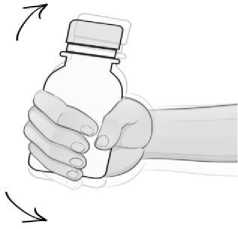
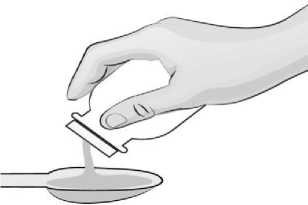
4) AUGMENTİN ES 600+42,9 mg/5 mL oral süspansiyonu hazırlamak için önce şişeüzerindeki sulandırma çizgisinin yaklaşık 2/3'üne denk gelecek kadar su ekleyiniz ve tozusüspansiyon haline getirmek için şişeyi iyice çalkalayınız (Süspansiyon hazırlamak içinönceden kaynatılmış ve soğutulmuş su tercih edilmelidir). 5) İlk sulandırılışta tam bir dağılma sağlamak için 5 dakika dinlendiriniz. 6) Kalan suyu (1/3) şişe üzerindeki sulandırma çizgisine kadar doldurunuz ve şişeyi yenidençalkalayınız (100 mL süspansiyon için toplam 90 mL su ilave edilmelidir).Süspansiyonhazırlamak için önceden kaynatılmış ve soğutulmuş su tercih edilmelidir.7) Doktorunuzun her uygulama için önerdiği miktarda ilacı 5 ml'lik ölçü kaşığını kullanarakhastaya veriniz. Her dozdan önce şişeyi iyice çalkalayınız. Kullanım sonrası şişeyi hemen ve sıkıca kapatınız. AUGMENTİN ES 600+42,9 mg/5 mL oral süspansiyon'un rengi, kullanımı sırasında sararma gösterebilir. Bu durumun ilacın etkililiği üzerinde herhangi bir etkisi yoktur. Eğer AUGMENTİN ES'i 2 yaşından küçük bir çocuğa verecekseniz, süspansiyonu vermeden hemen önce su kullanarak çalkalayıp seyreltebilirsiniz. Seyreltilmiş süspansiyonusaklamayınız. 7. RUHSAT SAHİBİGlaxoSmithKline İlaçları San. ve Tic. A.Ş. Büyükdere Cad. No.173, 1. Levent Plaza B Blok 34394 l.Levent/İstanbulTelefon: 0212 339 44 00Faks: 0212 339 45 00 8. RUHSAT NUMARASI2019/187 9. İLK RUHSAT TARİHİ/RUHSAT YENİLEME TARİHİİlk Ruhsat Tarihi: 27.03.2019 Ruhsat Yenileme Tarihi: 10. KÜB'ÜN YENİLEME TARİHİ1Üst solunum yolu enfeksiyonları (KBB dahil); örneğin: Streptococcus pneumoniaeHaemophilus influenzae1Moraxella catarrhalis1'ten1'tenkaynaklanan nükseden veya kronik ortakulak iltihabı. Böyle hastalar çoğunlukla önceki 3ay içinde akut orta kulak iltihabı için antibiyotik tedavisi almış, 2 yaşında ve daha küçükolan veya kreşe giden hastalardır. Tipik olarak Streptococcus pneumoniae, Haemophilus influenzae1, Moraxella catarrhalis1Streptococcuspyogenes'inneden olduğu tonsillo-farenjit ve sinüzit. Alt solunum yolu enfeksiyonları; örneğin tipik olarak Streptococcus pneumoniae,Haemophilus influenzae1Moraxella catarrhalis^'inneden olduğu lobar pnömoni vebronkopnömoni. |
İlaç BilgileriAugmentin Es 600 Mg+42.9mg/5 Ml Oral Süspansiyon Hazırlamak İçin Kuru TozEtken Maddesi: Amoksisilin, Klavulanik Asit Kullanma talimatı ve kısa ürün bilgileri
Google Reklamları
İlgili İlaçlar |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
Ana Sayfa | Hakkımızda | İlaçlar | İlaç Ara | İlaç Firmaları | Gizlilik | Bize Ulaşın
Telif Hakkı 2008-2026 © İlaç Prospektüsü. Tüm Hakları Saklıdır.Uyarı: Sitemizde yayınladığımız ilaç bilgileri ile doktora danışmadan kesinlikle ilaç kullanmayınız!
Aksi halde doğabilecek sağlık sorunlarından ilacprospektusu.com sorumlu tutulamaz.