Tisseel 2 mL Kullanıma Hazır Enjektör Kısa Ürün BilgisiÇeşitli İlaçlar » Diğer Tüm Terapötik İlaçlar » Diğer Tüm İlaçlar KISA URUN BILGISI 1. BEŞERI TIBBI ÜRÜNÜN ADITISSEEL 2 mL kullanıma hazır enjektör Kullanıma hazır fibrin yapıştırıcı2. KALITATIF VE KANTİTATIF BILEŞIMEtkin madde:Bileşen 1 : Yapıştırıcı protein çözeltisi İnsan fibrinojeni (pıhtılaşabilir protein) 91 mg(1)/mL Aprotinin (sentetik) 3000 KIU(2)/mL Bileşen 2: Trombin çözeltisi İnsan trombini 500 IU1/mL Kalsiyum klorür 40 ^mol/mL (1)(2)allidinogenaz İnaktivatör Ünitesi) ne karşılık gelir.(3)Çift bölmeli enjektör, bölmelerden birinde derin dondurulmuş 1 mL yapıştırıcı protein çözeltisi (sentetik aprotininli), diğerinde ise derin dondurulmuş 1 mL trombin çözeltisi (kalsiyum klorürlü) içerir. Bölmeler içerisindeki çözeltiler karıştırıldığında 2 mL kullanıma hazır çözelti oluşur.Kullanıma hazır 2 mL çözeltinin bileşimi aşağıdaki şekildedir: İnsan fibrinojeni (pıhtılaşabilir protein) 91 mg Sentetik aprotinin 3000 KIU İnsan trombini 500 IU Kalsiyum klorür 40 ^mol TISSEEL 0.6-5 IU/mL kadar insan fibrinojeni ile birlikte saflaştırılmış insan faktör XIII'ü içerir. Yardımcı madde(ler): İnsan Albumini 10-20 mg/mL Polisorbat 80 (Tween 80) 0.6-1.9 mg/mL Yardımcı maddeler için, bkz. 6.1. Derin dondurulmuş durumdaki görünümü:Renksiz ya da soluk sarı renkli ve donmuş opak çözeltilerÇözünmüş durumdaki görünümü:Renksiz ya da soluk sarı renkli berrak çözeltiler4. KLİNİK ÖZELLİKLER 4.1 Terapötik endikasyonlarStandart cerrahi tekniklerin yetersiz kaldığı şu durumların destekleyici tedavisinde endikedir (Bkz. Bölüm 5.1): Daha iyi bir hemostaz sağlanmasında. Vasküler cerrahide, gastrointestinal anastomozlarda, beyin cerrahisi girişimlerinde ve serebro-spinal sıvı veya dura mater ile temas oluşabilen cerrahi girişimlerde (örn., KBB, göz ve omurilik cerrahisinde) sütür desteği ve yara iyileşmesini kolaylaştırmak için doku yapıştırıcı olarak. Ayrılmış dokuların (örn., doku flepleri, greftleri, split skin greftler [mesh greftler]) yapışmasını teşvik ederek doku sızdırmazlığı sağlamak için. Tam heparizasyon yapılmış hastalarda etkinliği kanıtlanmıştır. 4.2. Pozoloji ve uygulama şekliTISSEEL yalnızca bu konuda deneyimli hekimler tarafından kullanılmalıdır.Pozoloji / Uygulama sıklığı ve süresi:Uygulanacak TISSEEL miktarı ve uygulama sıklığı hastanın klinik gereksinimine göre bireysel olarak belirlenmelidir.Uygulanacak dozu, sadece bunlarla sınırlı olmamakla beraber, cerrahi girişimin şekli, alanın büyüklüğü, uygulama şekli ve sayısı belirler. Ürünün uygulanma şekli, tedaviyi uygulayan hekim tarafından bireysel olarak belirlenmelidir. Klinik çalışmalarda 4 ile 20 mL arasında değişen bireysel dozlar kullanılmıştır. Bazı prosedürler (örn., karaciğer travması ya da geniş yanık alanlarının sızdırmazlığının sağlanması için yapılanlar) daha yüksek hacimler gerektirebilir. Tedavi başlangıcında seçilen anatomik alana veya hedef yüzeye uygulanacak ürün miktarı belirlenen alanı tamamen kaplayacak miktarda olmalıdır. Gerekirse uygulama tekrarlanabilir. Ancak TISSEEL polimerize olmuş bir tabakaya yapışmayacağından, daha önceden polimerize olmuş bir TISSEEL tabakası üzerine yeniden uygulanmasından kaçınılmalıdır. Yapıştırılacak yüzeyler için bir rehber olmak üzere 1 kutu TISSEEL 2 mL (1 mL yapıştırıcı protein çözeltisi artı 1 mL trombin çözeltisi) en az 10 cm2 lik bir alan için yeterli olacaktır. TISSEEL spreyleme yöntemiçok daha genişyüzeyleri kaplamak için yeterli olacaktır.Aşırı granülasyon dokusunun oluşumunun önlenmesi ve katılaşmış fibrin yapıştırıcının dereceli absorpsiyonun sağlanması için TISSEEL sadece ince bir tabaka halinde uygulanmalıdır. Uygulama şekli:Epilezyonel kullanım içindir.Uygulamadan önce, uygulanacak yüzey mümkün olduğunca kuru olmalıdır. Ayrıntılı kullanım talimatları için bölüm 6.6'ya bakınız. Minimal fibrin yapıştırıcı kullanımının yeterli olacağı cerrahi işlemlerde ürünün ilk birkaç damlasının uygulama kanülünden atılarak kullanılmaması önerilir. Özel popülasyonlara ilişkin ek bilgiler:Böbrek / Karaciğer yetmezliği:Lokal olarak etki göstermek amacıyla geliştirilmiştir. Böbrek veya karaciğer yetmezliği olan hastalarda dozaj ayarlamasına yönelik bir çalışma bulunmamaktadır.Pediyatrik popülasyon:Çocuklarda ürünün etkinlik ve güvenirliliği gösterilmemiştir. Kullanılacaksa doz erişkinlerdeki gibi cerrahi girişimin şekli, alanın büyüklüğü, uygulama tipi ve sayısına göre uygulamayı yapacak hekim tarafından belirlenmelidir.Geriyatrik popülasyon:Yaşlılarda doz erişkinlerdeki gibi cerrahi girişimin şekli, alanın büyüklüğü, uygulama tipi ve sayısına göre uygulamayı yapacak hekim tarafından belirlenmelidir.4.3. Kontrendikasyonlar TISSEEL'in konvansiyonel cerrahi tekniklerle kontrol edilemeyen aktif veya basınçlı arteriyel veya venöz kanamalarda tek başına kullanımı kontrendikedir. TISSEEL cerrahi yaranın kapatılmasında kullanılan deri sütürlerinin yerine kullanılamaz. TISSEEL, hiçbir şekilde intravasküler olarak uygulanmamalıdır. İntravasküler uygulama yaşamı tehdit eden tromboembolik olaylarla sonuçlanabilir. İçeriğindeki aktif veya yardımcı maddelerden herhangi birisine karşı aşırı duyarlılık durumunda kontrendikedir. 4.4. Özel kullanım uyarıları ve önlemleriSadece epilezyonel kullanım içindir. İntravasküler uygulamayınız.TISSEEL'in kazayla intravasküler olarak uygulanması durumunda yaşamı tehdit eden tromboembolik olaylar gelişebilir. Fibrin yapıştırıcıları basınçlı gaz ile kullanırken dikkatli olunmalıdır. Basınçlı gaz kullanılarak yapılan herhangi bir uygulamada yaşamı tehdit edebilecek boyutlarda hava ve gaz embolisi, doku yırtılması veya kompresyona neden olan gaz sıkışması riski bulunmaktadır. TISSEEL kapalı vücut boşlukları içinde Easy Sprey / Sprey Seti sistemleri ile kullanılmamalıdır. TISSEEL yalnızca gözle görülebilen uygulama alanlarında spreyleme yöntemiyle kullanılmalıdır. TISSEEL ince bir tabaka oluşturacak şekilde uygulanmalıdır. Fazla pıhtı kalınlığı ürünün etkinliğini ve yara iyileşmesi sürecini olumsuz etkileyebilir. TISSEEL uygulaması için basınç regülatörü içeren sprey cihazlarının kullanımı ile hava veya gaz embolisi vakaları bildirilmiştir. Bu olayların sprey cihazının önerilen basınçlardan daha yüksek basınçta ve doku yüzeyine yakın olarak kullanımıyla ilişkili olduğu düşünülmektedir. TISSEEL'i sprey cihazı kullanarak uygularken, kullanılacak basınç düzeyi sprey cihazı üreticisi tarafından önerilen basınç aralığı dahilindeki olmalıdır. Diğer üreticiler tarafından, TISSEEL kullanımı için ruhsatlandırılmamış olan cihazlarla sprey uygulaması yapılmaması konusunda dikkatli olunmalıdır. Özel bir öneri bulunmaması halinde 1.4.1.7 bar'ın üzerinde basınç kullanımından kaçınılmalıdır. Özel bir öneri bulunmaması halinde TISSEEL doku yüzeyine 10-15 cm'den daha yakın bir mesafeden püskürtülmemelidir. TISSEEL'i spreyle uygularken hava veya gaz embolisi oluşma ihtimali nedeniyle kan basıncındaki değişiklikler, nabız, oksijen saturasyonu ve end tidal CO2 düzeyleri izlenmelidir. İstenmeyen vücut bölgelerdeki doku yapışıklıklarının önlenmesi için, TISSEEL uygulamasından önce uygulama için belirlenen alanın dışındaki vücut bölgelerinin yeteri kadar korunduğu / örtüldüğünden emin olunmalıdır. Fibrin yapıştırıcıların beyin ve spinal kord gibi kapalı alanların içinde uygulandığı durumlarda basınca bağlı komplikasyon riski dikkate alınmalıdır. Yapıştırıcı protein bileşeniyle trombin bileşeninin uygun bir şekilde karıştığından emin olmak için ürünün ilk birkaç damlasının kullanımdan hemen önce uygulama kanülünden atılması önerilir. Herhangi bir protein ürününde olduğu gibi, alerjik tipte aşırı duyarlılık reaksiyonları mümkündür. İntravasküler uygulama, duyarlı hastalarda aşırı duyarlılık reaksiyonlarının görülme riskini ve şiddetini arttırır. TISSEEL kullanımıyla aşırı duyarlılık ve ölümcül olabilen anafilaktik şok dahil anaflaktoid reaksiyonlar bildirilmiştir. Aşırı duyarlılık reaksiyonlarının belirtileri arasında yerel veya yaygın ürtiker, göğüste sıkışma hissi, hırıltılı solunum ve hipotansiyon bulunur. Bu semptomlar ortaya çıkarsa uygulama derhal durdurulmalı ve standart şok tedavisi uygulanmalıdır. Uygulanan alandaki henüz polimerize olmamış ürün temizlenmelidir. TISSEEL sentetik bir protein (aprotinin) içermektedir. Aprotinin varlığına bağlı olarak lokal uygulamada dahi anaflaktik reaksiyon riski vardır. İlk uygulama iyi tolere edilmiş olsa bile tekrarlayan uygulamalarda risk daha yüksektir. Bu nedenle aprotinin veya aprotinin içeren ürün uygulamaları hasta kayıtlarına işlenmelidir. Sentetik aprotinin yapısal olarak sığır aprotinini ile aynı olduğundan, sığır proteinlerine alerjisi olanlarda TISSEEL kullanımı dikkatle değerlendirilmelidir. Koroner arter bypas cerrahisinde randomize olmayan iki retrospektif çalışmada, fibrin yapıştırıcı uygulanan hastalarda istatistiksel olarak anlamlı artmış mortalite riski gözlenmiştir. Çalışmalarda her ne kadar belirli bir neden-sonuç ilişkisi gösterilememiş olsa da, TISSEEL kullanımı ile artmış risk gözardı edilememektedir. Bu nedenle ürünün kazayla intravasküler uygulanmaması için azami çaba gösterilmelidir. Oftalmik arter bölgesinde tromboembolik komplikasyonlara neden olabileceğinden nazal mukozaya enjekte etmekten kaçınılmalıdır. TISSEEL'in dokuya enjeksiyonu lokal doku hasarı riski içermektedir. TISSEEL ince bir tabaka oluşturacak şekilde uygulanmalıdır. Fazla pıhtı kalınlığı ürünün etkinliğini ve yara iyileşmesi sürecini olumsuz etkileyebilir. Polisorbat 80 temas dermatiti gibi yerel deri iritasyonuna neden olabilir. Virüs güvenilirliğiTISSEEL insan plazmasından üretilmektedir. İnsan plazmasından elde edilen ürünler, virüsler gibi, hastalığa neden olabilecek enfeksiyon etkenlerini içerebilir. İnsan kanı veya plazmasından hazırlanan tıbbi ürünlerin kullanımından kaynaklanan enfeksiyonların önüne geçmek için alınan standart önlemler, donörlerin seçilmesini, münferit kan bağışlarının ve plazma havuzlarının belli enfeksiyon belirteçleri açısından izlenmesini ve virüslerin etkisizleştirilmesi / uzaklaştırılması için etkili üretim basamaklarını kapsamaktadır. Buna karşın, insan kanı veya plazmasından hazırlanan ürünler uygulandığında enfeksiyöz ajanların geçiş olasılığı bertaraf edilememektedir. Bu ürünlerde henüz bilinmeyen hastalık etkenlerinin bulunma olasılığı da mevcuttur. [ör. virüsler ve teorik olarak Creutzfeld-Jacobs hastalığı (CJD) etkeni].Alınan önlemlerin HIV, HBC, HCV gibi zarflı virüslerle HAV gibi zarfsız virüsler için etkili olduğu düşünülmektedir. Alınan önlemlerin Parvovirüs B19 gibi bazı zarfsız virüsleri uzaklaştırmak ya da inaktive etmek için etkisi ise kısıtlıdır. Parvovirus B19 virüsü en ciddi olarak gebe kadınları (fetusda enfeksiyona neden olabilmektedir), immün yetmezlikli hastaları veya artmış eritropoezi olan hastaları (örn. hemolitik anemi durumu) etkilemektedir. Virüs güvenilirliği açısından hasta ile ürün serisi arasındaki bağıntıyı koruyabilmek amacı ile, hastaya her TISSEEL uygulandığında ürünün ismi ve seri numarasının kaydedilmesi önemle tavsiye edilmektedir. Okside selüloz içeren preparatlar TISSEEL ile birlikte kullanılmamalıdır. 4.5. Diğer tıbbi ürünler ile etkileşimler ve diğer etkileşim şekilleriTISSEEL ile usulüne uygun etkileşim çalışmaları yapılmamıştır. Benzer ürünler veya trombin çözeltileri alkol, iyot, ya da ağır metal iyonları içeren çözeltilerle (örn. antiseptik çözeltilerle) denatüre olabilir. Yara bölgesini temizlemekte bunlardan herhangi birisi kullanıldıysa, TISSEEL uygulamasından önce bölge iyice yıkanmalıdır.Özel popülasyonlara ilişkin ek bilgilerÖzel popülasyonlarda hiçbir etkileşim çalışması yapılmamıştır.Pediyatrik popülasyon:Pediyatrik popülasyonda hiçbir etkileşim çalışması yapılmamıştır.4.6. Gebelik ve laktasyon Genel tavsiyeGebelik Kategorisi: CÇocuk doğurma potansiyeli bulunan kadınlar/Doğum kontrolü (Kontrasepsiyon)TISSEEL'in çocuk doğurma potansiyeli bulunan kadınlarda kullanımına ilişkin yeterli veri mevcut değildir. Bilinen olumsuz bir etkisi bulunmamaktadır.Gebelik dönemiTISSEEL'in gebe kadınlarda kullanımına ilişkin yeterli veri mevcut değildir.Hayvanlar üzerinde yapılan çalışmalar gebelik / ve-veya / embriyonal / fötal gelişim / ve-veya / doğum / ve-veya / doğum sonrası gelişim üzerindeki etkiler bakımından yetersizdir. İnsanlara yönelik potansiyel risk bilinmemektedir (Bkz. Kısım 5.3). Gebe kadınlara verilirken tedbirli olunmalıdır. Parvovirüs B19 enfeksiyonu açısından bölüm 4.4'e bakınız. Laktasyon dönemiTISSEEL'in anne sütüne geçip geçmediği bilinmemektedir. Birçok ilaç anne sütüne geçtiği için, TISSEEL laktasyonda uygulanırken dikkatli olunmalıdır.Üreme yeteneği/FertiliteHayvan üreme çalışmaları yürütülmemiştir. İnsanlardaki üreme yeteneği / fertiliteyi etkileyip etkilemediği bilinmemektedir.4.7. Araç ve makine kullanımı üzerindeki etkilerAraç ve makine kullanımı üzerinde bilinen bir etkisi bulunmamaktadır.4.8. İstenmeyen etkilerFibrin yapıştırıcılar/hemostatiklerle tedavi edilen hastalarda seyrek olarak aşırı duyarlılık veya alerjik reaksiyonlar (bunlarla sınırlı kalmamak kaydıyla anjiyoödem, uygulama yerinde yanma ve sızı, bradikardi, bronkospazm, titreme, solunum zorluğu, yüz ve boyunda kızarma ("flushing"), yaygın ürtiker, başağrısı, ürtiker, hipotansiyon, letarji, bulantı, kaşıntı, huzursuzluk, taşikardi, göğüste baskı hissi, karıncalanma, kusma, hırıltılı solunum dahil) ortaya çıkabilir.İzole olgularda bu reaksiyonlar ciddi anafilaksiye kadar ilerlemiştir. Bu reaksiyonlar preparat ile tekrarlanan uygulamalarda ya da aprotinine (bölüm 4.4'e bakınız) veya ürünün bileşimdeki diğer maddelerden herhangi birisine karşı aşırı duyarlılığı olduğu bilinen hastalara uygulandığında özellikle görülebilir. TISSEEL ile daha önce yapılmış uygulamalar iyi tolere edilmiş olsa bile, TISSEEL'in sonraki uygulanmaları ya da aprotininin sistemik olarak uygulanması ciddi bir anafilaktik reaksiyonla sonuçlanabilir. Seyrek olarak fibrin yapıştırıcı/hemostatik ürünlerin bileşenlerine karşı gelişen antikorlara reaksiyon oluşabilir. Kazayla intravasküler uygulama tromboembolik olaylara ve dissemine intravasküler koagülasyona neden olabilir; dahası böyle durumlarda anaflaktik reaksiyon riski de olabilir (bölüm 4.4'e bakınız). Viral bulaş ajanları ile ilgili güvenlik için bölüm 4.4'e bakınız. Aşağıda listelenmiş istenmeyen etkiler TISSEEL'in güvenirlik ve etkinliğini araştırmak amacıyla yapılan klinik çalışmalardan ve Baxter'in fibrin yapıştırıcılarla olan pazarlama sonrası deneyimden elde edilmiştir. Bu klinik çalışmalarda TISSEEL kardiyak, vasküler ve total kalça replasman cerrahisinde hemostaza ek olarak uygulanmış ya da karaciğer ve dalak cerrahisinde kullanılmıştır. Diğer klinik çalışmalar arasında aksiller lenf düğümü diseksiyonu uygulanan hastalarda lenf damarlarının sızdırmazlığının sağlanması, kolon anastomozlarında sızdırmazlığın sağlanması ve posterior fossa girişimlerinde duramater sızdırmazlığının sağlanması amacıyla kullanımı bulunmaktadır. Klinik çalışmalarda toplam 1084 hastaya TISSEEL uygulanmıştır. Sıklık aşağıdaki kriterlere göre değerlendirilmiştir. Çok yaygın (>1/10), yaygın (>1/100 ila <1/10), yaygın olmayan (>1/1.000 ila <1/100), seyrek (>1/10.000 ila <1/1.000), çok seyrek (<1/10.000) Enfeksiyon ve enfestasyonlarYaygın: Postoperatif yara enfeksiyonuKan ve lenf sistemi hastalıklarıYaygın olmayan: Fibrin D-dimer düzeyinde artış, Fibrin yıkım ürünlerinde artışBağışıklık sistemi hastalıklarıBilinmiyor: Aşırı duyarlılık reaksiyonları*, Anafilaktik reaksiyonlar*,Anafilaktik şok*, Parestezi, Bronkospazm, Hırıltılı solunum, Kaşıntı, Eritem Sinir sistemi hastalıklarıYaygın: His bozuklukl arıKardiyak hastalıklarBilinmiyor: Bradikardi, TaşikardiVasküler hastalıklarYaygın: Aksiller ven trombozu**Seyrek: Hipotansiyon Bilinmiyor: Hematom, Arteriyel emboli, Tromboembolizm, Serebral arter embolisi, Serebral enfarktüs** Solunum, göğüs bozuklukları ve mediastinal hastalıklarBilinmiyor: DispneGastrointestinal hastalıklarYaygın: BulantıBilinmiyor: Bağırsak tıkanıklığı Deri ve deri altı doku hastalıklarıYaygın: DöküntüBilinmiyor: Ürtiker, İyileşmede gecikme Kas iskelet bozuklukları, bağ doku ve iskelet hastalıklarıYaygın: Bir ekstremitede ağrıGenel bozukluklar ve uygulama bölgesine ilişkin hastalıklarYaygın: Ağrı, Vücut sıcaklığında artış, İşleme bağlı ağrıBilinmiyor: Yüzde ve boyunda kızarıklık (flushing), Ödem Yaralanma ve zehirlenmeÇok yaygın: SeromaBilinmiyor: Anjiyoödem * Anafilaktik reaksiyonlar ve anafilaktik şok şeklindeki advers etkilere fatal sonlanan vakalar dahildir. ** Superior petrozal sinüse intravasküler uygulamaya bağlı Sınıf etkileriFibrin doku yapıştırıcılar / hemostatik ürün sınıfından ilaçlarla bildirilen diğer advers ilaç etkileri arasında basınçlı gazla intravasküler uygulamaya bağlı hava veya gaz embolisi ile uygulama bölgesinde iritasyon, göğüste rahatsızlık hissi, titreme, baş ağrısı, letarji, huzursuzluk ve kusma gibi aşırı duyarlılığa ilişkin belirtiler bulunur.4.9. Doz aşımı ve tedavisiHerhangi bir doz aşımı vakası bildirimi bulunmamaktadır.5. FARMAKOLOJİK ÖZELLİKLER5.1. Farmakodinamik özelliklerFarmakoterapötik Grubu: lokal hemostatikler, ATC kodu: B02BC; doku yapıştırıcılar, ATC kodu: V03AKFibrin adezyon sistemi, fizyolojik kan pıhtılaşmasının son dönemini taklit eder. Fibrinojenin fibrin monomerleri ve fibrinopeptidlere parçalanmasıyla fibrinojenin fibrine dönüşümü gerçekleşir. Fibrin monomerleri biraraya toplanır ve bir fibrin pıhtısı oluşur. Trombinin ve kalsiyum iyonlarının birlikte etkisiyle faktör XIII'den oluşan faktör XIIIa, fibrin liflerinin çapraz bağlanmasıyla pıhtıyı sabitleştirir. Yarada iyileşme süreci ilerlerken, plazmin uyarısıyla fibrinolitik aktivite artar ve fibrinin fibrin yıkım ürünlerine dönüşümü başlar. Fibrinin proteolitik yıkımı anti-fibrinolitiklerce inhibe edilir. TISSEEL bileşiminde bulunan aprotinin bir anti-fibrinolitik olarak pıhtının prematür yıkımını önler. Etkinliği kanıtlamak için gerçekleştirilen in vivoçalışmalarda hastaların durumunu mümkün olduğunca yansıtan dört hayvan modeli seçilmiştir. Çalışmalarda TISSEEL yara iyileşmesinde olduğu kadar primer ve sekonder hemostazın sağlanmasında da etkili olarak bulunmuştur.TISSEEL, paralel olarak dizayn edilmiş, prospektif randomize, çift kör, çok merkezli bir klinik çalışmada, kardiyopulmoner baypas ve medyan sternotomi uygulanması gereken 317 kardiyak cerrahi hastasında, ürünün tek virüs inaktivasyon yapılmış eski formülasyonu ile karşılaştırılarak değerlendirilmiştir. Hastalar, yalnızca konvansiyonel yöntemlerle hemostaz sağlanamadığı durumlarda, TISSEEL ile ya da kontrol preparatıyla tedavi edilmiştir. Sonlanım noktası olarak hemostazın ilk 5 dakika içinde sağlanması ve cerrahi yara kapanana kadar devam etmesi alınmıştır. Tek taraflı %97.5 güvenlik aralığı kullanılarak ölçülen sonuçlara göre, başarıyla tedavi edilenlerde TISSEEL (çift virüs inaktivasyonu yapılmış), daha önceki formülasyona göre daha aşağıda kalmamıştır. TISSEEL (çift virüs inaktivasyonu _ yapılmış)_Fibrin doku yapıştırıcı (tek virüs inaktivasyonu _ yapılmış)_Tedavi başlangıcında amaçlıanaliz_
127/144 (% 88.2)
129/144 (% 89.6) Protokolden sonraki başınaanaliz
108/123 (% 87.8)
122/135 (% 90.4) TISSEEL'in kalça eklem replasmanında postoperatif kan kaybı için kullanıldığı bir çalışma ile aksiller bölge lenf düğümü diseksiyonunda aksiller drenaj süresini kısaltmak için kullanıldığı bir çalışmada, TISSEEL almayan kontrol grubuyla arasında bir fark bulunamamıştır. 5.2. Farmakokinetik özelliklerTISSEEL sadece lokal uygulama için tasarlanmıştır, intravasküler uygulama kontrendikedir. Bu nedenle dolayısıyla insanda intravasküler farmakokinetik çalışmalar yapılmamıştır.Değişik tür laboratuvar hayvanlarında farmakokinetik çalışmalar gerçekleştirilmemiştir. Emilim:Yerel olarak TISSEEL uygulanan vücut bölgelerinden vücut sıvı ve dokularına emilim olmaz. Dağılım:Vücutta karaciğerden doğal olarak üretilen fibrinojen en yoğun olarak plazmada bulunur. Kan plazmasının yaklaşık %5'i fibrinojendir. Plazmadaki fibrinojen miktarı yaklaşık olarak 5 g/litre'dir. Fibrinojen sadece kan plazmasında değil, aynı zamanda çeşitli vücut sıvılarında da (lenf sıvısı, iltihabi sıvı birikintileri vb) bulunur. Kanı pıhtılaştıran bir protein olan trombin normalde vücut sıvılarında bulunmaz. İhtiyaç halinde karaciğerde üretilen protrombinin enzimatik yıkımıyla oluşur ve fibrinojeni fibrine yani suda erimeyen haline dönüştürür. Aprotinin vücutta doğal olarak üretilmez ve bulunmaz. Sığır kaynaklı aprotinin intravenöz yoldan uygulandığında plazma yarılanma süresinin yaklaşık 150 dakika olduğu ve terminal yarılanma süresinin ise yaklaşık 10 saat olduğu bilinmektedir. Biyotransformasyon:Trombinin etkisiyle fibrinojenin fibrine dönüşümü sonucu oluşmuş fibrin monomerleri biraraya toplanır ve fibrin pıhtısı oluşur. Fibrin liflerinin çapraz bağlanmasıyla sabitleşen pıhtıdaki fibrin ise daha sonra yani pıhtıya artık gerek kalmadığı zaman fibrin yıkım ürünlerine dönüşür. Karaciğerde metabolize edilen fibrin yıkım ürünleri ise böbreklerden atılır. Vücuda dışarıdan uygulanan aprotinin lizozomal emzimler tarafından yavaş bir yıkıma uğrarlar. Eliminasyon:Fibrin yıkım ürünleri böbreklerden elimine olmaktadır. Tek bir intravenöz doz radyoaktif işaretli aprotinin uygulanması sonrası, radyoaktivitenin yaklaşık %25-40 kadarı idrarla elimine edilmiştir. Bir milyon KIU aprotininin 30 dakikada infüzyonu sonrası yaklaşık %2'si, 2 milyon KIU'luk daha yüksek bir doz aprotininin 30 dakikada infüzyonu sonrası ise yaklaşık %9'u idrarla değişmeden atılmaktadır. 5.3. Klinik öncesi güvenlilik verileriTISSEEL genellikle bir dozda uygulanır, sadece az sayıdaki istisnai durumda birkaç mL daha uygulama gerekmektedir. Uygulama yöntemlerinin özel olması yanında yapısı ve etki mekanizması (sistemik etki olmadan veya diğer organ ve dokulara dağılım olmadan yerel etki oluşturması) nedeniyle kronik toksisite, karsinojenite, üreme ve gelişim toksisitesi ya da immun stimulasyon açısından TISSEEL ile preklinik güvenlilik verileri mevcut değildir.Sıçan ve tavşanlarda yapılan tek doz toksisite çalışmalarında TISSEEL akut toksisiteye neden olmamıştır. Dahası usulüne uygun yapılan in vitroin vitroinsan fibroblast kültürlerinde iyi tolere edilmiştir. Detaylı literatür gözden geçirmeye dayanarak, çözücü/deterjan rezidülerinin TISSEEL üzerindeki toksisitesinin ihmal edilebilir düzeylerde olduğu kabul edilir. Polisorbat 80 (Tween 80) Sodyum Sitrat Dihidrat Enjeksiyonluk Su Bileşen 2: Trombin Çözeltisi İnsan Albumini Sodyum Klorür Enjeksiyonluk Su 6.2. GeçimsizliklerDüşük pH trombin aktivitesini etkileyebileceğinden, okside selüloz içeren preparatlar TISSEEL ile birlikte kullanılmamalıdır.Bu tıbbi ürün bölüm 6.6'da bahsedilenlerin dışındaki diğer ilaçlarla karıştırılmamalıdır. 6.3. Raf ömrü24 ay.Çözülmüş ürünün raf ömrü için bölüm 6.6'ya bakınız. 6.4. Saklamaya yönelik özel tedbirlerÇocukların göremeyeceği ve erişemeyeceği yerlerde saklayınız.Dondurucuda (< -20°C) saklayınız. Kullanılıncaya kadar soğuk zincir kırılmamalıdır. Işıktan korumak için TISSEEL'i kutusu içinde saklayınız. Bir kez çözüldükten sonra ürün 72 saat içinde kullanılmalıdır. Bir kez çözüldükten sonra yeniden dondurmayınız ya da buzdolabında saklamayınız. 6.5. Ambalajın niteliği ve içeriğiHem Yapıştırıcı Protein Çözeltisi, hem de Trombin Çözeltisi tek kullanımlık çift hazneli polipropilen enjektör içinde yer alır.TISSEEL ambalajı içinde şu bileşenler bulunmaktadır: - Bir adet tek kullanımlık çift hazneli polipropilen enjektör (bölmelerden birinde 1 mL derin dondurulmuş Yapıştırıcı Protein Çözeltisi, diğerinde 1 mL derin dondurulmuş Trombin Çözeltisi). - Bir uygulama cihazı (DUO-Set): 2 birleştirme parçası, 4 uygulama kanülü (künt uçlu), 1 çift enjektör pistonu. 6.6. Beşeri tıbbi üründen arta kalan maddelerin imhası ve diğer özel önlemler GenelTISSEEL uygulanmasından önce, uygulama istenen alan dışındaki vücut alanının korunarak istenmeyen adezyonların oluşması önlenmelidir.TISSEEL'in eldiven ve aletlere yapışmasını önlemek için buralar serum fizyolojik ile ıslatılmalıdır. Yapıştırılacak yüzeyler için bir rehber olmak üzere 1 kutu TISSEEL 2 mL (1 mL yapıştırıcı protein çözeltisi artı 1 mL trombin çözeltisi) en az 10 cm2 lik bir alan için yeterli olacaktır. Kullanılacak doz uygulama alanının genişliğine göre değişir. TISSEEL'in iki bileşeninin ardışık olarak ayrı ayrı kullanımından kaçınılmalıdır. Kullanıma hazırlamaHem Yapıştırıcı Protein Çözeltisi, hem de Trombin Çözeltisi tek kullanımlık çift hazneli enjektör içinde yer alır. Önceden doldurulmuş çift hazneli enjektörün uygulama uçları birer kapakla kapalı durumdadır ve her bir enjektörün piston tarafı silikondan mamül lastik bir stoperle kapalıdır. Bu bileşkenin tümü alüminyum-plastik karışımından mamül iki adet steril torbayla aseptik koşullarda sarılmıştır. Dıştaki ambalajın bütünlüğü bozulmadıysa, içteki torba ve içindekiler sterildir.Çift hazneli kullanıma hazır enjektörün çözme işlemi aşağıdaki yöntemlerle yapılabilir: İki bileşenli yapıştırıcının çözülmesi ve ısıtılması işleminin 33 - 37°C arası sıcaklıkta steril su banyosuyla yapılması önerilir. Su banyosunun sıcaklığı 37°C'ı geçmemelidir (belirlenmiş bu sıcaklıklar arasında tutulması için su banyosunun sıcaklığı bir termometre aracılığıyla sürekli izlenmeli ve gerektiğinde içindeki su yenilenmelidir. Çözme ve ısıtma için steril su banyosu kullanılırken, önceden doldurulmuş çift hazneli enjektör bileşkesi aluminyum-plastik torbalarından çıkarılmalıdır). Çözme işlemi tamamlanana ve uygulama ucu iliştirilmeye hazır olana kadar, enjektördeki koruyucu kapak yerinden çıkarılmamalıdır. TISSEEL tümüyle çözülene ve vücut sıcaklığına gelene kadar kullanılmamalıdır. 1) Hızlı çözme (steril su banyosu ile) Piston ile iç torbayı steril alana getiriniz ve kullanıma hazır çift hazneli enjektörü iç torbasından çıkararak doğrudan steril suya yerleştiriniz. Çözme işlemi boyunca enjektörün tümüyle suya battığından emin olunuz. Tablo : 33°C (maksimum 37°C) sıcaklıkta steril su banyosunda çözme süreleri
Tablo: Steril alan dışında 33°C (maksimum 37°C) sıcaklıkta su banyosunda çözme süreleri
Üçüncü bir seçenek olarak doku yapıştırıcı bileşenler 33°C (maksimum 37°C) sıcaklıkta tutulan bir inkübatör içinde çözülebilir. İnkübatör içindeki ısıtma ve çözme süreleri aşağıdaki tabloda belirtilmiştir. Bu veriler alüminyum-plastik torbası içindeki ürünle ilgili verilerdir. Tablo: İnkübatörde 33°C (maksimum 37°C) sıcaklıkta çözme süreleri
Çözme işlemi oda sıcaklığında da yapılabilir. Oda sıcaklığındaki çözme süreleri aşağıdaki tabloda belirtilmiştir. Ürün çözüldükten sonra oda sıcaklığında saklanmalı ve 72 saat içinde kullanılmalıdır. Ürün oda sıcaklığında çözüldükten sonra, kullanımdan kısa süre öncesinde 33°C (maksimum 37°C) sıcaklığa ısıtılmalıdır. Aşağıdaki tabloda ürün çözüldükten sonraki bu ek ısıtma süreleri de yer almaktadır. Tablo: Oda sıcaklığında çözme süresi + kullanmadan kısa bir süre önce inkübatörde 33°C (maksimum 37°C) sıcaklığa ısıtma süresi
Not:Ürünü elleriniz arasında tutarak çözmeye çalışmayınız.Çözme/ısıtma için mikrodalga fırın kullanmayınız. Çözdükten sonra yeniden soğutmayınız / dondurmayınız ya da buzdolabında saklamayınız. Çözüldükten sonrası stabilitesiHızlı çözme işlemi (33-37°C arası sıcaklıkta) gerçekleştirilmişse, TISSEEL çözüldükten sonra 33-37°C arası sıcaklıkta en fazla 12 saat saklanabilir.Oda sıcaklığında çözünmüş ürün ambalajı açılmadığı sürece kontrollü oda sıcaklığında (+25 °C'ı geçmeyen) 72 saate kadar saklanabilir. Çözüldükten sonra 72 saat içinde kullanılmayan TISSEEL atılmalıdır. Çözdükten sonra / uygulama öncesi yapılması önerilenlerİki çözeltinin en uygun şekilde harmanlanması için, her iki bileşenin de kullanımdan hemen öncesine kadar 33 - 37 °C arası sıcaklığı ısıtılması gerekmektedir. Bu amaçla 37°C sıcaklık aşılmamalı ve mikrodalga fırın kullanılmamalıdır!Yapıştırıcı Protein ve Trombin Çözeltileri berrak ya da hafif opelasan olmalıdır. Bulanık olan ya da partikül içeren çözeltileri kullanmayınız. Çözülmüş ürünlerin kullanmadan önce partikül içerip içermediği ve renk değiştirip değiştirmediği kontrol edilmelidir. Partikül içeren ya da renk değiştirmiş ürünler kullanılmamalıdır. Çözülmüş Yapıştırıcı Protein Çözeltisi sıvı halde olmalıdır, kıvamı hafifçe visköz olabilir. Çözeltinin kıvamı jöle gibiyse, denatüre olduğu varsayılmalıdır (soğuk zincirde olan bir kırılmaya bağlı olarak veya ısıtma sırasında aşırı sıcaklığa maruz kalma sonucu). Bu durumda TISSEEL kullanılmamalıdır. Çift hazneli kullanıma hazır enjektör yalnızca kullanım öncesinde plastik torbalarından çıkarılmalıdır. Enjektördeki koruyucu kapağı ise yalnızca uygulamadan hemen önce çıkarınız. TISSEEL'i yalnızca uygun bir şekilde tümüyle çözülmüş ve ısıtılmış olduğu durumlarda (sıvı kıvam sağlanmışsa) kullanınız. Daha ayrıntılı bilgi için sorumlu hemşire ya da doktora danışınız. UygulamaUygulama için set içindeki birleştirme parçası ve uygulama kanülü Yapıştırıcı Protein Çözeltisi ve Trombin Çözeltisi içeren çift hazneli enjektöre iliştirilir. Çift bölmeye uygulanan çift kollu ortak piston sayesinde, uygulama kanülü içinde karışarak dışarıya çıkmadan önce birleştirme parçasına her iki çözeltiden eşit miktarda iletilir.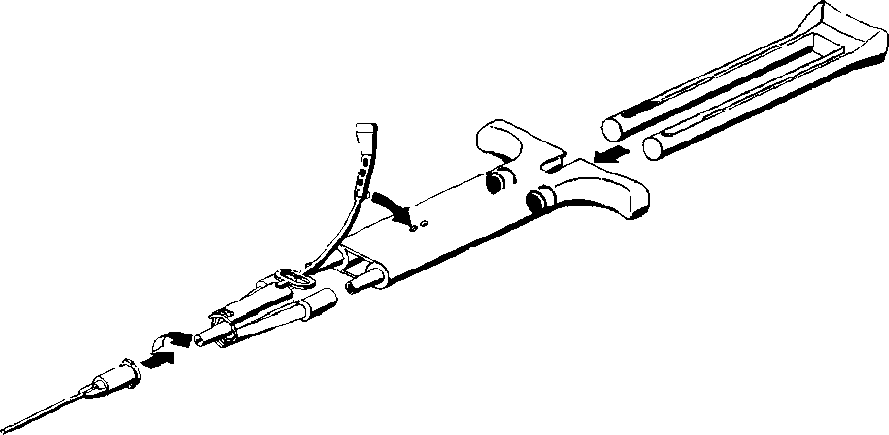 Çift hazneli enjektör
Çift hazneli enjektörY - birleştirme parçası Uygulama kanülü- Bağlantı şeridi çift hazneli enjektöre iliştirilerek, birleştirme parçası sabitlenir. Şeridin kopması durumunda yedek birleştirme parçası kullanılır. Yedek parçadaki şeridin de kopması durumunda ürün yine de kullanılabilir ama sızıntı olmaması için bağlantının sağlamlığı iyice kontrol edilmelidir.- Birleştirme parçasına bir uygulama kanülü iliştirilir. Uygulama kanülünün tıkanmaması için birleştirme parçası ve uygulama kanülü içindeki havayı uygulamaya başlamadan hemen öncesine kadar çıkarmayınız. - Uygulama yapılacak yüzeye ya da yapıştırılacak parçaların yüzeyine karışmış Yapıştırıcı Protein - Trombin Çözeltisini uygulayınız. Fibrin yapıştırıcı bileşenlerin uygulanması kesintisiz olmalıdır; kesinti durumunda kanül içinde hızla tıkanıklık oluşur. Bu durumda uygulama kanülü değiştirilir. Birleştirme parçasında tıkanma olması durumunda ambalajdaki yedek birleştirme parçasını kullanınız. Not:Yüksek Trombin konsantrasyonu (500 IU/mL) nedeniyle yapıştırıcı bileşenlerin harmanlanmasından saniyeler sonra fibrin yapıştırıcı oluşmaya başlar.Endoskopik kullanım, minimal invazif girişimlerde kullanım, büyük ya da uygulamanın zor olduğu yerlere uygulama için BAXTER tarafından sağlanan diğer aksesuarlarla da uygulama mümkündür. Bu uygulama cihazlarıyla uygulanması sırasında, ilgili cihazın Kullanım Talimatı'na uyulmalıdır. TISSEEL uygulanmasından sonra yeterli polimerizasyonun sağlanması için en az 2 dakika beklenmelidir. Bazı uygulamalarda, taşıyıcı madde olarak ya da sağlamlaştırma için kolajen parçası gibi biyo-uyumlu materyal kullanılabilir. TISSEEL'i sprey cihazı kullanarak uygularken, cerrah sadece sprey cihazı üreticisi tarafından önerilen basınç aralığı dahilindeki basıncı kullandığına emin olmalıdır. Sprey cihazı üreticisi tarafından önerilen mesafenin daha yakınından püskürtme yapmaktan kaçınılmalıdır. TİSSEEL'i spreyle uygularken hava veya gaz embolisi oluşma ihtimali nedeniyle kan basıncındaki değişiklikler, nabız, oksijen saturasyonu ve son tidal CO2 izlenmelidir. Kapalı toraks ve abdominal boşluklara TISSEEL uygulaması için DuploSpray MIS aplikatör ve regülatör sistemi'nin kullanımı önerilir. Kullanım sırasında lütfen DuploSpray MIS cihazının kullanım talimatına uyunuz. Artan ürünün atılmasıKullanılmamış olan ürünler ya da atık materyaller Tıbbi Atıkların Kontrolü Yönetmeliği ve Ambalaj Atıkların Kontrolü Yönetmeliklerine uygun olarak imha edilmelidir.7. RUHSAT SAHİBİEczacıbaşı-Baxter Hastane Ürünleri Sanayi ve Ticaret A.Ş.Cendere Yolu, Pırnal Keçeli Bahçesi 34390 Ayazağa-İSTANBUL Tel: (0.212) 329 62 00 Faks: (0.212) 289 92 75 8. RUHSAT NUMARASI859. İLK RUHSAT TARİHİ/RUHSAT YENİLEME TARİHİ10.12.201210. KÜB'ÜN YENİLEME TARİHİ1FARMASÖTIK FORMDoku yapıştırıcılar Derin dondurulmuş2 Steril olmayan su banyosu ile çözme Ürünü çözmenin bir diğer yolu da işlemi steril alan dışındaki bir bölgedeki steril olmayan bir sıcak su banyosu içinde gerçekleştirmektir. |
İlaç BilgileriTisseel 2 mL Kullanıma Hazır EnjektörEtken Maddesi: İnsan fibrinojeni, aprotinin, insan trombini, kalsiyum klorür Atc Kodu: V03AK Kullanma talimatı ve kısa ürün bilgileri
Google Reklamları
İlgili İlaçlar |
Ana Sayfa | Hakkımızda | İlaçlar | İlaç Ara | İlaç Firmaları | Gizlilik | Bize Ulaşın
Telif Hakkı 2008-2026 © İlaç Prospektüsü. Tüm Hakları Saklıdır.Uyarı: Sitemizde yayınladığımız ilaç bilgileri ile doktora danışmadan kesinlikle ilaç kullanmayınız!
Aksi halde doğabilecek sağlık sorunlarından ilacprospektusu.com sorumlu tutulamaz.