Fixflow 27.5 Mcg Burun Spreyi, Süspansiyon Kısa Ürün BilgisiKISA ÜRÜN BILGISI1. BEŞERI TIBBİ ÜRÜNÜN ADIFİXFLOW 27,5 mikrogram burun spreyi, süspansiyon 2. KALİTATİF VE KANTİTATİF BİLEŞİMEtkin madde:Flutikazon furoat.........................27,5 mikrogram Yardımcı maddeler:Benzalkonyum klorür (%50'lik).......16,5 mikrogram Yardımcı maddeler için bölüm 6.1'e bakınız. 3. FARMASÖTİK FORMBurun spreyi, süspansiyon. Beyaz renkli homojen süspansiyondur. 4. KLİNİK ÖZELLİKLER4.1. Terapötik endikasyonlarYetişkinler ve 12 yaşından büyük ergenlerde: Mevsimsel alerjik rinitin nazal ve oküler belirtilerinin tedavisinde endikedir. Yıl boyu devam eden alerjik rinitin nazal belirtilerinin tedavisinde endikedir. Çocuklar (2 - 11 yaş): Mevsimsel ve yıl boyu devam eden alerjik rinitin nazal belirtilerinin tedavisinde endikedir. 4.2. Pozoloji ve uygulama şekliPozoloji:Yetişkinlerde ve 12 yaşından büyük ergenlerde: Önerilen başlangıç dozu, her burun deliğine günde bir kez uygulanan iki spreydir (her spreyde 27,5 mikrogram flutikazon furoat, günlük toplam doz 110 mikrogram). Belirtiler yeterincekontrol altına alındıktan sonra her burun deliğine günde bir kez uygulanan birer sprey (toplamgünlük doz 55 mikrogram), idame tedavisinde etkilidir. Uygulama sıklığı ve süresi:Tedavi süresi hekim tarafından belirlenmelidir. Tam terapötik fayda sağlanması için, düzenli kullanım önerilir. Etkisi, başlangıçtaki uygulamayı izleyen 8. saat gibi erken bir dönemde gözlenmiştir. En üst düzeyde faydasağlayabilmek için, daha uzun süreli tedavi gerekmektedir. Düzenli kullanım ile belirtilerindüzeleceği konusunda hasta bilgilendirilmelidir. Tedavi süresi alerjene maruz kalınan süre ilesınırlı olmalıdır. Uygulama şekli:FİXFLOW Burun Spreyi, sadece intranazal uygulama içindir. FİXFLOW spreyin test edilmesi: Eğer FİXFLOW ilk kez kullanılacaksa, sprey cihazının hatasız çalışıp çalışmadığı test edilmelidir. Belge DoCihaz kullanıma lSHY3M0FyZl^xZLA.xQ3NRRG83 Jlelge Takip/\.dresi:https://www.turkiye.gov.tr/saglik-titck-ebys hazırlandığındaKuvvetlice çalkalanır, püskürtme mekanizmasınıçalıştırmak üzere koruyucu kapağı çıkarılır ve sprey pompası ince bir duman çıkıncaya kadar birkaç kez çalıştırılır. Kapak, kullanım sonrası kapatılmalıdır. FİXFLOW spreyin uygulanması: 1. 2. 3. Sprey uygulanmadan önce, sümkürülerek burun delikleri temizlenmelidir. Sprey gözlere püskürtülmemelidir, kazara sprey gözlere temas ederse, gözler suyla iyice yıkanmalıdır. Baş öne doğru biraz eğilir. Sprey dik olarak tutulup uç parçası burun deliklerinden birine yerleştirilir. Uç parçası, burnun dış duvarına doğru tutulur (bkz.Şekil 1).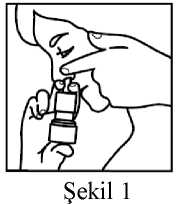
4.
Burundan soluk alınırken, aşağıya doğru bir kez basılarak ilacın buruna püskürmesi sağlanır (bkz.Şekil 2). Uç parçası burundan çıkarılır ve ağızdan soluk verilir.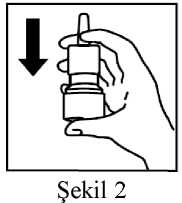 5. Uygulama diğer burun deliğinde de tekrarlanır. Eğer 2 püskürtme yapılması gerekliyse, 4'üncü ve 5'inci basamaklar tekrarlanır. Her uygulamadan sonra uç parçası ve kapağın iç yüzü temiz, kuru bir bezle silinerek temizlenmelidir. Temiz kalmasını sağlamak için her zaman kapağı kapalı tutulmalıdır. Özel popülasyonlara ilişkin ek bilgiler Böbrek yetmezliği:Böbrek yetmezliğinde doz ayarlaması gerekmemektedir (Bkz. Bölüm 5.2). Karaciğer yetmezliği:Karaciğer bozukluğu olan hastalarda herhangi bir doz ayarlaması gerekmemektedir. Karaciğer bozukluğu olan hastalar kortikosteroidler ile ilişkili sistemik advers reaksiyonlar açısındandaha yüksek risk altında olabileceğinden şiddetli karaciğer bozukluğu olan hastalara dozuygulanırken dikkatli olunmalıdır (Bkz. Bölüm 4.4 ve 5.2). Pediyatrik popülasyon:Çocuklarda kullanımı: 2-6 yaş aralığı kullanımı için yarar zarar durumu gözetilerek kullanılmalıdır. ioğMİ^a K-qdu: 1ZW56SH|Y3SHY3M0F\^1AxZ1AxQ3NKJİ-G83rrBel<^ Takip Adresi:lıttDs://www.tm'k\4e.govıtr/saglik-titck-eeysz7,5 mıkrogram nuükazon turoaf, ğunluk doz 55 mfkroğram). Çocuklaraauler Burun dengineÖnerilen başlangıç dozu, her burun deliğine günde bir kez uygulanan bir spreydir (her spreyde Belge Do_ c rBel^_Takip. Adr^si:trttnsL//^^w.turki'v^e.govıtr/şaglik-titçl(-ebyş_ _
günde bir kez uygulanan bir spreye (toplam günlük doz, 55 mikrogram) yeterli yanıt vermeyen hastalar; her burun deliğine günde bir kez iki sprey (toplam günlük doz 110mikrogram) uygulayabilir. Belirtiler yeterince kontrol altına alındıktan sonra dozun; her burundeliğine günde bir spreye (toplam günlük doz 55 mikrogram) düşürülmesi önerilir. Bu ilacı kullanırken bazı çocukların büyüme hızı daha yavaş olabilir. Çocuklar semptomların giderilmesini sağlamak için gereken en kısa süre boyunca ilacı kullanmalıdır. FİXFLOW bir yetişkinin gözetimi altında kullanılmalıdır. 2 yaşın altındaki çocuklarda kullanılmamalıdır. 2 yaşın altındaki çocuklarda mevsimsel ve yıl boyu devam eden (pereniyal) alerjik rinitin tedavisinde intranazal flutikazon furoat kullanımının önerilmesi için yeterince veri yoktur. Geriyatrik popülasyon:Normal yetişkin dozu kullanılır (Bkz. Bölüm 5.2). 4.3. KontrendikasyonlarFİXFLOW içeriğindeki etkin maddeye veya Bölüm 6.1'de listelenen yardımcı maddelerden herhangi birine karşı aşırı duyarlılığı olanlarda kontrendikedir. 4.4. Özel kullanım uyarıları ve önlemleriSistemik kortikosteroid etkileri Özellikle uzun periyotlarda ve yüksek dozlarda reçete edilen nazal kortikosteroidlerle sistemik etkiler meydana gelebilir. Oral kortikosteroidlerle kıyaslandığında bu etkilerinmeydana gelme ihtimali çok daha düşüktür ve bu etkiler her hastada ve çeşitli kortikosteroidpreparatları arasında değişiklik gösterebilir. Potansiyel sistemik etkiler Cushing sendromu,Cushingoid özellikler, adrenal supresyon, çocuklarda ve ergenlerde büyüme geriliği, katarakt,glokom ve daha seyrek olarak psikomotor hiperaktivite, uyku bozuklukları, anksiyete,depresyon veya agresyon (özellikle çocuklarda) içeren bir dizi psikolojik veya davranışsaletkileri içerebilir. Önerilenden daha yüksek dozlarda kullanılan nazal kortikosteroidler klinikolarak anlamlı adrenal supresyon ile sonuçlanabilir. Önerilenden yüksek dozlarınkullanıldığına dair bir kanıt varsa, stres veya elektif ameliyat dönemlerinde ilave sistemikkortikosteroid ile takviye düşünülmelidir. Günde bir kez flutikazon furoat 110 mikrogramyetişkin, ergen veya pediyatrik gönüllülerde hipotalamus-hipofiz-böbreküstü (HPA) aksıbaskılanması ile ilişkilendirilmemiştir. Bununla birlikte intranazal flutikazon furoat dozu rinitsemptomlarının etkili kontrolünün korunduğu en düşük doza azaltılmalıdır. Tüm intranazalkortikosteroidler ile olduğu gibi, eşzamanlı olarak diğer kortikosteroid tedavisi formlarınınreçete edildiği her seferinde kortikosteroidlerin toplam sistemik yükü dikkate alınmalıdır. Böbreküstü bezi fonksiyonunun bozulduğundan şüphe etmek için bir neden varsa, hastalar sistemik steroid tedavisinden flutikazon furoata geçirilirken dikkatli olunmalıdır. Görme bozukluğu Sistemik ve topikal kortikosteroid kullanımı ile görme bozukluğu bildirilebilir. Bir hasta bulanık görme veya diğer görme bozuklukları gibi semptomlarla başvurursa, hastanınsistemik ve topikal kortikosteroidlerin kullanımından sonra bildirilmiş katarakt, glokom veyasantral seröz koryoretinopati (CSCR) gibi nadir hastalıkları içerebilecek olası nedenlerindeğerlendirilmesi için bir oftalmoloji uzmanına sevki düşünülmelidir.
Büyüme geriliği Ruhsatlı dozlarda nazal kortikosteroid alan çocuklarda büyüme geriliği bildirilmiştir. Bir yıl boyunca günde bir kez 110 mikrogram flutikazon furoat ile tedavi edilen çocuklarda büyümehızında bir azalma gözlenmiştir (Bkz. Bölüm 4.8 ve 5.1). Bu nedenle çocuklar yeterlisemptom kontrolü sağlayan en düşük olası etkili dozda idame ettirilmelidir (Bkz. Bölüm 4.2).Nazal kortikosteroidlerle uzun süreli tedavi alan çocukların büyümesinin düzenli olarakizlenmesi önerilir. Büyüme yavaşlarsa, mümkün olduğunda nazal kortikosteroid dozununsemptomların etkili kontrolünün sürdürüldüğü en düşük doza azaltılması amacıyla tedavigözden geçirilmelidir. Buna ilaveten, hastanın bir pediyatri uzmanına sevk edilmesidüşünülmelidir (Bkz. Bölüm 5.1). Ritonavir kullanan hastalar Artmış sistemik flutikazon furoat maruziyeti riskinden dolayı ritonavir ile eşzamanlı uygulama önerilmemektedir (Bkz. Bölüm 4.5). Yardımcı maddeler FİXFLOW benzalkonyum klorür içerir. İrritan, deri reaksiyonlarına sebep olabilir. Uzun süreli kullanımı nazal mukozada ödeme sebep olabilir. 4.5. Diğer tıbbi ürünler ile etkileşimler ve diğer etkileşim şekilleriCYP3A inhibitörleri ile etkileşim Flutikazon furoat, karaciğerdeki sitokrom P450 3A4 izoenzimi ile gerçekleştirilen ilk geçiş metabolizmasıyla dolaşımdan hızla temizlenir. CYP3A4 yoluyla metabolize olan başka bir glukokortikoidden (flutikazon propionat) elde edilen verilere dayalı olarak, ritonavir ile eşzamanlı uygulama, flutikazon furoata artmışsistemik maruziyet riski nedeniyle önerilmemektedir. Sistemik yan etki riskinde bir artış beklendiğinden, flutikazon furoatın, kobisistat içeren ürünler dahil olmak üzere potent CYP3A inhibitörleri ile eşzamanlı uygulanması sırasındadikkatli olunması önerilmektedir. Fayda, sistemik kortikosteroid yan etkileri riskindekiartıştan daha ağır basmadıkça eşzamanlı uygulamadan kaçınılmalıdır; eşzamanlı uygulamadurumunda hastalar sistemik kortikosteroid yan etkileri açısından takip edilmelidir. İntranazalflutikazon furoat ile potent CYP3A4 inhibitörü ketokonazolün incelendiği bir ilaç etkileşimiçalışmasında, plasebo (20 gönüllünün 1'inde) ile karşılaştırıldığında ketokonazol grubunda(20 gönüllünün 6'sında) ölçülebilir flutikazon furoat konsantrasyonlarının olduğu gönüllüsayısı daha fazla olmuştur. Maruziyetteki bu küçük artış, iki grup arasında 24 saatlik serumkortizol düzeylerinde istatistiksel olarak anlamlı bir farklılığa yol açmamıştır. Enzim inhibisyonu ve indüksiyonu verilerine göre klinikte kullanılan dozlarda flutikazon furoat ile diğer bileşiklerin sitokrom P450 enzimleri tarafından gerçekleştirilenmetabolizmaları arasında teorik olarak ilaç-ilaç etkileşimi beklenmez. Bu nedenle flutikazonfuroatın diğer ilaçlar üzerindeki etkilerini araştırmak için klinik çalışmalar yürütülmemiştir. Özel popülasyonlara ilişkin ek bilgilerBu yaş grubunda herhangi bir etkileşim çalışması yapılmamıştır. Pediyatrik popülasyon:Bu yaş grubunda herhangi bir etkileşim çalışması yapılmamıştır.
4.6. Gebelik ve laktasyonGenel tavsiye:Gebelik Kategorisi C Çocuk doğurma potansiyeli bulunan kadınlar/Doğum kontrolü (Kontrasepsiyon):FIXFLOW' un çocuk doğurma potansiyeli bulunan kadınlarda kullanımına ilişkin yeterli veri mevcut değildir. Gebelik dönemi:FİXFLOW' un gebe kadınlarda kullanımına ilişkin yeterli veri mevcut değildir. Hayvanlar üzerinde yapılan çalışmalar, gebelik / ve-veya / embriyonal / fetal gelişim / ve-veya / doğum /ve-veya / doğum sonrası gelişim üzerindeki etkiler bakımından yetersizdir (bkz. Bölüm 5.3).insanlara yönelik potansiyel risk bilinmemektedir. Flutikazon furoatın gebe kadınlarda kullanımına ilişkin yeterli veri mevcut değildir. Hayvan çalışmalarında glukokortikoidlerin yarık damak ve intrauterin büyüme geriliği dahilmalformasyonları indüklediği gösterilmiştir. Bu durum, minimum sistemik maruziyetlesonuçlanan önerilen nazal dozlar verilen insanlar için ilişkili değildir (Bkz. Bölüm 5.2).Flutikazon furoat hamilelik sırasında yalnızca anne adayında elde edilmesi beklenen faydalar,fetusun karşılaşabileceği risklerden fazlaysa kullanılmalıdır. FIXFLOW gerekli olmadıkça gebelik döneminde kullanılmamalıdır. Laktasyon dönemi:Nazal olarak uygulanan flutikazon furoatın insan sütüne geçip geçmediği bilinmemektedir. Emziren kadınlarda flutikazon furoat kullanımı, yalnızca annede elde edilmesi beklenen fayda çocukta oluşturduğu herhangi bir olası risklerden fazla olduğunda düşünülmelidir. Üreme yeteneği / Fertilite:Insanlarda fertilite verisi bulunmamaktadır. 4.7. Araç ve makine kullanımı üzerindeki etkilerFIXFLOW' un araç veya makine kullanma yeteneği üzerinde bir etkisi yoktur ya da önemsiz düzeydedir. 4.8. İstenmeyen etkilerGüvenlilik profilinin özeti Flutikazon furoat tedavisi sırasında en yaygın bildirilen advers reaksiyonlar epistaksis, nazal ülserasyon ve baş ağrısıdır. En ciddi istenmeyen etkiler seyrek olarak bildirilen anafilaksidahil aşırı duyarlılık reaksiyonlarıdır (1000 hastada 1 vakadan daha az). Advers reaksiyonların listesi Flutikazon furoatın güvenlilik ve etkililik çalışmalarında mevsimsel ve pereniyal alerjik rinit için tedavi gören 2700'den fazla hasta yer almıştır. Flutikazon furoatın güvenlilik ve etkililikçalışmalarında mevsimsel ve pereniyal alerjik rinitte pediyatrik maruziyet, 12 ila <18 yaşta243 hasta, 6 ila <12 yaşta 790 hasta ve 2 ila <6 yaşta 241 hasta olmuştur. Belge DoBelge Takip Adresi:https://www.turkiye.gov.tr/saglik-titck-ebysAdvers reaksiyonların sıklığını belirlemek amacıyla, büyük klinik çalışmalarda elde edilen veriler kullanılmıştır. Advers olay âiıkilğıekaşağidakie gib^adeğıerlendirilmiştir:  Çok yaygın (>1/10); yaygın (>1/100 ila <1/10); yaygın olmayan (>1/1.000 ila <1/100); seyrek (>1/10.000 ila <1/1.000); çok seyrek (<1/10.000), bilinmiyor (mevcut verilerden tahminedilemiyor). Bağışıklık sistemi hastalıklarıSeyrek: Anaflaksi, anjiyoödem, deri döküntüsü ve ürtikeri de kapsayan aşırı duyarlılık reaksiyonları Sinir sistemi hastalıklarıYaygın: Baş ağrısı Göz hastalıklarıBilinmiyor:Gözle ilgili geçici değişiklikler (Bkz. Bölüm 5.1), bulanık görme (Bkz. Bölüm 4.4) Solunum, göğüs bozuklukları ve mediastinal hastalıklar
Çok yaygın: Yaygın:
Yaygın olmayan: Çok seyrek: Bilinmiyor: Burun kanaması* Nazal ülserasyon, dispne** Rinalji, burun rahatsızlıkları (burunda yanma, burunda tahriş ve burunda ağrı gibi), burun kuruluğu. *Burun kanaması, genellikle hafif-orta şiddette olmuştur. Burun kanamasının yetişkinlerdeki ve ergenlerdeki insidansı uzun süreli (>6 hafta) kullanımda, kısa süreli (<6 hafta) kullanımakıyasla daha yüksek olmuştur. Pediyatrik hastalarda yapılan süresi 12 haftaya varançalışmalardaki burun kanaması insidansı, flutikazon furoat veya plasebo kullanan hastalardabirbirine yakın bulunmuştur. **Flutikazon furoat ile yapılan klinik çalışmalar sırasında hastaların %1'inden fazlasında dispne vakaları bildirilmiştir; benzer oranlar plasebo gruplarında da gözlenmiştir. Kas-iskelet bozuklukları, bağ doku ve kemik hastalıklarıBilinmiyor: Çocuklarda büyüme geriliği*** (Bkz. Bölüm 5.1) ***Puberte öncesi günde bir kez 110 mikrogram flutikazon furoat kullanan çocuklarda büyümeyi değerlendiren bir yıllık klinik çalışmada, plasebo ile karşılaştırıldığında ortalamayıllık büyüme hızı farkı -0,27 cm olarak gözlenmiştir (Bkz. Bölüm 5.1). Sistemik etkiler Nazal kortikosteroidlerin sistemik etkileri özellikle uzun periyotlarda yüksek dozlarda reçete edildiğinde meydana gelebilir (Bkz. Bölüm 4.4). Nazal kortikosteroidleri alan çocuklardabüyüme geriliği bildirilmiştir. Özel popülasyonlara ilişkin ek bilgiler Pediyatrik popülasyon:6 yaşın altındaki çocuklarda güvenlilik tam olarak belirlenmemiştir. Pediyatrik popülasyonda gözlemlenen advers reaksiyonların sıklığı, tipi ve ciddiyeti yetişkin popülasyondakilerebenzerdir. Şüpheli advers reaksiyonların raporlanmasıRuhsatlandırma sonrası şüpheli ilaç advers reaksiyonlarının raporlanması büyük önem taşımaktadır. Raporlama yapulması^^ıilacknoıyarar^riskzidengesinin sürekli olarak izlenmesine Belge herl^ll^f
Farmakovijilans Merkezi (TÜFAM)'ne bildirmeleri gerekmektedir (www.titck.gov.tr; e-posta: [email protected]; tel: 0 800 314 00 08; faks: 0 312 218 35 99). 4.9. Doz aşımı ve tedavisiBir biyoyararlanım çalışmasında, günde 2640 mikrograma varan intranazal dozların 3 gün boyunca kullanılmasına eşlik eden hiçbir advers sistemik etki gözlenmemiştir (Bkz. Bölüm5.2). Akut doz aşımı, hastanın gözlem altında tutulmasının dışında genellikle herhangi birtedavi gerektirmez. 5. FARMAKOLOJİK ÖZELLİKLER5.1. Farmakodinamik özelliklerFarmakoterapötik grup: Nazal preparatlar, dekonjestanlar ve topikal kullanılan diğer nazal preparatlar, kortikosteroidlerATC kodu: R01AD12 Flutikazon furoat; glukokortikoid reseptör affinitesi ileri derecede yüksek, güçlü anti-inflamatuvar etkilere sahip, sentetik, triflorlu bir kortikosteroiddir. Klinik etkililik ve güvenlilik: Yetişkinlerde ve ergenlerde mevsimsel alerjik rinit:Plaseboya kıyasla günde bir kez 110 mikrogram flutikazon furoat burun spreyi 4 çalışmanın tümünde nazal semptomları (rinore, nazal konjesyon, hapşırmak, nazal kaşıntı) ve okülersemptomları (kaşıntı/yanma, gözde yaşlanma/sulanma ve gözlerde kızarma) anlamlı olarakiyileştirmiştir. Etkililik günde bir kez uygulama ile 24 saatlik doz uygulama periyodu boyuncakorunmuştur. Terapötik etki başlangıcı ilk uygulama sonrası 8 saat gibi erken bir dönemde görülmüş ve bunu izleyen birkaç günde ilave iyileşme gözlenmiştir. Flutikazon furoat burun spreyi 4 çalışmanın tümünde hastaların tedaviye genel yanıt algısını ve hastaların hastalıkla bağlantılı yaşam kalitesini (Rinokonjonktivit yaşam kalitesi anketi-RQLQ) anlamlı olarak iyileştirmiştir. Yetişkinler ve ergenlerde kronik ya da uzun süreli devam eden alerjik rinit:Günde bir kez 110 mikrogram flutikazon furoat burun spreyi üç çalışmada plaseboya kıyasla nazal semptomları ve hastaların tedaviye genel yanıt algısını anlamlı olarak iyileştirmiştir. Günde bir kez 110 mikrogram flutikazon furoat burun spreyi bir çalışmada plaseboya kıyasla oküler semptomları ve hastaların hastalıkla bağlantılı yaşam kalitesini (RQLQ) anlamlı olarakiyileştirmiştir. Etkililik günde bir kez uygulama ile 24 saatlik periyot boyunca korunmuştur. Flutikazon furoatın (günde bir kez 110 mikrogram intranazal sprey) oküler güvenliliğini değerlendirmek üzere tasarlanmış iki yıllık çalışmada, pereniyal alerjik riniti olan yetişkinlerve ergenler ya flutikazon furoat (n=367) ya da plasebo (n=181) kullanmıştır. Birincil sonuçlar [posterior subkapsüler opasitede artışa kadar geçen süre (Lens Opasiteleri Sınıflama Sistemi (LOSS), Versiyon IlI'de başlangıca göre >0,3 (LOSS III derece)) veintraoküler basınç (İOB) a#ttşıpagikadarekgeçeteızsüreni(£baflangıca göre >7 mmHg)] iki grup (başlangıca göre >0,3) 110 mikrogram flutikazon furoat ile tedavi edilen kişilerde [14 (%4)] plaseboya kıyasla [4 (%2)] daha sık olmuş ve flutikazon furoat grubundan on kişide veplasebo grubundan iki kişide yapısal olarak geçici bulunmuştur. İOB artışları (başlangıca göre>7 mmHg) 110 mikrogram flutikazon furoat ile tedavi edilen kişilerde daha sık olmuştur:günde bir kez 110 mikrogram flutikazon furoat için 7 (%2) ve plasebo için 1 (<%1). Buolaylar flutikazon furoat grubundan altı kişi ve plasebo grubundan bir kişide yapısal olarakgeçici olmuştur. 52 ve 104. haftalarda her iki tedavi grubundan hastaların %95'inde her bir gözde posterior subkapsüler opasite değerleri başlangıç değerinin ± 0,1'i içinde olmuştur, 104. haftada her ikitedavi grubundan hastaların <%1'inde posterior subkapsüler opasitede başlangıca göre >0,3artış olmuştur. 52 ve 104. haftalarda hastaların çoğunda (>%95) İOB değerleri başlangıçdeğerinin ± 5mmHg içinde olmuştur. Posterior subkapsüler opasite ya da İOB artışlarınakatarakt ya da glokom gibi herhangi bir advers olay eşlik etmemiştir. Pediyatrik popülasyon:Çocuklarda mevsimsel ve kronik ya da uzun süreli devam eden alerjik rinit:Pediyatrik pozolojide çocuklarda alerjik rinit popülasyonundan etkililik verilerinin değerlendirilmesi temel alınır. Mevsimsel alerjik rinitte, günde bir kez 110 mikrogram flutikazon furoat burun spreyi etkili olmakla birlikte, günde bir kez 55 mikrogram flutikazon furoat burun spreyi ve plaseboarasında hiçbir sonlanım noktasında anlamlı farklar gözlenmemiştir. Perennial alerjik rinitte, günde bir kez 55 mikrogram flutikazon furoat burun spreyi 4 haftalık tedavi boyunca günde bir kez 110 mikrogram flutikazon furoat burun spreyinden daha tutarlıbir etkililik profili ortaya koymuştur. Aynı çalışmada 6 ve 12 hafta boyunca ve 6 haftalıkHPA ekseni güvenlilik çalışmasında yürütülen post-hoc analiz günde bir kez 110 mikrogramflutikazon furoat burun spreyinin etkililiğini desteklemiştir. Günde bir kez 110 mikrogram flutikazon furoat burun spreyinin 2 ila 11 yaşındaki çocuklarda adrenal fonksiyon üzerindeki etkisinin değerlendirildiği 6 haftalık bir çalışma, plaseboyakıyasla 24 saatlik serum kortizolü üzerinde anlamlı bir etkinin söz konusu olmadığınıgöstermiştir. Randomize, çift kör, paralel gruplu, çok merkezli, bir yıllık plasebo kontrollü bir klinik büyüme çalışmasında ergenlik öncesi çağda 474 çocukta (kızlar için 5 ila 7,5 yaş ve erkekleriçin 5 ila 8,5 yaş) stadiometri ile günde bir kez 110 mikrogram flutikazon furoat burunspreyinin büyüme hızı üzerindeki etkisi değerlendirilmiştir. 52 haftalık tedavi periyodundaortalama büyüme hızı plaseboya (5,46 cm/yıl) kıyasla flutikazon furoat (5,19 cm/yıl) kullananhastalarda daha düşüktür. Ortalama tedavi farkı yılda -0,27 cm'dir [%95 CI -0,48 ila -0,06]. Çocuklarda mevsimsel ve kronik ya da uzun sureli devam eden alerjik rinit (6 yaş altı):Hem mevsimsel hem de pereniyal alerjik rinitte 2 ila 5 yaşındaki, 176'sı flutikazon furoata maruz kalmış toplamda 271 hastada güvenlilik ve etkililik çalışmaları yürütülmüştür. Bugrupta güvenlilik ve etkililik iyi bilinmemektedir. 5.2. Farmakokinetik özelliklerGenel özelliklerEmilim:Bdg.DY*.:,yl'Ji|f£gLseçiş metabolizmasına uğrar; bu da ihmal edilebilir sıstemık maruzıyet ile sonuçlanır. Günde bir kez 110 mikrogram intranazal doz uygulaması tipik olarak ölçülebilir plazma konsantrasyonları (<10 pg/ml) ile sonuçlanmaz. İntranazal flutikazon furoat için mutlakbiyoyararlanım %0,50 olup, 110 mikrogramın uygulanmasından sonra sistemik olarak 1mikrogramdan az flutikazon furoat tespit edilir (Bkz. Bölüm 4.9). Dağılım:Flutikazon furoatın plazma proteinlerine bağlanma oranı %99'dan fazladır. Flutikazon furoat vücutta yaygın olarak dağılır ve kararlı plazma düzeylerindeki ortalama dağılım hacmi 608litredir. Biyotransformasyon:Flutikazon furoat sistemik dolaşımdan, başlıca hepatik metabolizma aracılığıyla sitokrom P450 enzimi CYP3A4 ile (toplam plazma klerensi 58,7 L/s) inaktif 17P-karboksilikmetabolitine (GW694301X) dönüştürülerek hızla temizlenir. Başlıca metabolizma yolu S-florometil karbotioat fonksiyonunun17P-karboksilik metaboliti oluşturmak üzere hidrolizidir. In vivoçalışmalarda furoat kısmının flutikazon oluşturmak üzere parçalandığına dair birkanıta rastlanmamıştır.Eliminasyon:Oral veya intravenöz flutikazon furoatın esas olarak dışkı yoluyla eliminasyonu, bu kortikosteroidin ve metabolitlerinin safra yoluyla atıldığını göstermektedir. İntravenözkullanımı izleyen eliminasyon fazı yarı-ömrü 15,1 saattir. Oral ve intravenöz dozlarınsırasıyla %1'i ve %2'si, böbrekler yoluyla vücuttan atılır. Hastalardaki karakteristik özelliklerBöbrek bozukluğu:Sağlıklı gönüllülerde intranazal uygulama sonrası flutikazon furoat, idrarda ölçülebilen düzeylerde değildir. Dozla ilişkili materyalin %1'inden daha küçük bir bölümü idrarlaatıldığından böbrek bozukluğunun, flutikazon furoat farmakokinetiğini etkilemesibeklenmemektedir. Karaciğer bozukluğu:
enmez.
jö3 ' Belge Takip Adresi:https://www.turkiye.gov.tr/saglik-titck-ebysKaraciğer bozukluğu olan hastalarda intranazal flutikazon furoat ile yapılmış bir çalışma bulunmamaktadır. Karaciğer bozukluğu olan hastalara flutikazon furoatın inhaleuygulamasından sonra (flutikazon furoat ya da flutikazon furoat/vilanterol şeklinde), eldeedilen veriler intranazal uygulama için de geçerlidir. Tek doz oral inhale 400 mikrogramlıkflutikazon furoatla ilgili bir çalışmada, orta derecede karaciğer yetmezliği (Child Pugh B) olanhastalarda sağlıklı deneklere kıyasla, artan Cmaks (%42) ve EAA(0-ro) (%172) ile ortadüzeyde kortizol düzeylerinde azalma (ortalama olarak %23) ile sonuçlanmıştır. Oral inhaleflutikazon furoat/vilanterolun 7 gün süreyle tekrarlı dozlarından sonra orta dereceli ila şiddetlikaraciğer bozukluğu (Child-Pugh B - C) olan hastalarda, sağlıklı gönüllüler ilekarşılaştırıldığında, flutikazon furoat sistemik maruziyetinde artış olmuştur (EAA(0-24) ileölçüldüğünde ortalama iki kat). Flutikazon furoat sistemik maruziyetinde orta derecelikaraciğer bozukluğu olan hastalardaki artış (flutikazon furoat/vilanterol 200/25 mikrogram),sağlıklı gönüllüler ile karşılaştırıldığında serum kortizol düzeyinde ortalama %34'lük birdüşüş ile ilişkilendirilmiştir. Şiddetli karaciğer bozukluğu olan hastalarda serum kortizolüzerinde herhangi bir etki olmamıştır (flutikazon furoat/vilanterol 100/12,5 mikrogram). Bubulgulara dayanılarak, 110 mikrogram intranazal flutikazon furoatın orta derecede şiddetlikaraciğer bozukluğu (Child-Pugh B) olan hastalardaki öngörülen ortalama maruziyetinin, Bdg.D£i-«3be Pediyatrik popülasyon:Hastaların çoğunda, günde bir kez 110 mikrogram dozunda verilen flutikazon furoat tipik olarak plazmada ölçülemeyecek düzeylerdedir (<10 pikogram/mL). Pediyatrik hastaların%15,1'inde günde bir kez 110 mikrogram intranazal flutikazon furoatı takiben ve yalnızca%6,8'sinde günde bir kez 55 mikrogram intranazal flutikazon furoatı takiben ölçülebilirdüzeyler tespit edilmiştir. Daha küçük çocuklarda (6 yaşın altındaki çocuklar) flutikazonfuroatın ölçülebilir düzeylerinin daha yüksek insidansına dair bir kanıt yoktur. 55mikrogramda ölçülebilir düzeye sahip deneklerde ortalama flutikazon furoat konsantrasyonu2-5 yaş ve 6-11 yaş için sırasıyla 18,4 pikogram/mL ve 18,9 pikogram/mL'dir. 110mikrogramda ölçülebilir düzeylere sahip olan deneklerde ortalama flutikazon furoatkonsantrasyonu 2-5 yaş ve 6-11 yaş için sırasıyla 14,3 pikogram/mL ve 14,4pikogram/mL'dir. Sonuçlar 12 yaş üzeri ergenlerde görülen sonuçlar ile benzerdir (55mikrogramda ölçülebilir düzeye sahip deneklerde ortalama konsantrasyon 15,4 pikogram/mL,110 mikrogramda ölçülebilir düzeye sahip deneklerde ortalama konsantrasyon 21,8pikogram/mL). Geriyatrik popülasyon:Bu yaş grubuna ait farmakokinetik veriler yalnızca az sayıda (> 65 yaş, n=23/872; %2,6) hastadan elde edilmiştir. Plazmada ölçülebilen flutikazon furoat konsantrasyonlarıinsidansının ileri yaşlardaki hastalarda, gençlerdekinden daha yüksek olduğunu gösterenhiçbir kanıt yoktur. 5.3. Klinik öncesi güvenlilik verileriGenel toksikoloji çalışmalarından elde edilen bulgular, diğer glukortikoidlerle gözlemlenenlere benzer olup, aşırı farmakolojik aktivite ile ilişkilidir. Önerilen nazal dozlarınminimum sistemik maruziyetle sonuçlandığı göz önünde bulundurulduğunda, bu bulgularıninsanlar için geçerli olması muhtemel değildir. Konvansiyonel genotoksisite testlerindeflutikazon furoat ile genotoksik etki gözlemlenmemiştir. Ayrıca, sıçanlar ve farelerdeyürütülen iki yıllık inhalasyon çalışmalarında tümör insidansında tedaviyle ilişkili artışolmamıştır. 6. FARMASÖTİK ÖZELLİKLER6.1. Yardımcı maddelerin listesiGlukoz anhidrat Mikrokristalize selüloz ve karmelloz sodyum Polisorbat 80 Benzalkonyum klorür (%50'lik) Disodyum edetat Saf su 6.2. GeçimsizliklerGeçerli değildir. 6.3. Raf ömrü24 ay. 6.4. Saklamaya yönelik özel tedbirler25°C altındaki oda sıcaklığında saklanmalıdır. Buzdolabında saklamamalı veya dondurulmamalıdır.
6.5. Ambalajın niteliği ve içeriğiFİXFLOW, ölçülü doz sprey pompası takılı 15 mL'lik amber renkli cam şişe (Tip III) içerisinde sunulmaktadır. Bir şişe burun spreyinde 120 püskürtmelik ürün bulunmaktadır. 6.6. Beşeri tıbbi üründen arta kalan maddelerin imhası ve diğer özel önlemlerKullanılmamış olan ürünler ya da atık materyaller Tıbbi atıkların kontrolü yönetmeliği ve Ambalaj atıklarının kontrolü yönetmeliğine uygun olarak imha edilmelidir. 7. RUHSAT SAHİBİAbdi İbrahim İlaç San. ve Tic. A.Ş. Reşitpaşa Mahallesi, Eski Büyükdere Caddesi No:4 34467 Maslak/Sarıyer/İstanbulTel: 0212 366 84 00Faks: 0212 276 20 20 8. RUHSAT NUMARASI2023/468 9. İLK RUHSAT TARİHİ/RUHSAT YENİLEME TARİHİİlk ruhsat tarihi: 29.11.2023 Ruhsat yenileme tarihi: 10. KÜB'ÜN YENİLENME TARİHİ
|
İlaç BilgileriFixflow 27.5 Mcg Burun Spreyi, SüspansiyonEtken Maddesi: Flutikazon Furoat Kullanma talimatı ve kısa ürün bilgileri
Google Reklamları
İlgili İlaçlar |
Ana Sayfa | Hakkımızda | İlaçlar | İlaç Ara | İlaç Firmaları | Gizlilik | Bize Ulaşın
Telif Hakkı 2008-2026 © İlaç Prospektüsü. Tüm Hakları Saklıdır.Uyarı: Sitemizde yayınladığımız ilaç bilgileri ile doktora danışmadan kesinlikle ilaç kullanmayınız!
Aksi halde doğabilecek sağlık sorunlarından ilacprospektusu.com sorumlu tutulamaz.




