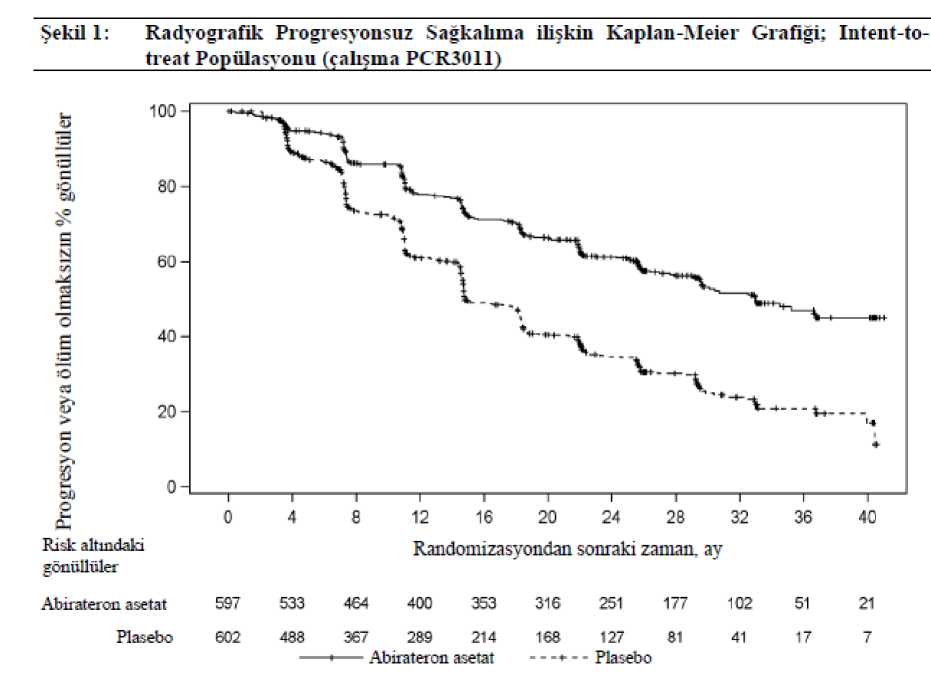
Abetyl 250 Mg Tablet Kısa Ürün BilgisiKISA URUN BILGISI¡Bu ilaç ek izlemeye tabidir. Bu üçgen yeni güvenlilik bilgisinin hızlı olarak belirlenmesini sağlayacaktır. Sağlık mesleği mensuplarının şüpheli advers reaksiyonları TÜFAM'abildirmeleri beklenmektedir. Bakınız Bölüm 4.8 Advers reaksiyonlar nasıl raporlanır?1. BEŞERI TIBBİ ÜRÜNÜN ADIABETYL 250 mg tablet 2. KALİTATİF VE KANTİTATİF BİLEŞİMEtkin madde:Her bir tablet 250 mg abirateron asetat içerir.Yardımcı maddeler:Her bir tablet 198,65 mg laktoz monohidrat (sığır sütünden elde edilir), 42,9 mg kroskarmelloz sodyum ve 28,6 mg sodyum lauril sülfat içerir.Yardımcı maddeler için Bölüm 6.1'e bakınız. 3. FARMASÖTİK FORMTablet. Beyazdan kirli beyaza renkli, oval, bikonveks, bir yüzü A 250 baskılı diğer yüzü düz tabletler. 4. KLİNİK ÖZELLİKLER4.1 Terapötik endikasyonlarABETYL, prednizon veya prednizolon ile birlikte aşağıdaki durumların tedavisinde endikedir: - Yetişkin erkeklerde androjen baskılama tedavisi (ADT) ile birlikte yeni teşhis edilmiştanımlanan yüksek risk* faktörlerinden en az 2tanesi olan metastatik hormona duyarlıprostat kanserinin (mHDPK) tedavisinde progresyona ya da kabul edilemeyecek yan etkioluşana kadar endikedir.*Yüksek Risk Faktörleri: 1) Gleason skorunun >8olması2) Üç veya daha fazla sayıda kemik lezyonu olması3) Ölçülebilir visseral (lenf nodu hastalığı hariç) metastaz olması - Kemoterapinin henüz klinik olarak endike olmadığı androjen baskılama tedavisininbaşarısızlığından sonra asemptomatik veya hafif semptomatik olan viseral metastazı olmayan yetişkin erkeklerde metastatik kastrasyon dirençli prostat kanserinin (mKDPK) tedavisinde progresyona ya da kabul edilemeyecek yan etki oluşana kadar endikedir.Dosetaksel bazlı bir kemoterapi tedavisinde veya sonrasında hastalığı ilerleyen yetişkinerkeklerde mKDPK tedavisinde endikedir. 4.2 Pozoloji ve uygulama şekliPozoloji/uygulama sıklığı ve süresiBu tıbbi ürün uygun bir sağlık mesleği mensubu tarafından reçete edilmelidir. ABETYL günde tek seferde 1.000 mg (dört adet 250 mg tablet) olarak yutulmalı ve yiyeceklerle birlikte alınmamalıdır (uygulama şekli bölümüne bakınız). ABETYL'inyiyeceklerle birlikte alınması ilaca sistemik maruziyeti arttırır (bkz. Bölüm 4.5 ve 5.2). Prednizon veya Prednizolon dozu ABETYL, metastatik hormona duyarlı prostat kanserli hastalarda günde 5 mg prednizon veya prednizolon ile birlikte kullanılır. ABETYL, metastatik kastrasyona dirençli prostat kanserli hastalarda günde 10 mg prednizon veya prednizolon ile birlikte kullanılır. Cerrahi kastrasyon uygulanmamış hastalarda tedavi sırasında luteinizan hormon serbestleyici hormon (LHRH) analoğu ile tıbbi kastrasyona devam edilmelidir. Önerilen izlemABETYL ile tedaviye başlamadan önce serum transaminaz düzeyleri ölçülmelidir; tedavininilk üç ayında iki haftada bir, daha sonra ayda bir bu testler tekrarlanmalıdır. Hastalar kanbasıncı, serum potasyumu ve sıvı retansiyonu açısından aylık olarak izlenmelidir. Bununlabirlikte, konjestif kalp yetmezliği açısından anlamlı bir risk taşıyan hastalar tedavinin ilk 3 ayıboyunca iki haftada bir, daha sonra ise ayda bir kere izlenmelidir (bkz. Bölüm 4.4). Daha önceden hipokalemisi olan ya da ABETYL tedavisi sırasında hipokalemi gelişen hastalarda, hastanın potasyum düzeyinin 4,0 mM ve üzerinde tutulması değerlendirilmelidir. Hipertansiyon, hipokalemi, ödem ve diğer mineralokortikoid dışı toksisiteler dahil olmak üzere, Derece 3 ve üzerinde toksisite gelişen hastalarda, tedavi durdurulmalı ve uygun tıbbitedaviye başlanmalıdır. Toksisite semptomları Derece 1 ya da başlangıç düzeyine dönünceyekadar ABETYL tedavisine yeniden başlanmamalıdır. ABETYL, prednizon veya prednizolonun günlük dozunun alınmasının unutulması durumunda, tedaviye ertesi gün olağan günlük dozla devam edilmelidir. Uygulama şekli:ABETYL ağızdan alınır. Tabletler günde bir kez aç karnına tek doz olarak alınmalıdır. ABETYL, yemeklerden en az 1 saat önce ya da yemekten en az iki saat sonra alınmalıdır. Tabletler bütün olarak suylayutulmalıdır. Özel popülasyonlara ilişkin ek bilgiler HepatotoksisiteABETYL tedavisi sırasında hepatotoksisite gelişen hastalarda (alanin aminotransferaz [ALT] veya aspartat aminotransferaz [AST] düzeylerinin normal kabul edilen üst sınırın 5 katındanfazla yükselmesi) tedavi hemen durdurulmalıdır (bkz. Bölüm 4.4). Karaciğer fonksiyontestleri tedaviye başlamadan önceki başlangıç değerlerine döndükten sonra tedaviye azaltılmışdozla günde 500 mg (iki tablet) olarak başlanabilir. Tedaviye yeniden başlanan bu hastalardaserum transaminaz düzeyleri, tedavinin ilk üç ayında iki haftada bir, daha sonra ise ayda birölçülmelidir. Azaltılmış 500 mg'lık günlük dozla da hepatotoksisite tekrarlarsa, tedavitümüyle kesilmelidir. Tedavinin herhangi bir döneminde ağır hepatotoksisite gelişmesi durumunda (ALT ya da AST düzeylerinin normal kabul edilen üst sınırın 20katı kadar yükselmesi) tedaviye hemen sonverilmeli ve ABETYL ile yeniden tedavi uygulanmamalıdır.Karaciğer yetmezliği:Önceden hafif şiddette karaciğer bozukluğu olan hastalarda (Child-Pugh Sınıf A) doz ayarlamasına gerek yoktur. Orta şiddette karaciğer yetmezliğinin (Child Pugh sınıf B), abirateron asetatın oral yoldan tek doz halinde 1.000mg alınması sonrası abiraterona sistemik maruziyeti yaklaşık dört katarttırdığı gösterilmiştir (bkz. Bölüm 5.2). Orta şiddette veya ağır karaciğer yetmezliği (Child-Pugh sınıf B veya C) olan hastalarda abirateron asetatın birden fazla dozunun klinik güvenlilikve etkililiğini gösteren bir veri bulunmamaktadır. Bu tür hastalarda doz ayarlamasıöngörülemez. ABETYL kullanımı faydanın olası riskten açıkça ağır bastığı, orta şiddettekaraciğer yetmezliğine sahip hastalarda dikkatle değerlendirilmelidir (bkz. Bölüm 4.2 ve 5.2).ABETYL şiddetli karaciğer yetmezliği olan hastalarda kullanılmamalıdır (bkz. Bölüm 4.3, 4.4 ve 5.2). Böbrek yetmezliği:Böbrek yetmezliği olan hastalarda doz ayarlamasına gerek yoktur (bkz. Bölüm 5.2). Ancak prostat kanserli ağır böbrek yetmezliği olan hastalarda klinik deneyim bulunmamaktadır. Butür hastalarda dikkatli olunması tavsiye edilmektedir (bkz. Bölüm 4.4). Pediyatrik popülasyon:Pediyatrik popülasyonda prostat kanseri görülmediğinden ABETYL'in çocuklarda ve adolesanlarda kullanımı bulunmamaktadır. Geriyatrik popülasyon:Yaşlı hastalarda herhangi bir doz ayarlaması gerekmemektedir. 4.3 Kontrendikasyonlar- Abirateron asetata veya Bölüm 6.1'de listelenen herhangi bir yardımcı maddeye karşı aşırıduyarlılık varsa, - Gebe olan ya da gebe olma olasılığı bulunan kadınlarda (bkz. Bölüm 4.6), - Ağır karaciğer yetmezliği olanlarda [Child-Pugh sınıf C (bkz. Bölüm 4.2, 4.4 ve 5.2)]kontrendikedir. - ABETYL ile prednizon veya prednizolon Ra-223 ile kombine kullanımda kontrendikedir. 4.4 Özel kullanım uyarıları ve önlemleriMineralokortikoid fazlalığına bağlı hipertansiyon, hipokalemi, sıvı retansiyonu ve kalp yetmezliğiABETYL, CYP17 inhibisyonu sonucunda (bkz. Bölüm 5.1) artan mineralokortikoid düzeylerindeki artışa bağlı olarak hipertansiyon, hipokalemi ve sıvı retansiyonuna (bkz.Bölüm 4.8) yol açabilir. ABETYL ile birlikte kortikosteroid uygulanması,adrenokortikotropik hormon (ACTH) salgılanmasını baskılayarak bu advers etkilerin görülmesıklığı ve şiddetinde bir azalma sağlar. Kan basıncının yükselmesi, hipokalemi (örneğinkardiyak glikozidleri kullanan hastalar) veya sıvı retansiyonu (örneğin kalp yetmezliği olanhastalar, ağır veya stabil olmayan anjina pektoris, yakın zamanda miyokard enfarktüsü veyaventriküler aritmi ve ağır böbrek yetmezliği) nedeniyle altta yatan tıbbi durumu risk altınagirebilecek hastalar tedavi edilirken dikkatli olunmalıdır. ABETYL kardiyovasküler hastalık öyküsü olan hastalarda dikkatle kullanılmalıdır. Hipertansiyonu kontrol altına alınamayan, miyokard enfarktüsüyle ortaya çıkmış klinik açıdananlamlı kalp hastalığı olan, son 6ayda arteriyel trombotik olay geçirmiş olan, ağır ya daunstabil anjinası olan, New York Kalp Cemiyeti (NYHA) Sınıf III ve IV kalp yetmezliği olan(çalışma 301) ya da Sınıf II'den IV'e kalp yetmezliği (çalışma 3011 ve 302) olan ya dakardiyak ejeksiyon fraksiyonu %50'nin altında olan hastalar Faz 3 çalışmalara dahiledilmemiştir. Medikal terapi gerektiren atriyal fibrilasyonu veya diğer kardiyak aritmisi olanhastalar çalışma 3011 ve 302'den çıkarılmıştır. Sol ventrikül ejeksiyon fraksiyonu (LVEF)%50'nin altında olan hastalar ya da New York Kalp Cemiyeti (NYHA) Sınıf III ve IV kalpyetmezliği olan (çalışma 301'de) ya da NYHA Sınıf II'den IV'e kalp yetmezliği (çalışma3011 ve 302) olan hastalarda güvenlilik değerlendirilmemiştir (bkz. Bölüm 4.8 ve 5.1).Konjestif kalp yetmezliği açısından anlamlı risk taşıyan hastaların tedavi edilmesinden önce (örneğin, kalp yetmezliği, kontrol altına alınamayan hipertansiyon ya da iskemik kalphastalığı gibi kalp olayları), kalp fonksiyonunun bir değerlendirmesinin yapılmasıdüşünülmelidir (örneğin, ekokardiyogram). ABETYL ile tedaviden önce, kalp yetmezliğitedavi edilmeli ve kalp fonksiyonu mümkün olan en iyi düzeyeçıkarılmalıdır. Hipertansiyon,hipokalemi ve sıvı retansiyonu düzeltilmeli ve kontrol altına alınmalıdır. Tedavi sırasında, 3ay süreyle 2haftada bir ve daha sonra ayda bir kere olmak üzere kan basıncı, serum potasyum,sıvı retansiyonu (kilo artışı, periferik ödem) ve diğer konjestif kalp yetmezliği bulgu vebelirtileri izlenmeli ve anormallikler düzeltilmelidir. Abirateron asetat ile ilişkili hipokalemigörülen hastalarda QT uzaması gözlenmiştir. Kalp fonksiyonunda klinik olarak anlamlı birazalma olması durumunda, kalp fonksiyonu klinik endikasyona göre değerlendirilmeli, uyguntedavi başlatılmalı ve ABETYL tedavisinin kesilmesi değerlendirilmelidir (bkz. Bölüm 4.2).Hepatotoksisite ve karaciğer yetmezliğiKontrollü klinik çalışmalarda karaciğer enzimlerinde ilacın kesilmesine ya da doz değişikliğine neden olan belirgin artışlar bildirilmiştir (bkz. Bölüm 4.8). ABETYL ile tedaviyebaşlamadan önce serum transaminaz düzeyleri ölçülmelidir; tedavinin ilk üç ayında ikihaftada bir, daha sonra ayda bir bu testler tekrarlanmalıdır. Hepatotoksisitenin klinik belirtiveya bulguları görülür görülmez, hemen serum transaminaz düzeyleri ölçülmelidir. Tedavininherhangi bir yerinde ALT ya da AST düzeyleri normal kabul edilen üst sınırın (NÜS) 5katından fazla yükselen hastalarda ABETYL tedavisine hemen ara verilmeli ve karaciğerfonksiyonları yakından takip edilmelidir. ABETYL ile yeniden tedaviye ancak karaciğer fonksiyon testleri başlangıç değerlerine döndüğünde ve azaltılmış dozlarla başlanabilir (bkz. Bölüm 4.2). Tedavinin herhangi bir döneminde ağır hepatotoksisite gelişmesi durumunda (ALT ya da AST düzeylerinin normal kabul edilen üst sınırın 20 katı kadar yükselmesi) ABETYL tedavisikesilmeli ve bir daha başlatılmamalıdır. Klinik çalışmalara aktif veya semptomatik viral hepatiti olan hastalar dahil edilmemiştir; bu nedenle abirateron asetatın bu popülasyonda kullanımını destekleyen bir veribulunmamaktadır. Orta şiddette veya ağır karaciğer yetmezliği (Child-Pugh sınıf B veya C) olan hastalarda abirateron asetatın birden fazla dozunun klinik güvenlilik ve etkililiğini gösteren bir veribulunmamaktadır. ABETYL kullanımı faydanın olası riskten açıkça ağır bastığı, orta şiddettekaraciğer yetmezliğine sahip hastalarda dikkatle değerlendirilmelidir (bkz. Bölüm 4.2 ve 5.2).ABETYL şiddetli karaciğer yetmezliği olan hastalarda kullanılmamalıdır (bkz. Bölüm 4.2,4.3 ve 5.2). Akut karaciğer yetmezliği ve fulminant hepatit tanımlayan az sayıda pazarlama sonrası rapor mevcuttur. Bunların bazıları ölümle sonuçlanmıştır (bkz. Bölüm 4.8). Kortikosteroidin geri çekilmesi ve stresli durumların karşılanmasıPrednizon veya prednizolon tedavisinin kesilmesi durumunda dikkatli olunması ve adrenokortikal yetmezlik gelişmemesi için hastaların izlenmesi önerilir. Kortikosteroidlerkesildikten sonra ABETYL tedavisine devam edilecekse, hastalar mineralokortikoidfazlalığına bağlı semptomlar açısından izlenmelidir (bkz. Bölüm 4.4 Mineralokortikoidfazlalığına bağlı hipertansiyon, hipopotasemi, hipokalemi sıvı retansiyonu ve kalp yetmezliğibaşlığı). Prednizon veya prednizolon kullanan hastalarda olağan dışı stres ortaya çıktığında, bu stresli durum öncesinde, sırasında ve sonrasında kortikosteroid dozunun arttırılması gerekebilir. Kemik dansitesiİleri evre metastatik prostat kanseri olan erkeklerde kemik dansitesinde azalma görülebilir. ABETYL'in bir glukokortikoid ile birlikte kullanımı bu etkiyi arttırabilir. Daha önceden ketokonazol kullanımıDaha önceden prostat kanseri için ketokonazol kullanmış olan hastalarda daha düşük yanıt oranları beklenebilir. HiperglisemiGlukokortikoid kullanımı hiperglisemiyi artırabileceğinden, diyabetli hastalarda kan şekeri sıklıkla ölçülmelidir. Diyabetik hastalarda abirateron ile birlikte kullanılacak kortikosteroidlerkan şekeri regülasyonunu bozabileceğinden dikkatli kullanılmalıdır. HipoglisemiPioglitazon veya repaglinid alan önceden diyabeti olan hastalara abirateron asetat ve prednizon/prednizolon uygulandığında hipoglisemi vakaları bildirilmiştir (bkz. bölüm 4.5);bu nedenle diyabetli hastalarda kan şekeri takibi yapılmalıdır. Kemoterapi ile kullanımABETYL'in sitotoksik kemoterapi ile eşzamanlı olarak kullanılmasının güvenliliği ve etkililiği gösterilmemiştir (bkz. Bölüm 5.1). Potansiyel risklerABETYL ile tedavi görenler de dahil, prostat kanseri olan erkeklerde anemi ve cinsel işlev bozukluğu görülebilir. İskelet kası etkileriAbirateron asetat ile tedavi gören hastalarda miyopati ve rabdomiyoliz vakaları bildirilmiştir. Bu olayların çoğu tedavinin ilk 6ayında ortaya çıkmış ve abirateron asetatın kesilmesindensonra düzelmiştir. Miyopati/rabdomiyoliz ile ilişkili olduğu bilinen ilaçlarla eş zamanlı tedavigören hastalarda dikkatli olunması önerilir.Diğer tıbbi ürünler ile etkileşimAzalmış ABETYL maruziyeti riski nedeniyle, başka bir tedavi seçeneği olmadığı sürece tedavi sırasında güçlü CYP3A4 indükleyicilerinden kaçınılmalıdır (bkz. Bölüm 4.5). Abirateron ve prednizon/ prednizolonun Ra-223 ile kombinasyonuRa-223 ile kombinasyon halinde abirateron ve prednizon/prednizolon ile tedavi, asemptomatik veya hafif semptomatik prostat kanseri hastalarda yürütülen klinik çalışmalarda gözlendiğiüzere artmış kırık riski ve artmış mortalite eğilimi nedeniyle kontrendikedir (bkz. Bölüm 4.3). ABETYL'in prednizon/ prednizolon ile kombine kullanıldığı son dozunu takiben en az 5 gün süreyle ardışık tedavide Ra-223 başlanması önerilmemektedir. Yardımcı maddelere karşı intoleransBu tıbbi ürün laktoz ihtiva eder. Nadir kalıtımsal galaktoz intoleransı, totallaktaz yetmezliği ya da glukoz-galaktoz malabsorbsiyon problemi olan hastaların bu ilacı kullanmamalarıgerekir. Bu tıbbi ürünün dört tabletlik her bir dozunda 24,8 mg sodyum ihtiva eder. Bu durum, kontrollü sodyum diyetinde olan hastalarda göz önünde bulundurulmalıdır. 4.5 Diğer tıbbi ürünler ile etkileşimler ve diğer etkileşim şekilleriYiyeceklerin abirateron asetat üzerindeki etkisiABETYL'in yiyeceklerle birlikte alınması abirateron asetatın emilimini anlamlı derecede arttırır. ABETYL'in yiyeceklerle birlikte alınması halindeki etkililik ve güvenliliğigösterilmemiştir, bu yüzden ABETYL yiyeceklerle birlikte alınmamalıdır (bkz. Bölüm 4.2 ve5.2). Diğer tıbbi ürünler ile etkileşimlerDiğer ilaçların abirateron maruziyetlerini etkileme potansiyeli Güçlü bir CYP3A4 indükleyicisi olan rifampisin ile önce 61.000mg'lık abirateron asetat dozu verilensağlıklı gönüllülerde yürütülen bir klinik farmakokinetik etkileşim çalışmasında, ortalamaabirateron plazma EAA® değeri %55 azalmıştır.Başka bir tedavi seçeneği olmadığı sürece tedavi sırasında güçlü CYP3A4 indükleyicilerinden kaçınılmalıdır (örneğin; fenitoin, karbamazepin, rifampisin, rifabutin, rifapentin, fenobarbital,St. John's wort (sarı kantaron - Rypericum perforatum).Sağlıklı gönüllülerde yürütülen ayrı bir klinik farmakokinetik etkileşim çalışmasında, güçlü bir CYP3A4 inhibitörü olan ketokonazolün eşzamanlı uygulaması abirateronunfarmakokinetiği üzerinde klinik olarak anlamlı bir etki yaratmamıştır. Abirateronun diğer ilaçların maruziyetini etkileme potansiyeliAbirateron, hepatik ilaç metabolize eden CYP2D6 ve CYP2C8 enzimlerinin bir inhibitörüdür. Abirateron asetatın (artı prednizon) tek dozda alınan CYP2D6 substratı dekstrometorfanüzerindeki etkisini belirlemek için yapılan bir çalışmada, dekstrometorfanın sistemikmaruziyetinin (EAA) yaklaşık 2,9 kat arttığı bildirilmiştir. Dekstrometorfanın aktif metabolitidekstrorfanın EAA 24'ü ise yaklaşık %33 artmıştır.ABETYL, özellikle dar terapötik indekse sahip ilaçlar olmak üzere, CYP2D6 tarafından aktive veya metabolize edilen ilaçlarla birlikte alındığında dikkatli olunmalıdır. CYP2D6tarafından metabolize edilen dar terapötik indekse sahip ilaçların dozunun azaltılmasıdeğerlendirilmelidir. CYP2D6 tarafından metabolize edilen ilaçlara örnek olarak metoprolol,propranolol, desipramin, venlafaksin, haloperidol, risperidon, propafenon, flekanid, kodein,oksikodon ve tramadol gösterilebilir (kodein, oksikodon ve tramadolun aktif analjezikmetabolitlerinin oluşabilmesi için CYP2D6 gereklidir). Sağlıklı gönüllüler üzerinde yapılan bir CYP2C8 ilaç-ilaç etkileşim çalışmasında, pioglitazon 1.000 mg'lık tek doz abirateron asetat ile birlikte verildiğinde, pioglitazonun EAA değeri %46artmış ve pioglitazonun aktif metabolitleri olan M-III ve M-IV için EAA değerleri %10azalmıştır. CYP2C8 substratı olan dar terapötik aralıklı ilaçlar ile birlikte ABETYLkullanılması durumunda hastalar toksisite semptomları açısından izlenmelidir. CYP2C8tarafından metabolize edilen tıbbi ürünlere örnekler arasında pioglitazon ve repaglinidbulunmaktadır (bkz. bölüm 4.4). İn vitroortamda, abirateronun majör metabolitleri olan abirateron sülfat ve N-oksit abirateron sulfatın karaciğer alım taşıyıcısı OATP1B1'i inhibe ettiği ve sonuçta da OATP1B1 tarafındanelimine edilen ilaçların konsantrasyonlarını artırabileceği gösterilmiştir. Taşıyıcı bağlıetkileşimi teyit edecek klinik veri yoktur.QT aralığını uzattığı bilinen ilaçlar ile kullanımıAndrojen azaltma tedavisi QT aralığını uzattığından, QT aralığını uzattığı bilinen ilaçlar ile ABETYL verirken veya sınıf IA (örn. kinidin, disopiramid) gibi Torsade de pointesindükleyebilecek ya da sınıf III (örn. amiadoron, sotalol, dofetilid, ibutilid) gibi antiaritmatikürünler, metadon, moksifloksasin, antipsikotikler gibi ürünler ile verilirken dikkatli olunmasıönerilir. Spironolakton ile kullanımSpironolakton androjen reseptörüne bağlanır ve prostat spesifik antijen (PSA) seviyelerini artırabilir. ABETYL ile kullanımı önerilmez (bkz. Bölüm 5.1). Özel popülasyonlara ilişkin ek bilgilerHerhangi bir etkileşim çalışması yapılmamıştır. Pediyatrik popülasyon:Herhangi bir etkileşim çalışması yapılmamıştır. 4.6 Gebelik ve laktasyonGenel tavsiyeGebelik kategorisi: X ABETYL kadınlarda kullanımı olan bir ilaç değildir. ABETYL gebe olan ya da gebe olma olasılığı bulunan kadınlarda kontrendikedir (bkz. Bölüm 4.3 ve 5.3). Çocuk doğurma potansiyeli bulunan kadınlarGebelikte ABETYL kullanımına ilişkin klinik bir veri mevcut değildir ve ABETYL çocuk doğurma potansiyeli bulunan kadınlarda kullanım için bir ilaç değildir. ABETYL'in gebelik döneminde uygulandığı takdirde ciddi doğum kusurlarına yol açtığından şüphelenilmektedir. ABETYL, gebelik döneminde kontrendikedir (bkz. Bölüm 4.3). Doğum kontrolü (kontrasepsiyon)ABETYL ya da metabolitlerinin semende bulunup bulunmadığı bilinmemektedir. Hastanın gebe bir kadınla cinsel ilişkiye girmesi durumunda kondom kullanması gerekir. Hastanınçocuk doğurma potansiyeli bulunan bir kadınla cinsel ilişkiye girmesi durumunda etkili birdoğum kontrol yöntemine ek olarak kondom kullanması gerekir. Hayvanlarda yapılançalışmalar üreme toksisitesi olduğunu göstermiştir (bkz. Bölüm 5.3). Gebelik dönemiABETYL kadınlarda kullanımı olan bir ilaç değildir ve gebelik döneminde ya da gebelik potansiyeline sahip kadınlarda kontrendikedir (bkz. Bölüm 4.3 ve 5.3). Laktasyon dönemiABETYL kadınlarda kullanımı olan bir ilaç değildir. Üreme yeteneği / FertiliteAbirateron asetat erkek ve dişi sıçanlarda fertiliteyi etkilemiş olmakla birlikte bu etkiler tamamen geri dönüşümlü olmuştur (bkz. Bölüm 5.3). 4.7 Araç ve makine kullanımı üzerindeki etkilerABETYL'in araç ve makine kullanımı yeteneği üzerinde etkisi yoktur ya da ihmal edilebilir düzeydedir. 4.8 İstenmeyen etkilerGüvenlilik profilinin özetiBirleştirilmiş Faz 3 çalışmalarının istenmeyen yan etkiler üzerindeki bir analizinde, abirateron asetat ile hastaların % 10'unda veya fazlasında gözlemlenen istenmeyen etkiler; periferiködem, hipokalemi, hipertansiyon, idrar yolu enfeksiyonu ve alanin aminotransferazdüzeylerinde yükselme ve/veya aspartat aminotransferaz düzeylerinde yükselmedir. Diğerönemli advers etkiler arasında kalp hastalıkları, hepatotoksisite, kırıklar ve alerjik alveolitbulunur.ABETYL, etki mekanizmasının farmakodinamik sonucu olarak hipertansiyon, hipokalemi ve sıvı retansiyonuna neden olabilir. Faz 3 çalışmalarında, abirateron asetat ile tedavi edilenhastalarda, plasebo ile tedavi edilen hastalara oranla beklenen mineralokortikoid advers etkilerdaha yaygın olarak görülmüştür. Çalışmada hipokalemi abirateron asetat alanlarda %18 ikenplasebo alanlarda % 8%22%6iken plasebo alanlarda %1;abirateron asetat ile tedavi edilen hastalarda Grad 3 ve 4 hipertansiyon (CTCAE, versiyon 4.0sınıflamasına göre) %7 iken plasebo alanlarda %5; abirateron asetat ile tedavi edilenhastalarda Grad 3 ve 4 sıvı retansiyonu (periferal ödem) %1 iken plasebo alanlarda %1 olarakgözlemlenmiştir. Mineralokortikoid reaksiyonlar tıbbi tedaviyle genellikle başarıylayönetilebilmiştir. Kortikosteroidlerin birlikte kullanılması bu advers ilaç reaksiyonlarınınsıklık ve şiddetini azaltır (bkz. Bölüm 4.4).Advers reaksiyonların özetiLuteinizan hormon salgılayıcı hormon (LHRH) analoğunun kullanılmakta olduğu ya da daha önceden orşiektomi tedavisi uygulanmış ileri evre metastatik prostat kanserli hastalardakiçalışmalarda, abirateron asetat, düşük doz prednizon veya prednizolon (endikasyona bağlıolarak günlük 5 veya 10 mg) ile kombine olarak günde 1.000 mg dozunda kullanılmıştır. Klinik çalışmalarda ve pazarlama sonrası deneyimlerde gözlenen advers etkiler aşağıdaki sıklık derecelerine göre listelenmiştir. Çok yaygın (>1/10); yaygın (>1/100 ila <1/10); yaygınolmayan (> 11.0001100110.00011000110000),bilinmiyor (eldeki verilerden hareketle tahmin edilemiyor).Her bir sıklık grubunda, istenmeyen etkiler azalan ciddiyet sırasına göre sunulmuştur. Enfeksiyonlar ve enfestasyonlarÇok yaygın: İdrar yolu enfeksiyonu Yaygın: Sepsis Bağışıklık sistemi hastalıklarıBilinmiyor: Anafilaktik reaksiyonlar Endokrin hastalıklarıYaygın olmayan: Adrenal yetmezlik Metabolizma ve beslenme hastalıklarıÇok yaygın: Hipokalemi Yaygın: Hipertrigliseridemi Kardiyak hastalıklarYaygın: Kalp yetmezliği*, anjina pektoris, atrial fibrilasyon, taşikardi Yaygın olmayan: Diğer aritmiler Bilinmiyor: Miyokard enfarktüs, QT uzaması (bkz. Bölüm 4.4 ve 4.5) Vasküler hastalıklarÇok yaygın: Hipertansiyon Solunum, göğüs hastalıklarıve mediastinal hastalıklarSeyrek: Alerjik alveolita Gastrointestinal hastalıklarÇok yaygın: Diyare Yaygın: Dispepsi Hepato-bilier hastalıklarÇok yaygın: Alanin aminotransferaz düzeylerinde yükselme ve/veya aspartat aminotransferaz düzeylerinde yükselmeb Seyrek: Fulminant hepatit, akut karaciğer yetmezliği Deri ve deri altı doku hastalıklarıYaygın: Döküntü Kas-iskelet bozuklukları, bağ doku ve kemik hastalıklarıYaygın olmayan: Miyopati, rabdomiyoliz Böbrek ve idrar yolu hastalıklarıYaygın: Hematüri Genel bozukluklar ve uygulama bölgesine ilişkin hastalıklarÇok yaygın: Periferik ödem Yaralanma ve zehirlenmeYaygın: Kırıklar** * Kalp yetmezliği aynı zamanda konjestif kalp yetmezliği, sol ventriküler disfonksiyon ve ejeksiyon fraksiyonunda azalmayı da içermektedir. **Kırıklar, osteoporozu ve patolojik kırık dışındaki tüm kırıkları içerir. a Pazarlama sonrası deneyimden spontan bildirimler b Alanin aminotransferaz düzeyinde yükselme ve/veya aspartat aminotransferaz düzeyinde yükselme, ALT düzeyinde yükselmeyi, AST düzeyinde yükselmeyi ve anormal karaciğerfonksiyonunu içerir. Abirateron asetat ile tedavi edilen hastalarda aşağıdaki Grad 3 advers ilaç reaksiyonları (CTCAE, versiyon 4.0 sınıflamasına göre) görülmüştür: %5 hipokalemi; %2 idrar yoluenfeksiyonu; %4 alanin aminotransferaz düzeyinde yükselme ve/veya aspartataminotransferaz düzeyinde yükselme, %6%2%1periferik ödem, kalpyetmezliği ve atrial fibrilasyon. CTCAE (versiyon 4.0) Grad 3 hipertrigliseridemi ve anjinapektoris hastaların %1'inden azında meydana gelmiştir. Hastaların %1'inden azında Grad 4idrar yolu enfeksiyonu, alanin aminotransferaz düzeyinde yükselme ve/veya aspartataminotransferaz düzeyinde yükselme, hipokalemi, kalp yetmezliği, atriyal fibrilasyon vekırıklar görülmüştür.Hormona duyarlı popülasyonda (çalışma 3011) hipertansiyon ve hipokalemi daha yüksek bir insidansta gözlemlenmiştir. Hormona duyarlı popülasyonda (çalışma 3011) hastaların%36,7'sinde hipertansiyon rapor edilmişken, çalışma 301 ve 302'de sırasıyla %11,8 ve%20,2'idi. Hormona duyarlı popülasyonda hastaların %20,4'ünde hipokalemigözlemlenmişken (çalışma 3011), çalışma 301 ve 302'de sırasıyla %19,2 ve %14,9'idi. ECOG2 performans durum skoru temel olan alt grup hastalarda ve ayrıca yaşlı hastalarda (>75 yaş), yan etkilerin görülme sıklığı ve ciddiyeti daha yüksekti. Seçilmiş advers reaksiyonların tanımlanmasıKardiyovasküler etkilerAbirateron asetat ile yürütülen üç Faz 3 çalışmasında da, hipertansiyonu kontrol altına alınamayan, miyokard enfarktüsüyle ortaya çıkmış klinik açıdan anlamlı kalp hastalığı olan,son 6ayda arteriyel trombotik olay geçirmiş olan, ağır ya da unstabil anjinası olan, New YorkKalp Cemiyeti (NYHA) Sınıf III ve IV kalp yetmezliği (çalışma 301) ya da Sınıf II ila IV kalpyetmezliği (çalışma 3011 ve 302) olan ya da kardiyak ejeksiyon fraksiyon ölçümü %50'dendüşük olan hastalar çalışmaya dahil edilmemiştir. Çalışmaya alınan diyabet, miyokardenfarktüsü, serebrovasküler olay ve ani kardiyak ölüm riski olan tüm hastalara (hem aktif ilaç,hem de plasebo alanlar) aynı zamanda öncelikle LHRH analogları kullanılarak androjenazaltma tedavisi uygulanmıştır. Faz 3 çalışmasında kardiyovasküler advers reaksiyonlarınsıklığı abirateron asetat alanlarda ve plasebo alanlarda aşağıdaki gibi bulunmuştur: atriyalfibrilasyon %2,6 ve %2,0; taşikardi, %1,9 ve %1,0; anjina pektoris %1,7 ve %0,8; kalpyetmezliği %0,7 ve %0,2 ve aritmi, %0,7 ve %0,5.HepatotoksisiteAbirateron asetat ile tedavi edilen hastalarda ALT, AST ve total bilirubin düzeylerinde yükselmeyle seyreden hepatotoksisite bildirilmiştir. Faz 3 klinik çalışmalarında, abirateronasetat alan hastaların yaklaşık % 6'sında tipik olarak tedaviye başladıktan sonraki ilk 3 aydaGrad 3 ve 4 karaciğer toksisitesi (örneğin, ALT ve AST düzeylerinde normal kabul edilen üstsınırın 5 katından fazla yükselme veya bilirubin düzeylerinde normal kabul edilen üst sınırın1,5 katından fazla yükselme) bildirilmiştir. Çalışma 3011'de, abirateron asetat ile tedavi edilenhastaların %8,4'ünde Grad 3 ve 4 hepatotoksisite gözlemlenmiştir. Abirateron asetat alanhastalardan 10'unda hepatotoksisite sebebiyle tedavi sonlandırılmıştır; bunlardan ikisi Grad 2hepatotoksisite, altı tanesi Grad 3 hepatotoksisite ve 2 tanesi Grad 4 hepatotoksisitedir.Çalışma 3011'de hepatotoksisite sebebiyle ölen hasta olmamıştır. Faz 3 klinik çalışmalarında,başlangıç ALT veya AST düzeyleri yüksek olan hastalarda, başlangıç değerleri normalolanlara göre karaciğer fonksiyon testlerinde artış olasılığı daha yüksek olmuştur.ALT veya AST düzeylerinde normal kabul edilen üst sınırın 5 katından fazla yükselme olduğunda ya da bilirubin düzeylerinde normal kabul edilen üst sınırın 3 katından fazlayükselme olduğunda abirateron asetat tedavisine ara verilmiş ya da kesilmiştir. İki vakadakaraciğer fonksiyon testlerinde belirgin yükselmeler görülmüştür (bkz. Bölüm 4.4). Başlangıçdeğerleri normal olan bu iki hastada ALT veya AST düzeyleri normal üst sınır değerlerin 15ila 40 katı ve bilirubin düzeyleri ise normal üst sınır değerlerin 2 ila 6110,6olarak bildirilmiştir; hepatotoksisite olaylarınabağlı hiçbir ölüm vakası bildirilmemiştir.Klinik çalışmalarda başlangıçta hepatiti ya da karaciğer fonksiyon testlerinde anlamlı anormallikleri olan hastalar hariç tutulmak suretiyle hepatotoksisite riski azaltılmıştır.Çalışma 3011'de, başlangıç ALT ve AST değerleri NÜS'ün 2,5 katından fazla olan hastalar,bilirubin değerleri normal kabul edilen üst sınırın 1,5 katından fazla olan hastalar ve aktif veyasemptomatik viral hepatit veya kronik karaciğer hastaları; karaciğer fonksiyon bozukluğunabağlı assit veya kanama bozukluğu olan hastalar çalışmaya alınmamıştır. Çalışma 301'de,başlangıç ALT ve AST düzeyleri karaciğer metastazının olmadığı durumlarda normal kabuledilen üst sınırın >2,5 katı, metastaz olanlarda ise normal kabul edilen üst sınırın >5 katı olanhastalar çalışmaya dahil edilmemiştir. Çalışma 302'de, karaciğer metastazı olanlar vebaşlangıç ALT ve AST düzeyleri > 2,5 x NÜS olan hastalar çalışmaya alınmamıştır. Klinikçalışmaya alınan hastalarda karaciğer fonksiyon testlerinde anormalleşme olduğunda ise, buhastaların tedavileri kesilmiş ve ancak karaciğer fonksiyon testleri tedavinin başlangıcındakidüzeylerine döndükten sonra yeniden tedavi almalarına izin verilmiştir (bkz. Bölüm 4.2). ALTve AST düzeyleri normal kabul edilen üst sınırın 20 katından fazla yükselen hastalardayeniden tedavi uygulanmamıştır. Bu tür hastalarda tedaviye yeniden başlamanın güvenliliğibilinmemektedir. Abirateron asetat tedavisi sırasında gelişen hepatotoksisitenin mekanizmasıbilinmemektedir. Şüpheli advers reaksiyonların raporlanmasıRuhsatlandırma sonrası şüpheli ilaç advers reaksiyonlarının raporlanması büyük önem taşımaktadır. Raporlama yapılması, ilacın yarar / risk dengesinin sürekli olarak izlenmesineolanak sağlar. Sağlık mesleği mensuplarının herhangi bir şüpheli advers reaksiyonu TürkiyeFarmakovijilans Merkezi (TÜFAM)'ne bildirmeleri gerekmektedir (www.titck.gov.tr; e-posta: [email protected]; tel: 0 800 314 00 08; faks: 0 312 218 35 99). 4.9 Doz aşımı ve tedavisiAbirateron asetat ile doz aşımına dair insan deneyimi sınırlıdır. Spesifik antidotu yoktur. Doz aşımı durumunda ABETYL uygulaması durdurularak aritmilerin, hipokalemi ve sıvı retansiyonunun bulgu ve belirtilerinin izlenmesi de dahil olmaküzere genel destekleyici önlemler alınmalıdır. Karaciğer fonksiyonları dadeğerlendirilmelidir. 5. FARMAKOLOJİK ÖZELLİKLER5.1 Farmakodinamik özelliklerFarmakoterapötik grup: Endokrin tedavisi, diğer hormon antagonistleri ve ilişkili ajanlar ATC kodu: L02BX03 Etki mekanizmasıAbirateron asetat (ABETYL) in vivoolarak bir androjen biyosentez inhibitörü olan abiraterona dönüşür. Spesifik olarak abirateron 17a-hidroksilaz/C17,20-liyaz (CYP17)enzimini seçici olarak inhibe eder. Bu enzim testiküler, adrenal ve prostatik tümör dokularındaeksprese olur ve androjenin biyosentezi için gereklidir. CYP17 enzimi, sırasıyla 17a-hidroksilasyon ve C17,20 bağının kırılmasıyla pregnenolon ve progesteronun testesteronprekürsörleri olan DHEA ve androstenediona dönüşümünü katalize eder. CYP17 inhibisyonuaynı zamanda adrenaller tarafından mineralokortikoid üretiminde artışa da yol açar (bkz.Bölüm 4.4).Androj ene duyarlı prostat karsinomu, androj en düzeylerini azaltan tedaviye yanıt verir. LHRH agonistleri ya da orşiektomi gibi androjen azaltıcı tedaviler, testislerdeki androjen üretiminiazaltmalarına rağmen, adrenaller ya da tümör dokusundaki androjen üretimini etkilemezler.LHRH agonistleri (ya da orşiektomi) ile birlikte ABETYL tedavisi uygulandığında serumtestesteron düzeyleri (ticari testlerle ölçüldüğünde) saptanabilir düzeylerin altına düşer. Farmakodinamik etkilerABETYL, serum testesteron ve diğer androjen seviyelerini, tek başına LHRH analogları ya da orşiektomi ile elde edilen seviyelerin altına düşürür. Bu, androjen biyosentezi için gerekliolan CYP17 enziminin selektif olarak inhibe edilmesinin bir sonucudur. Prostat spesifikantijen (PSA) prostat kanserli hastalarda bir biyogösterge olarak kullanılır. Daha öncetaksanlarla yapılan kemoterapiden fayda görmeyen hastalarda gerçekleştirilen bir Faz 3 klinikçalışmada, abirateron asetat ile tedavi edilen hastaların %38'inde başlangıç PSA değerlerinegöre en az %50 azalma sağlanabilmişken, bu azalma oranı plasebo ile tedavi edilenlerin ancak% 10'unda sağlanabilmiştir.Klinik etkililik ve güvenlilikAbirateron asetatın etkililiği metastatik hormona duyarlı prostat kanseri (mHDPK) ve metastatik kastrasyona dirençli prostat kanseri (mKDPK) olan hastalarda gerçekleştirilenplasebo kontrollü çok merkezli randomize üç Faz 3 çalışmayla (çalışma 3011, 302 ve 301)gösterilmiştir. Çalışma 3011'e, yüksek riskli prognostik faktörlere sahip yeni tanı almış(randomizasyondan önceki 3 ay içerisinde) mHDPK'li hastalar dahil edilmiştir. Yüksek riskliprognoz aşağıdaki 3 risk faktöründen en az 2'sine sahip olmak olarak tanımlanmıştır: (1)Gleason skorunun >8olması; (2) kemik taramasında 3 veya daha fazla lezyon olması; (3)ölçülebilir visseral (lenf nodu hastalığı hariç) metastaz olması. Aktif tedavi kolunda, standarttedavi olan ADT'ye (LHRH analoğu veya orşiektomi) ilave olarak, abirateron asetat günde1.000 mg dozunda, günde tek doz 5 mg düşük doz prednizon ile kombine olarak uygulandı.Kontrol kolundaki hastalara abirateron asetat ve prednizon yerine ADT ve plasebo verildi.Çalışma 301'e daha önceden dosetaksel kullanmış hastalar, çalışma 302'ye ise daha öncedosetaksel kullanmamış hastalar dahil edilmiştir. Hastalar bir LHRH agonisti kullanıyorlardıya da daha önce orşiektomi olmuşlardı. Aktif tedavi uygulanan kolda, abirateron asetat, gündeiki defa 5 mg düşük doz prednizon ya da prednizolonla kombine olarak günde 1.000 mgdozunda kullanılmıştır. Kontrol grubundaysa plaseboya ek olarak günde iki defa 5 mg düşükdoz prednizon ya da prednizolon uygulanmıştır.Serum PSA konsantrasyonlarındaki değişiklikler bağımsız olarak her zaman klinik faydayı göstermeyebilir. Bu nedenle, tüm çalışmalarda hastaların aşağıda verilen tedavi kesilmekriterlerini karşılamalarına kadar tedaviye devam etmeleri önerilir. Spironolakton androjen reseptörüne bağlandığından ve PSA seviyelerini artırabileceğinden, tüm çalışmalarda spironolakton kullanımına izin verilmemiştir. Çalışma 3011 (yeni tanı almış yüksek riskli mHDPK hastaları)Çalışma 3011'e (n=1.199) dahil edilen hastaların medyan yaşı 67 idi. Abirateron asetat ile tedavi edilen hastaların 832'si (%69,4) beyaz ırka mensup, 246'sı (%20,5) Asyalı, 25'i (%2,1)Siyahi veya Afro Amerikan, 80'i (%6,7) diğer, 13'ü (%1,1) bilinmeyen/raporlanmamış ve 3'ü(%0,3) Amerikan yerlisi veya Alaska yerlisi idi. Hastaların %97'si için ECOG performansstatüsü 0 veya 1 idi. Bilinen beyin metastazı, kontrol altına alınamayan hipertansiyonu, önemlikalp hastalığı olan veya NYHA Sınıf II-IV kalp yetmezliği olan hastalar çalışmayaalınmamıştır. Metastatik hastalıktan kaynaklanan semptomların tedavisi için 3 aya kadar ADTveya 1kür palyatif radyasyon veya operasyon tedavisi alan hastalar haricinde daha öncefarmakoterapi, radyasyon terapisi veya metastatik prostat kanseri operasyonu geçirerek tedaviedilen hastalar çalışmaya alınmamıştır. Ortak birincil etkililik sonlanım noktaları genelsağkalım (OS) ve radyografik progresyonsuz sağkalım (rPFS) idi. Kısa Ağrı Envanteri KısaForm (BPI-SF) ile ölçülen medyan başlangıç ağrı skoru hem tedavi kolunda hem de plasebogruplarında 2.0 idi. Ortak birincil sonlanım noktaları ölçümlerine ilave olarak; iskeletle ilişkiliolaya (SRE) kadar geçen süre, prostat tedavisi için sonraki tedaviye kadar geçen süre,kemoterapi başlangıcına kadar geçen süre, ağrı progresyonuna kadar geçen süre ve PSAprogresyonuna kadar geçen süre kullanılarak tedavi faydası da değerlendirildi. Tedavi hastalıkprogresyonuna, onamın geri çekilmesine, kabul edilemez toksisite veya ölüme kadar devametti.Radyografik progresyonsuz sağkalım, randomizasyondan radyografik progresyon görülmesine veya herhangi bir nedene bağlı ölüme kadar geçen süre olarak tanımlandı.Radyografik progresyon, kemik taramasıyla progresyonu (modifiye PCWG2'ye göre) veyaBT veya MRG ile yumuşak doku lezyonlarındaki progresyonu (RECIST 1.1'e göre)kapsıyordu. Tedavi grupları arasında rPFS bakımından anlamlı bir farklılık gözlendi (bkz. Tablo 1 ve Şekil 1).
Not: += sansürlenmiş gözlem, NE=hesaplanamaz. rPFS olayını tanımlamada radyografik progresyon ve ölüm dikkate alınmıştır. AA-P= abirateron asetat ve prednizolon alan hastalar.a p değeri, ECOG PS skoruna (0/1 veya 2) ve visseral varlığına (yok veya var) göretabakalandırılmış bir log-rank testinden hesaplanmıştır. b Risk oranı tabakalandırılmış orantısal riskler modelinden hesaplanmıştır. Risk oranı < 1 AA-P lehine Plasebo artı ADT'ye kıyasla ölüm riskinde %34'lük bir azalma ile OS'de AA-P artı ADT lehine istatistiksel olarak anlamlı bir iyileşme gözlemlendi (HR=0,66; %95 CI: 0,56, 0,78; p<0,0001)(bkz. Tablo 2 ve Şekil 2).
NE= Hesaplanmadı 1Risk oranı, tabakalandırılmış orantısal riskler modelinden hesaplanmıştır. Risk oranı <1 AA-P (abirateron asetat ve prednizolon alan hastalar) lehine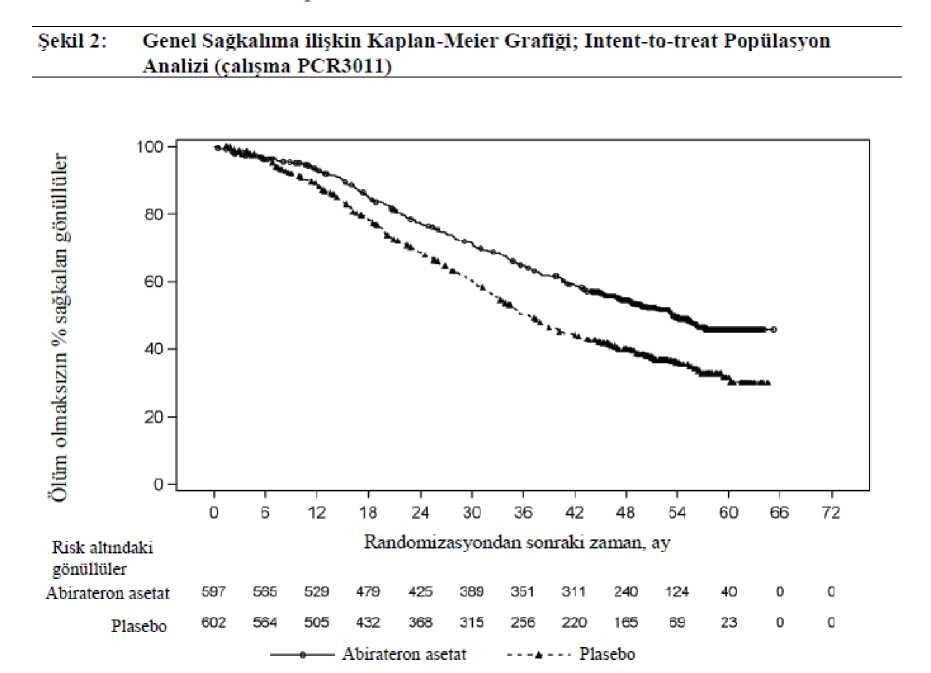
Alt grup analizleri AA-P ile tedaviyi sürekli olarak desteklemektedir. Önceden belirlenmiş alt gruplarda AA-P'nin rPFS ve OS üzerindeki tedavi etkisi genel çalışma popülasyonundadaha üstün ve tutarlı olurken, ECOG skoru 2 olan alt grupta lehde bir yarar gözlenememiştir,ancak örneklem büyüklüğünün küçük olması (n=40) anlamlı bir sonuç çıkarılmasınıkısıtlamıştır. Genel sağkalım ve rPFS'de gözlenen artışlara ilave olarak, prospektif olarak tanımlanan tüm ikincil sonlanım noktaları için plasebo karşısında abirateron asetat lehine faydalargösterilmiştir. Çalışma 302 (daha önce kemoterapi almamış hastalar)Bu çalışmaya asemptomatik veya hafif düzeyde semptomatik olan ve henüz kemoterapi endikasyonu bulunmayan kemoterapi almamış hastalar dahil edilmiştir. Kısa Ağrı Envanteri- Kısa Formunun (BPI-SF) son 24 saat içindeki en kötü ağrı maddesinin puanının 0-1 olmasıasemptomatik, puanın 2-3 olması ise hafif semptomatik olarak değerlendirildi. Çalışma 302'de (n = 1.088) yer alan hastaların medyan yaşı abirateron asetat ile birlikte prednizon veya prednizolon alan hastalar için 71, plasebo ile birlikte prednizon veyaprednizolon alan hastalar için 70 idi. Abirateron asetat ile tedavi edilen hastaların ırklarınagöre dağılımı şöyleydi: 520 (%95,4) beyaz ırk, 15 (%2,8) siyah ırk, 4 (%0,7) sarı ırk ve 6(%1,1) diğer ırklar. Doğu Ortak Onkoloji Grubu (ECOG) performans durumu, her iki koldakihastaların %76'sı için 0 ve %24'ü için 1 idi. Hastaların %50'si yalnızca kemik metastazlarına,%31'i kemik ve yumuşak doku veya lenf nodu metastazlarına ve %19'u yalnızca yumuşakdoku veya lenf nodu metastazlarına sahipti. Visseral metastazı olan hastalar çalışmayaalınmamıştır. Ortak birincil etkinlik sonlanım noktaları genel sağkalım ve radyografikprogresyonsuz sağkalım (rPFS) idi. Ortak birincil sonlanım noktaları ölçümlerine ilave olarak;kanser ağrısı için opiat kullanımına kadar geçen süre, sitotoksik kemoterapi başlangıcınakadar geçen süre, ECOG performans durumunda > 1 puanlık kötüleşmeye kadar geçen süreve Prostat Kanseri Çalışma Grubu 2 (PCWG2) kriterlerine göre PSA progresyonuna kadargeçen süre kullanılarak tedavi faydası da değerlendirildi. Bariz klinik progresyon durumundaçalışma tedavilerine son verildi. Araştırmacı kararıyla, doğrulanmış radyografik progresyonile de tedavi kesilebilecekti. Radyografik progresyonsuz sağkalım (rPFS) PCWG2 kriterlerinde (kemik lezyonları için) tanımlanan seri görüntüleme çalışmalarına ve Solid Tümörlerde Yanıt DeğerlendirmeKriterleri'ne (RECIST) göre (yumuşak doku lezyonları için) değerlendirildi. rPFS analizinde,radyografik progresyon değerlendirmesi merkezi inceleme ile yapılmıştır. Planlı rPFS analizi 401 olayı kapsamış, abirateron asetat ile tedavi edilen hastaların 150'si (%28) ve plasebo ile tedavi edilen hastaların 251'i (%46) ya radyografik progresyon bulgusugöstermiş ya da hastalar ölmüştür. Tedavi grupları arasında rPFS bakımından anlamlı birfarklılık gözlendi (bkz. Tablo 3 ve Şekil 3).
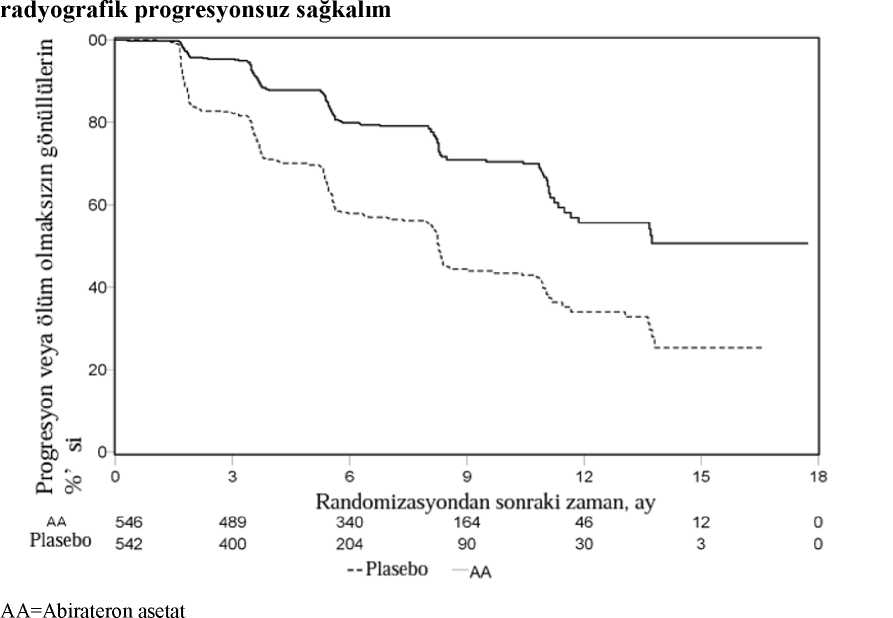
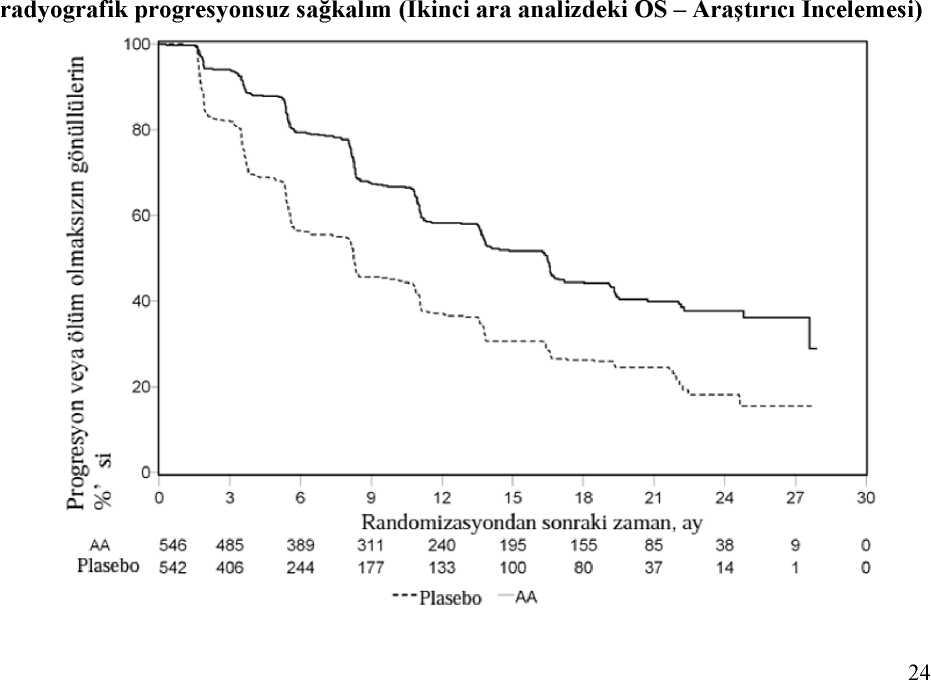
Ancak, Genel Sağkalıma (OS) ilişkin ikinci ara analiz tarihine kadar hasta verisi toplanmaya devam edilmiştir. Araştırmacının rPFS üzerinde bir takip duyarlılık analizi olarak yaptığıradyografik inceleme Tablo 4 ve Şekil 4'te sunulmuştur. 271'i (%50) abirateron asetat grubundan, 336'sı (%62) plasebo grubundan olmak üzere toplam 607 hasta radyografik progresyon göstermiş veya ölmüştür. Abirateron asetat iletedavi, plaseboya kıyasla radyografik progresyon riskini %47'ye kadar azaltmıştır (HR =0,530; %95 GA: [0,451; 0,623], p < 0,0001). Medyan rPFS, abirateron asetat grubunda 16,5ay, plasebo grubunda ise 8,3 ay olmuştur.
* p-değeri, başlangıçtaki ECOG skoruna (0 veya 1) göre tabakalandırılmış bir log-rank testinden hesaplanmıştır. Risk oranı < 1 abirateron asetat lehine
AA=Abirateron asetat333 ölüm gözlendikten sonra, OS için planlı bir ara analiz (lA) yapıldı. Gözlenen klinik faydanın büyüklüğü dikkate alınarak çalışmanın körlüğü kaldırıldı ve plasebo grubundakihastalara abirateron asetat ile tedavi olmaları teklif edildi. Abirateron asetat ölüm riskini %25azaltarak plaseboya kıyasla daha uzun bir genel sağkalım sağladı (HR = 0,752; %95 GA:[0,606; 0,934], p = 0,0097), ancak OS olgunlaşmamıştı ve ara analiz sonuçları istatistikselanlamlılık için önceden belirlenmiş durdurma sınırını karşılamıyordu (bkz. Tablo 3). Bu araanaliz sonrasında, sağkalım takibine devam edildi. OS için planlanan nihai analiz 741 ölüm gözlendikten sonra yapıldı (medyan takip süresi 49 ay). Abirateron asetat ile tedavi edilen hastaların %65'inin (354/546), plasebo ile tedavi edilenhastaların ise %71'inin (387/542) öldüğü saptandı. Ölüm riskinde %19,4'lük bir azalma ile,OS bakımından abirateron asetat ile tedavi edilen grup lehine istatistiksel olarak anlamlı birfayda (HR = 0,806; %95 GA: [0,697; 0,931], p = 0,0033) ve 4.4 aylık medyan OS artışısağlanmıştır (abirateron asetat 34,7 ay, plasebo 30,3 ay) (bkz. Tablo 5 ve Şekil 5). Bu iyileşme,plasebo kolundaki hastaların %44'ü müteakip tedavi olarak abirateron asetat almış olmalarınarağmen gösterilmiştir.
NE = Hesaplanmadı * p-değeri, başlangıçtaki ECOG skoruna (0 veya 1) göre tabakalandırılmış bir log-rank testinden hesaplanmıştır. ** Risk oranı < 1 abirateron asetat lehine Şekil 5: Kaplan Meier grafiğinde abirateron asetat veya plasebo ile birlikte prednizon veya prednizolon ve LHRH agonistleri ya da öncesinde orşiektomi olmuş hastalardakigenel sağkalım - nihai analiz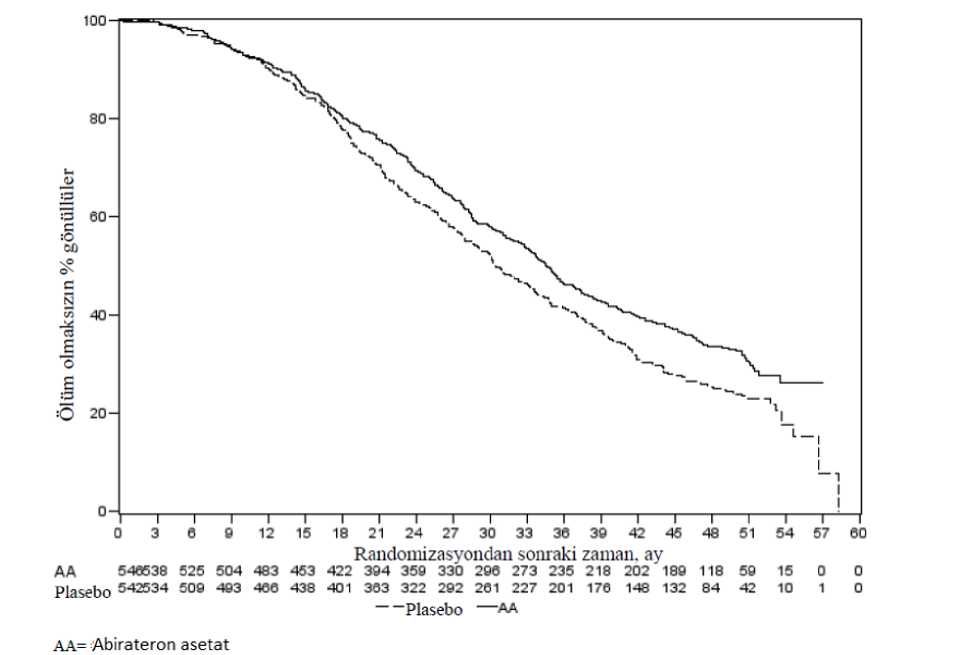
Genel sağkalım ve rPFS'de gözlenen artışlara ilave olarak, tüm ikincil sonlanım noktaları için plasebo karşısında abirateron asetat lehine aşağıdaki faydalar gösterilmiştir: PCWG2 kriterlerine göre PSA progresyonuna kadar geçen süre: PSA progresyonuna kadar geçen medyan süre abirateron asetat alan hastalar için 11,1ay, plasebo alan hastalar için ise5,6 ay olmuştur (HR = 0,488; %95 GA: [0,420; 0,568], p < 0,0001). PSA progresyonuna kadargeçen süre abirateron asetat tedavisi ile yaklaşık iki katına çıkmıştır (HR = 0,488). PSA yanıtıbelgelenmiş olan hastaların oranı abirateron asetat grubunda, plasebo grubuna oranla dahafazla olmuştur (%24 karşısında %62, p=0,0001). Yumuşak doku hastalığı ölçülebilir olanhastalarda, abirateron asetat ile anlamlı düzeyde artmış tam ve kısmı yanıt oranlarıgörülmüştür.Kanser ağrısı için opiat kullanımına kadar geçen süre: Nihai analiz sırasında, prostat kanseri ağrısı için opiat kullanımına kadar geçen medyan süre abirateron asetat alan hastalar için 33,4ay, plasebo alan hastalar için 23,4 ay olmuştur; (HR = 0,721; %95 GA: [0,614; 0,846], p < 00001).Sitotoksik kemoterapi başlangıcına kadar geçen süre: Sitotoksik kemoterapi başlangıcına kadar geçen medyan süre abirateron asetat alan hastalar için 25,2 ay, plasebo alan hastalar için16,8 ay olmuştur (HR = 0,580; %95 GA: [0,487; 0,691], p < 0,0001). ECOG performans skorunda > 1 puan gerilemeye kadar geçen süre: ECOG performans skorunda > 1puan gerilemeye kadar geçen medyan süre abirateron asetat alan hastalar için12,3 ay, plasebo alan hastalar için 10,9 ay olmuştur (HR = 0,821; %95 GA: [0,714; 0,943], p= 0,0053).Aşağıdaki çalışma sonlanım noktaları abirateron asetat tedavisi lehine istatistiksel olarak anlamlı bir üstünlük göstermiştir: Objektif yanıt: Objektif yanıt, RECIST kriterlerine göre ölçülebilir hastalığa sahip olup tam veya kısmı yanıt elde eden hastaların oranı olarak tanımlanmıştır (hedef lezyon olarakdeğerlendirilebilmesi için başlangıçtaki lenf nodu büyüklüğünün > 2cm olması gerekmiştir).Başlangıçta ölçülebilir hastalığı olup objektif yanıt elde eden hastaların oranı abirateron asetatgrubunda %36, plasebo grubunda ise %16 olmuştur (p < 0,0001).Ağrı: Abirateron asetat tedavisi, plasebo ile karşılaştırıldığında, ortalama ağrı şiddeti progresyonunu anlamlı şekilde %18'e kadar azaltmıştır (p = 0,0490). Progresyona kadargeçen medyan süre abirateron asetat grubunda 26,7 ay, plasebo grubunda ise 18,4 ay olmuştur. FACT-P (Toplam Skor) anketinde kötüleşmeye kadar geçen süre: abirateron asetat tedavisi, plasebo ile karşılaştırıldığında, FACT-P (Toplam Skor) anketindeki kötüleşme riskini anlamlışekilde %22'ye kadar azaltmıştır (p = 0,0028). FACT-P (Toplam Skor) anketindekötüleşmeye kadar geçen süre abirateron asetat grubunda 12,7 ay, plasebo grubunda ise 8,3ay olmuştur. Çalışma 301 (daha önce kemoterapi almış olan hastalar)Çalışma 301'e daha önceden dosetaksel kullanmış olan hastalar dahil edilmiştir. Bu kemoterapiden kaynaklanan toksisite tedavinin kesilmesine neden olmuş olabileceği için,hastaların dosetaksel tedavisi sırasında hastalık ilerlemesi göstermiş olması gerekmemiştir.Hastalar protokole tanımlanan radyografik ilerleme ve semptomatik ya da klinik ilerleme ilebirlikte PSA ilerlemesi oluncaya kadar (hastanın başlangıç/en düşük düzeyine göredoğrulanmış %25 artış) hastalar çalışma tedavilerine devam etmiştir. Daha önceden prostatkanseri için ketokonazol tedavisi gören hastalar bu çalışmaya alınmamıştır. Birincil etkililiksonlanım noktası genel sağkalım olmuştur. Çalışmaya alınan hastaların medyan yaşı 69 idi (yaş aralığı 39 - 95 yaş). Abirateron asetat ile tedavi edilen hastaların ırklarına göre dağılımı şöyleydi: 737'si (%93,2) beyaz ırktan, 28'i(%3,5) siyah ırktan, 11'i (%1,4) sarı ırktan ve geri kalan 14'ü (%1,8) ise diğer ırklardandı.Çalışmaya alınan hastaların %11'inin ECOG performans skoru 2 idi; %70'i için PSAilerlemesi olsun ya da olmasın, hastalık ilerlemesine dair radyografik kanıtlar mevcuttu; %70'idaha önce bir sitotoksik kemoterapi, %30'u ise iki sitotoksik kemoterapi almıştı. Abirateronasetat ile tedavi edilen hastaların % 11'inde karaciğer metastazı vardı.552 ölüm gözlendikten sonra yapılan planlı bir analizde, abirateron asetat ile tedavi edilen hastaların %42'sinin (797 hastanın 333'ü), plasebo ile tedavi edilen hastaların ise %55'inin(398 hastanın 219'u) öldüğü saptandı. Abirateron asetat ile tedavi edilen hastaların medyangenel sağkalımda istatistiksel olarak anlamlı bir artış görüldü (bkz. Tablo 6).
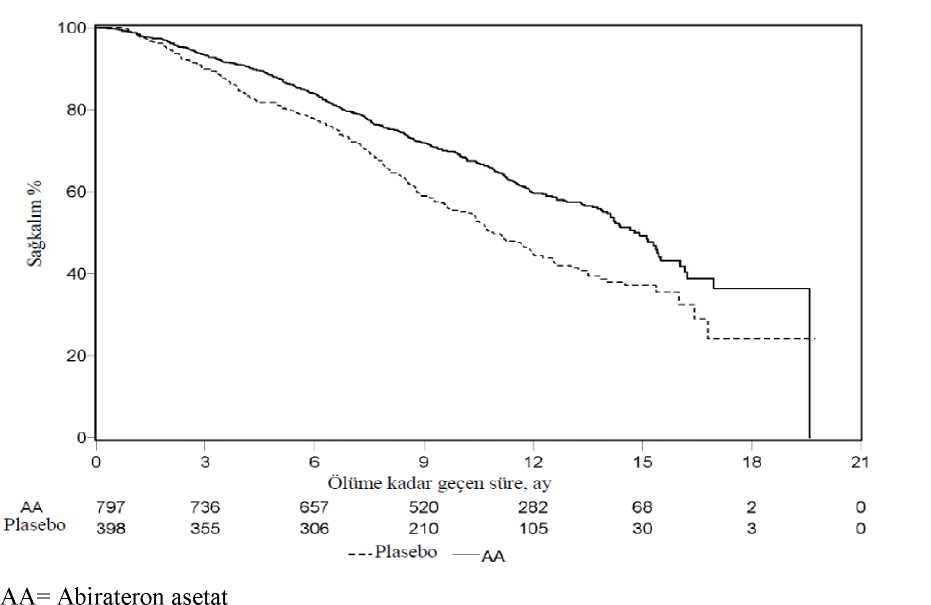
a p-değeri ECOG performans durumu skoruna (0-1 veya 2), ağrı skoruna (yok veya var), daha önceden alınmış kemoterapi rejimlerinin sayısına (12) ve hastalık ilerlemesinin tipine(yalnızca PSA veya radyografik) göre tabakalaştırılmış bir logaritmik-sıralama testindenelde edilmiştir.b Risk oranı tabakalandırılmış orantısal bir risk modeline göre hesaplanmıştır. Risk oranı < 1 abirateron asetat lehine Tedavinin başlangıçtaki ilk birkaç ayından sonra her değerlendirme noktasında, plasebo ile tedavi edilip hayatta kalan hastaların oranıyla karşılaştırıldığında, abirateron asetat ile tedaviedilen hastaların daha yüksek sağkalım oranına sahip olduğu belirlenmiştir (bkz. Şekil 6).
Altgrup sağkalım analizleri abirateron asetat tedavisi için tutarlı bir sağkalım faydası gösterdi (bkz. Şekil 7).
AA=Abirateron asetat; BPI=Kısa ağrı envanteri; GA=Güven aralığı; ECOG=Doğu kooperatif onkoloji grubu (eastern cooperative oncology group) performans skoru; HR=Tehlike oranı;NE=Değerlendirilebilir değil Genel sağkalımda gözlenen artışa ek olarak, tüm ikincil sonlanım noktaları abirateron asetat lehine idi ve aşağıda gösterildiği şekilde bu farklılıklar birden fazla test için ayarlandığındaistatistiksel olarak anlamlı idi: Abirateron asetat alan hastalarda, plasebo alanlara göre istatistiksel olarak anlamlı düzeylerde daha yüksek PSA yanıt oranı (başlangıç değerinden >%50 olarak tanımlanmış) elde edildi,abirateron asetat ile %38 iken, plaseboyla %10, p < 0,0001. Abirateron asetat ile tedavi edilen hastalarda, PSA ilerlemesine kadar olan medyan süre 10,2 ay iken, bu süre plasebo ile tedavi edilen hastalarda 6,6ay idi (HR=0,58; %95 GA: [0,462;0,728], p < 0,0001).Abirateron asetat ile tedavi edilen hastalarda medyan radyografik progresyonsuz sağkalım 5,6 ay iken, bu süre plasebo ile tedavi edilen hastalarda 3,6 ay idi (HR=0,673; %95 GA: [0,585;0,776], p < 0,0001). AğrıAğrısında hafifleme olan hastaların oranı abirateron asetat grubunda, plasebo grubuna oranla istatistiksel olarak anlamlı derecede daha fazlaydı (%44'e karşı %27, p=0,0002). Bir hastadadört hafta arayla yapılan iki ardışık değerlendirmede 24 saatlik bir sürede analjezik kullanımskorunda herhangi bir artış olmaksızın BPI-SF en kötü ağrı yoğunluğu skorunda başlangıcagöre en az %30 azalma sağlanması ağrının hafiflemesi yanıtı olarak tanımlandı. Ağrıpalyasyonu için yalnızca başlangıç ağrı puanı > 4 olan hastalar değerlendirildi ve en az birbaşlangıç-sonrası ağrı skoru analiz edildi (N=512). Abirateron asetat ile tedavi edilen hastalarda, plasebo ile tedavi edilenlere oranla daha düşük oranda ağrı ilerlemesi görüldü: 6. ayda abirateron asetat tedavisi alanların %22'sine karşılıkplasebo alanların %28'i, 12. ayda abirateron asetat tedavisi alanların %30'una karşılık plaseboalanların %38'i ve 18. ayda abirateron asetat tedavisi alanların %35'ine karşılık plaseboalanların %46'sında ağrıda ilerleme vardı. Ağrının hafiflemesi yanıtı, iki ardışıkdeğerlendirmede son 24 saatlik bir sürede analjezik kullanım skorunda herhangi bir azalmaolmaksızın BPI-SF en kötü ağrı yoğunluğu skorunda başlangıca göre en az %30 veya dahafazla bir artış ya da iki ardışık değerlendirmede analjezik kullanım skorunda %30 veya dahafazla bir artış olarak tanımlandı. 25. persentilde ağrı ilerlemesine kadar geçen süre abirateronasetat grubunda 7,4 ay iken, plasebo grubunda 4,7 ay idi. İskelet sistemiyle ilişkili olaylar6. ayda, 12'inci ayda ve 18'inci ayda abirateron asetat grubunda iskelet sistemiyle ilişkili olaygörülen hasta oranı plasebo ile karşılaştırıldığında daha düşüktü (sırasıyla 6. ayda %18'e karşı%28, 12. ayda %30'a karşı %40 ve 18. ayda %35'e karşı %40). 25. persentilde iskeletsistemiyle ilişkili ilk olayın görülme süresi abirateron asetat grubunda 9,9 ay ile, 4,9 ay olankontrol grubundan iki kat daha uzundu. Patolojik kırık, spinal kord basısı, kemiğe palyatifradyoterapi veya kemiğe yönelik cerrahi girişim iskelet sistemiyle ilişkili olay olaraktanımlandı. Pediyatrik popülasyonPediyatrik popülasyonda prostat kanseri görülmediğinden ABETYL'in pediyatrik hastalarda kullanımı bulunmamaktadır. ABETYL'e ait pediatrik popülasyonda klinik etkililik vegüvenlilik verisi yoktur (bkz. Bölüm 4.2). 5.2 Farmakokinetik özelliklerGenel özelliklerAbirateron asetat uygulamasından sonra, abirateron ve abirateron asetatın farmakokinetiği sağlıklı gönüllülerde, ilerlemiş metastatik prostat kanserli hastalarda ve kanser hastasıolmayan karaciğer veya böbrek yetmezliği olan gönüllülerde çalışılmıştır. Abirateron asetat in vivoolarak hızla bir androjen biyosentez inhibitörü olan abiraterona dönüşür (bkz. Bölüm5.1).Emilim:Abirateron asetat açlık durumunda oral yoldan uygulandıktan sonra, yaklaşık 2 saatte maksimum plazma abirateron konsantrasyonlarına ulaşılır. Abirateron asetatın yemekle birlikte alınması, yemeğin yağ içeriğine bağlı olarak, aç karınakarnına alınmasına oranla 10 kata kadar (EAA açısından) ve 17 kata kadar (Cmaks açısından)daha fazla ortalama sistemik abirateron maruziyetine yol açar.Yemeklerin içerik ve bileşimindeki normal farklılıklar göz önüne alındığında, ABETYL'in yemeklerle birlikte alınması oldukça değişken maruziyetine yol açabilir. Bu nedenle,ABETYL yemekle birlikte alınmamalıdır. ABETYL, yemeklerden en az 1 saat önce ya dayemek yedikten en az iki saat sonra alınmalıdır. Tabletler bütün olarak suyla yutulmalıdır(bkz. Bölüm 4.2). Dağılım:İnsan plazmasında 14C-abirateronun proteine bağlanma oranı %99,8'dir. Görünür dağılım hacmi yaklaşık 5,630 litre olup, abirateronun periferik dokulara yoğun bir şekilde dağıldığınıgösterir. Biyotransformasyon:14C-abirateron asetat kapsül formunda oral yoldan alındıktan sonra, abirateron asetat abiraterona hidrolize olur ve daha sonra birincil olarak karaciğerde olmak üzere sülfasyon,hidroksilasyon ve oksidasyona uğrar. Dolaşımdaki radyoaktivitenin büyük çoğunluğu(yaklaşık %92) abirateronun metabolitleri halinde bulunur. Belirlenebilen 15 metabolitten ikitemel metabolit, her biri toplam radyoaktivitenin yaklaşık %43'ünü temsil eden abirateronsülfat ve N-oksit abirateron sülfattır. Eliminasyon:Sağlıklı gönüllülerden elde edilen verilere göre, plazmadaki abirateronun yarılanma süresi yaklaşık 15 saattir. 1.000 mg 14C-abirateron asetatın oral yoldan alınmasından sonraradyoaktif dozun yaklaşık %88'i feçeste ve yaklaşık %5'i idrarda görülür. Feçeste bulunanmajör bileşikler değişmemiş abirateron asetat ve abiraterondur (sırasıyla uygulanan dozunyaklaşık %55 ve %22'si). Hastalardaki karekteristik özelliklerKaraciğer yetmezliği olan hastalar:Abirateron asetatın farmakokinetiği hafif ya da orta şiddette karaciğer yetmezliği olan hastalar (sırasıyla Child-Pugh Sınıf A ve B) ile sağlıklı kontrollerde çalışılmıştır. 1.000 mg'lık tek biroral doz sonrası abiraterona sistemik maruziyet hafif ve orta şiddette karaciğer yetmezliği olanhastalarda sırasıyla %11 ve %260 oranında artmaktadır. Abirateronun ortalama yarılanmaömrü hafif karaciğer yetmezliği olan hastalarda yaklaşık 18 saate ve orta şiddette karaciğeryetmezliği olan hastalarda ortalama 19 saate uzamaktadır. Bir başka çalışmada, abirateronun farmakokinetiği daha önceden ciddi karaciğer yetmezliği (Child-Pugh Sınıf C) olan (n=8) ve normal hepatik fonksiyona sahip 8 sağlıklı birey üzerindeincelenmiştir. Abirateronenin sistemik etkisi (EAA) yaklaşık %600 oranında yükselmiş veserbest ilacın etkisi şiddetli karaciğer bozukluğu olanlarda normal karaciğer fonksiyonuolanlara göre %80 oranında artmıştır. Daha önceden hafif karaciğer yetmezliği olan hastalarda doz ayarlamasına gerek yoktur. ABETYL kullanımı faydanın olası riskten açıkça ağır bastığı, orta şiddette karaciğeryetmezliğine sahip hastalarda dikkatle değerlendirilmelidir (bkz. Bölüm 4.2 ve 4.4). ABETYLağır karaciğer yetmezliği olan hastalarda kullanılmamalıdır (bkz. Bölüm 4.2, 4.3 ve 4.4). ABETYL tedavisi sırasında hepatotoksisite gelişen hastalarda, tedavinin durdurulması ve doz ayarlaması gerekebilir (bkz. Bölüm 4.2 ve 4.4). Böbrek yetmezliği olan hastalar:Stabil bir hemodiyaliz programında olan son dönem böbrek yetmezliği olan hastalar ile böbrek fonksiyonları normal olan eşlenmiş kontrol hastalarında abirateron asetatın farmakokinetiğikarşılaştırılmıştır. Diyaliz programında olan son dönem böbrek yetmezliği olan hastalarda 1.000 mg'lık tek bir oral doz sonrası abiraterona sistemik maruziyet artmamıştır. Ağır böbrekyetmezliği dahil, böbrek yetmezliği olan hastalarda ABETYL uygulanması sırasında dozuazaltmaya gerek yoktur (bkz. Bölüm 4.2). Ancak prostat kanseri ve ağır böbrek yetmezliğiolan hastalarla ilgili klinik deneyim bulunmamaktadır. Bu tür hastalarda dikkatli olunmasıtavsiye edilir. 5.3 Klinik öncesi güvenlilik verileriTüm hayvan toksisite çalışmalarında, dolaşımdaki testesteron düzeyleri anlamlı derecelerde azalmıştır. Buna bağlı olarak üreme organlarıyla adrenal, hipofiz ve meme bezlerininağırlıklarında azalma ile morfolojik ve/veya histopatolojik değişiklikler gözlenmiştir. Tümdeğişiklikler tamamen ya da kısmen geri döndürülebilir nitelikteydi. Üreme organları veandrojene duyarlı organlardaki değişiklikler abirateronun farmakolojisiyle uyumludur.Tedaviyle ilişkili tüm hormonal değişiklikler eski haline dönmüştür veya 4 haftalık birtoparlanma dönemi sonunda geri düzeldiği gösterilmiştir. Hem erkek hem de dişi sıçanlarda yapılan fertilite çalışmalarında, abirateron asetat fertiliteyi azaltmış, fakat abirateron asetat kesildikten sonra 4 ila 16 haftada fertilite tam olarak eskihaline dönmüştür. Sıçanlarda yapılan bir gelişim toksisitesi çalışmasında, abirateron asetat azalmış fetüs ağırlığı ve sağkalım da dahil olmak üzere gebeliği etkilemiştir. Abirateron asetat teratojenik olmasada, dış genital organlarda etkiler görülmüştür. Sıçanlarda yürütülen bu fertilite ve gelişim toksisitesi çalışmalarında, tüm etkiler abirateronun farmakolojik aktivitesine bağlı olmuştur. Tüm hayvan toksikoloji çalışmalarında görülen üreme organlarındaki değişiklikler dışında, klasik güvenlilik farmakolojisi, tekrarlayan doz toksisitesi, genotoksisite ve karsinojenikpotansiyel çalışmalarından elde edilen klinik dışı veriler insanlar için özel bir tehlikeyigöstermemiştir. Transjenik farelerde (Tg.rasH2) yapılan 6 aylık bir çalışmada abirateronasetat karsinojenik bulunmamıştır. Sıçanlarda yapılan 24 aylık bir karsinojenisiteçalışmasında, abirateron asetat testislerde interstisyel hücre neoplazmalarının insidansınıarttırmıştır. Bu bulgu abirateronun farmakolojik etkisine bağlı ve sıçanlara özgü olarakdeğerlendirilmiştir. Abirateron asetat dişi sıçanlarda karsinojenik bulunmamıştır. Çevresel Risk DeğerlendirmesiAbirateron etkin maddesi, sucul ortam (özellikle balıklar) için çevresel bir risk göstermektedir. 6. FARMASÖTİK ÖZELLİKLERİ6.1 Yardımcı maddelerin listesiLaktoz monohidrat (sığır sütünden elde edilir) Mikrokristalin selüloz Sodyum lauril sülfatKroskarmelloz sodyumPovidon K30Kolloidal silikon dioksitMagnezyum stearat 6.2 GeçimsizliklerBilinen herhangi bir geçimsizliği bulunmamaktadır. 6.3 Raf ömrü36 ay. 6.4 Saklamaya yönelik özel tedbirler25oC altındaki oda sıcaklığında saklanmalıdır. Çocukların göremeyeceği, erişemeyeceği yerlerde ve ambalajında saklayınız. 6.5 Ambalajın niteliği ve içeriğiABETYL 250 mg tablet, 120 tablet içeren Alüminyum-Alüminyum blister ambalajlarda kullanma talimatı ile birlikte karton kutuda piyasaya sunulmaktadır. 6.6 Beşeri tıbbi üründen arta kalan maddelerin imhası ve diğer özel önlemlerEtki mekanizmasına dayanarak, bu tıbbi ürün gelişmekte olan fetüse zarar verebilir, bu yüzden gebe olan ya da gebe olma olasılığı bulunan kadınlar ABETYL ile korunmasız temasetmemeli; örneğin eldiven kullanmalıdır (bkz. Bölüm 4.6). Kullanılmamış olan ürünler ya da atık materyaller "Tıbbi Atıkların Kontrolü Yönetmeliği" ve "Ambalaj Atıklarının Kontrolü Yönetmeliği"ne uygun olarak imha edilmelidir. Bu tıbbi ürün akuatik ortam için bir risk oluşturabilir (bkz. Bölüm 5.3). 7. RUHSAT SAHİBİAbdi İbrahim İlaç San. ve Tic. A.Ş. Reşitpaşa Mahallesi, Eski Büyükdere Caddesi No:4 34467 Maslak/S arıyer/İstanbulTel: 0212 366 84 00Faks: 0212 276 20 20 8. RUHSAT NUMARASI2020/1 9. İLK RUHSAT TARİHİ/RUHSAT YENİLEME TARİHİİlk ruhsat tarihi: 15.01.2020 Ruhsat yenileme tarihi: 10. KÜB'ÜN YENİLENME TARİHİ |
İlaç BilgileriAbetyl 250 Mg TabletEtken Maddesi: Abirateron Asetat
Google Reklamları
İlgili İlaçlar |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
Ana Sayfa | Hakkımızda | İlaçlar | İlaç Ara | İlaç Firmaları | Gizlilik | Bize Ulaşın
Telif Hakkı 2008-2026 © İlaç Prospektüsü. Tüm Hakları Saklıdır.Uyarı: Sitemizde yayınladığımız ilaç bilgileri ile doktora danışmadan kesinlikle ilaç kullanmayınız!
Aksi halde doğabilecek sağlık sorunlarından ilacprospektusu.com sorumlu tutulamaz.