Enbrel 25 Mg Pediyatrik Kullanim İçin Sc Enjektab... Kısa Ürün BilgisiAntineoplastik ve İmmünomodülatör Ajanlar » İmmünsupresif Ajanlar » İmmünsupresif Ajanlar » Tumor necrosis factor alpha (tnf-a) inhibitors » Etanercept KISA ÜRÜN BİLGİSİ1. BEŞERİ TIBBİ ÜRÜNÜN ADIENBREL® 25 mg Pediyatrik Kullanım İçin SC Enjektabl Çözelti İçin Toz ve Çözücü2. KALİTATİF VE KANTİTATİF BİLEŞİM Etkin madde.*Etanercept.........................25 mgYardımcı maddeler:Mannitol (E 421)..............40 mg/mlSukroz..............................10 mg/ml Benzil alkol......................9 mg/ml Yardımcı maddeler için 6.1'e bakınız. 3. FARMASÖTİK FORMToz ve enjeksiyonluk çözelti için çözücü.Flakon içerisindeki toz beyaz renkte olup, şırınganın içerisinde yer alan çözücü berrak ve renksizdir. Enjeksiyon için hazırlanan çözelti, berrak, renksiz- açık sarı renktedir. 4. KLİNİK ÖZELLİKLER4.1 Terapötik endikasyonlarPediyatrik hastalarENBREL®; Juvenil idiopatik artriti veya pediyatrik plak psöriazisi olan aşağıda tanımlanmış çocuk hastalarda; - 2-17 yaş arası metotreksata yeterli cevabı olmayan veya metotreksatı kullanamayan, poliartriti (romatoid faktör pozitif veya negatif) veya yaygın oligoartriti olan hastalarda, 12-17 yaş arası adölesanlarda plak psöriazisi varlığında veya metotreksata yeterli cevabı olmayan veya metotreksatı kullanamayan psöriatik artritli hastalarda, 12-17 yaş arası adölesanlarda metotreksata cevap vermeyen veya metotreksatı kullanamayan enthesit ilişkili artritli hastalarda, endikedir. ENBREL® 2 yaşından küçük çocuklarda çalışılmamıştır. 4.2 Pozoloji ve uygulama şekliENBREL® tedavisi juvenil idiopatik artrit veya pediyatrik plak psöriazis tanı ve tedavisinde uzman bir doktor tarafından başlatılmalı ve takip edilmelidir. Her ENBREL® 25 mg flakonu uygulamadan önce 1 mİ bakteriyostatik enjeksiyonluk su içinde eritilmelidir.Pozoloji / Uygulama sıklığı ve süresi:Her ENBREL® 25 mg/ml flakonu, aynı hastaya maksimum 2 dozda uygulanacak şekilde kullanılmalıdır. ENBREL® çözeltinin hazırlanması, uygulanması ve hazırlanmış olan ENBREL® flakonunun tekrar kullanımı ile ilgili ayrıntılı talimatlar, Kullanma Talimatı'nda yer almaktadır.2013-0003340 Uygulama şekli:Çözücü şırıngasının iğne kılıfı lateks (kuru doğal lastik) içerir. Bilinen veya muhtemel lateks alerjisi söz konusu olan hastalar veya iğne kapağına dokunmak durumunda olan örneğin hastaya bakan kişiler, etanercept kullanmadan Önce, doktorlarına danışmalıdırlar.Etanercept, uyluk, karın veya üst kola subkutan enjeksiyon ile uygulanır. Enjeksiyon bölgesi değiştirilmelidir. Her yeni enjeksiyon, bir önceki enjeksiyondan en az 3 cm uzakta olmalıdır. Derinin hassas, çürük, kırmızı veya sert olan bölgelerine enjeksiyon YAPILMAMALIDIR. ENBREL® çözeltinin hazırlanması, uygulanması ve hazırlanmış olan ENBREL flakonunun tekrar-kullanımı ile ilgili ayrıntılı talimatlar Kullanma Talimatı'nda yer almaktadır. Özel popülasyonlara ilişkin ek bilgiler:Pediyatrik popülasyon:MA25 mg ENBREL® İmi enjeksiyonluk su ile seyreltilir ve haftada iki kez, dozlar arasında 3-4 gün bırakarak 0.4 mg/kg (her doz için maksimum 25 mg'a kadar) veya haftada bir kez 0.8 mg/kg (tek dozda maksimum 50 mg) olacak şekilde, subkutan enjeksiyon ile uygulanır. 4 ay sonrasında tedaviye cevap alınamayan hastalarda, tedavinin sonlandırılması düşünülmelidir. 2 ile 3 yaş arasındaki çocuklarda klinik ilaç geliştirme programı çerçevesinde klinik araştırma yapılmamıştır. Ancak bir hasta kayıt kütüğünden elde edilen kısıtlı güvenlilik verileri, 2 ile 3 yaş arasındaki çocuklarda güvenlilik profilinin haftada bir kez subkutan uygulanan 0.8 mg/kg alan yetişkinler ve 4 yaşından büyük çocuklarda görülen ile benzer olduğunu göstermektedir. ENBREL®'in 2 yaşından küçük çocuklarda aktif JİA tedavisinde kullanımı bulunmamaktadır. Pediyatrik plak psöriazisÖnerilen doz 24 haftaya kadar haftada bir kez olmak üzere 0.8 mg/kg'dır (tek dozda maksimum 50 mg). 12 haftanın sonunda tedaviye hiç yanıt alınmazsa tedavi kesilmelidir. ENBREL® ile tekrar tedaviye başlanacaksa tedavi süresi için yukarıda belirtilen yol izlenmelidir. Doz, haftada 1 kez olmak üzere 0.8 mg/kg olmalıdır (tek dozda maksimum 50 mg). 12 yaşından küçük plak psöriazis hastalarında ENBREL® kullanımı bulunmamaktadır. Böbrek yetmezliği:Doz ayarlaması yapılmasına gerek yoktur.Karaciğer yetmezliği:Doz ayarlaması yapılmasına gerek yoktur.4.3 Kontrendikasyonlarİlacın etkin maddesine veya içindeki diğer maddelere aşırı hassasiyet ile sepsis veya sepsis riskinin bulunduğu durumlarda kullanılmamalıdır. Kronik veya lokalize enfeksiyonlar dahil olmak üzere aktif enfeksiyonu bulunan hastalarda ENBREL® tedavisine başlanmamalıdır. Çözücü olarak benzi 1 alkol içerdiği için prematüre bebeklere ve yeni doğanlara ENBREL® uygulanmaması gerekir.4.4 Özel kullanım uyarıları ve önlemleriHastalar, etanercept'in ortalama eliminasyon yarı ömrünün 70 saat olduğu da dikkate alınarak (standart sapma; 7 ila 300 saat arasında) ENBREL® ile tedaviden önce, tedavi sırasında ve sonrasında enfeksiyonlar açısından değerlendirilmelidir.ENBREL® kullanımı ile birlikte ciddi enfeksiyonlar, sepsis, tüberküloz ve invazif fungal enfeksiyonlar dahil olmak üzere diğer fırsatçı enfeksiyonlar görüldüğü rapor edilmiştir. Ciddi EnfeksiyonlarTNF-alfa Blokeri ilaçlarla tedavi olan hastalarda Legionella ve Listeria'yı da içeren bakteri yel, mikobakteriyel, mantar, viral, parazitik enfeksiyonlara (protozoa dahil) bağlı ölüme veya hastaneye yatışa sebep olabilen, çoklu-organ sistem ve bölgeleri etkileyebilen ciddi enfeksiyon riski artmıştır.Bazı vakalarda, belirli bir fungal ve başka fırsatçı enfeksiyonların tanısı konulamamış ve bunun sonucunda, uygun tedavinin yapılmasında gecikmeler ve bazı durumlarda ölüm meydana gelmiştir. Hastalar enfeksiyon açısından değerlendirilirken hastadaki fırsatçı enfeksiyon riski (örn. endemik mikozlara maruz kalma) dikkate alınmalıdır. ENBREL® ile tedavi gören hastalar, yeni bir enfeksiyon ortaya çıkması durumunda yakından takip edilmelidir. Hastada ciddi enfeksiyon gözlenirse etanercept uygulaması durdurulmalıdır. Kronik veya lokalize enfeksiyonlar dahil aktif enfeksiyonu olan hastalarda etanercept tedavisi uygulanmamalıdır. Tekrarlayan veya kronik enfeksiyon öyküsü olan hastalar ile, ilerlemiş ya da kontrol edilemeyen diyabet gibi hastanın enfeksiyonlara direncini azaltan durumlarda etanercept kullanımı düşünülüyorsa azami dikkat gösterilmelidir. TüberkülozENBREL® ile tedavi gören hastalarda akciğer dışına yerleşmiş tüberküloz ve milier tüberkülozu içeren aktif tüberküloz vakalarının görüldüğü bildirilmiştir.ENBREL® ile tedaviye başlamadan önce tüberküloz açısından yüksek risk altındaki her hasta aktif ya da latent enfeksiyon açısından değerlendirilmelidir. Bu değerlendirme kişisel tüberküloz geçmişi veya tüberkülozla daha önceden olası bir temasın olması, daha önceden görülmüş veya halen görülmekte olan immünosupresif tedaviyi kapsayan ayrıntılı bir anamnezi içermektedir. Tüm hastalara tüberkülin deri testi ve göğüs radyografisi gibi uygun tarama testleri uygulanmalıdır. Özellikle şiddetli hastalığı olan veya immunitesi zayıflamış hastalarda negatif tüberkülin deri testi sonuçlarının yanıltıcı olma riski hatırda tutulmalıdır. Şayet hastaya aktif tüberküloz tanısı konmuşsa, ENBREL® tedavisine başlanılmaması gerekmektedir. Eğer inaktif tüberküloz ('latent') tanısı konmuşsa, latent tüberkülozun tedavisi için ENBREL® tedavisine başlamadan önce anti-tüberküloz tedavisine başlanması gerekmektedir. Bu durumda, ENBREL® tedavisinin uygulamasıyla elde edilecek fayda/risk dengesi dikkatle gözden geçirilmelidir. Tüm hastalar ENBREL® tedavisi devam ederken veya sonrasında tüberküloz bulunduğunu akla getiren belirti ve semptomların (örneğin inatçı öksürük, aşırı zayıflama/kilo kaybı, düşük dereceli ateş gibi) görülmesi halinde doktor tavsiyesine başvurması için bilgilendirilmelidir. Hepatit B reaktivasyonuÖnceden hepatit B virüsü (HBV) ile enfekte olmuş ve beraberinde ENBREL'i de içeren TNF-antagonistleri alan hastalarda hepatit B reaktivasyonu rapor edilmiştir. Bu raporlar; anti-HBc pozitif fakat HBsAg negatif olan hastalarda hepatit B reaktivasyonu raporlarını da içerir. ENBREL ile tedaviye başlanmadan önce hastalar HBV enfeksiyonu için test edilmelidir. HBV enfeksiyon testi pozitif olan hastalar için hepatit B tedavisinde uzmanlaşmış bir hekime danışılması önerilir. Daha önceden HBV ile enfekte olmuş hastalara ENBREL uygulanırken dikkatli olunmalıdır. Bu hastalar tedavi boyunca ve tedavinin sonlandırılmasını takip eden birkaç hafta boyunca aktif HBV enfeksiyonunun belirti ve semptomları açısından izlenmelidir. HBV ile enfekte olmuş hastaların TNF antagonist tedavisi ile bağıntılı olarak antiviral tedavi ile tedavi edilmesine dair uygun verilerbulunmamaktadır. HBV enfeksiyonu geliştiren hastalarda ENBREL sonlandırıİmalı ve uygun destekleyici tedavi ile etkin antiviral tedaviye başlanmalıdır. Hepatit C'nin kötüleşmesiEtanercept alan hastalarda hepatit C kötüleşmesi bildirimleri yapılmıştır. Hepatit C hikayesi olan hastalarda ENBREL dikkatli kullanılmalıdır.ENBREL ve anakinra tedavisinin eş zamanlı uygulanmasıENBREL® ve anakinra'nın birlikte uygulanmasıyla ciddi enfeksiyon ve nötropeni riskinin tek başına ENBREL®'e oranla arttığı düşünülmektedir. Bu kombinasyonun daha fazla bir klinik yararı olmadığı kanıtlanmış olduğundan birlikte kullanım önerilmez.ENBREL ve abatasept tedavisinin eş zamanlı uygulanmasıKlinik çalışmalarda ENBREL® ve abatasept'in birlikte uygulanması ciddi advers etkilerin görülme sıklığının artması ile sonuçlanmıştır. Bu kombinasyonun daha fazla bir klinik yararı olmadığı kanıtlanmış olduğundan birlikte kullanım önerilmez.Alerjik reaksiyonlarÇözücü şırıngasının iğne kılıfı lateks (kuru doğal lastik) içerir. Bilinen veya muhtemel lateks alerjisi söz konusu olan hastalar veya iğne kapağına dokunmak durumunda olan örneğin hastaya bakan kişiler, etanercept kullanmadan önce, doktorlarına danışmalıdırlar.Etanercept kullanımı ile ilgili alerjik reaksiyonlar sıklıkla rapor edilmiştir. Anjiyoödem ve ürtiker görülebilen alerjik reaksiyonlardandır ve ciddi reaksiyonlar görülmüştür. Ciddi alerjik veya anaflaktik reaksiyonlar görülmesi durumunda etanercept kullanımına derhal son verilmeli ve uygun bir tedavi başlatılmalıdır. İ m mü nosupresy onTNF'nin inflamasyona aracılık etmesi ve hücresel bağışıklık sistemini düzenlemesi nedeniyle, etanercept dahil anti-TNF tedavileri, vücudun enfeksiyonlara ve kanser gelişmesine karşı savunma mekanizmalarını etkileyebilir. Romatoid artriti bulunan ve ENBREL® ile tedavi gören 49 yetişkin hastayı içeren bir çalışmada, gecikmiş tip aşırı duyarlılık reaksiyonu, immunglobulin seviyesinin baskılanması veya efektör hücre popülasyonunun sayısında değişiklik olduğuna dair bulgular görülmemiştir.İki juvenil idiyopatik artritli hastada, sekeller olmaksızın iyileşen aseptik menenjit bulguları ve belirtileri ile su çiçeği enfeksiyonu gelişmiştir. Su çiçeği virüsüne önemli derecede maruz kalan hastalarda ENBREL® tedavisine geçici süre ara verilmesi gerekmektedir ve bu hastalara Varicella Zoster immunglobulini ile profilaktik tedavi yapılması düşünülmelidir. İmmünosupresyon altında olan ve kronik enfeksiyonu bulunan hastalarda ENBREL®'in güvenliliği ve etkililiği değerlendirilmemiştir. Maligniteler ve lenfoproliferatif bozukluklarSolid ve hematopoietik maligniteler (cilt kanserleri hariç):Pazarlama sonrası dönemde ENBREL® kullanımı ile gelişen çeşitli maligniteler görüldüğüne (göğüs ve akciğer kanseri ve lenfomayı içeren) dair bildirimler alınmıştır.TNF antagonistleri ile yapılan klinik çalışmaların kontrollü bölümlerinde, TNF antagonisti alan hastalar ile kontrol grubundaki hastalar ile karşılaştırıldığında, lenfoma sıklığında artış gözlenmiştir. Ancak, lenfoma oluşumu ender olarak görülmüştür ve plasebo hastalarının takip periyodu TNF-antagonisti tedavisi uygulanan hastalarınkinden kısadır. Pazarlama sonrası dönemde TNF antagonistleri ile tedavi gören hastalarda lösemi vakaları rapor edilmiştir Uzun süreli, yüksek aktiviteli, inflamatuvar hastalığı olan romatoid artrit hastalarında lenfoma ve lösemi riskinin artması risk tahminini zorlaştırmaktadır. Güncel bilgiye göre TNF antagonisti ile tedavi gören hastalarda lenfoma, lösemi veya diğer malignite oluşumu muhtemel riski göz ardı edilemez. Malignite öyküsü olan hastalarda TNF antagonisti ile tedavi başlanması ya da malignite gelişen hastalarda tedaviye devam edilmesi değerlendirilirken dikkatli olunmalıdır.ENBREL®'in de dahil olduğu TNF-antagonistleri ile tedavi edilen çocuklar, ergenler ve genç erişkinler arasında bazıları ölümcül olabilen maligniteler (özellikle Hodgkin ve non-Hodgkin lenfoma) bildirilmiştir. Hastaların çoğu, eşlik eden immünosupresanlar kullanmaktadır. Güncel bilgilere dayanılarak, TNF-antagonisti ile tedavi edilen hastalarda lenfonıalar veya diğer hematopoietik veya solid malignansiler geliştirme riski dışlanamamaktadır TNF blokerlerinin kullanımına bağlı olarak lösemi-kan kanseri (Akut myeloid lösemi, kronik lenfositik lösemi ve kronik myeloid lösemi) geliştiği bildirilmiştir.Cilt kanserleriEtanercept dahil olmak üzere TNF-antagonistleri ile tedavi edilen hastalarda melanom ve melanom dışı cilt kanserleri (NMSC) rapor edilmiştir. Etanercept ile tedavi edilen hastalarda pazarlama sonrası dönemde Merkel hücreli karsinom vakaları çok seyrek rapor edilmiştir. Cilt kanseri riski yüksek olan tüm hastalarda periyodik cilt muayenesi yapılması önerilmektedir Etanercept klinik çalışmalarının kontrollü bölümlerine ait sonuçların birleştirilmesiyle, özellikle psöriazis hastalarında olmak üzere etanercept kolunda kontrol hastalarına kıyasla daha fazla melanom dışı cilt kanseri vakası gözlemlenmiştir.AşılarENBREL® kullanan psöriatik artrit hastalarının çoğunluğu, polisakkarid pnömokok aşılarına etkili B-hücre bağışıklık yanıtı verebilmektedir, fakat toplam antikor titreleri oldukça düşüktür ve ENBREL® kullanmayan hastalar ile kıyaslandığında az sayıda hastada antikor düzeyinde iki kat artış görülmüştür. Bu durumun klinik açıdan önemi bilinmemektedir. Canlı aşılar, etanercept ile birlikte verilmemelidir. Etanercept tedavisine başlamadan önce, mümkün olduğu oranda pediyatrik hastaların geçerli lokal bağışıklama takvimine uygun olarak tüm aşıların tamamlanması önerilmektedir.Otoantikor oluşumlarıENBREL® ile tedavi, otoimmun antikorların oluşmasına neden olabilir.Hematolojik ReaksiyonlarEtanercept kullanan hastalarda, bazıları ölüm ile sonuçlanan nadir olarak pansitopeni ve çok nadir olarak aplastik anemi rapor edilmiştir.Geçmişinde kan diskrazisi bulguları olup etanercept tedavisi görmekte olan hastalara dikkat edilmelidir. Etanercept kullanmakta olan tüm hastalar kan diskrazisi veya enfeksiyonların (sürekli ateş, boğaz ağrısı, çürük, kanama, solukluk) muhtemel belirti ve semptomlarının gelişimine karşı uyarılmalı ve derhal medikal yardım istenmelidir. Bu tip hastalar acil olarak tüm kan sayımları dahil incelenmeli; eğer kan diskrazisi tespit edilir ise etanercept kullanımı durdurulmalıdır. Nörolojik OlaylarMültipl skleroz hastalarında etanercept tedavisini değerlendiren klinik çalışmalar yapılmamasına rağmen, bu hastalarda diğer TNF antagonistleri ile yapılan klinik çalışmalar hastalığın aktivitesinde artış göstermiştir. Etanercept ile tedavi gören hastalarda nadir olarak SSS'nde demiyelinizan hastalıklar rapor edilmiştir (Bkz. Bölüm 4.8 İstenmeyen Etkiler.) İlaveten, çok nadir olarak periferik demiyelinizan polinöropatiler (Guillain-Barre sendromu dahil) rapor edilmiştir. Önceden varolan veya yeni ortaya çıkmış demiyelinizan SSS hastalığı bulunan veya bu tür riskleri olan hastalara etanercept tedavisi önerilirken nörolojik inceleme dahil risk/yarar değerlendirimi dikkatli bir şekilde yapılmalıdır.Kombinasyon tedavisiRomatoid artritli hastalarda iki yıl süren kontrollü bir klinik çalışmada, ENBREL® ve metotreksatın kombinasyon halinde uygulaması sonucunda bilinen güvenlilik sonuçları dışında bir sonuca rastlanmamıştır. Ayrıca bu çalışmada metotreksat ile ENBREL® kombinasyonunun güvenlik profilinin, tek başına ENBREL® veya metotreksat uygulanan çalışmalarda bildirilen profiller ile benzer olduğu bildirilmiştir. Kombinasyonun güvenliğini değerlendirmek açısından uzun süreli çalışmalar devam etmektedir. Hastalık modifiye edici diğer antiromatizmal ilaçlar (DMARD) ile ENBREL®'in kombinasyon halinde uygulanmasının uzun süreli güvenliliği belirlenmemiştir.Psöriazis tedavisinde diğer sistemik tedavi çeşitleri veya fototerapi ile ENBREL®'in kombinasyon halinde kullanımına ilişkin çalışma mevcut değildir. Böbrek ve karaciğer bozukluğuBöbrek veya karaciğer bozukluğu olan hastalarda, farmakokinetik verilere dayanarak doz ayarlamasının yapılmasına gerek yoktur. Bu hastalarda yapılan klinik çalışmalar sınırlıdır.Kardiyak HastalıklarEtanercept kullanmakta olup presipitasyon, faktörleri bulunan ya da bulunmayan hastalarda, konjestif kalp yetmezliğinin kötüleştiğine dair raporlar bildirilmiştir. Konjestif kalp yetmezliğinde etanercept kullanımının değerlendirildiği iki büyük klinik çalışmadan birinin verileri, etanercept grubundaki hastalarda konjestif kalp yetmezliğinin kötüleşmesine doğru bir eğilim olduğu ihtimalini düşündürmüştür. Ayrıca, konjestif kalp yetmezliği tedavisinde infliximab (TNF-alfa'ya bağlanan monoklonal antikor) kullanımının değerlendirildiği bir klinik çalışma, infliximab verilen hastalar arasında mortalite artışından dolayı erken sonlandırılmıştır.Hekimler, konjestif kalp yetmezliği bulunan hastalarda etanercept'i kullanırken dikkatli olmalıdırlar. Alkole bağlı hepatitAlkole bağlı orta şiddette-şiddetli hepatit nedeniyle ENBREL® veya plasebo ile tedavi edilen 48 hospitalize hastada yapılan bir faz II randomize plasebo-kontrollü çalışmada, ENBREL®'in etkisiz olduğu belirlenmiş ve ENBREL® ile tedavi edilen hastalarda 6 ay sonrasında mortalite oranı anlamlı derecede yüksek bulunmuştur. Dolayısıyla ENBREL® alkole bağlı hepatit tanısı alan hastaların tedavisinde kullanılmamalıdır. Hekimler ENBREL® kullanırken, alkole bağlı orta şiddette-şiddetli hepatit vakaları olan hastalarda dikkatli olmalıdır.Wegener granülomatoz tedavisinde kullanılmasıMediyan olarak 25 ay süren standart tedaviye (siklofosfamid veya metotreksat ve glikokortikoidleri içeren) ek olarak ENBREL® ile de tedavi gören 89 yetişkin hastada yapılan plasebo kontrollü bir çalışmada, Wegener granülomatozunda ENBREL®'1 in etkili bir tedavi olduğu gösterilememiştir. Etanercept kullanan grupta değişik tipte nonkutanöz tümörlere, standart tedavi uygulanan hastalara oranla daha çok rastlanmıştır. Etanercept'in Wegener granülomatozu tedavisinde kullanılması önerilmemektedir.Diyabet tedavisi gören hastalarda hipoglisemiDiyabet nedeniyle ilaç tedavisi gören hastalarda etanercept başlanmasının ardından, bu hastaların bazılarında anti-diyabetik ilaç tedavisinde bir azaltma gerektiren hipoglisemi bildirimleri olmuştur.Benzil alkol®** « ENBREL yardımcı madde olarak 9 mg/ml benzil alkol içerir; benzil alkol, bebeklerde ve 3 yaşma kadar olan çocuklarda toksik reaksiyonlara ve anafllaktoid reaksiyonlara neden olabilir. Prematüre bebekler ve yeni doğanlara ENBREL® uygulanmaması gerekir. Özel popülasyonlarGeriyatrik Popülasyon (>65 yaş)Çocuklarda kullanımı nedeniyle geçerli değildir. Pediyatrik popülasyonENBREL® tedavisine başlamadan önce, mümkün olduğu oranda pediyatrik hastaların geçerli lokal bağışıklama takvimine uygun olarak tüm aşıların tamamlanması önerilmektedir (bkz. Aşılar) Juvenil İdiyopatik Artrit (JİA) hastalarında inflamatuvar barsak hastalığı (IBH) ve üveitEtanercept ile tedavi edilen JİA hastalarında IBH ve üveit bildirimleri olmuştur.4.5 Diğer tıbbi ürünler ile etkileşimler ve diğer etkileşim şekilleri ENBREL® ve anakinra tedavisinin eş zamanlı uygulanmasıENBREL® ve anakinra ile tedavi edilen yetişkin hastaların, tek başına ENBREL® veya anakinra uygulanan (geçmiş veriler) hastalarla karşılaştırıldığında ciddi enfeksiyonlar açısından yüksek bir orana sahip olduğu gözlenmiştir.Ayrıca, geçmişinde metotreksat alan, ENBREL® ve anakinra ile tedavi gören yetişkin hastalarda yapılan çift kör, plasebo kontrollü bir çalışmada, kombinasyon tedavisi alan hastalarda ENBREL® ile tedavi gören hastalara göre daha yüksek oranda ciddi enfeksiyon (7%) ve nötropeni geliştiği gözlenmiştir. ENBREL® ve anakinra kombinasyonu klinik olarak sağlanan faydayı artırmadığından, birlikte kullanımları tavsiye edilmemektedir. ENBREL® ve abatasept tedavisinin birlikte uygulanmasıKlinik çalışmalarda ENBREL® ve abatasept'in birlikte uygulanması ciddi advers etkilerin görülme sıklığının artması ile sonuçlanmıştır. Bu kombinasyonun daha fazla bir klinik yararı olmadığı kanıtlanmış olduğundan birlikte kullanım önerilmez.ENBREL® ve sülfosalazin tedavisinin birlikte uygulanmasıBir klinik çalışmada daha önceden sulfasalazin kullanmakta olan bir gruba etanercept eklenmiş ve tek başına etanercept veya sulfasalazin alan gruplarla karşılaştırıldığında ortalama beyaz kan hücreleri sayısında istatistiksel olarak belirgin düşüş gözlemlenmiştir. Bu etkileşimin klinikteki Önemi bilinmemektedir.Etkileşime girmediği ilaçlar:Klinik denemelerde, ENBREL® ile birlikte glukokortikoidler, salisilatlar (sulfasalazin dışında), non-steroid antiinflamatuvar ilaçlar (NSAIDs), analjezikler ve metotreksat kullanıldığında herhangi bir etkileşim rapor edilmemiştir.Digoksin ve varfarin ile yapılan çalışmalarda, klinik olarak önemli bir farmakokinetik etkileşiminin olmadığı gözlenmiştir. Özel popülasyon la ra ilişkin ek bilgiler:Özel popülasyonlara ilişkin herhangi bir etkileşim çalışması tespit edilmemiştir.Pediyatrik popülasyon:Pediyatrik popülasyona ilişkin herhangi bir etkileşim çalışması tespit edilmemiştir.4.6 Gebelik ve laktasyon Genel tavsiyeGebelik Kategorisi: BÇocuk doğurma potansiyeli bulunan kadınlar/Doğum kontrolüÇocuk doğurma potansiyeli bulunan kadınlara ENBREL® tedavisi sırasında ve tedavi bırakıldıktan sonraki üç hafta süreyle hamile kalmamaları için uygun bir kontrasepsiyon yöntemi kullanmaları önerilmelidir.Gebelik dönemiHayvanlar üzerinde yapılan çalışmalar, gebelik / embriyonal / fetal gelişim / doğum ya da doğum sonrası gelişim ile ilgili olarak doğrudan ya da dolaylı zararlı etkiler olduğunu göstermemektedir.(bknz. Bölüm 5.3)Hamile kadınlarda ENBREL® ile yapılmış çalışma bulunmamaktadır. Bu nedenle hamile kadınlarda ENBREL® kullanımı tavsiye edilmemektedir. Etanersept plasentayı geçmektedir ve hamileliği sırasında ENBREL ile tedavi edilmiş kadın hastaların doğurduğu bebeklerin serumunda tespit edilmiştir. Bu durumun klinik etkisi bilinmemektedir; ancak bebekler enfeksiyon risiki taşıyabilir. Annenin son ENBREL dozundan sonraki 16 hafta boyunca bebeklere canlı aşıların uygulanması genel olarak önerilmemektedir. Laktasyon dönemiENBREL®'in emzirme sırasındaki güvenliliği değerlendirilmemiştir. ENBREL®'in SC uygulamanın ardından insan sütüne geçtiği bildirilmiştir. Emziren sıçanlarda SC uygulamayı takiben, Enbrel süte geçmiştir ve yavruların serumlarında tayin edilmiştir. Diğer tıbbi ürünlerle benzer olarak immünoglobulinler insan sütüne geçebilir.Emzirmenin durdurulup durdurulmayacağına ya da ENBREL® tedavisinin durdurulup durduramayacağına/ tedaviden kaçınılıp kaçınılmayacağına ilişkin karar verilirken, emzirmenin çocuk açısından faydası ve ENBREL® tedavisinin emziren anne açısından faydası dikkate alınmalıdır. Üreme yeteneği / FertiliteFare ve tavşanlar üzerinde yapılan gelişimsel toksisite çalışmalarında etanercept'e bağlı fetüste veya yeni doğan farede herhangi bir zarar görülmemiştir.Etanercept'in doğum öncesi ve doğum sonrası toksisite, fertilite üzerindeki etkileri ve genel üreme performansı ile ilgili preklinik çalışmalar bulunmamaktadır. 4.7 Araç ve makine kullanımı üzerindeki etkilerÇocuklarda kullanılması nedeniyle geçerli değildir.4.8 İstenmeyen etkilerJİA olan pediyatrik hastalarda görülen istenmeyen etkilerPediyatrik hastalardaki istenmeyen etkiler genellikle sıklık ve tip olarak yetişkin hastalarda görülenler ile benzerdir. Erişkinlere kıyasla farklılıklar ve diğer özel durumlar, aşağıdaki paragraflarda tartışılmaktadır.2-18 yaş arasındaki JİA hastalarında yapılan klinik çalışmalarda görülen enfeksiyon tipleri, genellikle hafif ve orta şiddettedir ve ayaktan tedavi gören pediyatrik popülasyonlarda sık olarak görülenlerle uyumludur. Bildirilmiş olan ciddi advers olaylar arasında, aseptik menenjit bulgu ve belirtileri ile birlikte giden ve sekelsiz iyileşen su çiçeği, apandisit, gastroenterit, depresyon / kişilik bozukluğu, deride ülser, özefajit / gastrit, A grubu streptokokal septik şok, tip I diabetes mellitus ve yumuşak doku ile post-operatıf yara enfeksiyonlarıdır. JİA olan 4-17 yaşlar arasındaki çocuklarda yapılan bir çalışmada, 69 çocuktan 43'ünde (% 62) çalışmanın 3 aylık dönemi sırasında (1. kısım, açık-etiketli) enfeksiyon ortaya çıkmış ve 12-ay süreli açık-etiketli uzatma tedavisini tamamlayan 58 hastada, enfeksiyonların şiddeti benzer bulunmuştur. JİA hastalarındaki advers olayların türleri ve oranları, romatoid artriti olan erişkin hastalarda ENBREL®'le yürütülen çalışmalarda görülenlere benzerdir ve çoğunluğu hafif şiddettedir. Bazı advers olaylar, 3 ay süreyle ENBREL® alan 69 JİA hastasında, 349 erişkin romatoid artrit hastasına kıyasla daha sık rapor edilmiştir. Bu advers olaylar, başağrısı (hastaların % 19'unda, 1.7 olay / hasta yılı), bulantı (%9, 1.0 olay / hasta yılı), karın ağrısı (%19, 0.74 olay / hasta yılı) ve kusma ( %13, 0.74 olay / hasta yılı). JİA hastalarında yapılan klinik çalışmalarda 4 makrofaj aktivasyon sendrom vakası rapor edilmiştir. Pazarlama sonrası kaynaklardan,ENBREL® ile tedavi edilen JİA hastalarında IBH (inflamatuvar barsak hastalığı) ve üveit bildirimleri olmuştur. Bu bulgular çok az sayıda hastada ilacın kesilmesi ile kaybolmuş ve tekrar verilmesi ile yeniden ortaya çıkmıştır (positive rechallenge). Plak psöriazisi olan pediyatrik hastalarda görülen istenmeyen etkiler 4 ile 17 yaşları arasında 211 pediyatrik plak psöriazis hastalarında yapılan 48 hafta süreli bir çalışmada raporlanan yan etkiler yetişkin plak psöriazis hastaları için daha önce yapılan çalışmalarda görülenler ile benzerdir. Erişkinlerde istenmeyen etkilerYaygın olarak raporlanan yan etkiler enjeksiyon bölgesi reaksiyonları (ağrı, kaşınma, kızarıklık ve enjeksiyon bölgesinde kanama gibi), enfeksiyonlar (üst solunum yolu enfeksiyonları, bronşit, idrar yolu ve cilt enfeksiyonları gibi), allerjik reaksiyonlar, otoantikor oluşumu, kaşınma ve ateştir.ENBREL® kullanımı ile birlikte ciddi yan etkiler de bildirilmiştir. ENBREL® gibi TNF-antagonistleri bağışıklık sistemini etkiler ve kullanımları vücudun enfeksiyon ve kansere karşı savunmasını etkileyebilir. Ciddi enfeksiyonlar ENBREL® kullanan 100 hastada l'den azını etkiler. Raporlar ölümcül ve hayat tehdit edici enfeksiyonları ve sepsisi içermektedir. ENBREL® kullanımı ile birlikte göğüs, akciğer, cilt ve lenfoma dahil çeşitli maligniteler bildirilmiştir. Çeşitli hematolojik, nörolojik ve otoimmün reaksiyonları da bildirilmiştir. Bunlar seyrek olarak bildirilen pansitopeni ve çok seyrek olarak bildirilen aplastik anemiyi içermektedir. ENBREL® kullanımı ile seyrek olarak merkezi demiyelinizan olaylar, çok seyrek olarak periferik demiyelinizan olaylar gözlenmiştir. Seyrek olarak lupus, lupus ilişkili olaylar ve vaskülit bildirilmiştir. İstenmeyen etkiler aşağıdaki kategorilere göre listelenmiştir: Çok yaygın (> 1/10); yaygın (> 1/100 ila <1/10); yaygın olmayan ( >1/1.000 ila <1/100); seyrek (> 1/10.000 ila <1/1.000); çok seyrek (<1/10.000); bilinmiyor: eldeki verilerden hareketle tahmin edilemiyor. Enfeksiyonlar ve enfestasyonlarÇok yaygın : Enfeksiyonlar (üst solunum yolu enfeksiyonları, bronşit, sistit, derienfeksiyonlarını içeren) Yaygın olmayan : Ciddi enfeksiyonlar (pnömoni, selülit, septik artrit, sepsis ve parazitik enfeksiyon) Seyrek : Tüberküloz, fırsatçı enfeksiyonlar (invazif fungal, protozoal, bakteriyel ve atipik mikobakteriyel enfeksiyonlar ve Legionella dahil) Bilinmiyor : Listeria, Hepatit B reaktivasyonu Neoplazm benign, malign ve belirlenmemiş (kistler ve polipler dahil)Yaygın olmayan : Melanom dışı cilt kanserleri Seyrek : Lenfoma, melanomBilinmiyor : Lösemi, Merkel hücreli karsinom Kan ve lenfatik sistem hastalıklarıYaygın olmayan : TrombositopeniSeyrek : Anemi, lökopeni, nötropeni, pansitopeni Çok Seyrek : Aplastik anemi Bağışıklık sistem hastalıklarıYaygın : Alerjik reaksiyonlar (Bkz.Deri ve subkutan doku hastalıkları),otoantikor oluşumu Yaygın olmayan : Sistemik vaskülit (anti-nötrofılik sitoplazmik antikor (ANCA) pozitif vaskülit dahil) Seyrek : Ciddi alerjik/anafılaktik reaksiyonlar (anjiyoödem, bronkospazm dahil), sarkoidoz Bilinmiyor : Makrofaj aktivasyon sen d romu, dermatomiyozit semptomlarının kötüleşmesi Sinir sistemi hastalıklarıSeyrek : Nöbet, multipl skleroz veya optik nörit ve transvers miyelit gibi lokalizeedici durumlar dahil SSS demiyelinizan olaylar Çok seyrek : Guillain-Barre sendromu, kronik inflamatuvar demiyelinizan polinöropati, demiyelinizan -polinöropati ve multifokal motor nöropati dahil periferal demiyelinizan olaylar (bkz. Bölüm 4.4) Göz hastalıklarıYaygın olmayan : Üveit, skleritKardiyak hastalıklarSeyrek : Konjestif kalp yetmezliğinde kötüleşmeSolunum, torasik ve mediastinal hastalıklarYaygın olmayan : Intertisyel akciğer hastalığı (pulmoner fibrozis ve pnömonitis dahil)Hepato-biliyer bozukluklarSeyrek : Karaciğer enzimlerinde yükselme, otoimmün hepatitDeri ve subkutan doku hastalıklarıYaygın : KaşıntıYaygın olmayan : Döküntü, ürtiker, anjioödem, psöriazise benzer döküntü, psöriazis (yeni veya alevlenme; daha çok el ayası ve ayak tabanında yeni başlayan ve püstüler tarzdakiler dahil), Seyrek : Kutanöz vaskülit (lökositoklastik vaskülit dahil), Stevens-Johnson sendromu, eritema multiforme Çok seyrek : Toksik epidermal nekroliz Kas-iskelet, bağ dokusu ve kemik hastalıklarıSeyrek : Subakut kutanöz lupus eritematozus, diskoid lupus eritematozus, Lupusbenzeri sendrom Genel hastalıklar ve uygulama bölgesi durumlarıÇok yaygın : Enjeksiyon bölgesi reaksiyonları (kanama, morarma, kaşıntı, eritem, ağrı, şişkinlik)Maligniteler ve lenfoproliferatif bozukluklarKlinik çalışmalarda 6 yıl boyunca ENBREL® uygulanan 4,114 romatoid artritli hastadan 129 çeşitli yeni malignite gözlenmiştir| bu gruba 2 yıllık aktif kontrollü çalışma sürecinde metotreksatla birlikte ENBREL ile tedavi edilen 231 hasta da dahildir. Bu klinik çalışmalarda gözlenen oran ve insidanslar üzerinde çalışılan popülasyondan beklenen sonuçlar ile benzer düzeyde bulunmuştur. ENBREL® ile tedavi edilen 240 psöriatik artrit hastasını içeren ve yaklaşık 2 yıl süren klinik çalışmalarda toplam 2 malignite vakası bildirilmiştir. 2 yıldan daha uzun bir süre içinde 351 ankilozan spondilit hastası ile yapılan klinik çalışmalarda, ENBREL tedavisi gören hastalarda 6 malignite raporlanmıştır. 2.5 yıla kadar süren çift-kör ve açık etiketli yürütülen psöriazis çalışmalarında, ENBREL® ile tedavi edilen 2711 psöriazis hastasında 30 kanser gelişimi ve 43 melanom dışı deri kanseri rapor edilmiştir.Romatoid artrit, psöriatik artrit, ankilozan spondilit ve psöriazis çalışmalarında ENBREL® ile tedavi edilen 7416 hastadan toplam 18' inde lenfoma rapor edilmiştir. Pazarlama sonrası süreçte de farklı malignitelerin raporları (meme ve akciğer karsinomu ve lenfoma dahil) alınmıştır (bkz. Bölüm 4.4) Enjeksiyon bölgesinde reaksiyonPlasebo kullanan hastalar ile kıyaslandığında etanercept kullanan romatizma hastalarinda enjeksiyon bölgesinde reaksiyon daha fazla oranda (%36'ya karşılık % 9) görülmüştür. Enjeksiyon bölgesi reaksiyonları genellikle ilk ayda ortaya çıkmıştır. Ortalama süre yaklaşık 3 ila 5 gündür. ENBREL® tedavi gruplarındaki enjeksiyon bölgesi reaksiyonlarının çoğunda herhangi bir tedavi uygulanmamıştır ve tedavi uygulananların büyük kısmı, kortikosteroidler veya oral antihistaminik gibi topikal preparatlar almıştır. Ayrıca bazı hastalarda, en yakın zamanda enjeksiyon yapılan bölgede bir deri reaksiyonu ile birlikte daha önceki enjeksiyon bölgelerinde de enjeksiyon bölgesi reaksiyonu görünümlerinin eşzamanlı ortaya çıkması şeklinde bir enjeksiyon bölgesi hatırlama (recall) reaksiyonu görülmüştür. Bu reaksiyonlar geçicidir ve tedavinin sürdürülmesi durumunda tekrarlamamıştır.Kontrollü klinik çalışmalarda psöriazis hastalarında, ilk 12 haftalık tedavi periyodunda plasebo kullanan hastalarda enjeksiyon bölgesinde reaksiyon görülme oram %3,4 iken ENBREL® ile tedavi gören hastalarda yaklaşık % 13,6'dır. Ciddi EnfeksiyonlarPlasebo kontrollü çalışmalarda, ciddi enfeksiyonların (öldürücü, yaşamı tehdit eden veya hospitalizasyon veya damar içi antibiyotik uygulaması gerektiren enfeksiyonlar) görülme sıklığında artış gözlenmemiştir. 48 ay süre ile ENBREL® tedavisi gören romatoid artritli hastaların % 6.3'ünde ciddi enfeksiyonlar meydana gelmiştir. Bu enfeksiyonlar apseler (çeşitli bölgelerde), bakteriyemi, bronşit, bursit, selülit, kolesistit, ishal, divertikülit, endokardit (şüphelenilen), gastroenterit, hepatit B, herpes zoster, bacak ülseri, ağız enfeksiyonları, osteomiyelit, otitis, peritonit, pnömoni, piyelonefrit, sepsis, septik artrit, sinüzit, deri enfeksiyonu, deri ülseri, idrar yolu enfeksiyonu, vaskülit ve yara enfeksiyonlarını kapsamaktadır. Tek başına ENBREL® veya metotreksat veya ikisinin kombinasyonu ile tedavi edilen hastaları içeren ve 2 yıl süren aktif kontrollü bir çalışmada ciddi enfeksiyonların oranının, tüm uygulama grupları arasında benzer olduğu gözlenmiştir. Fakat bu çalışma metotreksat ile ENBREL® kombinasyonu uygulamasının enfeksiyonların oranında bir artışla ilişkisinin olabileceğini dışlamamıştır.24 haftaya varan sürelerde yürütülen plasebo kontrollü plak psöriazis çalışmalarında, ENBREL® ve plasebo ile tedavi edilen hastalarda enfeksiyon oranlarında fark yoktur. ENBREL® ile tedavi edilen hastalarda ortaya çıkan ciddi enfeksiyonlar arasında sellülit, gastroenterit, pnömoni, safra kesesi iltihabı, osteomiyelit, gastrit, apandisit, Streptokokkal fasiit, myozit, septik şok, divertikülit ve apseyi içeren ciddi enfeksiyonlar bulunmaktadır. Çift kör ve açık etiketli psöriatik artrit çalışmalarında, 1 hasta ciddi bir enfeksiyon rapor lam ıştır (zatürre). ENBREL kullanımı sırasında ciddi ve ölümcül enfeksiyonlar raporlanmıştır; raporlanan patojenler arasında bakteriler, (tüberküloz dahil) mikobakteriler, virüsler ve mantar yer alır. Bunların bazıları, romatoid artritlerine (bkz. Bölüm 4.4) ek olarak altta yatan koşullan (diyabet, konjestif kalp yetmezliği, aktif ya da kronik enfeksiyonların olduğu bir geçmiş gibi) taşıyan hastalarda ENBREL tedavisinin uygulanmaya başlanmasından sonraki birkaç hafta içinde meydana gelmiştir. ENBREL tedavisi bilinen sepsisi olan hastalarda ölüm oranını arttırabilir. İnvazif fungal, parazitik (protozoal dahil), bakteriyel {ListeriaLegionellaPneumocystisAspergillus''Pneumocystis(bkz., Bölüm 4.4).Otoantikor OluşumuErişkin hastalardan alınan serum örnekleri, değişik zaman noktalarında otoantikor testine tabi tutulmuştur. Antinükleer antikorlar (ANA) için değerlendirilen romatoid artrit hastalarında, yeni pozitif ANA (ANA >1:40) gelişen hasta yüzdesi, ENBREL® ile tedavi edilen hastalarda (%11), plasebo alan hastalara kıyasla (%5) daha yüksektir. Yeni pozitif anti- çift-zincirli DNA antikorlar gelişen hasta yüzdesi de radyoimmün tayin metodu (ENBREL® ile tedavi edilen hastalarda %15'e karşılık plasebo alan hastalarda %4) veCrithidia luciliaetayini ile (ENBREL® ile tedavi edilen hastalarda %3'e karşılık plasebo alan hastalarda sıfır) daha yüksek bulunmuştur. Antikardiolipin antikorlar geliştiren hastaların oranı da, benzer şekilde, plasebo grubuna kıyasla yüksek bulunmuştur. Etanercept'in uzun dönem kullanımının otoimmün hastalıkların gelişimine etkisi bilinmemektedir.Romatoid faktör pozitif olan romatoid artritli hastalar da dahil, bazı hastalarda lupus benzeri sendrom veya klinik görünüm ve biopsi sonucu subakut deri lupus veya diskoid lupusu ile uyumlu döküntülerle birlikte başka otoantikorların geliştiği nadir advers etkiler bildirilmiştir. Pansitopeni ve aplastik anemiPansitopeni ve aplastik anemiye dair pazarlama sonrası raporlar bulunmaktadır ve bunlardan bazısı ölümle sonuçlanmıştır.İntersitisyel akciğer hastalığıİntersitisyel akciğer hastalığına dair (pnömoni ve pulmoner fibrozis dahil) pazarlama sonrası raporlar bulunmaktadır ve bunlardan bazısı ölümle sonuçlanmıştır.Eş zamanlı ENBREL® ve anakinra tedavisiErişkin hastalarda, ENBREL®'in anakinra ile eşzamanlı olarak uygulandığı çalışmalarda, tek başına ENBREL®'e kıyasla daha yüksek bir ciddi enfeksiyon oranı gözlemlenmiş ve hastaların %2'sinde (3/139) nötropeni gelişmiştir (mutlak nötrofıl sayısı <1000/mm3). Nötropenik olan bir hastada, hospitalizasyonla düzelen selülit gelişmiştir.4.9 Doz aşımı ve tedavisiRomatoid artritli hastalar ile yapılan klinik çalışmalarda doz-limitleyici toksisiteler saptanmamıştır. Değerlendirilen en yüksek doz seviyesi 32 mg/m2 olarak intravenöz uygulanan yükleme dozunu takip eden, haftada iki kez 16 mg/m subkutan olarak uygulanan dozdur. Bir romatoid artrit hastası yanlışlıkla kendine, 3 hafta boyunca haftada iki kez subkutan 62 mg ENBREL® uygulamış ve herhangi bir istenmeyen etkiyle karşılaşmamıştır.Etanercept'in antidotu yoktur. 5. FARMAKOLOJİK ÖZELLİKLEREtanercept, rekombinan DNA teknolojisi ile üretilmiş, insan tümör nekrotize edici faktör reseptör p75 (TNFR2/p75) ve insan IgGl-Fc proteininin birleştirilmesi ile elde edilen bir insan tümör nekrotize edici faktör reseptör p75 -Fc füzyon proteinidir.5.1 Farmakodinamik özelliklerFarmakoterapötik grup: Tümör nekrozis faktör (TNF)ATC kodu: L04AB01 Etki mekanizması:Romatoid artritte ve ankilozan spondilitte eklem patolojisi ve psöriazis vulgaris'te deri patolojisi, büyük oranda TNF tarafından kontrol edilen pro-inflamatuvar moleküller aracılığıyla düzenlenir. Etanercept etkisini, TNF'nin hücre yüzeyindeki TNFR'lere bağlanmasını kompetitif olarak inhibe ederek, biyolojik aktivitelerini yok edip, TNF'e bağlı gelişen hücresel yanıtlarını önleyerek göstermektedir. Ayrıca etanercept, TNF'nin düzenlediği veya diğer moleküllerin (örneğin, sitokinler, adhezyon molekülleri veya proteinazlar) kontrol ettiği biyolojik yanıtları da değiştirebilmektedir.Farmakodinamik etkiler:Tümör nekrotize edici faktör (TNF), romatoid artrite bağlı inflamasyonda dominant sitokin işlevini görür. Psöriatik artritli hastaların sinovyalarında ve psöriatik plaklarında da TNF miktarları yükselir. Ankilozan spondilitli hastaların sinovyal dokularında ve serumlarında da TNF miktarları yükselir.Psöriazis plaklarında, psöriatik lezyon görülmeyen derideki seviyelerle kıyaslandığında T-hücreleri de dahil inflamatuvar hücrelerin infıltrasyonu, psöriatik lezyonlarda TNF seviyelerinin yükselmesine sebep olur. ENBREL® TNF'in kompetitif inhibitörü olarak hücre yüzeyi reseptörlerine bağlanmasını engeller ve biyolojik aktivitesini önler. TNF ve lenfotoksin iki ayrı hücre yüzeyi reseptörlerine bağlanan pro-inflamatuvar sitokinlerdir : 55 kilodalton (p55) ve 75 kilodalton (p75) tümör nekrotize edici faktör reseptörleri (TNFR). İki TNFR de, doğal olarak membrana bağlı ve çözünen formdadır. TNF ve lenfotoksinlerin biyolojik aktiviteleri hücre yüzeyindeki TNFR'lere çapraz biçimde bağlanmaları esasına dayanır. Etanercept gibi çözülen dimerik reseptörler, monomerik reseptörlere kıyasla TNF'ye daha yüksek bir afinite gösterirler ve kendi hücre reseptörlerine bağlanan TNF'nin çok daha güçlü kompetitif inhibitörleridir. Bunlara ilaveten, dimerik reseptör yapısında immunoglobulinlerin Fc bölgesinin füzyon yapılar olarak kullanılması, etanercept'in serum yarılanma ömrünü uzatmaktadır. Klinik etkililik ve güvenlilikBu bölümde; poliartiküler jüvenil idiyopatik artrit ile ilgili üç çalışmanın, plak psöriazisli pediyatrik hastalarla ilgili bir çalışmanın, romatoid artritli yetişkin hastalardaki dört çalışmanın ve plak psöriazisli yetişkin hastalardaki dört çalışmanın verileri sunulmaktadır. Pediyatrik popülasyonJİA'lı pediyatrik hastalarENBREL®'in güvenliliği ve etkililiği, farklı jüvenil idiyopatik artrit başlangıç tipleri olan (poliartrit, oligoartrit, sistemik başlangıçlı) poliartiküler jüvenil idiyopatik artrit hastası 69 çocukta yapılan iki bölümlü bir çalışmada değerlendirilmiştir. 4 ila 17 yaşları arasında, metotreksata refrakter ya da toleransı olmayan, orta ila şiddetli aktif poliartiküler jüvenil idiyopatik artrit hastaları dahil edilmiş; hastalar sabit dozda non-steroid anti-inflamatuvar ilaç ve/veya prednizon (<0.2 mg/kg/gün veya maksimum 10 mg) almaya devam etmiştir. Birinci bölümde bütün hastalar haftada iki defa subkutan olarak 0.4 mg/kg (tek dozda maksimum 25 mg) ENBREL® almıştır. İkinci bölümde 90. günde klinik yanıtı olan hastalar ENBREL®'de devam etmeye ya da dört ay boyunca plasebo tedavisine randomize edilmiş ve hastalık alevlenmesi için değerlendirilmiştir. Yanıtlar; aktif eklem sayısı, hareket kısıtlanması, hekim ve hasta/ebeveyn global değerlendirmeleri, fonksiyonel değerlendirme ve eritrosit sedimantasyon hızı (ESR) dahil JRA temel kriterlerinin altı tanesinden en az üçünde >%30 iyileşme ve altı tanesinden en fazla birinde >%30 kötüleşme olarak tanımlanan ACR Pedi30 (DOI) kullanılarak değerlendirilmiştir. Hastalık alevlenmesi; altı JRA temel kriterinden üçünde >%30 kötüleşme ve altı JRA temel kriterinden en fazla birinde >%30 iyileşme ve minimum iki aktif eklem olarak tanımlanmıştır. Çalışmanın 1. bölümünde 69 hastadan 5İM (%74) klinik yanıt göstermiş ve 2. bölüme devam etmiştir. İkinci bölümde ENBREL®'e devam eden 25 hastadan 6'sı (%24) hastalık alevlenmesi geçirmiştir, bu oran plasebo alan hastalarda 26 hastada 20'dir (%77) (p=0.007). İkinci bölümün başlangıcından itibaren alevlenmeye kadar olan medyan süre ENBREL® alan hastalarda >116 gün ve plasebo alan hastalarda 28 gündür. 90 günde klinik yanıt veren ve çalışmanın 2. bölümüne geçen hastalardan, ENBREL® alan bir kısım hasta 3. aydan 7. aya kadar iyileşme göstermeye devam etmişken, plasebo alan hastalarda herhangi bir iyileşme gözlenmemiştir. Bir açık etiketli güvenlilik uzatma çalışmasında, yukarıdaki çalışmadan 58 pediyatrik hasta (kayıt anında 4 yaşından itibaren) 10 yıla kadar ENBREL® kullanımına devam etmiştir. Uzun dönem kullanım ile birlikte ciddi advers olaylar ve ciddi enfeksiyonların oranında artış olmamıştır. 39'u 2 ila 3 yaşlarında olan jüvenil idiyopatik artritli 2 ila 18 yaşlarındaki 594 çocuğa ilişkin kayıt kütüğünde ENBREL® monoterapisinin (n=103), ENBREL artı metotreksatm (n=294) veya metotreksat monoterapisinin (n=197) uzun dönem güvenliliği değerlendirilmiştir. Genel olarak, tek başına metotreksata kıyasla ENBREL® uygulanan hastalarda enfeksiyonlar daha yaygın bildirilmiştir (%2'ye karşı %3.8) ve ENBREL® kullanımıyla ilişkili enfeksiyonlar daha şiddetli olmuştur. Diğer bir açık etiketli, tek kollu çalışmada, 60 yaygın oligoartrit hastası (15 hasta 2 ile 4 yaş arasında, 23 hasta 5 ile 11 yaş arasında, 22 hasta 12 ile 17 yaş arasında), 38 entezit ilişkili artrit hastası (12 ile 17 yaş arasında) ve 29 psöriatik artrit hastası (12 ile 17 yaş arasında) 12 hafta boyunca haftada bir kez uygulanan 0.8 mg/kg dozuyla (bir dozda maksimum 50 mg) tedavi edilmiştir. Her bir JİA alt tipinde, hastaların çoğunluğu ACR Pedi 30 kriterini karşılamış ve hassas eklem sayısı ve hekim global değerlendirmeleri gibi sekonder sonlanım noktalarında klinik iyileşme göstermiştir. Güvenlilik profili diğer JİA çalışmalarında gözlemlenen ile uyumludur. ENBREL® tedavisi başladıktan sonraki 3 ay boyunca yanıt vermemiş JİA hastalarında devamlı Enbrel tedavisinin etkilerinin değerlendirilmesi için çalışmalar yapılmamıştır. Ayrıca JİA olan hastalarda uzun dönem kullanımın ardından, önerilen ENBREL® dozunun sonlandırılmasınm veya azaltılmasının etkilerini değerlendirmek için çalışmalar yapılmamıştır. Plak psöriazisli pediyatrik hastalarENBREL®'in etkililiği, orta ila şiddetli plak psöriazisli (vücut yüzeyi alanının >%10'ıınu kapsayan sPGA skoru >3 ve PASI >12 şeklinde tanımlanmıştır) 4 ila 17 yaşlarındaki 211 pediyatrik hastada yapılan randomize, çift kör, plasebo kontrollü bir çalışmada değerlendirilmiştir. Uygun hastalar fototerapi veya sistemik tedavi öyküsü veya top i kal tedaviyle yetersiz kontrolü olan hastalardı. Hastalar, 12 hafta boyunca haftada bir kez ENBREL® 0.8 mg/kg (50 mg'ye kadar) veya plasebo almıştır. 12. haftada, plaseboya randomize edilen hastalara kıyasla ENBREL® tedavisine randomize edilen daha fazla hastada pozitif etkililik yanıtı (örn. PASI 75) gözlenmiştir.
Haftada bir kez ENBREL® 0.8 mg/kg'nin (50 mg'ye kadar) uzun dönem güvenliliği ve etkililiği, yukarıda açıklanan 48 haftalık çalışmadan sonra 2 yıla kadar plak psöriazis olan 181 pediyatrik hastada açık etiketli bir uzantı çalışmasında değerlendirilmiştir. ENBREL® ile uzun dönem deneyimler genellikle orijinal 48 haftalık çalışmaya benzer olmuştur ve herhangi bir yeni güvenlilik bulgusu ortaya koymamıştır. Romatoid artritliyetişkin hastalarENBREL®'in etkililiği randomize, çift kör, plasebo kontrollü bir çalışmada değerlendirilmiştir. Bu çalışmada, en az bir ancak en fazla dört hastalık modifıye edici antiromatizmal ilaçla (DMARD'lar) tedavisi başarısız olmuş aktif romatoid artrit olan 234 yetişkin hasta değerlendirilmiştir. Altı ardışık ay boyunca haftada iki kez subkutan olarak 10 mg veya 25 mg ENBREL® veya plasebo uygulanmıştır. Bu kontrollü çalışmanın bulguları, Amerikan Romatoloji Koleji (ACR) yanıt kriterleri kullanılarak romatoid artritteki yüzde iyileşme olarak ifade edilmiştir. ENBREL® ile tedavi edilen hastalarda 3. ve 6. ayda ACR 20 ve 50 yanıtları, plasebo uygulanan hastalardan daha yüksek olmuştur (ACR 20: 3. ve 6. ayda sırasıyla ENBREL® %62 ve %59, plasebo %23 ve %11; ACR 50: 3. ve 6. ayda sırasıyla ENBREL® %41 ve %40, plasebo %8 ve %5; ACR 20 ve ACR 50 yanıtları için tüm zaman noktalarında plaseboya karşı ENBREL® p<0.01). ENBREL® alan olguların yaklaşık %15'i 3. ayda ve 6. ayda ACR 70 yanıtı elde ederken, bu oran plasebo kolunda %5'ten düşük olmuştur. ENBREL® alan hastalarda klinik yanıtlar genellikle tedavi başlangıcından 1 - 2 hafta sonra görülür ve nerdeyse 3. ayda hep yanıt alınır. Doz yanıt orantısallığı görülmüştür; 10 mg ile sağlanan etkililik, plasebo ile 25 mg arasındadır. ENBREL®, hem ACR kriterlerinde hem de sabah katılığı gibi ACR yanıt kriterlerine dahil edilmeyen diğer romatoid artrit hastalığı aktivite ölçümlerinde plasebodan anlamlı şekilde daha iyi bulunmuştur. Çalışma boyunca 3 ayda bir fonksiyon kaybı, aktiflik, ruhsal sağlık, genel sağlık durumu ve artritle ilişkili sağlık durumu alt alanlarını içeren bir Sağlık Değerlendirme Anketi (HAQ) uygulanmıştır. Kontrollere kıyasla ENBREL® alan hastalarda 3. ve 6. ayda tüm HAQ değerleri iyileşmiştir. ENBREL®'in sonlandırıİması ardından artrit semptomları genellikle bir ay içinde geri dönmüştür. Açık etiketli çalışmaların bulguları temelinde, 24 aya kadar tedaviye ara verilip ardından ENBREL® tedavisine tekrar başlanması ile elde edilen sonuçlarla, tedaviye ara verilmeden ENBREL® alan hastalarda elde edilen sonuçlar aynıdır. Açık etiketli uzatma çalışmalarında, hastalar ara vermeden ENBREL® aldıklarında 48 aya kadar devam eden sürekli yanıtlar görülmüştür. Aktif romatoid artrit olan (hastalık süresi <3 yıl), daha önce hiç metotreksat tedavisi almamış 632 yetişkin hastada, primer sonlanım noktası olarak körleştirilmiş radyografık değerlendirmelerin kullanıldığı randomize, aktif kontrollü bir çalışmada ENBREL®'in etkililiği metotreksat ile karşılaştırılın ıştır. 24 aya kadar haftada iki kez subkutan (SC) yolla 10 mg veya 25 mg dozlarda ENBREL® uygulanmıştır. Metotreksat dozları, çalışmanın ilk 8 haftasında 7.5 mg/haftadan 20 mg/haftaya arttırılmış ve 24 aya kadar devam etmiştir. ENBREL® 25 mg ile 2 hafta içindeki etki başlangıcı dahil klinik iyileşme, önceki çalışmalarda görülene benzer olmuş ve 24 aya kadar devam etmiştir. Hastalar, başlangıçta 1.4 ila 1.5 HAQ skorları ile orta derecede engelli idi. ENBREL® 25 mg tedavisi 12 ayda belirgin iyileşme sağlamış, hastaların yaklaşık %44'ü normal bir HAQ skoruna ulaşmıştır (0.5'ten düşük). Bu fayda çalışmanın 2. yılında devam etmiştir. Bu çalışmada, yapısal eklem hasarı radyografık olarak değerlendirilmiş ve bileşenleri erozyon skoru ve eklem aralığında daralma (JSN) olan Total Sharp Skoru (TSS)'nda değişiklik olarak ifade edilmiştir. El/bilek ve ayak radyografileri başlangıçta, 6., 12. ve 24. Aylarda değerlendirilmiştir. 10 mg ENBREL® dozu, 25 mg doza kıyasla yapısal hasar üzerinde tutarlı şekilde daha az etki göstermiştir. ENBREL® 25 mg hem 12 hem de 24 ayda erozyon skorları açısından metotreksata göre anlamlı olarak üstün olmuştur. Metotreksat ve ENBREL® 25 mg arasında TSS ve JSN'deki farklılıklar istatistiksel olarak anlamlı bulunmamıştır. Sonuçlar aşağıdaki şekilde gösterilmektedir. Radyografik Progresyon: <3 Yıl Süreyle RA olan Hastalarda ENBREL® ile Metotreksatın Karşılaştırılması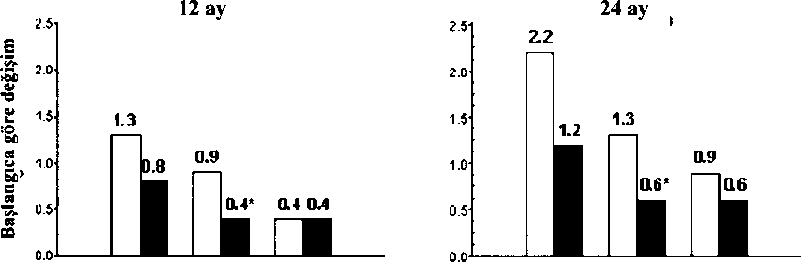
TSS Erozyonlar JSN TSS Erozyonlar JSN?? NTX¦ Enbrel 25 mg 'p <aos Başka bir aktif kontrollü, çift kör, randomize çalışmada; 6 ay ila 20 yıl süreyle (medyan 5 yıl) aktif romatoid artriti olan, metotreksat dışında en az 1 DMARD'a yeterli yanıt vermeyen 682 yetişkin hastada tek başına ENBREL® (haftada iki kez 25 mg), tek başına metotreksat (haftada bir kez 7.5 ila 20 mg, medyan doz 20 mg) ve eş zamanlı başlanan ENBREL® ile metotreksat kombinasyonunun klinik etkililik, güvenlilik ve radyografik progresyona etkisi karşılaştırılmıştır. Metotreksat ile kombinasyon halinde ENBREL® tedavisi alan gruptaki hastalarda hem 24., hem de 52. haftalarda ACR 20, ACR 50, ACR 70 yanıtları ve DAS ile HAQ skorlarındaki iyileşme monoterapi grubundaki hastalardan anlamlı şekilde daha yüksek olmuştur (bulgular aşağıdaki tabloda gösterilmiştir). ENBREL® monoterapisine ve nıetotreksat monoterapisine kıyasla metotreksatla kombinasyon halinde ENBREL® için belirgin avantajlar 24 ay sonra da gözlenmiştir.
Radyografık Progresyon: 6 Ay ila 20 Yıl Süreyle RA Olan Hastalarda ENBREL , Metotreksat ve Metotreksatla Kombinasyon Halinde EnbrePin Karşılaştırılması (12 Aylık Bulgular)7.8tı-ıMetotreksatH Enbrri ¦¦Enbrel + Metotreksat -1.231*-0JS4t'*
410
L21'
1.12
1.6* 'O
TSS -Erozyonlar- J5N
:0 Öt
İkili karşılaştırma p-değerleri: * = ENBREL ile metotreksat karşılaştırması için p <0.05, t = ENBREL® + metotreksat ile metotreksat karşılaştırması için p <0.05 ve O =
türcıloctıcmocı ı/'in r\<""fi A^3İ)2 .5 H2ü--0.5-10 J
]L
e «s aa
mf'trtfrpl/c'it ılp PMRPFT ENBREL® monoterapisine ve metotreksat monoterapisine kıyasla metotreksatla kombinasyon halinde ENBREL® için belirgin avantajlar 24 ay sonra da gözlenmiştir. Benzer şekilde, metotreksat monoterapisine kıyasla ENBREL® monoterapisi için belirgin avantajlar 24 ay sonra da gözlenmiştir. Herhangi bir nedenle çalışmadan ayrılan tüm hastaların progresyon gösterdiği kabul edilen bir analizde, metotreksatla kombinasyon halinde ENBREL® grubunda 24 ayda progresyon olmayan (TSS değişimi <0.5) hastaların oranı, tek başına ENBREL® ve tek başına metotreksat gruplarına kıyasla daha yüksek olmuştur (sırasıyla %62, %50 ve %36; p<0.05). Tek başına ENBREL® ve tek başına metotreksat arasındaki fark da anlamlı olmuştur (p<0.05). Çalışmada 24 aylık tedaviyi tamamlayıp progresyon görülmeyen hastaların oranları sırasıyla %78, %70 ve %61 bulunmuştur. Plak psöriazisli yetişkin hastalarHedef popülasyonda tedaviye yanıt vermeyen hastalar; yetersiz yanıt olmasıyla (PASI<50 veya PGA iyiden az) veya tedavi alırken hastalığın kötüleşmesiyle ve üç majör sistemik tedavinin en az her biriyle yanıt değerlendirilecek kadar uzun süre yeterli doz uygulanan hastalar ile tanımlanır. Orta ila şiddetli psöriazis olan (diğer sistemik tedavilere yanıt veren) hastalarda diğer sistemik tedavilere karşı ENBREL 'in etkililiği, doğrudan karşılaştırmalı çalışmalarda değerlendirilmemiştir. Bunun yerine, ENBREL®'in güvenliliği ve etkililiği randomize, çift kör, plasebo kontrollü dört çalışmada değerlendirilmiştir. Bu dört çalışmanın tümünde primer etkililik sonlamm noktası, her tedavi grubunda 12 haftada PASI 75 (yani Psöriazis Alan ve Şiddet İndeksi skorunda başlangıca göre en az %75 iyileşme) yanıtına ulaşan hastaların oranı olmuştur. 1. Çalışma, vücut yüzeyi alanının >%10'unu kapsayan aktif ancak klinik açıdan stabil plak psöriazisi olan >18 yaşındaki hastalarda yapılan bir Faz 2 çalışmadır. 112 hasta, 24 hafta boyunca haftada iki kez 25 mg ENBREL® (n=57) veya plasebo (n=55) almak üzere randomize edilmiştir. 2. Çalışmada, I. çalışmayla aynı dahil etme kriterleri kullanılarak ve tarama sırasında minimum PASI skorunun 10 olması kriteri eklenerek, kronik plak psöriazisi olan 652 hasta değerlendirilmiştir. ENBREL®, 6 ardışık ay boyunca haftada bir 25 mg, haftada iki 25 mg veya haftada iki 50 mg dozlarda uygulanmıştır. Çift kör tedavi döneminin ilk 12 haftası boyunca hastalar plasebo veya yukarıdaki üç ENBREL® dozundan birini almıştır. 12 haftalık tedaviden sonra plasebo grubundaki hastalar körleştirilmiş ENBREL® tedavisine (haftada iki kez 25 mg) başlamıştır; aktif tedavi gruplarındaki hastalar ise başlangıçta randomize edilen dozla 24. haftaya kadar devam etmiştir. 3. Çalışmada 583 hasta değerlendirilmiş ve 2. çalışmayla aynı dahil etme kriterleri kullanılmıştır. Bu çalışmadaki hastalar 12 hafta boyunca haftada iki kez 25 mg veya 50 mg ENBREL® veya plasebo almıştır ve ardından tüm hastalar ilave 24 hafta boyunca haftada iki kez açık etiketli 25 mg ENBREL®almıştır. 4. Çalışmada 142 hasta değerlendirilmiş, 2. ve 3. çalışmayla aynı dahil etme kriterleri kullanılmıştır. Bu çalışmadaki hastalar 12 hafta boyunca haftada bir kez 50 mg ENBREL® veya plasebo almıştır ve ardından tüm hastalar ilave 12 hafta boyunca haftada bir kez açık etiketli 50 mg ENBREL® almıştır.
2. Çalışma, en az %50 PASI yanıtına ulaşan hastaların 24. haftada tedavi kesildikten sonra da gözlendiği ilaçsız bir dönem içermiştir. Hastalar, rebound oluşumu (PASI başlangıcın >%150'si) ve nükse (başlangıç ve 24. hafta arasında elde edilen iyileşmenin en az yarısının kaybı olarak tanımlanmıştır) kadar geçen süre açısından tedavisiz dönemde gözlenmiştir. İlaçsız dönem sırasında, hastalık nüksüne kadar geçen medyan süre 3 ay olmak üzere, psöriazis semptomları aşamalı olarak tekrar belirmiştir. Hastalık rebound alevlenmesi ve psöriazis ile ilişkili ciddi advers olaylar gözlenmemiştir. Başlangıçta tedaviye yanıt veren hastalarda ENBREL® ile tekrar tedavinin yararını destekleyen kanıtlar vardır. 3. Çalışmada, başlangıçta haftada iki kez 50 mg'ye randomize edilen ve 12. haftada ENBREL® dozu haftada iki kez 25 mg'ye azaltılan hastaların büyük bölümü (%77), 36. haftaya kadar PASI 75 yanıtını korumuştur. Çalışma boyunca haftada iki kez 25 mg alan hastaların PASI 75 yanıtı 12. ve 36. haftalar arasında iyileşmeyi sürdürmüştür. 4. Çalışmada, ENBREL® tedavisi uygulanan grupta 12. haftada PASI 75 olan hastaların oranı (%38), plasebo uygulanan gruptan (%2) daha yüksek olmuştur (p<0.0001). Çalışma boyunca haftada bir kez 50 mg alan hastalarda etkililik yanıtları artmayı sürdürmüş, 24. haftada hastaların %71'i PASI 75 yanıtına ulaşmıştır. ENBREL®'in kesintisiz verildiği uzun dönem (34 ay) açık etiketli çalışmalarda, klinik yanıtlar korunmuş ve güveni ilik kısa dönem çalışmalarla benzer olmuştur. Klinik çalışma verilerinin bir analizi, klinisyenlere en uygun doz seçeneğinin (aralıklı veya sürekli) belirlenmesinde yardımcı olacak, hastalığa ilişkin bir başlangıç özelliği ortaya koymamıştır. Sonuç olarak, aralıklı veya sürekli tedavi uygulama tercihi, hekimin kararına ve hastanın bireysel ihtiyaçlarına dayalı olmalıdır. Enbrel 'e karşı antikorlarEtanercept'e karşı antikorlar, etanercept ile tedavi uygulanan bazı olguların serumunda saptanmıştır. Bu antikorların tümü non-nötralizandır ve genellikle geçicidir. Antikor gelişimi ve klinik yanıt veya advers olaylar arasında ilişki görünmemektedir. Klinik çalışmalarda onaylanmış etanercept dozlarıyla 12 aya kadar tedavi uygulanan olgularda anti-etanercept antikorlarının kümülatif oranları; romatoid artritli olguların yaklaşık %6'sı, psöriatik artritli olguların %7.5'i, ankilozan spondilitli olguların %2'si, psöriazisli olguların %7'si, pediyatrik psöriazisli olguların %9.7'si ve jüvenil idiyopatik artritli olguların %3'ü şeklinde bulunmuştur. Uzun dönem çalışmalarda (3.5 yıla kadar) etanercepte karşı antikor gelişen olguların oranı, beklendiği üzere zaman içinde artmaktadır. Bununla birlikte, her değerlendirme noktasında saptanan antikorların insidansı, geçici yapıları nedeniyle, tipik şekilde romatoid artrit olgularının ve psöriazis olgularının %7'sinden azı şeklindedir. Hastaların 96 hafta boyunca haftada iki kez 50 mg aldığı bir uzun dönem psöriazis çalışmasında, her değerlendirme noktasında gözlenen antikorların insidansı yaklaşık %9 olmuştur. 5.2 Farmakokinetik özellikler Genel Özellikler:Emilim:Etanercept, subkutan (s.c) enjeksiyonundan sonra yavaş absorbe olur, tek dozda 48 saat içinde maksimum konsantrasyona ulaşır. Mutlak biyoyararlanımı % 76'dır. Dağılım:Haftada iki defa alınan dozda beklenen sabit konsantrasyonları tek doz alımında gözlenenden iki kat fazla olur. 25'mg lık tek doz ENBREL®, sağlıklı gönüllülere s.c. olarak uygulandığında, ortalama maksimum serum konsantrasyonları 1.65 ± 0.66 |^g/ml ve eğri altındaki alan da 235 ± 96.6 Hg.saat/ml olarak saptanmıştır. B i votran sformas von:Etanercept metabolizmasını inceleyen raporlanmış farmakokinetik çalışmalar bulunmamaktadır. Etanercept'in TNF'e bağlandıktan sonra bileşiğin, aminoasit geri döngüsü veya safra ve idrar yolu eliminasyonu ile olmak üzere peptid ve amino asit yolu ile metabolize olduğu düşünülmektedir. Eliminasvon:Etanercept vücuttan yavaş yavaş itrah edilir. Yarılanma ömrü, yaklaşık 70 saattir. Romatoid artritli hastalarda klerens hızı 0.066 litre/saat olup bu değer klerens hızı 0.11 litre/saat olan sağlıklı bireylerden daha düşüktür. Romatoid artrit, ankilozan spondilit ve psöriazis hastalarında ENBREL®'in farmakokinetik özellikleri benzerdir. Kararlı durumda ortalama serum konsantrasyon profillerinin, haftada bir kere 50 mg ENBREL® uygulanan ve haftada iki kere 25 mg ENBREL® uygulanan romatoid artrit hastalarında karşılaştırılabilir olduğu görülmüştür [ sırasıyla, Cmaks (2.4 mg/l ve 2.6 mg/1), Cmjn (1.2 mg/1 ve 1.4 mg/1) ve kısmi EAA (297 mgh/1 ve 316 mgh/1) ]. Doğrusallık/Dogrusal olmayan durum:Doz oransallığı değerlendirilmemiştir, ancak doz aralığı boyunca klerenste belirgin doygunluk bulunmamaktadır. Hastalardaki karakteristik özelliklerBöbrek yetmezliği:Hastalara ve gönüllülere radyoaktif işaretli etanercept uygulandığında idrardan radyoaktivitenin itrah olduğu saptanmasına rağmen akut böbrek yetersizliğinde etanercept dozunda bir birikme olduğu saptanmamıştır. Böbrek yetersizliğinde özel bir doz ayarı yapılmasına gerek yoktur. Karaciğer yetmezliği:Akut karaciğer yetersizliğinde artmış etanercept konsantrasyonları saptanmamıştır. Karaciğer yetersizliğinde özel bir doz ayarı yapılmasına gerek yoktur. Pediyatrik popülasyon:JİA'lı hastalar: ENBREL® ile yürütülen bir poliartiküler jüvenil idiyopatik artrit çalışmasında, 69 hastaya (4-17 yaş arası) 3 ay süreyle haftada iki kez 0.4 mg ENBREL® /kg uygulanmıştır. Serum konsantrasyon profilleri, erişkin romatoid artrit hastalarında görülenlere benzer bulunmuştur. En küçük yaş grubundaki çocuklarda (4 yaş) klerens, daha büyük çocuklara (12 yaş) ve erişkinlere kıyasla azalmıştır. Doz simülasyonu, daha büyük çocuklarda (10-17 yaş arası) serum düzeylerinin erişkinlere yakın olacağını, buna karşılık küçük çocuklarda önemli ölçüde daha düşük düzeyler görüleceğini düşündürmektedir. Plak psöriazisli pediyatrik hastalar Pediyatrik plak psöriazisli (4-17 yaş arasında) hastalara 48 haftaya kadar haftada bir defa 0.8 mg/kg (haftada maksimum 50 mg) uygulanmıştır. Ortalama serum konsantrasyonları 12., 24. ve 48. haftalarda 1.6 ila 2.1 mcg/ml arasındadır. Serum konsantrasyonları, JİA'lı hastalarda (haftada maksimum 50 mg doza kadar, haftada 2 kez 0.4 mg/kg etanercept alan) görülenlere benzer bulunmuştur Bu serum konsantrasyonları, haftada 2 kez 25 mg etanercept alan erişkin plak psöriazis hastalarında görülenlere benzer bulunmuştur Yetişkinler:Etanercept, subkutan (s.c) enjeksiyonundan sonra yavaş absorbe olur, tek dozda 48 saat içinde maksimum konsantrasyona ulaşır. Mutlak biyoyararlanımı % 76 dır. Haftada iki defa alınan dozda beklenen sabit konsantrasyonları tek doz atımında gözlenenden iki kat fazla olur. 25'mg tık tek doz ENBREL®, sağlıklı gönüllülere s.c. olarak uygulandığında, ortalama maksimum serum konsantrasyonları 1.65 ± 0.66 |ag/ml ve eğri altındaki alan da 235 ± 96.6 ng.saat/ml olarak saptanmıştır. Etanercept vücuttan yavaş yavaş itrah edilir. Yarılanma ömrü, yaklaşık 80 saattir.. Romatoid artritli hastalarda klerens hızı 0.066 litre/saat olup bu değer klerens hızı 0.11 litre/saat olan sağlıklı bireylerden daha düşüktür. Romatoid artrit, ankilozan spondilit ve psöriazis hastalarında ENBREL®'in farmakokinetik özellikleri benzerdir. Kararlı durumda ortalama serum konsantrasyon profillerinin, haftada bir kere 50 mg ENBREL® uygulanan ve haftada iki kere 25 mg ENBREL® uygulanan romatoid artrit hastalarında karşılaştırılabilir olduğu görülmüştür [ sırasıyla, Cmax (2.4 mg/1 ve 2.6 mg/lXCmm 0<2 mg/1 ve 1.4 mg/1) ve kısmi AUC (297 mgh/1 ve 316 mgh/1) ]. Hastalara ve gönüllülere radyoaktif işaretli etanercept uygulandığında idrardan radyoaktivitenin itrah olduğu saptanmasına rağmen akut böbrek ve karaciğer yetersizliklerinde etanercept dozunda bir birikme olduğu saptanmamıştır. Karaciğer ve böbrek yetersizliklerinde özel bir doz ayarı yapılmasına gerek yoktur. Farmakokinetik açıdan kadın ve erkek arasında bir fark yoktur. Metotreksat etanercept'in farmakokinetiğini etkilemez. ENBREL®'in metotreksat'ın insandaki farmakokinetiğine ve güvenilirliğine etki edip etmediği henüz kesin olarak belirlenmemiştir. Farmakokinetik açıdan kadın ve erkek arasında bir fark yoktur. Metotreksat etanercept'in farmakokinetiğini etkilemez. ENBREL®'in metotreksat'ın insandaki farmakokinetiğine ve güvenilirliğine etki edip etmediği henüz kesin olarak belirlenmemiştir. 5.3 Klinik öncesi güvenlilik verileriENBREL® ile yapılan toksikolojik çalışmalarda, doz- limitleyici veya hedef organ toksisitesi saptanmamıştır. ENBREL®,in vitroin vivoçalışmaların sonuçlarına göre genototoksik değildir. Kemirgenlerde nötralize edici antikorların gelişmesi nedeni ile karsinojenite çalışmaları ile standart doğurganlık ve postnatal toksisite değerlendirmeleri yapılamamıştır.2000 mg/kg tek subkutan veya 1000 mg/kg tek intravenöz dozu takiben fare ve sıçanlarda ENBREL® letalite ve dikkate değer toksisite belirtileri indüklememiştir.Cynomolgus maymunlarına haftada iki kez, birbirini takip eden 4 veya 26 hafta, insanlarda önerilen doz olan 25 mg'dan 27 kattan daha fazla EAA-temelli serum konsantrasyonları veren dozda (15 mg/kg) subkutan ENBREL® uygulaması doz- limitleyici veya hedef organ toksisitesi göstermemiştir. 6. FARMASÖTİK ÖZELLİKLER6.1 Yardımcı maddelerin listesiMannitol (E 421)Sukroz Trometamol Trometamin HC1 (pH ayarlamak için) Enjeksiyonluk su % 0,9'luk benzil alkol 6.2 GeçimsizliklerGeçimsizlik çalışmaları yapılmadığından bu ürün başka tıbbi ürünler ile karıştırılarak alınmamalıdır.6.3 Raf ömrüENBREL®'in raf ömrü 2-8 0 C saklama koşullarında 36 aydır.6.4 Saklamaya vönelik özel uyarılarENBREL® 2 - 8 C 'de (buzdolabında) saklanmalıdır. Dondurulmamalıdır.İlaç hazırlandıktan sonra, kullanıma hazır haldeki kimyasal ve fiziksel stabilitesinin, 2 -8°C'de 14 gün süreyle korunduğu gösterilmiştir. Mikrobiyolojik açıdan, ilaç hazırlandıktan sonra, 2 -8°C'de 14 gün süreyle saklanabilir. 6.5 Ambalajın niteliği ve içeriğiAlüminyum mühürlü, ''flip-off' plastik kapaklı ve plastik tıpalı Tip I berrak 4 mİ cam flakon.ENBREL® 4 flakonluk ambalajlarda, 4 adet önceden doldurulmuş İmi bakteriyostatik enjeksiyonluk su içeren şırınga, 8 adet boş plastik şırınga, 20 adet iğne ve 24 adet alkollü ped ile birlikte sunulur. 6.6 Beşeri tıbbi üründen arta kalan maddelerin imhası ve diğer özel önlemlerKullanılmamış olan ürünler ya da atık materyaller Tıbbi Atıkların Kontrolü Yönetmeliği ve Ambalaj ve Ambalaj Atıklarının Kontrolü Yönetmeliklerine uygun olarak imha edilmelidir.ENBREL® 25 mg, 1 mİ bakteriyostatik enjeksiyonluk su ile rekonstitue edilirek subkutan uygulanır. Enjeksiyon için hazırlanan çözelti, berrak, renksiz-açık sarı renkte, tanecik ve uçuşan partiküller içermemelidir. Flakonda beyaz bir köpük kalabilir - bu normaldir. ENBREL® flakonundaki bütün toz 10 dakika içinde çözülmez ise, çözülmeyen flakon kullanılmamalı, bir başka doz paketi ile yeniden başlanmalıdır. Her ENBREL® 25 mg/ml flakonu, aynı hastaya maksimum 2 dozda uygulanacak şekilde kullanılmalıdır. ENBREL® çözeltinin hazırlanması, uygulanması ve hazırlanmış olan ENBREL® flakonunun tekrar-kullanımı ile ilgili ayrıntılı talimatlar, Kullanma Talimatı'nda yer almaktadır. 7. RUHSAT SAHİBİPfizer İlaçları Ltd.Şti.Muallim Naci Cad. No:55 34347 Ortaköy/İstanbul Tel: 0212 310 70 00 Fax: 0212 310 70 58 8. RUHSAT NUMARASI129/569. İLK RUHSAT TARİHİ/RUHSAT YENİLEME TARİHİİlk ruhsat tarihi: 22.12.200910. KÜB'ÜN YENİLENME TARİHİ2013-000334023 1 Çalışmada, plasebo verilen gruba (%2) kıyasla ENBREL® tedavisi uygulanan grupta (%30) anlamlı şekilde daha yüksek oranda hasta 12. haftada PASI 75 yanıtı elde etmiştir (p<0.0001). 24. haftada, ENBREL® tedavi grubundaki hastaların %56'sı PASI 75 yanıtına ulaşırken, plasebo uygulanan hastalarda bu oran %5 olmuştur. 2., 3. ve 4. çalışmaların önemli bulguları aşağıda gösterilmiştir. |
İlaç BilgileriEnbrel 25 Mg Pediyatrik Kullanim İçin Sc Enjektab...Etken Maddesi: Etanercept Atc Kodu: L04AB01 Kullanma talimatı ve kısa ürün bilgileri
Google Reklamları
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
Ana Sayfa | Hakkımızda | İlaçlar | İlaç Ara | İlaç Firmaları | Gizlilik | Bize Ulaşın
Telif Hakkı 2008-2026 © İlaç Prospektüsü. Tüm Hakları Saklıdır.Uyarı: Sitemizde yayınladığımız ilaç bilgileri ile doktora danışmadan kesinlikle ilaç kullanmayınız!
Aksi halde doğabilecek sağlık sorunlarından ilacprospektusu.com sorumlu tutulamaz.