Klavon Bid Fort 400 Mg/57 Mg Oral Süspansiyon Hazırlamak İçin Kuru Toz Kısa Ürün BilgisiEnfeksiyona Karşı Kullanılan (Antienfektif) İlaçlar » Antibakteriyel (Antibiyotik) İlaçlar » Penisilinler » Penisilinli Kombinasyonlar » Amoksisilin ve Klavulanik Asit KISA ÜRÜN BİLGİSİ1. BEŞERİ TIBBİ ÜRÜNÜN ADIKLAVON BID FORT 400 mg/57 mg oral süspansiyon hazırlamak için kuru toz2. KALİTATİF VE KANTİTATİF BİLEŞİMEtkin madde:Her 5 mL'de:Amoksisilin (Amoksisilin trihidrat olarak)...............................400 mg Klavulanik asit (Potasyum klavulanat olarak)............................57 mg Yardımcı maddeler:Her 5 mL'de:Sodyum sitrat dihidrat.................................................8,35 mg Sodyum benzoat (E211)...................................................2,05 mg Mikrokristalin selüloz+Sodyum karboksimetil selüloz............25 mg Granül pudra şekeri (sukroz)...................................................k.m.1 *Miktarı etkin maddelerin potenslerine bağlı olarak değişir. Yardımcı maddeler için bölüm 6.1.' e bakınız. 3. FARMASÖTİK FORMSüspansiyon hazırlamak için kuru toz.Krem-beyaz renkli ahududu kokulu homojen toz karışımı Sulandınldığında krem-beyaz renkli ahududu kokulu homojen bir süspansiyon oluşur. 4. KLİNİK ÖZELLİKLER4.1. Terapötik endikasyonlarKLAVON, lokal resmi antibiyotik reçeteleme kılavuzları ve duyarlılık verilerine uygun olarak kullanılmalıdır.KLAVON BID Fort 400/57 mg Oral Süspansiyon, aşağıdaki sistemlerde amoksisiline dirençli beta laktamaz üreten suşlann neden olduğundan şüphelenilen bakteriyel enfeksiyonların kısa süreli tedavisinde endikedir. Diğer durumlarda sadece amoksisilin düşünülmelidir. Üst Solunum Yolu Enfeksiyonları (KBB dahil): örneğin tekrarlayan tonsillit, sinüzit, otitis media. Dental enfeksiyonlar: örneğin yayılan selülit ile birlikte şiddetli dental abseler. KLAVON'a duyarlılık, coğrafya ve zamana göre değişecektir. Mevcut ise lokal duyarlılık verilerine danışılmalı ve gerektiğinde mikrobiyolojik örnekleme ve duyarlılık testleri yapılmalıdır. Duyarlı organizmaların listesi Farmakolojik Özellikleri/Mikrobiyoloji bölümünde verilmiştir (bkz. bölüm 5.1.). Amoksisiline duyarlı organizmaların KLAVON'a duyarlı beta-laktamaz üreten organizmalar ile birlikte, neden olduğu karma enfeksiyonlar KLAVON BID Fort 400/57mg Oral Süspansiyon ile tedavi edilebilir. Bu enfeksiyonlar beta laktamazlara dirençli başka bir antibiyotiğin ilave edilmesini gerektirmez. 4.2. Pozoloji ve uygulama şekli Pozoloji:Tavsiye edilen genel günlük doz: Hafif ve orta şiddetteki enfeksiyonlarda (tekrarlayan tonsilit gibi üst solunum yolu enfeksiyonları, alt solunum yolu enfeksiyonları, deri ve yumuşak doku enfeksiyonları) 25/3.6mg/kg/gün kullanılır. Daha ciddi enfeksiyonların tedavisi için (otitis media ve sinüzit gibi üst solunum yolu enfeksiyonları, bronkopnömoni gibi alt solunum yolu enfeksiyonları ve idrar yollan enfeksiyonları) 45/6.4 mg/kg/gün kullanılır. 2 yas üzeri çocuklar:
2 avdan 2 yasına kadar olan çocuklar:2 yaşından küçük çocuklarda doz vücut ağırlığına göre ayarlanmalıdır.
Uygulama sıklığı ve süresi:Günde 2 kez alınır. Tedavi süresi, endikasyona uygun olmalı ve tedavi gözden geçirilmeden 14 günü aşmamalıdır.Uygulama şekli:Oral kullanım içindir. Gastrointestinal intolerans potansiyelini en aza indirmek için yemek başlangıcında alınmalıdır. KLAVON'un absorpsiyonu yemek başlangıcında alındığında optimum seviyededir.Süspansiyonun Hazırlanması:Süspansiyonu hazırlamak için önce şişe üzerindeki işaret çizgisinin yarısına kadar kaynatılmış, soğutulmuş içme suyu koyarak iyice çalkalanmalıdır. Homojen dağılım için 5 dakika beklenmelidir. Daha sonra şişe üzerindeki işaret çizgisine kadar kaynatılmış, soğutulmuş içme suyu ekleyerek tekrar çalkalanmalıdır. Hekimin her uygulama için önerdiği miktarda ilaç, şişe ile birlikte bulunan 5 mL'lik ölçü kaşığı kullanılarak hastaya verilir. Sulandırılmamış toz 250C',nin altındaki oda sıcaklığında ve kuru bir yerde saklanmalıdır. Sulandırılan süspansiyon buzdolabı içinde (2-8°C) saklanmalı ve 7-10 gün içinde kullanılmalıdır. Buzluğa koyulmamalıdır. Özel popülasyonlara ilişkin ek bilgiler:Böbrek/Karaciğer yetmezliği:Glomerüler filtrasyon hızı 30 mL/dak. üzerinde olan çocuklarda doz ayarlamasına gerek yoktur. Glomerüler filtrasyon hızı 30 mL/dak. altında olan çocuklarda KLAVON BID Fort 400/57 mg Oral Süspansiyon kullanımı tavsiye edilmemektedir.Böbrek fonksiyonu gelişmemiş olan bebeklerde KLAVON BID Fort 400/57 mg Oral Süspansiyon kullanımı tavsiye edilmemektedir. Karaciğer bozukluğu olan hastalarda doz ayarlaması dikkatli yapılmalı ve düzenli aralıklarla karaciğer fonksiyonları izlenmelidir. Henüz doz ayarlamasına temel teşkil edecek yeterli veri bulunmamaktadır. 4.3. KontrendikasyonlarKLAVON penisilinler ve sefalosporinler gibi beta-laktamlara karşı aşın duyarlılık hikayesi olanlarda kontrendikedir.Geçmişinde KLAVON'a bağlı sarılık/karaciğer fonksiyon bozukluğu hikayesi olan hastalarda kontrendikedir. 4.4. Özel kullanım uyarıları ve önlemleriKLAVON ile tedaviye başlanmadan önce geçmişinde penisilin, sefalosporin ve diğer aleıjenlere karşı aşın duyarlılık hikayesi varlığı dikkatlice sorgulanmalıdır.Penisilin tedavisi alan hastalarda ciddi ve bazen öldürücü aşın duyarlılık (anafılaktoid) reaksiyonları bildirilmiştir. Bu reaksiyonların geçmişinde penisiline karşı aşın duyarlılık hikayesi olan bireylerde görülmesi daha olasıdır (bkz. bölüm 4.3. Kontrendikasyonlar). Amoksisilin kullanımını takiben görülen kızamık benzeri döküntü enfeksiyöz mononükleoz ile ilişkili olabileceğinden eğer enfeksiyöz mononükleoza ilişkin bir şüphe var ise KLAVON tedavisinden kaçınılmalıdır. Uzun süreli kullanım zamanla duyarlı olmayan organizmaların aşın çoğalmasına neden olabilir. KLAVON ve oral antikoagülan kullanan bazı hastalarda seyrek olarak protrombin zamanında uzama (INR değerinde yükselme) bildirilmiştir. Antikoagülanlar ile birlikte reçete edildiğinde uygun şekilde izlenmesi gereklidir. İstenilen antikoagülasyon düzeyini sürdürebilmek için oral antikoagülan dozunda ayarlama yapılması gerekebilir. KLAVON kullanan bazı hastalarda karaciğer fonksiyon testlerinde değişiklikler gözlenmiştir. Bu değişikliklerin klinik önemi bilinmemektedir; ancak karaciğer fonksiyon bozukluğu bulgusu olan hastalarda KLAVON dikkatli kullanılmalıdır. Seyrek olarak bildirilmiş kolestatik sarılık şiddetli olmakla birlikte genellikle geri dönüşümlüdür. Tedavinin kesilmesinden sonra 6 haftaya kadar bulgu ve belirtiler kaybolabilir. Böbrek bozukluğu olan hastalarda KLAVON BID Fort 400/57 mg Oral Süspansiyon kullanımı tavsiye edilmemektedir. Azalmış idrar çıkışı olan hastalarda, özellikle parenteral tedavide çok seyrek olarak kristalüri görülmüştür. Yüksek doz amoksisilin tedavisi sırasında, amoksisilin kristalüri olasılığını azaltmak için uygun miktarda sıvı alınması ve idrar miktarının düzenlenmesi tavsiye edilebilir (bkz. bölüm 4.9. Doz aşımı ve tedavisi). KLAVON'un her dozu 1 mmol (23 mg)'den daha az sodyum ihtiva eder; bu dozda sodyuma bağlı herhangi bir yan etki beklenmemektedir. Bu tıbbi ürün granül pudra şekeri (sukroz) içerdiğinden, nadir kalıtımsal früktoz intoleransı, glikoz-galaktoz malabsorpsiyon veya sükraz-izomaltaz yetmezliği problemi olan hastaların bu ilacı kullanmamaları gerekir. 4.5. Diğer tıbbi ürünler ile etkileşimler ve diğer etkileşim şekilleriProbenesidProbenesid ile birlikte kullanımı önerilmemektedir. Probenesid amoksisilinin renal tübüler sekresyonunu azaltır. Probenesidin KLAVON ile birlikte kullanımı amoksisilinin kan seviyelerinin artışına ve kanda bulunma süresinin uzamasına neden olabilirken, klavulanatı etkilemez. AllopurinolAmoksisilin tedavisi sırasında allopurinol kullanımı alerjik cilt reaksiyonları olasılığını artırabilir. Allopurinol ve KLAVON'un birlikte kullanımına ait veri yoktur. Oral kontraseptiflerDiğer antibiyotiklerde de olduğu gibi KLAVON, barsak florasını etkileyebilir, östrojen reabsorpsiyonunun azalmasına yol açar ve kombine oral kontraseptiflerin etkinliğini azaltır. Oral antikoagülanlarLiteratürde, asenokumarol veya warfarin kullanan ve amoksisilin tedavisi verilen bazı hastaların INR değerinde seyrek olarak yükselme görüldüğü bildirilmiştir. Eğer bu birlikte kullanım gerekli ise, KLAVON kullanımı veya bırakılması sürecinde protrombin zamanı veya INR değeri dikkatle izlenmelidir. MetotreksatPenisilinler metotreksatın atılımını azaltabilir ve bu da toksisitede potansiyel bir artışa neden olur. Özel popülasyonlara ilişkin ek bilgilerVeri bulunmamaktadır.Pediyatrik popülasyon:Yukarıda verilen bilgiler pediyatrik popülasyon için geçerlidir.4.6. Gebelik ve laktasyon Genel tavsiyeGebelik Kategorisi: BÇocuk doğurma potansiyeli bulunan kadınlar/Doğum kontrolü (Kontrasepsiyon)Diğer antibiyotiklerde de olduğu gibi KLAVON, barsak florasını etkileyebilir, östrojen reabsorpsiyonunun azalmasına yol açar ve kombine oral kontraseptiflerin etkililiğini azaltır. Bu nedenle tedavi süresince alternatif, etkili ve güvenilir bir doğum kontrol yöntemi uygulanmalıdır.Gebelik dönemiGebe kadınlara verilirken dikkatli olunmalıdır.Sınırlı sayıda gebelikte maruz kalma olgularına ilişkin veriler, KLAVON'un gebelik üzerinde ya da fetusun/yeni doğan çocuğun sağlığı üzerinde advers etkileri olduğunu göstermemektedir. Bugüne kadar herhangi önemli bir epidemiyolojik veri elde edilmemiştir. Hayvanlar üzerinde yapılan çalışmalar, gebelik / embriyonal / fetal gelişim / doğum ya da doğum sonrası gelişim ile ilgili olarak doğrudan ya da zararlı etkiler olduğunu göstermemektedir (bkz. bölüm 5.3.). Preterm, fetal membran yırtılması (pPROM) olan kadınlarda yapılan bir çalışmada, amoksisilin/klavulanik asidin profilaktik kullanımının yeni doğanlarda nekroze enterokolit riskinin artması ile ilişkili olabileceği bildirilmiştir. Tüm ilaçlarda olduğu gibi, doktor tarafından gerekli görülmedikçe gebelik esnasında özellikle gebeliğin ilk üç ayında kullanılmamalıdır. Laktasyon dönemiKLAVON'un iki etkin maddesi de anne sütüne geçer (klavulanik asitin anne sütü alan sütçocukları üzerindeki etkisi ile ilgili herhangi bir bilgi yoktur). Dolayısıyla anne sütüyle beslenen sütçocuklannda ishal ve mukoz mebranlarda mantar enfeksiyonu olasılığı vardır, bu nedenle emzirmenin kesilmesi gerekebilir. Emzirme döneminde amoksisilin/klavulanik asit sadece tedaviyi uygulayan hekimin fayda/risk değerlendirmesinden sonra kullanılmalıdır.Üreme yeteneği/FertiliteOral ve parenteral yolla verildiği hayvanlar (fare ve sıçanlar) üzerinde yapılan reprodüktif çalışmalarda, amoksisilin/klavulanik asit teratojenik etki göstermemiştir.4.7. Araç ve makine kullanımı üzerindeki etkilerKLAVON'un araç ve makine kullanımı üzerindeki etkileriyle ilgili bir çalışma gerçekleştirilmemiştir. Ancak, hastalar araç ve makine kullanımını etkileyebilecek istenmeyen etkiler (örn. aleıjik reaksiyonlar, sersemlik hali, kon vül siy onlar) oluşabileceği ile ilgili bilgilendirilmelidir (bkz. bölüm 4.8.)*4.8. İstenmeyen etkilerÇok yaygın görülenlerden seyrek görülenlere kadar, istenmeyen etkilerin görülme sıklığını saptamak için geniş çaplı klinik çalışmaların verileri kullanılmıştır. Diğer istenmeyen etkilere (1/10.000'den az görülenler) ait sıklıklar pazarlama sonrası verilere göre saptanmıştır ve gerçek bir sıklıktan çok raporlama oranına dayanmaktadır.Sıklık sınıflandırması aşağıdaki gibidir: Çok yaygın >1/10 Yaygın >1/100 ila <1/10 Yaygın olmayan >1000 ila <1/100 Seyrek >1/10.000 ila <1/1000 Çok seyrek <1/10.000 Bilinmiyor (mevcut verilerden tahmin edilemiyor) Enfeksiyonlar ve enfestasyonlarYaygın: Mukokutanöz kandidiyazisBilinmiyor: Duyarlı olmayan organizmaların aşırı çoğalması Kan ve lenf sistemi hastalıklarıSeyrek: Geri dönüşümlü lökopeni (nötropeni dahil) ve trombositopeni.Çok seyrek: Geri dönüşümlü agranülositoz ve hemolitik anemi. Kanama ve protrombin zamanında uzama (bkz. bölüm 4.4. Özel kullanım uyarıları ve önlemleri) Bağışıklık sistemi hastalıklarıÇok seyrek: Anjiyonörotik ödem, anafilaksi, serum hastalığı benzeri sendrom, aşırı duyarlılık vaskülitiSinir sistemi hastalıklarıYaygın olmayan: Baş dönmesi, baş ağrısıÇok seyrek: Geri dönüşümlü hiperaktivite ve konvülziyonlar. Konvülziyonlar renal fonksiyon bozukluğu olanlarda veya yüksek doz alanlarda görülebilir. Gastrointestinal hastalıklarYaygın: Diyare, bulantı, kusma.Bulantı sıklıkla yüksek oral dozlar ile ilişkilidir. Eğer gastrointestinal reaksiyonlar görülür ise, KLAVON yemek başlangıcında alınarak bunlar azaltılabilir. Yaygın olmayan: Sindirim güçlüğü Çok seyrek: Antibiyotiğe bağlı kolit (psödomembranöz kolit ve hemorajik kolit dahil). Dildeki papillalann belirginleşip siyah renk alması Çocuklarda çok seyrek olarak yüzeysel diş rengi değişikliği bildirilmiştir. Genellikle fırçalama ile giderildiğinden, iyi bir ağız hijyeni ile diş rengi değişimi engellenebilir. Hepato-bilier bozukluklarYaygın olmayan: Beta-laktam sınıfı antibiyotiklerle tedavi edilen hastalarda AST ve/veya ALT değerlerinde orta derecede artış görülmüştür; ancak bu bulguların önemi bilinmemektedir.Çok seyrek: Hepatit ve kolestatik sarılık. Bu olaylar diğer penisilin ve sefalosporinlerle bildirilmiştir. Hepatik olaylar çoğunlukla erkeklerde ve yaşlılarda bildirilmiştir ve uzun süreli tedavi ile ilişkili olabilir. Bu olaylar çocuklarda çok seyrek olarak bildirilmiştir. Bulgu ve belirtiler genellikle tedavi sırasında veya tedavi kesildikten kısa bir süre sonra görülür; ancak bazı durumlarda tedavi kesildikten birkaç hafta sonrasına kadar farkedilmeyebilir. Bunlar genellikle geri dönüşümlüdür. Hepatik olaylar şiddetli olabilir ve son derece seyrek olmakla birlikte bu duruma bağlı ölüm bildirilmiştir. Bunlar hemen hemen her zaman altta yatan ciddi bir hastalığı olan ya da hepatik etki potansiyeline sahip ilaçlan aynı anda alan hastalarda görülmüştür. Deri ve derialtı doku hastalıklarıYaygın olmayan: Deride döküntü, kaşıntı, ürtikerSeyrek: Eritema multiforme Çok seyrek: Stevens-Johnson sendromu, toksik epidermal nekrolizis, bülloz döküntülü dermatit ve akut jeneralize egzantemli püstüloz (AGEP) Eğer herhangi bir aşırı duyarlılık dermatiti görülürse tedavi kesilmelidir. Böbrek ve idrar hastalıklarıSeyrek: HematüriÇok seyrek: İnterstisyel nefrit, kristalüri (bkz. bölüm 4.9. Doz aşımı ve tedavisi). 4.9. Doz aşımı ve tedavisiGastrointestinal semptomlar ve sıvı ile elektrolit dengesinin bozulması açıkça görülebilir. Gastrointestinal semptomlar semptomatik olarak ve su ile elektrolit dengesine dikkat edilerek tedavi edilebilir.Bazı olgularda, böbrek yetmezliğine yol açan amoksisilin kristalürisi görülmüştür (bkz. bölüm 4.4.). KLAVON dolaşımdan hemodiyaliz ile uzaklaştırılabilir. Zehir kontrol merkezinde yapılan 51 pediatrik hastanın katıldığı prospektif bir çalışma amoksisilinin 250 mg/kg'dan daha düşük aşırı dozlarının anlamlı klinik belirtilerle ilişkili olmadığını ve midenin yıkanmasını gerektirmediğini göstermiştir. 5. FARMAKOLOJİK ÖZELLİKLER5.1. Farmakodinamik özelliklerFarmakoterapötik grup: Beta-Iaktamaz inhibitörlerini de içeren penisilin kombinasyonları ATC kodu: J01C R02Etki mekanizması:Amoksisilin, geniş spektrumlu yarısentetik, Gram-pozitif ve Gram-negatif mikroorganizmalara karşı antibakteriyel aktiviteye sahip bir antibiyotiktir. Ancak, amoksisilin beta-laktamazlar tarafından parçalanmaya duyarlı olduğundan tek başına kullanıldığında etki spektrumu beta-laktamaz üreten organizmaları kapsamaz. Klavulanik asit, penisilinlere yapısal olarak benzer bir beta-laktam olup, penisilin ve sefalosporinlere dirençli mikroorganizmalarda sıklıkla karşılaşılan geniş yelpazedeki beta-laktamaz enzimlerini inaktive etme yeteneğine sahiptir. Özellikle direnç gelişiminde etkili olan plazmid aracılı beta-laktamazlara karşı iyi bir aktiviteye sahiptir. Genel olarak kromozomal aracılı tip 1 beta-laktamazlara karşı etkililiği daha düşüktür. Klavulanik asitin KLAVON formülasyonlanndaki varlığı, amoksisilini beta-laktamaz enzimlerince parçalanmaktan korur ve amoksisilinin etki spektrumunu amoksisilin, penisilin ve sefalosporinlere normalde dirençli olan çok sayıda bakteriyi de içine alacak şekilde genişletir. Böylece KLAVON geniş spektrumlu bir antibiyotik ve beta-laktamaz inhibitörünün özelliklerine sahip olur. KLAVON geniş bir yelpazedeki organizmalara karşı bakterisid etkilidir. Birçok antibiyotiğe direncin nedeni olan bakteriyel enzimler, antibiyotiği, patojen üzerinde herhangi bir etki gösteremeden harap ederler. KLAVON'un içindeki klavulanat, beta-laktam enzimlerini bloke ederek savunma mekanizması oluşturur; bu da vücutta hali hazırda elde edilmiş olan konsantrasyonlarda, organizmaların, amoksisilinin hızlı bakterisid etkisine duyarlı olmasını mümkün kılar. Klavulanatın kendisi düşük bir antibakteriyel etkiye sahiptir. Bununla birlikte KLAVON'da olduğu gibi amoksisilin ile birlikte kullanıldığında genel kullanımda ve hastanede geniş kullanım bulan, geniş spektrumlu bir antibiyotik oluşturur. Farmakodinamik etkiler:Organizmalar, amoksisilin/klavulanata karşı in viiroduyarlılıklanna göre aşağıda kategorize edilmektedir.Klinik çalışmalarda amoksisilin-klavulanatın klinik etkililiği kanıtlanmışsa, bu durum bir yıldız işareti (*) ile gösterilmektedir. Beta-laktamaz üretmeyen organizmalar (f) işareti ile tanımlanmıştır. Bir izolatın amoksisiline karşı duyarlı olması durumunda, amoksisilin/klavulanata karşı da duyarlı olduğu düşünülebilir. Genellikle duvarlı türlerAerobik Gram-pozitif mikroorganizmalarBacillius arıthracis Enterococcus faecalis Listeria monocytogenes Nocardia ast er o ide sStaphylococcus aureus(metisiline duyarlı)*Streptococcus agalactiae*fStreptococcus pyogenes*ve diğer beta hemolitik streptokoklar*Streptococcus viridansgrubuStaphylococcus saprophyticus(metisiline duyarlı)Koagülaz negatif stafılokoklar (metisiline duyarlı) Aerobik Gram-neeatif mikroorganizmalarBordetelia pertussis Haemophiius infiuenzae1*Neisseria gonorrhoeae Pasteurella multocida Vibrio choieraDiğerBorreiia burgdorferi_Leptospira ictterohaemorrhagiae Treponema pallidumAnaerobik Gram-pozitif mikroorganizmalarCiostridiumPeptococcus niger Peptostreptococcus magnus Peptostreptococcus mi eros PeptostreptococcustürleriAnaerobik Gram-negatif mikroorganizmalarBacteroides fragilis BacteroidesCapnocytophagaE i kene ila corrodens Fusobacterium nucleatum FusobacteriumPorphyromonastürleriPrevotellatürleri_Edinilmiş direncin bir sorun oluşturabileceği türlerAerobik Gram-negatif mikroorganizmalarEscherichia coli*Klebsiella oxytoca Klebsiella pneumoniae*KlebsiellaProteus mirabilis Proteus vulgaris ProteusSalmonellaShigellatürleriAerobik Gram-pozitif mikroorganizmalarCorynebacteriumEnterococcus faecium4* 'Viridans grup streptococcusf____Dolası ucrcöj dirençli organizmalarAerobik Gram-negatif mikroorganizmalarAcinetobactertürleriCitrobacter freundiiEnterobactertürleriHafnia alveiLegionella pneumophilaMorganella morganiiProvidenciatürleriPseudomonastürleriSerratiatürleriStenotrophomonas maltophilia Yersinia enteroliticaDiğer mikroorganizmalarChlamydophila pneumoniae Chlamydophila psittaci ChlamydiaCoxiella burnetii Mycoplasma pneumoniaeMycoplasmatürleri_Edinilmiş direnç mekanizmasının yokluğunda orta düzeyde doğal duyarlılık 3 Metisiline dirençli tüm stafılokoklar amoksisilin/klavulanik asite dirençlidir. 1 Bazı AB ülkelerinde duyarlılığı azalmış suşlar, %10'dan daha yüksek bir sıklıkta bildirilmiştir. 2 # ( Penisiline dirençli olan Streptococcus pneumoniaeamoksisilin/klavulanik asitin busunumuyla tedavi edilmemelidir (bkz. bölüm 4.2. ve 4.4.)._5.2. Farmakokinetik özellikler Genel özellikler:Emilim:KLAVON'un her iki bileşeni, hem amoksisilin hem de klavulanik asit, fizyolojik pH'da sulu çözeltilerde tamamen dissosiye olurlar. İki bileşik de oral uygulama sonrası hızla ve iyi absorbe olur. KLAVON'un iki bileşeninin farmakokinetikleri birbirine benzer. Oral uygulamadan 1 saat sonra serum doruk seviyelerine ulaşırlar. KLAVON'un dozu ikiye katlandığında ulaşılan serum seviyeleri de iki katına çıkar. Klavulanat ve amoksisilinin serum proteinlerine bağlanma oranlan düşüktür. Her ikisi de %70 oranında serumda serbest halde bulunur. Yapılan bir çalışmanın sonuçlarına göre, sağlıklı erişkinlerde aç kamına amoksisilin/klavulanik asit 875/125 mg tabletin günde iki kere uygulanması sonucunda aşağıdaki sonuçlar elde edilmiştir.
Dağılım:Toplam plazma klavulanik asitinin %25ve toplam plazma amoksisilinin %18 kadarı proteine bağlanır. Görünürdeki dağılım hacmi amoksi sil inde 0,3-0.4 L/kg ve klavulanik asitte 0.2 L/kg dolayındadır.İntravenöz uygulamadan sonra safra kesesinde; abdominal dokularda; deri, yağ, kas dokularında; sinoviyal ve peritoneal sıvılarda; safra ve iltihapta hem amoksisilin hem de klavulanik asit bulunmuştur. Amoksisilinin beyin omurilik sıvısına dağılımı yeterli değildir. Hayvan çalışmalarında, bileşenlerden herhangi biri için ilaçtan kaynaklanan materyallerle önemli doku tutulumuna ilişkin kanıt yoktur. Penisilinlerin çoğu gibi amoksisilin de anne sütünde saptanabilir. Anne sütünde eser miktarda klavulanik asit de saptanabilmektedir (bkz. bölüm 4.6.). Hem amoksisilin hem de klavulanik asitin plasenta bariyerini geçtiği gösterilmiştir (bkz. bölüm 4.6.). Bivotransformasyon:Amoksisilin kısmen idrarla, başlangıç dozunun yaklaşık %10-25'i oranında inaktif penisiloik asit şeklinde atılır. Klavulanik asit insanda geniş oranda 2,5-dihidro-4-(2-hidroksietil)-5-okso-lH-pirol-3-karboksilik asit ve l-amino-4-hidroksi-bütan-2-ona metabolize olarak, idrar ve feçes içinde ve karbondioksit şeklinde hava ile atılır. Eliminasvon:Amoksisilinin başlıca eliminasyon yolu böbreklerdir, buna karşılık klavulanik asit hem renal hem de renal olmayan mekanizmalarla atılır. Amoksisilin/klavulanik asitin ortalama eliminasyon yanlanma Ömrü yaklaşık bir saattir ve ortalama total klerens sağlıklı kişilerde yaklaşık 25 L/saattir. 250 mg/125 mg ya da 500 mg/125 mg'lık tek bir amoksisilin/klavulanik asit tabletinin uygulanmasından sonraki ilk 6 saatte amoksisilinin yaklaşık %60-70'i ve klavulanik asitin yaklaşık %40-65'i idrarla değişikliğe uğramadan atılır. Çeşitli çalışmalarda, 24 saatlik bir dönemde amoksisilinin idrarla atılım miktannın %50-85 ve klavulanik asitin %27-60 arasında olduğu bulunmuştur. Klavulanik asitte, ilacın en büyük miktarı uygulamadan sonraki ilk 2 saatte atılmaktadır. Eşzamanlı probenesid kullanılması, amoksisilin atılmasını geciktirmekle birlikte klavulanik asitin böbreklerden atılmasını geciktirmez (bkz. bölüm 4.5.). Hastalardaki karakteristik özelliklerBöbrek yetmezliği:Böbrek işlevinin azalmasıyla doğru orantılı olarak amoksisilin/klavulanik asitin total serum klerensi de azalır. İlaç klerensindeki azalma, amoksisilinin daha büyük bir bölümünün böbrek yoluyla atılması nedeniyle, amoksisilinde klavulanik asitten daha belirgindir. Bu yüzden, böbrek yetmezliğinde dozlar, amoksisilinin fazla birikmesini önlerken, yeterli klavulanik asit düzeylerinin sürdürülmesini sağlamalıdır (bkz. bölüm 4.2.). Karaciğer yetmezliği:Karaciğer yetmezliği bulunan hastalarda doz dikkatle belirlenmeli ve karaciğer işlevleri düzenli aralıklarla izlenmelidir. Yas:Amoksisilinin eliminasyon yarılanma ömrü 3 aylıktan 2 yaşma kadar olan çocuklarda ve daha büyük çocuklarda aynıdır. Yaşlı hastalarda böbrek işlevlerinde azalma olasılığı daha fazla olduğundan, doz seçiminde dikkatli olunmalıdır ve böbrek işlevinin izlenmesi yararlı olabilir. Cinsiyet:Sağlıklı erkek ve kadınlara oral yoldan amoksisilin/klavulanik asit uygulanmasından sonra cinsiyetin amoksisilin ya da klavulanik asitin farmakokinetikleri üzerinde önemli bir etkisi görülmemiştir. 5.3. Klinik öncesi güvenlilik verileriKlinik öncesi veriler, farmakoloji, genotoksisite ve üreme toksisitesi güvenliliğine yönelik çalışmalar temelinde insanlar açısından özel bir tehlike ortaya koymamıştır.Köpeklerde amoksisilin/klavulanik asitle yapılan tekrarlanan doz toksisitesi çalışmalarında, gastrik tahriş, kusma ve dilde renk bozukluğu görülmüştür. Amoksisilin/klavulanik asit ya da diğer bileşenlerle karsinojenisite çalışmaları yapılmamıştır. 6. FARMASÖTİK ÖZELLİKLER6.1. Yardımcı maddelerin listesiSusuz sitrik asit (pH ayarlayıcı)Sodyum sitrat dihidrat (pH ayarlayıcı) Sodyum benzoat (E211) Mikrokristalin selüloz + Sodyum karboksimetil selüloz Ksantan zamkı Kolloidal susuz silika Silikon dioksit Ahududu esansı Granül pudra şekeri (Sukroz) 6.2. GeçimsizliklerBilinen bir geçimsizliği bulunmamaktadır.6.3. Raf ömrü36 ay6.4. Saklamaya yönelik özel tedbirlerSulandırılmadan önce 25°C'nin altındaki oda sıcaklığında ve kuru bir yerde saklayınız.Süspansiyon hazırlandıktan sonra, 35 - 70 mL süspansiyon 7 gün, 100 mL ve 140 mL süspansiyon 10 gün buzdolabında (2-8°C) saklanabilir. Dondurulmamalıdır. Nem çekeceğinden, şişelerin ağzı kapalı tutulmalıdır. 6.5. Ambalajın niteliği ve içeriğiKarton kutuda, HDPE kapak ile kapatılmış, üzerinde 35 mL, 70 mL, 100 mi veya 140 mL seviye çizgisi bulunan amber renkli Tip III cam şişelerde. 2,5 5 mL işaretli PE kaşık ile birlikte sunulmaktadır.6.6. Beşeri tıbbi üründen arta kalan maddelerin imhası ve diğer özel ÖnlemlerKullanılmamış olan ürünler ya da atık materyaller "Tıbbi Atıkların Kontrolü Yönetmeliğr1 ve Ambalaj ve Ambalaj Atıklarının Kontrolü Yönetmeliğine uygun olarak imha edilmelidir.KLAVON süspansiyonun hazırlanması:KLAVON toz halindedir, bu yüzden ilk önce sulandırmak gerekir. KLAVON'u sulandırmak için aşağıdaki talimatları takip ediniz: Tüm toz serbestçe akana kadar şişeye hafifçe vurunuz. 1. KLAVON BID Fort 400/57 mg Oral süspansiyonu hazırlamak için önce şişe üzerindeki işaret çizgisinin yarısına kadar su ekleyiniz ve tozu süspansiyon haline getirmek için şişeyi iyice çalkalayınız (Süspansiyon hazırlamak İçin Önceden kaynatılmış ve soğutulmuş su tercih edilmelidir.) 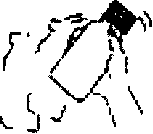 2. İlk sulandırılışta tam bir dağılma sağlamak için 5 dakika dinlendiriniz.
2. İlk sulandırılışta tam bir dağılma sağlamak için 5 dakika dinlendiriniz.3. Kalan suyu (1/2) şişe üzerindeki işaretli çizgiye kadar doldurunuz ve şişeyi yeniden çalkalayınız. 4. Süspansiyon 5 mL'lik ölçü kaşığı ile uygulanabilir. 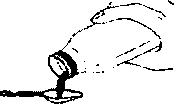 Her dozdan önce şişeyi iyice çalkalayınız.
Her dozdan önce şişeyi iyice çalkalayınız.Kullanım sonrası şişeyi hemen ve sıkıca kapatınız. 7. RUHSAT SAHİBİHÜSNÜ ARSAN İLAÇLARI A.Ş.34440 Beyoğlu - İSTANBUL 8. RUHSAT NUMARASI2014/2809. RUHSAT TARİHİ/RUHSAT YENİLEME TARİHİİlk ruhsat tarihi: 07.04.2014 Ruhsat yenileme tarihi:10. KÜB'ÜN YENİLENME TARİHİ1Alt Solunum Yolu Enfeksiyonları: örneğin kronik bronşitin akut alevlenmeleri, lobar ve bronkopnömoni. Üriner Sistem Enfeksiyonları: örneğin sistit, üretrit, piyelonefrit. Deri ve Yumuşak Doku Enfeksiyonları: örneğin selülit, hayvan ısırmaları. |
İlaç BilgileriKlavon Bid Fort 400 Mg/57 Mg Oral Süspansiyon Hazırlamak İçin Kuru TozEtken Maddesi: Amoksisilin Trihidrat + Potasyum Klavulanat Atc Kodu: J01CR02 Kullanma talimatı ve kısa ürün bilgileri
Google Reklamları
|
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
Ana Sayfa | Hakkımızda | İlaçlar | İlaç Ara | İlaç Firmaları | Gizlilik | Bize Ulaşın
Telif Hakkı 2008-2026 © İlaç Prospektüsü. Tüm Hakları Saklıdır.Uyarı: Sitemizde yayınladığımız ilaç bilgileri ile doktora danışmadan kesinlikle ilaç kullanmayınız!
Aksi halde doğabilecek sağlık sorunlarından ilacprospektusu.com sorumlu tutulamaz.