Poena 4/400 Mcg İnhalasyon İçin Toz İçeren Kapsül Kısa Ürün BilgisiKISA ÜRÜN BİLGİSİ1. BEŞERİ TIBBİ ÜRÜNÜN ADIPOENA 4/400 mcg inhalasyon için toz içeren kapsül2. KALİTATİF VE KANTİTATİF BİLEŞİM Etkin maddeler:Karmoterol hidroklorür*4,4 mcg 400 mcgBudesonid*4 mcg Karmoterol'e eşdeğerYardımcı madde:Laktoz12,5956 mgYardımcı maddeler için 6.1'e bakınız.3. FARMASÖTİK FORMİnhalasyon için toz içeren kapsülKapak; şeffaf, Gövde; natural transparan kapsül içinde, beyaz toz4. KLİNİK ÖZELLİKLER4.1. Terapötik endikasyonlarAstım semptomlarının düzeltilmesi ve kontrol altına alınması amacıyla kullanılır. Astım hastalığının basamaklı tedavisinde 3. basamaktan itibaren verilir.Orta ve ağır KOAH olgularında semptomları ve atak sıklığını azaltır.4.2. Pozoloji ve uygulama şekli Pozoloji/uygulama sıklığı ve süresi:POENA yalnızca oral inhalasyon yoluyla kullanılmak içindir.Astım ve KOAH hastaları için önerilen doz, günde bir kez bir veya iki kapsül içeriğinin inhale edilmesidir.Eğer daha önceden kullanılan POENA dozu astım kontrolünün sağlanmasında yetersiz olursa, tedavi rejimi yeniden değerlendirilmeli ve ek tedavi seçenekleri, örneğin, POENA tedavi dozunun yeniden gözden geçirilmesi, ilave inhale kortikosteroid dozunun eklenmesi veya oral kortikosteroidlere başlanılması göz önünde bulundurulmalıdır.İnhalasyon her gün, aynı saatte inhalasyon cihazı kullanılarak yapılmalıdır.POENA'nın dozu hastanın kişisel ihtiyacına göre ayarlanmalı ve terapötik amaca ulaşılmasını sağlayan en düşük dozda uygulanmalıdır.Hastanın cihazı doğru kullandığından emin olunmalıdır.POENA, astım ve KOAH ataklarının akut semptomlarını hafifletmek için kullanılmamalıdır. Akut atak durumunda kısa etkili bir beta2Uygulama şekli:POENA, sadece oral inhalasyon içindir.POENA inhalasyon kapsülleri yalnızca kutudan çıkan cihaz ile tatbik edilmelidir.İnhalasyon cihazı yoluyla nefes alındığında ilaç akciğerlere ulaşır. Bu nedenle, cihazın ağız parçası aracılığıyla derin ve güçlü nefes alınması önemlidir.Olası bir kandida enfeksiyonu riskini azaltmak için her POENA kapsül uygulamasından sonra ağzın su ile iyice çalkalanması ve tükürülmesi önerilmektedir. Ayrıca ağzın su ile çalkalanması boğaz irritasyonunu engellemeye ve sistemik etki riskinin azaltılmasına muhtemelen yardımcı olabilir.İlacın akciğerlerdeki hedef bölgelere ulaşabilmesi ve uygun şekilde kullanıldığından emin olunması için doktor veya bir başka sağlık personeli kullanım talimatına uygun olarak cihazın nasıl kullanılacağını hastalara öğretmeli ve göstermeli, kapsüllerin sadece cihaz aracılığıyla inhalasyon yolu ile uygulanması gerektiği ve yutulmaması konusunda hastayı uyarmalıdır.Hastaların jelatin kapsülün parçalanab ileceğini ve küçük jelatin parçalarının inhalasyondan sonra ağız veya boğaz bölgesine ulaşabileceğini bilmesi önemlidir. Hastaya jelatinin zararsız olduğu, ağızda yumuşayacağı ve yutulabildiği söylenmelidir. Kapsülü bir defadan fazla delmemek suretiyle parçalanma olasılığı asgari düzeye indirilebilir.Kapsüller blister ambalajından kullanımdan hemen önce çıkarılmalıdır.Kullanıma ilişkin detaylı bilgi, kullanma talimatında mevcuttur. İnhalasyon cihazının doğru kullanımı için aşağıda verilen kuralları dikkatle izleyiniz.inhalasyon cihazı kullanım talimatları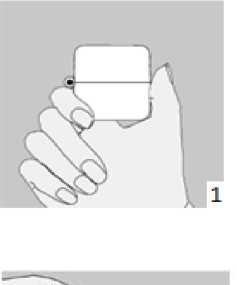 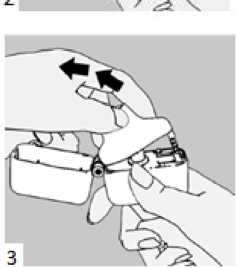
1., 2. ve 3. Toz başlığını yukarı doğru çekerek açınız. Daha sonra ağızlık parçasını açınız.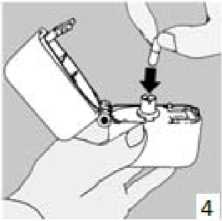
4. Blister ambalajından bir POENA inhalasyon için toz içeren kapsülü çıkarınız (kullanımdan hemen önce çıkarınız) ve şekilde gösterildiği gibi merkezi hazneye yerleştiriniz. Kapsülün hazneye hangi yönde yerleştirildiği önemli değildir.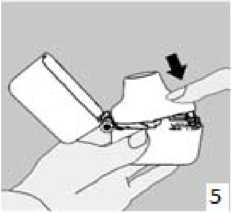
5. Ağızlık parçasını bir klik sesi duyuncaya değin sıkıca kapatınız. Toz başlığını açık bırakınız.
6. ve 7. İnhalasyon cihazını ağızlık parçası yukarıda olacak şekilde tutunuz ve kapağı bastırarak kapatınız.Böylece kapsülde delikler açılacak ve nefes aldığınızda ilacın salıverilmesini sağlayacaktır.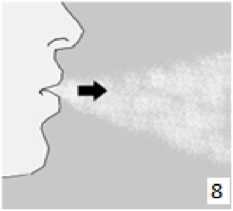
8. Nefesinizi tam olarak veriniz.Önemli: Hiçbir zaman ağızlık parçasına doğru nefes vermeyiniz.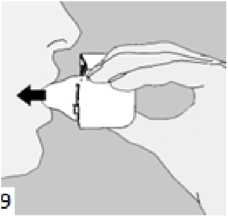
9. İnhalasyon cihazının ağzını açıp, cihazı ağzınıza kadar kaldırınız ve dudaklarınızı ağızlık parçasının çevresinde sıkıca kapayınız. Başınızı dik bir şekilde tutarak, yavaş ve derin bir nefes alınız; nefes alma hızınızı, kapsülün titreştiğini algılayacak şekilde ayarlayınız. Akciğerleriniz doluncaya kadar nefes alınız; nefesinizi sizi zorlamayacak bir süreyle tutunuz ve bu esnada inhalasyon cihazını ağzınızdan çıkarınız. Şimdi normal nefes alıp vermeye başlayabilirsiniz.Basamak 8 ve 9'u bir kez daha tekrarlayınız, bu kapsülün tamamen boşalmasını sağlayacaktır.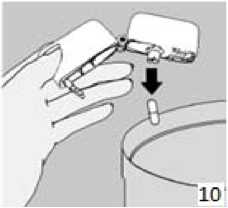
10. Ağızlık parçasını yeniden açınız. Cihazı çevirerek kullanılmış kapsülü çıkarınız ve atınız. Sonrasında ağzınızı su ile çalkalayınız. Ağızlık parçasını ve toz başlığını kapatınız ve inhalasyon cihazınızı yerine kaldırınız.İnhalasyon cihazının temizleme işlemiİnhalasyon cihazını ayda bir kez yıkayınız. Kapağı ve ağızlığı açınız. Cihazı sıcak su ile yıkayarak içerisindeki tozlardan arındırınız. Cihaz içerisindeki suyu boşaltarak kağıt bez üzerinde kapak, ağızlık ve gövde kısımları açık kalacak şekilde kurumaya bırakınız. Kurumaya bırakılan cihaz kullanılmaya hazırdır. Eğer ihtiyaç varsa ağızlık kısmının dış yüzeyi ıslak olmayan nemli bir bezle silinebilir.Özel popülasyonlara ilişkin ek bilgiler:Böbrek yetmezliği:POENA'nın içeriğindeki karmoterolün böbrek yetmezliği olan hastalarda kullanımına yönelik veri mevcut değildir. POENA'nın içeriğindeki budesonid böbrek yetmezliği olan hastalarda doz ayarlaması gerektirmemektedir.Karaciğer yetmezliği:POENA'nın içeriğindeki karmoterolün karaciğer yetmezliği olan hastalarda kullanımına yönelik veri mevcut değildir. Karaciğer fonksiyonlarının azalması, kortikosteroidlerin atılımını etkileyebilir. Bununla birlikte intravenöz yoldan uygulanan budesonidin plazma klerensi, sirozlu hastalarda ve sağlıklı kişilerde benzerdir. Karaciğer fonksiyonlarının azaldığı durumlarda, ilk geçiş metabolizmasındaki azalma nedeniyle, oral yoldan alınan budesonidin sistemik yararlanımı artar. İnhalasyon yoluyla alınan budesonid için herhangi bir veri bulunmadığından, bunun POENA ile tedavi için klinik anlamı bilinmemektedir; ancak plazma düzeylerinin yükselmesi ve dolayısıyla sistemik advers etkiler açısından riskin artması beklenebilir.Pediyatrik popülasyon:Pediyatrik popülasyonda (18 yaş altı) karmoterol kullanımına yönelik veri mevcut değildir. Bu nedenle POENA'nın pediyatrik popülasyonda kullanılmaması önerilir.Geriyatrik popülasyon:POENA'nın içeriğindeki karmoterolün geriyatrik popülasyonda kullanımına yönelik veri mevcut değildir. POENA'nın içeriğindeki budesonid için yaşlılarda özel doz gereksinimleri yoktur.inhalasyon yoluyla idame glukokortikosteroid kullanan hastalardaİnsanlarda yapılan klinik araştırmalar, aynı miktardaki kuru toz inhaler budesonid dozunun ölçülü doz inhalerden daha etkili olduğunu göstermiştir. Bu nedenle ölçülü doz inhaler ile budesonid tedavisi uygulanan hastalarda, kuru toz inhaler ile uygulanan budesonid tedavisine geçilirken, hastalar stabil ise dozun yarı yarıya azaltılması mümkündür. Bu durum, hastaların başka inhalasyon glukokortikosteroid tedavisinden kuru toz inhaler ile uygulanan budesonid tedavisine geçmeleri durumunda da, transferden öncesinde de aynı doz verilmesi lüzumlu ise de geçerlidir.Oral yoldan glukokortikosteroid kullanan hastalardaPOENA, astım kontrolünde azalmaya yol açmaksızın ya da daha iyi bir kontrol sağlayarak, oral yoldan kullanılan glukokortikosteroid tedavisinin kesilmesini ya da dozunun büyük oranda azaltılmasını sağlayabilir.Oral steroidlerden POENA'ya geçiş başlatıldığında, hasta nispeten stabil bir fazda olmalıdır. Başlangıçta POENA, hastanın alışkın olduğu oral glukokortikosteroid idame dozu ile birlikte aynı zamanda yaklaşık 10 gün boyunca kullanılmalıdır. Bu uygulamayı takiben, oral doz örneğin her ay 2,5 miligram prednizolon ya da eşdeğeri düzeyinde azaltılarak yavaş yavaş düşürülebileceği en düşük doza indirilmelidir. Oral dozun yavaş bir oranda kesilmesi önerilir. Pek çok hastada oral glukokortikosteroidin yerini POENA'nın tamamen alması mümkündür.Oral dozun kesilmesi sırasında idameye ya da akciğer fonksiyonlarında gelişmeye rağmen bazı hastalar sistemik kortikosteroid eksikliği semptomu yaşayabilirler örn. eklem ve/veya adale ağrıları, halsizlik ve depresyon gibi. Böyle hastalara POENA ile devam etmeleri öğütlenmeli, ancak adrenal yetersizliği oluşması bakımından dikkatle izlenmelidir. Adrenal yetersizlik oluşursa, sistemik kortikosteroid dozu geçici olarak yükseltilmeli ve oral dozun kesilmesi daha da yavaşlatılmalıdır. Stres ya da şiddetli astım nöbetinde, POENA'ya geçiş dönemindeki hastalara sistemik kortikosteroid tedavisi gerekebilmektedir.POENA reçete edilmiş oral glukokortikosteroid kullanan KOAH'lı hastalarda oral doz azaltılırsa astımlı hastalar için belirtilen tavsiyeler verilmelidir.4.3. KontrendikasyonlarPOENA, karmoterole, budesonide ve/veya içeriğindeki yardımcı madde laktoza karşı aşırı duyarlılığı olan hastalarda kontrendikedir.4.4. Özel kullanım uyarıları ve önlemleriKarmoterol hidroklorürKarmoterol; astımlı hastalarda tek başına monoterapi olarak kullanılmamalıdır.POENA'nın içeriğindeki karmoterol, uzun etkili beta2POENA başka bir uzun etkili beta2POENA, astımda ilk tedavi seçeneği olarak kullanılmamalıdır. POENA, hafif astım hastalığının başlangıç tedavisi olarak önerilmez.Uzun etkili beta agonistler astım semptom kontrolünü sağlayan en kısa süre boyunca kullanılmalı ve astım kontrolüne ulaşıldığında eğer mümkünse kullanımları durdurulmalıdır. Sonrasında hastaların kontrol edici bir tedaviyle idamesi sağlanmalıdır.Antienflamatuvar tedavi:Astım hastalarını tedavi ederken uzun etkili bir betaagonist (LABA) olan karmoterol, tek başına bir inhale kortikosteroid ile yeterli düzeyde kontrol edilemeyen ya da hastalığının şiddeti bir LABA ve inhale kortikosteroidin her ikisi ile tedavinin başlatılmasını kesin olarak gerektiren hastalarda bir inhale kortikosteroide ilave tedavi olarak kullanılmalıdır.Günlük POENA dozu, önerilen maksimum dozu aşmamalıdır.Astım semptomları kontrol altına alındıktan sonra, karmoterol dozunun kademeli olarak azaltılması düşünülmelidir. Tedavinin azaltılması sırasında hastalar yakından izlenmeli ve en düşük dozda karmoterol dozu içeren etkin POENA dozu kullanılmalıdır.Hastalığın kötüleşmesi:POENA, akut bronkospazm epizodlarının tedavisi için (yani kurtarma tedavisi olarak) endike değildir. POENA tedavisi sırasında KOAH'ta kötüleşme görülürse hastanın ve KOAH tedavi rejiminin tekrar değerlendirilmesi gerekir.Astım atakları:Semptomlar devam ettiği takdirde, doktorlar böyle bir gelişmenin genellikle altta yatan durumun kötüleştiğini gösteriyor olması nedeniyle kullanılan astım tedavisini yeniden değerlendirmelidir.Astım alevlenmesi esnasında POENA tedavisine başlanmamalı ya da doz arttırılmamalıdır. Hastalar alevlenme döneminde ise ya da önemli ölçüde veya akut olarak kötüye giden astım şikayetleri varsa, uzun etkili beta agonistlerle tedaviye başlanmamalıdır.POENA, akut astım semptomlarının rahatlatılması için kullanılmamalıdır. Akut ataklarda kısa etkili bir beta2Kardiyovasküler etkiler ve eşlik eden şartlar:POENA kullanan hastalarda aşağıdaki durumların varlığında, özellikle doz sınırları konusunda olmak üzere, özel dikkat ve denetleme gereklidir: İskemik kalp hastalığı, kardiyak aritmiler (özellikle üçüncü derece atriyoventriküler blok), şiddetli kardiyak dekompansasyon, idiyopatik subvalvüler aortik stenoz, şiddetli hipertansiyon, anevrizma, feokromositoma, hipertrofik obstrüktif kardiyomiyopati, tirotoksikoz, QT aralığında bilinen veya şüphe edilen uzama (QTc >0.44 saniye; Bkz. Bölüm 4.5). Bu tür etkiler olursa tedavinin kesilmesi gerekebilir.Daha önceden kardiyak problemleri bulunan ve teofilin ile karmoterolü bir arada kullanan hastalarda dikkatli olunmalıdır.Hiperglisemi:POENA beta2 uyarıcı olan karmoterol içermektedir. Beta2 uyarıcıların hiperglisemik etkileri nedeniyle, diyabetik hastalarda POENA tedavisi başlatıldığında kan glukoz değerlerinin izlenmesi tavsiye edilir.Hipokalemi:POENA, beta2Paradoksal bronkospazm:Diğer inhalasyon tedavilerinde olduğu gibi yaşamı tehdit edebilen paradoksal bronkospazm ihtimali akılda tutulmalıdır. Böyle bir durum görüldüğünde, POENA tedavisi derhal kesilmeli ve alternatif tedavi başlatılmalıdır.Karmoterol gibi uzun etkili beta-agonistler kullanılırken, özellikle astım ile ilgili advers olaylar bakımından, POENA başlandıktan sonra ilk üç ay hastalar yakından takip edilmelidir.BudesonidAktif veya sessiz seyreden akciğer tüberkülozlu hastalarda ve solunum yollarında fungal ya da viral enfeksiyonu olan hastalarda özellikle dikkatli olunmalıdır.Akut astım alevlenmelerinde oral yoldan kortikosteroid verilmesi ve/veya bir enfeksiyon varsa antibiyotik ile kısa süreli ek tedavi uygulanması gerekebilir. Hastaya akut astım semptomlarını hafifletmek için kurtarıcı ilaç olarak kısa etkili inhalasyon yoluyla alınan bir bronkodilatör kullanması önerilmelidir. Kısa etkili bronkodilatör tedavisi etkisiz kalıyorsa, ya da normalden daha fazla inhalasyon gerekiyorsa, bir sağlık kurumuna başvurulmalıdır. Bu tür durumlarda, anti-enflamatuvar tedavinin arttırılması ya da oral yoldan glukokortikosteroid kürüne başlanması gerekli olabilir.Yüksek dozlarda, özellikle de önerilen dozlardan daha yüksek dozlarda inhalasyon yoluyla kullanılan kortikosteroidlerle uzun süreli tedavi, klinik olarak anlamlı adrenal baskılanmaya neden olabilir. Stres durumlarında veya elektif operasyon uygulanan dönemlerde ilave sistemik kortikosteroid tedavisi düşünülmelidir. Bu hastalar, ihtiyaçlarının belirtildiği steroid uyarı kartını yanlarında taşımaları konusunda bilgilendirilmelidir. Sistemik steroid takviyesi ya da POENA ile tedavi birden kesilmemelidir.İnhalasyon yoluyla uygulanan diğer tedavilerde olduğu gibi, ilaç alındıktan sonra hırıltılı soluk alıp vermekte ani bir artış ile birlikte paradoksal bronkospazm görülebilir. Şiddetli bir reaksiyon ortaya çıkarsa, tedavi yeniden değerlendirilmeli ve gerekirse başka bir tedavi başlatılmalıdır.Budesonid KOAH'ta tek başına monoterapi olarak kullanılmamalıdır. KOAH alevlenmelerinde sorumlu hekim tarafından belirlenen ek tedavi uygulanmalıdır.Geçmişte oral steroidlere bağımlı olan hastalarda, uzun süreli sistemik steroid tedavisinin sonucu olarak adrenal fonsiyonlarda yetmezlik etkileri görülebilir. Oral steroid tedavisinin kesilmesinden sonra iyileşme oldukça uzun sürebilir; dolayısıyla oral steroidlere bağımlı olan ve budesonide geçiş yapılan hastalarda adrenal fonsiyonlarda yetmezlik riski uzun bir süre devam edebilir. Bu tür durumlarda Hipotalamik-pitüiter-adrenal (HPA) ekseni fonksiyonları düzenli olarak izlenmelidir.Oral yoldan kullanılan glukokortikosteroid dozu azaltılırken, bazı hastalarda solunum fonksiyonları korunsa ya da iyileşse dahi, kas ve eklem ağrısı gibi spesifik olmayan rahatsızlık duyguları ortaya çıkabilir. Aksini gösteren klinik belirtiler olmadığı sürece, hastalar oral steroid tedavisinin kesilmesi sırasında POENA tedavisine devam etmeye teşvik edilmelidir. Bu tür ender durumlarda, yorgunluk, baş ağrısı, bulantı ve kusma başlarsa genel bir glukokortikosteroid etkisi yetmezliğinden kuşkulanılmalıdır. Bu vakalarda bazen oral yoldan kullanılan glukokortikosteroid dozunun geçici olarak yükseltilmesi gerekli olabilir.Oral tedaviden POENA tedavisine geçilmesi sırasında, rinit, egzama ve kas ve eklem ağrısı gibi alerjik ya da artiritik semptomların görülmesine neden olabilen genellikle daha düşük sistemik steroid etkiler görülür. Bu tür durumlar için spesifik tedavi başlatılmalıdır.Karaciğer fonksiyonlarının azalması, kortikosteroidlerin atılımını etkileyebilir. Bununla birlikte, intravenöz yoldan uygulanan budesonidin plazma klerensi, sirozlu hastalarda ve sağlıklı kişilerde benzerdir. Karaciğer fonksiyonlarının azaldığı durumlarda, ilk geçiş metabolizmasındaki azalma nedeniyle, oral yoldan alınan budesonidin sistemik yararlanımı artar. İnhalasyon yoluyla alınan budesonid için herhangi bir veri bulunmadığından, bunun POENA ile tedavi için klinik anlamı bilinmemektedir; ancak plazma düzeylerinin yükselmesi ve dolayısıyla sistemik advers etkiler açısından riskin artması beklenebilir.İn vivoçalışmalarda ketokonazol ve itrakonazolün (CYP3A4 aktivitesinin karaciğer ve bağırsak mukozasındaki inhibitörleri, ayrıca Bkz. Bölüm 4.5) oral yolla verilmesi ile budesonidin sistemik maruziyetinde artış olabileceği gözlenmiştir. Bu durumun klinik olarak önemi kısa süreli (1-2 haftalık) tedavide sınırlıdır, ancak uzun süreli tedavide göz önüne alınmalıdır. Ketokonazol ve itrakonazol ya da diğer potent CYP3A4 inhibitörleri ile eşzamanlı tedaviden kaçınılmalıdır (Bkz. Bölüm 4.5). Bu mümkün değilse, etkileşen ilaçların uygulamaları arasında mümkün olan en uzun zaman aralığı bırakılmalıdır. Budesonid dozunun azaltılması da düşünülmelidir.
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
MedDRA sistem organ sınıfı |
istenmeyen etkiler |
Sıklık | |
Karmoterol |
Budesonid | ||
Enfeksiyonlarveenfestasyonlar |
Nazofarenjit, üst solunum yolu enfeksiyonu, sinüzit |
Bilinmiyor |
|
Orofarenkste candida enfeksiyonu |
|
Yaygın | |
Bağışıklıksistemihastalıkları |
Aşırı duyarlılık (ürtiker, anjiyonörotik ödem) |
Bilinmiyor |
Seyrek |
Aşırı duyarlılık (hipotansiyon, kaşıntı, egzantem dahil) |
Bilinmiyor |
| |
Deri döküntüsü, kontakt dermatit, bronkospazm ve anafilaktik reaksiyon dahil ani ve geç aşırı duyarlılık reaksiyonları |
|
Seyrek | |
Endokrinhastalıklari |
Adrenal baskılanma gibi sistemikkortikosteroidlerin bulgu ve belirtileri |
|
Seyrek |
Metabolizma ve beslenme hastalıkları |
Hipokalemi, diyabet ve hiperglisemi |
Bilinmiyor |
|
Psikiyatrikhastalıklar |
Sinirlilik |
Bilinmiyor |
Seyrek |
Ajitasyon, anksiyete, uykusuzluk, baş dönmesi, tat alma duyusu bozuklukları |
Bilinmiyor |
| |
Psikomotor hiperaktivite, uyku bozuklukları, huzursuzluk, depresyon, davranış bozuklukları |
|
Seyrek | |
Sinir sistemi hastalıkları |
Baş ağrısı, titreme, parestezi, vertigo |
Bilinmiyor |
|
Gözhastalıkları |
Katarakt, glokom |
Bilinmiyor |
|
Kardiyakhastalıklar |
Palpitasyonlar, iskemik kalp hastalığı, taşikardi, elektrokardiyogramda QT uzaması, anjina pektoris, atriyal fibrilasyon gibi kardiyak aritmiler, ventriküler ekstrasistol, taşiaritmi |
Bilinmiyor |
|
|
|
Boğaz irritasyonu |
Bilinmiyor |
Yaygın |
|
|
Paradoksal bronkospazm dahil bronkospazm, |
Bilinmiyor |
Seyrek |
Solunum, göğüs bozuklukları ve mediastinal hastalıklar |
Orofaringeal ağrı, rinore, solunum yolu konjesyonu, akut astım alevlenmesi, dispne |
Bilinmiyor |
|
|
|
Öksürük |
Bilinmiyor |
Yaygın |
|
|
Ses boğuklaşması |
|
Yaygın |
|
|
Disfoni |
|
Seyrek |
Gastrointestina l hastalıklar |
Ağız kuruluğu, bulantı |
Bilinmiyor |
|
Deri ve deri altı |
Deri döküntüsü |
Bilinmiyor |
|
dokuhastalıkları |
Deride morarma |
|
Seyrek |
Kas-iskelet bozuklukları, bağ doku ve kemik hastalıkları |
Kas spazmı, miyalji, kas-iskelet ağrısı, kas krampları |
Bilinmiyor |
|
Genelbozukluklar veuygulamabölgesineilişkinhastalıklar |
Periferik ödem, göğüs ağrısı, kalple bağlantılı olmayan göğüs ağrısı |
Bilinmiyor |
|
Araştırmalar |
Kan basıncında artış (hipertansiyon dahil) |
Bilinmiyor |
|
Orofarenkste candida enfeksiyonu riskindeki artış ilacın birikmesinden kaynaklanmaktadır. Hastaya her doz uygulamasından sonra ağzını su ile yıkamasının tavsiye edilmesi riski minimum düzeye indirecektir.
İnhalasyon yoluyla kullanılan ilaçlar, etki mekanizması bilinmemekle birlikte, nadiren bronkospazma yol açabilir.
İnhalasyon yoluyla kullanılan kortikosteroidlerde, özellikle de uzun süreler için reçetelenen yüksek dozlarda, sistemik etkiler ortaya çıkabilir. Bu etkilerin görülme olasılığı oral kortikosteroidlerdekine oranla çok daha azdır. Oluşabilecek sistemik etkiler arasında, adrenal baskılanma, çocuklarda ve adolesanlarde büyüme geriliği, kemik mineral yoğunluğunda azalma, katarakt ve glokom yer almaktadır. Etki muhtemelen doza, maruziyet süresine, eşzamanlı ve daha önceki steroid maruziyetine ve bireysel duyarlılığa bağlıdır.
4.9. Doz aşımı ve tedavisi
Karmoterol hidroklorür Belirtiler:
Karmoterolün aşırı dozuna bağlı olarak beta-adrenerjik uyarıcıların tipik etkilerinin görülmesi beklenir: bulantı, kusma, baş ağrısı, tremor, sedasyon, palpitasyonlar, taşikardi, ventriküler aritmiler, metabolik asidoz, hipokalemi, hiperglisemi, hipertansiyon.
Tedavi:
Destekleyici ve semptomatik tedavi uygulanır. Ciddi vakalarda hastalar hastaneye yatırılmalıdır.
Kardiyoselektif beta-blokörlerin kullanılması düşünülebilir, fakat beta-adrenerjik blokör kullanımı bronkospazma neden olabileceğinden bu tedavi yalnızca doktor gözetimi altında ve çok dikkatli uygulanmalıdır.
Budesonid
Çok yüksek dozlarda olsa bile, budesonid akut doz aşımının klinik açıdan sorun oluşturması beklenmez.
5. FARMAKOLOJİK ÖZELLİKLER
5.1. Farmakodinamik özellikler
Farmakoterapötik grup: Obstrüktif Solunum Yolu Hastalıklarında Kullanılan İlaçlar (Selektif Beta--Adrenoreseptör Agonisti [Karmoterol], Glukokortikosteroidler [Budesonid])
ATC kodu:
Karmoterol R03AC
Budesonid R03BA02
Karmoterol hidroklorür
Karmoterol çok uzun etkili yeni bir betaagonisttir. Çok uzun etkili betaagonistlerinin inhale kullanımı (örneğin karmoterol) bronkokonstriksiyonda yer alan mast hücrelerinin solunum yolu lümenine yakın olmasından dolayı oral kullanımına tercih edilmektedir. Karmoterol, beta-reseptörü için oldukça güçlü ve seçici bir beta2in vitrohem dein vivodeneysel koşullarda hızlı etki başlangıcı ve uzun süreli etki göstermektedir. Hayvanlarla gerçekleştirilen çalışmalarda karmoterolün formoterolden ve salmeterolden daha güçlü bir etkiye sahip olduğu ve kalp kasına göre bronşiyal kaslara 100 kat daha fazla seçicilik gösterdiği belirtilmiştir.
Budesonid
Budesonid, güçlü lokal anti-enflamatuvar etkileri olan bir glukokortikosteroiddir.
Topikal antienflamatuvar etki
Glukokortikosteroidlerin astım ve KOAH tedavisindeki etki mekanizmaları tam olarak aydınlatılamamıştır. Enflamatuvar mediyatörlerin salgılanmasının ve sitokinlerce yönlendirilen immün yanıtların inhibisyonları gibi anti-enflamatuvar etkiler, muhtemelen önemlidir. Glukokortikosteroid reseptör afinitelerine göre, budesonidin etki gücü, prednizolondan yaklaşık 15 kat fazladır.
Astımlı hastalarda inhalasyon ve oral yoldan kullanılan budesonidin karşılaştırıldığı bir klinik çalışmada, plaseboya göre inhalasyon yoluyla kullanılan budesonidin istatistiksel açıdan anlamlı bir şekilde etkili olduğu, oral yoldan kullanılan budesonid ve plasebo arasında ise anlamlı bir farkın olmadığı görülmüştür. Alışılmış dozlarda inhalasyon yoluyla kullanılan budesonidin etkisi, solunum yolları üzerindeki doğrudan etkisi ile açıklanabilir.
Budesonid hayvanlar ve insanlar üzerinde yapılan provokasyon çalışmalarında, antianafilaktik ve antienflamatuvar etki göstermiş, hem erken hem de geç alerjik reaksiyonlarda bronşiyal obstrüksiyonu azaltmıştır.
Astımın alevlenmesi
Günde bir veya iki kez uygulanan inhale budesonidin hem çocuk hem de erişkinlerde astımın alevlenmesini etkili olarak önlediği gösterilmiştir.
Egzersizle ortaya çıkan astım
İnhalasyon yoluyla günde bir veya iki kez uygulanan budesonid tedavisi, egzersizle ortaya çıkan bronkokonstrüksiyonun önlenmesinde etkili olmuştur.
Solunum yolu reaktivitesi
Budesonidin aşırı duyarlılığı olan hastalarda hem doğrudan hem de dolaylı provokasyonlarda solunum yolları reaktivitesini azalttığı gösterilmiştir.
Plazma kortizol düzeyi üzerine etkisi
Sağlıklı gönüllülerde kuru toz inhaleri aracılığıyla uygulanan budesonid plazma ve idrar kortizolü üzerinde doz ile orantılı bir etki göstermiştir. Kuru toz inhaleri yoluyla önerilen dozlarda kullanılan budesonid, ACTH testlerine göre, adrenal fonksiyonlarını 10 mg prednizolondan belirgin olarak daha az etkiler.
Büyüme
Uzun süreli çalışmalar, inhale budesonid ile tedavi edilen çocuk ve ergenlerde yetişkin hedef boyuna sonuçta ulaşıldığını göstermiştir. Ancak büyümede başlangıçta küçük ancak çabuk geçen bir büyüme azalması (yaklaşık 1 cm) gözlenmiştir. Bu genellikle tedavinin ilk yılında ortaya çıkmaktadır.
5.2. Farmakokinetik özellikler Genel özellikler
Emilim:
Karmoterol hidroklorür
Karmoterolün tekrarlayan tedavi dozlarının ardından nonlineer birikiminin ihmal edilebilir olduğuna dair kanıt sağlanmıştır. İlginç şekilde hidrofloroalkan püskürtücü kullanılarak karmoterolün akciğerde birikimi nominal dozunun %41'ine ulaşılabilir. Hidrofloroalkan basınçlı dozimetre inhaler aerosolün partikül boyutunun küçük olması nedeniyle (0.8 p,m) karmoterolün akciğerde birikiminde sağlıklı bireyler, astımlı ve KOAH hastaları arasında anlamlı farklılıklar olduğu gösterilmemiştir.
Budesonid
Kuru toz inhaler yoluyla uygulanan budesonid dozunun yaklaşık %25-30'u akciğerlere ulaşır, ki bu ölçülü doz inhalatörün yaklaşık iki katıdır.
Oral yoldan tek doz halinde 800 mg budesonid inhale edildikten sonra en yüksek plazma konsantrasyonu yaklaşık 4 nmol/L'dir ve bu değere inhalasyondan yaklaşık 30 dakika sonra ulaşılır. Kuru toz inhaleri ile uygulanan budesonidin sistemik yararlanımı, ölçülü dozun %38'i kadardır ve bunun 1/6'sı yutulan ilaçtan kaynaklanmaktadır.
Dağılım:
Karmoterol hidroklorür Veri mevcut değildir.
Budesonid
Budesonidin dağılım hacmi yaklaşık 3 L/kg'dır. Plazma proteinlerine ortalama % 85-90 oranında bağlanır.
Biyotransformasyon:
Karmoterol hidroklorür
Gerçekleştirilen çalışmalarda karmoterolün başlıca biyotransformasyon yolunun glukuronidasyon olduğu gösterilmiştir. Çalışmalar hem insan hem de sıçan akciğer ve karaciğer mikrozomlarında karmoterolün glukuronide dönüşümünün gerçekleştiğini ancak esas glukuronidasyonun karaciğerde meydana geldiğini göstermiştir. Mikrozom örneklerinde ve A549 hücrelerinde karmoterolün 2 ayrı glukuronidi saptanmıştır: fenolik ve benzilik glukuronid. İnsan karaciğer ve akciğer dokusunda bu detoksifikasyon yolunun ana metaboliti fenolik glukuroniddir. Farklı rekombinant insan UGT süperzomları ile karmoterolün in vitro inkübasyonu tüm esas UGT enzimlerinin karmoterolün glukuronide dönüşümünü sağlayabildiğini ve tüm izoformların benzilik glukuronid ile karşılaştırıldığında karmoterolü başlıca fenolik glukuronide metabolize ettiğini göstermiştir. UGT1A1, 1A6 ve 1A9 bu metabolik yolda en büyük role sahiptir.
Budesonid
Budesonid, karaciğerden ilk geçiş sırasında yüksek oranda (~%90) metabolize edilerek glukokortikosteroid aktivitesi düşük metabolitlerine dönüşür. En önemli metabolitleri 6B-hidroksibudesonid ve 16a-hidroksiprednizolonun glukokortikosteroid aktivitesi, budesonidin aktivitesinin %1'inden azdır. Budesonid metabolizması temel olarak sitokrom p450'nin alt sınıfı olan CYP3A4 aracılığıyla olur.
Eliminasyon:
Karmoterol hidroklorür Veri mevcut değildir.
Budesonid
Budesonidin metabolitleri, aynen ya da konjuge edilerek, temel olarak böbrekler aracılığıyla atılır. İdrarda değişime uğramamış halde budesonid bulunmaz. Budesonidin sistemik klerensi yüksektir (dakikada yaklaşık 1.2 L) ve intravenöz yoldan uygulandığında plazma yarılanma süresi ortalama 2-3 saattir.
Doğrusallık/Doğrusal olmayan durum:
Karmoterol hidroklorür
Sağlıklı gönüllüler ve astımlı hastalardan elde edilen bulgular karmoterol farmakokinetiğinin doz ile orantılı olduğunu göstermiştir.
Budesonid
Klinik dozlarda budesonid kinetiği, doz ile orantısaldır.
Hastalardaki karakteristik özellikler
Karmoterol hidroklorür Veri mevcut değildir.
BudesonidBöbrek yetmezliği:
Böbrek yetmezliği olan hastalarda doz ayarlaması gerekmemektedir.
Karaciğer yetmezliği:
Karaciğer fonksiyonlarının azalması, kortikosteroidlerin atılımını etkileyebilir. Bununla birlikte, intravenöz yoldan uygulanan budesonidin plazma klerensi, sirozlu hastalarda ve sağlıklı kişilerde benzerdir. Karaciğer fonksiyonlarının azaldığı durumlarda, ilk geçiş metabolizmasındaki azalma nedeniyle, oral yoldan alınan budesonidin sistemik yararlanımı artar. İnhalasyon yoluyla alınan budesonid için herhangi bir veri bulunmadığından, bunun POENA ile tedavi için klinik anlamı bilinmemektedir; ancak plazma düzeylerinin yükselmesi ve dolayısıyla sistemik advers etkiler açısından riskin artması beklenebilir.
5.3. Klinik öncesi güvenlilik verileri
Karmoterol hidroklorür Veri mevcut değildir.
Budesonid
Budesonidin akut toksisitesi düşüktür ve incelenen referans glukokortikosteroidlerle (beklometazon dipropiyonat, fluoksinolon asetonid) aynı büyüklükte ve tiptedir.
Subakut ve kronik toksisite çalışmalarının sonuçları, vücut ağırlığındaki artışın azalması ve lenfoid dokular ile adrenal korteks atrofisi gibi budesonidin sistemik etkilerinin, diğer glukokortikosteroidlerin uygulanmasında gözlenenlerden daha hafif ya da benzer düzeyde olduğunu göstermektedir.
Altı test sisteminde incelenen budesonid mutajenik ya da klastojenik etki göstermemiştir.
Yapılan bir karsinojenik etki araştırmasında erkek sıçanlarda gözlenen beyin glioma insidans artışı, tekrarlanan çalışmada doğrulanamamıştır. Tekrarlanan bu çalışmada, glioma insidansı, aktif tedavi (budesonid, prednizolon, triamsinolon asetonid) gruplarında ve kontrol gruplarında aynı bulunmuştur.
İlk karsinojenite çalışmasında erkek sıçanlarda gözlenen karaciğer değişiklikleri (primer hepatoselüler tümörler), yinelenen çalışmada da, budesonid yanında referans glukokortikosteroidlerin uygulandığı gruplarda da görülmüştür. Bu etkilerin bir reseptör etkisine bağlı olması ve bir sınıf etkisini göstermesi kuvvetle muhtemeldir.
Mevcut klinik deneyimlere göre, budesonid ya da diğer glukokortikosteroidlerin insanlarda beyin gliomalarını ya da primer hepatoselüler tümörleri uyardığına dair hiçbir işaret yoktur.
Üreme ile ilgili hayvanlar üzerinde yürütülen çalışmalarda, budesonid gibi kortikosteroidlerin malformasyonları (yarık damak, iskelet malformasyonları) indüklediği gösterilmiştir. Bununla birlikte, önerilen dozlarda hayvanlara ait bu deneysel bulgular insanlar için anlamlı görünmemektedir.
Hayvan çalışmaları ile ayrıca, teratojenik doz aralığının altındaki maruziy etlerde aşırı prenatal glukokortikosteroidlerin rahim içi büyüme geriliği, erişkinlerde kardiyovasküler hastalık ve
glukokortikosteroid reseptör yoğunluğunda, nörotransmitter döngüsünde ve davranışında kalıcı değişiklik riskini arttırdığı saptanmıştır.
6. FARMASÖTİK ÖZELLİKLER
6.1. Yardımcı maddelerin listesi
Laktoz
6.2. Geçimsizlikler
Bilinen geçimsizliği yoktur.
6.3. Raf ömrü
24 ay
6.4. Saklamaya yönelik özel tedbirler
25°C'nin altındaki oda sıcaklığında ve kuru yerde saklayınız.
6.5. Ambalajın niteliği ve içeriği
POENA 4/400 mcg inhalasyon için toz içeren 60 ve 120 kapsül, PVC/PVDC/Alü blister ambalajlarda inhalasyon cihazı ve kullanma talimatı ile birlikte karton kutuda sunulmaktadır.
6.6. Beşeri tıbbi üründen arta kalan maddelerin imhası ve diğer özel önlemler
Kullanılmamış olan ürünler ya da atık materyaller Tıbbi Atıkların Kontrolü Yönetmeliği Ambalaj ve Ambalaj Atıklarının Kontrolü Yönetmeliklerine uygun olarak imha edilmelidir.
7. RUHSAT SAHİBİ
Neutec İnhaler İlaç San. Ve Tic. A.Ş.
Sakarya 1. Organize Sanayi Bölgesi 2. Yol No:3 Arifiye / Sakarya Telefon numarası: 0850 201 23 23 Faks numarası: 0212 482 24 78 e-mail:[email protected]
8. RUHSAT NUMARASI (LARI)
255/70
9. İLK RUHSAT TARİHİ/ RUHSAT YENİLEME TARİHİ
İlk ruhsat tarihi: 31.12.2013 Ruhsat yenileme tarihi:
10. KÜB'ÜN YENİLENME TARİHİ
26
8. RUHSAT NUMARASI (LARI)
255/70
9. İLK RUHSAT TARİHİ/ RUHSAT YENİLEME TARİHİ
İlk ruhsat tarihi: 31.12.2013 Ruhsat yenileme tarihi:
10. KÜB'ÜN YENİLENME TARİHİ
26İlaç Bilgileri
Poena 4/400 Mcg İnhalasyon İçin Toz İçeren Kapsül
Etken Maddesi: Karmoterol Hidroklorür/budesonid
Kullanma talimatı ve kısa ürün bilgileri
Google Reklamları
Ana Sayfa | Hakkımızda | İlaçlar | İlaç Ara | İlaç Firmaları | Gizlilik | Bize Ulaşın
Telif Hakkı 2008-2026 © İlaç Prospektüsü. Tüm Hakları Saklıdır.Uyarı: Sitemizde yayınladığımız ilaç bilgileri ile doktora danışmadan kesinlikle ilaç kullanmayınız!
Aksi halde doğabilecek sağlık sorunlarından ilacprospektusu.com sorumlu tutulamaz.