Kas İskelet Sistemi » Kas Gevşeticiler » Periferik Etkili Kas Gevşeticiler » Diğer Kuaterner Amonyumlar » Atrakuryum KISA URUN BILGISI
1. BEŞERİ TIBBİ ÜRÜNÜN ADI
NEUCURİUM 25mg/2.5tnL İ.V. İnfijzyon ve Enjeksiyon İçin Çözelti İçeren Ampul
2. KALİTATİF VE KANTİTATİF BİLEŞİM Etkin Madde:
Bir ampulde;
Atrakuryum besilat 25 mg (10 mg/ml)
Yardımcı Madde(ler):
Yardımcı maddeler için ö.l'e bakınız.
3. FARMASÖTİK FORM
Ampul
Berrak cam ampul içinde renksiz, steril çözelti. pH=3.0-3.65
4. KLİNİK ÖZELLİKLER
4.1. Terapötik endikasyonlar
NEUCURİUM, cerrahi girişimlerde veya kontrollü ventilasyon sırasında trakeal entUbasyonu sağlamak ve iskelet kaslarını gevşetmek ve yoğun bakım ünitelerindeki (YBÜ) hastalarda mekanik ventilasyonu kolaylaştırmak amacıyla genel anesteziye ek olarak uygulanır. Son derece selekti f, kompetitif veya non-depoİarizan bİr nöromüsküler blokördür.
4.2. Pozoloji ve uygulama şekli
İzleme:TÜM NÖROMÜSKÜLER BLOKÖRLERDE OLDUĞU GİBİ, NEUCURİUM UYGULAMASI SIRASINDA BİREYSEL DOZ İHTİYACINI BELİRLEMEK İÇİN NÖROMÜSKÜLER FONKSİYONUN İZLENMESİ ÖNERİLİR.
Pozoloji/uygulama sıklığı ve süresi:
Erişkinler;
Enjeksiyon şeklinde; Erişkinlerde doz (gereken tam blok süresine bağlı olarak) 0.3-0.6 mg/kg'dır ve 15-35 dakika süre ile yeterli gevşeme sağlar. Endotrakeal entübasyon genellikle 0.5-0.6 mg/kg'lık dozun i.v, enjeksiyonundan sonraki 90 saniye içinde gerçekleştirilebilir. Tam blok süresi, gerektikçe 0.1-0.2 mg/kg'iık ek dozların uygulanması ile uzatılabilir. Artarda uygulanan ek dozlar birikmeye neden olmaz. Tam blok sonunda kendiliğinden düzelme, tetanik cevabin normal nöromüsküler fonksiyonun %95'ine ulaşması ölçü olarak alındığında, yaklaşık 35 dakikada gerçekleşir. Atrakuryum'un oluşturduğu nöromüsküler blok, öncesinde ya da birlikte atropin uygulanan, standart dozlarda neostigmin ve edrofonyum gibi ^ antikolinesteraz ilaçlarla, hiçbir rekürarizasyon belirtisi olmaksızın hızla geri döndürülebilir.
İnfüzyon şeklinde; NEUCURİUM, uzun süren cerrahi girişimlerde, bolus olarak uygulanan 0.3-0.6 mg/kg'lık ilk dozdan sonra nöromüsküler blokun sürdürülmesi için G.3-0.6 mg/kg/saat hızında sürekli inflizyon şeklinde uygulanabilir. NEUCURİUM önerilen infüzyon hızında kardiyopulmoner bypass ameliyatlarında infüzyon şeklinde uygulanabilir. Vücut ısısının, oluşturulan hipotermi ile, 25-26°C'ye düşürülmesi atrakuryum inaktivasyonunu yavaşlatır, bu nedenle düşük ısılarda normal inflizyon hızının yaklaşık yarısı ile tam nöromüsküler blok sürdürülebilir. NEUCURİUM aşağıdaki İnfüzyon solüsyonları ile aşağıda belirtilen sürelerde geçimlidir:
İnfüzyon solüsyonu Stabilite süresi
Sodyum klorür intravenöz infüzyon BP (%0,9 a/h) 24 saat
Glukoz intravenöz inflizyon BP (%5 a/h) 8 saat
Ringer solüsyonu US? 8 saat
Sodyum klorür (%0.18 a/h) ve glukoz (%4 a/h) intravenöz inflizyon BP 8 saat
Bileşik sodyum laktat intravenöz İnfüzyon BP (Hartmann solüsyonu) 4 saat
0.5 mg/ml ve üzerinde atrakuryum besilat konsantrasyonları verecek şekilde bu solüsyonlarla
seyrekilme yapıldığında elde edilen solüsyonlar gün ışığında ve 30C'ye kadar olan ısı derecelerinde belirtilen sürelerde stabil kalır.
Uygulama şekli;
NEUCURİUM i.v. enjeksiyon yoluyla uygulanır. Nöromusküler bloğun sürdürülmesi için sUrekli NEUCURİUM infüzyonu uygulanmalıdır.
NEUCURİUM kesinlikle intramüsküler uygulanmamalıdır.
BU İLAÇ SADECE HASTANEDE VE BİR ANESTEZİ UZMANI DENETİMİNDE KULLANILMALIDIR.
Özel popülasyonlara ilişkin ek bilgiler:
Böbrek/Karaciğer yetmezliği:
NEUCURİUM son dönem yetmezliği de içeren her düzeyde böbrek ve karaciğer yetersizliği olan hastalarda standart dozlarda uygulanabilir.
Pediyatrik popülasyon:
I aydan daha büyük çocuklar için gerekli doz, vücut ağırlığına göre hesaplanan erişkin dozları ile aynıdır. I aydan daha küçük yenidoğanlarda ilacın güvenliliği ile ilgili veri yetersizdir. Bu nedenle kullanımı önerilmez.
Geriyatrik popülasyon:
NEUCURİUM, yaşlı hastalarda standart dozlarda uygulanabilir. Ancak başlangıç dozunun yavaş uygulanması ve doz aralığının düşük bölümünden seçilmesi önerilir.
9 Diğer:
Kardiyovasküler hastalığı olan hastalar: Klinik olarak önemli kardiyovasküler hastalığı olan hastalarda NEUCURİUM'un başlangıç dozu 60 saniyeden daha uzun bir sürede uygulanmalıdır.
Yoğun bakım ünitesindeki (YBÜ) hastalar: 0.3-0.6 mg/kg'lık NEUCURİUM'un tercih edilen başlangıç bolus dozundan sonra, NEUCURİUM nöromUsküler bloku devam ettirmek için 11-13 mikrogram/kg/dak (0.65-0.78 mg/kg/saat) hızlarında sUrekli infüzyon şeklinde uygulanabilir, fakat doz gereksinmelerinde hastalar arasında geniş değişkenlikler olabilir. Doz gereksinmeleri zaman ile değişebilir. Bazı hastalarda 4.5 mikrogram/kg/dak (0.27 mg/kg/saat) kadar az veya 29.5 mikrogram/kg/dak (1.77 mg/kg/saat) kadar yüksek infüzyon hızlarına gerek olabilir. YBÜ hastalarına Atrakuryum'un infüzyon olarak uygulanmasından sonra
nöromUsküler bloktan kendiliğinden düzelme hızı, uygulama süresinden bağımsızdır. Spontan düzelmeden dörtlü uyarı oranı >0.75'e (train-of-four ratio, dörtlü uyarıda dördüncü seğirmenin yüksekliğinin birincisine oranı) dönüşün yaklaşık 60 dakika içinde gerçekleşmesi beklenir. Klinik çalışmalarda 32-108 dakika arasında gözlenmiştir.
4.3. Kontrendikasyonlar
NEUCURİUM, atrakuryum, sisatrakuryum ya da benzensülfonik aside aşırı duyarlı olduğu bilinen hastalara uygulanmamalıdır.
4.4. Özel kullanım uyarılan ve önlemleri
BÜTÜN NÖROMÜSKÜLER BLOKÖRLER GİBİ, NEUCURİUM DA DİĞER İSKELET KASLARI İLE BİRLİKTE SOLUNUM KASLARINDA FELÇ OLUŞTURUR, ANCAK ŞUUR ÜZERİNE HERHANGİ BİR ETKİSİ YOKTUR. NEUCURİUM SADECE UYGUN GENEL ANESTEZİ İLE BİRLİKTE VE DENEYİMLİ BİR ANESTEZİST TARAFINDAN VEYA ONUN YAKIN DENETİMİ ALTINDA, ENDOTRAKEAL ENTÜBASYON VE YAPAY SOLUNUM İÇİN UYGUN OLANAKLARIN MEVCUDİYETİNDE UYGULANMALIDIR.
Diğer nöromüsküler blokörlerde olduğu gibi, duyarlı kişilerde NEUCURİUM uygulaması sırasında histamin açığa çıkma ihtimali vardır. Histamin etkilerine artmış duyarlılık hikayesi olan hastalarda NEUCURİUM uygulaması sırasında, dikkatli olunmalıdır. NEUCURİUM'un önerilen dozlarda anlamlı bir vagal veya gangliyon blokör etkisi yoktur. Bu nedenle, NEUCURİUM önerilen dozlarda kalp hızı üzerine klinik olarak anlamlı bir etki göstermez. Nöromüsküler blokörler arasında çapraz hipersensitivite bulunur. Diğer NMB ilaçlara duyarlı hastalara verilmemelidir. Ameliyat sırasındaki vagal stimülasyon veya birçok anestezik ilacın neden olduğu bradikardiyi önlemez. Miyastenia gravis, diğer nöromüsküler hastalıklar ve ciddi elektrolit dengesizliği olan hastalarda diğer non-depolarizan nöromüsküler blokörler gibi NEUCURİUM'a da artmış duyarlılık görülebilir. NEUCURİUM, arteriyel kan basıncı düşmelerine çok hassas olan hastalarda (öm. hipovolemik hastalarda), 60 saniyeden daha uzun bir sürede uygulanmalıdır. NEUCURİUM yüksek pH'da inaktive olduğu için, tiyopenton veya herhangi bir alkali ajan ile birlikte aynı şırıngada karıştırılmamalıdır. NEUCURİUM uygulaması için küçük bir ven seçilmişse, uygulama sonrası serum fizyolojik ile ven yıkanmalıdır. Diğer anestezik ilaçların da NEUCURİUM'la aynı iğne ya da kanülden uygulanması halinde her ilacın yeterli hacimde serum fizyolojik ile yıkanması çok önemlidir.
NEUCURİUM hipotoniktir ve kan transfuzyonunun infilzyon yolundan uygulanmamalıdır. Malign hipertermiye duyarlı hayvanlardaki (domuz) çalışmalar ve malign hipertermiye duyarlı hastalarda yapılan klinik çalışmalarda, Atrakuryum|un bu sendromun oluşmasını kolaylaştırıcı etki göstermediği saptanmıştır. Diğer non-depolarizan nöromüsküler blokörlerde olduğu gibi yanıklı hastalarda direnç gelişebilir. Bu hastalarda yanıktan beri geçen süre ve yanığın büyüklüğüne göre doz artırılması gerekebilir.
Voğufj bakım ünitesi (YBÜ) hastalan: Atrakuryumun metaboliti olan lodanozin, yüksek dozlarda laboratuar hayvanlarına uygulandığında geçici hipotansiyon ve bazı türlerde serebral eksitatör etkilerle ilişkili bulunmuştur. Atrakuryum alan YBÜ hastalarında nöbetler görülmesine rağmen bunun lodanozin ile nedensel ilişkisi saptanmamıştır (Bkz. İstenmeyen etkiler).
4.5. Diğer tıbbi ürünler ile etkileşimler ve diğer etkileşim şekilleri
Halotan, izofluran ve enfluran gibi inhalasyon anesteziklerinin birlikte uygulanması ile NEUCURİUM'un oluşturduğu nöromüsküler blok uzayabilir.
Diğer non-depolarizan nöromüsküler blokörlerle olduğu gibi, NEUCURİUM ile birlikte uygulandıklarında aşağıdaki İlaçlar non-depolarizan nöromüsküler blokun derinliğini ve/veya süresini artırabilirler:
Antibiyotikler (aminoglikozidler, polimİksinler, spektinomisin, tetrasiklinler, linkomisin ve klindamisin)
Antiaritmik ilaçlar (propranolol, kalsiyum-antagonistleri, lidokain, prokainamid ve kinidin)
Diüretikler (ftırosemid ve muhtemelen mannitol, tiazid diüretikleri ve asetazolamid)
Magnezyum sültat
Ketamin
Lityum tuzları
Gangliyon blokörleri (trimetafan, heksametonyum)
Nadiren bazı ilaçlar latent miyastenia gravisi maskeleyebilir, kötüleştirebilir veya miyastenik sendromu indUkleyebilir. Böyle bir gelişme, NEUCURİUM'a artmış bir duyarlılığa neden olabilir. Bu tür ilaçlar şunlardır: Çeşitli antibiyotikler, beta-blokörler (propranolol, oksprenolol), antiaritmik ilaçlar (prokainamid, kin id in), antiromatizmal ilaçlar (klorokin, D-penisilamin), trimetafan, klorpromazin, steroidler, fenitoin ve lityum. Kronik antikonvülsan tedavi uygulanan hastalarda non-depolarizan nÖromUsküler blok başlaması için geçen süre uzayabilir ve blok süresi kısalabilir.
NEUCURİUM ile birlikte diğer non-depolarizan nöromüsküler blokörlerin uygulanması halinde, uygulanan NEUCURİUM'un eşdeğer etkili toplam dozlarından beklenenden çok daha fazla nöromüsküler blokaj oluşabilir. Farklı ilaç kombinasyonlarında görülebilecek sinerjik etkiler değişkendir.
Süksametonyum klorür gibi depolarizan kas gevşeticiler, atrakuryum gibi nondepolarizan ajanların nöromüsküler blok etki sürelerini uzatmak amacıyla uygulanmamalıdır, çünkü bu antikolinesteraz ilaçlarla geri döndürülmesi zor olabilen, uzamış ve kompleks bir bloka yol açabilir.
Özel popülasyonlara Hişkin ek bilgiler
Veri bulunmamaktadır.
Pediyatrik popülasyon:
Veri bulunmamaktadır.
4.6. Gebelik ve laktasyon Genel tavsiye
Gebelik kategorisi C.
Çocuk doğurma potansiyeli bulunan kadınlar/Doğum kontrolü (Kontrasepsiyon)
NEUCURİUM'un doğum kontrol yöntemleri üzerine etkisi olup olmadığına dair herhangi bir bilgi bulunmamaktadır.
Gebelik dönemi
Diğer bütün nöromüsküler bloker ajanlarda olduğu gibi NEUCURİUM hamilelikte anneye beklenen yararları, fetüs üzerine muhtemel risklerinden fazla olduğuna inanılan durumlarda kullanılmalıdır. NEUCURİUM sezaryen ameliyatlarında kas gevşemesini sürdürmek için uygundur; çünkü atrakuryum önerilen dozları takiben plasentadan klinik açıdan anlamlı miktarda geçmez. NEUCURİUM gerekli olmadıkça gebelik döneminde kullanılmamalıdır.
Laktasyon dönemi
NEUCURİUM'un anne sütüne geçip geçmediği bilinmemektedir.
Üreme yeteneği/FertiIite
NEUCURİUM'un üreme yeteneği ve fertilite üzerindeki etkisi bilinmemektedir.
4.7. Araç ve makine kullanımı üzerindeki etkiler
Veri yoktur.
4.8. İstenmeyen etkiler
Rapor edilen istenmeyen etkiler aşağıdaki sıklık derecesine göre listelenmiştir:
Çok yaygın (>1/10); yaygın (>1/100 ila <1/10); yaygın olmayan (>1/1.000 ila <1/100); seyrek (>1/10.000 ila <1/1.000); çok seyrek (<1/10.000), bilinmiyor (eldeki verilerden hareketle tahmin edilemiyor).
Bağışıklık sistemi hastalıkları
Çok seyrek; Anatilaksi. Atrakuryum ile birlikte, bir ya da daha fazla anestezik ilaç verilen hastalarda çok seyrek olarak anafilaksiye benzeyen reaksiyonlar bildirilmiştir.
Sinir sistemi hastalıklan
Yaygınlığı bilinmiyor; Nöbet. Nadiren atrakuryum yanında birçok ilaç alan YBÜ hastalarında nöbetler bildirilmiştir. Ancak bu hastaların genellikle nöbetleri tetikleyen bir veya daha çok medikal durumları olduğu bildirilmiştir (Örn: kraniyel travma, serebral ödem, viral ensefalit, hipoksik ensefalopati, üremi). Bu nöbetlerin laudanosin ile nedensel ilişkisi saptanmamıştır. Klinik çalışmalarda, plazma laudanosin konsantrasyonu ile nöbet oluşumu arasında herhangi bir korelasyon görülmemiştir.
Vasküler hastalıklar
Yaygın; Hafif geçici hipotansiyon, deride kızarıklık
Solunum, göğüs bozuklukları ve mediastinal hastalıklan
Yaygın olmayan: Bronkospazm
Deri ve derialtı hastalıkları
Seyrek: Ürtiker
Kas-iskelet sistemi bozuklukları, bağ doku ve kemik hastahklan
Yaygınlığı bilinmiyor: Kas güçsüzlüğü ve/veya miyopati. YBÜ'ndeki ciddi hastalarda kas gevşeticilerin uzun süreli kullanımını takiben bazı kas güçsüzlüğü ve/veya miyopati raporları vardır. Bu hastaların birçoğu aynı zamanda kortikosteroid de kullanan hastalardır. Atrakuryum kullanımı sırasında bu semptomlar nadiren görülmektedir ve aralarında nedensel ilişki saptanmamıştır.
4.9. Doz aşımı ve tedavisi
Belirtiler: Uzamış kas paralizi ve bunun sonuçları aşırı dozajın ana belirtisidir.
Tedavisi: Spontan solunum yeterli oluncaya kadar pozitif basınçlı ventilasyon ile suni solunumun sürdürülmesi gerekir. Bilinç bozulmayana kadar tam sedasyon gerekebilir. Geri dönüş atropin veya glikopirolat ile birlikte antikolinesteraz ilaçlar uygulanarak hızlandırılabilir.
5. FARMAKOLOJİK ÖZELLİKLER
5.1. Farmakodinamik özellikler
Farmakoterapötik grup: Kas gevşeticiler, periferik etkili ajanlar ATC kodu; M03AC04
Atrakuryum yüksek derecede selektif, kompetitif veya non-depo 1arizan nöromüsküler blokör İlaçtır (Non-depolarizan nöroblokörler, motor son-plaktaki reseptörlere bağlanarak asetilkolinin etkisini antagonize ederler. Atrakuryum cerrahi girişimlerde ve kontrollü ventilasyonun kolaylaştırılmasında yaygın olarak kullanılır). Atrakuryumun göz içi basıncına hiçbir direkt etkisi yoktur, dolayısıyla göz ameliyatlarında kullanılmaya uygundur.
5.2. Farmakokinetik özellikler Genel özellikler
Emilim:
Atrakuryum farmakokinetiği 0.3-0.6 mg/kg doz aralığında doğrusaldır. Eliminasyon yarı ömrü yaklaşık 20 dakikadır.
Dağılım:
Dağılım hacmi 0.16 1/kg'dır. Atrakuryumun plazma proteinlerine bağlanma oranı %82'dir. Biyotransformasyon:
Atrakuryum, fizyolojik pH ve ısıda enzimatik olmayan parçalanma (Hofmann eliminasyonu) ve spesifik olmayan esterazlarla katalize edilen ester hidrolizi ile inaktive olur. Atrakuryumun nöromUsküler blokaj etkisinin sona ermesi karaciğer veya böbreklerdeki metabolizmasına veya atılımına bağımlı değildir. Bu nedenle etki süresinin böbrek, karaciğer veya dolaşım fonksiyon bozukluklarından etkilenmesi beklenmez. Psödokolinesteraz düzeyleri düşük olan hastalardan alınan plazma ile yapılan testler atrakuryum inaktivasyonunun etkilenmeden ilerlediğini göstermiştir. Hastada fizyolojik sınırlarda kan pH'ı ve vücut ısısı değişikliklerinin oluşması atrakuryumun etki süresini anlamlı bir şekilde değiştirmez. Hemofiltrasyon ve hemodiafiltrasyonun atrakuryumun ve laudanosin dahil metabolitlerinin plazma düzeylerine etkisi minimaldir. Hemodiyaliz ve hemoperfüzyonun atrakuryum ve metabolitlerinin plazma düzeylerine etkisi bilinmemektedir.
Eliminasvon:
Atrakuryum eliminasyonu böbrek ya da karaciğer fonksiyonlarına bağlı değildir.
Hastalardaki karakteristik özellikler
Yoğun bakım ünitesindeki hastalar:
Anormal böbrek ve/veya karaciğer fonksiyonu otan yoğun bakım ünitesi (YBÜ) hastalarında metabolitlerin konsantrasyonu daha yüksektir (bkz. Özel kullanım uyarıları ve önlemleri). Ancak bu metabol itlerin nöromüsküler bloke edici etkisi yoktur.
5.3.Klinik öncesi gUvenliIik verileri
Atrakutyum in vitroin vivo sıçan kemik iliği tayininde nöromusküler blokaj dozlarında mutajenik bulunmamıştır. Fare lenfoma tayininde hücrelerin yarısının öldüğü 60 mikrogram/ml dozda mutajenite gözlenmezken, 80 mikro gram/m 1 dozda orta derecede ve çok yüksek konsantrasyonda (1200 mikrogram/ml) zayıf mutajenite saptanmıştır. Atrakuryumun insanda kullanımı dikkate alındığında, insanlarda cerrahi relaksasyon sırasında kullanımında mutajenik riskin önemli olmadığı düşünülmektedir. Karsinojenite çalışması yapılmamıştır.
6. FARMASÖTİK ÖZELLİKLER
6.1. Yardımcı maddelerio listesi Benzensüifonik asit (pH ayan için)
Enjeksiyonluk su
6.2. Geçimsizlikler
NEUCURİUM yüksek pH'da inaktive olduğu için, herhangi bir alkali ajan ile birlikte aynı şırıngada karıştırılmamalıdır.
6.3. Raf ömrü
24 ay
6.4. Saklamaya yönelik özel tedbirler
2-8°C arasında saklayınız. Işıktan koruyunuz. Dondurmayınız.
Sadece taşıma veya soğuk depo dışında geçici depolama için 25±2''C'ye kadar ısı derecelerinde kısa sürelerde tutulmasına izin verilebilir.
Açılmış ampullerdeki kullanılmamış NEUCURİUM atılmalıdır.
6.5. Ambalajm niteliği ve içeriği
Karton kutu içerisinde 2.5 ml'lik 5 adet Tip I renksiz cam ampul.
6.6. Beşeri tıbbi üriinden arta kalan maddelerin imhası ve diğer özel önlemler
Kullanılmamış olan ürünler ya da atık materyaller 'Tıbbi Atıkların Kontrolü Yönetmeliği' ve 'Ambalaj Ve Ambalaj Atıklarının Kontrolü Yönetmelikleri'ne uygun olarak imha edilmelidir.
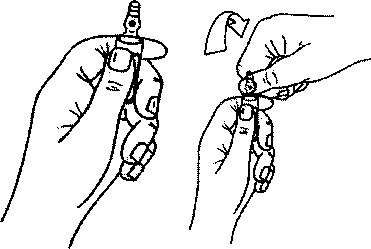
Ampul açma talimatlan
Ampuller OPC (Tek Kırma Noktası) açma sistemi ile donatılmıştır ve aşağıdaki talimatlar doğrultusunda açılmalıdır;
Resim rde gösterildiği gibi ampulü ak kısmından tutunuz.
Resim 2'de gösterildiği gibi diğer elinizin başparmağını ampuldeki renkli noktaya bastırınız.
Şekü 1 Şekil 2
7. RUHSAT SAHİBİ
VEM İlaç San. ve Tic. Ltd. Şti.
Cinnah Cad. Yeşilyurt Sok. No: 3/2 Çankaya / Ankara Telefon : (0312) 427 43 57-58
Faks : (0312) 427 43 59
8. RUHSAT NTJMARASI(LARI)
242 / 72
9. İLK RUHSAT TARİHİ/RUHSAT YENİLEME TARİHİ
ilk ruhsat tarihi: 30.05.2012 Ruhsat yenileme tarihi:
10. KÜB'ÜN YENİLENME TARİHİ
|
|
