Lantus Solostar 100u/ml Subkutan Kullanim İçin En... Kısa Ürün BilgisiSindirim Sistemi ve Metabolizma » Diyabet (Şeker Hastalığı) İlaçları » İnsülinler ve Analogları » İnsülin ve Analogları enjektabl (uzun etkili) » İnsülin Glargine KISA ÜRÜN BİLGİSİ 1. BEŞERİ TIBBİ ÜRÜNÜN ADILANTUS® SoloStar® 100 U/ml Subkutan Kullanım için Enjeksiyonluk Çözelti2. KALİTATİF VE KANTİTATİF BİLEŞİMİ Etkin madde:Enjeksiyonluk çözeltinin her bir ml'si, 100 U insülin glarjine eşdeğer 3.64 mg insülin glarjin içermektedir.Her bir kalem, 300 U'ye eşdeğer 3 ml enjeksiyonluk çözelti içermektedir. İnsülin glarjin Escherichia colikullanılarak rekombinant DNA teknolojisi ile üretilmiş bir insülin analoğudur.Yardımcı maddeler:Sodyum hidroksit 0.10 mg/mlYardımcı maddeler için 6.1'e bakınız. 3. FARMASÖTİK FORMKullanıma hazır enjeksiyon kalemi SoloStar içinde enjeksiyonluk çözelti LANTUS berrak ve renksiz çözeltidir.4. KLİNİK ÖZELLİKLER4.1. Terapötik endikasyonlarTip 1 diyabetli yetişkin ve 2 yaş ve üzerindeki çocuk hastalarda ve uzun etkili insülinin gerekli olduğu Tip 2 diyabetli yetişkin hastalarda endikedir.4.2. Pozoloji ve uygulama şekli Pozoloji/uygulama sıklığı ve süresiBu preparatın potensi ünite bazında belirtilmektedir. Bu birim LANTUS'a özeldir ve IU ile veya diğer insülin analoglarının potensi için kullanılan birimler ile aynı değildir (Bkz. Bölüm5.1. Farmakodinamik özellikler). LANTUS, uzatılmış etkiye sahip insülin analoğu olan insülin glarjin içermektedir. Her gün aynı saatte olmak şartıyla, günün herhangi bir saatinde, günde bir kez uygulanmalıdır. İnsülin glarjin dozu ve uygulama zamanı kişiye göre ayarlanmalıdır. Tip 2 diabetes mellitus hastalarında LANTUS oral etkili antidiyabetik tıbbi ürünlerle beraber uygulanabilir. Uygulama şekli:LANTUS subkütan uygulanır.LANTUS intravenöz uygulanmamalıdır. LANTUS'un uzun süreli etkisi subkütan dokuya enjeksiyonuna bağlıdır. Normal subkütan dozun intravenöz yoldan uygulanması şiddetli hipoglisemiye yol açabilir. LANTUS'un karın, uyluk veya deltoid yoldan uygulanmasından sonra serum insülin veya glukoz seviyelerinde klinik olarak anlamlı farklılıklar bulunmamıştır. Enjeksiyon yerleri her bir enjeksiyonda dönüşümlü olarak kullanılmalıdır. LANTUS başka bir insülinle karıştırılmamalı veya seyreltilmemelidir. Karıştırma veya seyreltme, zaman/etki profilini değiştirebilir ve karıştırma ürünün çökmesine yol açabilir. SoloStar'ı kullanmadan önce Bölüm 6.6. ve Kullanma Talimatı dikkatle okunmalıdır. (Bkz. Bölüm 6.6) Özel popülasyonlara ilişkin bilgilerSınırlı deneyim nedeniyle, LANTUS'un aşağıdaki hasta gruplarında etkililiği ve güvenliliği değerlendirilememiştir: 2 yaşın altındaki çocuklar, karaciğer yetmezliği veya orta/şiddetli böbrek yetmezliği olan hastalar (Bkz. 4.4. Özel kullanım uyarıları ve önlemleri) .Böbrek yetmezliği:Böbrek yetmezliği olan hastalarda, azalan insülin metabolizması nedeniyle, insülin ihtiyacı düşebilir.Karaciğer yetmezliği:Ciddi karaciğer yetmezliği olan hastalarda, azalan glukoneogenez kapasitesi ve azalan insülin metabolizması nedeniyle, insülin ihtiyacı düşebilir.Pediyatrik popülasyon:LANTUS'un güvenliliği ve etkililiği, adolesanlarda ve 2 yaş ve üzerindeki çocuklarda gösterilmiştir. 2 yaşın altındaki çocuklarda değerlendirme yapılmamıştır.Geriyatrik popülasyon:Yaşlılarda, böbrek fonksiyonlarının zamanla bozulması, insülin ihtiyacında sabit bir düşüşe neden olabilir.Diğer insülinlerden LANTUS'a geçişOrta veya uzun etkili insülinden, LANTUS'a geçerken, bazal insülin dozunda bir değişiklik yapılması ve birlikte kullanılan antidiyabetik tedavisinin (ilave regüler insülinlerin veya hızlı etkili insülin analoglarının dozu ve zamanlaması veya oral antidiyabet ajanların dozu) ayarlanması gerekebilir.Bazal insülinle tedavi şemasını günde iki kez NPH insülinden, günde tek doz LANTUS'a değiştiren hastalar, gece ve sabah erken saatlerde hipoglisemi riskini azaltmak için, tedavinin ilk haftalarında günlük bazal insülin dozlarını %20-30 oranında azaltmalıdırlar.İlk haftalardaki bu doz azaltımı, en azından kısmen, öğün vakti alınan insülin artırılarak telafi edilmeli, bu dönemden sonra doz şeması kişiye göre ayarlanmalıdır. Diğer insülin analogları ile olduğu gibi, insan insülinine karşı antikor oluşumu nedeniyle yüksek insülin dozları ile tedavi edilmekte olan hastalar LANTUS ile düzelen bir insülin yanıtı gösterebilirler. Diğer insülinlerden LANTUS'a geçiş sırasında ve bunu izleyen ilk haftalarda yakın metabolik kontrol önerilmektedir. Düzelen metabolik kontrol ve bunun sonucunda insülin duyarlılığında meydana gelen artış nedeniyle dozlam şemasında yeniden ayarlama yapılması gerekebilir. Hastanın vücut ağırlığı veya yaşam tarzı, insülin alım zamanı değiştiğinde ya da hipoglisemiye veya hiperglisemiye duyarlılığı arttıran başka koşulların geliştiği durumlarda da doz ayarlaması gerekebilir (Bkz. 4.4. Özel kullanım uyarıları ve önlemleri) . 4.3. Kontrendikasyonlarİnsülin glarjin veya formülündeki herhangi bir yardımcı maddeye karşı aşırı duyarlılık.4.4. Özel kullanım uyarıları ve önlemleriLANTUS, diyabetik ketoasidozun tedavisi için uygun bir insülin seçeneği değildir. Bu gibi durumlarda intravenöz olarak uygulanan regüler insülin tavsiye edilmektedir.LANTUS'un güvenliliği ve etkililiği, adolesanlarda ve 2 yaş ve üzerindeki çocuklarda gösterilmiştir. 2 yaş ve üzerindeki çocuk hastalarda etkinlik ve güvenlilik verileri yalnız 6 ay süreli tek bir çalışmaya dayanmaktadır. Sınırlı deneyim nedeniyle LANTUS'un etkililik ve güvenliliği; 2 yaşın altındaki çocuklarda, karaciğer yetmezliği olan hastalarda veya orta/şiddetli böbrek yetmezliği olan hastalarda değerlendirilememiştir (Bkz. 4.2. Pozoloji ve uygulama şekli). Böbrek yetmezliği olan hastalarda, azalan insülin metabolizması nedeniyle, insülin ihtiyacı düşebilir. Yaşlılarda, böbrek fonksiyonlarındaki ilerleyici bozulma, insülin ihtiyacında sabit bir düşüşe neden olabilir. Ciddi karaciğer yetmezliği olan hastalarda, azalan glukoneogenez kapasitesi ve azalan insülin metabolizması nedeniyle, insülin ihtiyacı düşebilir. Yetersiz kan şekeri kontrolü veya hipo- veya hipergliseminin epizotlarına bir eğilim olması durumunda, doz ayarlaması yapmadan önce hastanın tedavi şemasına uyumu, enjeksiyon yerleri, uygun enjeksiyon tekniği ve diğer ilgili faktörler gözden geçirilmelidir. Hastanın başka bir tip veya marka insüline geçmesi sıkı bir tıbbi gözlem altında yapılmalıdır Form, marka (üretici), tip (regüler, NPH, lente, uzun etkili, vs.), orijin (hayvan, insan, insan insülin analoğu) ve/veya üretim metodu değişimleri; doz değişim ihtiyacı ile sonuçlanabilir. İnsülin uygulanması, insülin antikorlarının oluşmasına sebep olabilir. Bazı insülin antikorlarının varlığı, nadiren hiper- veya hipoglisemiye eğilimi düzeltmek için insülin doz ayarlamasını gerektirebilir. Hipoglisemi Hipogliseminin ortaya çıkma zamanı kullanılan insülinlerin etki profiline bağlıdır ve dolayısıyla tedavi şeması değiştiğinde değişebilir. LANTUS'un bazal insülin sağlamasının daha sürekli olması nedeniyle geceleri daha az ama çoğunlukla erken sabah hipoglisemisi beklenebilir. Hipoglisemik epizotların özel bir klinik anlam taşıyabileceği hastalarda özellikle dikkatli olunmalıdır ve kan şekeri izlenmesinin yoğunlaştırılması tavsiye edilebilir. Bu hastalar şunlardır: beyni besleyen kan damarlarında veya koroner arterlerde anlamlı daralma (kardiyak veya serebral hipoglisemi komplikasyonları riski) olan hastalar ya da proliferatif retinopatisi olan hastalar, özellikle de fotokoagülasyonla tedavi edilmediği (hipoglisemi sonrası geçici körlük riski) durumlar. Hastalar, hipogliseminin uyarıcı semptomlarının azaldığı durumlar hakkında uyanık olmalıdırlar. Bazı risk gruplarında hipogliseminin uyarıcı semptomları değişebilir, daha az belirgin olabilir veya hiç görünmeyebilir. Bu hastalar şunlardır; - kan şekeri kontrolü belirgin biçimde düzelmiş olanlar - yavaş gelişen hipoglisemisi olanlar - yaşlılar - hayvan insülininden insan insülinine geçiş yapanlar - otonomik nöropatisi bulunanlar - uzun süredir diyabeti olanlar - bir psikiyatrik hastalığı bulunanlar - belirli bazı tıbbi ürünleri birlikte kullananlar (Bkz. Bölüm 4.5) Bu gibi durumlarda, hasta hipogliseminin farkına varmadan, ağır hipoglisemi (ve hatta bilinç kaybı) gelişebilir. Subkütan insülin glarjinin uzatılmış etkisi hipogliseminin düzelmesini geciktirebilir. Eğer glikozillenmiş hemoglobin için normal veya azalmış değerler saptanırsa, tekrarlayan, fark edilmemiş (özellikle gece) hipoglisemi epizotları olasılığı düşünülmelidir. Hastanın tedavi ve diyet şemasına uyumu, doğru insülin uygulaması ve hipoglisemi semptomları hakkında haberdarlık, hipoglisemi riskini azaltmak için son derece önemlidir. Hipoglisemiye yatkınlığı artıran faktörlerin varlığı özellikle yakın izlemeyi zorunlu kılar ve doz ayarlamasını gerektirebilir. Bu faktörler şunlardır: - enjeksiyon bölgesinde değişiklik - artan insülin duyarlılığı (örneğin stres faktörlerinin uzaklaştırılması) - alışık olunmayan, artan veya uzamış fiziksel aktivite - eşlik eden hastalık durumu (örneğin kusma, diyare) - yetersiz gıda alımı - kaçırılan öğünler - alkol tüketimi - kompanse edilmeyen endokrin bazı bozukluklar (örneğin hipotiroidizm ve ön hipofiz veya adrenokortikal yetersizlik) - belirli bazı tıbbi ürünlerin birlikte kullanılması (Bkz. Bölüm 4.5) Eşlik eden hastalık Eşlik eden bir hastalık olması durumunda daha yoğun bir metabolik izleme gerekir. Pek çok olguda, ketonlar için idrar testleri endikedir ve çoğunlukla insülin dozunun ayarlanması gerekir. İnsülin gereksinimi çoğunlukla artar. Tip 1 diyabeti olan, hastalar çok az yiyebilseler veya hiç yiyemeseler veya kusma vb. sorunları yaşasalar bile az da olsa karbonhidrat tüketimini sürdürmeli ve insülini asla tamamen bırakmamalıdır. Kalem kullanımı SoloStar'ı kullanmadan önce Bölüm 6.6. ve Kullanma Talimatı dikkatle okunmalıdır. SoloStar Kullanma Talimatında önerildiği gibi kullanılmalıdır (Bkz. Bölüm 6.6) Uygulama hataları Diğer insülinlerin, özellikle de kısa etkili insülinlerin yanlışlıkla insülin glarjin yerine uygulandığı ilaç uygulama hataları bildirilmiştir. Uygulama sırasında insülin glarjinle diğer insülinleri karıştırmamak için, her enjeksiyondan önce insülinin etiketi mutlaka kontrol edilmelidir. LANTUS'un pioglitazonla birlikte uygulanması Özellikle kalp yetmezliği gelişimi açısından risk faktörleri bulunan hastalarda, pioglitazonun insülinle birlikte kullanılması sırasında kalp yetmezliği olguları bildirilmiştir. LANTUS'un pioglitazonla birlikte uygulanması düşünüldüğünde bu risk göz önünde bulundurulmalıdır. Bu kombinasyonun uygulanması halinde, hastalar kalp yetmezliği belirti ve semptomları, kilo alımı ve ödem açısından takip edilmelidir. Kardiyak semptomlarda bozulma görülmesi durumunda, pioglitazon tedavisine son verilmelidir. 4.5. Diğer tıbbi ürünler ile etkileşimler ve diğer etkileşim şekilleriÇok sayıda madde glukoz metabolizmasını etkiler ve insülin glarjinin dozunun ayarlanmasını gerektirebilir.Kan şekerini düşürücü etkiyi artırabilecek ve hipoglisemi yatkınlığını arttırabilecek maddeler; oral antidiyabetik ajanlar, anjiyotensin dönüştürücü enzim (ADE) inhibitörleri, disopiramid, fibratlar, fluoksetin, monoamino oksidaz (MAO) inhibitörleri, pentoksifilin, propoksifen, salisilatlar veya sülfonamid antibiyotikleri içermektedir. Kan şekerini düşürücü etkiyi azaltabilecek maddeler; kortikosteroidler, danazol, diazoksid, diüretikler, glukagon, izoniazid, östrojenler ve projestojenler, fenotiazin türevleri, somatropin, sempatomimetik ajanlar (örneğin, epinefrin [adrenalin], salbutamol, terbutalin) ve tiroid hormonları, atipik antipsikotik tıbbi ürünler (örneğin klozapin ve olanzapin) ve proteaz inhibitörlerini içermektedir. Beta-blokörler, klonidin, lityum tuzları veya alkol insülinin kan şekerini düşürücü etkisini kuvvetlendirebilir veya zayıflatabilir. Pentamidin hipoglisemiye yol açabilir ve bazen bunu hiperglisemi izleyebilir. Bunun yanı sıra, beta-blokörler, klonidin, guanetidin ve rezerpin gibi sempatolitik ilaçların etkisiyle, adrenerjik karşı-düzenleme belirtileri azalabilir veya kaybolabilir. 4.6. Gebelik ve laktasyon Genel tavsiyeGebelik kategorisi C'dir.Çocuk doğurma potansiyeli olan kadınlar/doğum kontrolü (Kontrasepsiyon)İnsülin glarjin için, kontrollü klinik çalışmalardan, gebelik ile ilgili klinik veri bulunmamaktadır. Pazarlama sonrası araştırmalarda gebe kadınlardan elde edilen sınırlı sayıda veri (300-1000 gebelikteki sonuçlar) insülin glarjinin gebelik veya fetüsün ve yeni doğanın sağlığı üzerine herhangi bir advers etkisini işaret etmemiştir. Bu tarihe kadar, ilgili başka epidemiyolojik veri mevcut değildir.Gebelik dönemiMevcut klinik veri, riskin tamamen dışlanması için yetersizdir. Gerekli ise gebelikte LANTUS kullanımı düşünülebilir.Önceden var olan veya gestasyonal diyabeti olan hastalar için tüm gebelik süresince iyi metabolik kontrolün sürdürülmesi çok önemlidir. İnsülin gereksinimi ilk trimesterde azalabilir ve genellikle ikinci ve üçüncü trimesterde artar. Doğumdan hemen sonra, insülin gereksinimi hızla düşer (artan hipoglisemi riski). Bu nedenle kan şekerinin dikkatli izlenmesi çok önemlidir. Laktasyon dönemiİnsülin glarjinin insan sütüne geçip geçmediği bilinmemektedir. Bir peptid olan insülin glarjin insan sindirim sisteminde sindirilerek aminoaistlere indirgendiğinden, ağızdan alınan insülin glarjinin emzirilen yenidoğanlarda/süt çocuklarında metabolik etki yapması beklenmez. Emziren kadınlarda insülin dozu ve diyette ayarlama yapılması gerekebilir.Üreme yeteneği (fertilite)Hayvan çalışmaları, gebelik, embriyo/fetüs gelişimi, doğum veya postnatal gelişim açısından herhangi bir doğrudan zararlı etkiyi işaret etmemektedir (Bkz. 5.3. Klinik öncesi güvenlilik verileri).4.7. Araç ve makine kullanımı üzerindeki etkilerHipoglisemi veya hiperglisemi veya örneğin görme bozukluğunun bir sonucu olarak hastanın konsantre olma ve tepki verme yeteneği etkilenebilir. Bu durum, bu yeteneklerin özellikle önemli olduğu (örn. araç veya makine kullanma gibi) durumlarda bir risk oluşturur.Hastalara araba kullanırken hipoglisemiden kaçınmak için önlemler almaları tavsiye edilmelidir. Bu durum, hipogliseminin uyarıcı semptomlarına farkına varma yeteneği azalmış veya kaybolmuş kişilerde ya da sık hipoglisemi epizotları yaşayan kişilerde özellikle önemlidir. Bu koşullarda araç veya makine kullanmanın tavsiye edilebilir olup olmadığı düşünülmelidir. 4.8. İstenmeyen etkilerİnsülin tedavisinin genellikle en sık görülen istenmeyen etkisi olan hipoglisemi, insülin dozunun insülin gereksinimine oranla fazla yüksek olması halinde meydana gelebilir.Aşağıda klinik çalışmalarda gözlenen ilgili advers reaksiyonlar sistem organ klasifikasyonuna ve azalan sıklığa göre listelenmiştir: Çok yaygın (> 1/10); yaygın (> 1/100 ila <1/10); yaygın olmayan (> 1/1.000 ila <1/100); seyrek (> 1/10.000 ila <1/1.000); çok seyrek (< 1/10.000). Her bir sıklık grubunda, istenmeyen etkiler azalan ciddiyet (şiddet) düzeyine göre sıralanmıştır. Metabolizma ve beslenme bozukluklarıÇok yaygın: HipoglisemiŞiddetli hipoglisemik ataklar, özellikle eğer tekrarlayan ataklar ise, nörolojik hasarlara yol açabilirler. Uzayan veya şiddetli hipoglisemik epizotlar yaşamı tehdit edici olabilir. Pek çok hastada, nöroglikopeni belirti ve semptomları adrenerjik karşı-düzenleme (kontr-regülasyon) belirtilerini takip eder. Genellikle, kan glukozundaki düşüş ne kadar fazla ve hızlı olursa, karşı-düzenleme fenomeni ve bunun semptomları o kadar belirgin olur. Bağışıklık sistemi bozukluklarıSeyrek: alerjik reaksiyonlarİnsüline karşı ani gelişen tipte alerjik reaksiyonlar seyrektir. İnsülinlere (insülin glarjin dahil) veya yardımcı maddelere karşı görülen bu tip reaksiyonlar genel deri reaksiyonları, anjiyo-ödem, bronkospazm, hipotansiyon ve şok ile bağlantılı olabilir ve yaşamı tehdit edici olabilir. İnsülin uygulaması, insülin antikorlarının oluşmasına neden olabilir. Klinik çalışmalarda, insan insülini ve insülin glarjin ile çapraz reaksiyona giren antikorlar hem NPH-insülin hem de insülin glarjin tedavi gruplarında aynı sıklıkta gözlenmiştir. Seyrek olgularda, bu gibi insülin antikorlarının varlığı, hiper- veya hipoglisemi eğilimini düzeltmek üzere insülin dozunun ayarlanmasını gerekli kılabilir. Sinir sistemi bozukluklarıÇok seyrek: tat alma duyusunda bozuklukGöz bozukluklarıSeyrek: görme bozukluğuGlisemik kontrolde belirgin bir değişiklik, göz merceklerinin dolgunluğu ve refraktif indeksindeki geçici değişikliklerden dolayı, geçici görme bozukluğuna neden olabilir. Seyrek: Retinopati Uzun süreli düzelen glisemik kontrol diyabetik retinopatinin ilerleme riskini azaltır. Bununla birlikte, glisemik kontrolde ani düzelme sağlayan yoğun insülin tedavisi de diyabetik retinopatinin geçici bir süre kötüleşmesine neden olabilir. Proliferatif retinopatisi olan hastalarda, özellikle fotokoagülasyon ile tedavi edilmemişse, şiddetli hipoglisemik epizotlar geçici görme kaybına yol açabilir. Deri ve derialtı doku bozukluklarıDiğer insülin tedavilerinde olduğu gibi, enjeksiyon yerinde lipodistrofi oluşabilir ve lokal insülin absorpsiyonunu geciktirebilir. Enjeksiyon yerinin devamlı olarak değiştirilmesi bu reaksiyonların azalmasına veya önlenmesine yardımcı olabilir.Yaygın: Lipohipertrofi Yaygın olmayan: Lipoatrofi Kas iskelet ve bağlayıcı doku bozukluklarıÇok seyrek: Kas ağrısı (miyalji)Genel bozukluklar ve uygulama yeri koşullarıYaygın: Enjeksiyon yeri reaksiyonlarıBu reaksiyonlar, kızarıklık, ağrı, kaşıntı, ürtiker, şişme veya enflamasyonu içermektedir. İnsülinlere karşı enjeksiyon yerinde gözlenen çoğu minör reaksiyonlar çoğunlukla birkaç gün veya hafta içinde kaybolur. Seyrek: Ödem Seyrek olarak ve özellikle daha önceki zayıf metabolik kontrol yoğun insülin tedavisi ile düzeltildiğinde, insülin sodyum tutulmasına ve ödeme neden olabilir. Yaralanma, zehirlenme ve prosedürel komplikasyonlarBilinmiyor: İnsulin glarjin yerine özellikle kısa etkili insülin olmak üzere diğer insülinlerin yanlışlıkla uygulanması gibi ilaç kullanım yanlışlıkları bildirilmiştir (bkz. bölüm 6.6).Pediyatrik popülasyonGenel olarak, 18 yaş ve altındaki hastalar için güvenlilik profili 18 yaş üstü hastalar ile benzerdir.Pazarlama sonrası çalışmalardan elde edilen yan etki bildirimleri; 18 yaş ve altındaki hastalarda 18 yaş üstü hastalara göre, nispeten daha sık enjeksiyon yeri reaksiyonlarını (enjeksiyon yerinde ağrı, reaksiyon) ve deri reaksiyonlarını (döküntü, ürtiker) içermekteydi. 2 yaş altındaki hastalarda herhangi bir klinik çalışma güvenlilik verisi mevcut değildir. 4.9. Doz aşımı ve tedavisi Belirtilerİnsülin doz aşımı şiddetli ve bazen uzun süreli ve yaşamı tehdit edebilen hipoglisemiye yol açabilir.TedaviHafif hipoglisemi epizotları çoğunlukla oral karbonhidratlarla tedavi edilebilir. Tıbbi ürünün dozu, öğün alışkanlıkları veya fiziksel aktivitede ayarlamalar gerekebilir.Koma, nöbet veya nörolojik bozukluğun eşlik ettiği daha şiddetli epizodlar intramusküler/subkütan glukagon ya da konsantre intravenöz glukoz ile tedavi edilebilir. Hipoglisemi belirgin klinik düzelmeden sonra da tekrarlayabileceği için karbonhidrat alınımının ve hastanın izlenmesinin sürdürülmesi gerekebilir. 5. FARMAKOLOJİK ÖZELLİKLER5.1. Farmakodinamik özelliklerFarmakoterapötik grup: Enjeksiyonluk uzun-etkili insülinler ve analogları.ATC Kodu: A10A E04 LANTUS, insülin glarjin içeren bir antidiyabetiktir. İnsülin glarjin rekombinant DNA teknolojisi ile üretilen bir insan insülini analoğudur. Nötral pH'de düşük çözünürlük göstermek üzere tasarlanmıştır. İnsülin glarjin, LANTUS enjeksiyonluk çözeltinin asidik pH'sında (pH 4'de) tamamen çözünür. Subkütan enjeksiyonu takiben, asidik çözelti nötralleşerek mikroçökeltilerin oluşmasına yol açar. Bunlardan sürekli az miktarda salıverilen insülin glarjin düzgün pikler içermeyen, uzun süreli ve öngörülebilir konsantrasyon/zaman profili oluşturur. İnsülin glarjin M1 ve M2 olmak üzere 2 aktif metabolite metabolize olur. (bkz. Bölüm 5.2) İnsülin reseptörüne bağlanma: In vitro çalışmalar, insülin glarjin ile M1 ve M2 metabolitlerinin insan insülin reseptörüne afinitesinin insan insülini ile benzer olduğunu göstermektedir. IGF-1 reseptörüne bağlanma: İnsülin glarjinin insan IGF-1 reseptörüne afinitesi insan insülinin afinitesinden yaklaşık 5 ila 8 kat daha fazladır (ancak IGF-1'in afinitesinden yaklaşık 70 ila 80 kat daha düşüktür), oysa M1 ve M2 IGF-1 reseptörüne insan insülinine kıyasla biraz daha düşük afiniteyle bağlanmaktadır. Tip I diyabetik hastalarda bulunan total insülin konsantrasyonunun (insülin glarjin ve metabolitleri), IGF-1 reseptörlerin yarı maksimal işgali ve sonrasında IGF-1 reseptörü ile başlatılan mitojenik-proliferatif yolağın aktivasyonu için gerekenden belirgin olarak daha düşük olduğu gösterilmiştir. Endojen IGF-1'in fizyolojik konsantrasyonları mitojenik-proliferatif yolağı aktive edebilir; ancak, Lantus tedavisi dahil olmak üzere insülin tedavisinde bulunan terapötik konsantrasyonlar IGF-1 yolağını aktive etmek için gereken farmakolojik konsantrasyonlardan belirgin olarak daha düşüktür. İnsülin glarjin de dahil olmak üzere insülinin primer aktivitesi glukoz metabolizmasının düzenlenmesidir. İnsülin ve analogları, özellikle iskelet kası ve yağ tarafından periferik glukoz alımını uyararak ve hepatik glukoz üretimini inhibe ederek kan glukoz düzeylerini düşürürler. İnsülin, adipositte lipolizi inhibe eder, proteolizi inhibe eder ve protein sentezini artırır. Klinik farmakoloji çalışmalarında, aynı dozlarda verildiğinde, intravenöz insülin glarjin ve insan insülininin eşit etki gücüne sahip olduğu gösterilmiştir. Tüm insülinlerde olduğu gibi, insülin glarjinin etki süresi fiziksel aktivite ve diğer değişkenlerden etkilenebilmektedir. Sağlıklı bireylerde veya tip 1 diyabeti olan hastalarda yapılan öglisemik klemp çalışmalarında, subkütan uygulanan insülin glarjinin etki başlangıcı, insan NPH insülinine kıyasla daha yavaş, etki profili düz, piksiz ve etkisi daha uzundur. Aşağıdaki grafik hastalarda yapılan çalışmanın sonuçlarını göstermektedir. İnsülin glarjinin daha uzun süreli etkisi, daha yavaş olan absorpsiyon hızıyla doğrudan ilişkilidir ve günde tek doz uygulamayı desteklemektedir. İnsülin glarjin gibi insülin ve insülin analoglarının etki süresi farklı bireylerde ya da bireyin kendisinde belirgin değişkenlik gösterebilir. Bir klinik çalışmada, hem sağlıklı gönüllülerde hem de tip 1 diyabeti olan hastalarda intravenöz uygulanan insülin glarjin ve insan insülininden sonra hipoglisemi semptomları veya karşı-düzenleyici hormon yanıtları benzer bulunmuştur. Şekil 1: Tip I Diyabet hastalarında aktivite profili6i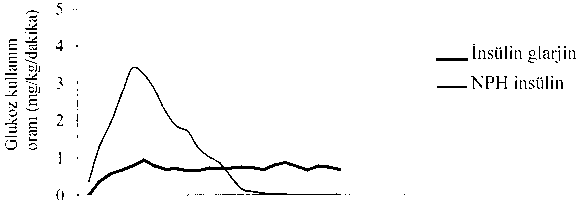 01020
01020^30s.c enjeksiyonundan sonraki süre (saat) t toztem dönemi sonu *Sabit plazma glukoz düzeyleri sağlamak üzere infüzyon yapılan glukoz miktarı olarak belirlenmiş (saat başı ortalama değerler) Tip 2 diyabeti olan 1024 hastada günde tek doz LANTUS'un diyabetik retinopati üzerindeki etkileri açık-etiketli 5 yıllık NPH (günde iki doz) kontrollü bir çalışmada değerlendirildi. Diyabetik retinopatinin erken tedavi çalışmasında (ETDRS), derecesi 3 veya üzerindeki basamakta retinopatisi olan bu hastaların retinopati ilerlemesi fundus fotografisi ile incelendi. LANTUS ile NPH insülin karşılaştırıldığında, diyabetik retinopatinin ilerlemesinde anlamlı bir farklılık görülmedi. Pediyatrik popülasyon:Randomize, kontrollü bir çalışmada, yaşları 6-15 arasında değişen tip 1 diyabetli pediyatrik hastalar (n=349), 28 hafta süreyle bazal-bolus insülin rejimiyle tedavi edildi; her öğünden önce regüler insan insülini uygulandı. İnsülin glarjin günde bir kez yatmadan önce, NPH insan insülini günde bir veya iki kez uygulandı. Her iki tedavi grubunda glikohemoglobin ve semptomatik hipoglisemi insidansı üzerinde benzer etkiler gözlendi. Bununla beraber, insülin glarjin grubunda açlık plazma glukozunda başlangıç değerine göre gözlenen düşüş, NPH grubuna kıyasla daha fazla oldu. İnsülin glarjin grubunda gözlenen hipoglisemi de daha hafifti. Bu çalışmada insülin glarjinle tedavi edilen hastaların 143'ü, ortalama takip süresi 2 yıl olan kontrolsüz devam çalışmasında insülin glarjinle tedaviye devam etti. İnsülin glarjinle tedavinin uzatıldığı bu dönemde, güvenlilikle ilgili yeni bir uyarı işareti saptanmadı. Yaşları 12-18 arasında değişen, tip 1 diyabetli 26 adolesanın dahil edildiği çapraz bir çalışmada, insülin glarjin + insülinlispro, NPH + regüler insan insüliniyle karşılaştırıldı. Her bir tedavi, rastgele sıra ile 16 hafta süreyle uygulandı. Yukarıda tanımlanan pediyatrik çalışmada olduğu gibi bu çalışmada da, başlangıç değerine kıyasla açlık plazma glukozunda gözlenen azalma, insülin glarjin grubunda NPH grubundan daha fazlaydı. HbA1c'de başlangıç değerine göre gözlenen değişiklikler her iki tedavi grubunda benzer bulundu. Bununla beraber, gece boyunca kaydedilen kan glukozu değerleri, insülin glarjin/lispro grubunda, NPH/regüler grubuna kıyasla anlamlı derecede daha yüksekti (ortalama en düşük nokta sırasıyla 5.4 mM'ye karşılık 4.1 mM). Buna paralel olarak, noktürnal hipoglisemi insidansları insülin glarjin/lispro grubunda %32, NPH/regüler grubunda %52 olarak saptandı. Yaşları 2-6 arasında değişen tip 1 diabetes mellituslu 125 çocuğun dahil edildiği 24 haftalık paralel grup çalışmasında, günde bir kez sabahları uygulanan insülin glarjin ve günde bir veya iki kez uygulanan NPH insülinden oluşan çoklu günlük enjeksiyon rejimleri karşılaştırıldı. Her iki gruba da yemeklerden önce bolus insülin verildi. Tüm hipoglisemilerde insülin glarjinin NPH'a üstünlüğünü gösteren birincil hedefle karşılaşılmadı ve insülin glarjin hipoglisemi olaylarını arttırma trendi gösterdi (insülin glarjin:NPH oranı (%95 Cl)=1.18 (0.97-1.44) . Her iki grupta da glikohemoglobin ve glukoz değişkenlikleri karşılaştırıldı. Bu çalışmada yeni güvenlik sinyalleri gözlemlenmedi. Sürekli glukoz takibinde 70 mg/dl'nin altındaki sapmalar her iki grupta da benzer oranlarda kaydedildi ve glikohemoglobin üzerindeki etkiler her iki grupta benzer bulundu. 5.2. Farmakokinetik özelliklerEmilim:Sağlıklı bireylerde ve diyabetik hastalarda, insülin glarjinin subkütan enjeksiyonunu takiben, serum insülin konsantrasyonları insan NPH insülinine kıyasla daha yavaş ve çok daha uzun süreli absorpsiyon olduğunu ve bir doruk (peak) olmadığını göstermiştir. Dolayısıyla, konsantrasyonlar insülin glarjinin farmakodinamik aktivitesinin zaman profiliyle uyumlu bulunmuştur. Şekil 1'deki grafik insülin glarjin ve NPH insülinin zamana göre aktivite profilini göstermektedir. Dağılım:Günde bir kez enjekte edilen insülin glarjin, ilk dozdan sonraki 2-4 gün içinde kararlı durum düzeyine ulaşır. Biyotransformasyon:Diyabetik hastalarda subkutan LANTUS enjeksiyonundan sonra, insülin glarjin Beta zincirinin karboksil ucunda hızla metabolize olarak, iki aktif metabolit olan M1 (21A-Gly-insülin) ve M2 (21A-Gly-des-30B-Thr-insülin) oluşmaktadır. Plazmada, dolaşımdaki başlıca bileşik M1 metabolitidir. M1'e maruziyet uygulanan LANTUS dozuyla birlikte artar. Farmakokinetik ve farmakodinamik bulgular, LANTUS ile subkutan enjeksiyonun etkisinin esas olarak M1'e maruziyete dayandığını göstermektedir. İnsülin glarjin ve M2 metaboliti bireylerin büyük çoğunluğunda saptanabilir düzeyde bulunmamıştır ve saptanabildiklerinde de konsantrasyonlarının uygulanan LANTUS dozundan bağımsız olduğu bulunmuştur. Eliminasyon:İntravenöz yoldan uygulandığında insülin glarjin ve insan insülininin eliminasyon yarılanma ömrü benzerdir. Doğrusallık/doğrusal olmayan durum:İnsülin glarjinin konsantrasyonları, farmakodinamik aktivitesinin zaman profiliyle uyumlu bulunmuştur. Hastalardaki karakteristik özelliklerYaş ve cinsiyet:Klinik çalışmalarda yaş ve cinsiyete dayanan alt-grup analizleri, insülin glarjin ile tedavi edilen hastalarla bütün araştırma popülasyonu karşılaştırıldığında, güvenlilik ve etkililik açısından herhangi bir farklılık göstermemiştir. Pediyatrik popülasyon:Yaşları 2-6 arasında değişen tip 1 diabetes mellituslu çocuklardaki farmakokinetik özellikler bir klinik çalışmada değerlendirilmiştir (bkz. Bölüm 5.1). İnsülin glarjinle tedavi edilen çocuklarda, insülin glarjinin ve aktif metabolitleri olan M1 ve M2'nin plazma çukur (vadi) düzeyleri ölçülmüş, plazma konsantrasyonu değerlerinin erişkinlerle benzer olduğu ve kronik kullanımda insülin glarjinin veya metabolitlerinin birikme eğilimi göstermediği saptanmıştır. Böbrek yetmezliği:Böbrek yetmezliği olan hastalarda, azalan insülin metabolizması nedeniyle, insülin ihtiyacı düşebilir. Karaciğer yetmezliği:Ciddi karaciğer yetmezliği olan hastalarda, azalan glukoneogenez kapasitesi ve azalan insülin metabolizması nedeniyle, insülin ihtiyacı düşebilir. Geriyatrik popülasyon:Yaşlılarda, böbrek fonksiyonlarının zamanla bozulması, insülin ihtiyacında sabit bir düşüşe neden olabilir. 5.3. Klinik öncesi güvenlilik verileriKlinik öncesi veriler konvansiyonel güvenlilik farmakolojisi, tekrarlayan doz toksisitesi, genotoksisite, karsinojenik potansiyel ve üreme toksisitesi ile ilgili çalışmalar baz alındığında insanlar için özel bir tehlike göstermemektedir.6. FARMASÖTİK ÖZELLİKLER6.1. Yardımcı maddelerin listesiÇinko klorürM-krezol Gliserol Hidroklorik asit Sodyum hidroksit Enjeksiyonluk su 6.2. GeçimsizliklerLANTUS diğer tıbbi ürünlerle karıştırılmamalıdır.6.3. Raf ömrü36 ayKalemin ilk kullanımdan sonraki raf ömrüDirekt ışıktan ve sıcaklıktan korumak şartıyla, tıbbi ürün maksimum 4 hafta süre ile 25 °C'nin altında saklanabilir. Kullanımdaki kalemler buzdolabında saklanmamalıdır. Her enjeksiyondan sonra ışıktan korumak için kalemin kapağı geri takılmalıdır. 6.4. Saklamaya yönelik özel tedbirlerKullanılmamış kalemlerBuzdolabında (2 oC - 8 oC'de) saklayınız.Dondurmayınız. LANTUS'un buzdolabında dondurucu bölme veya soğutma paketi ile doğrudan temasını önleyiniz. Kullanıma hazır dolu enjeksiyon kalemlerini ışıktan korumak için dış kutusunda saklayınız. Kullanımdaki kalemlerSaklama koşulları için Bkz. 6.3.6.5. Ambalajın niteliği ve içeriğiSiyah tıpa (bromobütil kauçuk) ve başlık (alüminyum halkalı) ve kapak (bromobütil veya poliizopren lamine ve bromobütil kauçuk) içeren kartuşlarda (Tip I, renksiz, cam) 3 ml çözelti. Kartuşlar kullanılıp atılabilen kalem içine yerleştirilmiştir. Ambalaj iğne ucu içermez.5 kalem içeren ambalajları bulunmaktadır. 6.6. Beşeri tıbbi üründen arta kalan maddelerin imhası ve diğer özel önlemlerKartuş kullanmadan önce, oda sıcaklığında 1-2 saat süre ile tutulmalıdır.Kartuş kullanmadan önce incelenmelidir. Sadece çözelti berrak, renksiz ve görülebilir katı partikül içermeyen ve su gibiyse kullanılmalıdır. LANTUS çözelti olduğundan, kullanılmadan önce yeniden süspansiyon haline getirilmesi gerekmemektedir. Enjeksiyon öncesi kartuşlardan hava kabarcığı çıkarılmalıdır (Bkz. Kalem kullanma talimatları). Boş kalemler asla yeniden kullanılmamalıdır ve uygun bir şekilde atılmalıdır. Herhangi bir kontaminasyonu önlemek için, her bir kullanıma hazır dolu enjeksiyon kalemi yalnız bir hasta tarafından kullanılmalıdır. İnsülin glarjin ve diğer insülinler arasındaki ilaç kullanım yanlışlığını önlemek için insülin etiketi her enjeksiyon öncesi kontrol edilmelidir (bkz. bölüm 4.8). Kullanılmamış olan ürünler ya da atık materyaller Tıbbi Atıkların Kontrolü Yönetmeliği ve Ambalaj ve Ambalaj Atıklarının Kontrolü Yönetmelik'lerine uygun olarak imha edilmedir. 7. RUHSAT SAHİBİSanofi aventis İlaçları Ltd. Şti.Büyükdere Cad. No:193 Levent 34394, İstanbul Tel: 0 212 339 10 00 Faks: 0 212 339 10 89 8. RUHSAT NUMARASI (LARI)114/859. İLK RUHSAT TARİHİ / RUHSAT YENİLEME TARİHİİlk ruhsat tarihi: 07.10.2003 Ruhsat yenileme tarihi:-10. KÜB'ÜN YENİLENME TARİHİİğne dış |
|||||||||
|
|
JCalem gövdesi | |
|
İnsülin haznesi |
|
|
|
|
| |
penceresi
i 1 i5 *
İlaç Bilgileri
Lantus Solostar 100u/ml Subkutan Kullanim İçin En...
Etken Maddesi: Insülin Glarjin
Atc Kodu: A10AE04
Kullanma talimatı ve kısa ürün bilgileri
Google Reklamları
Ana Sayfa | Hakkımızda | İlaçlar | İlaç Ara | İlaç Firmaları | Gizlilik | Bize Ulaşın
Telif Hakkı 2008-2026 © İlaç Prospektüsü. Tüm Hakları Saklıdır.Uyarı: Sitemizde yayınladığımız ilaç bilgileri ile doktora danışmadan kesinlikle ilaç kullanmayınız!
Aksi halde doğabilecek sağlık sorunlarından ilacprospektusu.com sorumlu tutulamaz.