Mictonorm Sr 30 Mg Sürekli Salımlı Kapsül Kısa Ürün BilgisiÜrogenital Sistem ve Cinsiyet Hormonları » Ürolojik İlaçlar » DİĞER ÜROLOJİK ÜRÜNLER » Üriner Antispazmodikler » Propiverin KISA ÜRÜN BİLGİSİ1. BEŞERİ TIBBİ ÜRÜNÜN ADIMICTONORM® SR 30 mg Sürekli Salımlı Kapsül2. KALİTATİF VE KANTİTATİF BİLEŞİM Etkin madde:Her bir kapsül 27.28 mg propiverine eşdeğer 30 mg propiverin hidroklorür içerir.Yardımcı maddeler:Laktoz monohidrat 5.667 mgYardımcı maddeler için 6.1'e bakınız. 3. FARMASÖTİK FORMSürekli salımlı sert jelatin kapsülBeyaz ya da beyazımsı pelletler içeren, turuncu ve beyaz renkte sert jelatin kapsül. 4. KLİNİK ÖZELLİKLER4.1. Terapötik endikasyonlarMICTONORM SR, aşırı aktif mesaneye bağlı ani idrar sıkışması ve sık idrara çıkma ve/veya idrar tutamama problemlerinin semptomatik tedavisinde, endikedir.4.2. Pozoloji ve uygulama şekli Pozoloji/uygulama sıklığı ve süresiÖnerilen günlük dozlar aşağıdaki gibidir:Yetişkinler:Standart bir doz olarak, günde bir kapsül (=30 mg propiverin hidroklorür) tavsiye edilir.Metimazolle kombine halde CYP 3A4'ün potent inhibitörleri olan ilaçlarla eşzamanlıtedavi alan hastalarPotent CYP 3A4/5 inhibitörleriyle metimazol gibi potent FMO inhibitörlerini kombine kullanan hastalarda, tedavi 15 mg/ gün dozu ile başlamalıdır. Doz, daha yüksek bir doza yükseltilebilir. Ancak dikkatli kullanılmalıdır ve klinisyenler, hastaları yan etkiler açısından dikkatlice izlemelidir (bkz. bölüm 4.4, 4.5, 5.2). Uygulama sıklığı ve süresiGünlük bir tane MICTONORM SR Kapsüldür.Uygulama şekliKapsüller oral kullanım içindir. Kapsülleri kırmayınız veya çiğnemeyiniz.Özel popülasyonlara ilişkin ek bilgiler Böbrek yetmezliğiHafif ve orta derecede böbrek yetmezliği olan hastalarda, doz ayarlaması gerekmemektedir (5.2).Karaciğer yetmezliğiHafif karaciğer yetmezliği olan hastalarda doz ayarlaması gerekmemektedir; ancak bu tip hastalara MICTONORM SR verirken dikkatli olunmalıdır. Orta ve ağır karaciğer yetmezliği olan hastalarda ise, bu tip hasta grubunda yeterli veri bulunmadığından, MICTONORM SR kullanımı önerilmemektedir.Pediyatrik popülasyonYeterli veri olmadığından propiverin çocuklarda kullanılmamalıdır.Geriyatrik popülasyonBu yaş grubunda doz ayarlaması gerekmemektedir. Doz yetişkinlerde olduğu gibidir. (Bakınız bölüm 5.2)4.3. KontrendikasyonlarMICTONORM SR, Etkin madde propiverine veya kapsül bileşiminde yer alan yardımcı maddelerden herhangi birine karşı duyarlı olduğu bilinen kişilerde, Bağırsak tıkanması Üriner retansiyon oluşturabilecek önemli derecede mesane çıkış obstrüksiyonu Miyastenia gravis İntestinal atoni Ciddi ülseratif kolit Toksik megakolon Kontrol edilememiş kapalı açılı glokom Orta veya şiddetli karaciğer yetmezliği Taşiartimide, kontrendikedir. 4.4. Özel kullanım uyarıları ve önlemleriPropiverin, otonomik nöropati, ciddi böbrek yetmezliği olan hastalarda dikkatle kullanılmalıdır.Propiverin uygulamasını takiben aşağıda yer alan hastalıkların semptomları ağırlaşabilir; Ciddi konjestif kalp yetmezliği (NYHA Evre IV) Prostat hipertrofisi Reflü özofajiti olan hastalardaki hiatüs hernisi (fıtık) Kardiyak aritmi Taşikardi Diğer antikolinerjik ilaçlarda olduğu gibi propiverin de midriyazise neden olabilir. Bu nedenle, propiverinin, ön kamaradaki açının darlaşabileceği yetişkinlerdeki akut kapalı açılı glokom başlatma riski artabilmektedir. Propiverin ile tedaviye başlamadan önce, böbrek hastalığına ya da konjestif kalp yetmezliğine bağlı pollaküri ve noktüri ve ayrıca organik mesane hastalıkları (örn: idrar yolu enfeksiyonları, malignite) tedavi edilmelidir. Metimazol ile birlikte CYP 3A4'ün güçlü inhibitörlerini alan hastalarda, propiverin ile tedaviye başlandığında, hastalar dikkatle izlenmelidirler. Yiyeceklerin klinik olarak propiverinin farmakokinetiği üzerine etkisi bulunmamaktadır (bkz. bölüm 5.2). Buna bağlı olarak, yiyeceklerle propiverin alımına ilişkin özel bir öneri bulunmamaktadır. Bu tıbbi ürün laktoz içerir. Galaktoz intoleransı, Lapp laktoz yetersizliği veya glukoz galaktoz malabsorbsiyonu gibi nadir kalıtsal problemleri olan hastalar, bu ilacı kullanmamalıdır. 4.5. Diğer tıbbi ürünler ile etkileşimler ve diğer etkileşim şekilleriTrisiklik antidepresanlar (örn: imipramin), trankilizanlar (örn: benzodiazepinler), antikolinerjikler (sistematik uygulandığında), amantadin, nöroleptikler (örn: fenotiyazinler) ve beta-adrenoseptör agonistler (beta-sempatomimetikler) ile birlikte kullanıldığında, propiverinin etkisi artar. Kolinerjik ilaçlarla birlikte kullanıldığında, propiverinin etkisi azalır. İzoniazid ile tedavi edilen hastalara propiverin uygulandığında, kan basıncında azalma görülür. Propiverin, metoklopramid gibi prokinetiklerin etkisini azaltabilir.Propiverin ve sitokrom P450 3A4 (CYP 3A4) ile metabolize olan diğer ilaçlar arasında farmakokinetik etkileşimler görülmüştür. Bununla beraber, propiverinin etkileri klasik enzim inhibitörleriyle (örn: ketokonazol ya da greyfurt suyu) karşılaştırıldığında az olduğundan, bu tip ilaçların konsantrasyonlarında çok belirgin artış beklenmemektedir. Propiverin, sitokrom P450 3A4'ün zayıf bir inhibitörü olarak düşünülebilir. Eş zamanlı olarak, azol antifungallari (örn: ketokonazol, itrakonazol) ya da makrolid antibiyotikler (örn: eritromisin, klaritromisin) gibi güçlü CYP 3A4 inhibitörlerini alan hastalar üzerinde farmakokinetik çalışmalar yapılmamıştır. 4.6. Gebelik ve laktasyon Genel tavsiyeGebelik kategorisi: CGebelik dönemiHamilelerde MICTONORM SR kullanımına ilişkin yeterli veri bulunmamaktadır. Hayvanlar üzerinde yapılan çalışmalar üreme toksisitesi göstermiştir (bkz. bölüm 5.3). İnsanlar için potansiyel risk durumu bilinmemektedir.LaktasyonMICTONORM SR süte geçmektedir. Yeni doğanlar üzerindeki risk göz ardı edilemez.Üreme yeteneği/FertiliteSıçanlarla yapılan toksikolojik çalışmalarda erkek ve dişi fertilitede ve üreme davranışında olumsuz etki gözlenmemiştir.Gebelik sırasında MICTONORM SR kullanımı önerilmemektedir ve emzirme boyunca kullanılmamalıdır. 4.7. Araç ve makine kullanımı üzerindeki etkilerAraç ve makine kullanımı kabiliyeti üzerine herhangi bir çalışma yapılmamıştır. MICTONORM SR ile tedavi edilen hastalarda bulanık görme ve uyuşukluk hali gelişebilir. Bu makine ya da motorlu araç kullanımı ya da tehlikeli işlerde çalışılması gibi mental dikkat gerektiren aktivitelerin yapılma kabiliyetini etkileyebilir.Sedatif ilaçlar, propiverin hidroklorür kullanımına bağlı uyuşukluk durumunu artırıcı etki gösterirler. 4.8. İstenmeyen etkilerPropiverin ile ilişkili olası istenmeyen etkilerin sıklık sıralaması aşağıdaki gibidir:Çok yaygın (>1/10), yaygın (>1/100 ila <1/10); yaygın olmayan (>1/1.000 ila <1/100); seyrek (>1/10.000 ila <1/1.000); çok seyrek (<1/10.000), bilinmiyor (eldeki verilerden hareketle tahmin edilemiyor) Psikiyatrik hastalıklarıÇok seyrek: Huzursuzluk, konfüzyon Bilinmiyor: HalüsinasyonSinir sistemi hastalıklarıYaygın : Baş ağrısıYaygın olmayan : Baş dönmesi, titreme, tat alma duyusunda değişiklikler Göz hastalıklarıYaygın: Anormal akomodasyon, akomodasyon güçlükleri, görüş anormallikleriKardiyak bozuluklarÇok seyrek: ÇarpıntıVasküler bozukluklarYaygın olmayan: Kızarıklık, uyuşukluk hali ile birlikte düşük kan basıncıGastrointestinal hastalıklarıÇok yaygın: Ağızda kurulukYaygın: Karın ağrısı, dispepsi, konstipasyon Yaygın olmayan: Bulantı, kusma Deri ve deri altı doku bozukluklarıSeyrek: Aşırı duyarlılık (propiverine bağlı) veya hassasiyete(yardımcı maddelere bağlı) bağlı döküntüBöbrek ve idrar hastalıklarıYaygın olmayan: İdrar retansiyonuGenel bozukluklar ve uygulama bölgesine ilişkin hastalıklar:Yaygın: Yorgunlukİstenmeyen etkilerin tümü geçicidir ve dozun azaltılması ya da tedavinin sonlandırılmasından sonraki, en fazla 1-4 gün içinde kaybolur. Uzun süreli tedavi esnasında, nadir vakalarda karaciğer enzimlerinde geri dönüşür değişiklikler görüldüğünden, karaciğer enzimleri izlenmelidir. Glokom geliştirme riski taşıyan hastalarda intraoküler basıncın da izlenmesi önerilmektedir. İdrar yolu enfeksiyonlarında, rezidüel idrar hacmine özellikle dikkat edilmelidir. 4.9. Doz aşımı ve tedavisiMuskarinik reseptör antagonisti olan propiverin hidroklorür ile doz aşımı, huzursuzluk, baş dönmesi, vertigo, konuşma ve görme bozuklukları, kas güçsüzlüğü gibi merkezi antikolinerjik etkilere neden olabilir. Bunun yanı sıra, mukozada ciddi kuruluk, taşikardi ve üriner retansiyon da görülebilir.Tedavi semptomatik ve destekleyici olmalıdır. Doz aşımı tedavisi için hasta kusturulmak ya da yağlı tüp kullanılarak gastrik lavaj başlatılmalıdır. Gastrik lavaj uygulanan hastalarda mukoza kuruluğuna dikkat edilmelidir. Bunu takiben hastaya, atropin doz aşımı tedavisinde olduğu gibi yavaş intravenöz enjeksiyon yoluyla, 1.0 -2.0 mg (örn: fizostigmin) içeren semptomatik ve destekleyici tedavi uygulanmalıdır. Destekleyici tedavi gerektiğinde 5 mg'a kadar tekrarlanabilir. 450 mg propiverin hidroklorür almış 14 yaşındaki bir kız çocuğunda konfabulasyon bildirilmiştir. Hasta tamamen iyileşmiştir. 5. FARMAKOLOJİK ÖZELLİKLER5.1. Farmakodinamik özelliklerATC kodu: G04BD06Farmakoterapötik grup: Üriner Antispazmodik Etki MekanizmasıPropiverin kalsiyumun içeri alımını inhibe eder ve muskulotropik spazmolize neden olan mesane düz kas hücrelerinde hücre içi kalsiyumun modülasyonunu engeller. Propiverin antikolinerjik etkiye bağlı olarak pelvik sinirin efferent bağlantısını da inhibe eder.Farmakodinamik etkilerHayvan modellerinde propiverin hidroklorür, intravezikal basınçta doza bağlı azalma ve mesane kapasitesinde artışa neden olur. Bu etki, propiverinin ve ayrıca insan ve hayvan kaynaklı izole detrusor şeritlerde gösterilen üç aktif üriner metabolitinin, farmakolojik özelliklerinin toplamına dayanmaktadır. 5.2. Farmakokinetik özelliklerEtkin maddenin genel özellikleriPropiverin'in hemen hemen tamamı gastrointestinal sistem tarafından emilir.Yoğun bir şekilde ilk geçiş etkisine maruz kalır.İdrar kesesi düz kas hücreleri üzerindeki etkisi, idrar yoluyla vücuttan hızlı bir şekilde atılan üç aktif metabolit ve ana bileşen ile sağlanmaktır. Emilim:MICTONORM SR oral yolla alındıktan sonra, propiverin gastrointestinal sistem tarafından emilir ve 9.9 saat sonra maksimum plazma seviyesine ulaşır. MICTONORM SR'ın ortalama mutlak biyoyararlanımı 60.8± %17.3'tür.(AUC0-aı (po.) / AUC0-» (i.v.) için aritmetik ortalama değeri±SD) Yiyecekler propiverinin farmakokinetiğini etkilemez. Yemeklerden sonraki biyoyararlanım, açlık koşullarıyla karşılaştırıldığında, %99'dur. Sürekli salımlı kapsülün uygulanması, uygulamadan sonraki 9.5 saat içinde propiverinin ortalama Cmax değerinin yaklaşık 70 ng/ml'ye ulaşmasını sağlar. Ana metabolit propiverin-N-oksidin Cmax değeri, yiyeceklerle bir miktar azalır (f=1.26), ancak emilim derecesi değişmez. Propiverin-N-oksit, tüm farmakokinetik parametreler için, kabul aralığında %90 güvenlik aralığı sergilemiştir. Yiyecek alımına göre doz alımı gerekmemektedir. MICTONORM SR'ın besinlerle birlikte alımıyla ilgili olarak bir doz ayarlaması gerekli değildir Dağılım:Uygulamayı takiben, dört ila beş gün sonra, kararlı duruma, tek doz uygulamasına göre daha yüksek konsatrasyonda (Cortalama=71 ng/ml) ulaşılır. Dağılım hacmi, intravenöz propiverin hidroklorür uygulanan 21 sağlıklı gönüllüde, 125 - 473 litre (ortalama 279 litre) olarak belirlenmiştir. Bu, propiverinin yüksek miktarlarda periferal kompartmanlara dağıldığını göstermektedir. Ana bileşen için plazma proteinlerine bağlanma % 90 -95 ve ana metabolit için yaklaşık % 60'dır. 10 sağlıklı gönüllüye MICTONORM SR 30 mg Sürekli Salımlı Kapsül ve MICTONORM SR 45 mg Sürekli Salımlı Kapsül 'ün tek doz uygulanmasının ardından farmakokinetik özellikleri (geometrik ortalama,± SD, aralık)
10 sağlıklı gönüllüye MICTONORM SR 30 mg Sürekli Salımlı Kapsül ve MICTONORM SR 45 mg Sürekli Salımlı Kapsül'ün tek doz uygulanmasının ardından propiverin plazma konsantrasyonları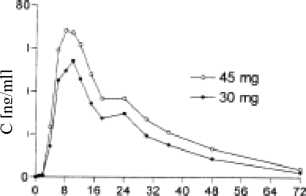 Zaman (saat)
Zaman (saat)MICTONORM SR 45 mg Sürekli Salımlı Kapsül'ün 24 sağlıklı gönüllüye günde bir kez 7 gün süreyle çoklu-doz uygulamasının ardından propiverinin kararlı durum özellikleri:
MICTONORM SR 45 mg Sürekli Salımlı Kapsül'ün 24 sağlıklı gönüllüye günde bir kez 7 gün süreyle çoklu-doz şeklinde uygulanmasının ardından 7. gündeki propiverin plazma konsantrasyonu ve tedavi süresince en düşük seviyeleri:
-2İÛ li> 20 30Zaman (saat) Biyotransformasyon:Propiverin, bağırsak ve karaciğer enzimleri tarafından büyük oranda metabolize edilir. Başlıca metabolik yol, Piperidil-N'in oksidasyonunu içerir. Piperidinil-N'in oksidasyonu, CYP 3A4 ve Flavin-monooksijenaz (FMO) 1 ve 3 ile yürütülür ve bu oksidasyonun sonucunda daha az etkili olan N-oksit oluşur. N-oksitin plazma konsantrasyonu ana metabolitinkinden fazladır. İdrarda dört metabolit belirlenmiştir; bu metabolitlerden üçü farmakolojik olarak aktiftir ve terapötik etkiye katkıda bulunabilir. İn vitro, terapötik plazma konsantrasyonlarını 10- ila 100- kat aşan konsantrasyonlarda oluşan, gözlenebilir hafif bir CYP 3A4 ve CYP 2D6 inhibisyonu olur (bakınız bölüm 4.5). Eliminasyon:Sağlıklı gönüllülere 30 mg 14C-propiverin hidroklorürün oral uygulanımını takiben, 12 gün içinde, radyoaktivitenin %60'ı idrarla ve %21'i dışkı ile atılmıştır. Oral dozun %1'den daha azı idrarda değişmeden atılmıştır. 30 mg'lık tek doz uygulamanın ardından ortalama toplam klerens 371 ml/dakika'dır (191-870 ml/dk). Doğrusallık ve doğrusal olmayan durum10-45 mg propiverin hidroklorürün oral uygulanımını takiben, propiverinin farmakokinetik parametreleri doza bağlı olarak doğrusaldır. Sürekli salımlı propiverinin oral dozu ve sonuç EAAo-k arasındaki korelasyon: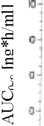 r = &-TO61 0= 423 i- İ7J Q ---¦ ----_ d Sff 20 Jü 4c
Sürekli salımlı propiverinin oral dozu ve sonuç Cmaksr= 0 b 1.72a = A500 Û 10 70 İd 4Ü Doz (mg) Hastalardaki karakteristik özelliklerBöbrek yetmezliği olan hastalarKreatinin klerensi <30 ml/dk olan 12 hasta üzerindeki tek doz çalışmasından elde edilen verilere göre, ciddi böbrek yetmezliği, propiverin ve başlıca metaboliti olan propiverin-N-oksidin atılımını etkilememektedir. Böbrek yetmezliği olan hastalarda, doz ayarlaması gerekmemektedir. Karaciğer yetmezliği olan hastalarKaraciğer yağlanmasına bağlı olarak hafif ila orta derecede karaciğer fonksiyon bozukluğu olan 12 hastanın kararlı durum farmakokinetikleri, 12 sağlıklı gönüllüden oluşan kontrol grubu ile benzer bulunmuştur. Ciddi karaciğer yetmezliği ile ilişkili veri bulunmamaktadır. Pediyatrik hastalarPediyatrik popülasyonda farmakokinetik bilgi mevcut değildir. Geriyatrik hastalarKararlı durumda vadi plazma konsantrasyonları karşılaştırıldığında yaşlı hastalar (6085 yaş; yaş ortalaması 68) ve genç sağlıklı gönüllüler arasında fark görülmemiştir. Ana ilacın metabolite oranı yaşlı hastalarda değişmeden kalmıştır. Bu durum propiverinin ana metaboliti olan propiverin-N-okside metabolik dönüşümünün yaşa bağlı ya da atılımı sınırlandırıcı bir aşama olmadığını göstermektedir. Günde 3 kez uygulanan 15 mg propiverin draje ile günde bir kez uygulanan 45 mg sürekli salımlı propiverin kapsülün biyoeşdeğerliğinin GCP uyumulu bir çalışmada kanıtlanması ile aynı durum 30 mg sürekli salımlı propiverin kapsül için de geçerli sayılabilir. Glokomlu hastalar30 mg sürekli salımlı propiverin kapsül ile tedavi, açık açılı glokomlu hastalarda ve kapalı açılı glokomlu (kontrollü) hastalarda intraoküler basıncın artmasına neden olmamaktadır. Bu durum, 7 gün boyunca günde üç kez 15 mg propiverin kaplı tablet uygulandığı iki plasebo-kontrollü çalışma ile gösterilmiştir. 5.3. Klinik öncesi güvenlilik verileriİki memeli türünde, uzun süreli oral doz çalışmalarında, ana tedaviyle ilişkilendirilmiş etki, karaciğerdeki değişikliklerdir (karaciğer enzimlerinin artması dahil). Bu değişiklikler, karaciğer hipertrofisi ve yağ dejenerasyonu ile karakterizedir. Yağ dejenerasyonu, tedavinin sonlandırılmasına bağlı olarak, geri dönüşümlüdür.Hayvan çalışmalarında, propiverin gebe dişilere yüksek dozlarda uygulandığında, yavrularda iskelet gelişiminde gerileme gözlenmiştir. Emziren memelilerde, propiverin hidroklorür, anne sütüne geçmektedir. Hayvanlar üzerinde yapılan çalışmalarda, mutajenik etki görülmemiştir. Fareler üzerinde yapılan karsinojenite çalışmasında, yüksek doz uygulanan erkek farelerde hepatoselüler adenoma ve karsinom riskinde artış görülmüştür. Sıçanlar üzerinde yapılan karsinojenite çalışmasında, yüksek doz alan erkek sıçanlarda hepatoselüler adenoma, böbrek adenomu ve mesane papillomu görülürken, dişi sıçanlarda yüksek doz seviyelerinde endometriyal stromal polipler artmıştır. Hem sıçanlarda hem de farelerdeki tümörler türe özgü olarak değerlendirilmiştir, bu nedenle bu verinin klinik önemi bulunmamaktadır. 6. FARMASÖTİK ÖZELLİKLER6.1. Yardımcı maddelerin listesiSitrik asit (susuz)Povidon Laktoz monohidrat Talk Trietil sitrat Magnezyum stearat Metakrilik asit-metil metakrilat kopolimeri (1:1) Metakrilik asit-metil metakrilat kopolimeri (1:2) Amonyo metakrilat kopolimeri tip A Amonyo metakrilat kopolimeri tip B Jelatin Titanyum dioksit (E171) Kırmızı demir oksit (E172) Sarı demir oksit (E172) 6.2. GeçimsizliklerBilinen herhangi bir geçimsizliği yoktur.6.3. Raf ömrü36 ay.6.4. Saklamaya yönelik özel tedbirler25 °C'nin altındaki oda sıcaklığında, orijinal ambalajında saklayınız.Işıktan ve nemden koruyunuz. 6.5. Ambalajın niteliği ve içeriğiMICTONORM® 30 mg Sürekli Salımlı Kapsül, 30 kapsül içeren PVC/PVDC alüminyum folyo blisterlerde6.6. Beşeri tıbbi üründen arta kalan maddelerin imhası ve diğer özel önlemlerKullanılmamış olan ürünler ya da atık materyaller Tıbbi Atıkların Kontrolü Yönetmeliği ve Ambalaj ve Ambalaj Atıklarının Kontrolü Yönetmeliğine uygun olarak imha edilmelidir.7. RUHSAT SAHİBİAdı : Recordati İlaç San. ve Tic. A.Ş.Adresi : Doğan Araslı Cad. No: 219 34510 Esenyurt / İSTANBUL Tel : 0212 620 28 50 Fax : 0212 596 20 65 8. RUHSAT NUMARASI252/389. İLK RUHSAT TARİHİ / RUHSAT YENİLEME TARİHİİlk ruhsatlandırma tarihi:Son yenileme tarihi :10. KÜB'ÜN YENİLENME TARİHİ12 / 12 |
İlaç BilgileriMictonorm Sr 30 Mg Sürekli Salımlı KapsülEtken Maddesi: Propiverin Hidroklorür Atc Kodu: G04BD06 Kullanma talimatı ve kısa ürün bilgileri
Google Reklamları
İlgili İlaçlar |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
Ana Sayfa | Hakkımızda | İlaçlar | İlaç Ara | İlaç Firmaları | Gizlilik | Bize Ulaşın
Telif Hakkı 2008-2026 © İlaç Prospektüsü. Tüm Hakları Saklıdır.Uyarı: Sitemizde yayınladığımız ilaç bilgileri ile doktora danışmadan kesinlikle ilaç kullanmayınız!
Aksi halde doğabilecek sağlık sorunlarından ilacprospektusu.com sorumlu tutulamaz.