Neulastim 6 Mg/0,6 Ml Kısa Ürün BilgisiAntineoplastik ve İmmünomodülatör Ajanlar » İmmünostimülanlar » İmmünostimülan İlaçlar » Koloni Stimulan Faktörleri KISA ÜRÜN BİLGİSİ1. BEŞERİ TIBBİ ÜRÜNÜN ADI NEULASTIM 6 mg/0.6 mL S.C. enjeksiyon için kullanıma hazır şırınga Steril 2. KALİTATİF VE KANTİTATİF BİLEŞİM Etkin madde: Bir enjeksiyon için kullanıma hazır şırınga 0.6 mL'de 6 mg pegfilgrastim (10 mg/mL*) içerir. * Yalnızca protein temel alınmıştır. PEG kısmı da dahil edildiğinde konsantrasyon 20 mg/mL olmaktadır. Pegfilgrastim, filgrastim (Rekombinant metiyonil insan G-CSF) ile N-terminal metiyonin kalıntısına kovalen bağla bağlanan 20 kDa polietilen glikol (PEG) molekülünden oluşmaktadır. Filgrastim, E. coliiçerisinde rekombinant DNA teknolojisi ile üretilmektedir.Yardımcı maddeler (0.6 mL başına): Sodyum asetat * : 0.35 mg Sorbitol : 30 mg Sodyum hidroksit: pH ayarı için yeterli miktar içermektedir. * Sodyum asetat glasiyel asetik asidin sodyum hidroksit ile titre edilmesiyle oluşmuştur. Yardımcı maddeler için 6.1'e bakınız. 3. FARMASÖTİK FORM Enjeksiyon için kullanıma hazır şırınga, 0.6 mL. Partikülsüz, berrak çözelti. 4. KLİNİK ÖZELLİKLER 4.1 Terapötik endikasyonlar NEULASTIM, solid tümörlerde sitotoksik kemoterapi sonrasında nötrofil sayısının o 500/mm ve altında olduğu gösterilen hastalarda, daha sonraki kürlerde profilaktik amaçla kullanılır. 4.2 Pozoloji ve uygulama şekli Pozoloji/ uygulama sıklığı ve süresi: NEULASTIM tedavisi yalnızca onkoloji ve/veya hematoloji alanında deneyimli hekimlerle işbirliği içerisinde verilmelidir. Yetişkinler (> 18 yaş): Her kemoterapi kürü için, sitotoksik kemoterapiyi takiben yaklaşık 24 saat sonrasında deri altı enjeksiyon olarak uygulanan bir adet 6 mg NEULASTIM dozu (Tek bir enjeksiyona hazır şırınga) önerilmektedir. Uygulama şekli: Subkutan enjeksiyon yoluyla uygulanır. Özel popülasyonlara ilişkin ek bilgiler: Böbrek/Karaciğer yetmezliği: Böbrek hastalığının son evresi dahil, böbrek yetmezliği olan hastalarda doz değişikliği tavsiye edilmemektedir (Bkz. bölüm 5.2). Pediyatrik popülasyon: NEULASTIM'in çocuklar ve 18 yaş altındaki adolesanlarda kullanımını önermek için yeterli veri mevcut değildir. Geriyatrik popülasyon: Bölüm 5.2'ye bakınız (Farmakokinetik özellikler/Hastalardaki karakteristik özellikler). 4.2 Kontrendikasyonlar Pegfilgrastim, filgrastim, E. colitürevi proteinler veya ilacın içerdiği diğer yardımcı maddelerden herhangi birine karşı aşırı duyarlılığı olduğu bilinen hastalarda NEULASTIM kullanımı kontrendikedir.4.4 Özel kullanım uyarıları ve önlemleri Sınırlı klinik veriler, pegfilgrastim ve filgrastimin ciddi nötropeninin iyileşme süresi üzerindeki etkisinin de novoakut miyeloid lösemili (AML) hastalarda karşılaştırılabilir olduğunu göstermektedir (Bkz. bölüm 5.1). Ancak NEULASTIM'in uzun süreli etkileri AML'de tespit edilmemiştir; bu nedenle bu hasta popülasyonunda dikkatle kullanılmalıdır.Granülosit koloni uyarıcı faktörü, malign hücreler dahil miyeloid hücrelerin büyümesini in vitroin vitrogörülebilir.NEULASTIM'in güvenliliği ve etkinliği, miyelodisplastik sendromlu, kronik miyeloid lösemili hastalarda ve sekonder AML'li hastalarda araştırılmamıştır; bu nedenle bu tür hastalarda kullanılmamalıdır. Kronik miyeloid löseminin blast transformasyon tanısını akut miyeloid lösemiden ayırmaya özen gösterilmelidir. Hücre genetiği t (15;17) ile <55 yaşındaki de novoAML hastalarında NEULASTIM uygulamasının güvenliliği ve etkinliği tespit edilmemiştir.NEULASTIM'in güvenliliği ve etkinliği yüksek doz kemoterapi uygulanmakta olan hastalarda araştırılmamıştır. NEULASTIM, sitotoksik kemoterapinin dozunu artırmak amacıyla, belirlenmiş doz şemaları dışında kullanılmamalıdır. G-CSF uygulaması sonrasında, özellikle interstisiyel pnömoni gibi yaygın olmayan pulmoner advers etkiler bildirilmiştir. Yakın zamanda pulmoner infiltrasyon veya pnömoni geçirmiş olan hastalar daha yüksek bir risk altında bulunabilir (Bkz. bölüm 4.8). Pulmoner infiltrasyona dair radyolojik belirtilerle birliktelik gösteren öksürük, ateş ve dispne gibi pulmoner belirtilerin ortaya çıkması ve artan nötrofil sayısı ile birlikte pulmoner fonksiyonların bozulması Yetişkin Solunum Sıkıntısı Sendromunun (Adult Respiratory Distress Syndrome; ARDS) ön belirtileri olabilir. Bu gibi durumlarda NEULASTIM hekimin takdirine bağlı olarak kesilmeli ve uygun tedavi uygulanmalıdır (Bkz. bölüm 4.8). Pegfilgrastim uygulanması sonrasında, yaygın olmayan fakat genellikle asemptomatik dalak büyümesi vakaları ve bazı vakalarda ölümcül olabilen yaygın olmayan dalak yırtılması vakaları, bildirilmiştir (Bkz. bölüm 4.8). Bu sebeple dalak büyüklüğü dikkatlice izlenmelidir (Örneğin klinik muayene, ultrason). Sol üst batın ağrısı veya omuz ucunda ağrı bildiren hastalar dalak yırtılması açısından değerlendirilmelidir. Tam doz miyelosupresif tedavi planlanan şemaya uygun olarak sürdürüldüğünden, tek başına NEULASTIM ile tedavi, trombositopeni ve aneminin önüne geçmek için yeterli değildir. Düzenli trombosit sayısı ve hematokrit takibi önerilmektedir. Ciddi trombositopeniye sebep oldukları bilinen tek veya kombinasyon halindeki kemoterapötik ajanların uygulanması sırasında özel dikkat gösterilmelidir. Orak hücre krizleri, orak hücre hastalığı bulunan hastalarda pegfilgrastim kullanımıyla ilişkilendirilmiştir (Bkz. bölüm 4.8). Bu sebeple hekimler, orak hücre hastalığı bulunan hastalarda pegfilgrastim kullanırken dikkatli olmalı, uygun klinik parametreleri ve laboratuvar durumunu gözlemlemeli ve NEULASTIM'in dalak büyümesi ve vaso-oklusif krizlerle ilişkili olabileceği konusunda dikkatli olmalıdırlar. NEULASTIM verilen hastaların %1'inden daha azında 100 x 109/l veya daha yüksek akyuvar sayımı gözlenmiştir. Doğrudan bu düzeyde bir lökositoza bağlanabilecek hiçbir advers olay bildirilmemiştir. Akyuvar sayılarındaki bu tür yükselmeler geçici olup, tipik olarak uygulamanın 24 ile 48 saat sonrasında görülmektedir ve bu da NEULASTIM'in farmakodinamik etkileri ile tutarlıdır. NEULASTIM'in klinik etkileri ile tutarlı ve lökositoz için potansiyel olması sebebiyle, tedavi sırasında düzenli aralıklarla akyuvar sayımı yapılmalıdır. Lökosit sayısı beklenen alt seviyenin 50 x 109/L üzerinde ise, NEULASTIM tedavisi derhal kesilmelidir.Eğer ciddi alerjik bir reaksiyon gelişirse, uygun bir tedavi verilmeli ve hasta birkaç gün boyunca yakından izlenmelidir. Ciddi alerjik reaksiyon yaşayan hastalarda NEULASTIM tamamen kesilmelidir (Bkz. bölüm 4.8). Hastalarda ve sağlıklı donörlerde progenitör kan hücrelerinin mobilizasyonunda, NEULASTIM'in güvenliliği ve etkinliği yeterince değerlendirilmemiştir. Büyüme faktörü tedavisine yanıt olarak kemik iliğinin artan hematopoietik etkinliği geçici pozitif kemik görüntüleme değişiklikleriyle ilişkilendirilmiştir. Kemik görüntüleme sonuçları yorumlanırken bu durum dikkate alınmalıdır. NEULASTIM sorbitol içerir. Nadir kalıtımsal früktoz intolerans problemi olan hastaların bu ilacı kullanmamaları gerekir. NEULASTIM her dozunda 1 mmol (23 mg)'dan daha az sodyum ihtiva eder; yani esasında sodyum içermez. 4.5 Diğer tıbbi ürünlerle etkileşimler ve diğer etkileşim şekilleri Hızlı bölünen miyeloid hücrelerin sitotoksik kemoterapiye karşı olan potansiyel duyarlılıkları nedeniyle, NEULASTIM sitotoksik kemoterapi uygulamasından yaklaşık 24 saat sonra uygulanmalıdır. Klinik çalışmalarda, NEULASTIM kemoterapiden 14 gün önce güvenli şekilde uygulanmıştır. NEULASTIM'in herhangi bir kemoterapi ajanı ile eş zamanlı kullanımı hastalarda değerlendirilmemiştir. Hayvan modellerinde NEULASTIM ve 5-florourasil (5-FU) veya diğer antimetabolitlerin eş zamanlı uygulanmasının miyelosupresyonu artırdığı gösterilmiştir. Diğer hematopoietik büyüme faktörleri ve sitokinler ile olası etkileşimler klinik çalışmalarda özel olarak araştırılmamıştır. Kendisi de nötrofil salıverilmesini artıran bir madde olan lityum ile potansiyel etkileşim özel olarak araştırılmamıştır. Böyle bir etkileşimin zararlı olabileceği yolunda hiçbir kanıt yoktur. NEULASTIM'in güvenliliği ve etkinliği nitrozüreler gibi gecikmiş miyelosupresyon ile ilişkili kemoterapi görmekte olan hastalarda değerlendirilmemiştir. Spesifik etkileşim veya metabolizma çalışmaları gerçekleştirilmemiştir, bununla beraber klinik çalışmalar NEULASTIM'in herhangi bir diğer tıbbi ürün ile etkileşimine işaret etmemiştir. Özel popülasyonlara ilişkin ek bilgiler Özel popülasyonlara ilişkin hiçbir etkileşim çalışması yürütülmemiştir. Pediyatrik popülasyon: Pediyatrik popülasyona ilişkin hiçbir etkileşim çalışması yürütülmemiştir. 4.6 Gebelik ve laktasyon Genel tavsiye Gebelik kategorisi: C Çocuk doğurma potansiyeli bulunan kadınlar/ Doğum kontrolü (Kontrasepsiyon) Çocuk doğurma potansiyeli bulunan kadınlarda ve doğum kontrolü (Kontrasepsiyon) uygulayanlarda ilacın kullanımı yönünden bir öneri bulunmamaktadır. Gebelik dönemi Pegfilgrastimin gebe kadınlarda kullanımı ile ilgili yeterli veri mevcut değildir. Hayvanlar üzerinde yapılan çalışmalar üreme toksisitesinin bulunduğunu göstermiştir (Bkz. bölüm 5.3). İnsan embriyosuna veya fötusuna yönelik potansiyel risk bilinmemektedir. Açık olarak gerekli olmadıkça, NEULASTIM gebelik sırasında kullanılmamalıdır. Laktasyon dönemi Emziren kadınlarla ilgili klinik deneyim mevcut değildir, bu nedenle NEULASTIM emziren kadınlara uygulanmamalıdır. Üreme yeteneği/ Fertilite Hayvanlardaki çalışmalar reprodüktif toksisite göstermiştir (Bkz. bölüm 5.3). İnsan embriyosuna ve fetüse olan potansiyel risk bilinmemektedir. 4.6 Araç ve makine kullanımı üzerindeki etkiler Araç ve makine kullanımı üzerine etkileri ile ilgili bir çalışma yapılmamıştır. 4.8 İstenmeyen etkiler İstenmeyen etkiler, aşağıda tanımlanan sıklığa göre listelenmiştir: Çok yaygın (> 1/10); yaygın (> 1/100 ila <1/10); yaygın olmayan (> 1/1,000 ila <1/100); seyrek (> 1/10,000 ila <1/1,000); çok seyrek (< 1/10,000); bilinmiyor (Eldeki verilerden hareketle tahmin edilemiyor). Güvenlilik profilinin özeti En sık bildirilen advers olay kemik ağrısı (Çok yaygın) ve kas-iskelet sistemi ağrısıdır (Çok yaygın). Kemik ağrısı genel olarak hafif-orta şiddette, geçici olmuş ve çoğu hastada standart ağrı kesicilerle kontrol altına alınabilmiştir. NEULASTIM'in ilk veya takip eden tedavisi sırasında, deri döküntüsü, ürtiker, anjiyoödem, dispne, eritem, yüzde kızarıklık ve hipotansiyonu içeren hipersensitivite reaksiyonları bildirilmiştir (Yaygın olmayan sıklıkta). NEULASTIM kullanan hastalarda anafilaksiyi içeren ciddi alerjik reaksiyonlar meydana gelebilir (yaygın olmayan sıklıkta) (Bkz. bölüm 4.4). Yaygın olmayan sıklıkta, genellikle asemptomatik, splenomegali vakaları bildirilmiştir (Bkz. bölüm 4.4). Pegfilgrastim uygulaması sonrasında bazıları ölümcül olabilen dalak yırtılması vakaları yaygın olmayan sıklıkta bildirilmiştir (Bkz. bölüm 4.4). İnterstisyel pnömoni, pulmoner ödem, pulmoner infiltratlar ve pulmoner fibrozisi içeren pulmoner advers olaylar yaygın olmayan sıklıkta bildirilmiştir. Yaygın olmayan sıklıkta, bu vakaların bazıları, ölümcül olabilen erişkin respiratuvar distres sendromu (ARDS) veya solunum yetmezliği ile sonuçlanmıştır (Bkz. bölüm 4.4). Orak hücre hastalığı bulunan hastalarda izole orak hücre krizleri bildirilmiştir (Orak hücre hastalarında yaygın olmayan sıklıkta) (Bkz. bölüm 4.4). Advers reaksiyonların özeti Aşağıdaki veriler, klinik çalışmalardan alınan ve spontan raporlama yoluyla bildirilen advers reaksiyonları tanımlamaktadır. Her bir sıklık gruplandırmasında, istenmeyen etkiler azalan ciddiyet sıralamasına göre sunulmuşlardır. Kan ve lenf sistemi hastalıkları Yaygın: Trombositopeni1. Yaygın olmayan: Orak hücre krizi2, lökositoz1. Bağışıklık sistemi hastalıkları Yaygın olmayan: Hipersensitivite reaksiyonları, anafilaksi. Metabolizma ve beslenme hastalıkları Yaygın olmayan: Ürik asit seviyelerinde yükselme. Sinir sistemi hastalıkları Çok yaygın: Baş ağrısı. Solunum, göğüs bozuklukları ve mediastinal hastalıkları Yaygın olmayan: Erişkin respiratuvar distres sendromu (ARDS)2, pulmoner advers olaylar (İnterstisyel pnömoni, pulmoner ödem, pulmoner infiltratlar ve pulmoner fibrozis). Gastrointestinal bozukluklar Çok yaygın: Bulantı. 2 2 Yaygın olmayan: Dalak büyümesi , dalak yırtılması . Deri ve deri altı doku ile ilgili bozukluklar 12 12 Yaygın olmayan: Sweet sendromu (Akut febril dermatoz) , , kütanöz vaskülit ' . Kas-iskelet bozuklukları, bağ dokusu ve kemik hastalıkları Çok yaygın: Kemik ağrısı, kas-iskelet ağrısı (Miyalji, artralji, ekstremitelerde ağrı, sırt ağrısı, kas-iskelet ağrısı, boyun ağrısı). Genel bozukluklar ve uygulama bölgesine ilişkin hastalıklar Yaygın: Enjeksiyon bölgesinde reaksiyon (Enjeksiyon bölgesinde ağrıyı da içerir). Yaygın olmayan: Göğüs ağrısı (Kalple ilişkisi olmayan). Araştırmalar Yaygın olmayan: Laktat dehidrojenaz ve alkalin fosfataz seviyelerinde yükselme1, ALT veya AST'nin karaciğer fonksiyon testlerinde geçici yükselme1. 1 Seçilmiş advers reaksiyonlarla ilgili bölüme bakınız 2 Bu advers reaksiyon pazarlama sonrası izleme çalışmalarında tespit edilmiş ancak pazarlama onayını destekleyen ve yetişkinlerde yapılmış olan randomize, kontrollü klinik çalışmalarda gözlemlenmemiştir. Sıklık kategorisi, yedi adet randomize klinik çalışmadaki NEULASTIM kullanan 932 hastadan elde edilen verilerin istatistiksel hesaplaması yoluyla tayin edilmiştir. Seçilmiş advers olaylar hakkında bilgilendirme Yaygın olmayan sıklıkta Sweet sendromu vakaları bildirilmiştir. Bu vakaların bazılarında hematolojik malignansilerin rolünün olabileceği düşünülmektedir. NEULASTIM ile tedavi edilen hastalarda yaygın olmayan sıklıkta kütanöz vaskülit vakaları bildirilmiştir. NEULASTIM kullanan hastalarda vaskülitin mekanizması bilinmemektedir. NEULASTIM'in ilk veya takip eden tedavilerinde, yaygın sıklıkta, enjeksiyon bölgesinde ağrı ve enjeksiyon bölgesinde eritemi içeren enjeksiyon bölgesi reaksiyonları meydana gelmiştir. Yaygın olmayan sıklıkta lökositoz ( [WBC]> 100x109/l) bildirilmiştir. Sitotoksik kemoterapi sonrasında, NEULASTIM verilen hastalarda, ürik asit ve alkalin fosfataz düzeylerinde, klinik etkisi olmayan, geri dönüşlü, yaygın olmayan oranda, hafif ile orta düzeylerde yükselmeler; laktat dehidrojenaz düzeylerinde klinik etkisi olmayan, geri dönüşlü, yaygın olmayan, hafif ile orta düzeylerde yükselmeler ortaya çıkmıştır. Kemoterapi alan hastalarda, çok yaygın sıklıkta bulantı ve baş ağrısı gözlemlenmiştir. Sitotoksik kemoterapi sonrası pegfilgrastim alan hastalarda, karaciğer fonksiyon testlerinden ALT (Alanin aminotransferaz) veya AST'de (Aspartat aminotrasferaz) yaygın olmayan sıklıkta yükselmeler gözlemlenmiştir. Bu yükselmeler geçici olmuş ve sonradan başlangıç seviyesine dönmüştür. Yaygın trombositopeni vakaları bildirilmiştir. Pediyatrik popülasyon Çocuklardaki deneyim sınırlıdır. 0-5 yaş arası çocuklarda (%92), 6-11 ve 12-21 yaşındaki çocuklara (Sırasıyla %80 ve %67) ve yetişkinlere kıyasla daha yüksek sıklıkta ciddi advers reaksiyon gözlemlenmiştir. Bildirilen en sık advers reaksiyon kemik ağrısıdır (Bkz. bölüm 5.1 ve 5.2). 4.9 Doz aşımı ve tedavisi Sınırlı sayıda sağlıklı gönüllüye ve küçük hücreli dışı akciğer kanseri hastalarına 300 mikrogram/kg'lik tek dozlar, ciddi advers etkiler görülmeden verilmiştir. Advers olaylar, daha düşük dozda pegfilgrastim alan hasta veya sağlıklı gönüllülerde görülenlere benzer düzeyde seyretmiştir. 5. FARMAKOLOJİK ÖZELLİKLER 5.1 Farmakodinamik özellikler Farmakoterapötik grubu: Hematopoietik büyüme faktörü/ Sitokinler ATC kodu: L03AA13 Etki mekanizması İnsan granülosit koloni stimülan faktörü (G-CSF) kemik iliğinde nötrofil oluşumu ve salıverilmesini düzenleyen bir glikoproteindir. Pegfilgrastim rekombinant G-CSF'nin (r-metHuG-CSF) tek 20 kDa polietilen glikol (PEG) moleküllü kovalent bileşiğidir. Pegfilgrastim azalmış renal klerens nedeniyle filgrastimin uzun etki süreli bir formudur. Lökosit sayımındaki artış (Lökositoz), pegfilgrastim uygulamasının beklenen bir sonucudur. Doğrudan lökositozla ilişkilendirilebilecek bir advers olay bildirilmemiştir. Lökosit sayımındaki artış geçicidir ve pegfilgrastimin farmakodinamik etkileriyle tutarlıdır. Pegfilgrastim ve filgrastimin, monositler ve/veya lenfositlerde minör yükselmelerle birlikte periferik kan nötrofil sayılarında 24 saat içinde belirgin bir artışa neden olan, aynı etki tarzına sahip oldukları gösterilmiştir. Kemotaktik ve fagositik fonksiyon testleri ile gösterildiği üzere, pegfilgrastime yanıt olarak üretilen nötrofiller, filgrastime benzer şekilde normal veya artmış fonksiyon göstermektedir. Diğer hematopoietik büyüme faktörleri ile olduğu gibi, G-CSF'nin insan endotelyel hücreleri üzerine in vitro stimülan özellikleri gösterilmiştir. Klinik etkinlik ve güvenlilik Doksorubisin ve dosetakselden oluşan miyelosupresif kemoterapi uygulanmakta olan yüksek riskli evre II-IV meme kanserli hastalarda gerçekleştirilen iki randomize, çift-kör pivotal çalışmada her kür başına tek doz olarak pegfilgrastim kullanılması, günlük filgrastim uygulamaları (Ortanca değeri olarak 11 günlük uygulama) ile gözlenene benzer şekilde, nötropeni süresini ve febril nötropeni görülme sıklığını düşürmüştür. Büyüme faktörü desteği verilmediğinde, bu rejimin ortalama 5 ile 7 gün arasında evre 4 nötropeni süresine ve %30-40 febril nötropeni görülme sıklığına neden olduğu bildirilmiştir.6 mg sabit doz pegfilgrastim kullanılan ilk çalışmada (n= 157), evre 4 nötropeni ortalama süresi pegfilgrastim grubunda 1.8 gün olurken, filgrastim grubunda 1.6 gün olmuştur (Fark 0.23 gün, %95 GA -0.15, 0.63). Tüm çalışma boyunca febril nötropeni oranı pegfilgrastimle tedavi edilen hastalarda %13 olurken, filgrastimle tedavi edilen hastalarda % 20 olmuştur (Fark - %7, %95 GA -%19, %5).Vücut ağırlığına göre ayarlanmış (100 mikrogram/kg) doz kullanılan ikinci bir çalışmada (n= 310), evre 4 nötropeni ortalama süresi pegfilgrastim grubunda 1.7 gün, filgrastim grubunda 1.8 gün olmuştur (Fark 0.03 gün, %95 GA -0.36, 0.30). Genel febril nötropeni oranı pegfilgrastimle tedavi edilen hastalarda % 9 ve filgrastimle tedavi edilen hastalarda % 18 olmuştur (fark - %9, %95 GA -%16.8, -%1.1). Plasebo kontrollü bir çalışmada pegfilgrastimin febril nötropeni sıklığı üzerindeki etkisi, %10-20'lik bir febril nötropeni oranıyla ilişkili olduğu bildirilen bir kemoterapi rejiminin (4 kür boyunca her 3 haftada bir 100mg/m2 dosetaksel) uygulanmasından sonra değerlendirilmiştir. Bu çalışmada 928 hasta her siklusta kemoterapiden yaklaşık 24 saat (Yani Gün 2'de) sonra tek bir doz pegfilgrastim veya plasebo almak üzere randomize edilmiştir. Febril nötropeni sıklığı, plaseboyla karşılaştırıldığında pegfilgrastim almak üzere randomize edilen hastalarda önemli ölçüde düşüktür (Sırasıyla %17'ye karşılık %1, p<0.001). Febril nötropeni klinik tanısıyla ilişkili hastaneye yatma ve IV anti-infektif kullanımı sıklığı, pegfilgrastim grubunda plasebo grubuyla karşılaştırıldığında önemli ölçüde düşüktür (Sırasıyla %1'e karşılık %14, p<0.001 ve %2'ye karşılık %10, p<0.001). De novoakut miyeloid lösemi için kemoterapi alan hastalarda yapılan küçük bir (n=83), Faz II, randomize, çift kör çalışmada, pegfilgrastim (Tek doz 6 mg) indüksiyon kemoterapisi sırasında verilen filgrastimle karşılaştırılmıştır. Ciddi nötropeniden ortanca iyileşme süresinin her iki tedavi grubunda 22 gün olduğu tahmin edilmiştir. Uzun süreli sonuç çalışılmamıştır (Bkz. bölüm 4.4)5.2 Farmakokinetik özellikler Genel özellikler Emilim:Tek bir deri altı pegfilgrastim dozu sonrasında, pegfilgrastim doruk serum konsantras yonu doz uygulamasının 16 ile 120 saat sonrasında ortaya çıkar. Dağılım:Pegfilgrastim serum konsantrasyonları miyelosupresif kemoterapi sonrasındaki nötropeni dönemi boyunca korunur. Pegfilgrastim dağılımı plazma kompartmanı ile sınırlıdır. Biyotransformasyon:Veri yoktur. Eliminasyon:Pegfilgrastimin eliminasyonu doz açısından non-lineerdir: pegfilgrastimin serum klerensi doz arttıkça düşer. Pegfilgrastim başlıca olarak, yüksek dozlarda doyuma ulaşan, nötrofil aracılı klerens ile (> %99) atılmaktadır. Kendini-düzenleyici bir klerens mekanizması ile tutarlı olarak, pegfilgrastim serum konsantrasyonu nötrofil tablosunda düzelmenin ortaya çıkması ile birlikte hızla düşer (Bkz. Şekil 1). Doğrusallık/ Doğrusal Olmayan Durum:Pegfilgrastimin eliminasyonu doz açısından non-lineerdir. Şekil 1. Kemoterapi ile tedavi edilen hastalarda tek 6 mg enjeksiyonu sonrasında ortanca pegfilgrastim serum konsantrasyonu ve mutlak nötrofil sayısı (MNS) profili
F 100
100 - 10 - 1 1 0.1 J 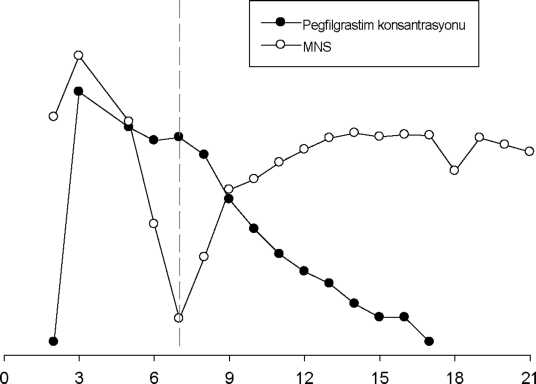 r 10
r 10r 1 L 0.1 Çalışma Günü
E ^5/
X VÖ o .c (f>02 oo£ ro o c (ü nO
c ro -e O Hastalardaki karakteristik özellikler Böbrek/Karaciğer yetmezliği:Nötrofil aracılı klerens mekanizmasına bağlı olarak, pegfilgrastimin farmakokinetiğinin böbrek veya karaciğer bozukluğu tarafından etkilenmesi beklenmez. Pediyatrik popülasyon:NEULASTİM'in güvenliliği ve farmakokinetiği sarkoma hastası olan 37 pediyatrik hastada çalışılmıştır. NEULASTIM'in 100 mikrogram/kg subkutan uygulaması sonrasında elde edilen sistemik maruziyet (EAA0-inf, ortalama ± Standart Sapma) 6-11 yaş grubunda (n=10) 22.0 (±13.1) mikrogram.saat/mL, 12-21 yaş grubunda (n=13) 29.3 (±23.2) mikrogram.saat/mL ve en genç yaş grubunda (0-5 yaş, n=11) 47.9 (±22.5) mikrogram.saat/mL olmuştur. İlgili yaş gruplarına karşılık gelen terminal yarılanma ömrü sırasıyla 20.2 (±11.3), 21.2 (±16.0) ve 30.1 (±38.2) saat olmuştur. En yaygın advers olay yetişkinlerde olduğu gibi kemik ağrısı olmuştur (Bkz. bölüm 4.8 ve bölüm 4.5). Geriyatrik popülasyon:Sınırlı veriler, yaşlı hastalardaki (>65 yaş) pegfilgrastim farmakokinetiğinin erişkinlerdeki ile benzer olduğunu göstermiştir. 5.3 Klinik öncesi güvenlilik verileri Karsinojenisite: Belli malign hücrelerin, granülosit koloni uyarıcı faktör (G-CSF) reseptörlerini ifade ettiği gösterilmiştir. Pegfilgrastimin herhangi bir tümör tipi için büyüme faktörü olarak etki etme olasılığı göz ardı edilemez. Pegfilgrastimin karsinojenitik potansiyeli uzun süreli hayvan çalışmalarında değerlendirilmemiştir. Haftada bir 1000 mcg/kg'a (İnsan için önerilen dozdan yaklaşık 23 kat fazla) kadar pegfilgrastimden oluşan subkutan enjeksiyon verilen sıçanlarda yapılan 6 aylık bir toksisite çalışmasında, prekanseröz veya kanseröz lezyon görülmemiştir. Mutajenisite: Mutajenisite çalışmaları yapılmamıştır. Teratojenisite: Subkutan olarak pegfilgrastim verilen gebe sıçanların yavrularında advers etki gözlenmemiştir ancak tavşanlarda pegfilgrastimin düşük subkutan dozlarda embriyo/fetal toksisiteye (Embriyo kaybı) yol açtığı gösterilmiştir. Sıçanlarla yapılan çalışmalarda pegfilgrastimin plasentayı geçebileceği gösterilmiştir. Bu bulguların insanlar açısından ilgisi bilinmemektedir. Diğer: Tekrarlayan doz toksisitesiyle ilgili geleneksel çalışmalardan alınan preklinik veriler, lökosit sayımında artışlar, kemik iliğinde miyeloid hiperplazi, ekstramedüler hematopoez ve dalak büyümesi dahil beklenen farmakolojik etkiler göstermiştir. 6. FARMASÖTİK ÖZELLİKLER 6.1 Yardımcı maddelerin listesi Sodyum asetat* Sorbitol Polisorbat 20 Enjeksiyonluk su Sodyum hidroksit (pH 4'e ayarlamak için yeter miktar kullanılabilir) *: Sodyum asetat, glasiyal asetik asidin sodyum hidroksit ile titre edilmesiyle elde edilmiştir. 6.2 Geçimsizlikler NEULASTIM sodyum klorür solüsyonları ile geçimsizdir. 6.3 Raf ömrü 36 ay. 6.4 Saklamaya yönelik özel tedbirler 2-8 °C'de (Buzdolabında) saklayınız. Dondurmayınız. NEULASTIM steril ancak koruyucu içermeyen bir çözeltidir. Işıktan korumak için ilacı orijinal ambalajında muhafaza ediniz. 6.5 Ambalajın niteliği ve içeriği NEULASTIM 6 mg/0.6 mL S.C. enjeksiyon için kullanıma hazır şırınga, 1 adet. Paslanmaz çelik bir iğnesi olan, Tip I kalite camdan üretilmiş, 0.6 mL tek kullanımlık enjeksiyona hazır şırınga. NEULASTIM enjeksiyon için kullanıma hazır şırınga bir defalık kullanım içindir. 6.6 Beşeri tıbbi üründen arta kalan maddelerin imhası ve diğer özel önlemler Kullanmadan önce, NEULASTIM çözeltisi gözle görünen partiküller açısından incelenmelidir. Sadece berrak ve renksiz olan çözelti enjekte edilmelidir. Aşırı çalkalama, pegfilgrastimi topaklaştırarark biyolojik olarak inaktif hale çevirebilir. Enjeksiyon öncesinde enjeksiyona hazır şırınganın oda sıcaklığına ulaşmasına izin verilmelidir. Farmasötik ürünlerin çevreye bırakılmasından kaçınılmalıdır. İlaçlar, atık suları ve evsel atık ile imha edilmemelidir. Varsa bulunduğunuz yerdeki donanımlı atık toplama sistemlerini kullanınız. Kullanılmamış olan ürünler ya da atık materyaller Tıbbi Atıkların Kontrolü Yönetmeliği ve Ambalaj ve Ambalaj Atıklarının Kontrolü Yönetmeliği'ne uygun olarak imha edilmelidir. 7. RUHSAT SAHİBİ Roche Müstahzarları Sanayi Anonim Şirketi, Eski Büyükdere Caddesi, No: 13, 34398 Maslak, İstanbul Tel: (0 212) 366 90 00 Faks: (0 212) 285 22 00 8. RUHSAT NUMARASI 136/57 9. İLK RUHSAT TARİHİ/RUHSAT YENİLEME TARİHİ İlk ruhsat tarihi: 06.09.2013 Ruhsat yenileme tarihi: 10. KÜB'ÜN YENİLENME TA RİHİ12/12 |
İlaç BilgileriNeulastim 6 Mg/0,6 MlEtken Maddesi: Pegfilgrastim Atc Kodu: L03AA13 Kullanma talimatı ve kısa ürün bilgileri
Google Reklamları
|
Ana Sayfa | Hakkımızda | İlaçlar | İlaç Ara | İlaç Firmaları | Gizlilik | Bize Ulaşın
Telif Hakkı 2008-2026 © İlaç Prospektüsü. Tüm Hakları Saklıdır.Uyarı: Sitemizde yayınladığımız ilaç bilgileri ile doktora danışmadan kesinlikle ilaç kullanmayınız!
Aksi halde doğabilecek sağlık sorunlarından ilacprospektusu.com sorumlu tutulamaz.