Anbinex 500iu İnfüzyon İçin Liyofilize Toz İçeren Flakon Kısa Ürün BilgisiKan ve Kan Yapıcı Organlar » Antitrombotikler » Antitrombotik İlaçlar » Heparin » Antitrombin III KISA ÜRÜN BİLGİSİ1. BEŞERİ TIBBİ ÜRÜNÜN ADIANBINEX 500 I.U. IV infiizyon için liyofılize toz içeren flakon2. KALİTATİF VE KANTİTATİF BİLEŞİM Etkin madde:Her flakonda; 500 I.U. insan plazmasından elde edilen antitrombin içeren infiizyon için liyofılize toz bulunur.İlaç, 10 mL enjeksiyonluk suda çözüldükten sonra, yaklaşık olarak 500 I.U/10 mL insan plazmasından elde edilen antitrombin içerir. Potens I.U. olarak, Avrupa Farmakopesi'ndeki kromojenik tayin metodu ile saptanır. ANBINEX'in spesifik aktivitesi en az 5 I.U./mg protein'dir. Yardımcı maddeler:ANBINEX 500 I.U., 10 mL'de (enjektör) 1.45 mmol (33.35 mg) sodyum içerir.Yardımcı maddeler için 6.1'e bakınız. 3. FARMASÖTİK FORMİnfüzyon için liyofılize toz.Beyaz renkli, nem çekici, akışkan katı veya toz içeren renksiz cam flakon ve enjeksiyonluk su içeren enjektör. 4. KLİNİK ÖZELLİKLER4.1. Terapötik endikasyonlar-Kalıtımsal antitrombin eksikliği olan hastalarda:a) Klinik risk durumlarında (özellikle cerrahi ve peri-partum dönemi süresince) derin ven trombozu ve tromboembolinin profilaksisinde, eğer endike ise heparinle birlikte. b) Derin ven trombozu ve tromboembolinin ilerlemesinin önlenmesinde, eğer endike ise heparinle birlikte. -Sonradan edinilmiş antitrombin eksikliğinde. 4.2. Pozoloji ve uygulama şekliANBINEX'le tedavi, antitrombin eksikliği olan hastaların tedavisinde deneyimli bir doktorun denetimi altında başlatılmalıdır.Pozoloji/Uygulama sıklığı ve süresi:Kalıtımsal eksikliği olan hastalarda uygulanacak ilaç miktarı ve uygulamanın sıklığı, tromboembolik olaylar, güncel klinik risk faktörleri ve laboratuvar değerlerine göre hastanın ihtiyacı doğrultusunda tayin edilmelidir.Sonradan edinilmiş antitrombin eksikliğinin substitüsyon tedavisinin dozu ve süresi; plazma antitrombin düzeyine, artan tumover belirtilerinin durumuna, asıl hastalığa ve klinik şartın ciddiyetine bağlıdır. Uygulanacak miktar ve uygulama sıklığı, hastanın ihtiyacına göre, klinik etkinlik ve laboratuvar değerleri bazında olmalıdır. Uygulanan antitrombin'in ünite sayısı, antitrombin için geçerli DSÖ standardı doğrultusunda uluslararası ünite (I.U) ile ifade edilir. Plazmadaki antitrombin aktivitesi %olarak (normal insan plazması ile ilgili olarak) ya da uluslararası ünite ile (plazmadaki antitrombin için uluslar arası standardla ilgili olarak) tanımlanır.Antitrombin aktivitesinin 1 I.U.'si, normal insan plazmasının 1 mL'si içindeki antitrombin miktarına eşdeğerdir. Antitrombin'in gerekli dozu; vücut ağırlığının kg'ı başına 1 I.U. antitrombin'in, plazma antitrombin aktivitesini yaklaşık olarak % 1.1-% 1.6 yükseltmesi bazında hesaplanır. Başlangıç dozu aşağıdaki formül kullanılarak hesaplanır: Gerekli ünite = Vücut ağırlığı (kg) x (100- bazal antitrombin aktivitesi (%)) x 0.8Antitrombin aktivitesinin başlangıç hedefi klinik duruma bağlıdır. Antitrombin substitüsyonunun endikasyonu belirlendiği zaman, doz, hedef antitrombin aktivitesine ulaşılmasında ve etkili düzeyin sürdürülmesinde yeterli olmalıdır. ANBINEX'in dozu, antitrombin aktivitesinin laboratuvar ölçümlerine göre tayin edilir. Ölçümler, hastanın durumu kararlılık gösterinceye kadar günde 2 defa yapılmalı ve daha sonra günde bir defa ve sonraki infuzyondan hemen önce gerçekleştirilmelidir. Dozun düzeltilmesi, laboratuvar kontrollerine ve klinik gidişata göre artan antitrombin tumoverinin her iki belirtisi dikkate alınarak yapılır. Klinik özellikler farklı bir efektif düzeyi belirtmiyorsa, tedavi süresince antitrombin aktivitesinin % 80'in üzerinde olması sağlanmalıdır.Kalıtımsal eksikliği olan hastalarda mutad başlangıç dozu 30-50 IU/kg olmalıdır. Daha sonra, tedavi süresine ek olarak, uygulama sıklığı ve süresi, hastanın biyolojik verileri ve klinik durumuna göre ayarlanmalıdır. Uygulama şekli:Çözeltinin hazırlanma şekli 4.4'te belirtilmiştir. Ürün i.v. infüzyon şeklinde uygulanmalıdır. Uygulama hızı 0.08 mL/kg/dk'yı aşmamalıdır.Özel popülasyonlara ilişkin ek bilgiler Böbrek/ Karaciğer yetmezliği:Böbrek/karaciğer yetmezliği olan insanlar için hiçbir veri mevcut değildir. ANBINEX, eğer sadece tıbbi karara göre açıkça belirtildiyse hastalara uygulanmalıdır.Pediyatrik popülasyon:6 yaş ve altındaki çocuklarda kullanımı, güvenlik ve etkinlik için eldeki verilerin yeterli olmaması nedeniyle önerilmemektedir.Geriyatrik popülasyon:Yaşlı hastalar için herhangi bir veri mevcut değildir. ANBINEX, yaşlı hastalarda sadece tıbbi karara göre mutlak endike ise kullanılmalıdır.4.3. KontrendikasyonlarEtken maddeye ya da yardımcı maddelerden herhangi birisine karşı aşırı duyarlılığı olanlarda kontrendikedir.4.4. Özel kullanım uyarıları ve önlemleri Virüs güvenliğiANBINEX, insan plazmasından elde edilmektedir. İnsan plazmasından elde edilen ilaçlar, virüsler ve teorik olarak Varyant Creutzfeldt-Jacob (v-CJD) gibi, çeşitli hastalıklara yol açabilen enfeksiyon yapıcı ajanlar içerebilirler. ANBINEX'de Varyant Creutzfeldt-Jacob hastalığının bulaşma riski teorik olarak minimumken, klasik Creutzfeldt-Jacob hastalığının bulaşma riski hiçbir kanıtla desteklenmez. Alınan önlemlere rağmen, bu tür ürünler halen potansiyel olarak hastalık bulaştırabilir.Bu tip ürünlerin enfeksiyon yapıcı ajanları bulaştırma riski, plazma verenlerin belirli virüslere önceden maruz kalıp kalmadığının izlenmesi, belirli virüs enfeksiyonlarının halihazırda varlığının test edilmesi ve belirli virüslerin yok edilmesi ve/veya inaktivasyonu ile azaltılmıştır. Bütün bu önlemlere rağmen, bu ürünler hala potansiyel olarak hastalık bulaştırabilirler. Ayrıca, henüz bilinmeyen enfeksiyon yapıcı ajanların bu ürünlerin içersinde bulunma ihtimali mevcuttur.HIV, HBV, HCV gibi zarflı virüsler ve HAV gibi zarflı olmayan virüsler için etkili önlemlerin alınmasına dikkat edilmelidir. Parvovirüs B19 gibi zarflı olmayan virüslere karşı alınan tedbirler sınırlı sayıda olabilir. Parvovirüs B19 enfeksiyonu, gebelikte (fetal infeksiyon) ve immün yetmezlik ya da kırmızı kan hücre üretiminde artış olan hastalarda tehlikeli olabilir (hemolitik anemi gibi).Doktor, bu ilacı hastaya reçete etmeden veya uygulamadan önce hastası ile risk veyararlarını tartışmalıdır.__İntravenöz protein ürünleri uygulamalarında alerjik tipte aşırı duyarlılık reaksiyonları olasıdır. İnfuzyon periyodu süresince hastalar yakından gözlenmeli ve herhangi bir semptom varlığı dikkatle izlenmelidir. Hastalar; kurdeşen, yaygın ürtiker, göğüs daralması, hışırtılı solunum, hipotansiyon ve anaflaksi gibi aşırı duyarlılık reaksiyonlarının erken belirtileri konusunda bilgilendirilmelidir. ANBINEX uygulamasından sonra bu semptomların oluşması halinde doktora başvurulmalıdır.Şok oluşumu halinde standart tıbbi tedavi uygulanmalıdır. ANBINEX bir hastaya uygulandığı zaman, hasta ve ürünün seri numarası arasındaki bağı oluşturmak için, ürünün adı ve parti numarasının kaydedilmesi önemle tavsiye edilmektedir. İnsan plazmasından elde edilen antitrombin ürünlerinin düzenli olarak uygulandığı hastaların hepatit A ve B'ye karşı aşılanmaları önerilmektedir. Antitrombin, heparinle birlikte kullanıldığı zaman, klinik ve biyolojik olarak gözetimi: -Heparin dozunu ayarlamak ve aşırı hipokoagülabiliteden kaçınmak için, antikoagülasyon düzeyinin kontrolleri (APPT ve uygun anti-FXa aktivitesi), yakın aralıklarla ve özellikle antitrombin kullanımının başlangıcını izleyen ilk dakikalarda/saatlerde, düzenli olarak uygulanmalıdır. -Fraksiyonlanmamış heparinle uzayan tedavinin sonucunda antitrombin düzeylerinin azalma riski nedeniyle, bireysel dozların ayarlanması için antitrombin düzeylerinin günlük ölçümü yapılmalıdır. ANBINEX 500 I.U., 10 mL'de (enjektör) 1.45 mmol (33.35 mg) sodyum içerir. Kontrollü sodyum diyetinde olan hastalar tarafından dikkat edilmelidir. Çözeltinin hazırlanması:1- Flakon ve enjektör 30°C'ın üzerine çıkmayacak şekilde ısıtılır. 2- Çözücüyü içeren enjektöre piston yerleştirilir. 3- Filtre ambalajdan çıkartılır. Enjektör başlığı çıkartılır ve enjektör filtreye tutturulur. 4- Flakon adaptörü ambalajından çıkartılır, enjektör ve filtreye tutturulur. 5- Flakonun başlığı çıkartılır ve kauçuk tıpanın yüzeyi bir antiseptik ile silinir. 6- Adaptör iğnesi ile tıpa delinir. 7- Tüm çözücü enjektörden fiakona aktarılır. 8- Toz tümüyle çözününceye kadar flakon hafifçe çalkalanır. 9- Enjektör/filtre, flakon/adaptörden ayrılır. Piston, çözeltinin toplam hacmine benzer hacimdeki havayı çekmek için geri çekilir. Enjektör/filtre, flakon/adaptör ile birleştirilir. 10- Flakon ters çevrilir ve çözeltinin enjektöre geçmesi sağlanır. 11- Enjektör ayrılır ve solüsyon yavaşça i.v. yolla uygulanmaya başlanır. Akış hızı 0.08 mL/kg/dk'yı geçmemelidir. Rekonstitüe çözelti uygulamadan önce yabancı partikül ve/veya renklenme açısından gözle incelenmelidir. Çözelti berrak ya da hafif opelesan olmalıdır. Bulanık veya çökelti içeren çözeltiler kullanılmamalıdır. Uygulamadan artakalan çözelti atılmalıdır. Uygulama seti tekrar kullanılmamalıdır. 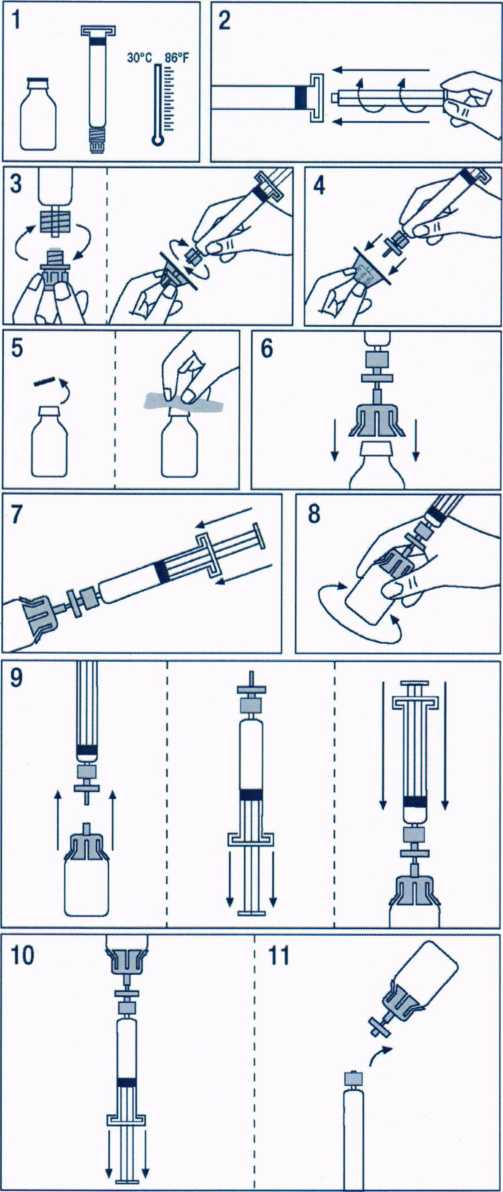
4.5. Diğer tıbbi ürünler ile etkileşimler ve diğer etkileşim şekilleriHeparinin terapötik dozlarda uygulanımı sırasında antirombin tedavisi kanama riskini arttırır. Antitrombin' in etkisi heparin ile önemli düzeyde arttırılabilir. Hızlandırılmış antitrombin tumoverine bağlı olarak, heparinle birlikte tedavisiyle, antitrombinin yarı ömrü oldukça azalabilir. Bu yüzden heparin ve antitrombinin hastaya eş zamanlı uygulamasında kanama riski artacağından, hasta klinik ve biyolojik olarak monitörize edilmelidir.Özel popülasyona ilişkin ek bilgilerHerhangi bir veri mevcut değildir.Pediyatrik popülasyon:Herhangi bir veri mevcut değildir.4.6. Gebelik ve laktasyon Genel tavsiyeGebelik kategorisi: CÇocuk doğurma potansiyeli bulunan kadınlar/ Doğum kontrolü (Kontrasepsiyon)Hayvanlar üzerinde yapılan çalışmalarda, gebelik ve/veya embriyonal/fetal gelişim ve/veya doğum ve/veya doğum sonrası gelişim üzerindeki etkiler hakkında yeterli veri yoktur.Gebelik dönemiGebe kadınlarda yeterli ve iyi kontrol edilmiş çalışma bulunmamaktadır. Hastalar ANBINEX tedavisi sırasında gebe kalırlarsa veya gebe kalmaya niyetleri varsa doktorları tarafından bilgilendirilmelidirler.Laktasyon dönemiEmziren annelerde kullanım için ANBINEX'in güvenilirliği kontrollü klinik çalışmalarla kanıtlanmamıştır. ANBINEX emziren annelerin tedavisi için mutlak gerekli ise kullanılmalıdır.Üreme yeteneği/FertiliteBu konuda yapılmış herhangi bir klinik ya da klinik dışı bir çalışma bulunmamaktadır.4.7. Araç ve makine kullanımı üzerindeki etkilerANBINEX'in araç ve makine kullanımı üzerinde olumsuz bir etkisi yoktur.4.8. İstenmeyen etkilerKlinik çalışmalarda aşağıdaki advers etkiler muhtemel ya da olası olarak gözlenmiştir. Şu terimler ve sıklık dereceleri kullanılmıştır:Bunlar; çok yaygın (>1/10), yaygın (>1/100 ila <1/10), yaygın olmayan (>1/1.000 ila <1/100) ve seyrek (>1/10.000 ila <1/1.000), çok seyrek (<1/10.000), bilinmiyor (eldeki verilerden hareketle tahmin edilemiyor, olarak sınıflandırılır. Bağışıklık sistemi hastalıklarıÇok seyrek: Şoku da içerebilen anafılaksilerSeyrek Baş ağrısı, uyuşukluk, titreme, huzursuzluk Kardiyovasküler sistem bozukluklarıSeyrekGöğüs darlığı, taşikardi, hipotansiyon Solunum, göğüs bozuklukları ve mediastinal hastalıklarıSeyrek:Islık (vizing) Gastrointestinal sistem bozukluklarıSeyrekBulantı, kusma Deri ve deri altı doku bozukluklarıSeyrekAnjiyoödem, kızarma, yaygın ürtiker, kurdeşen Genel bozukluklar ve uygulama bölgesine ilişkin bozukluklarSeyrekİnfüzyon yerinde yanma ve kaşıntı hissi, karıncalanma Çok seyrek Vücut sıcaklığında yükselme İlaca bağlı istenmeyen etkiyle ilgili olarak ANBINEX ile 8 hastayı içeren klinik bir çalışma yapılmıştır. Çalışmanın sonucu olarak; hiçbir vakada, çalışma ilacı klinik olarak yan etkilere neden olmadığı gibi, ne yaşamsal belirtilerin değişimine, ne de laboratuvar parametrelerinin (hematolojik tayin, koagülasyon ve karaciğer/böbrek yetmezlik göstergeleri) geniş bir panel içindeki değişikliklerine neden olmamaktadır. Çalışma ilacı hiçbir zaman HAV, HBV, HCV ve HIV-1 ve 2 için serokonversiyona neden olmamıştır. Viral güvenliği için 4.4'e bakınız. 4.9.Doz aşımı ve tedavisi
Doz aşımı vakaları rapor edilmediği için doz aşımı sonuçları bilinmemektedir. |
İlaç BilgileriAnbinex 500iu İnfüzyon İçin Liyofilize Toz İçeren FlakonEtken Maddesi: Antitrombin Atc Kodu: B01AB02 Kullanma talimatı ve kısa ürün bilgileri
Google Reklamları
İlgili İlaçlar |
Ana Sayfa | Hakkımızda | İlaçlar | İlaç Ara | İlaç Firmaları | Gizlilik | Bize Ulaşın
Telif Hakkı 2008-2026 © İlaç Prospektüsü. Tüm Hakları Saklıdır.Uyarı: Sitemizde yayınladığımız ilaç bilgileri ile doktora danışmadan kesinlikle ilaç kullanmayınız!
Aksi halde doğabilecek sağlık sorunlarından ilacprospektusu.com sorumlu tutulamaz.