Humira Enjeksiyonluk Çözelti İçeren(adalimumab 40... Kısa Ürün BilgisiAntineoplastik ve İmmünomodülatör Ajanlar » İmmünsupresif Ajanlar » İmmünsupresif Ajanlar » Tumor necrosis factor alpha (tnf-a) inhibitors » Adalimumab KISA ÜRÜN BİLGİSİ1.BEŞERİ TIBBİ ÜRÜNÜN ADI HUMIRA enjeksiyonluk çözelti içeren (Adalimumab 40 mg/0.8 mİ) kullanıma hazır enjektörUYARI |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
Tablo 1Pazarlama Sonrası Gözlemsel ve Faz IV Klinik |
Çalışmalardaki İstenmeyen Etkiler |
Sistem Organ Sınıfı |
Advers Reaksiyon |
|
Enfeksiyonlar ve enfestasyonlar |
Divertikülit |
|
Benign neoplazmalar, kötü huylu ve belirlenmemiş (kistler ve polipler dahil) * |
Hepatosplenik T hücreli lenfoma, lösemi merkel hücreli karsinomu (cildin nöroendokrin tümörleri) |
|
Bağışıklık sistemi hastalıkları |
Anaflaksi ,sarkoidoz |
|
Sinir sistemi hastalıklar * |
Demiyelinizan hastalıklar (örn, optik nörit, Guillan-Barre sendromu), serebrovasküler kaza |
|
Kardiyak hastalıklar |
Miyokard infarktüsü |
|
Solunum , Göğüs boşluğu ve mediyastinal hastalıklar |
Pulmoner emboli, plevral efüzyon, pulmoner fıbroz |
|
Gastrointestinal hastalıklar * |
intestinal perforasyon |
|
Hepatobiliyer hastalıklar* |
Hepatit B reaktivasyonu, karaciğer yetmezliği |
|
Deri ve derialtı dokusu hastalıkları * |
Kütanöz vaskülit, Stevens Johnson sendromu, anjiyoödem, psöriyazis yeni oluşumu veya kötüleşmesi (palmoplantar püstüler psöriyazis dahil), eritema multiforme, alopesi |
|
Kas-iskelet bağ dokusu ve kemik bozukluklan |
Lupus benzeri sendrom |
|
|
|
|
Genel bozukluklar ve uygulama bölgesine ilişkin hastalıklar |
Pireksi (ateş) |
4.9 Doz aşımı ve tedavisi
Klinik çalışmalar sırasında doz kısıtlayıcı toksisite gözlenmemiştir. Değerlendirilen en yüksek doz düzeyi 10 mg/kg'lık multipl intravenöz dozlardır.5. FARMAKOLOJİK ÖZELLİKLER
Adalimumab, insan tümör nekroz faktörüne karşı spesifik olan rekombinant insan immünoglobülini (IgGl) monoklonal antikorudur. Adalimumab, insan ağır ve kappa hafif zincir değişken bölgeleri ve insan immünoglobülini sabit bölgeleri ile sonuçlanan faj görüntüleme teknolojisi kullanılarak üretilmiştir.Farmakoterapötik grup: Tümör nekröz faktörü alfa (TNF-alfa) inhibitörleri ATC kodu: L04AB04
Etki mekanizması
Adalimumab, Tümör Nekroz Faktörü (TNF)'ne spesifik olarak bağlanır ve TNF'nin p55 ve p75 hücre yüzey reseptörleriyle etkileşimini bloke ederek bu faktörün biyolojik fonksiyonunu nötralize eder.Adalimumab, lökosit migrasyonundan sorumlu adezyon moleküllerinin düzeylerinin değişmesi de dahil TNF tarafından indüklenen veya düzenlenen biyolojik yanıtlan da modüle eder (ELAM-1, VCAM-1 ve ICAM-1 için IC50 değeri 1-2 X İO'10 M).
Farmakodinamik etkiler
Romatoid artrit hastalarında HUMIRA tedavisinden sonra inflamasyonun akut faz reaktanlannda (C-reaktif protein (CRP) ve eritrosit sedimentasyon hızı (ESR)) ve serum sitokinlerinin (IL-6) düzeylerinde bazal değerlere göre hızlı bir azalma gözlenmiştir. Kıkırdak hasanndan sorumlu olan doku yeniden yapılanması sürecine yol açan matriks metalloproteinazların (MMP-1 ve MMP-3) düzeyleri de HUMIRA uygulamasından sonra düşmüştür. HUMIRA ile tedavi edilen hastalarda kronik inflamasyonun hematolojik bulgulannda çoğunlukla düzelme meydana gelmiştir.Ülseratif kolit , crohn hastalarında CRP düzeylerinde de hızlı bir azalma gözlemlenmiştir. Buna ek olarak Crohn hastalığı bulunan hastalann kolonundaki insan lökosit antijeni (HLA-DR) ve miyeloperoksidaz (MPO) gibi enflamasyon belirteçleri ve TNF ekspresyonunda belirgin azalma gözlenmiştir.
Poliartiküler jüvenil idiyopatik artrit hastalannda da CRP düzeylerinde hızlı bir azalma gözlemlenmiştir.
Klinik ÇalışmalarRomatoid Artrit
HUMIRA, bütün romatoid artrit klinik çalışmalannda 3000'i aşkın hasta üzerinde değerlendirilmiştir. Bazı hastalar 60 ayı geçen sürelerle tedavi edilmiştir. HUMIRA'nm romatoid artrit tedavisindeki etkililiği ve güvenliliği beş adet randomize, çift kör ve iyi kontrollü çalışmada değerlendirilmiştir.
I numaralı çalışmada, en az bir tane hastalık modifiye edici anti-romatizmal ilaçla tedavide başansız kalınan ve haftada 12.5-25 mg (metotreksat intoleransı olanlarda 10 mg) metotreksat tedavisiyle yeterli etki görülmeyen ve metotreksat dozu haftada 10-25 mg arasında sabit seyreden, 18 yaş ve üstü 271 orta veya şiddetli aktif romatoid artrit hastası değerlendirilmiştir.
Hastalara 24 hafta süreyle 2 haftada bir, 20, 40 veya 80 mg HUMIRA ya da plasebo dozları verilmiştir.
II numaralı çalışmada en az bir adet hastalık modifiye edici anti-romatizmal ilaçla tedavide başansız kalınan, 18 yaş ve üstü 544 orta veya şiddetli aktif romatoid artrit hastası değerlendirilmiştir. Yirmi altı hafta süreyle, 20 veya 40 mg dozunda subkütan HUMIRA enjeksiyonu (alternatif haftalarda plasebo verilmek üzere) iki haftada bir, ya da her hafta uygulanmış ve plasebo grubuna aynı süreyle her hafta plasebo verilmiştir. Başka hiçbir hastalık modifiye edici ilacın kullanılmasına izin verilmemiştir.
III numaralı çalışmada haftada 12.5-25 mg (metotreksat intoleransı olanlarda 10 mg) metotreksat tedavisiyle yeterli etki görülmeyen ve metotreksat dozu haftada 12.5-25 mg arasında sabit seyreden, 18 yaş ve üstü 619 orta veya şiddetli aktif romatoid artrit hastası değerlendirilmiştir. Bu çalışmada üç grup vardır. İlk gruba 52 hafta süreyle her hafta plasebo enjeksiyonu uygulanmıştır. İkinci gruba 52 hafta süreyle her hafta 20 mg HUMIRA uygulanmıştır. Üçüncü gruba dönüşümlü olarak alternatif haftalarda plasebo enjeksiyonları yapılmak üzere iki haftada bir 40 mg HUMIRA uygulanmıştır. Hastalar daha sonra, 60 aya varan süreyle iki haftada bir 40 mg HUMIRA uygulanan açık etiketli bir uzatma fazına kaydedilmiştir.
IV numaralı çalışmada, 18 yaş ve üstü 636 orta veya şiddetli aktif romatoid artrit hastasında primer olarak güvenlilik değerlendirilmiştir. Hastaların ya hiç hastalık modifiye edici anti-romatizmal ilaç kullanmamış olmalarına ya da tedavinin en az 28 gün stabil olması şartıyla, mevcut romatolojik tedavilerini sürdürmelerine izin verilmiştir. Bu tedavi rejimleri metotreksat, leflunomid, hidroksiklorokin, sulfasalazin ve/veya altın tuzlarım içermektedir. Hastalar 24 hafta süreyle 2 haftada bir 40 mg HUMIRA veya plasebo alacak şekilde randomize edilmiştir.
V numaralı çalışmada, daha önce hiç metotreksat kullanmamış, erken dönemli (ortalama hastalık süresi 9 aydan daha az), orta derecede veya şiddetli aktif romatoid artriti olan 799 erişkin hasta değerlendirilmiştir. Bu çalışmada 104 hafta süreyle iki haftada bir HUMIRA 40 mg ve metotreksat kombinasyon tedavisi ile iki haftada bir HUMIRA 40 mg monoterapisi ve metotreksat monoterapisinin, romatoid artrit bulgu ve semptomları ve eklem hasarındaki progresyon hızını azaltmadaki etkililiği incelenmiştir.
Çalışma I, II ve IH'de primer sonlanım noktası ve Çalışma IV'de sekonder sonlamm noktası 24. veya 26. haftalarda ACR 20 yanıtına ulaşan hastaların yüzdesidir. V numaralı çalışmada primer sonlanım noktası, 52. haftada ACR 50 yanıtı elde edilen hastaların yüzdesidir. III ve V numaralı çalışmaların ilave primer sonlanım noktalan 52. haftada hastalık progresyonunun (röntgen sonuçlarıyla saptanan) gerilemesi olmuştur. Çalışma IU'de aynı zamanda yaşam kalitesindeki değişimler de primer sonlanım noktası olmuştur.
ACR Yanıtı
HUMIRA ile tedavi edilen ve ACR 20, 50 ve 70 yanıtlarına ulaşılan hastaların yüzdesi I, II ve
III numaralı çalışmalar arasında tutarlı olmuştur. İki haftada bir 40 mg dozu ile alınan sonuçlar Tablo 2'de özetlenmektedir.
|
Yanıt |
|
Çalışma Ia* |
Çalışma IIa* |
Çalışma IIIa* | ||
|
|
Plasebo/MTXc HUMIRAb/MTXc |
Plasebo |
HUMIRAb |
Plasebo/MTXc |
HUMIRAb/MTXc | |
|
|
n=60 |
n=63 |
n=110 |
n=113 |
o o CN II c |
n=207 |
|
ACR 20 |
%13.3 |
%65.1 |
%19.1 |
%46.0 |
%29.5 |
%63.3 |
|
6 |
GD |
GD |
GD |
GD |
%24.0 |
%58.9 |
|
ay 12 ay ACR 50 |
%6.7 |
%52.4 |
%8.2 |
%22.1 |
%9.5 |
%39.1 |
|
6 |
GD |
GD |
GD |
GD |
%9.5 |
%41.5 |
|
ay 12 ay ACR 70 |
%3.3 |
%23.8 |
%1.8 |
%12.4 |
%2.5 |
%20.8 |
|
6 |
GD |
GD |
GD |
GD |
%4.5 |
%23.2 |
|
ay 12 ay |
|
|
|
|
|
|
b İki haftada bir uygulanan 40 mg HUMIRA
c MTX= Metotreksat
*p<0.01, plaseboya karşı HUMIRA
GD= Geçerli değil
I-IV numaralı çalışmalarda ACR yanıtı kriterlerinin bütün bireysel bileşenleri (duyarlı ve şiş eklemlerin sayısı, doktor ve hasta tarafından yapılan hastalık aktivitesi ve ağrı değerlendirmeleri, iş göremezlik indeksi (HAQ) skorları ve CRP (mg/dl) değerleri), 24. veya 26. haftalarda plaseboya göre düzelme göstermiştir. III numaralı çalışmada bu düzelmeler 52 hafta boyunca devamlı olmuştur. Bunlara ek olarak, açık etiketli uzatma fazında izlenen hastaların çoğunluğunda ACR yanıt oranlan 104 hafta boyunca devam etmiştir. 207 hastadan 114 hasta, 60 ay boyunca iki haftada bir 40 mg HUMIRA almaya devam etmiştir. Bu hastalar arasında 86, 72 ve 41 hastada, 60. ayda sırasıyla ACR 20/50/70 yanıtları elde edilmiştir.
m
IV numaralı çalışmada HUMIRA artı standart tedavi ile tedavi edilen hastalann ACR 20 yanıtı, plasebo artı standart tedavi ile tedavi edilen hastalardaki yanıta göre istatistiksel anlamlılık taşıyacak şekilde daha iyiydi (p<0.001).
I-IV numaralı çalışmalarda, HUMIRA ile tedavi edilen hastalarda tedaviye başlandıktan sonra bir-iki hafta gibi erken bir sürede, plasebo ile karşılaştmldığında istatistiksel olarak anlamlı ACR 20 ve 50 yanıtlarına ulaşılmıştır.
Erken dönemdeki ve daha önce metotreksat kullanmamış romatoid artrit hastalarının yer aldığı V numaralı çalışmada, HUMIRA ve metotreksat ile yapılan kombinasyon tedavisi 52. haftada, metotreksat monoterapisi ve HUMIRA monoterapisinden daha hızlı ve anlamlı olarak daha büyük ACR yanıtlan elde edilmiş ve bu yanıtlar 104, haftada kalıcı olmuştur (Tablo 3'e bakınız).
Tablo 3: Çalışma V'te ACR Yanıtları _(hastaların yüzdesi)_
Yanıt |
MTXn=257 |
HUMIRAn=274 |
HUMIRA/MTXn=268 |
p değeri8 |
Lp değeri |
p değeri0 |
|
ACR 20 |
|
|
|
|
|
|
|
52. Hafta |
%62.6 |
%54.4 |
%72.8 |
0.013 |
<0.001 |
0.043 |
|
104. Hafta |
%56.0 |
%49.3 |
%69.4 |
0.002 |
<0.001 |
0.140 |
|
ACR 50 |
|
|
|
|
|
|
|
52. Hafta |
%45.9 |
%41.2 |
%61.6 |
<0.001 |
<0.001 |
0.317 |
|
104. Hafta |
%42.8 |
%36.9 |
%59.0 |
<0.001 |
<0.001 |
0.162 |
|
ACR 70 |
|
|
|
|
|
|
|
52. Hafta |
%27.2 |
%25.9 |
%45.5 |
<0.001 |
<0.001 |
0.656 |
|
104. Hafta |
%28.4 |
%28.1 |
%46.6 |
<0.001 |
<0.001 |
0.864 |
L
p değeri HUMIRA monoterapisi ve HUMIRA/metotreksat kombinasyon tedavisi arasında Mann-Whitney U testi kullanılarak yapılan çiftli kıyaslamadan elde edilmiştir.
0 p değeri HUMIRA monoterapisi ve metotreksat monoterapisi arasında Mann-Whitney U testi kullanılarak yapılan çiftli kıyaslamadan elde edilmiştir.
52. haftada HUMIRA/metotreksat kombinasyon tedavisi gören hastalann %42.9'unda klinik remisyon (DAS28<2.6) sağlanırken, bu oran metotreksat monoterapisi alan hastalarda %20.6 ve HUMIRA monoterapisi alan hastalarda %23.4 olmuştur. HUMIRA/metotreksat kombinasyon tedavisi, yakın dönemde tam konulmuş orta ile şiddetli romatoid artriti olan hastalarda düşük düzeyli hastalık hali sağlanmasında metotreksat ve HUMIRA monoterapilerinden klinik ve istatistik olarak daha üstündür (sırasıyla p <0.001 ve p <0.001). İki monoterapi kolundaki yanıtlar benzerdir (p=0.447).
Radyo grafik Yanıt
Hastalardaki ortalama romatoid artrit süresinin yaklaşık 11 yıl olduğu III numaralı çalışmada, yapısal eklem harabiyeti radyografık olarak değerlendirilmiş ve modifiye total Sharp skoru ve bileşenlerinde, erozyon skorunda ve eklem aralığı daralma skorunda değişim şeklinde ifade edilmiştir. HUMIRA/metotreksat hastalan 6 ve 12. aylarda, tek başına metotreksat alan hastalara kıyasla anlamlı olarak daha az radyografik progresyon göstermişlerdir (Tablo 4'e bakınız). Açık etiketli uzatma fazına ilişkin bilgiler, bir grup hastada yapısal harabiyetin progresyon hızındaki azalmanın 60 aya kadar süreyle de devam etmekte olduğuna işaret etmektedir. Başlangıçta iki haftada bir 40 mg HUMIRA ile tedavi edilen 207 hastadan 113'ü,
5. yılda radyografik olarak değerlendirilmiştir. Bu hastalardan 66 hastada, 0 veya daha az TSS değişimi olarak tanımlandığında, yapısal hasarda ilerleme tespit edilmemiştir.
|
|
Plasebo/MTXa |
HUMIRA/MTX iki haftada bir 40 mg |
Plasebo/MTX-HUMIRA/MTX (%95 Güven Aralığıb) |
p değeri |
|
Total Sharp skoru |
2.7 |
0.1 |
2.6 (1.4, 3.8) |
<0.001° |
|
Erozyon skoru |
1.6 |
0.0 |
1.6 (0,9, 2.2) |
<0.001 |
|
EADÜ skoru |
1.0 |
0.1 |
0.9 (0.3, 1.4) |
0.002 |
t*
Metotreksat ve HUMIRA arasında değişim skorlarındaki farklılıkların %95 güven aralıkları
c Sıralı analize (rank analysis) dayalı olarak d Eklem Aralığında Daralma
V numaralı çalışmada, yapısal eklem haşan radyografik olarak değerlendirilmiş ve modifiye total Sharp skorunda değişim şeklinde ifade edilmiştir (Tablo 5'e bakınız).
Tablo 5: Çalışma V'te 52. Haftada Radyografik Ortalama Değişimler
|
|
MTX n=257 (%95 Güven Aralığı) |
HUMIRA n=274 (%95 Güven Aralığı) |
HUMIRA/M TX n=268 (%95 Güven Aralığı) |
p değeria |
p değerib |
p değeric |
|
Total Sharp skoru |
5.7 (4.2-7.3) |
3.0 (1.7-4.3) |
1.3 (0.5-2.1) |
<0.001 |
0.0020 |
<0.001 |
|
Erozyon skoru |
3.7 (2.7-4.7) |
1.7(1.0-2.4) |
0.8 (0.4-1.2) |
<0.001 |
0.0082 |
<0.001 |
|
EAD skoru |
2.0 (1.2-2.8) |
1.3 (0.5-2.1) |
0.5 (0-1.0) |
<0.001 |
0.0037 |
0.151 |
0 p değeri HUMIRA monoterapisi ve metotreksat monoterapisi arasında Mann-Whitney U testi kullanılarak yapılan çiftli kıyaslamadan elde edilmiştir.
Elli iki haftalık ve 104 haftalık tedavilerden sonra progresyon göstermeyen (modifiye total Sharp skorunda başlangıç dönemine göre değişim <0.5) hastalann yüzdesi, HUMIRA/metotreksat kombinasyon tedavisi ile (sırasıyla %63.8 ve %61.2), metotreksat monoterapisi (sırasıyla %37.4 ve %33.5, p<0.001) ve HUMIRA monoterapisine (sırasıyla %50.7, p<0.002 ve %44.5, p<0.001) kıyasla anlamlı derecede daha yüksektir.
Yasam Kalitesi ve Fiziksel Fonksiyon
Başlangıçtaki dört adet yeterli ve iyi kontrollü çalışmanın hepsinde de, Sağlık Değerlendirme Anketi'nin (HAQ) iş göremezlik indeksi kullanılarak sağlığa ilişkin yaşam kalitesi ve fiziksel
fonksiyon değerlendirilmiştir; bu değerlendirmeler III numaralı çalışmanın 52. haftası için önceden tanımlanmış bir primer sonlanım noktasıdır. Dört çalışmanın tümünde, HUMIRA'mn bütün dozlan/doz şemaları plasebo ile karşılaştırıldığında 6. ayda HAQ anketinin iş göremezlik indeksinde başlangıç dönemine göre istatistiksel olarak anlamlı bir iyileşme olduğu görülmüş ve aynı durum III numaralı çalışmada 52. haftada da gözlenmiştir.
Kısa Sağlık Araştırma Formu (SF 36) sonuçları dört çalışmanın tümünde, fiziksel bileşen özeti (PCS) skorları istatistiksel anlamlılık taşıyacak şekilde, HUMIRA'mn bütün dozlan/doz şemalan için bu bulgulan desteklemektedir; ağn ve canlılık alan skorlan ise, iki haftada bir 40 mg dozu için istatistiksel olarak anlamlıdır. Kronik hastalık tedavisi fonksiyonel değerlendirme (FACIT) skorlarının değerlendirildiği üç çalışmanın hepsinde de (Çalışma I, III, IV), bu skorlar ile ölçülen yorgunluğu istatistiksel olarak anlamlı bir azalma vardır,
III numaralı çalışmada fiziksel fonksiyondaki iyileşmeler, açık etiketli tedavinin 260. haftasında (60 ay) da devam etmektedir. Yaşam kalitesindeki iyileşmeler 156. haftaya (36 ay) kadar ölçülmüştür ve iyileşmelerin bu döneme kadar kalıcı olduğu görülmüştür.
V numaralı çalışmada HAQ iş göremezlik indeksi ve SF 36'nın fiziksel bileşenindeki iyileşmeler, HUMIRA/metotreksat kombinasyon tedavisi ile, metotreksat monoterapisi ve
_
HUMIRA monoterapisine kıyasla 52. haftada daha yüksektir ve bu yükseklik 104. haftada daV devam etmektedir (p <0.001).
Poliartiküler iüvenil idiyopatik artrit(J1A)
HUMIRA'mn güvenlik ve etkinliği poliartiküler jüvenil idiyopatik artrit olan 171 çocukta (4-
17 yaş) çok merkezli, randomize, çift-kör, paralel-gruplu bir çalışmada değerlendirildi. Açık etiket giriş fazında (OL LI) hastalar, MTX (metotreksat) ile tedavi edilen veya MTX (metotreksat) ile tedavi edilmeyen şeklinde iki grupta kademelendirildiler. MTX ile tedavi edilmeyenler katmanında bulunan hastalar metotreksata naif veya çalışmadaki ilaç uygulamasından en az iki hafta önce metotreksat tedavisi kesilen hastalardı. Hastalar NSAID ve/veya prednisonun stabil dozlannda (<0.2 mg/kg/gün veya maksimum 10 mg/gün) kaldılar. OL LI fazında, tüm hastalar 16 hafta boyunca iki haftada bir 24 mg/m2'den maksimum 40 mg'a kadar HUMIRA aldılar. Hastalann yaş ve OL LI fazında aldıklan minimum, ortalama ve maksimum dozlara göre dağılımı Tablo 6'da sunulmaktadır.
Tablo 6 : Hastaların yaş ve OL LI fazında aldıkları adalimumab dozuna göre dağılımı
|
Yaş Grubu |
Başlangıçtaki hasta sayısı n(%) |
Minimum, ortalama ve maksimum doz |
|
4-7 yaş |
31 (18.1) |
10, 20 ve 25 mg |
|
8-12 yaş |
71 (41.5) |
20, 25 ve 40 mg |
|
13-17 yaş |
69 (40.4) |
25, 40 ve 40 mg |
|
Katman |
MTX olan |
MTX olmayan | ||
|
Faz |
|
| ||
|
OL-LI16 hafta |
|
| ||
|
Pediatrik ACR 30 yanıtı (n/N) |
%94.1 (80/85) |
%74.4 (64/86) | ||
|
| ||||
|
Çift Kör |
HUMIRA (n=38) |
Plasebo (n=37) |
HUMIRA (n=30) |
Plasebo (n=28) |
|
32. haftanın sonunda hastalık alevlenmesi (n/N) |
%36.8 (14/38) |
%64.9 (24/37)b |
%43.3 (13/30) |
%71.4 (20/28)° |
|
Hastalık alevlenmesine ortalama zaman |
>32 hafta |
20 hafta |
>32 hafta |
14 hafta |
|
a 48. haftada Pediatrik ACR 30 |
/50/70 yanıtlan plasebo ile tedavi edilen hastalara göre önemli | |||
16. haftada yanıt verenler (n=144) arasından, çalışma boyunca HUMIRA alan hastalarda OLE fazında Pediatrik ACR 30/50/70/90 yanıtlan iki yıla kadar devam ettirilmiştir.
Tüm yanıtlar genel olarak iyiydi ve tek başına HUMIRA ile tedavi edilen hastalara göre HUMIRA ve metotreksat kombinasyonu ile tedavi edilen hastalann çok azında antikor gelişmiştir. Bu sonuçlar dikkate alındığında, HUMIRA, metotreksat ile kombinasyon halinde kullanılmak üzere ve metotreksat kullanması uygun olmayan hastalarda monoterapi olarak kullanılmak üzere önerilmektedir.
W
Psöriyatik Artrit
İki haftada bir 40 mg şeklinde uygulanan HUMIRA, Çalışma VI ve Çalışma VII adlanndaki plasebo kontrollü iki çalışmada, orta dereceli ile şiddetli aktif psöriyatik artrit hastalannda incelenmiştir. Yirmi dört hafta süreli Çalışma VI*da, non-steroid anti-enflamatuvar ilaç tedavisine yetersiz yanıt veren 313 erişkin hasta tedavi edilmiştir; bunlann yaklaşık %50'si metotreksat almaktaydı. On iki hafta süreli Çalışma VII'de, DMARD tedavisine yetersiz yanıt veren 100 hasta tedavi edilmiştir. İki çalışmanın bitiminde, 383 hasta açık etiketli uzatma çalışmasına alınmıştır ve bu çalışmada iki haftada bir 40 mg HUMIRA uygulanmıştır.
İncelenen hasta sayısının küçük olması nedeniyle, HUMIRA'nın ankilozan spondilit benzeri psöriyatik artropati hastaları üzerinde gösterdiği etkililiği konusundaki veriler yetersizdir (Tablo 8'e bakınız).
|
|
Çalışma VI |
Çalışma VII | ||
|
Yanıt |
Plasebo |
HUMIRA |
Plasebo |
HUMIRA |
|
|
N=162 |
N=151 |
N=49 |
N=51 |
|
ACR 20 |
|
|
|
|
|
12 hafta |
%14 |
%58~* |
%16 |
%39* |
|
24 hafta |
%15 |
%57*" |
GD |
GD |
|
ACR 50 |
|
|
|
|
|
12 hafta |
%4 |
%36*** |
%2 |
%25*** |
|
24 hafta |
%6 |
%39*** |
GD |
GD |
|
ACR 70 |
|
|
|
|
|
12 hafta |
%1 |
%20*** |
%0 |
%14* |
|
24 hafta |
%1 |
%23*** |
GD |
GD |
|
'p<0.001,] |
-IUMIRA ve plase |
)o sırasındaki tüm |
karşılaştırmalar için. | |
GD= Geçerli değil.
Çalışma Vl'daki ACR yanıtları, eş zamanlı metotreksat tedavisi uyugulandığında veya uygulanmaksızın, benzer niteliktedir. Açık etiketli uzatma çalışmasında ACR yanıtlan, 136. haftaya kadar devam etmiştir.
Psöriyatik artrit çalışmalarında radyografik yanıtlar değerlendirilmiştir. Çalışmanın çift kör döneminde, hastalara HUMIRA veya plasebo uygulanırken, başlangıçta ve 24. haftada, aynca çalışmanın açık etiketli döneminde, bütün hastalara HUMIRA uygulanırken 48. haftada, el, bilek ve ayak radyografileri çekilmiştir. Distal inter falanjiyal eklemleri içeren (romatoid artrit için kullanılan TSS ile aynı olmayan) Modifiye Total Sharp Skoru (mTSS) kullanılmıştır. HUMIRA tedavisinin periferal eklem hasarı gelişmesini azaltması, plasebo ile karşılaştırıldığında, başlangıçtan itibaren değişim olarak alındığında, mTSS skoru (ortalama + SD) 0.8±2.5 plasebo grubunda (24. haftada) ve 0.0±1.9 HUMIRA grubunda (48. haftada) olmuştur; (p<0.001).
HUMIRA ile tedavi edilen ve başlangıçtan itibaren 48. haftaya kadar radyografik progresyon olmayan hastalardan (n=102) %84'ünde, tedavinin 144 haftalık süresi boyunca radyografik progresyon görülmemiştir.
HUMIRA ile tedavi edilen hastalar 24. haftada, HAQ ve Kısa Sağlık Araştırma Formu (SF 36) olarak değerlendirildiğinde, plasebo uygulanan hastalara göre istatistiksel olarak önemli fiziksel fonksiyon gelişmesi göstermiştir. Fiziksel fonksiyonlann iyileşmesi, açık etiketli uzatma çalışmasında 136. haftaya kadar devam etmiştir.
Ankilozan Spondilit (AS)
İki haftada bir HUMIRA 40 mg, 24 hafta süreli, randomize çift-kör, plasebo kontrollü iki çalışmada, konvansiyonel tedaviye yeterli yanıt vermeyen aktif ankilozan spondilitli (tüm gruplarda ortalama bazal hastalık aktivitesi skoru [Bath Ankilozan Spondilit Hastalık Aktivitesi İndeksi (BASDAI)] 6.3 idi) 393 hasta üzerinde değerlendirildi. Yetmiş dokuz hasta (%20.1) eş zamanlı olarak hastalık modifiye edici ilaçlar ile, ve 37 hasta (%9.4) ise yine eş
zamanlı olarak glukokortikoidler ile de tedavi edilmiştir. Kör dönemi, hastalara iki haftada bir HUMIRA 40 mg uygulanan, 28 haftaya kadar süren, ilave bir açık etiketli dönem izlemiştir. 12, 16 veya 20. haftalarda AS AS 20 yanıtı elde edilemeyen hastalara (n=215, %54.7), açık etikete erken kaçış prensibiyle iki haftada bir subkütan adalimumab 40 mg uygulanmıştır, ve bu hastalar daha sonra, çift kör istatistik analizlerde yanıt vermeyenler olarak kabul edilmiştir. 315 hastalı daha büyük çalışmada (VIII) sonuçlar, HUMIRA ile tedavi edilen hastaların, ankilozan spondilit bulgu ve semptomlarında plaseboya kıyasla istatistiksel olarak anlamlı derecede daha fazla iyileşme sağladıklarını göstermiştir. Anlamlı yanıt ilk kez 2. haftada gözlenmiştir ve 24. haftaya kadar devam etmiştir (Tablo 9).
Tablo 9: Plasebo Kontrollü AS Çalışmasında (Çalışma VIII) Etkinlik Yanıtları
Yanıt |
PlaseboN=107 |
HUMIRAN=208 |
|
ASASa 20 |
|
|
|
2 hafta |
%16 |
%42"' |
|
12 hafta |
%21 |
%58w |
|
24 hafta |
%19 |
%5f |
|
ASAS 50 |
|
|
|
2 hafta |
%3 |
%16*** |
|
12 hafta |
%10 |
%38*** |
|
24 hafta |
%11 |
%35*** |
|
ASAS 70 |
|
|
|
2 hafta |
%0 |
%7** |
|
12 hafta |
%5 |
%23*** |
|
24 hafta |
%8 |
%24*** |
|
BASDAI8 50 |
|
|
|
2 hafta |
%4 |
%20*** |
|
12 hafta |
%16 |
%45*** |
|
24 hafta |
%15 |
%42*** |
12 ve 24. haftalarda HUMIRA
vt
HUMIRA ile tedavi edilen hastalarda gerek SF 36, gerekse Ankilozan Spondilit Yaşam Kalitesi Anketinde (ASQoL) 12. haftada anlamlı olarak daha büyük iyileşme elde edilmiştir ve bu iyileşme 24. haftaya kadar kalıcı olmuştur.
Aktif ankilozan spondiliti olan 82 erişkin hastanın alındığı daha küçük, randomize çift kör, plasebo kontrollü çalışmada (IX) da benzer eğilimler görülmüştür (tamamı istatistiksel yönden anlamlı değildir).
Crohn Hastalığı
Multipl HUMIRA dozlarının güvenliliği ve etkililiği, 1400'ü aşkın orta dereceli veya şiddetli Crohn hastalığı bulunan hastada (Crohn Hastalığı Aktivite İndeksi (CDAI) >220 ve <450) randomize, çift-kör, plasebo kontrollü çalışmalarda değerlendirilmiştir. Çalışmaya katılan hastaların 478 (%32)'i, endikasyon bölümünde (Bkz. 4.1) belirtilen popülasyona karşılık gelen şiddetli hastalığa sahipti (CDA skoru >300'dü ve eşzamanlı olarak kortikosteroid ve/veya immünsupresan kullanmaktaydılar). Aminosalisilatların, kortikosteroidlerin ve/veya
immünomodülatör ajanların stabil dozlarda konkomitan kullanımına izin verilmiştir ve hastaların %79'u bu ilaçlardan en az birini almaya devam etmiştir.
Klinik remisyonun indüksiyonu (CDAI<150 olarak tammlanmıştır) iki çalışmada, (- M02-403 ve M04-691 çalışmaları) değerlendirilmiştir. M02-403 çalışmasında daha önce TNF antagonisti kullanmamış olan 299 hasta dört tedavi grubundan birine randomize edilmiştir; plasebo grubu 0. haftada ve 2. haftada plasebo almış, 160/80 grubu 0. haftada 160 mg ve 2. haftada 80 mg HUMIRA almıştır, 80/40 grubu 0. haftada 80 mg ve 2. haftada 40 mg HUMIRA almıştır ve 40/20 grubu 0. haftada 40 mg ve 2. haftada 20 mg HUMIRA almıştır. M04-691 çalışmasında infliksimaba yanıtı kaybolmuş veya tolere edemeyen 325 hasta, 0. haftada 160 mg ve 2. haftada 80 mg HUMIRA veya 0. hafta ve 2. haftada plaseboya randomize edilmişlerdir.
Klinik remisyonun idamesi M02-404 çalışmasında değerlendirilmiştir. M02-404 çalışmasında 854 hasta, önce açık etiketli olarak 0. haftada 80 mg HUMIRA ve 2. haftada 40 mg HUMIRA almışlardır. Hastalar daha sonra 4. haftada iki haftada bir 40 mg HUMIRA veya plaseboya randomize edilmişlerdir, toplam çalışma süresi 56 haftadır. 4. haftada klinik yanıt veren hastalar (CR-70 = CDAI>70 kadar düşüş) 4. haftada klinik yanıt vermeyenlerden ayrı olarak analiz edilmişlerdir. Sekizinci haftadan sonra kortikosteroidin azaltılarak kesilmesine izin verilmiştir.
Klinik Sonuçlar
M02-403 ve M04-691 çalışmasında hastaların daha önce TNF antagonisti almasına veya infliksimaba maruz kalmasına bakılmaksızın 4. haftada plaseboya kıyasla 160/80 mg HUMIRA ile tedavi edilen gruplarda istatistiksel olarak anlamlı ölçüde daha büyük klinik remisyon indüksiyonu sağlanmıştır (bakınız Tablo 11).
Tablo 10: Klinik Remisyon İndüksiyonu ve Yanıt (Hastaların Yüzdesi)
|
|
CLASSIC I: Önceden Infliksimab Kullanmamış Hastalar |
GAIN: Önceden İnfliksimab Kullanmış Hastalar | ||
|
|
Plasebo N=74 |
HUMIRA 160/80 mg N=76 |
Plasebo N=166 |
HUMIRA 160/80 mg N=159 |
|
Hafta 4 |
|
|
|
|
|
Klinik remisyon |
%12 |
%36* |
%7 |
%21 * |
|
Klinik yanıt (CR-100) |
%24 |
%501 |
%25 |
%38** |
|
Klinik yanıt (CR-70) |
%34 |
%58** |
%34 |
%52** |
|
Bütün p-değerleri H1 |
JMIRA ve plasebonun eşlenik karşılaştırmalarıdır | |||
ve 56. haftalarda plasebo idame grubundaki hastalarla karşılaştırıldığında HUMIRA idame gruplarında en az 90 gün için kortikosteroid kullanımını kesebilen hastaların oranı istatistiksel olarak anlamlı ölçüde daha fazladır (bakınız Tablo 12).
Tablo 11: Klinik Rcmisyon ve Yanıtın İdamesi (Hastaların Yüzdesi)
|
|
Plasebo |
İki haftada bir 40 mg HUMIRA |
Haftada bir 40 mg HUMIRA |
Hafta26 |
N=170 |
N=172 |
N=157 |
|
|
|
|
|
|
Klinik remisyon |
%17 |
%40* |
%47* |
|
|
|
|
|
|
Klinik yanıt (CR-100) |
%27 |
%52* |
%52* |
|
Klinik yanıt (CR-70) |
%28 |
%54* |
%56* |
|
En az 90 güna steroidsiz remisyonda olan hastalara |
%3 (2/66) |
%19 (11/58)** |
%15 (11/74)** |
Hafta56 |
N=170 |
N=172 |
N=157 |
|
|
|
|
|
|
Klinik remisyon |
%12 |
%36* |
%41* |
|
|
|
|
|
|
Klinik yanıt (CR-100) |
17% |
41%* |
48%* |
|
Klinik yanıt (CR-70) |
18% |
43%* |
49%* |
|
En az 90 güna steroidsiz remisyonda olan hastalara |
5% (3/66) |
29% (17/58)* |
20% (15/74)** |
56. haftada plasebo ile karşılaştırıldığında hastalığa bağlı hospitalizasyon ve cerrahi HUMIRA ile istatistiksel olarak anlamlı bir şekilde azaltılmıştır.
M02-403 çalışmasında 117/276 hasta ve M04-691 ile M02-404 çalışmalarından 272/777 hasta en az 3 yıl boyunca açık etiketli olarak adalimumab tedavisi ile izlenmiştir. Sırasıyla 88 (%75.2) ve 189 (%69.5) hasta klinik remisyonda kalmaya devam etmiştir. Klinik yanıt (CR-70) sırasıyla 107 (%91.5) ve 248 (%91.2) hastada devam ettirilmiştir.
135 hastanın dahil olduğu bir endoskopi çalışması (M05-769) HUMIRA'nın mukozal iyileşmedeki etkisini göstermiştir. 12. haftada plasebo verilen hastaların %13.1'i ile karşılaştırıldığında HUMIRA ile tedavi edilen hastaların %27.4'ünde mukozal iyileşme olmuştur (p=0.056) ve 52. haftada plasebo verilen hastaların %0'ı ile karşılaştırıldığında HUMIRA ile tedavi edilen hastaların %24.2'sinde mukozal iyileşme olmuştur (p<0.001).
Tablo lTde sunulan klinik remisyon sonuçlan, önceki TNF antagonisti maruziyetinden bağımsız olarak oldukça sabit kalmıştır.
Çalışma sırasında remisyona girenlerden 4. haftada yanıt verenler içinde, HUMIRA idame gruplarındaki hastaların remisyonda kalma süresi plasebo idame grubundaki hastalardan anlamlı ölçüde daha uzundur (bakınız Şekil 1).
Plasebo ___HUMIRA, her iki haftada bir - HUMIRA 40 mg, her hafta
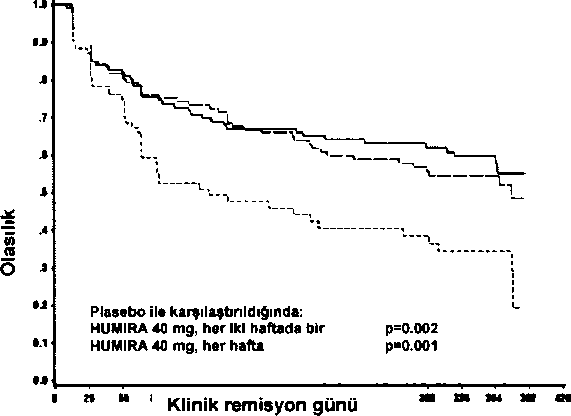
Remisyondaki Günler
Dördüncü haftada yanıt vermeyen hastalar arasından, HUMIRA idame grubunda 12. haftada yanıt verenlerin oranı %43 iken plasebo idame hastalarında bu oran %30 olmuştur. Bu sonuçlar 4. haftada yanıt vermeyen bazı hastaların, sürdürülen idame tedavisinden 12. haftada yarar görebileceğini düşündürmektedir.On ikinci haftadan sonra sürdürülen tedavi anlamlı ölçüde daha fazla yanıtla sonuçlanmamıştır (bakınız bölüm 4.2).
Hasta Tarafından Bildirilen Sonlanımlar
M02-403 ve M04-691 çalışmalarında plaseboyla karşılaştırıldığında, HUMIRA 160/80 mg tedavisine randomize edilmiş hastalarda 4 haftada hastalığa özgü inflamatuar barsak hastalığı anketinde (IBDQ) istatistiksel olarak anlamlı düzelme olmuştur. Plasebo grubuyla karşılaştırıldığında adalimumab tedavi gruplarında M02-404 çalışmasının 26. ve 56. haftalarında IBDQ başlangıç skorlarında başlangıca göre istatistiksel olarak anlamlı düzelme görülmüştür.
Ülseratif Kolit
Çoklu Humira dozlarının güvenilirliği ve etkililiği, randomize, çift-kör, plasebo kontrollü çalışmalarda orta şiddetli ila şiddetli ülseratif koliti (6-12 arasında Mayo skoru ile birlikte endoskopi alt skorun 2-3 arasında olması ) bulunan erişkin hastalarda değerlendirilmiştir.
UC-I Çalışmasında, daha önce TNF-antagonisti kullanmamış 390 hasta, 0. ve 2. Haftada plasebo, 0. Haftada 160 mg Humira, takiben 2. Haftada 80 mg veya 0. Haftada 80 mg Humira, ardından 2. Haftada 40 mg alacak şekilde randomize edilmiştir. 2. Haftadan sonra her iki adalimumab kolundaki hastalar iki haftada bir 40 mg almışlardır. Klinik remisyon ( Mayo skoru <2 ve alt skorlarının 1 den büyük olmaması) 8. Haftada değerlendirilmiştir.
UC-II Çalışmasında, 248 hasta 0. Haftada 160 mg, 2. Haftada 80 mg ve iki haftada bir 40 mg Humira almış, 246 hasta da plasebo almıştır. Klinik sonuçlar 8. Haftadaki remisyon indüksiyonu ve 52. Haftadaki remisyon idamesi yönünden değerlendirilmiştir.
160/80 mg Humira ile indüksiyon dozu alanlar , UC-I çalışmasında (sırasıyla %18'e karşı %9, p=0.031) ve UC-II çalışmasında (sırasıyla %17'ye karşı %9, p=0.019) 8. Haftada plaseboya karşı istatistiksel olarak anlamlı düzeyde daha yüksek oranlarda klinik remisyon sağlamıştır. UC-II çalışmasında, 8. Haftada remisyonda olan Humira tedavisi alanlardan 21/41 (%51) olgu 52. Haftada remisyondadır.
Genel UC-II çalışma popülasyonundan alınan sonuçlar Tablo 13 de sunulmaktadır.
Tablo 12 :UC-I1 Çalışmasında Yanıt, Remisyon ve Mukozal İyileşme _(Hasta Yüzdesi)_
|
|
Plasebo |
HUMIRA 40 mg |
|
|
|
İki haftada bir |
|
Hafta 52 |
N=246 |
N=248 |
|
Klinik Yanıt |
%18 |
% 30* |
|
Klinik Remisyon |
%9 |
%17* |
|
Mukozal İyileşme |
%15 |
%25* |
|
> 90 gün süreyle steroidsiz remisyon 3 |
%6 |
%13 * |
|
|
(N-140) |
2 II UtO |
|
Hafta 8 ve 52 | ||
|
Sürdürülen Yanıt |
%12 |
%24** |
|
Sürdürülen Remisyon |
%4 |
%8* |
|
Sürdürülen Mukozal İyileşme |
%11 |
%19* |
|
Klinik remisyon, Mayo skoru <2 ve alt skorlannın 1 den büyük olmaması: | ||
a
_UC-II çalışmasındaki hastaların yaklaşık %40'ı İnfliksimab ile anti-TNF tedavisinde başarısız olmuşlardır. Anti-TNF ile tedavi görmemiş (naif) hastalardaki
n
e kıyasla, bu hastalarda adalimumab etkililiği azalmıştır. Önceki Anti-TNF tedavisinde başarısız olan hastalar arasında; 52. Haftada plasebo ile %3 ve adalimumab ile %10 remisyona ulaşılmıştır.UC çalışmaları I ve II hastalan, açık etiketli uzun süreli uzatma çalışmasına geçiş için tercih hakkına sahip olmuştur. Doz sıklığının haftada 40 mg'a çıkartılması, tedaviden bir yıl veya daha fazla süre sonra yanıt vermemeye başlayan hastalara fayda sağlayabilmektedir (bkz. 4.2).
Psöriyazis
HUMIRA'mn güvenliliği ve etkililiği, randomize, çift kör çalışmalarda sistemik terapi veya fototerapi adayları olan kronik plak psöriyazisli erişkin hastalarda (>%10 BSA tutulumu ve Psöriyazis Alan ve Şiddet İndeksi (PASI) >12 veya >10) araştırılmıştır. Psöriyazis Çalışmaları
I ve H'ye katılan hastaların %73'ü daha önce sistemik terapi veya fototerapi almışlardır.
Psöriyazis Çalışması I (M03-656)'de üç tedavi dönemi içinde 1212 hasta değerlendirilmiştir. A Döneminde, hastalar plasebo veya başlangıç 80 mg HUMIRA dozunu takiben, başlangıç dozundan bir hafta sonra başlanarak iki haftada bir 40 mg HUMIRA almışlardır. On altı haftalık tedaviden sonra en az PASI 75 yanıtına ulaşan hastalar (PASI skorunda başlangıca göre en az %75 düzelme olması) B Dönemine girmişler ve iki haftada bir açık etiketli olarak 40 mg HUMIRA almışlardır. Hafta 33'de >PASI 75 yanıtını sürdüren ve A Döneminde
orijinal olarak aktif terapiye randomize edilmiş olan hastalar, tekrar randomize edilerek C Döneminde 19 hafta boyunca, iki haftada bir 40 mg HUMIRA tedavisi veya plasebo almışlardır. Bütün tedavi gruplarında ortalama başlangıç PASI skoru 18.9 olup, başlangıç Doktor Global Değerlendirme (PGA) skoru orta dereceli (dahil edilen hastalann %53'ü) ile şiddetli (%41) veya çok şiddetli (%6) arasındadır.
Psöriyazis Çalışması II (M04-716)'de, 271 hastada metotreksat ve plasebo karşısında HUMIRA'mn etkililiği ve güvenliliği karşılaştırdımştır. Hastalar plasebo, başlangıç dozu olarak MTX 7.5 mg almışlar ve daha sonra doz, hafta 12'ye kadar artınlarak 25 mg maksimum doza ulaşmıştır veya 16 hafta boyunca 80 mg HUMIRA başlangıç dozunu takiben iki haftada bir 40 mg (başlangıç dozundan bir hafta sonra başlayarak) verilmiştir.
On altı haftalık tedavinin ötesinde HUMIRA ve MTX'ı karşılaştıran veriler mevcut değildir. Hafta 8 ve/veya hafta 12'de >PASI 50 yanıtına ulaşan MTX alan hastalarda, doz daha fazla artınlmamıştır. Bütün tedavi gruplannda ortalama bazal PASI skoru 19.7 olup bazal PGA skoru hafif5 (<%1) ile orta dereceli (%48) ve şiddetli (%46) ile çok şiddetli (%6) arasındadır.
Faz II ve Faz III psöriyazis çalışmalanna katılan hastaların hepsi, ilave en az 108 hafta HUMIRA verilen açık etiketli uzatma çalışmasına (M03-658) dahil olmak için uygundu.
Psöriyazis Çalışmalan I ve IFde, primer sonlanım noktası, başlangıca göre hafta 16'da PASI 75 yanıtına ulaşan hastaların oranıdır (Tablo 13 ve 14).
Tablo 13: Ps Çalışma I (REVEAL), 16. Haftadaki Etkinlik Sonuçları
|
|
Plasebo N=398 n (%) |
iki haftada bir HUMIRA 40 mg N=814 n (%) |
£PASI75 |
26 (6.5) |
578 (70.9)° |
PASI 100 |
3 (0.8) |
163 (20.0)b |
PGA: temiz/minimal |
17(4.3) |
506 (62.2)b |
|
|
Plasebo N=53 n (%) |
MTX N=110 n (%) |
iki haftada bir HUMIRA 40 mg N=108 n (%) |
>PASI 75 |
10(18.9) |
39 (35.5) |
86 (79.6) * D |
PASI 100 |
1(1.9) |
8 (7.3) |
18 (16.7)c,d |
PGA: Temiz/minimal |
6(11.3) |
33 (30.0) |
79 (73.1)^D |
Psöriyazis Çalışması I'de, PASI 75 yanıtı veren ve hafta 33'te plaseboya yeniden randomize edilen hastaların %28'ine karşılık HUMIRA'ya devam edenlerin %5'inde, p<0.001, yeterli yamt kaybı meydana gelmiştir (33. haftadan sonra ve 52. haftada veya daha önce PASI skorunda başlangıca göre <PASI 50 yanıtı ile 33. haftada göre PASI skorunda minimum 6 puanlık artış olması). Plaseboya yeniden randomizasyondan sonra yeterli yanıtı kaybeden hastalardan daha sonra açık etiketli uzatma çalışmasına katılanlann %38'i (25/66) ve %55'inde (36/66) sırasıyla, yeniden tedaviden 12 ve 24 hafta sonra PASI 75 yanıtı elde edilmiştir.
16. hafta ve 33. haftada, PASI 75 yanıtı veren toplam 233 kişi, Psöriyazis Çalışması I'de (M053-656) 52 hafta süreyle sürekli HUMIRA tedavisi görmüştür ve açık etiketli uzatma çalışmasında HUM IRA'ya devam edilmiştir. 108 haftalık ek bir açık etiketli tedaviden sonra (toplam 160 hafta), bu hastalardaki PASI 75 ve PGA temiz veya minimal yanıt oranlan sırasıyla %74.7 ve %59.0'dır.
Psöriyazis Çalışması 11'de (M04-716) toplam 94 hasta HUMIRA tedavisine randomize edilmiştir ve açık etiketli uzatma çalışmasında HUMIRA'ya devam edilmiştir. Ek bir 108 haftalık açık etiketli tedaviden sonra (toplam 124 hafta), bu hastalardaki PASI 75 ve PGA temiz veya minimal yamt oranları sırasıyla %58.1 ve %46.2'dir.
Açık etiketli uzatma çalışmasında kesilme ve yeniden tedavi değerlendirmesine toplam 347 stabil yanıt veren hasta katılmıştır. Ortalama nüksetme süresi (PGA 'orta derecede' veya daha kötüye doğru gerileme) yaklaşık 5 aydır. Kesilme periyodu sırasında bu hastalann hiçbiri ribaund yaşamamıştır. Yeniden tedavi periyoduna giren hastalann toplamda %76.5'i (218/285), kesilme sırasında hastalığın nüksedip nüksetmemesinden bağımsız olarak, 16 haftalık yeniden tedaviden sonra PGA 'temiz' veya 'minimal' yanıtı vermiştir (Kesilme periyodunda nüksetme görülen veya görülmeyen hastalarda sırasıyla %69.1 [123/178] ve %88.8 [95/107]).
DLQI'de (Dermatoloji Yaşam Kalitesi İndeksi) plasebo (Çalışma I ve II) ve MTX (Çalışma II) ile karşılaştırıldığında, başlangıca göre 16. haftada anlamlı düzelmeler olduğu gösterilmiştir. Çalışma I'de, SF 36'nın fiziksel ve zihinsel bileşenlerinin toplam skorlanndaki düzelmeler de plaseboya göre anlamlıdır.
Açık etiketli bir uzatma çalışmasında, PASI skorunun %50'nin altında olması nedeniyle dozu iki haftada bir 40 mg'dan haftada 40 mg'a yükseltilen hastalar, doz yükseltildikten 12 hafta sonra değerlendirildiğinde, hastaların 93/349'unda (%26.6) yeniden PASI 75 yanıtı elde edilmiştir.
İmmünoienite
Anti-adalimumab antikorlarının oluşumu, adalimumabın klerensinde artış, etkinliğinde ise azalma ile ilişkilidir. Anti-adalimumab antikorları varlığıyla advers olaylar arasında görünür bir bağıntı bulunmamaktadır.
RA Çalışmaları I, II ve IIP deki hastalar, 6'dan 12. aya kadar olan dönemde anti-adalimumab antikorları bakımından çok sayıda zaman noktasında test edilmiştir. Pivotal çalışmalarda, anti-adalimumab antikorları, adalimumab ile tedavi edilen 1053 hastanın 58'inde (%5.5) saptanmış, plasebo ile bu oran 2/370 (%0.5) olmuştur. Eş zamanlı metotreksat verilmeyen hastalarda insidans %12.4 iken, adalimumabın metotreksata ilave olarak verildiği hastalarda %0.6 idi.
Poliartiküler jüvenil idiyopatik artrit hastalarında, adalimumab ile tedavi edilen 171 hastanın 27'sinde (%15.8) adalimumab antikorları saptanmıştır. Eş zamanlı metotreksat verilmeyen hastalarda insidans 22/86 (%25.6) iken, adalimumabın metotreksata ilave olarak verildiği hastalarda 5/85 (%5.9) oldu.
Psöriyatik artritli hastalarda anti-adalimumab antikorları, adalimumab ile tedavi edilen 376 hastanın 38'inde (%10) saptanmıştır. Eş zamanlı metotreksat verilmeyen hastalarda insidans %13.5 (24/178 hasta) iken, adalimumabın metotreksata ilave olarak verildiği hastalarda %7 oldu (198 hastadan 14'ü).
Ankilozan spondilitli hastalarda anti-adalimumab antikorları, adalimumab ile tedavi edilen 204 hastanın 17'sinde (%8.3) saptanmıştır. Eş zamanlı metotreksat verilmeyen hastalarda insidans 16/185 (%8.6) iken, adalimumabın metotreksata ilave olarak verildiği hastalarda 1/19 (%5.3) oldu.
Crohn hastalığı olan hastalarda anti-adalimumab antikorları, adalimumab ile tedavi edilen 269 hastanın
T
sinde (%2.6) saptanmıştır ve ülseratif kolit hastalığı olan hastalarda ise 487 hastanın 19 'sinde ( %3.9) saptanmıştır.Psöriyazisli hastalarda anti-adalimumab antikorları, adalimumab ile tedavi edilen 920 hastanın
İT
sinde (%8.4) saptanmıştır.İmmunojenisite analizleri ürün için spesifik olduğundan bu üründeki antikor oranlarının başka ürünlerle karşılaştırılması uygun değildir.
5.2 Farmakokinetik özellikler
Emilim:
40 mg'lık tek bir dozun subkütan uygulanmasından sonra adalimumabın absorpsiyonu ve dağılımı yavaştır ve doruk serum konsantrasyonlarına uygulamadan yaklaşık 5 gün sonra ulaşılmaktadır. HUMIRA ile yapılan 3 çalışmada, 40 mg'lık tek bir subkütan dozu takiben, ortalama mutlak biyoyararlanımı %64 olmuştur. 0.25 ile 10 mg/kg arasında değişen tek intravenöz dozdan sonraki konsantrasyonlar dozla orantılıdır.Dağılım:
0.5 mg/kg (-40 mg) dozlarından sonra klerensler tipik olarak 11-15 ml/saat arasında olup dağılım hacmi (Vss) 5-6 litre arasında ve ortalama terminal faz yarı ömrü ortalama iki haftadır. Bir kaç romatoid artritli hastada sinovyal sıvıdaki adalimumab konsantrasyonları, serum konsantrasyonlarına göre %31 -96 arasında değişmektedir. Romatoid artritli hastalarda2 haftada bir 40 mg dozunda subkütan HUMIRA uygulamasını takiben ortalama kararlı durum konsantrasyonları eş zamanlı uygulanan metotreksat olmaksızın yaklaşık 5 mikrogram/ml ve eş zamanlı uygulanan metotreksat ile 8-9 mikrogram/ml'dır. Kararlı durumda serum adalimumabın çukur düzeyleri 2 haftada bir ve haftada bir 20, 40 ve 80 mg'lık subkütan dozu takiben doz ile kabaca orantılı biçimde yükselmiştir. Romatoid artrit hastalarının sinovyal sıvılarındaki adalimumab konsantrasyonları serumdaki konsantrasyonun %31-%96'sı arasındadır.
Poliartiküler jüvenil idiyopatik artrit (JIA) hastalarına iki haftada bir subkutan olarak 24 mg/m2 (maksimum 40 mg'a kadar) uygulanmasının ardından kararlı durum serum adalimumab çukur konsantrasyonu, HUMIRA monoterapide 5.6 ± 5.6 ng/ml (%102 CV) ve metotreksat ile birlikte 10.9 ± 5.2 jag/ml'dir (%47.7 CV).
Crohn hastalığı olan hastalarda, 0. haftada 80 mg HUMIRA yükleme dozunu takiben 2. haftada 40 mg HUMIRA dozu ile indüksiyon döneminde ortalama 5.5 mikrogram/ml olan serum adalimumab vadi konsantrasyonlarına ulaşılmıştır. 0. haftada 160 mg HUMIRA yükleme dozunu takiben 2. haftada 80 mg HUMIRA ile, indüksiyon döneminde ortalama
12 mikrogram/ml serum adalimumab vadi konsantrasyonlarına ulaşılmıştır. İki haftada bir 40 mg HUMIRA idame dozu alan Crohn hastalığı hastalarında ortalama 7 mikrogram/ml olein ortalama kararlı durum vadi düzeyleri gözlemlenmiştir.
Psöriyazisli hastalarda, iki haftada bir adalimumab 40 mg monoterapisiyle 5 mikrogram/ml olan ortalama kararlı durum vadi konsantrasyonuna ulaşılmıştır.
Bivotransformasvon:
Serbest adalimumabın (anti-adalimumab antikorlara (AAA) bağlanmayan) serum düzeylerinin ölçülebilir AAA bulunan hastalarda daha düşük olduğu gözlemlenmiştir.Eliminasvon:
1300'den fazla hastadan alman veriler üzerinde yürütülen popülasyon farmakokinetik analizleri, adalimumab görünür klirensinin vücut ağırlığında artış ile arttığını açığa çıkarmıştır. Kilo farklılıklarına göre uyarlama yapıldıktan sonra, cinsiyet ve yaşın adalimumab klirensini minimal düzeyde etkiledikleri görülmüştür.HUMIRA ile çocuklarda veya hepatik ya da renal bozukluğu olan hastalarda çalışma yapılmamıştır.
5.3 Klinik öncesi güvenlilik verileri
Klinik öncesi veriler tek doz toksisitesi, yinelenen doz toksisitesi ve genotoksisite çalışmalarına dayanarak insanlarda özel bir tehlike olmadığını göstermiştir.Sinomologus maymunlarında 0, 30 ve 100 mg/kg dozlarında bir embriyo-fetal gelişimsel toksisite/perinatal gelişim çalışması yapılmış (her bir grupta 9-17 maymun vardır) ve fetüslerde adalimumaba bağlı hasara ilişkin bulgular görülmemiştir. Adalimumab ile karsinojenisite çalışmaları, fertilite ve postnatal toksisite için standart değerlendirme çalışmaları yapılmamıştır çünkü kemirgen TNF'sine karşı sınırlı çapraz reaktivitesı olan bir antikor ve kemirgenlerde nötralizan antikor gelişimi için uygun bir model bulunmamaktadır.
6. FARMASÖTİK ÖZELLİKLER 6.1. Yardımcı maddelerin listesi
MannitolSitrik asit monohidrat Sodyum sitrat Disodyum fosfat dihidrat
Sodyum dihidrojen fosfat dihidrat Sodyum klorür Polisorbat 80 Enjeksiyonluk su Sodyum hidroksit
6.2 Geçimsizlikler
Geçimlilik çalışmaları bulunmadığından bu tıbbi ürün başka tıbbi ürünlerle karıştırılmamalıdır.6.3 Raf ömrü
Raf ömrü 24 aydır.Bu ilaç, kutusu üzerindeki son kullanım tarihi geçtikten sonra kullanılmamalıdır.
6.4 Saklamaya yönelik özel tedbirler
2-8°C'de buzdolabında saklanmalıdır. Enjektör kullanım anına kadar kutusunun içinde muhafaza edilmelidir. Dondurulmamalıdır.6.5 Ambalajın niteliği ve içeriği
Birincil ambalaj:
Avr. Farm. 3.2.1 ve USP <660> Kimyasal dirençli cam konteynerler, Tip I: Cam tipi I Krom-nikel çelik
Avr. Farm. 3.2.9, bromobutil lastik tıpa tip I ve USP <381> Enjektörler için elastomer tıpa
Avr. Farm. 3.2.9 lastik tıpa tip II(Isı sterilizasyonu sonrası) ve USP <381> Enjektörler için lateks içermeyen thermoplastik elestomer kılıf
Avr. Farm. 3.2.9, bromobutil lastik tıpa tip I ve USP <381> Enjektörler için elastomer tıpa
Avr. Farm. 3.2.9 lastik tıpa tip II(Isı sterilizasyonu sonrası) ve USP <381> Enjektörler için lateks içermeyen thermoplastik elestomer kılıf
Cam silindir:
İğne-29 Gf Gri piston contası:
Gri iğne kılıfı:
İkincil ambalaj:
Geniş flanşlı piston: Polistiren
Kanatlı geri stop: Polipropilen
Koruyucu (İğne kılfı için): Polipropilen
6.6 Beşeri tıbbi üründen arta kalan maddelerin imhası ve diğer özel önlemler
HUMIRA (Adalimumab 40 mg) Enjeksiyonluk Çözelti İçeren Kullanıma Hazır Enjektör bir doktorun rehberliği ve gözetimi altında kullanılmak içindir. Gerekli uygun tıbbi takibin yapılması ve uygun enjeksiyon tekniğinin hastaya yeterince öğretilmesinden sonra doktorun karar vermesi durumunda hasta HUMIRA enjeksiyonunu kendi kendine uygulayabilir.HUMIRA, aynı enjektör veya flakonda başka bir ilaç ile karıştırılmamalıdır.
Tüm kullanılmayan ürün veya atık maddeler ulusal mevzuat doğrultusunda imha edilmelidir.
7.
RUHSAT SAHİBİ
AbbVie Tıbbi İlaçlar Sanayi ve Ticaret Limited Şirketi Saray Mah. Dr. Adnan Büyükdeniz Cad.No:2 Akkom Ofis Park Kelif Plaza 3.Blok Kat 16-17,
Ümraniye /İstanbul
TelFaks
: 0216 425 09 698. RUHSAT NUMARASI
134/809. İLK RUHSAT TARİHİ/RUHSAT YENİLEME TARİHİ
İlk ruhsat tarihi: 10.12.201210. KÜB'ÜN YENİLENME TARİHİ
1p<0.01
M02-404 çalışmasında 4. haftada hastaların %58'i (499/854) klinik yanıt vermiş ve primer analizde değerlendirilmiştir. Dördüncü haftada klinik yanıt verenlerden %48'i daha önce başka anti-TNF tedaviler uygulanmış olan hastalardır. Dördüncü haftada klinik remisyona giren hastalar içinde, 26 ve 56. haftalarda klinik yanıt veren hastaların oranı, plasebo idame gruplarıyla karşılaştırıldığında, HUMIRA idame gruplarında istatistiksel olarak anlamlı ölçüde daha fazladır. İlaveten, başlangıçta konkomitan kortikosteroid alan hastalar içinde, 26
İlaç Bilgileri
Humira Enjeksiyonluk Çözelti İçeren(adalimumab 40...
Etken Maddesi: Adalimumab
Atc Kodu: L04AB04
Kullanma talimatı ve kısa ürün bilgileri
Ana Sayfa | Hakkımızda | İlaçlar | İlaç Ara | İlaç Firmaları | Gizlilik | Bize Ulaşın
Telif Hakkı 2008-2026 © İlaç Prospektüsü. Tüm Hakları Saklıdır.Uyarı: Sitemizde yayınladığımız ilaç bilgileri ile doktora danışmadan kesinlikle ilaç kullanmayınız!
Aksi halde doğabilecek sağlık sorunlarından ilacprospektusu.com sorumlu tutulamaz.