İmatenil 200 mg Kapsül Kısa Ürün BilgisiAntineoplastik ve İmmünomodülatör Ajanlar » Antineoplastik İlaçlar (Kanser İlaçları) » Diğer Kanser İlaçları » Protein Kinaz İnhibitörleri » Imatinib KISA URUNBILGISI1.BEŞERI TıBBı ÜRÜNÜNADIİMATENİL 200 mg kapsül2.KALITATIF VE KANTİTATIF BİLEŞİMEtkin madde:Her bir kapsül 200 mg imatinib'e eşdeğer miktarda 240,96 mg imatinib mesilat içerir.Yardımcı maddeler:Yardımcı maddeler için 6.1'e bakınız.3.FARMASÖTIK FORMKapsülKrem rengi kapsül içinde beyaz toz. 4.KLINIK ÖZELLIKLER4.1. Terapötik endikasyonlarİMATENİL'in endikasyonları:Yeni tanı konmuş Philadelphia kromozomu pozitif kronik faz kronik miyeloid lösemi (KML) hastalarında, Akselere faz Philadelphia kromozomu pozitif kronik miyeloid lösemi (KML) hastalarında, Blastik faz Philadelphia kromozomu pozitif kronik miyeloid lösemi (KML) hastalarında, Diğer tedavilere dirençli Philadelphia kromozomu pozitif kronik miyeloid lösemi (KML) hastalarında, İlk tanısı Philadelphia kromozomu pozitif kronik miyeloid lösemi (KML) olan ancak tedavi ile Philadelphia kromozomu negatif hale gelen kronik/akselere/blastik faz kronik miyeloid lösemi hastalarında, Kronik miyeloid lösemili (KML) olan 3 yaş ve üzerindeki çocuklarda birinci basamak tedavide, Yeni tanı konulmuş Philadelphia kromozomu pozitif akut lenfoblastik lösemi (Ph+ ALL) hastalarında klinik yararı gösterilmiş çoklu ajanlı kemoterapi şemaları ile kombine olarak remisyon indüksiyonu amacıyla, Relaps-refrakter Philadelphia kromozomu pozitif akut lenfoblastik lösemi (Ph+ ALL) hastalarında klinik yararı gösterilmiş çoklu ajanlı kemoterapi şemaları ile kombine olarak remisyon indüksiyonu amacıyla, FIP1L1-PDGFRA füzyon geni laboratuvar incelemeleriyle gösterilen hipereozinofilik sendrom ve sistemik mastositoz hastalarında kullanılabilir. İmatinibin etkinliği, KML vakalarındaki bir bütün olarak hematolojik ve sitogenetik yanıt oranları ve hastalıksız sağkalım süresi ve Philadelphia kromozomu pozitif akut lenfoblastik lösemi (Ph+ ALL) vakalarındaki hematolojik ve sitogenetik sağkalım oranları, sistemik mastositoz (SM), hipereozinofilik sendrom (HES) vakalarındaki hematolojik yanıt oranları (bkz. Bölüm 5.1 Farmakodinamik özellikler) göz önünde tutularak değerlendirilmektedir. Yeni tanı konulmuş kronik fazda bulunan KML hastaları dışında, sağkalım süresinin uzadığını gösteren, kontrol grubuna yer verilerek yapılmış herhangi bir çalışma yoktur. 4.2. Pozoloji ve uygulama şekli Pozoloji/uygulama sıklığı ve süresi:Tedavi, hematolojik malign hastalıklar ve malign sarkomlar bulunan hastaların tedavisinde deneyimi olan bir doktor tarafından başlatılmalıdır.Kronik Miyeloid Lösemi'de (KML) Dozaj Kronik faz KML bulunan hastalar için önerilen İMATENİL dozajı 400 mg/gün, hızlanmış faz ya da blast krizi bulunanlar için önerilen dozaj ise 600 mg/gün'dür. Tedavi, hastaya yarar sağladığı sürece devam ettirilmelidir. İlaca bağlı oluşan ciddi advers etki ve ağır lösemiyle ilişkili nötropeni veya trombositopeni gelişmemiş olması koşuluyla, hastalığın ilerlemesi (herhangi bir zamanda), en az 6 aylık tedaviden sonra tatmin edici bir hematolojik yanıt alınamaması, 12 aylık tedaviye rağmen sitogenetik cevap elde edilmemesi veya daha önce elde edilmiş olan hematolojik ve/veya sitogenetik yanıtın kaybolması gibi durumlarda; kronik fazda hastalık bulunanlarda dozun 400 mg'dan 600 mg'a yükseltilmesi, ya da hızlanmış faz veya blast krizi bulunan hastalarda da dozun 600 mg'dan maksimum 800 mg günlük doza yükseltilmesi düşünülebilir. Çocuklardaki pozoloji, vücut yüzölçümüne göre, mg/m2 olarak hesaplanmaktadır. Kronik ve ilerlemiş faz KML vakalarında önerilen pediyatrik dozlar, günde 340 mg/m2'dir. Ancak çocuklarda kullanılan total günlük doz, erişkinlerdeki sırasıyla 400 ve 600 miligramlık eşdeğerlerini aşmamalıdır. Günlük doz, 1 defada ya da biri sabah, diğeri akşam olmak üzere 2 defada verilebilir. Dozaj önerileri şimdilik, az sayıdaki pediyatrik hastada kazanılan tecrübeyi temel almaktadır (bkz. 5.1 Farmakodinamik özellikler ve 5.2 Farmakokinetik özellikler). İmatinibin 2 yaşından küçük çocuklarda kullanılması konusunda herhangi bir tecrübe mevcut değildir. Philadelphia Kromozomu Pozitif, Akut Lenfoblastik Lösemi'de (Ph+ ALL) Dozaj Ph+ ALL hastalarında önerilen İMATENİL dozajı, remisyon indüksiyon kemoterapi şemaları çerçevesinde belirlenir. Hipereozinofilik Sendrom ve Sistemik Mastositoz'da Dozaj Hipereozinofilik sendrom ve sistemik mastositoz hastalarında önerilen İMATENİL dozajı, günde 100 mg'dır. Yanıtsız hallerde 400 mg'a dek çıkılabilir. Bu doz aşılamaz. Tedavi, hasta fayda gördüğü sürece devam ettirilmelidir. Advers reaksiyonlar için doz ayarlamaları Hematolojik olmayan advers reaksiyonlar İMATENİL kullanıldığında eğer ciddi hematolojik olmayan advers reaksiyon gelişirse, tedavi bu olay ortadan kalkıncaya kadar durdurulmalıdır. Daha sonra, olayın ilk ciddiyetine göre değişecek şekilde tedavi devam ettirilir. Eğer bilirubin, normal sınırın üst limitini (NSÜL) 3 kattan fazla aşacak şekilde yükselirse ya da karaciğer transaminazlarında NSÜL değerinin 5 katından fazla artış olursa, İMATENİL, bilirubin düzeyleri < 1.5 x NSÜL ve transaminaz düzeyleri < 2.5 x NSÜL seviyesine ininceye kadar durdurulmalı ve daha sonra da azaltılmış günlük dozlarla devam ettirilmelidir. Yetişkinlerde doz 400 mg'dan 300 mg'a veya 600 mg'dan 400 mg'a veya 800 mg'dan 600 mg'a, çocuklarda ise 260 mg/m2/gün'den 200 mg/m2/gün'e veya 340 mg/m2/gün'den 260 mg/m2/gün'e düşürülmelidir. Hematolojik advers reaksiyonlar Ağır nötropeni ve trombositopeni geliştiği takdirde dozun azaltılması ya da tedavinin kesilmesi aşağıdaki tabloda belirtildiği şekilde düzenlenmelidir. Tablo 1.Nötropeni ve trombositopeni için doz ayarlamalarıEozinofili ile ilişkili SM ve FIP1L1-PDGFR-alfa füzyon kinaz ile birlikte HES (başlangıç dozu 100 mg)
ANC < 1.0 x 109/L
1.ANC > 1.5 x 109/L ve trombosit sayısı > 75 x 109/L oluncaya kadar İMATENİL durdurulur.ve/veya Trombosit sayısı < 50 x 109/L 2.İMATENİL tedavisine önceki dozda (yani ciddi advers reaksiyon gerçekleşmeden önceki dozda) devam edilir. Kronik faz KML, SM ve HES (başlangıç dozu 400 mg)b
ANC < 1.0 x 109/L
1.ANC > 1.5 x 109/L ve trombositler > 75 x 109/L oluncaya kadar İMATENİL'i kesin.ve/veya Trombositler <50 x 109/L 2.Tedaviye önceki İMATENİL dozu ile (ciddi advers reaksiyon gelişmesinden önce) yeniden başlayın. 3.ANC < 1.0 x109/L ve/veya trombositler < 50 x109/L olacak şekilde olay tekrarladığında, 1. basamağı tekrarlayın ve İMATENİL'e azaltılmış olarak 300 mg'lık dozla başlayın. d Pediyatrik kronik fazda KML (340 mg/m dozda)
ANC < 1.0 x 109/L
1.ANC > 1.5 x 109/L ve trombosit sayısı > 75 x 109/L oluncaya kadar İMATENİL durdurulur.ve/veya Trombosit sayısı < 50 x 109/L 2.İMATENİL tedavisine önceki dozda (yani ciddi advers reaksiyon gerçekleşmeden önceki dozda) devam edilir. 3.ANC < 1.0 x109/L ve/veya trombosit sayısının < 50 x109/L olduğu durum yinelendiği takdirde, 1. adım yeniden uygulanır ve İMATENİL tedavisine doz 260 mg/m2'ye düşürülerek devam edilir. Hızlanmış faz KML ve blast krizi ve Ph+ALL (başlangıç dozu 600 mg)c
aANC < 0.5 x109/L
1.Sitopeninin lösemiye bağlı olup olmadığını kontrol edin (kemik iliği aspiratı ya da biyopsisi)ve/veya Trombositler < 10 x 109/L 2.Eğer sitopeni lökopeniye bağlı değil ise İMATENİL dozunu 400 mg'a düşürün.b 3.Eğer sitopeni 2 hafta devam ederse, dozu 300 mg'a düşürün.d 4.Eğer sitopeni 4 hafta devam ederse ve hala lösemiyle ilişkili değil ise ANC > 1 x 10 /L ve trombositler > 20 x 10 /L oluncaya kadar İMATENİL'i durdurun ve daha sonra 300 mg ile tedaviye başlayın.daANC= Mutlak nötrofil sayısı a en az 1 aylık tedaviden sonra ortaya çıkan b veya çocuklarda 260 mg/m2 c veya çocuklarda 340 mg/m d veya çocuklarda 200 mg/m2 Uygulama şekli:Reçetedeki doz yemek sırasında ve büyük bir bardak suyla yutulmalıdır. Günde 400 veya 600 miligramlık dozlar bir defada; 800 miligramlık doz ise, her birinde 400'er miligram olmak üzere sabah ve akşam iki bölümde alınmalıdır.Özel popülasyonlara ilişkin ek bilgiler: Karaciğer yetmezliği:İmatinib, temel olarak karaciğer yoluyla metabolize olur. Hafif, orta şiddette veya şiddetli karaciğer fonksiyon bozukluğu olan hastalara, önerilen minimal doz olan günde 400 mg verilmelidir. Bu doz, tolere edilemediği takdirde azaltılabilir (bkz. Bölüm 4.4 Özel kullanım uyarıları ve önlemleri, 4.8 İstenmeyen etkiler, 5.1 Farmakodinamik özellikler ve 5.2 Farmakokinetik özellikler).Böbrek yetmezliği:İmatinib ve metabolitleri böbrek yoluyla önemli miktarda atılmazlar. İmatinib'in böbrek klerensi çok az olduğu için, böbrek yetmezliği bulunan hastalarda serbest ilaç klerensinde bir azalma beklenmez. Hafif ya da orta şiddette böbrek yetmezliği olan hastalara (Kreatinin klerensi: hafif; KrCL: 40-59 ml/dakika ve şiddetli; KrCL: <20 ml/dakika) böbrek bozukluğu başlangıç dozu olarak, önerilen minimum doz, günlük 400 mg verilmelidir. Eldeki bilgiler çok sınırlı olmasına rağmen (bkz. 5.1 Farmakodinamik özellikler ve 5.2 Farmakokinetik özellikler), şiddetli böbrek yetmezliği olan ya da diyaliz gören hastalara da 400 mg'lık aynı dozda başlanabilir. Bununla birlikte, bu hastalarda dikkatli olunması önerilir. Tolere edilememesi halinde doz azaltılabilir ya da etki görülmemesi halinde doz arttırılabilir (bkz. 4.4 Özel kullanım uyarıları ve önlemleri).Pediyatrik popülasyon:İmatinibin KML endikasyonunda 2 yaşın altındaki çocuklarda kullanımıyla ilgili herhangi bir deneyim bulunmamaktadır. İmatinibin diğer endikasyonlarda 3 yaşından küçük çocuklarda kullanılması konusundaki tecrübeler çok sınırlıdır.Geriyatrik popülasyon:Yaşlılarda spesifik olarak imatinib farmakokinetiği araştırılmamıştır.Katılan hastaların %20'sinden fazlasının 65 ve daha yukarı yaşlarda olduğu klinik çalışmalarda, yetişkin hastalarda yaşla ilişkili anlamlı farmakokinetik farklılıklar gözlenmemiştir. Yaşlılarda, özel bir doz önerisi gerekli değildir. 4.3.KontrendikasyonlarAktif maddeye veya eksipiyanlardan herhangi birine karşı aşırı duyarlılık.4.4.Özel kullanım uyarıları ve önlemleriİMATENİL gastrointestinal rahatsızlık riskini minimuma indirmek için gıdalarla ya da büyük bir bardak suyla birlikte alınmalıdır.İMATENİL, başka ilaçlarla eşzamanlı olarak kullanıldığında önemli ilaç etkileşimleri görülme potansiyeli bulunmaktadır (bkz. Bölüm 4.5 Diğer tıbbi ürünler ile etkileşimler ve diğer etkileşim şekilleri). Ateş düşürücü olarak düzenli aralıklarla parasetamol (asetaminofen) alan bir hastanın akut karaciğer yetmezliği nedeniyle öldüğü bildirilmiştir. Etiyolojisi tam olarak bilinmemekle beraber, parasetamol/asetaminofen kullanımında dikkatli olunmalıdır (bkz. 4.5 Diğer tıbbi ürünler ile etkileşimler ve diğer etkileşim şekilleri). İmatinib tedavisi sırasında levotiroksin replasmanı yapılan tiroidektomi hastalarında klinik hipotiroidizm olguları bildirilmiştir. Bu tür hastalarda TSH düzeyleri yakından izlenmelidir. Karaciğer disfonksiyonu (hafif, orta şiddette ve şiddetli) olan hastalarda, periferik kan sayımları ve karaciğer enzimleri dikkatli bir şekilde izlenmelidir (bkz. 4.2 Pozoloji ve uygulama şekli, 4.8 İstenmeyen etkiler, 5.1 Farmakodinamik özellikler, 5.2 Farmakokinetik özellikler). İmatinib, yüksek doz kemoterapi kürleriyle birlikte kullanıldığında transaminaz ve bilirubin düzeylerinin yükselmesi şeklinde, geçici karaciğer toksisitesi görülmüştür. Buna ilave olarak yaygın olmayan akut karaciğer yetmezliği rapor edilmiştir. İmatinib, karaciğer fonksiyon bozukluğu potansiyeli olan kemoterapi kürleriyle birlikte kullanılacaksa, karaciğer fonksiyonlarının izlenmesi tavsiye edilir (bkz. 4.8 İstenmeyen etkiler). İmatinib alan yeni tanı konulmuş KML hastalarının yaklaşık %2,5'inde ciddi sıvı retansiyonu (plevra efüzyonu, ödem, pulmoner ödem, asit, yüzeysel ödem) ortaya çıktığı bildirilmiştir. Bu nedenle, hastalarda düzenli aralıklarla kilo kontrolü önerilir. Beklenmedik, ani bir kilo artışı dikkatli araştırılmalı ve gerektiğinde uygun destek tedavisi uygulanmalı ve terapötik önlemler alınmalıdır. Klinik çalışmalarda, yaşlı hastalarda ve daha önceden kardiyak hastalık hikayesi bulunanlarda bu olayların insidanslarının arttığı saptanmıştır. Kalp hastalığı ya da kalp yetmezliği açısından risk faktörleri bulunan hastalar dikkatlice takip edilmeli, kalp yetmezliğini düşündüren belirti ve semptomları olan her hasta değerlendirilmeli ve tedavi edilmelidir. Kardiyak komplikasyonların geliştiği hipereozinofilik sendromu (HES) olan hastalarda imatinib tedavisine başlanmasına, izole kardiyojenik şok/sol ventrikül disfonksiyon eşlik etmiştir. Bu durumun sistemik steroidler kullanılarak, dolaşımı destekleyen önlemler alarak ve imatinib tedavisini geçici olarak durdurarak düzeltilebileceği bildirilmiştir. Sistemik mastositoz, yüksek eozinofil düzeyleri ile ilişkili olabilir. Bu nedenle, eozinofil düzeylerinin yüksek olduğu SM vakalarında ve HES vakalarında ekokardiyografik inceleme yapılmalı ve serum troponin düzeyleri ölçülmelidir. Bunlardan birinde anormallik tespit edilirse, tedavi başlangıcında imatinible birlikte 1-2 hafta boyunca 1-2 mg/kg dozunda sistemik steroid kullanılması düşünülmelidir. Laboratuvar testleri İMATENİL ile tedavi sırasında düzenli olarak tam kan sayımları yapılmalıdır. KML hastalarında imatinib tedavisine, nötropeni ya da trombositopeni eşlik etmiştir. Bununla birlikte, bu sitopenilerin ortaya çıkışı, hastalığın tedavi edildiği evreye bağlıdır ve kronik fazda KML bulunan hastalarla karşılaştırıldığında, hızlanmış fazda KML ya da blast krizinde bulunan hastalarda daha sık olmaktadır. 4.2 Pozoloji ve uygulama şekli bölümünde önerildiği gibi İMATENİL tedavisi kesilebilir ya da dozu azaltılabilir. İMATENİL alan hastalarda karaciğer fonksiyonu (transaminazlar, bilirubin, alkalin fosfataz) düzenli olarak takip edilmelidir. 4.2 Pozoloji ve uygulama şekli, Hematolojik olmayan advers reaksiyonlar bölümünde önerildiği gibi bu laboratuvar anormallikleri, İMATENİL tedavisi kesilerek ve/veya dozu azaltılarak kontrol edilmelidir. İMATENİL ve metabolitleri böbrek yoluyla önemli bir miktarda atılmazlar. Kreatinin klerensinin (KrCL) yaşla birlikte azaldığı bilinmektedir ve yaş imatinib kinetiğini anlamlı olarak etkilememektedir. Böbrek fonksiyonları bozuk hastalarda, imatinib plazma maruziyeti böbrek fonksiyonları normal hastalardakinden daha yüksek görünmektedir (muhtemelen, imatinib-bağlayıcı bir protein olan alfa-asit glikoprotein (AGP) plazma düzeylerinin bu hastalarda daha yüksek olması nedeniyle). KrCL ölçümü ile sınıflandırıldığında, hafif (KrCL: 40-59 ml/dakika) ve şiddetli (KrCL: < 20 ml/dakika) böbrek bozukluğu olan hastalar arasında maruz kalınan imatinib ile böbrek bozukluğunun derecesi arasında herhangi bir korelasyon yoktur. Ancak, 4.2 Pozoloji ve uygulama şekli bölümünde önerildiği gibi, tolere edilemezse imatinib başlangıç dozu düşürülebilir. 4.5. Diğer tıbbi ürünler ile etkileşimler ve diğer etkileşim şekilleriİmatinibin plazma konsantrasyonlarını değiştiren ilaçlar İmatinibin plazma konsantrasyonlarını arttırabilen ilaçlar:Sitokrom P450 izoenzimlerinden CYP3A4 aktivitesini inhibe eden maddeler (örn. ketokonazol, itrakonazol, eritromisin, klaritromisin) metabolizmayı azaltabilir ve imatinib konsantrasyonlarını arttırabilirler. Sağlıklı deneklere tek doz ketokonazol (bir CYP3A4 inhibitörü) ile birlikte uygulandığında, imatinibe maruz kalma durumunda anlamlı bir artış ortaya çıkmıştır (imatinibin ortalama Cmaks ve EAA değerleri sırasıyla %26 ve %40 artmıştır). İMATENİL, CYP3A4 izoenziminin inhibitörleri ile birlikte verilirken dikkatli olunmalıdır. İmatinibin plazma konsantrasyonlarını azaltabilen ilaçlar: CYP3A4 aktivitesini uyaran maddeler metabolizmayı arttırabilir ve imatinibin plazma konsantrasyonlarını azaltabilirler. CYP3A4 indüksiyonu yapan ilaçlarla (örn. deksametazon, fenitoin, karbamazepin, rifampisin, fenobarbital ya da St. John's Worth olarak da bilinen Hypericum perforatum)eşzamanlı uygulama İMATENİL'e maruz kalmayı azaltabilir. Sağlıklı 14 gönüllünün 8 gün boyunca günde 600 mg rifampisin kullanmasından sonra verilen, 400 miligramlık tek doz imatinib, oral doz klerensini 3.8 kat arttırmıştır (%90 güven aralığı 3.5-4.5). Bu artış, ortalama Cmaks, EAA(0-24 saat) ve EAA(0-^) değerlerinin, daha önce rifampin kullanılmamasına kıyasla sırasıyla %54, %68 ve %74 azalması demektir. Karbamazepin, okskarbazepin, fenitoin, fosfenitoin, fenobarbital ve primidon gibi enzim indükleyici anti-epileptik ilaçlar (AEİ) kullanırken imatinib ile tedavi edilen malign gliyomlu hastalarda da benzer sonuçlar gözlenmiştir. İmatinib için plazma EAA değeri, AEİ'ler kullanmayan hastalarla karşılaştırıldığında %73 oranında azalmıştır.Yayınlanmış iki çalışmada, imatinib ve St. John's Worth içeren bir ürünün birlikte uygulanması imatinib EAA değerinde %30-32'lik bir azalmaya yol açmıştır. Rifampin veya CYP3A4 indüksiyonu yapan diğer ilaçların kullanılmasına ihtiyaç olduğunda, enzim indüksiyon potansiyeli daha az olan, başka ilaçların kullanılması düşünülmelidir. İmatinib ile plazma konsantrasyonu değişebilen ilaçlar: İmatinib, simvastatinin (CYP3A4 substratı) ortalama Cmaks ve EAA değerlerini sırasıyla 2 ve 3,5 kat arttırmaktadır ve bu durum CYP3A4'ün imatinib tarafından inhibe edildiğini göstermektedir. Bu nedenle İMATENİL, dar bir terapötik pencereye sahip CYP3A4 substratlarıyla (örn. siklosporin ya da pimozid) birlikte uygulandığında dikkatli olunmalıdır. İMATENİL, diğer CYP3A tarafından metabolize edilen ilaçların da plazma konsantrasyonunu arttırabilir (örn. triazolo-benzodiazepinler, dihidropiridin kalsiyum kanal blokörleri, bazı HMG-KoA redüktaz inhibitörleri, örn. statinler, vs.). İmatinib, aynı zamanda in vitro olarak CYP2C9 ve CYP2C19 aktivitesini de inhibe etmektedir. Varfarin ile eşzamanlı uygulama sırasında protrombin zamanı (PZ) uzaması gözlenmiştir. Kumarinler verildiğinde İMATENİL tedavisinin başında ve sonunda ve dozaj değiştirildiğinde kısa vadeli PZ takibi gereklidir. Alternatif olarak, düşük moleküler ağırlıklı heparin düşünülmelidir. İn vitro olarak imatinib, CYP3A4 aktivitesini etkileyen konsantrasyonların benzeri konsantrasyonlarda sitokrom P450 izoenzimlerinden CYP2D6 aktivitesini de inhibe etmektedir. Günde iki kez 400 mg dozda uygulanan imatinibin CYP2D6-aracılı metoprolol metabolizması üzerinde zayıf bir inhibitör etkisi vardır; metoprolol Cmaks ve EAA değerleri yaklaşık %23 kadar artar. Metoprolol gibi CYP2D6 substratlarının imatinib ile birlikte uygulanması, ilaç-ilaç etkileşimi açısından bir risk faktörü olarak görünmemektedir ve doz ayarlaması gerekli olmayabilir. İmatinib, parasetamolün in vitro O-glukuronidasyonunu inhibe eder (terapötik düzeylerdeki Ki değeri 58,5 mikromol/L) (bkz. 4.4 Özel kullanım uyarıları ve önlemleri). 4.6. Gebelik ve laktasyon Genel tavsiyeGebelik kategorisi D'dir.Çocuk doğurma potansiyeli bulunan kadınlar/Doğum kontrolü (Kontrasepsiyon)Çocuk doğurma potansiyeli bulunan kadınlara tedavi sırasında etkili bir kontrasepsiyon uygulamaları önerilmelidir.Gebelik dönemiİmatinibin gebe kadınlarda kullanımına ilişkin yeterli veri mevcut değildir. Hayvanlar üzerinde yapılan araştırmalar üreme toksisitesinin bulunduğunu göstermiştir (bkz. 5.3 Klinik öncesi güvenlilik verileri). İnsanlara yönelik potansiyel risk bilinmemektedir. İMATENİL, açıkça gerekli olmadığı sürece gebelik sırasında kullanılmamalıdır. Gebelik sırasında kullanılması durumunda, hastaya fetüs üzerindeki potansiyel riskleri hakkında bilgi verilmelidir.Laktasyon dönemiHem imatinib, hem de aktif metaboliti anne sütüne geçebilir. Süt/plazma oranı imatinib için 0,5, metaboliti için ise 0,9 olarak saptanmıştır; bu da metabolitin süte daha büyük oranda geçtiğini düşündürmektedir. İmatinib ve metabolitinin toplam konsantrasyonu ve bebeklerin maksimum günlük süt alımı düşünüldüğünde, toplam maruziyetin düşük olması beklenir (bir terapötik dozun ~%10'u). Bununla birlikte, bebeğin imatinibe düşük dozlarda maruz kalmasının etkileri bilinmediğinden, İMATENİL kullanan anneler bebeklerini emzirmemelidir.4.7.Araç ve makine kullanımı üzerindeki etkilerYeterli veriler olmasa da, hastalara imatinib ile tedavi sırasında baş dönmesi ya da bulanık görme gibi istenmeyen etkiler yaşayabilecekleri bildirilmelidir. Bu nedenle, araba ya da araç kullanırken dikkatli olunması önerilmelidir.4.8.istenmeyen etkilerİlerlemiş evrede maligniteler bulunan hastalarda, altta yatan hastalığa bağlı semptomların çok çeşitli olması, ilerlemesi ve beraberinde çok sayıda ilaç kullanılması nedeniyle advers olayların nedeninin saptanmasını zorlaştıran çeşitli yanıltıcı tıbbi koşullar bulunabilir.İmatinib, çocuk hastaları da içeren KML hastalarında uzun süre oral olarak her gün kullanıldığında genellikle iyi tolere edilmiştir. Hastaların büyük bölümünde, herhangi bir zamanda advers olaylar gelişmiş, ancak bunların büyük bölümü hafif-orta şiddette olmuş; klinik çalışmalara ilaçla ilişkili advers olaylar nedeniyle devam edemeyen hastaların oranı yeni teşhis edilenlerde %2,4, interferon tedavisinin başarısız kalmasının ardından geç kronik faz vakalarında %4, interferon tedavisinin başarısız kalmasının ardından hızlanmış faz vakalarında %4 ve interferon tedavisinin başarısız kalmasının ardından blast krizi vakalarında %5 olmuştur. En sık bildirilen ilaçla ilişkili advers olaylar hafif bulantı, kusma, diyare, miyalji, kas krampları ve döküntü olmuş, bunlar kolaylıkla tedavi edilmiştir. Yüzeysel ödemler, tüm çalışmaların ortak bir bulgusu olmuş, daha çok periorbital ya da alt ekstremite ödemleri şeklinde ortaya çıkmıştır. Bununla birlikte, bu ödemler nadiren ciddi olmuş, diüretiklerle, diğer destek tedavileriyle ya da bazı hastalarda imatinib dozu azaltılarak tedavi edilmiştir. İmatinib, Ph+ ALL hastalarında yüksek doz kemoterapiyle birlikte kullanıldığında, transaminaz ve bilirubin düzeylerinin yükselmesi şeklinde, geçici karaciğer toksisitesi gözlenmiştir. Plevra efüzyonları, asit, pulmoner ödem ve yüzeysel ödemle birlikte ya da ödemsiz hızlı kilo alımı gibi çeşitli advers olaylar bütün olarak "sıvı retansiyonu" şeklinde tanımlanabilir. Bu olaylar genellikle imatinib tedavisi kesilerek ve diüretiklerle ya da diğer uygun destek önlemleriyle tedavi edilebilir. Bununla birlikte, bu olayların çok azı ciddi ya da yaşamı tehdit eder nitelikte olmaktadır ve blast krizi olan birkaç hasta plevral efüzyon, konjestif kalp yetmezliği ve böbrek yetmezliğini içeren komplike bir klinik öyküyle kaybedilmiştir. Advers reaksiyonlar en sık görülen en önce olmak üzere ve şu sınıflandırma uygulanarak sıklıklarına göre sıralanmıştır: Çok yaygın (> 1/10); yaygın (> 1/100 ila < 1/10); yaygın olmayan (> 1/1.000, ila < 1/100); seyrek (> 1/10.000 ila < 1/1.000); çok seyrek (< 1/10.000); izole raporlar dahil. Aşağıda bildirilen advers reaksiyonlar ve sıklıkları, KML için yürütülen çalışmalara dayanmaktadır. KML çalışmalarında gözlenen advers reaksiyonlar Enfeksiyonlar ve enfestasyonlarYaygın olmayan: Herpes zoster, herpes simplex, nazofarenjit, pnömoni1, sinüzit, selülit, üst solunum yolu enfeksiyonu, influenza, idrar yolu enfeksiyonu, gastroenteritis, sepsis Seyrek: Fungal enfeksiyonKan ve lenf sistemi hastalıklarıÇok yaygın: Nötropeni, trombositopeni, anemi Yaygın: Pansitopeni, febril nötropeniYaygın olmayan: Trombositemi, lenfopeni, kemik iliği depresyonu, eozinofili, lenfadenopati Seyrek: Hemolitik anemi Metabolizma ve beslenme bozukluklarıYaygın: AnoreksiYaygın olmayan: Hipokalemi, iştah artışı, hipofosfatemi, iştah azalması, dehidrasyon, gut, hiperürikemi, hiperkalsemi, hiperglisemi, hiponatremi Seyrek: Hiperkalemi, hipomagnezemi Psikiyatrik hastalıklarYaygın: UykusuzlukYaygın olmayan: Depresyon, libido azalması, anksiyete Seyrek: Konfüzyon Sinir sistemi hastalıklarıÇok yaygın: Baş ağrısıYaygın: Göz kararması, parestezi, tat duyusu bozuklukları, hipoestezi Yaygın olmayan: Migren, somnolans, senkop, periferik nöropati, bellek bozukluğu, siyatik, huzursuz ayak sendromu, tremor, beyin kanaması Seyrek: Kafa-içi basıncının artması, konvülziyon, optik nörit Göz hastalıklarıYaygın: Göz kapağı ödemi, lakrimasyon artışı, konjunktiva kanaması, konjunktivit, göz kuruması, bulanık görmeYaygın olmayan: Göz tahrişi, göz ağrısı, orbita ödemi, sklera kanaması, retina kanaması, blefarit, maküla ödemi Seyrek: Katarakt, glokom, papilödem Kulak ve iç kulak hastalıklarıYaygın olmayan: Vertigo, kulak çınlaması, işitme kaybıKardiyak hastalıklarYaygın olmayan: Palpitasyonlar, taşikardi, konjestif kalp yetmezliği2, pulmoner ödem Seyrek: Aritmi, atriyal fibrilasyon, kardiyak arest, miyokard enfarktüsü, angina pektoris, perikardiyal efüzyonVasküler hastalıklar3Yaygın: Al basması, kanamaYaygın olmayan: Hipertansiyon, hematom, periferik soğukluk, hipotansiyon, Raynaud fenomeni Solunum, göğüs bozuklukları ve mediastinal hastalıklarYaygın: Dispne, burun kanaması, öksürükYaygın olmayan: Plevra efüzyonu4, faringolaringeal ağrı, farenjit Seyrek: Plevra ağrısı, pulmoner fibroz, pulmoner hipertansiyon, pulmoner kanama Gastrointestinal hastalıklarÇok yaygın: Bulantı, ishal, kusma, dispepsi, karın ağrısıYaygın: Aşırı miktarda barsak gazları, karında gerilme, gastro-özofageal reflü, kabızlık, ağız kuruması, gastrit Yaygın olmayan: Stomatit, ağız ülserasyonu, gastrointestinal kanama, geğirme, melena, özofajit, asit, gastrik ülser, kan kusma, dudak iltihabı, disfaji, pankreatit Seyrek: Kolit, ileus, enflamatuar barsak hastalığı Hepato-bilier hastalıklarYaygın: Karaciğer enzimlerinde artışYaygın olmayan: Hiperbilirubinemi, hepatit, sarılık Seyrek: Karaciğer yetmezliği5, hepatik nekroz5 Deri ve deri altı doku hastalıklarıÇok yaygın: Periorbital ödem, dermatit/egzama/deri döküntüsüYaygın: Kaşıntı, yüz ödemi, deride kuruma, eritem, alopesi, gece terlemeleri, ışığa duyarlılık reaksiyonu Yaygın olmayan: Püstüler döküntü, kontüzyon, terlemede artış, ürtiker, ekimoz, çürük eğiliminde artış, hipotrikoz, deride hipopigmentasyon, eksfoliyatif dermatit, tırnak kırılması, folikülit, peteşiler, psöriazis, purpura, deride hiperpigmentasyon, büllöz erüpsiyonlar Seyrek: Akut febril nötrofilik dermatoz (Sweet's hastalığı), tırnakta renk kaybı, anjiyonörotik ödem, veziküler döküntü, eritem multiform, lökositoklastik vaskülit, Stevens-Johnson sendromu, akut jeneralize ekzantematöz püstülozis (AGEP) Kas-iskelet bozukluklar, bağ doku ve kemik hastalıklarıÇok yaygın: Kas spazmları ve krampları, miyalji, artralji, kemik ağrısı da dahil olmak üzerekas-iskelet ağrıları Yaygın: Eklemlerde şişme Yaygın olmayan: Kaslarda ve eklemlerde sertlik Seyrek: Kas zayıflığı, artrit Böbrek ve idrar hastalıklarıYaygın olmayan: Böbrek ağrısı, hematüri, akut böbrek yetmezliği, sık sık idrar yapmakÜreme sistemi ve meme hastalıklarıYaygın olmayan: Jinekomasti, erektil disfonksiyon, menoraji, düzensiz menstrüasyon, cinsel disfonksiyon, meme başında ağrı, memelerde büyüme, skrotum ödemiGenel bozukluklar ve uygulama bölgesine ilişkin hastalıklarÇok yaygın: Sıvı retansiyonu ve ödem, yorgunlukYaygın: Güçsüzlük, pireksi, anazarka, titreme nöbetleri, kaslarda sertlikler Yaygın olmayan: Göğüs ağrısı, huzursuzluk Laboratuvar bulgularıÇok yaygın: Kilo artışı Yaygın: Kilo azalmasıYaygın olmayan: Kanda kreatinin düzeyinin yükselmesi, kandaki kreatin fosfokinaz düzeyinin yükselmesi, kandaki laktat dehidrojenaz düzeyinin yükselmesi, kanda alkalin fosfataz düzeyinin yükselmesi Seyrek: Kanda amilaz düzeyinin yükselmesi 1Transforme KML hastalarında en sık bildirilen pnömoni olmuştur. 2Bir hasta yılı esasında, konjestif kalp yetmezliği de dahil olmak üzere kardiyak olaylar transforme KML hastalarında kronik KML hastalarından daha sık gözlemlenmiştir. 3Transforme KML (KML-AP ve KML-BC) hastalarında en sık görülen kanamadır (hematom, hemoraji). 4Plevra efüzyonu, transforme KML (KML-AP ve KML-BC) hastalarında kronik KML hastalarından daha yaygın olmuştur. 5Bazı ölümcül hepatik yetmezlik ve hepatik nekroz vakaları bildirilmiştir. İmatinib ile yapılan ilave klinik çalışmalardan ve pazarlama sonrası deneyimden aşağıdaki reaksiyon türleri bildirilmiştir. Bunlar arasında, genişletilmiş erişim programlarından ve daha küçük veya devam etmekte olan klinik çalışmalardan bildirilen ciddi istenmeyen olayların yanı sıra kendiliğinden bildirilen vaka raporları da yer almaktadır. Bu reaksiyonların büyüklüğü bilinmeyen bir popülasyondan bildirilmesi nedeniyle, sıklıklarının güvenilir bir biçimde belirlenmesi veya imatinibe maruz kalma ile nedensel bir ilişkinin kesinleştirilmesi her zaman mümkün olmamaktadır. Pazarlama sonrası raporlarda bildirilen istenmeyen reaksiyonlar Sinir sistemi hastalıklarıYaygın olmayan: Serebral ödemGöz hastalıklarıSeyrek: Vitröz kanamaKardiyak hastalıklarSeyrek: Perikardit, kalp tamponadıVasküler hastalıklarYaygın olmayan: Tromboz/emboli Çok seyrek: Anafilaktik şokSolunum, göğüs bozuklukları ve mediastinal hastalıklarYaygın olmayan: Akut respiratuvar yetmezlik1, interstisyel akciğer hastalığıGastrointestinal hastalıklarYaygın olmayan: İleus/intestinal obstrüksiyon, tümör kanaması/tümör nekrozu, gastrointestinal perforasyon 2Seyrek: DivertikülitDeri ve deri altı doku hastalıklarıSeyrek: Liken keratoz, liken planuz Çok seyrek: Toksik epidermal nekrolizKas-iskelet bozukluklar, bağ doku ve kemik hastalıklarıSeyrek: Avasküler nekroz/kalça osteonekrozu, rabdomiyoliz/miyopatiÜreme sistemi hastalıklarıÇok seyrek: Hemorajik korpus luteum, hemorajik over kistiLaboratuvar testi anormallikleri Hematoloji KML'de başta nötropeni ve trombositopeni olmak üzere sitopeniler tüm çalışmaların devamlı bir bulgusu olmuş, > 750 mg gibi daha yüksek dozlarda daha sık oldukları düşünülmüştür (faz I çalışma). Bununla birlikte, sitopenilerin ortaya çıkışı, aynı zamanda açıkça hastalığın evresine de bağlı olmuştur. Sitopeniler, yeni tanı konulan KML vakalarında, diğer vakalara kıyasla daha seyrektir. Evre 3 veya 4 nötropenilerin (ANC < 1.0 x 109/L) ve trombositopenilerin (trombosit sayısı < 50 x 109/L) blast krizindeki ve hızlanmış fazdaki sıklığı, yeni tanı konulan kronik faz KML vakalarındakinin 4-6 katıdır. Yeni tanı konmuş kronik KML vakalarında % 16.7 nötropeni ve % 8.9 trombositopeni görülürken, bu oranlar hızlanmış ve blastik fazda sırasıyla, % 59-64 ve % 44-63 olarak bildirilmiştir. Yeni tanı konulmuş olan kronik faz KML vakalarında evre 4 nötropeni (ANC < 0.5 x 109/L) ve trombositopeni (trombosit sayısı < 10 x 109/L), sırasıyla yalnızca % 3.6 ve < %1 oranında görülmüştür. Nötropenik ve trombositopenik periyotların ortalama süresi genellikle sırasıyla 2 ve 3. haftalar arasında ve 3 ve 4. haftalar arasında yer almıştır. Bu olaylar, genellikle İMATENİL ile tedavinin dozu azaltılarak ya da tedavi kesilerek kontrol edilebilir, ancak bazı nadir vakalarda kalıcı olarak tedavinin bırakılmasına neden olabilir. Pediyatrik KML hastalarında en sık gözlenen toksisiteler; nötropeni, trombositopeni ve anemi dahil olmak üzere 3 ya da 4. derece sitopeniler olmuştur. Bunlar genellikle ilk birkaç ay içerisinde gerçekleşmektedir. Biyokimya KML hastalarında transaminazlarda (< % 5) ya da bilirubinde (< %1) ciddi artışlar nadir olmuştur (hastaların < % 3'ü ) ve genellikle doz azaltılarak ya da kesilerek (bu epizodların ortalama süresi yaklaşık 1 hafta olmuştur) kontrol altına alınmıştır. KML hastalarının % 1'inden azında karaciğer laboratuar anormallikleri nedeniyle tedavi sürekli olarak kesilmiştir. Bazıları ölümcül olabilen sitolitik ve kolestatik hepatit ve karaciğer yetmezliği vakaları mevcuttur. 4.9. Doz aşımı ve tedavisiTerapötik dozlardan daha yüksek dozlarla deneyim sınırlıdır. İmatinib doz aşımı ile ilgili bireysel vakalar spontan olarak ve literatürde bildirilmiştir. Genellikle, bu vakalarda bildirilen sonuçlar düzelme ya da iyileşme şeklinde olmuştur. Doz aşımı halinde, hasta gözlem altında tutulmalı ve uygun semptomatik tedavi uygulanmalıdır.Farklı doz aralıklarında bildirilen olaylar aşağıda verilmiştir: Erişkinlerde doz aşımı: 1,200 ila 1,600 mg (1 ila 10 gün arasında değişen sürelerle): Bulantı, kusma, diyare, döküntü, eritem, ödem, şişme, yorgunluk, kas spazmları, trombositopeni, pansitopeni, karın ağrısı, baş ağrısı, iştahta azalma. 1,800 ila 3,200 mg (6 gün boyunca günde 3,200 mg'a kadar dozlar): Güçsüzlük, miyalji, CPK düzeyinde yükselme, bilirubin düzeyinde yükselme, gastrointestinal ağrı. 6,400 mg (tek doz): Literatürde yer alan bir vakada, bulantı, kusma, karın ağrısı, pireksi, yüzde şişme, nötrofil sayısında azalma, transaminaz düzeylerinde yükselme görülen bir hasta bildirilmiştir. 8 ila 10 g (tek doz): Kusma ve gastrointestinal ağrı bildirilmiştir. Pediyatrik doz aşımı: 400 mg'lık tek doza maruz kalan 3 yaşındaki bir erkek çocukta kusma, diyare ve anoreksi; 980 mg'lık tek doza maruz kalan 3 yaşındaki diğer bir erkek çocukta ise lökosit sayısında azalma ve diyare görülmüştür. 5. FARMAKOLOJİK ÖZELLİKLER 5.1. Farmakodinamik özelliklerFarmakoterapötik grup: Protein-tirozin kinaz inhibitörü ATC kodu: L01XE01İmatinib, in vitro, hücresel ve in vivo düzeylerde kırılma noktalarının yoğunlaştığı bölge-Abelson (Bcr-Abl) tirozin kinazı güçlü bir şekilde inhibe eden bir protein-tirozin kinaz inhibitörüdür. Bileşik, Bcr-Abl pozitif hücre dizilerinde, Philadelphia kromozom pozitif Kronik Miyeloid Lösemi (KML) ve Akut Lenfoblastik Lösemili (ALL) hastaların yeni lösemi hücrelerinde selektif olarak proliferasyonu inhibe etmekte ve apoptozisi uyarmaktadır. Ex vivo periferik kan ve kemik iliği örneklerinin kullanıldığı koloni transformasyon tahlillerinde, imatinib KML hastalarındaki Bcr-Abl pozitif kolonilerde selektif inhibisyon göstermektedir. Bileşik in vivoolarak, Bcr-Abl pozitif tümör hücreleri kullanılan hayvan modellerinde tek ajan olarak anti-tümör aktivite gösterir.İmatinib, aynı zamanda trombosit türevi büyüme faktörü (Platelet derived growth factor -PDGF) ve kök hücre faktörü (Stem cell factor - SCF), c-Kit için reseptör tirozin kinazların bir inhibitörüdür ve PDGF- ve SCF- tarafından yönlendirilen hücresel olayları inhibe eder. HES patogenezinde; PDGF reseptör veya Abl protein kinazların, farklı ortak proteinlerin birleşimi sonucu sürekli olarak aktif duruma geçmesinin veya sürekli PDGF üretiminin rol oynadığı düşünülmektedir. Ayrıca, c-Kit ya da PDGFR'nin konstitütif aktivasyonu SM'nin patojenezinde rol oynayan muhtemel nedendir. İmatinib, düzensizleşen PDGFR veya Abl kinaz aktivitesinin neden olduğu sinyalizasyonu ve hücre proliferasyonunu inhibe eder. Kronik Miyeloid Lösemide Klinik Çalışmalar İmatinibin etkinliği, bir bütün olarak elde edilen hematolojik ve sitogenetik yanıt oranlarını ve hastalıksız sağkalım süresini temel alır. Yeni tanı konulmuş kronik fazdaki KML dışında, hastalıkla ilişkili semptomlarda düzelme gibi klinik yararı ya da artmış yaşam süresi gösteren kontrollü çalışmalar yoktur. Bütün klinik çalışmalarda hastaların %38-40'ının en az 60, %10-12'sinin en az 70 yaşında olduğu bildirilmiştir. Kronik faz, yeni tanı konulmuş: Bu faz III çalışmasında, imatinib monoterapisi, interferon-alfa (IFN) + sitarabin (ARA-C) kombinasyonuyla karşılaştırılmıştır. Kullanılan tedaviye yanıt vermeyen hastaların, kullandıkları tedaviyi bırakarak diğer tedaviyi kullanmalarına izin verilmiştir. İmatinib grubundaki hastalarda günde 400 miligramlık doz kullanılmıştır. IFN grubundaki hastalar, hedef alınan günlük subkütan IFN dozu 5 MlU/m2 + her ayın 10 günü, günde 20 mg/m2 Ara-C kombinasyonu kullanmıştır. 16 ülkedeki 177 çalışma merkezinden toplam 1106 (her grupta 553) hasta, randomize edilmiştir. Yaşları 18-70 arasında değişmek üzere medyan 51 olan hastaların %21.9'unun, 60 yaşında ya da daha ileri yaşta olduğu görülmüştür. Verilerin bu analizde kullanılmak üzere derlendiği sıradaki (son hastanın kaydedilmesinden 7 yıl sonra) medyan ilk seçenek tedavi süresi imatinib grubunda 82, IFN (kombinasyon) grubunda 8 aydır. İmatinib ile medyan ikinci seçenek tedavi süresi 64 aydır. İmatinib grubuna ayrılmış olan hastaların % 60'ı, başlangıçta kullandıkları ilaca (imatinib) devam etmektedir. Bu hastalarda ortalama imatinib dozu 403±57 mg'dir. Genel olarak, birinci seçenek olarak imatinib alan hastalarda dağıtılan ortalama günlük doz 406±76 mg'dır. IFN + ARA-C grubundaki hastaların yalnızca %2'si başlangıçta kullandıkları tedaviye devam etmektedir. IFN + ARA-C grubunda başlangıçtaki tedaviye devam etmeyen hastalarda bunun en sık rastlanan nedeni (%14), hastaların verdikleri onayı geri çekmesi; imatinib grubuna geçenlerde ise buna en sık (hastaların %26'sında) yol açan neden, şiddetli intolerans ve hastalığın ilerlemesidir (%14). Primer bitiş noktası, hastalıksız sağkalım süresidir. Sekonder sonlanım noktalarının yanıt verileri de Tablo 2'de gösterilmektedir. Tablo 2.Yeni tanı konulan KML çalışmasındaki yanıt oranları (84 aylık veri)(En iyi yanıt oranları)Hematolojik yanıtTHY oranın(%)[%95 güven aralığı]
IFN+Ara-C n=553
İmatinib n=553 534 (96.6)* 94.7, 97.9
313 (56.6)* 52.4, 60.8
Sitogenetik yanıtMajör yanıtn(%)[%95 güven aralığı] Tam CyR nn(%
490 (88.6) [85.7, 91.1] 456 (82.5) 34 (6.1)
129 (23.3) [19.9, 27.1]
64(11.6) 65(11.8) Moleküler yanıt12 aydaki majör yanıt (% 24 aydaki majör yanıt (%
% 40* % 54
% 2 * NA**
* p<0.001, Fischer's exact test**Yetersiz veri, numuneler ile yalnızca iki hasta var Hematolojik yanıt kriterleri (bütün yanıtlar >4 hafta sonra doğrulanmalıdır):Kandaki lökosit sayısı < 10 x109/L, trombosit sayısı < 450 x109/L, miyelosit+metamiyelosit < %5; kanda blast hücresi veya promiyelosit yok, bazofiller <%20, kemik iliği dışında hastalık yokSitogenetik yanıt kriterleri:tam (%0 Ph+ metafazlar), kısmi (%1-35), minör (%36-65) veya minimal (%66-95). Majör yanıt (%0-35), hem kısmi hem tam yanıtları içerir [1].Majör moleküler yanıt kriterleri:Gerçek-zaman kantitatif revers trans kriptaz polimeraz zincir reaksiyonuyla ölçülen BCR-ABL transkriptlerinin periferik kanda, başlangıç düzeyine göre en az 3 log azalması.İmatinib ile birinci seçenek tedavinin kümülatif yanıt oranları Tablo 3'te gösterilmektedir. Tablo 3.Birinci seçenek imatinib tedavisine verilen kümülatif yanıt tahmini
84 ayda tahmin edilen progresyonsuz sağkalım imatinib grubunda %95 Güven aralığı ile %81.2 (78, 85) ve kontrol grubunda %60.6 (56.5) olmuştur (p < 0.001) (Şekil 1). 84 ayda akselere faza ya da blast krizine ilerleme olmayan hastaların tahmin edilen oranı, IFN grubu ile karşılaştırıldığında imatinib grubunda anlamlı düzeyde yüksek olmuştur (%85.1 (82,89) karşısında %92.5 (90,95), p < 0.001) (Şekil 2). Yıllık progresyon hızı tedavide geçirilen süre ile birlikte azalmaktadır. Şekil 1.İlerleme kaydedilinceye kadar geçen süre (ITT ilkesi)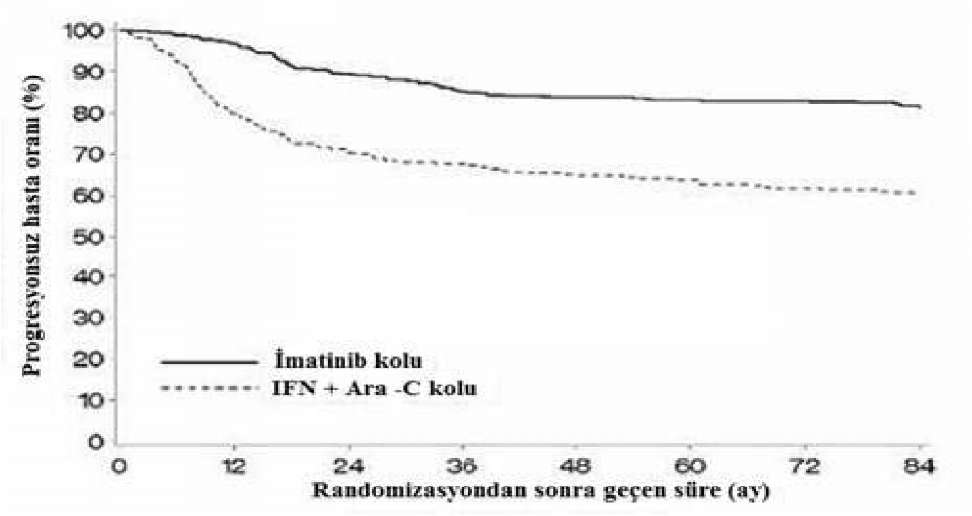
Şekil 2.Akselere Faz veya Blast krizinin gelişmesine kadar geçen süre (ITT ilkesi)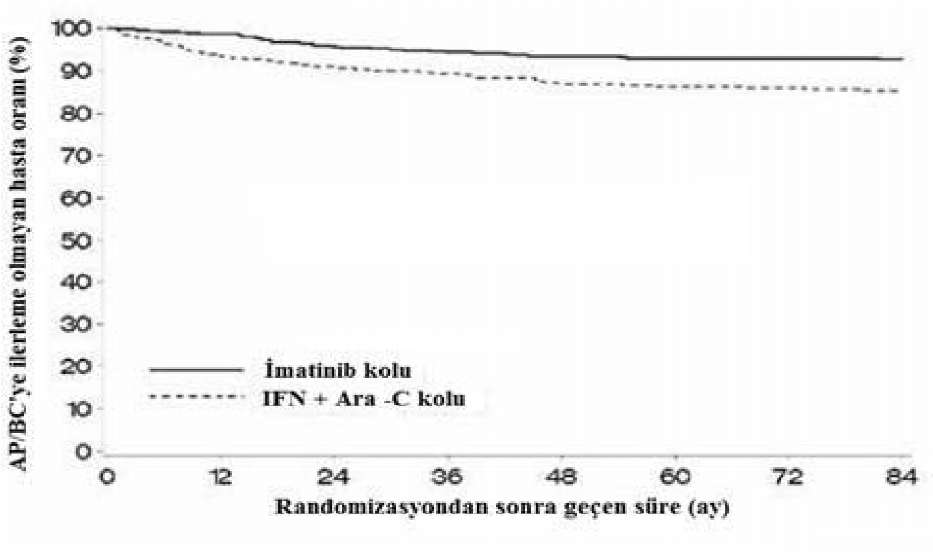 İmatinib ve IFN+Ara-C gruplarında, sırasıyla, toplam 71 (%12.8) ve 85 (%15.4) hasta ölmüştür. 84 ayda randomize imatinib ve IFN+Ara-C gruplarında tahmin edilen genel sağkalım, sırasıyla %86.4 (83, 90) ve %83.3 (80, 87) düzeyindedir (p=0.073, log-rank testi). Buna ek olarak, 84 aylık verilere göre imatinib hastalarında yalnızca 31 (%5.6) ölüm (BMT öncesi) KML ile ilişkilendirilmiştir. Buna karşılık IFN+Ara-C hastalarında 40 (%7.2) ölüm KML ile ilişkilendirilmiştir. Yalnızca KML ile ilişkili bu ölümler dikkate alınır ve BMT sonrası ya da diğer nedenlerle meydana gelen bütün ölümler sansürlenirse, tahmin edilen 84 aylık sağkalım oranları %93.6 ve %91.1 olmaktadır (p=0.1, log-rank testi). İmatinib tedavisinin kronik fazdaki, yeni tanı konulmuş KML'deki sağkalım etkisi, aynı rejimde IFN+Ara-C (n=325) kullanılan başka bir Faz III çalışmadan elde edilen birincil verilerle birlikte yukarıda belirtilen imatinib verilerinin retrospektif analizinde ayrıntılı olarak incelenmiştir. Bu yayında, genel sağkalım bakımından imatinibin IFN+Ara-C karşısındaki üstünlüğü kanıtlanmıştır (p<0.001); 42 ay içinde 47 (%8.5) imatinib hastası ve 63 (%19.4) IFN+Ara-C hastası ölmüştür.
İmatinib ve IFN+Ara-C gruplarında, sırasıyla, toplam 71 (%12.8) ve 85 (%15.4) hasta ölmüştür. 84 ayda randomize imatinib ve IFN+Ara-C gruplarında tahmin edilen genel sağkalım, sırasıyla %86.4 (83, 90) ve %83.3 (80, 87) düzeyindedir (p=0.073, log-rank testi). Buna ek olarak, 84 aylık verilere göre imatinib hastalarında yalnızca 31 (%5.6) ölüm (BMT öncesi) KML ile ilişkilendirilmiştir. Buna karşılık IFN+Ara-C hastalarında 40 (%7.2) ölüm KML ile ilişkilendirilmiştir. Yalnızca KML ile ilişkili bu ölümler dikkate alınır ve BMT sonrası ya da diğer nedenlerle meydana gelen bütün ölümler sansürlenirse, tahmin edilen 84 aylık sağkalım oranları %93.6 ve %91.1 olmaktadır (p=0.1, log-rank testi). İmatinib tedavisinin kronik fazdaki, yeni tanı konulmuş KML'deki sağkalım etkisi, aynı rejimde IFN+Ara-C (n=325) kullanılan başka bir Faz III çalışmadan elde edilen birincil verilerle birlikte yukarıda belirtilen imatinib verilerinin retrospektif analizinde ayrıntılı olarak incelenmiştir. Bu yayında, genel sağkalım bakımından imatinibin IFN+Ara-C karşısındaki üstünlüğü kanıtlanmıştır (p<0.001); 42 ay içinde 47 (%8.5) imatinib hastası ve 63 (%19.4) IFN+Ara-C hastası ölmüştür.Sitogenetik yanıtın derecesi imatinib tedavisi uygulanan hastalarda uzun vadeli sonuçlar üzerinde açık bir etkiye sahiptir. 12 ayda TSY (KSY) olan hastalardan 84 ayda AF/BK'ye ilerlemeden kalacağı tahmin edilenlerin oranı %96 (%93) düzeyindedir, 12 ayda MSY olmayan hastaların yalnızca %81'i 84 ayda ileri KML'ye ilerlemeden kalacaktır (genel olarak p<0.001, TSY ve KSY arasında p=0.25). 18 aylık dönüm noktası esas alındığında, tahminler sırasıyla %99, %90 ve %83 olmakta, ayrıca TSY ve KSY arasında istatistiksel olarak anlamlı bir fark (p<0.001) meydana gelmektedir. Molekül izlem önemli ek prognostik bilgiler sağlamıştır. TSY olan ve 12 ay sonra Bcr-Abl transkriptlerinde en az 3 log azalma olan hastalar için, 60 ayda hastalığın ilerlemeden kalma olasılığı, 12 ayda TSY olmayan hastalarda gözlemlenenden anlamlı düzeyde daha büyüktür (%70, p<0.001). Yalnızca AF/BK'ye ilerleme dikkate alındığında, tahmin edilen olaysızlık oranları, sırasıyla %100, %95 ve %88 olur (genel olarak p<0.001, MMR olan ya da olmayan TSY arasında p=0.007). 18 aylık dönüm noktası kullanıldığında, 60 ayda tahmin edilen AP/BC'sizlik oranları TSY ve MMR olan hastalar için %100, TSY olan ama MMR olmayan hastalar için %98 ve TSY olmayan hastalar için yalnızca %87 olmuştur (genel olarak p<0.001, MMR olan ya da olmayan TSY arasında p=0.105). Bu çalışmada kullanılan dozların günde 400 miligramdan 600 miligrama, daha sonra da 600 miligramdan 800 miligrama yükseltilmesine izin verilmiştir. Dozun günde 800 miligrama arttırıldığı 40 hastadaki bazı advers reaksiyonların yüzdesinin, doz arttırımından öncesine kıyasla yükseldiği görülmüştür (n=551). Gastrointestinal kanamalar, konjunktivit ve plazmadaki transaminaz ya da bilirubin düzeylerinin yükselmesi; doz arttırıldığında daha sık görülen advers reaksiyonlardandır. Diğer advers reaksiyonlar ise doz arttırıldıktan sonra, önceye kıyasla daha seyrek veya aynı sıklıkta görülmüştür. Yaşam kalitesi, geçerliliği kanıtlanmış bir enstrüman olan FACT-BRM anketiyle değerlendirildi. Bu anketin bütün bölümlerinde imatinib grubu, IFN + ARA-C grubuna kıyasla istatistik bakımdan anlam taşıyacak şekilde daha yüksek puan aldı. Sonuçlar, hastaların yaşam kalitesinin imatinib tedavisi sırasında iyi durumda kaldığını gösterdi. Kronik faz, interferon tedavisinin başarısız kaldığı hastalar: 532 hasta, 400 miligramlık başlangıç dozuyla tedavi edildi. Bu hastalar; hematolojik başarısızlık (%29), sitogenetik başarısızlık (%35) veya interferon intoleransı (%36) olmak üzere başlıca 3 gruptu. Hastalar, bu çalışma öncesinde medyan 14 ay boyunca haftada > 25 x106 IU dozunda interferon kullanmış bulunan, geç kronik faz vakalarıydı ve tanı konulduktan sonra geçen medyan süre 32 aydı. Majör sitogenetik yanıt (tam + kısmi yanıt, kemik iliğinde %0-35 Ph+ metafaz) oranı, bu çalışmadaki başlıca etkinlik parametresi olarak değerlendirildi. Bu çalışmada hastaların % 65'inde (% 53'ü tam olmak üzere) majör sitogenetik yanıt elde edildi (Tablo 4). Hastaların %95'i bu tedaviye tam hematolojik yanıt verdi. Hızlanmış faz: Bu fazdaki 235 KML vakasının ilk 77'sinde tedaviye günde 400 mg ile başlandı; daha sonra çalışma protokolü, daha yüksek imatinib dozlarının kullanılmasına olanak tanıyacak şekilde tadil edildi ve geriye kalan 158 hasta, başlangıçta 600 mg imatinib kullandı. Tam hematolojik yanıt, hiçbir lösemi kanıtının mevcut olmaması (kemik iliğindeki ve kandaki blast hücrelerinin kaybolması, ancak periferik kan tablosunda, tam yanıt için gereken düzelmenin gerçekleşmemesi) veya kronik faz kronik miyeloid lösemiye dönüş olarak tanımlanan tam hematolojik yanıt elde edilme oranı, bu çalışmanın etkinlik konusundaki değerlendirilen primer parametresiydi. Doğrulanmış hematolojik yanıt, hastaların % 71.5'inde elde edildi (Tablo 4). Bu hastalardan % 27.7'sinde ayrıca majör sitogenetik yanıt (% 20.4'ünde tam majör sitogenetik yanıt) alınmış olması önemlidir. 600 mg imatinib kullanan hastalarda bugünkü saptamalara göre tahmini medyan hastalıksız sağkalım ve genel sağkalım oranları, sırasıyla 22.9 ay ve 42.5 ay olarak hesaplandı. Miyeloid blast krizi: Bu çalışma, blast krizi gelişmiş olan 260 hasta üzerinde yapıldı. Bu hastaların 95'i (%37'si), hızlanmış faz veya yine blast krizi nedeniyle daha önce de kemoterapi görmüştü ("önceden tedavi edilmiş olan hastalar"), 165 (%63) hastada ise daha önce kemoterapi uygulanmamıştı ("önceden tedavi edilmemiş olan hastalar"). Başlangıç dozu, ilk 37 hastada 400 miligramdı; daha sonra yapılan protokol tadilatı, daha yüksek dozların kullanılmasına olanak verdiğinden, diğer 223 hasta, başlangıçta 600 mg imatinib kullandı. Primer etkinlik parametresi, hızlanmış faz çalışmasında olduğu gibi yine tam hematolojik yanıt, lösemi kanıtının mevcut olmaması veya kronik faza dönüş olarak tanımlanan, hematolojik yanıt oranıydı. Hastaların %31'inde hematolojik yanıt elde edildi. 600 mg imatinib kullanan hastalardaki hematolojik yanıt oranı, 400 mg imatinib kullanmış olanlara kıyasla daha yüksekti (%16'ya karşılık %33, p=0.0220). Daha önceden tedavi edilmemiş ve tedavi edilmiş hastaların mevcut tahmini ortalama sağkalımı sırasıyla 7.7 ve 4.7 aydır. Tablo 4.KML vakalarında elde edilen yanıtlar
1THY: çalışma 0110 [kandaki WBC <10 x109/L, trombosit sayısı <450 x109/L, miyelosit + metamiyelosit <%5; kanda blast veya promiyelosit yok; bazofiller < %20, kemik iliği dışında hastalık yok] ve çalışma 0102 ve 0109 [ANC>1.5 x109/L, trombosit sayısı >100 x109/L, kanda blast hücresi yok, BM blast hücresi oranı <%5 ve BM dışında hastalık yok]NEL: THY ile aynı kriterler; yalnızca ANC >1 x109/L ve trombosit sayısı >20 x109/L (çalışma 0102 ve 0109'da) RTC: BM ve PB blast hücresi oranı <%15; PM ve PB blast hücresi + promiyelosit oranı <%30, PB bazofil oranı <%20, dalak ve karaciğer hariç BM dışında hastalık yok (çalışma 0102 ve 0109'da). ANC = mutlak nötrofil sayısı, BM = kemik iliği, PB = periferik kan, WBC = lökosit sayısı 2Majör yanıt = tam (%0 Ph+ metafaz) + kısmi (%1-35) yanıtPediyatrik hastalar: Açık-etiketli, çok merkezli, tek kollu bir faz II çalışmaya, tanısı yeni konmuş ve tedavi edilmemiş kronik fazda KML'si olan toplam 51 pediyatrik hasta katılmıştır. Hastalara 340 mg/m2/gün dozla imatinib tedavisi uygulanmış ve doz sınırlayıcı toksisitenin olmadığı durumlarda tedaviye ara verilmemiştir. İmatinib tedavisiyle yeni tanı konmuş pediyatrik KML hastalarında hızlı bir yanıt sağlanmış, 8 haftalık tedaviden sonra THY oranı %78 olmuştur. Yüksek THY oranıyla birlikte tam sitogenetik yanıtın (TSY) %65 oranında gerçekleştiği de gözlenmiştir; bu oran erişkinlerde gözlenene yakındır. Ayrıca, kısmi sitogenetik yanıt (KSY) %16 oranında gözlenmiştir. TSY elde edilen hastaların büyük kısmında, TSY 3 ila 10 ay arasında gelişmiş, yanıta kadar süre için medyan değer Kaplan-Meier yöntemiyle 5.6 ay olarak hesaplanmıştır. Faz I doz arttırma çalışmasına, kronik faz KML (n=15) veya blast krizinde KML ya da Ph+ akut lösemi (n=16) vakası olan toplam 31 pediyatrik hasta katıldı. Hastaların büyük bölümü, önceden tedavi (%45'i BMT, %68'i polikemoterapi) görmüştü. Hastalar 260 mg/m2/gün (n=6), 340 mg/m2/gün (n=11), 440 mg/m2/gün (n=8) ve 570 mg/m2/gün (n=6) dozunda imatinib kullandı. Sitogenetik verileri mevcut olan 13 KML vakasından 7'sinde (%54) tam, 4'ünde (%31) kısmi olmak üzere %85'inde MSY elde edildi. Ph+ ALL hastalarında yapılan klinik çalışmalar Yeni teşhis edilen veya nükseden/tedaviye dirençli 758 Ph+ ALL hastası; biri randomize, diğerleri kontrol gruplarına yer vermeden yapılan 10 klinik çalışmada değerlendirilmiştir. Yeni teşhis edilen Ph+ ALL Kontrol grubuna yer vererek yapılan ve imatinibin, yeni teşhis edilmiş, en az 55 yaşındaki 55 hastada kemoterapi indüksiyonuyla karşılaştırıldığı bir çalışmada (ADE10) imatinib monoterapisiyle sağlanan tam hematolojik yanıt oranı, kemoterapiye kıyasla istatistiksel anlam taşıyacak şekilde daha yüksek (%50'ye karşılık %96.3, p=0.0001) bulunmuştur. Kemoterapiye yanıt vermeyen veya zayıf yanıt veren hastalarda imatinib, kurtarma tedavisi olarak kullanıldığında 9/11 (%81.8) hastada tam hematolojik yanıtla sonuçlanmıştır. Çalışma düzeninin özellikleri nedeniyle iki grup arasında remisyon süresi, hastalıksız sağkalım veya total sağkalım bakımından fark görülmemiş; ancak tam moleküler yanıt elde edilen ve minimal rezidüel hastalık düzeyinde kalan vakalarda, hem remisyon süresi (p=0.01) hem de hastalıksız sağkalım (p=0.02) bakımından prognoz, daha iyi olmuştur. Yeni teşhis edilmiş Ph+ ALL hastalarında kontrol grubuna yer vermeksizin yapılan 4 klinik çalışmada (AAU02, ADE04, AJP01 ve AUS01) alınan sonuçlar, yukarıda anlatılan çalışmanın sonuçlarıyla bağdaşmaktadır. İmatinib + kemoterapi indüksiyonuyla elde edilen tam hematolojik yanıt oranı %93 (değerlendirilebilen 147/158 hastada), majör sitogenetik yanıt oranı %90 (değerlendirilebilen 19/21 hastada) olmuş; değerlendirilebilen 49/102 (%48) hastada tam molekül er yanıt sağlanmıştır. Bunun gibi, 55 yaşında veya daha ileri yaşta olan, yeni teşhis edilmiş 49 Ph+ ALML hastasında kontrol grubu kullanılmaksızın yapılan iki çalışmada (AFR09 ve AIT04), kemoterapiyle birlikte veya kemoterapi olmaksızın kullanılan imatinib + steroid kombinasyonları; bütün çalışma popülasyonunun %89'unda tam hematolojik yanıt; değerlendirilebilen 39 hastanın %26'sında tam moleküler yanıt sağlamıştır. Hastalıksız sağkalım (DFS) ve total sağkalım (OS) bütün hastalarda 1 yıldan daha uzun ve daha önce yapılmış olan 3 çalışmadakinden (AJP01, AUS01 ve AFR09) üstün (DFS p<0.001; OS p<0.01) bulunmuştur. Nüksetmiş/tedaviye dirençli Ph+ ALL Nüksetmiş/tedaviye dirençli Ph+ ALL hastalarında kullanılan imatinib monoterapisiyle, elde edilen yanıtın değerlendirilebildiği 66/429 hastadaki hematolojik ve majör sitogenetik yanıt oranları, sırasıyla %33 (%12'si tam hematolojik yanıt) ve %23 olmuştur (429 hastanın 353'ü, primer yanıt verilerinin mevcut olmadığı, genişletilmiş erişim programı kapsamında tedavi edilmiştir). Nüksetmiş/tedaviye dirençli toplam 429 hastada, progresyona kadar geçen medyan süre 1.9-3.1 ay; değerlendirilebilen 409/429 hastadaki total sağkalım medyan 5-9 ay arasında değişmiştir. 14 hastada kullanılan imatinib + indüksiyon kemoterapisi kombinasyonu, değerlendirilebilen 12 hastanın %92'sinde tam hematolojik yanıt, değerlendirilebilen 8 hastanın tümünde (%100) majör sitogenetik yanıt sağlamıştır. Moleküler yanıt, ikisi tam olmak üzere 4 hastada elde edilmiştir. En az 55 yaşındaki, nüksetmiş veya tedaviye dirençli 146 Ph+ ALL hastası, imatinib monoterapisiyle tedavi edilmiş ve küratif tedavi kullanılmamış olması nedeniyle, ayrıca analiz edilmiştir. Bu tedaviye alınan yanıt, günde 600 mg imatinib ile tedavi edilen toplam 146 hastanın 14'ünde değerlendirilebilmiştir; bu hastaların 5'inde (%35) tam hematolojik yanıt, 7'sinde (%50) majör sitogenetik yanıt elde edilmiştir. Daha düşük dozda (günde 400 mg) imatinib kullanılarak tedavi edilen 4 hastada yanıt alınamamış olması, bu dozun yetersiz kaldığı izlenimini vermiştir. Bütün çalışma popülasyonundaki (n=146) hastalıksız medyan sağkalım 2.8-3.1 ay; total medyan sağkalım 7.4-8.9 ay olmuştur. SM ile İlgili Klinik Çalışmalar Abl, Kit ya da PDGFR protein tirozin kinazlarla ilişkili yaşamı tehdit edici hastalıkları olan farklı hasta popülasyonlarında imatinibin test edildiği açık-etiketli, çok merkezli bir faz II klinik çalışma (çalışma B2225) yürütülmüştür. Bu çalışmada tedavi edilen ve 45'inde hematolojik hastalıklar, 140'ında da çeşitli solid tümörler bulunan 185 hastadan 5'inde SM saptanmıştır. SM hastaları günlük 100 mg ila 400 mg imatinib ile tedavi edilmiştir. Yayınlanmış 10 vaka raporu ve vaka serisinde, yaşları 26 ila 85 arasında değişen 25 SM hastası daha bildirilmiştir. Bu hastalara da günlük 100 mg ila 400 mg dozda imatinib uygulanmıştır. SM için tedavi edilen toplam popülasyonun (30 hasta) 10'unda (%33) tam hematolojik yanıt, 9'unda (%30) kısmi hematolojik yanıt elde edilmiştir (toplam yanıt oranı %63). Sitogenetik anormallikler yayınlanmış raporlarda ve çalışma B2225'te tedavi edilen 30 hastanın 21'inde değerlendirilmiştir. Bu 21 hastanın sekizinde FIP1L1-PDGFR-alfa füzyon kinaz saptanmıştır. Çalışma B2225'te tedavi edilen hastalarda medyan tedavi süresi 13 ay olmuş (aralık: 1.4-22.3 ay), yayınlanmış literatürde yanıt veren hastalarda ise aralık 1 ay ila 30 ayın üzerinde bir süre arasında değişmiştir. Sonuçlar Tablo 5'te verilmiştir. Tablo 5.SM'de Elde Edilen Yanıt
HES ile İlgili Klinik Çalışmalar Abl, Kit ya da PDGFR protein tirozin kinazlarla ilişkili yaşamı tehdit edici hastalıkları olan farklı hasta popülasyonlarında imatinibin test edildiği açık-etiketli, çok merkezli bir faz II klinik çalışma (çalışma B2225) yürütülmüştür. Bu çalışmada, toplam 185 hastadan (45'i hematolojik hastalık, 140'ında çeşitli solid tümörler saptanmıştır) HES'i olan 14 hasta günde 100 mg ila 1000 mg dozda imatinib ile tedavi edilmiştir. Yayınlanmış 35 vaka raporu ve vaka serisinde, HES'i olan ve yaşları 11 ila 78 arasında değişen 162 hasta daha bildirilmiştir. Bu hastalara, günde 75 mg ila 800 mg dozda imatinib verilmiştir. HES için tedavi edilen toplam popülasyonun (176 hasta) 107'sinde (%61) tam hematolojik yanıt, 16'sında ise (%9) kısmi hematolojik yanıt elde edilmiştir (toplam yanıt oranı %70). Yayınlanmış raporlarda ve çalışma B2225'te, tedavi edilen 176 hastadan 117'sinde sitogenetik anormallikler değerlendirilmiştir. Bu 117 hastanın 61'i, FIP1L1-PDGFR-alfa füzyon kinaz pozitif bulunmuştur. Tüm bu FIP1L1-PDGFR-alfa füzyon kinaz pozitif hastalarda, tam hematolojik yanıt elde edilmiştir. 115 hastada FIP1L1-PDGFR- alfa füzyon ya negatif bulunmuştur, ya da bilinmemektedir. Bunların 62'sinde (%54) ya tam (n=46) ya da kısmi (n=16) hematolojik yanıt elde edilmiştir. Sonuçlar Tablo 6'da verilmiştir. Tablo 6.HES'de Elde Edilen Yanıt
Karaciğer yetersizliği olan hastalarda yapılan klinik çalışmalar Çeşitli derecelerde (hafif, orta şiddette veya şiddetli; karaciğer fonksiyon bozukluğunun sınıflandırılması için bkz. Tablo 7) karaciğer yetersizliği olan hastalarda yapılan bir çalışmada imatinibe ortalama maruz kalım (doza göre normalize edilmiş EAA değeri), karaciğer fonksiyonu normal olan hastalara kıyasla artmamıştır. Bu çalışma sırasında hafif karaciğer bozukluğu olan hastalarda günde 500 mg, diğer hastalarda günde 300 mg imatinib, güvenle kullanılmıştır. Orta-ileri derecede şiddetli karaciğer yetersizliği olan hastalarda yalnızca 300 miligramlık doz kullanılmıştır ama farmakokinetik analiz bunun, 400 miligrama güvenle yükseltilebileceğini göstermiştir (bkz. 4.2 Pozoloji ve uygulama şekli; 4.4 Özel kullanım uyarıları ve önlemleri; 4.8 İstenmeyen Etkiler ve 5.2 Farmakokinetik Özellikler). Tablo 7.Karaciğer yetersizliğinin sınıflandırılması
SGOT = Serum glutamik oksaloasetik transferaz Böbrek yetmezliği olan hastalarda yürütülen klinik çalışmalar Değişen derecelerde (hafif, orta ve şiddetli - böbrek fonksiyonu sınıflandırması için bkz. aşağıda Tablo 8) böbrek yetmezliği olan hastalarla yürütülen bir çalışmada, maruz kalınan ortalama imatinib (doz normalize EAA), böbrek fonksiyonları normal olan hastalarla karşılaştırıldığında 1.5-2 kat artmıştır, bu da, imatinibin güçlü bir biçimde bağlandığı bir protein olan AGP'nin plazma düzeyinde benzer bir artışa karşılık gelir. Maruz kalınan imatinib ile böbrek bozukluğunun şiddeti arasında hiçbir korelasyon gözlemlenmemiştir. Bu çalışmada, hafif böbrek yetmezliği olan hastalarda günlük 800 mg ve orta düzeyde böbrek yetmezliği olan hastalarda günlük 600 mg güvenle kullanılmıştır. Sınırlı sayıda hasta kaydedildiği için orta düzeyde böbrek yetmezliği olan hastalarda günlük 800 mg dozu test edilmemiştir. Aynı şekilde, şiddetli böbrek yetmezliği olan yalnızca 2 hasta düşük (100 mg) doza kaydedilmiş ve daha yüksek dozların hiçbiri test edilmemiştir. Çalışmaya hiçbir hemodiyaliz hastası kaydedilmemiştir. Literatür verileri, son evre böbrek hastalığı olan ve hemodiyaliz uygulanan bir kişide günlük 400 mg dozun çok iyi tolere edildiğini göstermiştir. Diyaliz, imatinibin plazma kinetiklerini engellememiştir. Böbrekler yoluyla atılım imatinib için minör bir eliminasyon yolu olduğundan, şiddetli böbrek yetmezliği olan ve diyaliz uygulanan hastalara 400 mg'lık başlangıç dozu ile tedavi uygulanabilmektedir. Ancak, bu hastalarda dikkatli olunması önerilmektedir. Tolere edilememesi halinde doz azaltılabilir ya da etki görülmemesi halinde doz arttırılabilir (bkz. 4.2 Pozoloji ve uygulama şekli; 4.4 Özel kullanım uyarıları ve önlemleri ve 5.2 Farmakokinetik özellikler).
5.2. Farmakokinetik özelliklerİmatinibin farmakokinetiği 25 - 1000 mg'lık bir doz aralığında değerlendirilmiştir. Plazma farmakokinetik profilleri 1. günde ve plazmada kararlı düzeylerin elde edildiği 7. ya da 28. günde analiz edilmiştir.Emilim:Kapsül formülünün ortalama mutlak biyoyararlanımı % 98'dir. Bir oral dozu takiben plazma imatinib eğri altında kalan alan (EAA) değerlerinde, yüksek oranda hastalar arası değişkenlik (% 40-60) görülmüştür. Yüksek yağ içeren bir gıda ile birlikte verildiğinde, imatinibin emilim oranı minimal düzeyde azalmış (Cmaks'ta % 11 azalma ve tmaks'ta 1.5 saatlik uzama), açlık koşullarına göre EAA değerinde küçük bir azalma (% 7.4) olmuştur. Dağılım:Klinik açıdan uygun konsantrasyonlarda kullanılan imatinibin plazma proteinlerine bağlanması yaklaşık % 95 olmuş, in vitro deneyler temelinde, daha çok albümin ve alfa- asit-glikoproteine, az miktarda da lipoproteine bağlanmıştır. Biyotransformasyon:İnsanlarda, dolaşımdaki temel metaboliti ana ilaç ile in vitro benzer etkinlikte olduğu gösterilmiş N-demetillenmiş piperazin (CGP71588) türevidir. Bu metabolitin plazma EAA değerinin imatinibin EAA değerinin sadece % 16'sı olduğu bulunmuştur. N-demetile metabolitin plazma proteinlerine bağlanması, asıl bileşikteki gibidir. Eliminasyon:İmatinibin 14C-işaretli tek oral dozundan sonra, dozun yaklaşık % 81'i 7 gün içinde feçesle (dozun % 68'i) ve idrarla (dozun % 13'ü) itrah edilmiştir. Değişmemiş durumdaki imatinib, dozun % 25'ini (% 5 idrar, % 20 feçes) oluşturmuştur, geriye kalan kısım metabolitlerdir. Doğrusallık / doğrusal olmayan durum:Sağlıklı gönüllülerde oral uygulamanın ardından, imatinibin t^ değerinin yaklaşık 18 saat olması günde tek doz şeklindeki pozolojinin uygun olduğu izlenimini vermektedir. Oral olarak 25-1000 mg imatinib uygulandıktan sonra artan dozla birlikte ortalama EAA artışı doğrusal bir seyir izlemiştir. Tekrarlanan dozlarda imatinib kinetiğinde değişiklik olmamış ve günde bir kez uygulandığında birikim, kararlı ilaç konsantrasyonunun 1.5-2.5 katı olmuştur. Farmakokinetik / farmakodinamik ilişkiler:Popülasyon farmakokinetikleri:Popülasyon farmakokinetiği analizlerine göre yaşın dağılım hacmi üzerinde küçük bir etkisi olmuştur (> 65 yaşındaki hastalarda % 12 artış). Bu değişimin klinik açıdan anlamlı olmadığı düşünülmüştür. Vücut ağırlığının imatinib klerensi üzerindeki etkisine bakıldığında, 50 kg ağırlığındaki bir kişide klerensin 8.5 L/s olması beklenirken, 100 kg ağırlığındaki bir kişideki klerens 11.8 L/s'e yükselmektedir. Bu değişiklikler vücut ağırlığına göre bir doz ayarlaması yapılması için yeterli olarak kabul edilmemiştir. Cinsiyetin imatinib kinetiği üzerinde etkisi olmamıştır. Yeni tanı konulmuş KML vakalarındaki Faz III çalışmada diğer popülasyon farmakokinetiği analizleri, kovariyans faktörlerinin ve birlikte kullanılan diğer ilaçların gerek klerens, gerekse hacim üzerindeki etkilerinin küçük olduğunu, doz ayarlamasına ihtiyaç bırakmadığını göstermiştir. Çocuklarda farmakokinetik:Bir Faz I ve Faz II çalışmasında oral imatinib, pediyatrik hastalarda da, erişkin hastalardaki gibi hızla emilmiştir. Çocuklarda 260 ve 340 mg/m2 imatinible elde edilen EAA değerleri, erişkinlerde sırasıyla 400 ve 600 mg imatinible elde edilenler gibidir. 340 mg/m2 imatinibin birinci ve sekizinci günlerdeki EAA(0-24 saat) değerleri bu ilacın, tekrarlanan dozlardan sonra 1.7 kat biriktiğini göstermiştir. Organ fonksiyonu bozukluğu:İmatinib ve metabolitleri böbrek yoluyla anlamlı miktarda atılmazlar. Böbrek fonksiyonlarında hafif ve orta şiddette bozukluk olan hastalar, böbrek fonksiyonları normal hastalardan daha yüksek plazma değerlerine sahip görünmektedir. Artış yaklaşık olarak 1.5-2 kattır ve imatinibin güçlü bir biçimde bağlandığı plazma AGP değerinde 1.5 katlık bir artışa karşılık gelir. Böbrek bozukluğu olan hastalarda imatinibin serbest ilaç klerensi muhtemelen böbrek fonksiyonları normal hastalardakinin bir benzeridir; çünkü böbrekler yoluyla atılım imatinib için minör bir eliminasyon yolunu oluşturmaktadır (bkz. 4.2 Pozoloji ve uygulama şekli, 4.4 Özel kullanım uyarıları ve önlemleri ve 5.1 Farmakodinamik özellikler). Farmakokinetik analiz sonuçları kişiden kişiye değişikliklerin söz konusu olduğunu göstermesine rağmen, değişik derecelerde karaciğer yetersizliği olan hastalardaki imatinibe ortalama maruz kalım, karaciğer fonksiyonları normal olan hastalara kıyasla yükselmemiştir (bkz. 4.2 Pozoloji ve uygulama şekli, 4.4 Özel kullanım uyarıları ve önlemleri, 4.8 İstenmeyen Etkiler, 5.1 Farmakodinamik Özellikler ve 5.2 Farmakokinetik Özellikler). 5.3. Klinik öncesi güvenlilik verileriİmatinibin güvenlilik farmakolojisi, tekrarlanan doz toksisitesi, genotoksisite ve üreme toksisitesi çalışmalarında değerlendirilmiştir. Kemik iliği, periferik kan, lenfoid doku, gonadlar ve gastrointestinal kanal, imatinibin farmakolojik etkisi altında kalan hedef organlardandır. Diğer hedef organlar arasında karaciğer ve böbrek yer almaktadır.İmatinib, sıçanlarda embriyotoksik ve teratojen etki göstermiştir. 2 yıllık sıçan karsinoj eni site çalışmasında 15, 30 ve 60 mg/kg/gün olarak imatinib uygulanması, erkeklerde 60 mg/kg/gün dozunda ve dişilerde > 30 mg/kg/gün dozunda yaşam süresi üzerinde istatistiksel açıdan anlamlı azalmaya neden olmuştur. Ölenlerde yapılan histopatolojik inceleme, ölümün temel nedeni ya da öldürülme nedeni olarak kardiyomiyopati (her iki cinsiyet), kronik ilerleyici nefropati (dişiler) ve prepusyal bez papillomunu ortaya koymuştur. Neoplastik değişiklikler açısından hedef organlar böbrekler, mesane, üretra, prepusyal ve klitoral bez, ince bağırsak, paratiroid bezleri, adrenal bezler ve glandüler-olmayan mide olmuştur. Neoplastik lezyonlar bulunan çeşitli hedef organlardaki etki görülmeyen düzeyler (NOEL) şu şekilde saptanmıştır: böbrekler, mesane, üretra, ince bağırsak, paratiroid bezleri, adrenal bezler ve glandüler-olmayan mide için 30 mg/kg/gün ve prepusyal ve klitoral bez için 15 mg/kg/gün. Prepusyal/klitoral bezde papilloma/karsinoma 30 ve 60 mg/kg/gün olarak saptanmıştır ve bu değer, insandaki günlük maruziyetin (EAA değerine dayanarak 400 mg/gün ya da 800 mg/gün) yaklaşık 0.5 ila 4 ya da 0.3 ila 2.4 katına ve çocuklardaki günlük maruziyetin (EAA değerine dayanarak 340 mg/m2) 0.4 ila 3.0 katına karşılık gelmektedir. 60 mg/kg/gün ile renal adenoma/karsinoma, mesane ve üretra papillomu, ince bağırsak adenokarsinomları, paratiroid bezi adenomları, adrenal bezlerde benign ve malign medüller tümörler ve glandüler-olmayan mide papillomaları/karsinomaları görülmüştür. Sıçan kar sinoj eni site çalışmalarından elde edilen bu bulguların insanlar için anlamı bilinmemektedir. Klinik çalışmalardan elde edilen güvenlilik verilerinin ve spontan advers olay bildirimlerinin bir analizi, genel popülasyonla karşılaştırıldığında imatinib ile tedavi edilen hastalarda genel malignite insidansında artışla ilgili bir kanıt ortaya koymamıştır. İlk klinik çalışmalarda saptanmayan non-neoplastik lezyonlar kardiyovasküler sistem, pankreas, endokrin organlar ve dişlerle ilgili olmuştur. En önemli değişiklikler bazı hayvanlarda kalp yetmezliği belirtilerine yol açan kardiyak hipertrofi ve dilatasyonu içermiştir. 6. FARMASÖTİK ÖZELLİKLER6.1.Yardımcı maddelerin listesiKrospovidon Magnezyum stearat Aerosil 200Titanyum dioksit (E171) Jelatin 6.2.GeçimsizliklerGeçerli değildir.6.3.Raf ömrü24 ay6.4.Saklamaya yönelik özel tedbirler25°C'nin altındaki oda sıcaklığında saklayınız.6.5.Ambalajın niteliği ve içeriği60 kapsül PVC/Al blister içinde kullanma talimatı ile beraber karton kutuda ambalajlanır.6.6.Beşeri tıbbi üründen arta kalan maddelerin imhası ve diğer özel önlemlerKullanılmamış olan ürünler ya da atık materyaller "Tıbbi Atıkların Kontrolü Yönetmeliği" ve "Ambalaj ve Ambalaj Atıklarının Kontrolü Yönetmelik" lerine uygun olarak imha edilmelidir.7.RUHSATSAHIBILogus İlaç San. Tic. Ltd. Şti.Tozkoparan Mah. General Ali Rıza Gürcan Cad. Merter İş Merkezi Bağımsız Bölüm No:2/8 Güngören / İSTANBUL Telefon: 0212 481 67 56 Faks: 0212 481 67 56 e-mail: [email protected] 8.RUHSAT NUMARASI(LARI)248/129.İLK RUHSAT TARIHI/RUHSAT YENİLEME TARIHI11.02.201310.KÜB'ÜNYENILENME TARIHI1İleri evrede hastalığı, ağır enfeksiyonları, şiddetli nötropenisi ve diğer ciddi eşlik eden rahatsızlıkları olan hastalarda fatal vakalar bildirilmiştir2Bazı ölümcül gastrointestinal perforasyon vakaları bildirilmiştir. |
İlaç Bilgileriİmatenil 200 mg KapsülEtken Maddesi: İmatinib mesilat Atc Kodu: L01XE01 Kullanma talimatı ve kısa ürün bilgileri
Google Reklamları
İlgili İlaçlar |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
Ana Sayfa | Hakkımızda | İlaçlar | İlaç Ara | İlaç Firmaları | Gizlilik | Bize Ulaşın
Telif Hakkı 2008-2026 © İlaç Prospektüsü. Tüm Hakları Saklıdır.Uyarı: Sitemizde yayınladığımız ilaç bilgileri ile doktora danışmadan kesinlikle ilaç kullanmayınız!
Aksi halde doğabilecek sağlık sorunlarından ilacprospektusu.com sorumlu tutulamaz.