Ricus 1 Mg/ml Oral Çözelti Kısa Ürün BilgisiKISA URUN BILGISI1. BEŞERI TIBBI URUNUN ADIRİCUS® 1 mg/ml oral çözelti 2. KALITATIF VE KANTİTATIF BILEŞIMHer 1 ml oral çözeltide, Etkin madde:Risperidon 1 mg Yardımcı maddeler:
1 mg
Sorbitol %70 Yardımcı maddeler için 6.1.'e bakınız. 3. FARMASÖTIK FORMOral çözelti. Berrak, renksiz çözelti. 4. KLINIK ÖZELLIKLER4.1. Terapötik endikasyonlarRİCUS®, pozitif (halüsinasyon, delüzyon, düşünce bozuklukları, saldırganlık, şüphecilik) ve/veya negatif (künt afekt, emosyonel ve sosyal çekingenlik ve konuşma yetersizliği)semptomların belirgin olduğu, erken dönem psikozlar, akut şizofrenik alevlenmeler, kronikşizofreni ve diğer psikotik durumlar dahil şizofreni hastalarının tedavisinde endikedir.RİCUS®, şizofreni ile ilgili afektif semptomları (depresyon, suçluluk duygusu, anksiyete) dahafifletir. RİCUS®, ilk tedaviye cevap verdiği gözlenen yetişkin hastalarda, idame tedavisisırasında klinik iyileşmenin devamı açısından da etkilidir. RİCUS®, bipolar bozukluğun manik epizodunun tedavisinde endikedir. Bu epizodlar; duygu durumu yükselmesi veya aşırı hassaslaşması, kendini aşırı beğenme, uykuya duyulanihtiyacın azalması, konuşmada zorlanma, düşüncelerin yarışması, şaşkınlık, agresif ve yıkıcıdavranışlar da dahil olmak üzere muhakeme güçlüğü gibi semptomlarla karakterizedir. RİCUS®, agresif veya diğer yıkıcı davranışların ön planda olduğu davranış ve diğer yıkıcı davranış bozukluklarının tedavisinde endikedir. RİCUS® ayrıca ilk tedaviye cevapverdiği gözlenen çocuk ve adolesanlarda idame tedavisi sırasında klinik iyileşmenin devamıaçısından da etkilidir.
RİCUS®, çocuklarda ve ergenlerde otistik bozukluğa bağlı huzursuzluk (agresif belirtiler, kendine zarar verme, öfke nöbetleri, ani duygu durum değişiklikleri) tedavisinde endikedir. 4.2. Pozoloji ve uygulama şekliPozoloji/ uygulama sıklığı ve süresi:ŞizofreniYetişkinler: RİCUS®, günde bir ya da iki kez verilebilir. Hastalar günde 2 mg RİCUS® ile başlamalıdır. Doz, ikinci gün 4 mg'a yükseltilebilir. Üçüncü günden sonra doz sabit kalabilir ya da gerektiğinde bireyselleştirilebilir. Çoğu hastaiçin optimal doz 4-6 mg/gün'dür. Bazı hastalarda, daha yavaş bir titrasyon fazı ve daha düşükbaşlangıç ve idame dozları uygun olabilir. Günde 10 mg'ın üzerindeki dozların düşük dozlara göre daha etkili olduğu gösterilmemiştir ve bu dozlar ekstrapiramidal semptomlara neden olabilir. Günde 16 mg'ın üzerindekidozların güvenliliği araştırılmadığından, bu dozun üzerinde kullanılmamalıdır. İlave sedasyon gerektiğinde, RİCUS® ile tedaviye bir benzodiazepin eklenebilir. Yaşlılar: Günde iki kez 0,5 mg ile başlanması önerilir. Bu doz günlük iki kez 0,5 mg'lık artışlarla günde iki kez 1-2 mg'a bireysel olarak ayarlanabilir. Adolesanlar: 18 yaş altındaki çocuklarda şizofreni tedavisinde veri yetersizliği nedeniyle risperidon kullanılması önerilmez. İdame Tedavisi Bir şizofreni hastasının RİCUS® tedavisine ne kadar devam etmesi gerektiği bilinmemekle birlikte, günde 2 mg ila 8 mg Risperidon'un relapsı geciktirmedeki etkililiği, kontrollü birçalışmada en az 4 hafta süreyle klinik olarak stabil kalıp daha sonra 1 ila 2 yıl süreyle takipedilen yetişkin hastalarda gösterilmiştir. Akut olarak yanıt veren hem yetişkin hem deadolesan hastaların, genellikle etkili dozlarını akut dönemin sonuna kadar sürdürmelerigerekmektedir. İdame tedavisinin gerekli olup olmadığı konusunda, hastaların belirliaralıklarla yeniden değerlendirmeleri gerekmektedir. ®Daha Önce Tedaviyi Bırakan Hastalarda Tedavinin Yeniden Başlatılması Tedavinin yeniden başlatılmasına ilişkin spesifik veri bulunmamakla birlikte, RİCUS
tedavisine ara verildikten sonra ilk titrasyon planına uyulması önerilir. Diğer Antipsikotik İlaçlardan Geçiş Yapma Şizofreni hastalarının diğer antipsikotik ilaçlardan RİCUS®'a geçiş yapmaları veya bu hastaların RİCUS® ile eşzamanlı olarak başka antipsikotiklerle tedavi edilmelerine ilişkinsistematik olarak toplanmış spesifik veri bulunmamaktadır. Bipolar maniYetişkinler: RİCUS®, 2 mg veya 3 mg ile başlanarak günde tek doz olarak verilmelidir. Endike olduğunda doz düzenlemeleri 24 saatten az sürede gerçekleştirilmemelidir ve doz artırımlarıgünde 1 mg olmalıdır. Etkinlik günde 1-6 mg arasında esnek dozlarda gösterilmiştir. 6 mgrisperidonu aşan günlük dozlar manik atağı olan hastalarda araştırılmamıştır. Bütün semptomatik tedavilerde olduğu gibi devam eden RİCUS® kullanımı sürekli olarak değerlendirilmeli ve uygunluğu kanıtlanmalıdır. Yaşlılar: Günde iki kez 0,5 mg ile başlanması önerilir. Bu doz günlük iki kez 0,5 mg'lık artışlarla günde iki kez l-2 mg'a bireysel olarak ayarlanabilir. Yaşlılarda klinik deneyim sınırlı olduğuiçin dikkatli kullanılmalıdır. Çocuklar ve adolesanlar: 18 yaş altındaki çocuklarda bipolar mani tedavisinde veri yetersizliği nedeniyle risperidon kullanılması önerilmez. İdame Tedavisi Akut bir manik epizotun RİCUS® ile tedavisi sırasında iyileşme gösteren hastaların daha uzun dönemli yönetimi konusunda klinisyenlere yol gösterecek kontrollü çalışmalardan eldeedilmiş kanıtlar mevcut değildir. Manide, hem ilk yanıtın sürdürülmesi hem de yeni manikepizotların önlenmesi için farmakolojik tedavinin akut yanıttan sonra da devam etmesi görüşühakim olmakla birlikte, RİCUS®'un bu tür uzun dönemli tedavilerde (yani 3 haftadan dahafazla süren) kullanımını destekleyen sistematik olarak elde edilmiş veri bulunmamaktadır.Uzun süreli olarak RİCUS® kullanmayı seçen doktorların, her bir hasta için ilacın uzundönemli risk ve faydalarını belirli aralıklarla yeniden değerlendirmeleri gerekmektedir. Davranış ve diğer yıkıcı davranış bozuklukları5-18 yaş arası çocuklar ve adolesanlar: 50 kg veya üzerinde olan hastalar:fazla gün aşırı 3 / 32 Başlangıç dozu olarak günde bir defa 0,5 mg önerilir. Bu d olmak kaydı yla 0,5 mg'lık dozlarla arttırılabilir. Birçok hasta için optimum doz günde bir defa 1 mg'dır. Yine de bazı hastalarda günde bir defa 0,5 mg ile, bazılarında ise günde birdefa 1.5 mg ile en iyi sonuç alınabilir. 50 kg'ın altında olan hastalar:Başlangıç dozu olarak günde bir defa 0,25 mg önerilir. Bu doz gerektiğinde, en fazla gün aşırı olmak kaydıyla 0,25 mg'lık dozlarla arttırılabilir. Birçok hasta için optimum doz günde birdefa 0,5 mg'dır. Yine de bazı hastalarda günde bir defa 0,25 mg ile, bazılarında ise günde birdefa 0,75 mg ile en iyi sonuç alınabilir. Tüm semptomatik tedavilerde olduğu gibi, RİCUS®'un sürekli kullanımı tedavi süresince değerlendirilmeli ve doğrulanmalıdır. 5 yaşın altındaki çocuklarda (bu hastalığa ilişkin) kullanımına dair deneyim yoktur. OtizmÇocuklar ve adolesanlar: RİCUS®'un dozajı, hastanın ihtiyaç ve cevabına (ilacı tolere etmesine) göre kişiselleştirilmelidir. Dozlamaya, 20 kg'ın altındaki hastalar için günde 0,25 mg, 20 kg ve üstündeki hastalar için ise günde 0,5 mg ile başlanmalıdır. 4. günde doz; 20 kg'ın altındaki hastalar için 0,25 mg, 20 kg ve üstündeki hastalar için de 0,5 mg artırılabilir. Bu doz devam ettirilmeli ve cevap yaklaşık olarak 14. günde değerlendirilmelidir. Sadece yeterli klinik cevap veremeyen hastalarda, ilave doz artırımı düşünülebilir. 20 kg'ın altındakihastalar için 0,25 mg ve 20 kg ve üstündeki hastalar için 0,5 mg doz artırımları, 2 hafta vedaha uzun aralıklarla yapılmalıdır. Klinik çalışmalarda, çalışılan en yüksek doz, 20 kg'ın altındaki hastalarda günlük 1,5 mg'ı, 20 kg ve üstündeki hastalarda günlük 2,5 mg'ı ve 45 kg üstündeki hastalarda günlük 3,5 mg'ıaşmamıştır. 15 kg'dan düşük ağırlığa sahip çocuklarda kullanılacak dozlara ilişkin herhangibir veri bulunmamaktadır.
Otistik bozukluğu olan pediyatrik hastalarda RİCUS® dozları (toplam mg/gün)
*45 kg'dan ağır vakalar daha yüksek doza gereksinim duyabilir; çalışılan en yüksek doz 3,5 mg/gündür. RİCUS®, günde bir kere veya günde iki kez uygulanabilir. Somnolansı olan hastalar yatmadan önce günde bir ya da iki kez kullanımda fayda görebilirler. Yeterli klinik cevaba ulaşıldığında ve devam ettirildiğinde, etkililik ve güvenliliğin optimal dengesine ulaşmak için dozun yavaş yavaş azaltılması düşünülebilir. 5 yaşın altındaki çocuklarda kullanımına dair yeterli deneyim yoktur. Uygulama şekli:Oral yoldan çay ve alkol haricinde bir içeceğe karıştırılarak kullanılır. Besinler RİCUS®'un absorbsiyonunu etkilemez. Diğer antipsikotiklerden geçiş: Tıbbi olarak uygun olduğu durumlarda, RİCUS® tedavisi başladığında daha önceki tedavinin yavaş yavaş kesilmesi önerilir. Ayrıca, tıbbi olarak uygun olduğunda, depo antipsikotiklerdengeçiş için bir sonraki planlanan enjeksiyon yerine, RİCUS® tedavisine başlanabilir. Halendevam etmekte olan antiparkinson ilaçlarla tedaviye devam edilip edilmeyeceği periyodikolarak tekrar değerlendirilmelidir. Tedavi bırakılacaksa ilacın yavaş yavaş kesilmesi önerilir. Antipsikotik ilaçların yüksek dozlarının aniden kesilmesinden sonra çok nadir olarak bulantı, kusma, terleme ve insomniada dahil olmak üzere akut ilaç kesilme semptomları bildirilmiştir. Psikotik semptomlartekrarlayabilir ve istem dış^eijharefeeteifeozuktuklarFHpnnnortaya çıktığı (akatizi, distoni ve
diskinezi gibi) bildirilmiştir. 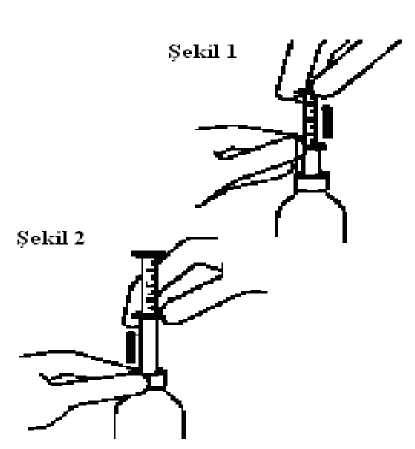 Şekil 1. Pipeti koruyucu kapağından çıkarıp şişeye üstten sokunuz. Althalkayı tutarken, üst halkayı ihtiyacınızolan mililitre veya miligram çizgisinegetiriniz. Şekil 2. Alt halkayı tutarak tüm pipeti şişeden çıkartınız. Üst halkayı aşağıdoğru kaydırarak, pipeti çay dışında,alkollü olmayan bir içeceğe boşaltınız.Şişeyikapatınız vepipetisuyla yıkayınız. Bir sonraki kullanıma kadar pipetin koruyucu kapağını takınız. Özel popülasyonlara ilişkin ek bilgiler:Böbrek/Karaciğer yetmezliği:Böbrek bozukluğu olan hastaların normal renal işleve sahip yetişkinlere göre ilacın aktif antipsikotik fraksiyonunu elimine etme yetenekleri azalmıştır. Bozulmuş karaciğer fonksiyonu olan hastalarda risperidonun serbest fraksiyonunun plazma konsantrasyonlarında artışlar görülür. Endikasyona bağlı olmaksızın başlangıç ve takip eden dozlar yarıya düşürülmeli, böbrek ve karaciğer bozukluğu olan hastalarda doz titrasyonu daha yavaş olmalıdır. Bu grup hastalarda RICUS® dikkatle kullanılmalıdır. Pediyatrik popülasyon:Pediyatrik popülasyon ile ilgili bilgiler yukarıda Pozoloji/uygulama sıklığı ve süresi başlığı altında verilmiştir. Geriyatrik popülasyon:Geriyatrik popülasyon ile ilgili bilgiler yukarıda Pozoloji/uygulama sıklığı ve süresi başlığı altında verilmiştir. 4.3. KontrendikasyonlarRisperidon veya yardımcı maddelerden herhangi birine karşı aşırı duyarlılığı olduğu bilinen
hastalarda kontrendikedir. Risperidon ve paliperidon ile tedavi edilen hastalarda anafilaktik reaksiyonlar ve anjiyoödem dahil olmak üzere hipersensitivite reaksiyonları bildirilmiştir.Paliperidon risperidonun bir metabolitidir. 4.4. Özel kullanım uyarıları ve önlemleriDemanslı yaşlı hastalar Genel Mortalite Konvansiyonel ve diğer yeni nesil (atipik) antipsikotik ilaçlarda olduğu gibi, bu ilaç da demansı olan yaşlı hastaların psikozlarında kullanıldığında serebrovasküler olaylar,enfeksiyon, kalp yetmezliği ile ani ölüm vb. nedenlerle ölüm riskinde artışa neden olmaolasılığı taşımaktadır. Risperidon dahil atipik antipsikotik ilaçların incelendiği 17 kontrollü çalışmaya ilişkin meta-analizde, plaseboya kıyasla atipik antipsikotik ilaçlarla tedavi gören demanslı yaşlıhastalarda mortalitenin daha yüksek olduğu belirlenmiştir. Bu hasta grubunda risperidon ileyapılan plasebo kontrollü çalışmalarda, plasebo uygulanan hastalardaki %3,1 oranına kıyaslarisperidon uygulanan hastalarda mortalite insidansı %4'tür. Olasılık oranı (%95 gerçek güvenaralığı) l,21 (0,7;2,1)'dir. Ölen hastaların ortalama yaşı 86'dır (yaş aralığı 67-100). İki genişgözlemsel çalışmanın verileri, konvansiyonel antipsikotiklerle tedavi edilen demanslı yaşlıkişilerde de, tedavi görmeyenlere kıyasla ölüm riskinde küçük bir artış olduğunu göstermiştir.Mevcut veriler, riskin gerçek boyutunun tam bir şekilde tahmin edilmesi için yetersizdir verisk artışının nedeni bilinmemektedir. Gözlemsel çalışmalardaki mortalite artışı bulgularınınhangi oranda antipsikotik ilaca veya hastaların sahip oldukları bazı özelliklere bağlanabileceğiaçık değildir. Furosemidle Birlikte Kullanım Risperidon ile yapılan plasebo kontrollü çalışmalarda demansı olan yaşlı hastalarda, tek başına risperidon (%3,1; ortalama yaş 84, yaş aralığı 70-96) ya da tek başına furosemid(%4,1; ortalama yaş 80, yaş aralığı 67-90) ile tedavi edilen hastalarla kıyaslandığında,furosemid+risperidon (%7,3; ortalama yaş 89, yaş aralığı 75-97) ile tedavi edilen hastalardadaha yüksek mortalite insidansı gözlenmiştir. Furosemid+risperidon ile tedavi edilenhastalarda mortalitedeki artış dört klinik çalışmanın iki tanesinde gözlenmiştir. Risperidonundiğer diüretiklerle birlikte uygulanması (esas olarak düşük dozda kullanılan tiyaziddiüretikleri) benzer bulgular ile ilişkili değildir. Bu bulguyu açıklayacak bir patofizyolojik mekanizma tanımlanamamış ve ölüme sebebiyette tutarlı bir neden gözlenmemiştir. Ancak, kullanım kararından önce dikkat edilmeli ve bukombinasyonun veya diğer begüçJ^enidıiürtetiklieFleiebiTlıi>fet®tııuygulamanın risk ve yararları
değerlendirilmelidir. Risperidon ile birlikte diğer diüretiklerin kullanımında hastalarda artan mortalite insidansına rastlanmamıştır. Tedaviden bağımsız olarak dehidratasyon mortalite içingenel bir risk faktörüdür ve demansı olan yaşlı hastalarda dehidratasyondan dikkatlekaçınılmalıdır. Serebrovasküler Advers Olaylar Demanslı popülasyonda, bazı atipik antipsikotiklerle yapılan randomize plasebo kontrollü klinik çalışmalarda serebrovasküler advers olay riskinde yaklaşık 3 kat artış görülmüştür.Çoğunlukla demanslı yaşlı hastalarda (>65 yaşında) risperidon ile altı plasebo kontrollüçalışmadan toplanan veriler, serebrovasküler advers olayların (ciddi ve ciddi olmayan,birlikte) risperidon ile tedavi edilen hastaların %3,3'ünde (33/1009) ve plasebo ile tedaviedilen hastaların %1,2'sinde (8/712) meydana geldiğini göstermiştir. İhtimal oranı (%95 tamgüven aralığı) 2,96'dır (1,34, 7,5). Bu artan riske yönelik mekanizma bilinmemektedir.Diğer antipsikotikler ve diğer hasta popülasyonlarında artan risk göz ardı edilemez.RİCUS®, inme için risk faktörü taşıyan hastalarda dikkatli kullanılmalıdır. Serebrovasküler advers olay riski, Alzheimer demansına kıyasla karma veya vasküler tip demans hastalarında anlamlı ölçüde yüksektir. Bu nedenle, Alzheimer'dan başka demanstiplerine sahip hastalar da risperidon ile tedavi edilmemelidir. Doktorlara, her bir hastada bireysel inme riski öngörülerini de göz önünde bulundurarak, demanslı yaşlı hastalarda RİCUS® kullanımının riskleri ve faydalarını değerlendirmeleriönerilir. Hastalar/bakıcılar yüzde, kollarda ya da bacaklarda beklenmedik halsizlik veyauyuşukluk ve konuşma veya görme bozuklukları gibi olası serebrovasküler advers olaybelirtileri ve semptomlarını hemen bildirme konusunda uyarılmalıdır. Risperidonun kesilmesidahil tüm tedavi seçenekleri gecikmeden değerlendirilmelidir. RİCUS®, orta ila ciddi Alzheimer demans hastalarının sürekli agresyonu için ve kendilerine veya başkalarına zarar verme olasılığı olduğunda, sınırlı etkililiği olan veya hiçbir etkililiğibulunmayan, farmakolojik olmayan yaklaşımlarda yalnızca kısa süreli olarak kullanılmalıdır.Hastalar düzenli olarak ve tedavilerinin sürdürülmeleri açısından yenidendeğerlendirilmelidir. Ortostatik Hipotansiyon Risperidonun alfa-bloke edici aktivitesi nedeniyle, özellikle tedavinin başlangıç doz-titrasyonu döneminde (ortostatik) hipotansiyon görülebilir. Risperidon ve antihipertansif tedavinin birlikte kullanımı ile, pazarlama sonrası klinik açıdan önemli hipotansiyongözlenmiştir. RİCUS® kardiyovasküler hastalığı (örneğin kalp yetmezliği, miyokardinfarktüsü, ileti anomalileriŞıdehidrataöyoffrohipovoleroiiveyai'serebrovasküler hastalık) olduğu
bilinen hastalarda dikkatle kullanılmalı ve doz yavaş yavaş, önerildiği gibi arttırılmalıdır (bkz. Bölüm 4.2). Hipotansiyon görüldüğünde doz azaltılmalıdır. Lökopeni, Nötropeni ve Agranülositoz Risperidon dahil olmak üzere, antipsikotik ajanlarla lökopeni, nötropeni ve agranülositoz olayları bildirilmiştir. Pazarlama sonrası izlemde agranülositoz çok nadiren (<1/10.000 hasta)bildirilmiştir. Klinik olarak anlamlı düzeyde düşük beyaz kan hücresi (WBC) sayımı veya ilaçla tetiklenmiş lökopeni/nötropeni öyküsüne sahip hastalar tedavinin ilk birkaç ayı boyunca izlenmeli veortada başka nedensel faktörler yokken WBC'de klinik olarak anlamlı bir düşüşe yönelik ilkbelirtide RİCUS® kullanımına son verilmesi düşünülmelidir. Klinik olarak anlamlı nötropenisi olan hastalar ateş veya diğer enfeksiyon semptomları veya belirtileri açısından dikkatle izlenmeli ve bu tür semptomlar veya belirtilerin ortaya çıkmasıhalinde derhal tedavi edilmelidir. Şiddetli nötropenisi olan hastalar (mutlak nötrofil sayımı <1X 109/L) RİCUS® kullanımına son vermeli ve iyileşene kadar WBC düzeylerini takipettirmelidir. Tardif Diskinezi/Ekstrapiramidal Semptomlar (TD/EPS) Dopamin reseptörlerinde antagonistik etkiler gösteren ilaçlar, özellikle dil ve/veya yüzde istemsiz ritmik hareketler ile karakterize tardif diskinezi gelişimi ile ilgili bulunmuştur.Ekstrapiramidal semptomların görülmesinin tardif diskinezi gelişiminde bir risk faktörüolduğu bildirilmiştir. Tardif diskinezi işaret ve semptomları görülürse tüm antipsikotikilaçların kesilmesi göz önünde tutulmalıdır. Psikostimulanlarla (örn. metilfenidat) risperidonu birlikte kullanan hastalarda, ilaçlardan birini veya her ikisini ayarlarken ekstrapiramidal semptomlar ortaya çıkabileceği için dikkatliolunmalıdır. Stimulan tedavisinin kademeli olarak kesilmesi önerilir (bkz. Bölüm 4.5). Nöroleptik Malign Sendrom (NMS) Antipsikotiklerin kullanımı sırasında hipertermi, kas rijiditesi, otonom instabilite, bilinç bulanıklığı ve yüksek serum kreatinin fosfokinaz düzeyleri ile kendini gösteren nöroleptikmalign sendromu oluştuğu bildirilmiştir. Miyoglobinüri (rabdomiyoliz) ve akut böbrekyetmezliği ilave işaretler olabilir. Bu durumunda, RİCUS® dahil olmak üzere tümantipsikotikler kesilmelidir. Parkinson Hastalığı veya Lewy Cisimlerinin bulunduğu Demans Parkinson Hastalığı veya Lewy > Ci'Biimteiklpii©>emfenBiai(LC©) olan hastalara RİCUS® dahil
antipsikotikler reçete edilirken, hekimler risk/yarar değerlendirmesi yapmalıdır, Parkinson hastalığı risperidon ile kötüleşebilir. Her iki grupta da antipsikotik ilaçlara duyarlılıkartabileceği gibi Nöroleptik Malign Sendrom riski de artabilir. Bu hastalar klinikaraştırmaların dışında tutulmuşlardır. Bu artan duyarlılığın semptomları arasında,ekstrapiramidal semptomlara ek olarak, konfüzyon, küntleşme ve sık düşmelerin olduğupostural instabilite bulunabilir. Hiperglisemi ve Diabetes Mellitus Risperidon tedavisi sırasında hiperglisemi, diabetes mellitus ve önceden var olan diyabetin kötüleşmesi bildirilmiştir. Bazı durumlarda vücut ağırlığında bir ön artış rapor edilmiştir. Bu bir yatkınlaştırıcı bir faktör olabilir. Ketoasidoz ile ilişki çok nadir olarak ve diyabetik koma ile ilişki nadir olarak raporedilmiştir. Uygun klinik izlem, kullanılan antipsikotik kılavuz kurallarına uygun olaraktavsiye edilebilir. Risperidon dahil olmak üzere herhangi bir atipik antipsikotik ile tedaviedilen hastalarda hiperglisemi semptomları (örneğin polidipsi, poliüri, iştah ve halsizlik gibi)izlenmelidir ve diyabet hastaları glukoz kontrolünün kötüleşmesi açısından düzenli olarakizlenmelidir. Kilo alımı Anlamlı kilo alımı bildirilmiştir. RİCUS® kullanıldığında kilo alımının izlenmesi önerilir. Hiperprolaktinemi Hiperprolaktinemi, risperidon tedavisinde görülen yaygın bir yan etkidir. Prolaktin ilişkili yan etki belirtilerin (örneğin; jinekomasti, menstrual düzensizlikler, anovülasyon, fertilitebozuklukları, libido kaybı, erektil disfonksiyon ve galaktore) görüldüğü hastalarda prolaktinplazma seviyelerinin değerlendirilmesi tavsiye edilmektedir. Doku kültürü çalışmaları insan meme tümörlerinde hücre büyümesinin prolaktin tarafından stimüle edilebileceğini belirtmektedir. Klinik ve epidemiyolojik çalışmalarda antipsikotikkullanımı ile ilişkisi açık bir şekilde gösterilememiş olsa da, ilgili tıbbi öyküsü olanhastalarda dikkatli olunması önerilmektedir. RİCUS®, daha önceden hiperprolaktinemisi veolası bir prolaktine bağlı tümörü olan hastalarda dikkatli kullanılmalıdır. QT Uzaması Belge DoQT uzaması, pazarlama sonrası çok nadir rapor edilmiştir. QT aralığını uzattığı bilinen ilaçlarla birlikte kullanıldığında diğer antipsikotiklerde olduğu gibi, bilinen kardiyovaskülerhastalığı, ailede QT uzaması öyküsü, bradikardi veya elektrolit bozukluğu olan hastalarda(hipokalemi, hipomagnezim'i),®. gariıtfeojenik imzetkizrp9kirti- artırabildiği için risperidon »ğralama Kodu: lZW56aklUZmxXZmxXS3k0SHY3ZW56SHY3 Belge Takip Adresi:https://www.turKye.gov.tr/saglik-titck-ebysverildiğinde dikkatli olunmalıdır. RİCUS®'un da dahil olduğu antipsikotikler, uzamış QT Sendromu/Torsades de Pointes'e neden olabileceği için tanısı konmuş veya şüpheli konjenitaluzamış QT sendromu veya Torsades de Pointes hastalarında RİCUS® kullanılmamalıdır. Nöbetler RİCUS®, nöbet eşiğini potansiyel olarak düşüren durumlarda veya nöbet hikayesi olan hastalarda dikkatli kullanılmalıdır. Priapizm Alfa-adrenerjik blokör özelliğinden dolayı RİCUS® ile tedavi sırasında priapizm görülebilir. Vücut Sıcaklığının Regülasyonu Vücudun vücut sıcaklığını düşürme yeteneğinin bozulması antipsikotik ilaçlarla ilişkilendirilmiştir. Ağır egzersiz, aşırı sıcağa maruz kalma, eş zamanlı antikolinerjik tedavigörme veya dehidratasyona uğrama gibi vücut ısısının artmasına katkıda bulunabilecektablolar geçirebilecek hastalara RİCUS® reçete edilirken, uygun bakım önlemleri alınmalıdır. Antiemetik etki Risperidon ile yapılan klinik öncesi çalışmalarda antiemetik etki gözlenmiştir. Bu etki, eğer insanlarda oluşursa, bağırsak tıkanması, Reye sendromu ve beyin tümörü gibi durumları veyabelli ilaçların aşırı doz bulgu ve semptomlarını maskeleyebilir. Böbrek ve karaciğer yetmezliği Normal böbrek fonksiyonu olan erişkinlere göre böbrek yetmezliği olan hastalar aktif antipsikotik fraksiyonunu daha az elimine etme yeteneğine sahiptir. Karaciğer yetmezliği olanhastaların plazma konsantrasyonunda risperidonun serbest fraksiyonu artış gösterir (bkz.Bölüm 4.2). Venöz tromboembolik olay Antipsikotik ilaçlarla venöz tromboembolik olaylar (VTE) bildirilmiştir. Antipsikotik ilaç tedavisi gören hastalarda çoğunlukla kazanılmış VTE risk faktörleri bulunduğu için, VTE içintüm olası risk faktörleri, RİCUS® ile tedaviden önce ve sonra tanımlanmalı ve koruyucuönlemler alınmalıdır. İntraoperatif Floppy İris Sendrom Katarakt ameliyatı sırasında, risperidon dahil alfa 1a adrenerjik antagonist etki gösteren ilaçları kullanan hastalarda İntraoperatif Floppy İris Sendromu (IFIS) gözlenmiştir. IFIS,ameliyat sırasında ve sonrasında göz komplikasyonları riskini arttırabilir. Ameliyat öncesindehastanın alfa 1a adrenerjikuaritagönjsteiflaçlârfngeçroFştenfcüllanmış veya halen kullanmakta
olduğu göz cerrahına mutlaka iletilmelidir. Katarakt ameliyatı öncesinde alfa 1 bloker tedavisinin kesilmesinin potansiyel faydası kanıtlanmamıştır ve antipsikotik tedavinin kesilmesinin oluşturabileceği risk göz önündebulundurulmalıdır. Uyku apnesi sendromu Risperidon kullanan hastalarda uyku apnesi sendromu rapor edilmiştir. Eş zamanlı olarak santral sinir sistemi depresanı kullanan hastalar ile uyku apnesi öyküsü olan ya da uyku apnesiriski taşıyan (örn; aşırı kilolu/obezler veya erkekler) hastalarda RİCUS® kullanılırken dikkatliolunmalıdır. Çocuklar ve adolesanlar Davranış bozukluğu olan bir çocuğa veya adolesana risperidon reçete edilmeden önce, bu hastalar ağrı veya uygunsuz çevresel talepler gibi agresif davranışa yol açabilecek fizikselve sosyal nedenler açısından tam olarak değerlendirilmelidir. Öğrenme yeteneğindeki olası sonuçları nedeniyle risperidonun sedatif etkisi bu popülasyonda yakından izlenmelidir. Risperidonun uygulanmasında zamanla yapılan bir değişiklik, çocukveya adolesanların dikkat kabiliyeti üzerindeki sedasyon etkisini geliştirebilir. Risperidon vücut ağırlığında ve vücut kitle indeksindeki ortalama artışlar ile ilişkili bulunmuştur. Tedaviden önce temel ağırlık ölçümü ve düzenli kilo izlenmesi tavsiye edilir.Açık etiketli uzun süreli uzatma çalışmalarında boy değişiklikleri beklenen yaşa uygunnormlar içinde kalmıştır. Uzun süreli risperidon tedavisinin cinsel olgunlaşma ve boy üzerineetkileri yeterince araştırılmamıştır. Çocuk ve adolesanlardaki gelişme ve cinsel olgunlaşmada uzun süreli hiperprolaktineminin olası etkisi nedeniyle boy, kilo, cinsel olgunluk, menstrüel işlevin izlenmesi ve diğer olasıprolaktinle ilgili etkileri içeren endokronolojik durumun düzenli klinik değerlendirmesi gözönünde bulundurulmalıdır. Pazarlama sonrası gözlemsel bir çalışmanın sonuçları, risperidona maruz kalan 8-16 yaş arası deneklerin boylarının diğer atipik antipsikotik ilaç tedavisi alanlardan ortalama olarakyaklaşık 3 ila 4,8 cm daha uzun olduklarını göstermektedir. Bu çalışma risperidona maruzkalmanın final yetişkin boyu üzerinde herhangi bir etkisinin olup olmadığı ya da kemikbüyümesi üzerine risperidonun doğrudan etkisinin olup olmadığı ya da kemik büyümesiüzerine altta yatan hastalığın etkisinin olup olmadığını ya da doğrusal büyüme artışı ile >u belge ı ı ıBelge Dintrolünün bir sonucu olup olmadığını belirlemek için yeterli değildir. Risperidon ile tedavi sırasında, ekstrapiramidal semptomlar ve diğer hareket bozuklukları açısından da düzenli muayene yapılmalıdır. Çocuk ve adolesanlarda spesifik pozoloji önerileri için Bölüm 4.2'ye bakınız. RİCUS®, sorbitol (E420) içerir. Nadir kalıtımsal fruktoz intolerans problemi olan hastaların bu ilacı kullanmamaları gerekir. 4.5. Diğer tıbbi ürünler ile etkileşimler ve diğer etkileşim şekilleriFarmakodinamik etkileşimler QT aralığını uzattığı bilinen ilaçlar: Diğer antipsikotiklerde olduğu gibi, antiaritmikler (örn. kinidin, dizopiramid, prokainamid, propafenon, amiodaron, sotalol), trisiklik antidepresanlar (örn. amitiriptilin), tetrasiklikantidepresanlar (örn. maprotilin), bazı antihistaminikler, diğer antipsikotikler, bazıantimalaryal ilaçlar (örn. kinidin ve meflokin) gibi QT aralığını uzattığı bilinen ilaçlar ilebirlikte risperidon reçete edilirken dikkatli olunmalıdır. Aynı şekilde elektrolit dengesizliği(hipokalemi, hipomagnezemi) ve bradikardiye yol açabilen ya da risperidonun hepatikmetabolizmasını inhibe eden ilaçlarla birlikte reçete edilirken dikkatli olunmalıdır. Bu listebelirleyicidir ve detaylandırılmamıştır. Merkezi sinir sistemini etkileyen ilaçlar ve alkol: Risperidon, alkol, opiatlar, antihistaminikler ve benzodiazepinleri de içeren diğer merkezi sinir sistemini etkileyen maddelerle kombinasyon halinde kullanılırken sedasyonunartabileceği riskine karşı dikkatli olunmalıdır. Levodopa ve dopamin agonistleri: RİCUS®, levodopa ve diğer dopamin agonistlerinin etkilerini antagonize edebilir. Eğer bu kombinasyon özellikle Parkinson hastalığının son aşamasında gerekli görülürse, her tedavininen düşük etkili dozu reçete edilmelidir. Hipotansif etkili ilaçlar: Pazarlama sonrasında risperidon ve antihipertansif tedavinin eşzamanlı kullanılması ile klinik olarak belirgin hipotansiyon gözlenmiştir. Psikostimulan İlaçlar Psikostimulanların (örn., metilfenidat) risperidon ile birlikte kullanılması, tedavilerden birinin ..... , .,,Bu belgeenli, elektronik imza ilş imzaUnmıştır.ı ı -i- zı ıBelge DoBölüm 4.4). Paliperidon Paliperidon, risperidonun aktif metaboliti olduğundan ve ikisinin kombinasyonu aditif aktif antipsikotik fraksiyon maruziyetine neden olabileceğinden oral RİCUS®'un paliperidon ile eşzamanlı kullanımı önerilmez. Farmakokinetik etkileşmeler Yiyecekler RİCUS®'un emilimini etkilemez. Risperidon büyük oranda CYP2D6 aracılığıyla, daha düşük oranla da CYP3A4 aracılığıyla metabolize olur. Risperidon ve aktif metaboliti olan 9-hidroksirisperidon, P-glikoprotein (P-gp) substratlarıdır. CYP2D6 aktivitesini değiştiren veya CYP3A4 ve/veya P-gp aktivitesinigüçlü indükleyen veya inhibe eden maddeler, risperidon aktif antipsikotik fraksiyonunfarmakokinetiğini etkileyebilirler. Güçlü CYP2D6 inhibitörleri RİCUS®'un güçlü CYP2D6 inhibitörleri ile birlikte uygulanması risperidon plazma seviyesini yükseltebilir, ancak ilacın aktif antipsikotik fraksiyonunun plazma seviyesini daha azyükseltir. Güçlü CYP2D6 inhibitörlerinin yüksek dozları, risperidonun aktif antipsikotikfraksiyonunun konsantrasyonunu yükseltebilir (örn. paroksetin, aşağı bakınız). Kinidin gibidiğer CYP2D6 inhibitörlerinin de risperidonun plazma konsantrasyonlarını benzer bir yollaetkilemesi beklenmektedir. Özellikle yüksek dozlarda olmak üzere paroksetin, kinidin veyabaşka bir güçlü CYP2D6 inhibitörü ile birlikte başlatıldığında veya kesildiğinde RİCUS®dozu doktorunuz tarafından tekrar değerlendirilmelidir. CYP3A4 ve/veya P-gp inhibitörleri RİCUS®'un güçlü CYP3A4 ve/veya P-gp inhibitörleri ile birlikte uygulanması risperidonun aktif antipsikotik fraksiyonunun plazma konsantrasyonunu yükseltebilir. Itrakonazol veyadiğer CYP3A4 ve/veya P-gp inhibitörleri tedaviye eklendiğinde veya kesildiğinde RİCUS®dozu doktorunuz tarafından tekrar değerlendirilmelidir. CYP3A4 ve/veya P-gp indükleyiciler RİCUS®'un güçlü CYP3A4 ve/veya P-gp indükleyicileri ile birlikte uygulanması risperidonun aktif antipsikotik fraksiyonunun plazma konsantrasyonunu düşürebilir.Karbamazepin veya diğer güçlü CYP3A4 ve/veya P-gp indükleyiciler tedaviye eklendiğindeveya kesildiğinde RİCUS® dozu doktorunuz tarafından tekrar değerlendirilmelidir. CYP3A4indükleyiciler etkilerini zamana bağlı bir şekilde gösterir ve başlama sonrası maksimum etkiseviyelerine ulaşmaları en az 2 hafta alabilir. Kesildiklerinde de CYP3A4 indüksiyonunun Rjd belgeazalması en az 2 hafta alabilir. Proteine yüksek oranda bağlı ilaçlar RİCUS® proteinlere yüksek oranda bağlı ilaçlarla birlikte kullanıldığında her iki ilacın plazma proteinlerinden klinikle ilişkili olarak yer değiştirmesi söz konusu değildir. İlaçlar ile birlikte kullanılırken, metabolizma yoluna veya muhtemel dozaj ayarlama ihtiyacına ilişkin bilgiler için ilgili etikete bakılmalıdır. Örnekler Risperidon ile potansiyel olarak etkileşen ya da etkileşme göstermemiş ilaçlarla ilgili örnekler aşağıda listelenmiştir: Diğer ilaçların risperidonun farmakokinetiği üzerine etkisi Antibakteriyeller: Orta dereceli bir CYP3A4 inhibitörü ve P-gp inhibitörü olan eritromisin, risperidon veaktif antipsikotik fraksiyonunun farmakokinetiğini değiştirmez. Güçlü CYP3A4 indükleyici ve P-gp indükleyici olan rifampisin, aktif antipsikotikfraksiyonun plazma konsantrasyonunu düşürür. Antikolinesterazlar: Her ikisi de CYP2D6 ve CYP3A4 substratı olan donepezil ve galantamin, risperidon veaktif antipsikotik fraksiyonunun farmakokinetiği üzerine klinik olarak anlamlı bir etkigöstermemektedir. Antiepileptikler: Güçlü CYP3A4 indükleyici ve P-gp indükleyici olan karbamazepin, risperidonun aktifantipsikotik fraksiyonunun plazma konsantrasyonunu düşürür. Fenitoin ve fenobarbitallergibi hem P-glikoproteini hem de CYP3A4 hepatik enzimlerini indükleyen ilaçlarla dabenzer etkiler görülebilir. Topiramat, risperidonun biyoyararlanımını ılımlı şekilde düşürmüş olup, aktif antipsikotikfraksiyonun biyoyararlanımını düşürmemiştir. Bu nedenle bu etkileşimin klinik açıdananlamlı olması muhtemel değildir. Antifungallar: Günde 200 mg dozunda olmak üzere güçlü bir CYP3A4 inhibitörü ve P-gp inhibitörü olanitrakonazol, 2 ila 8 mg/gün risperidon dozlarında aktif antipsikotik fraksiyonun plazmakonsantrasyonlarını yaklaşık %70 oranında arttırmıştır. Güçlü bir CYP3A4 inhi^örü.vePn-SBÂnhjıbiiıtörü fliânnketokonazol, günde 200 mg dozunda Belge Do belge,'^venlı eleKtromk imza ile imzalanmıştır. ^ ^fraksiyonunun konsantrasyonlarında klinik olarak anlamlı değişikliklerleilişkilendirilmemiştir. Ancak sertralin veya fluvoksaminin günde 100 mg'dan yüksek olandozları, risperidon etkin antipsikotik fraksiyonunun konsantrasyonlarını arttırabilir. Risperidonun diğer ilaçların farmakokinetikleri üzerine etkileri Antiepileptikler: Risperidon, valproat veya topiramat farmakokinetiği üzerinde klinik olarak anlamlı bir etkigöstermemektedir. Antipsikotikler: Bir CYP2D6 ve CYP3A4 substratıolan Aripiprazol:Risperidon tabletlerveya injeksiyonlar, ariprazol ve aktif metabolitidehidroaripiprazol farmakokinetiğini etkilememiştir. Digital glikozitleri: Risperidon,digoksin farmakokinetiğiüzerineklinikolarak anlamlı biretki göstermemektedir. Lityum: Risperidon,lityum farmakokinetiğiüzerineklinikolarak anlamlı biretki göstermemektedir. Risperidonun Furosemid ile birlikte kullanımı: Eşzamanlı olarak furosemid alan demanslı yaşlı hastalarda mortalitenin artışı ile ilgiliolarak bölüm 4.4'e bakınız. Özel popülasyonlara ilişkin ek bilgiler Pediyatrik popülasyon:Etkileşim çalışmaları sadece yetişkinlerde yapılmıştır. Bu çalışmaların sonuçlarının pediyatrik hastalar ile ilişkisi bilinmemektedir. Çocuklarda ve adolesanlarda risperidon ile psikostimülanların (örneğin metilfenidat) kombine kullanımı, risperidonun farmakokinetiğini ve etkinliğini değiştirmemiştir. Geriyatrik popülasyon:Birlikte furosemid kullanan demanslı yaşlı hastalarda artan mortalite ile ilgili olarak bölüm 4.4'e bakınız. 4.6. Gebelik ve laktasyonGenel tavsiyeGebelik Kategorisi: C Çocuk doğurma potansiyeli bulunan kadınlar/Doğum kontrolü (Kontrasepsiyon)Risperidonun çocuk doğurma potansiyeli bulunan kadınlarda kontrasepsiyon gerekliliğine işaret edecek yeterli bilgi mevcut değildir. Gebelik dönemiHayvan çalışmalarında risperidonun teratojenik etkisine rastlanmamış; fakat diğer üreme toksisitesi tipleri görülmüştür (bkz. Bölüm 5.3). İnsanlara yönelik potansiyel riskbilinmemektedir. Gebeliğin üçüncü trimesterinde antipsikotik ilaçlara (RİCUS® dahil)maruz kalan yeni doğanlar, doğumu takiben şiddeti değişebilen, anormal kas hareketleri(ekstrapiramidal işaretler/ekstrapiramidal semptomlar) ve/veya ilaç kesilme semptomlarıaçısından risk altındadırlar. Bu semptomlar, ajitasyon, hipertoni, hipotoni, tremor, somnolans,respiratuar distres veya beslenme bozukluklarını içermektedir. Yeni doğanlar dikkatliceizlenmelidir. RİCUS® kesinlikle gerekli olmadıkça gebelik sırasında kullanılmamalıdır.Gebelik sırasında tedavinin bırakılması gerekiyorsa, bu aniden yapılmamalıdır. Laktasyon dönemiHayvan çalışmalarında, risperidon ve 9-hidroksi-risperidon süt ile atılmaktadır (süte geçmektedir). Risperidon ve 9-hidroksi-risperidonun az miktarlarda anne sütüne de geçtiğikanıtlanmıştır. Emzirilen bebeklerdeki advers reaksiyonlar ile ilgili herhangi bir veri mevcutdeğildir. Bu nedenle emzirmenin çocuk açısından faydası, çocuğun karşılaşacağı potansiyelrisklere karşı değerlendirilmelidir. Üreme yeteneği/FertiliteDopamin D2 reseptörlerini antagonize eden diğer ilaçlarda olduğu gibi, risperidon prolaktin düzeyini yükseltir. Hiperprolaktinemi, hipotalamik GnRH'ı baskılayabilir ve pitüitergonadotropin salgısının azalmasına yol açabilir. Bu durum daha sonra, hem kadın hem deerkek hastalarda, gonadal steroidogenezi bozarak, reprodüktif fonksiyonu inhibe edebilir.Klinik dışı çalışmalarda konuya ilişkin etkiler gözlenmemiştir. 4.7. Araç ve makine kullanımı üzerindeki etkilerRİCUS® sinir sistemi ve görme duyusuna ilişkin potansiyel etkileri nedeniyle araç ve makine kullanma becerileri üzerinde minör ya da orta derecede etki gösterir (bkz. Bölüm 4.8). Bunedenle hastaların, bireysel duyarlılıkları anlaşılıncaya kadar, araç ve makine kullanmamalarıönerilir. 4.8. İstenmeyen etkiler(>%10 sıklıkta):Parkinsonizm, En sıkbildirilen advers ilaçreaksiyonları sedasyon/somnolans, baş ağrısı ve insomnia'dır. Aşağıda verilen tüm advers ilaç reaksiyonları klinik çalışmalarda bildirilmiştir. Şu terimler ve sıklık dereceleri kullanılmıştır: Çok yaygın (>1/10); yaygın (>1/100 ila <1/10); yaygın olmayan (>1/1000 ila <1/100); seyrek (>1/10.000 ila <1/1000); çok seyrek (<1/10.000), bilinmiyor (eldeki verilerden hareketletahmin edilemiyor).
Endokrin hastalıklar
Hiperprolaktinemia
Uygunsuz antidiüretik hormon salgılama, idrarda glukoz bulunması Metabolizma ve beslenmehastalıkları
Kilo alımı, iştah artışı, iştahazalması
Diyabetes mellitusb,hiperglisemi,polidipsi, kilokaybı, anoreksi,kan kolesteroldüzeyindeyükselme
Su intoksikasyonuc, hipoglisemi, hiperinsülinemic kan trigliserit düzeyinde yükselme Diyabetik ketoasidoz Psikiyatrik hastalıklar ¦tod
Insomnia'
Uyku bozuklukları, ajitasyon, depresyon, anksiyete Mani, kabus, konfüzyonaldurum, libidoazalması, sinirlilik
Katatoni, uyurgezerlik,uyku ilişkiliyeme problemi,künt afekt,anorgazmi Sinir sistemi hastalıkları
Baş ağrısı, parkinsonizmdsomnolans/sedasyon Akatizid, distonid, diskinezid, tremor,sersemlik
Tardif diskinezi, serebral iskemi,uyaranlara yanıtvermeme, bilinçkaybı, depresifbilinç durumu,konvülsiyond,senkop,psikomotorhiperaktivite,denge bozukluğu,anormalkoordinasyon,postural sersemlik, dikkat bozukluğu,disartri, disguzi,hipoestezi,parestezi
Nöroleptik malign sendrom,serebrovaskülerolay, diyabetikkoma, baştatitreme
a Hiperprolaktinemi bazı olgularda jinekomasti, menstrüel bozukluklar, amenore, anovülasyon, galaktore, fertilite bozuklukları, libido kaybı ve erektil disfonksiyona yol açabilir.bPlasebo kontrollü araştırmalarda, diabetes mellitus, risperidon tedavisindeki hastalarda %0,18 oranında, plasebo grubunda ise %0,11 oranında bildirilmiştir. Tüm klinik araştırmalardakigenel insidansı risperidon tedavisi gören tüm hastalarda %0,43 olmuştur. cRisperidon klinik çalışmalarında gözlenmemiş, ama risperidon ile pazarlama sonrası dönemde gözlenmiştir. d Ekstrapiramidal bozukluk ortaya çıkabilir: Parkinsonizm (tükürük salgısında artış, kas-iskelet katılığı, parkinsonizm, ağızda sulanma, dişli çark belirtisi, bradikinezi, hipokinezi, maske yüz,kaslarda gerginlik, akinezi, ense sertliği, kaslarda sertlik, parkinsoniyen adım, anormalglabella refleksi, parkinsoniyen dinlenme tremoru), akatizi (akatizi, huzursuzluk, hiperkinezive huzursuz bacak sendromu), tremor, diskinezi (diskinezi, kaslarda seğirme, koreatetozis,atetozis ve miyoklonus), distonie, DistfiSiışüSlastzikftpsLamsktadır; distoni, hipertoni, tortikollis,Belge Dcigtemsfzdkas'kasilffiâiafirfiaâ'^ksgıi^^^Kfefarospazmf©kui'ögipasyoffi:d^d^3e°paraffzi,,t^fssyal spazm, laringospazm, miyotoni, opistotonus, orofaringeal spazm, plörototonus, dilde spazm ve trismus. Mutlaka ekstrapiramidal orijine sahip olması gerekmeyen, daha geniş bir semptomspektrumunun verildiğine dikkat edilmelidir. İnsomnia şunları içerir; uykuyu başlatma,sürdürme güçlüğü. Grand-mal konvülsiyonu içeren konvülsiyon. Menstrüel bozukluk şunlarıiçerir; düzensiz menstrüasyon, oligomenore. Ödem şunları içerir; yaygın ödem, periferiködem, gode bırakan ödem. Paliperidon formülasyonlarıyla kaydedilen istenmeyen etkiler Paliperidon, risperidonun aktif metabolitidir. Bu nedenle, bu bileşenlerin advers reaksiyon profilleri (hem oral hem de enjektabl formülasyonlar dahil) birbirleri için geçerlidir. Yukarıdaki advers reaksiyonlara ek olarak, paliperidon ürünleriyle aşağıdaki advers reaksiyon kaydedilmiştir ve risperidon ile de meydana gelmesi beklenebilir: Kardiyak bozukluklar: Postüral ortostatik taşikardi sendromu Sınıf etkileri Diğer antipsikotiklerde olduğu gibi, risperidon ile pazarlama sonrası dönemde çok ender olarak QT uzaması olguları bildirilmiştir. QT aralığını uzatan antipsikotikler ile bildirilensınıfla ilişkili diğer kardiyak etkiler arasında ventriküler aritmi, ventriküler fibrilasyon,ventriküler taşikardi, ani ölüm, kardiyak arrest ve Torsades de Pointes bulunmaktadır. Venöz tromboembolizm Antipsikotik ilaçlarla venöz tromboembolizm olguları (pulmoner embolizm dahil) ve derin ven trombozu olguları bildirilmiştir (sıklık bilinmemektedir). Kilo alma Vücut ağırlığının > %7'si oranında kilo alma kriterini karşılayan risperidon ve plasebo ile tedavi edilen yetişkin şizofreni hastalarının oranları, 6 ila 8 haftalık bir havuzda plasebokontrollü çalışmalarda karşılaştırılmıştır ve plaseboya (%9) nazaran risperidon (%18) ile kiloalma insidansının istatistiksel olarak anlamlı ölçüde daha fazla olduğu görülmüştür. Akutmani hastası yetişkinlerde plasebo kontrollü 3 haftalık havuzda, son noktada kiloda >%7oranında artış insidansı risperidon (%2,5) ve plasebo (%2,4) gruplarında karşılaştırılmış veaktif kontrol grubunda (%3,5) biraz daha yüksek olduğu görülmüştür. Davranış ve diğer rahatsız edici davranış bozuklukları olan çocuk ve adolesan popülasyonunda yapılan uzun süreli çalışmalarda, kilo, 12 aylık tedaviden sonra ortalama 7,3kg artmıştır. 5-12 yaş arasındaki normal çocuklarda beklenen kilo alma oranı yılda 3 ila 5kg'dır. 12-16 yaşındaki hasta>feFda,'''©rkekfer kyıMae yaklaşıkır5 kg alırken bu durum kızlarda
yılda 3 ila 5 kg'da kalmıştır. Özel popülasyonlara ilişkin ek bilgilerYetişkin hastalara oranla demanslı yaşlı hastalarda veya pediyatrik hastalarda daha yüksek insidansın rapor edildiği advers ilaç reaksiyonları (AİR) aşağıda açıklanmaktadır: Demans hastalığına sahip yaşlılarda Demanslı yaşlı hastalarda yapılan klinik çalışmalarda geçici iskemik atak ve serebrovasküler olay sırasıyla %1,4 ve %1,5 sıklığa sahip AİR'ler olarak bildirilmiştir. Ayrıca, aşağıdakiAİR'lerin demanslı yaşlı hastalarda > %5 sıklığında olduğu ve diğer yetişkin popülasyondagörülen sıklığın en az iki katı olduğu bildirilmiştir: idrar yolu enfeksiyonu, periferal ödem,letarji ve öksürük. Pediyatrik hastalar Genel olarak çocuklarda gözlenen advers reaksiyon tiplerinin yetişkinlerde gözlenen ile benzer olması beklenir. Aşağıdaki AİR'lerin, pediyatrik hastalarda (5 ila 17 yaş) > %5 sıklığındaolduğu ve yetişkinlerde yapılan klinik çalışmalarda görülen sıklığın en az iki katı olduğubildirilmiştir: uyku basması/sedasyon, halsizlik, baş ağrısı, iştah artışı, kusma, üst solunumyolları enfeksiyonu, burun tıkanıklığı, karın ağrısı, baş dönmesi, öksürük, ateş, titreme, ishalve enürezis. Çocuklarda, cinsel gelişim ve boy üzerinde risperidonun uzun süreli etkileri yeterince araştırılmamıştır (bkz. Bölüm 4.4). Şüpheli advers reaksiyonların raporlanmasıRuhsatlandırma sonrası şüpheli ilaç advers reaksiyonlarının raporlanması büyük önem taşımaktadır. Raporlama yapılması, ilacın yarar/risk dengesinin sürekli olarak izlenmesineolanak sağlar. Sağlık mesleği mensuplarının herhangi bir şüpheli advers reaksiyonu TürkiyeFarmakovijilans Merkezi (TÜFAM)'ne bildirmeleri gerekmektedir (www.titck.gov.tr[email protected]. Doz aşımı ve tedavisiSemptomlar Genellikle, bildirilen işaret ve semptomlar ilacın bilinen farmakolojik etkilerinin artması şeklindedir. Doz aşımı semptomları, uyuşukluk ile sedasyon, taşikardi ile hipotansiyon veekstrapiramidal semptomlardır. Doz aşımı halinde QT-uzaması ve konvülsiyonlarbildirilmiştir. Oral risperidon ve paroksetinin birlikte kullanımındaki doz aşımı ile ilişkiliolarak Torsades de Pointes bildirilmiştir.
Akut doz aşımı durumlarında birden fazla ilaç ihtimali düşünülmelidir. Tedavi Solunum yolu açılmalı ve açık tutulmalı, yeterli oksijenasyon ve ventilasyon sağlanmalıdır. Gastrik lavaj (hastanın bilinci kapalı ise, entübasyondan sonra), aktif kömür ve birlikte birlaksatif uygulanması ilaç alındıktan sonra bir saatten az bir zaman dilimi içindedüşünülmelidir. Kardiyovasküler izleme hemen başlatılmalı ve sürekli elektrokardiyografikizleme ile muhtemel aritmiler takip edilmelidir. RİCUS®'a özgü bir antidot yoktur. Bu nedenle uygun destekleyici önlemler alınmalıdır. Hipotansiyon ve dolaşım kollapsı intravenöz sıvı ve/veya sempatomimetik ajanlar gibi uygunönlemlerle tedavi edilmelidir. Şiddetli ekstrapiramidal semptomlarda antikolinerjik tedaviuygulanmalıdır. Hasta durumu düzelinceye kadar yakın tıbbi gözlem altında tutulmalı veizlenmelidir. 5. FARMAKOLOJİK ÖZELLİKLER5.1. Farmakodinamik özelliklerFarmakoterapötik grup: Diğer antipsikotikler ATC kodu: N05AX08 Etki mekanizması: Risperidon, kendine özgü özellikleri olan selektif bir monoaminerjik antagonisttir. Serotoninerjik 5-HT2 ve dopaminerjik D2 reseptörlerine yüksek afiniteyle bağlanır. Alfa1-adrenerjik reseptörlere, daha düşük afiniteyle H1-histaminerjik ve alfa2-adrenerjik reseptörlerede bağlanır. Risperidonun kolinerjik reseptörlere afinitesi yoktur. Risperidon, güçlü birdopamin D2 reseptörü antagonisti olarak, şizofrenideki pozitif semptomları düzelttiği kabuledilirken, klasik nöroleptiklere kıyasla motor aktivitede depresyona ve katalepsi oluşumunadaha az neden olur. Dengeli bir santral serotonin ve dopamin antagonizması, ekstrapiramidalyan etkileri azaltabilir ve tedavinin etkililiğini şizofreninin negatif ve afektif semptomlarınayayabilir.Farmakodinamik etkiler Klinik etkililikŞizofreni Risperidonun kısa dönem şizofreni tedavisindeki etkililiği, şizofreni için DSM-IV kriterlerine uyan 2500'den fazla hastanın katıldığı, 4 ile 8 hafta süreli dört çalışmada belirlenmiştir.Günde iki kez uygulanan risperidon dozunun 10 mg/gün'e kadar titre edildiği 6 haftalık,plasebo kontrollü bir araştPrmadap'KısaeiPsikryatr^'kn®epec©lendirme Ölçeği (BPRS) toplam
skorunda, risperidon plasebodan üstün bulunmuştur. Dört sabit risperidon dozu kullamlan (günde iki kez uygulama ile 2, 6, 10 ve 16 mg/gün), 8 haftalık plasebo kontrollü biraraştırmada dört risperidon grubunun hepsi, Pozitif ve Negatif Sendrom Ölçeği (PANSS)toplam skorunda plasebodan üstün bulunmuştur. Beş sabit risperidon dozu (günde iki kezuygulama ile 1, 4, 8, 12 ve 16 mg/gün) ile yürütülen 8 haftalık bir doz kıyaslamaçalışmasında, 4,8 ve 16 mg/gün risperidon doz grupları PANSS toplam skorunda 1 mgrisperidon doz grubundan üstün bulunmuştur. İki sabit risperidon dozunun kullanıldığı (gündebir kez uygulama ile 4 ve 8 mg/gün) 4 hafta süreli, plasebo kontrollü bir doz kıyaslamaçalışmasında her iki risperidon doz grubu, toplam PANSS skoru ve bir yanıt ölçümünü de(PANSS toplam skorunda >%20 azalma) kapsayan çeşitli PANSS ölçümlerinde plasebodanüstün bulunmuştur. Daha uzun süreli bir araştırmada, ağırlıklı olarak şizofreni için DSM-IVkriterlerini karşılayan ve bir antipsikotik ilaç ile en az 4 hafta süreyle klinik olarak stabilkalmış, ayakta tedavi gören yetişkin hastalar, 2 ile 8 mg/gün risperidon ya da haloperidolerandomize edildi ve 1 ile 2 yıl boyunca nüks için gözlem yapıldı. Risperidon almakta olanhastalarda bu süre içinde nüks zamanı, haloperidol almakta olanlara kıyasla anlamlı ölçüdedaha uzun oldu. Bipolar bozuklukta manik epizotlar Bipolar I bozukluğa bağlı manik epizotların akut tedavisinde risperidon monoterapisinin etkililiği üç çift-kör plasebo kontrollü monoterapi çalışmasında, DSM-IV kriterleri temelindebipolar I bozukluğu olan yaklaşık 820 hasta üzerinde ortaya konulmuştur. Bu üç çalışmada, 1ile 6 mg/gün dozunda risperidonun (başlangıç dozu iki çalışmada 3 mg ve bir çalışmada 2mg), önceden tanımlanmış birincil sonlanım noktasında (Young Mani Derecelendirme Ölçeği(YMRS) toplam skorunda 3. haftada başlangıç dönemine göre değişim), plasebodan anlamlıölçüde üstün olduğu gösterilmiştir. İkincil etkililik sonlanımları da genel olarak birincilsonlanım ile uyumlu olmuştur. Toplam YMRS skorunda başlangıç döneminden 3 haftalıksonlanım noktasına kadar >%50 azalma gösteren hastaların yüzdesi, risperidon içinplasebodan anlamlı olarak daha yüksekti. Bu üç çalışmanın bir tanesinde, bir haloperidol koluve 9 haftalık bir çift-kör idame dönemi de bulunmaktaydı. Etkililik, 9 haftalık idame tedavisidönemi boyunca kalıcı oldu. Toplam YMRS skorunda başlangıca göre olan değişim, süreklibir düzelme gösterdi ve 12. haftada risperidon ve haloperidol arasında benzer nitelikteydi. Akut mani tedavisinde duygudurum stabilize edici ajanlara eklenen risperidonun etkililiği, bipolar I bozukluk için DSM-IV kriterlerine uyan yaklaşık 300 hastanın yer aldığı 3 haftalıkçift-kör iki çalışmanın birinde gösterildi. Bu 3 haftalık çalışmalardan birinde, lityum ya davalproat üzerine eklenen, 2 mg/gün ile başlanan 1 ile 6 mg/gün dozlarındaki risperidon,önceden tanımlanmış birincil sonlanım noktasında (YMRS toplam skorunda 3. haftadabaşlangıç dönemine göre değişim), tek başına lityum ya da valproata kıyasla üstündü. İkincibir 3 haftalık çalışmada, l^/üte, gvaför#atoveywakarbateaHepin ile kombinasyon şeklinde, 2
mg/gün ile başlanan 1 ile 6 mg/gün dozlarındaki risperidon, YMRS toplam skorunun azaltılmasında tek başına lityum, valproat veya karbamazepinden üstün bulunmadı. Buçalışmadaki başarısızlık için olası bir açıklama, risperidon ve 9-hidroksi-risperidonklerensinin karbamazepin tarafından indüklenmesi, böylelikle risperidon ve 9-hidroksi-risperidonun subterapötik düzeylere inmesiyle sonuçlanmasıdır. Yapılan bir post-hoc analizdekarbamazepin grubu analiz dışında tutulduğunda lityum ya da valproat ile kombine edilenrisperidon, YMRS toplam skorunun azaltılmasında tek başına lityum veya valproattan üstünbulunmuştur. Demansta Devam Eden Saldırganlık Risperidonun, saldırganlık, ajitasyon, psikoz, aktivite gibi davranışsal bozukluklar ve afektif bozukluklar içeren Davranışsal ve Psikolojik Demans Semptomları (BPSD) tedavisindekietkililiği, çift-kör, plasebo kontrollü üç çalışma kapsamında, orta dereceli ile şiddetli demansıolan 1150 yaşlı hasta üzerinde ortaya konulmuştur. Çalışmalardan biri, 0,5, 1 ve 2 mg/gün'lüksabit risperidon dozlarını içermekteydi. İki esnek doz çalışmasında sırasıyla 0,5 ile 4 mg/günve 0,5 ile 2 mg/gün aralıklarındaki risperidon doz grupları kullanılmıştır. Risperidon yaşlıdemans hastalarında saldırganlığın tedavisinde, istatistiksel olarak anlamlı ve klinik olarakönemli bir etkililik ve ajitasyon ve psikozun tedavisinde biraz daha az kalıcı nitelikte etkililikgösterdi (Alzheimer Hastalığında Davranışsal Patoloji Derecelendirme Ölçeği (BEHAVE-AD] ve Cohen-Mansfield Ajitasyon Envanteri [CMAI] yoluyla ölçüldüğü şekilde).Risperidonun tedavi etkisi, Mini-Mental Durum Muayenesi (MMSE) skorundan (ve bununsonucu olarak demans şiddetinden); risperidonun sedatif özelliklerinden; psikoz bulunupbulunmamasından ve demans tipinden (Alzheimer demansı, vasküler ya da mikst demans)bağımsızdı. (Aynı zamanda bkz. bölüm 4.4). Pediyatrik popülasyon Tavır/davranış bozukluğu Yıkıcı davranışların kısa dönem tedavisinde risperidonun etkililiği, çift-kör, plasebo kontrollü iki çalışmada, DSM-IV temelinde yıkıcı davranış bozuklukları (DBD) ve sınırda entelektüelişlev veya hafif ile orta dereceli mental retardasyon/öğrenme bozukluğu tanısı almış, 5 ile 12yaşlarında yaklaşık 240 hasta üzerinde ortaya konulmuştur. Bu iki çalışmada risperidon 0,02ile 0,06 mg/kg/gün, önceden tanımlanmış birincil sonlanım noktası olan, Nisonger-ÇocukDavranışları Derecelendirme Formu (N-CBRF)'nun Tavır/Davranış Sorunları alt-ölçeğinde 6.haftada başlangıç dönemine göre değişim üzerinde plasebodan anlamlı ölçüde üstünbulunmuştur. 5.2. Farmakokinetik özelliklerGenel ÖzelliklerBelge DoRisperidon farmakolojik afttiviit!esli''iiispieiFid 0bazbferizeyeffi#-hidroksi-risperidona metabolizeiğralama Kodu: lZW56aklUZm}AZmxXS3k0SHY3ZW56SHY3 Belge Takip Adresi:https://www.turkive.gov.tr/saglik-titck-ebvsolur. Emilim:Oral uygulamadan sonra risperidon tam olarak absorbe edilir ve en yüksek plazma düzeyine 1-2 saat içinde ulaşılır. Risperidonun oral mutlak biyoyararlanımı %70 (CV= %25)'tir.Risperidonun oral relatif biyoyararlanımı tablet için çözeltiye kıyasla %94 (CV= %10)'tür.Risperidonun absorpsiyonu besinlerden etkilenmez, bu nedenle risperidon besinlerle birlikteya da ayrı olarak alınabilir. Risperidon kararlı durum plazma konsantrasyonuna hastalarınçoğunda 1 günde ulaşır. 9-hidroksi-risperidon kararlı durum plazma konsantrasyonunauygulamanın 4-5'inci günlerinde ulaşır. Dağılım:Risperidon hızla dağılır. Dağılım hacmi yaklaşık 1-2 l/kg'dır. Risperidon plazmada albümin ve alfa 1-asit glikoproteine bağlanır. Risperidonun proteinlere bağlanma oranı %90, 9-hidroksi-risperidonun ise %77'dir.Biyotransformasyon:Risperidon, CYP2D6 aracılığı ile farmakolojik aktivitesi risperidona benzeyen 9-hidroksi-risperidona metabolize olur. Risperidon ve 9-hidroksi-risperidon birlikte aktif antipsikotik fraksiyonu oluşturur. CYP2D6 genetik polimorfizm göstermektedir. Yaygın CYP2D6metabolize ediciler risperidonu hızla 9-hidroksi-risperidona dönüştürürken, zayıf CYP2D6metabolize edicilerde bu dönüşüm çok daha yavaş gerçekleşir. Yaygın metabolize ediciler,zayıf CYP2D6 metabolize edicilere kıyasla daha düşük risperidon ve daha yüksek 9-hidroksi-risperidon konsantrasyonlarına sahip olmakla birlikte, risperidon ve 9-hidroksi-risperidonkombinasyonunun (yani, aktif antipsikotik fraksiyon) farmakokinetiği, tek ve çoklu dozlardansonra, yaygın ve zayıf CYP2D6 metabolize edicilerde benzer niteliktedir. Risperidonun başka bir metabolik yolağı N-dealkilasyondur. İnsan karaciğer mikrozomlarıyla yapılan in vitroçalışmalarda, klinikteki kullanım konsantrasyonlarındaki risperidonun,sitokrom P450 izoenzimleriyle (CYP 1A2, CYP 2A6, CYP 2C8/9/10, CYP 2D6, CYP 2E1,CYP 3A4 ve CYP 3A5) metabolize edilen ilaçların metabolizmalarını önemli ölçüde inhibeetmediği gösterilmiştir.Eliminasyon:eliminasyon yarılanma ömrü 24gsaatti^! elektronik imza ile imzalanmıştır. Belge Do Kodu: lZW56aklUZmxXZmxXS3k0SHY3ZW56SHY3 Belge Takip Adresi:https://www.turkiye.gov.tr/saglik-titck-ebysUygulamadan bir hafta sonra, dozun %70'i idrar ve %14'ü feçes ile itrah edilir. İdrarla itrah edilen dozun %35-45'ini risperidon ve 9-hidroksi-risperidon oluşturur. Geri kalan kısıminaktif metabolitlerdir. Psikotik hastalarda oral yoldan kullanılan risperidonun eliminasyonyarılanma ömrü yaklaşık 3 saattir. 9-hidroksi-risperidon ve aktif antipsikotik fraksiyonunyon ya du: 1ZW5Doğrusallık/Doğrusal olmayan durum:Risperidonun plazma konsantrasyonları, terapötik doz aralığında dozla orantılıdır. RİCUS® oral çözelti, RİCUS® oral tablet ile biyoeşdeğerdir. Hastalardaki karakteristik özelliklerYaşlılarda:Tek-doz oral risperidonun farmakokinetik çalışmasında, yaşlılarda ortalama olarak %43 daha yüksek aktif antipsikotik fraksiyon plazma konsantrasyonlarında artış ve %38 dahauzun bir yarı ömür ve aktif antipsikotik fraksiyonun klerensinde yaşlılarda %30 azalmagörülmüştür.Pediyatrik hastalarda:Risperidon, 9-hidroksi-risperidon ve aktif antipsikotik fraksiyonun çocuklardaki farmakokinetiği, yetişkinlerdeki ile benzerdir.Böbrek yetmezliğinde:Orta derecede böbrek yetmezliği olan yetişkinlerde aktif fraksiyonun klirensi, sağlıklı genç yetişkinlerinkinin %48'idir. Aktif fraksiyonun yarılanma ömrü gençyetişkinlerde 16,7 saat, orta derecede böbrek yetmezliği olanlarda 24,9 saat (ya da gençyetişkinlerden yaklaşık 1,5 kat daha uzun) ve şiddetli böbrek yetmezliği olanlarda 28,8 saat(genç yetişkinlerden 1,7 kat daha uzun)'dir.Karaciğer yetmezliğinde:Risperidonun plazma düzeyleri karaciğer yetmezliği olan hastalarda normal bulunmuştur, ancak risperidonun plazma ortalama serbest fraksiyonu yaklaşık%37,1 artmıştır. Bu verilere göre orta ve şiddetli karaciğer yetmezliği olan yetişkinlerde,risperidon ve risperidonun aktif fraksiyonunun oral klirensi ve eliminasyon yarı ömrü gençsağlıklı yetişkinlerden anlamlı derecede farklı değildir.Cinsiyet, ırk ve sigara alışkanlığı: B5.3. Klinik öncesi güvenlilik verileriSeksüel olarak immatüre sıçan ve köpeklerde dozlamanın başlatıldığı (sub)kronik toksisite çalışmalarında, erkek ve dişi genital yolu ile meme bezlerinde doza bağlı etkiler gözlenmiştir.Bu etkiler, risperidonun dopamin D 2reseptörünü bloke etmesi sonucu oluşan yüksek serumprolaktin seviyelerine bağlıdır.Aynı zamanda doku kültürü çalışmaları insan meme tümörlerindeki hücre büyümesinin prolaktin ile uyarılabileceğini düşündürmektedir. Risperidon sıçan ve tavşanda teratojenikbulunmamıştır. Risperidon ile yapılan sıçan üreme çalışmalarında, ebeveynlerin çiftleşmedavranışında ve dölün doğum ağırlığı ve sağkalımı üzerinde advers etkiler görülmüştür. Belge Do Kodu: lZW56aklUZmxXZmxXS3kOSH yBZW56SHY3 Belge Takip Adresi:https://www.turkiye.gov.tr«aglik-titck-ebysSıçanlarda risperidona rahim içi maruziyet yetişkinlikte kognitif yetmezlik ile ilişkilendirilmiştir. Gebe hayvanlara uygulandığında diğer dopamin antagonistleri dölünöğrenme ve motor gelişimi üzerinde negatif etkilere neden olmuştur. Juvenil sıçanlarlayapılan bir toksisite çalışmasında artmış yavru mortalitesi ve fiziksel gelişimde bir gecikmegözlenmiştir. Juvenil köpeklerle yapılan 40 haftalık bir çalışmada seksüel olgunlaşmagecikmiştir. Adolesanlarda EAA bazında maksimum insan dozunun 3,6 katı bir dozda (1,5mg/gün) uzun kemik büyümesi etkilenmemiştir; etkiler adolesanlarda EAA bazındamaksimum insan dozunun 15 katı bir dozda gözlenmiştir. Bir dizi testte risperidonun genotoksik olmadığı bulunmuştur. Sıçanlarda ve farelerde risperidona ilişkin oral karsinojenite çalışmalarında hipofiz bezi adenomaları (fare), endokrinpankreas adenomları (sıçan) ve meme bezi adenomlarında (her iki tür) artışlar görülmüştür.Bu tümörler uzamış dopamin D 2In vitroin vivo6. FARMASÖTİK ÖZELLİKLER6.1. Yardımcı maddelerin listesiTartarik asit (E334) Benzoik asit (E210) Sorbitol %70 (E420) Sodyum hidroksit (E524) (pH ayarlayıcı) Saf su 6.2. GeçimsizliklerÇay ile geçimsizlik görülür. 6.3. Raf ömrü24 ay İlk kez açıldıktan sonraki raf ömrü: 3 ay 6.4. Saklamaya yönelik özel tedbirler25°C'nin altındaki oda sıcaklığında saklayınız. Dondurmayınız. 6.5. Ambalajın niteliği ve içeriği100 ml amber cam şişe ile emniyet halkalı beyaz plastik kapak.
100 ml şişe ile birlikte sunulan minimum 0,25 ml, maksimum 3 ml hacimdeki koruyucu kapaklı pipet, miligram ve mililitre cinsinden kalibre edilmiştir. Pipet, 3 ml'ye kadar her 0,25ml'yi gösterecek şekilde işaretlenmiştir. 6.6. Beşeri tıbbi üründen arta kalan maddelerin imhası ve diğer özel önlemlerKullanılmamış olan ürünler ya da atık materyaller Tıbbi Atıkların Kontrolü Yönetmeliği ve Ambalaj ve Ambalaj Atıklarının Kontrolü Yönetmeliğine uygun olarak imha edilmelidir. 7. RUHSAT SAHİBİAd : Biofarma İlaç San. ve Tic. A.Ş. Adres : Akpınar Mah. Osmangazi Cad. No:156 34885 Sancaktepe/İstanbul Telefon : (0216) 398 10 63Faks : (0216) 398 10 20 8. RUHSAT NUMARASI210/34 9. İLK RUHSAT TARİHİ/RUHSAT YENİLEME TARİHİİlk ruhsat tarihi: 04.01.2007 Ruhsat yenileme tarihi: 10. KÜB'ÜN YENİLENME TARİHİ |
İlaç BilgileriRicus 1 Mg/ml Oral ÇözeltiEtken Maddesi: Risperidon Kullanma talimatı ve kısa ürün bilgileri
Google Reklamları
İlgili İlaçlar |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
Ana Sayfa | Hakkımızda | İlaçlar | İlaç Ara | İlaç Firmaları | Gizlilik | Bize Ulaşın
Telif Hakkı 2008-2024 © İlaç Prospektüsü. Tüm Hakları Saklıdır.Uyarı: Sitemizde yayınladığımız ilaç bilgileri ile doktora danışmadan kesinlikle ilaç kullanmayınız!
Aksi halde doğabilecek sağlık sorunlarından ilacprospektusu.com sorumlu tutulamaz.