Çeşitli İlaçlar » Kontrast Medya » X-RAY Kontrast Medya, İyotlu » Nephro Tropic, Water Soluble, Low osmolor X-ray kontrast medya » Ioversol KISA ÜRÜN BİLGİLERİ (KÜB)
1.BEŞERİ TIBBİ ÜRÜNÜN ADI
OPTİRAY 320 steril enjektabl çözelti içeren kullanıma hazır şırınga
2.KALİTATİF VE KANTİTATİF BİLEŞİMİ Etkin madde:
İoversol 678 mg/ml içerir. Bu da 320 mg/ml elementel iyota eşdeğerdir. Yardımcı madde(ler):
Sodyum Kalsiyum Edetat20 mg/100 ml
pH ayarlaması gerektiğinde Sodyum hidroksit içerebilir. Yardımcı maddeler için bkz. 6.1.
3.FARMASÖTİK FORMU
Kullanıma hazır şırıngada, enjeksiyon ya da infüzyon için çözelti
Renksiz ila soluk sarı renkte berrak çözelti.
Ozmolalite: 700 mOsm/kg
Viskozite: 9,9 mPa.s (25°C'de)
Viskozite: 5,8 mPa.s (37°C'de)
4.KLİNİK ÖZELLİKLERİ 4.1 Terapötik endikasyonlar
Optiray 320, serebral, koroner, periferik, viseral ve renal anjiyografide, aortografide, sol ventrikülografide, venografide ve intravenöz ürografide kullanımı endike olan, non-iyonik bir röntgen kontrast maddesidir. Optiray 320'nin, bilgisayarlı baş ve vücut tomografisinde (CT), kullanımı da endikedir.
4.2. Pozoloji ve uygulama şekli
Pozoloji/uygulama sıklığı ve süresi:
Erişkinler: Önerilen dozaj çizelgesi
ProsedürDozajSerebral Anyijografi
-Karotid veya vertebral arter2-12 ml
-Dört damarlı anjiyografi20-50 ml Tek doz gerekirse tekrarlanabilir.
Periferik Anjiyografi10-90 ml Tek doz gerekirse tekrarlanabilir.
Viseral Anjiyografi12-60 ml
-Çölyak arter
Tek doz gerekirse tekrarlanabilir.
Renal Anjiyografi6-15 ml Tek doz gerekirse tekrarlanabilir.
Aortografi10-80 ml Tek doz gerekirse tekrarlanabilir.
Sol ventrikülografi30-50 ml Tek doz gerekirse tekrarlanabilir.
Koroner arteriyografi1-10 ml Tek doz gerekirse tekrarlanabilir.
Maksimum Toplam Doz
200 ml 200 ml
250 ml
250 ml
250 ml
250 ml
250 ml
250 ml
Venografi50-100 ml250 ml
Her bir ekstremite için normal doz 50-100 ml'dir. Bazı durumlarda daha düşük veya
yüksek dozlar gerekebilir. İnceleme sonrasında venöz sistem uygun bir sıvıyla (örn.
serum fizyolojik çözeltisi) ile yıkanmalıdır. Ayrıca ekstremiteleri kontrast maddeden
temizlemek için, masaj yapmak ve bacakları daha yüksek bir seviyede tutmak da faydalı
olur.
İntravenöz Ürografi50-750 ml150 ml
Kötü görüntülemenin beklendiği, örn. yaşlı veya böbrek fonksiyonları azalmış hastalarda, doz 1,5-2 ml/kg vücut ağırlığına yükseltilebilir. İyi bir tanısal sonuç elde etmek için kontrast madde mümkün olduğunca hızlı uygulanmalıdır.
Baş CT50-150 ml150 ml
Vücut CT25-150 ml150 ml
Toplam vücut CT'sinde uygulama oranı, organlara göre değişmektedir. Optiray bolus olarak, kısa süreli infüzyonla veya her ikisinin kombinasyonuyla verilebilir. Bir bolus enjeksiyonunun normal dozu 25-75 ml'dir. Kısa süreli bir infüzyonun normal dozu 50150 ml'dir.
Genel olarak dozaj, hastanın yaşına, ağırlığına, kalp debisine ve genel durumuna ve ayrıca incelenmesi gereken vasküler alana bağlıdır. Dozaj, inceleme teknolojisine, enstrümental ekipmana ve seçilmiş iyot konsantrasyonuna da bağlıdır.
İntravasküler uygulanan iyotlu kontrast maddelerin enjeksiyondan önce ısıtılarak vücut sıcaklığına getirilmesi önerilir. Bütün radyopak kontrast ajanlarda olduğu gibi, yeterli görselleştirmeyi sağlayan muhtemel en düşük doz kullanılmalıdır. Özel popülasyonlara ilişkin ek bilgiler: Böbrek/Karaciğer yetmezliği:
Şiddetli böbrek fonksiyon bozukluğu olan ya da kombine böbrek ve karaciğer hastalığı olan hastalarda dikkatli olunmalıdır (bakınız bölüm 4.4). Pediyatrik popülasyon:
Optiray 320'nin çocuklarda güvenlik ve etkinliği henüz bilinmemektedir. Bu nedenle bu tıbbi ürün, daha fazla veri elde edilene kadar çocuklarda kullanılmamalıdır. Serebral, periferik ve viseral anjiyografi ve intravenöz ürografide, çocuklarda Optiray 300 kullanılabilir. Geriyatrik popülasyon:
Dozaj erişkinlerdeki gibidir. Kötü görüntüleme beklenen durumlarda dozaj maksimuma çıkarılabilir.
4.3.Kontrendikasyonlar:
İyot içeren kontrast maddeye karşı kanıtlanmış aşırı duyarlılık. Belirgin hipertiroidizm.
4.4.Özel kullanım uyarıları ve önlemleri
Ciddi bir advers reaksiyon oluşma olasılığı daima göz önünde bulundurulmalıdır. İyotlu kontrast maddeler intratekal kullanımda endike olmadıkları halde istenmeyen intratekal ( spinal kort içi ) uygulanması nedeniyle ciddi advers reaksiyonlar bildirilmiştir. Bu ciddi advers reaksiyonlar; ölüm, konvülsiyonlar, serebral hemoraji, koma, paralizler, araknoidit, akut böbrek yetmezliği, kardiyak arrest, kriz, rabdomiyaliz, hipertermi ve beyin ödemini içerir. Bu ürünün intratekal olarak uygulanmadığından emin olmak için özellikle dikkatli olunmalıdır. Diğer tüm röntgen kontrast maddelerinde olduğu gibi, Optiray anafilaksiye veya bulantı, kusma, dispne, eritem, ürtiker ve hipotansiyon gibi diğer anafilaktoid intolerans belirtilerine neden olabilir. Önceden iyotlu röntgen kontrast maddelerine karşı reaksiyon öyküsü, bilinen başka allerjiler, ( örn.bronşiyal astım, yüksek ateş ve yiyecek allerjileri ) veya aşırı duyarlı olduğu bilinen hastalarda risk yüksektir (Bakınız bölüm 4.3). Herhangi bir allerji veya aşırı duyarlılık öyküsü bulunan hastalarda, faydanın riskten çok daha fazla olması koşulu aranmalıdır. Ön testler yapılarak şiddetli reaksiyonların öngörülebilmesi mümkün değildir. Bir hastanın tıbbi öyküsünün bütünüyle değerlendirilmesi, potansiyel advers reaksiyonların öngörülmesi açısından daha doğru olacaktır. Pozitif allerji öyküsü kontrendikasyon değildir, ama dikkat edilmesini gerektirir. Uygun resüsitasyon önlemleri derhal alınabilmelidir. Allerjik reaksiyonları önlemek veya en aza indirmek için antihistaminikler ve kortikosteroidlerle pre-medikasyon tedavisi yapılabilir. Ancak bu pre-medikasyon tedavisi, şiddetli advers olayların ortaya çıkmasını her zaman engellemez. İyotlu intravasküler kontrast ajanların kullanıldığı diyagnostik prosedürler, uygulanacak özel prosedürde yetenekli ve deneyimli personel tarafından yapılmalıdır. İyotlu röntgen kontrast maddesinin uygulanması ile ilişkili ciddi veya fatal reaksiyonlar görülmüştür. Tam teçhizatlı acil arabası veya dengi malzeme ve teçhizat, ve her tür advers reaksiyonu tanıyacak ve müdahale edebilecek nitelikte personel daima hazır bulundurulmalıdır. Hasta, son enjeksiyondan sonra en az 15 dakika boyunca yakın gözlem altında tutulmalıdır, çünkü şiddetli reaksiyonların çoğu bu sırada ortaya çıkmaktadır.
Ciddi gecikmiş reaksiyon oluşabildiği bilindiğinden, acil yardım ve deneyimli personel en az 30 dakikadan 60 dakikaya kadar hastanın yanında bulundurulmalıdır, hasta enjeksiyondan sonra bir saat boyunca hastane ortamında ( mutlaka radyoloji / kardiyoloji ortamı olması gerekmez ) kalmalı ve herhangi bir semptom geliştiği takdirde radyoloji bölümüne dönmelidir.
Konjestif kalp yetmezliği olan hastalar, dolaşan ozmotik yükteki geçici bir artışla ilişkili olabilecek gecikmiş hemodinamik bozuklukları saptayabilmek için, prosedürden sonra birkaç saat boyunca gözlem altında tutulmalıdır. Allerjik reaksiyonların, uygulamayı izleyen birkaç gün içinde gelişebileceği ve böyle bir durumda derhal doktora başvurulması gerektiği konusunda hasta bilgilendirilmelidir. Şiddetli böbrek fonksiyon bozukluğu, kombine renal ve hepatik hastalık, multipl miyelom ya da diğer paraproteinemi, anürisi olan hastalarda, özellikle yüksek dozlar uygulandığında dikkatli olunmalıdır. Her ne kadar böbrek hasarının nedeni dehidrasyon ya da kontrast madde olarak ayrı ayrı kanıtlanmasa da ikisinin kombinasyonunun bu hasara neden olabileceği düşünülmüştür. Böbrek fonksiyon bozukluğu olan hastalardaki bu risk, uygulama için bir kontrendikasyon değildir. Bununla birlikte normal hidrasyon düzenlenmesi ve yakından izlemeyi içeren özel uyarılara gerek vardır. Enjeksiyon öncesi hazırlık sırasında hastalara uygulanan kısmi dehidratasyon zararlı olabilir ve özellikle miyeloma hastalarında önerilmez, çünkü bu hastalarda miyelom proteinlerinin çökmesine neden olan bir yatkınlık oluşturabilir. Optiray'ın kandan atılması için diyaliz uygulanabilir.
Homozigotik orak hücre hastalığı olan hastalarda, röntgen kontrast maddesi gibi hiperozmolar ajanlar eritrositlerin oraklaşmasını etkileyebilirler. Bu nedenle bu tür ajanların homozigotik orak hücre hastalığı olan hastalara intra-arteriyel uygulanmasından önce dikkatli bir değerlendirme yapılmalıdır. İyot içerikli kontrast madde, latent hipertiroidizmi ya da tiroid bezinde otonom alanları olan hastalarda da zararlı olabilir. Feokromositoma hastalarında, hipertansif kriz riski nedeniyle kontrast maddenin intravasküler uygulandığı durumlarda, önceden a-blokör verilmesi önerilir.
Serebral arterlere veya spinal kordu besleyen damarlara doğrudan enjeksiyon sonrasında, ya da kardiyak kateterizasyon sonrasında karotidlerin istenmeyen dolumu nedeniyle, ciddi nörolojik sekeller oluşabilir. Kontrast maddeye karşı neden-etki ilişkisi kurulmamıştır, çünkü hastanın önceki durumu ve prosedür teknikleri de, kendi içlerinde nedensel faktörlerdir.
Bazı hastalarda genel anestezi endike olabilir. Ancak muhtemelen anesteziklerin hipotansif etkileri nedeniyle, bu hastalarda advers reaksiyonların sıklığının daha yüksek olduğu görülmüştür.
Anjiyografi prosedürlerinde, kateter manipülasyonu ve kontrast madde enjeksiyonu sırasında plağı yerinden oynatma veya damara zarar verme ya da damar duvarını delme olasılıklarına dikkat edilmelidir. Kateterin doğru yerleştirilmesi için test enjeksiyonlarının yapılması tavsiye edilir.
Non-iyonik röntgen kontrast maddesinin antikoagülan etkisinin, benzer konsantrasyonlarda konvansiyonel iyonik ajanlara göre daha az olduğu in vitro kanıtlanmıştır. Non-iyonik kontrast maddenin şırıngada kanla uzun süreli temasında pıhtılaşma görülmüştür. Bu nedenle standart anjiografik kateterlerin sıklıkla yıkanması ve şırınga ya da kateter içinde bulunan kontrast maddenin kanla uzun süre temasının engellenmesi önerilir.
Bazı olgularda, hem iyonik hem de non-iyonik röntgen kontrast maddelerle arteriyografi sırasında, miyokart infarktüsü veya inmeye yol açan şiddetli ve fatal tromboembolizm görülmüştür. Bu yüzden özellikle anjiyografi prosedürlerinde tromboembolitik olayları minimize etmek için, çok dikkatli bir damar içi enjeksiyon tekniği uygulanması gereklidir. Hastanın altta yatan hastalıkları, incelemenin süresi, kateter ve şırınganın materyali ve eşlik eden ilaçlar, tromboembolizmin gelişmesine katkıda bulunabilirler. Bu nedenle rehber kablo ve kateterlerin doğru kullanımı, üçlü valf kullanımı, kateterin heparinize salinle sık sık yıkanması ve incelemenin vaktinde bitirilmesi gibi önlemleri kapsayan çok dikkatlibir inceleme yapılması önerilir. Cam şırıngaların yerine plastik şırıngaların kullanımı, pıhtılaşma olasılığını in vitro azaltmıştır.
İleri aterosklerozu, ağır hipertansiyonu, kardiyak dekompansasyonu, senilitesi, öncesinde serebral trombozu veya embolizmi olan hastalarda özellikle dikkatli olunmalıdır. Bradikardi ve kan basıncının yükselmesi veya düşmesi gibi kardiyovasküler reaksiyonlar bu hastalarda daha sık görülebilir.
Homosistinürili hastalarda, artan tromboz ve embolizm riski nedeniyle mümkün olduğu kadar anjiyografiden kaçınılmalıdır.
Optiray perivasküler uygulamayı önlemek için dikkatle enjekte edilmelidir. Ancak özellikle power enjektörlerin kullanımı sırasında Optiray'da önemli bir ekstravazasyon görülebilir.
Genellikle konservatif tedaviye ihtiyaç duyulacak önemli bir doku hasarı olmadan tolere edilir ancak özellikle elin dorsumu içine ektravazasyon sonrası cerrahi müdahale gerektiren ciddi doku hasarının (ülserasyon) olduğu bazı olgular bildirilmiştir.
İşlemsel risk açısından, selektif koroner arteriografi yalnızca beklenen yararın işleme bağlı risklerle kıyaslandığında çok yüksek olduğu hastalarda uygulanmalıdır. Kronik pulmoner amfizem hastalarında da anjiyokardiografinin taşıdığı risk, işlemin gerekliliğiyle dikkatle kıyaslanmalıdır.
Yalnızca spesifik endikasyonlara yönelik özel uyarı ve önlemler şöyledir: Venografi
Flebit şüphesi, ağır iskemi, lokal enfeksiyonlar veya venöz sisteminde komple oklüzyon olan hastalarda özellikle dikkatli olunmalıdır. Enjeksiyon sırasında ekstravazasyon oluşumunu engellemek için bir röntgen floroskopisi önerilir. Periferik anjiyografi
Röntgen kontrast maddesinin enjekte edileceği arterde puls olmalıdır. Tromboangiitis obliterans veya ağır iskemiyle kombine artan enfeksiyonları olan hastalarda, anjiyografi özel bir dikkatle uygulanmalı, mümkünse hiç yapılmamalıdır. Koroner arteriyografi ve sol ventrikülografi
Bu prosedürlerde kardiyak dekompansasyon, ciddi aritmiler, iskemi ve miyokart
infarktüsü görülebilir.
Sodyum
Bu tıbbi ürün her dozunda 1 mmol (23 mg)'dan daha az sodyum ihtiva eder; yani esasında "sodyum içermez".
4.5. Diğer tıbbi ürünlerle etkileşim ve diğer etkileşim şekilleri
Diğer iyotlu kontrast maddelerin uygulanmasından sonra aşağıdaki etkileşimler görülmüştür. Bunlar genellikle ilgili kontrast madde sınıfına özel etkileşimlerdir. - İyotlu kontrast maddenin parenteral uygulandığı bir röntgen incelemesi sırasında, metformin alan hastalarda laktik asidozla ilişkili akut böbrek yetmezliği görülmüştür. Bu nedenle metformin alan diyabetik hastalarda, serum kreatinin normalse, inceleme yapılmalı ve inceleme yapıldığı andan itibaren metformin alımı durdurulmalıdır.
Metformin 48 saat boyunca hastaya verilmemeli, ancak böbrek fonksiyonu/serum kreatinin normal aralıkta kalacak olursa metformin uygulamasına tekrar başlanmalıdır. Serum kreatinini artmış hastalarda iyotlu kontrast maddenin kullanılmadığı alternatif bir görüntüleme metodu değerlendirilmelidir; şayet röntgen incelemesi yapılmak zorunda ise metformin ile ilgili yukarıda açıklanan prosedüre uyulmalı ve incelemeden en az 24 saat önce nefrotoksik ilaçlar, mannitol ve kıvrım diüretiklerinin alımı durdurulmalıdır.
Karaciğer disfonksiyonu olan ve oral kolesistografik ajanları takiben intravasküler kontrast maddesi verilmiş birkaç hastada renal toksisite kaydedilmiştir. Bu nedenle yakın zamanda kolesistografik bir kontrast ajan almış hastalarda, intravasküler röntgen kontrast ajanı uygulamaları ertelenmelidir.
Literatürde interlökin ile tedavi edilen hastalarda, kontrast ajanın uygulanmasından sonra, advers reaksiyonların oranının daha yüksek olabileceği belirtilmektedir. Bunun nedeni henüz anlaşılamamıştır. İnterlökin uygulamasından sonra 2 haftalık bir periyot içinde bu reaksiyonlar artarak veya gecikerek ortaya çıkmıştır.
Bir röntgen kontrast maddesinin arteriyel enjeksiyonu asla vazopressör uygulandıktan sonra yapılmamalıdır, yoksa nörolojik etkileri güçlü bir şekilde artırırlar.
İyotlu röntgen kontrast maddesi, tiroid bezinin iyot alım kapasitesini azaltabilir. Bu nedenle iyot tahminlerine dayanan PBI (proteine bağlı iyot) ve radyoaktif iyot alımı çalışmalarının sonuçları, iyotlu röntgen kontrast maddesinin uygulanmasını takip eden 16 gün içinde tiroid fonksiyonunu doğru yansıtmaz. Ancak T3 resin alımı ve total veya serbest tiroksin (T4) tayinleri gibi iyot tahminlerine dayanmayan tiroid fonksiyon testleri bu durumdan etkilenmez. Fenotiazinler, trisiklik antidepresanlar, MAO-inhibitörleri, analeptikler ve nöroleptikler gibi spazm eşiğini düşüren ilaçlar, bilhassa epilepsi veya fokal beyin kayıpları olan hastalarda konvülsiyona yol açabilir. Bu nedenle tıbbi açıdan uygun görülürse, bu ilaçların kullanımı serebral anjiyografiden 48 saat öncesinden itibaren ve 24 saat sonrasına kadar bırakılmalıdır.
4.6.Gebelik ve laktasyon Genel tavsiye
Gebelik Kategorisi: B
Çocuk doğurma potansiyeline sahip kadınlar/Doğum kontrolü
Uygulanabilir değildir (Bakınız Gebelik dönemi). Gebelik dönemi
Optiray için, ilaca maruz kalmış gebelerde hiçbir klinik çalışma mevcut değildir. Hayvan çalışmaları; gebelik, embriyonal/fetal gelişim, doğum ya da doğum sonrası gelişimle ilgili olarak direkt ya da dolaylı zararlı etki göstermemiştir. Bu nedenle gebelikte reçete edilirken dikkatli olunmalıdır. Ancak gebelik sırasında yapılan herhangi bir röntgen incelemesi potansiyel bir risk taşıyabileceğinden, risk/fayda oranı dikkatle tartılmalıdır. Eğer daha iyi ve daha güvenli bir alternatif varsa, kontrast maddeli röntgen incelemesinden kaçınılmalıdır. Standart test modellerinde mutajen etkiler gözlenmemiştir.
Laktasyon dönemi
İoversol'ün insan anne sütüyle atılıp atılmadığı bilinmemektedir. Ancak pek çok enjektabl kontrast ajan, anne sütünden yaklaşık %1 oranında değişmeden atılmaktadır. Emzirilen bebeklerde istenmeyen etkiler görüldüğü kanıtlanmamış olsa da, potansiyel advers etkiler nedeniyle emziren kadınlara intravasküler röntgen kontrast madde uygulanırken dikkatli olunmalı, gerekirse emzirmeye bir gün ara verilmelidir. Üreme yeteneği (fertilite)
Klinik olmayan araştırmalardan alınan veriler, tavşan ve sıçanlarda, ioversolün fertilite üzerine negatif bir etkisi olmadığını kanıtlamıştır.
4.7.Araç ve makine kullanımı üzerindeki etkiler
Araç sürme ve makine kullanma üzerinde bilinen bir etkisi yoktur. Ancak erken reaksiyonların ortaya çıkma riski nedeniyle, enjeksiyonu izleyen bir saat içinde araç veya makine kullanılması önerilmemektedir.
4.8.İstenmeyen etkiler
Yan etkiler, kontrollü gözlemlere (ilaç izleme) göre tedavi edilen hastaların % 1,1'inde hafif veya orta dereceli olarak meydana gelmiştir. Ciddi veya yaşamı tehdit
eden yan etkiler ve ölümler, çoğunlukla kadiyovasküer orijinli olarak meydana gelmektedir.
Durumu ağırlaştıran ana faktör olarak kardiyovasküler bozuklukla birlikte oluşan kardiyak arrestin başlıca özelliği, ölümlerin büyük çoğunluğunun enjeksiyon sırasında ya da 5-10 dakika sonra meydana gelmesidir. Bununla birlikte nadiren meydana gelen gecikmiş intolerans reaksiyonları, uygulamadan günler sonra bildirilmiştir.Literatürde, hipotansif kolaps ve şoku içeren izole raporlar bulunmuştur. Klinik literatürlere dayanılarak konvansiyonel kontrast madde kullanımından dolayı bildirilen ölümlerin dağılımı; 1 milyonda 6,6'dan ( %0,00066 ) 10.000'de 1'e ( % 0.01 ) değişmektedir. Sıcaklık hissi gibi rahatsızlık reaksiyonları çok yaygındır ( % 10 - 50 ). Bunlar, dozajdan, kullanılan konsantrasyondan ve enjeksiyon yerinden bağımsızdır. Ağrı hisleri de yaygın olarak gözlenmiştir.
Allerji öyküsü olan hastalarda kontrast madde ile bildirilmiş advers reaksiyon insidansı, genel popülasyonun iki katıdır; kontrast maddeye karşı önceden reaksiyon öyküsü olan hastalarda, diğer hastalara kıyasla üç kat daha fazladır.Bununla birlikte kontrast maddeye karşı hassasiyet, tekrarlanan uygulamalarla artan bir şekilde ortaya çıkmaz.
Advers reaksiyonlar şu şekilde sınıflandırılabilir:
-Aşırı duyarlılık ya da anaflaktoid reaksiyonlar: Çoğunlukla hafif ya da orta derecelidir ve kaşıntı, deri döküntüleri, ürtiker ve rinit gibi belirtilerle seyreder. Bu belirtiler uygulanan dozdan ve uygulama yerinden bağımsız olarak oluşabilir ve kan basıncı düşüşü, taşikardi, dispne, solgunluk, şuurda azalma olarak tarif edilen semptomlarla birlikte seyreden bir şok gelişiminin ilk işaretleri olabilir. Fatal olgular rapor edilmiştir.
-Vazovagal reaksiyonlar: Sersemlik hissi ve hipotansiyondan senkopa kadar çeşitlilik gösteren, kontrast madde ya da röntgen prosedürünün kendisi ile ilişkilendirilen vazovagal reaksiyonlar.
-Kardiyolojik yan etkiler:Kardiyolojik kateterizasyon sırasında oluşan, EKG değişimleri, aritmi, koroner spazmla birlikte ileti sistemi bozukluklarını kapsayabilen kardiyolojik yan etkiler.Kontrast madde ya da röntgen prosedürünün kendisi ile ilişkilendirilen bu gibi kardiyolojik yan etkiler çok seyrek olarak bildirilmiştir.
-Nefrotoksik reaksiyonlar: Önceden mevcut böbrek hastalağı olan hastalarda, akut böbrek yetmezliğiyle seyreden nefrotoksik reaksiyonlar çok seyrektir. ( metformin ile etkileşim bilgileri için bkz. Bölüm 4.5 ).
-Sinir sistemi bozuklukları: Kontrast maddenin intra-arteriyel enjeksiyonu sonrasında oluşabilen, konfüzyon, görme bozuklukları, konvülsiyon ya da kriz gibi sinir sistemi bozuklukları. Bu belirtiler genellikle geçicidir ve birkaç saat içinde kendiliğinden azalır.
-Lokal reaksiyonlar: Enjeksiyon yerinde çok nadiren deri döküntüsü, şişme, enflamasyon ve ödem gibi lokal reaksiyonlar oluşabilir. Bu gibi reaksiyonlar, birçok olguda muhtemelen kontrast maddenin ekstravazasyonu nedeniyle oluşur. Uzatılmış paravazasyon, cerrahi tedavi gerektirebilir.
Aşağıdaki advers reaksiyonlar, klinik çalışmalarda Optiray uygulaması sonrasında ve
pazarlama sonrası dönemde bildirilmiştir. Sıklıklar, kontrollü çalışmalarda bildirildiği
gibi, aşağıdaki şekilde tanımlanmaktadır:
Çok yaygın ( > 1/10 )
Yaygın ( > 1/100 ila < 1/10 )
Yaygın olmayan ( > 1/1.000 ila < 1/100 )
Seyrek ( > 1/10.000 ila < 1/1.000 )
Çok seyrek ( < 1/10.000 )
Bilinmiyor ( eldeki verilerden hareketle tahmin edilemiyor ).
Psikiyatrik bozukluklar
Çok seyrek: Amnezi ; anksiyete; somnolans
Sinir sistemi bozuklukları
Seyrek: Sersemlik; tremor; parestezi
Çok seyrek: Ajitasyon; konfüzyonel durum; bilinç kaybı; dezoryantasyon; diskinezi; disfazi; hipoestezi; kas krampları; paraliz; konuşma bozuklukları; uyuşukluk
Göz hastalıkları
Çok seyrek: Konjunktivit ( göz iritasyonu, oküler hiperemi, gözlerde sulanma ve konjunktiva şişmesini de içeren); geçici körlük görme bozuklukları
Kulak ve labirent bozuklukları
Çok seyrek: Tinitus
Kardiak bozukluklar
Seyrek: Taşikardi
Çok seyrek: Palpitasyon; aritmi; atrial fibrilasyon; bradikardi; kardiyak arrest; dolaşım bozuklukları; EKG değişiklikleri; ekstrasistol; kalp bloğu; ventriküler fibrilasyon;
Vasküler bozukluklar
Seyrek: Hipotansiyon
Çok seyrek: Serebrovasküler bozukluklar; siyanoz; hipertansiyon; senkop; flebit; v azodilatasyon; vazospazm; kan basıncı dalgalanması
Solunum sistemi, toraks ve mediastin hastalıkları
Seyrek: Larengeal spazm; ödem ve obstrüksiyon ( boğazda daralma ve stridoru da içeren ); dispne; rinit ( hapşırma ve nazal konjestiyonu da içeren ); boğaz iritasyonu; öksürük
Çok seyrek: Apne; bronkospazm; hipoksi; larengeal ödem; farenjit; pulmoner ödem;
Gastrointestinal bozukluklar
Yaygın olmayan: Bulantı; kusma
Seyrek:Tat alma bozukluğu; ağız kuruluğu
Çok seyrek:Sialoadenit; hiperasalivasyon; dilde ödem; disfaji; diyare;
Deri ve deri altı doku bozuklukları
Yaygın olmayan: Ürtiker
Seyrek:Eritem; prurit; döküntü
Çok seyrek:Anjiyoödem; toksik epidermal nekroliz
Kas-iskelet, bağ dokusu ve kemik bozuklujları
Çok seyrek: Kas spazmları; miyalji
Böbrek ve üriner bozukluklar
Seyrek: Miktürisyon aciliyeti
Çok seyrek: İnkontinans; akut böbrek yetmezliği; anormal böbrek fonksiyonu; BUN artışı; oligüri; hematüri; kreatinin klerensinde azalma; nefropati
Genel bozukluklar ve uygulama yeri reaksiyonları
Çok yaygın: Sıcaklık hissi Yaygın: Ağrı
Seyrek: Farenjial ödem; ürperme (titreyerek ürperme ve soğukluk hissini de içeren ); baş ağrısı
Çok seyrek: Anaflaktik şok; yüz ödemi; periorbital ödem; ateş; ödem; solgunluk; göğüs ağrısı; abdominal ağrı; enjeksiyon yeri reaksiyonları ( özellikle ekstravazasyon sonrası ağrı, eritem ve hemorajiden, nekroza kadar belirtileri içeren, vasküler tramva ); astenik koşullar ( kırıklık, yorgunluk ve gevşemeyi de içeren ); anormal hissetme; terleme artışı
Optiray'in koroner arteriyografi ve ventrikülografi için kullanıldığı çift kör klinik çalışmalarda, ioversol enjeksiyonu ile oluşan elektrokardiyografik ve hemodinamik değişiklikler, diatrizoat meglumin ve diatrizoat sodyum'a kıyasla daha az sıklıkta ve daha az ciddiyette meydana gelmiştir. Koroner arter ve sol ventrikül ejeksiyonu sonrasında bradikardi, taşikardi, T dalgası amplitüdü, ST segment depresyonu, ST segment elevasyonu gibi elektrokardiyografik parametreler, diatrizoat meglumin ve diatrizoat sodyumla karşılaştırıldığında Optiray ile daha az etkilenmiştir. Aynı zamanda diğer konvansiyonel iyonik maddelere kıyasla Opiray'in kardiyak fonksiyonlar ve sistemik kan basıncında daha az değişikliğe yol açtığı gösterilmiştir. Bu değişiklikler; kalp debisi, sol ventriküler sistolik ve son diyastolik basınç, sağ ventriküler sistolik ve pulmoner arter sistolik basıncı, sistolik ve diyastolik kan basıncında azalmayı içerir.
Optiray için bildirilmiş bu advers reaksiyonlara ek olarak, diğer kontrast ajanların kullanımı ile bildirilmiş advers reaksiyonlar ( ve herhangi bir suda çözünen iyotlu kontrast ajan ile de oluşması muhtemel ) şu şekilde sıralanmıştır; geçici veya daha az sıklıkta kalıcı görsel alan kayıpları, dissemine intravasküler koagülasyon.
Diğer reaksiyonlar, uygulama hatalarının sonucu olarak herhangi bir kontrast ajan kullanımı ile de oluşabilir. Bu reaksiyonlar; enjeksiyon yerinde hemoraji ya da psödoanevrizma, aksiller arter enjeksiyonu sonrasında brakiyal sinir felci, göğüs ağrısı, miyokard enfarktüsü ve hepatorenal kimya testlerindeki geçici değişiklikler şeklinde olabilir. Arteriyel tromboz, arteriyel plakların displasmanı, venöz tromboz, koroner damarların disseksiyonu ve geçici sinüs arresti, seyrek görülen komplikasyonlardır.
4.9. Doz aşımı:
Tüm iyotlu röntgen kontrast maddelerinde olduğu gibi, Optiray'da da aşırı doz potansiyel olarak ölümcüldür ve solunum sistemiyle kardiyovasküler sistemi etkileyebilir. Tedavi semptomatik olmalıdır. Optiray'ı kandan temizlemek için diyaliz yapılabilir.
5. FARMAKOLOJİK ÖZELLİKLERİ
5.1.Farmakodinamik özellikleri
Farmakoterapötik Grup: Suda çözünen, nefrotropik, düşük ozmolar röntgen kontrast maddesi
ATC kodu: V08AB07
Optiray 320, non-iyonik bir röntgen kontrast maddesidir. Optiray'ın intravasküler enjeksiyonu, kontrast maddenin akış yolundaki damarları opasifiye ederek anlamlı hemodilüsyon oluşuncaya kadar iç yapıların radyografik yolla görülebilmesini sağlar.
5.2.Farmakokinetik özellikler Genel özellikler
Emilim
İntravenöz kullanım nedeniyle gastrointestinal yolla emilim söz konusu değildir. Dağılım
Optiray'ın farmakokinetik profili, hidrofilik özellikleri ve serum ve plazma proteinlerine çok düşük düzeyde bağlanmasıyla birlikte, Optiray'ın ekstraselüler sıvı boşluğunda dağıldığını göstermektedir. 50 ml'lik bir Optiray 320 dozu uygulanmasından sonra ortalama dağılım yarılanma ömrü (± SE)(serum) 15,5 ± 3,5 dakika olmuştur.
Biyotransformasyon
Optiray için anlamlı bir metabolizma, deiyodinasyon veya biyotransformasyon
görülmemiştir.
Eliminasyon
Optiray, böbreklerden glomerüler filtrasyon ile hızlı bir şekilde elimine olur. 50 ml'lik bir Optiray 320 dozu uygulanmasından sonra ortalama eliminasyon yarılanma ömrü (± SE)(serum) 2,06 ± 0,14 saat olarak bulunmuştur. Uygulanan dozun % 95'ten fazlası ilk 24 saat içinde atılır. Feçes yoluyla atılım ihmal edilebilir niteliktedir.
Hastalardaki karakteristik özellikler
Irk:
Bu konuda herhangi bir çalışma yapılmamıştır. Cinsiyet:
Bu konuda herhangi bir çalışma yapılmamıştır. Yaş etkileri:
Bu konuda herhangi bir çalışma yapılmamıştır. Böbrek yetmezliği:
Bu konuda herhangi bir çalışma yapılmamıştır.
5.3. Klinik öncesi güvenlilik verileri
Optiray'ın klinik öncesi testlerinde, izin verilen endikasyonlarda kullanıldığında bu ürünün güvenliğiyle ilgili olarak reçeteleyen açısından önem taşıyabilecek ve KÜB'ün diğer bölümlerine dahil edilmemiş herhangi bir bulgu elde edilmemiştir.
6. FARMASÖTİK ÖZELLİKLER 6.1. Yardımcı maddelerin listesi
Trometamin hidroklorür Trometamin
Sodyum Kalsiyum Edetat
Hidroklorik asit yada Sodyum hidroksit (pH 6,0'dan-7,4'e) Enjeksiyonluk su
6.2.Geçimsizlikler
Başka hiçbir tıbbi ürün Optiray ile karıştırılmamalıdır.
Geçimlilik çalışmaları yapılmamışsa, bu tıbbi ürün başka tıbbi ürünler ile karıştırılmamalıdır.
6.3.Raf ömrü
Raf ömrü: 3 yıl
6.4.Saklamaya yönelik özel tedbirler
Işıktan korumak için orijinal ambalajı içinde muhafaza ediniz. Gün ışığı ve röntgen ışınlarından koruyunuz. 25°C'nin altındaki oda sıcaklığında saklayınız. Soğutmayınız/dondurmayınız. Optiray bir ay boyunca, hava dolaşımlı bir kontrast madde ısıtıcısında 37°C'de saklanabilir.
6.5.Ambalajın niteliği ve içeriği
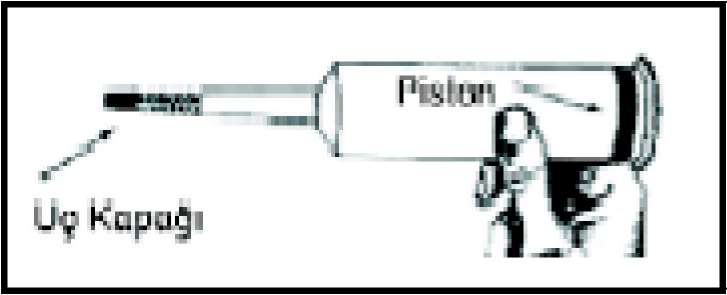
Optiray 320 steril enjektabl solüsyon/Şırıngada (100 ml), polipropilenden yapılmış power enjektör şırıngalarında sunulmaktadır. Şırınganın uç kapağı ve pistonu doğal kauçuktan yapılmıştır. Piston latekse allerjisi olan kullanıcıları korumak amacıyla, lastik bileşenleriyle doğrudan teması önleyecek şekilde teflonla kaplanmıştır. - Optiray 320 steril enjektabl kullanıma hazır şırınga, aşağıdaki ambalaj boyutlarında sunulmaktadır:
Kullanıma Hazır Power Enjektör Şırıngaları:1 x 100 ml
Tüm paket büyüklükleri satılmayabilir.
6.6.Tıbbi üründen arta kalan maddelerin imhası ve diğer özel önlemler
İlaç çözeltisi, içinde parçacıklar varsa veya bir renk bozukluğu görülüyorsa, kullanılmamalıdır. Çözeltide kristaller görülüyorsa, ambalajda bir hasar olup olmadığına bakılmalıdır. Ambalajda hasar yoksa, kristaller ilacın oda ısısına getirilmesiyle ve kuvvetle sallanarak çözülebilir.
Optiray tek dozluk ünitelerde sunulur. Yapılan incelemeden sonra kontrast maddenin kalan kısmı atılmalıdır. Kullanılmamış olan ürünler ya da atık materyaller "Tıbbi Atıkların Kontrolü Yönetmeliği" ve "Ambalaj Atıklarının Kontrolü Yönetmelik"'lerine uygun olarak imha edilmelidir.
Aşağıda şırıngalarla ilgili kullanım talimatı yer almaktadır.
OPTİRAYtm
NOT: Şırınganın dışı steril değildir. Şırınganın içindekiler, mavi uç kapağı ve piston çubuklarının altındaki alan sterildir, ve buna göre davranılmalıdır.
Mavi uç kapağının şırıngadan çıkarmak için bastırın ve çevirerek çıkartın, sonra da atın. Kapağın altındaki alan sterildir. Temas ederken artık dikkatli olunmalıdır.
Kullandıktan sonra şırıngayı ve içindeki kontrast maddenin artan kısmını atın.
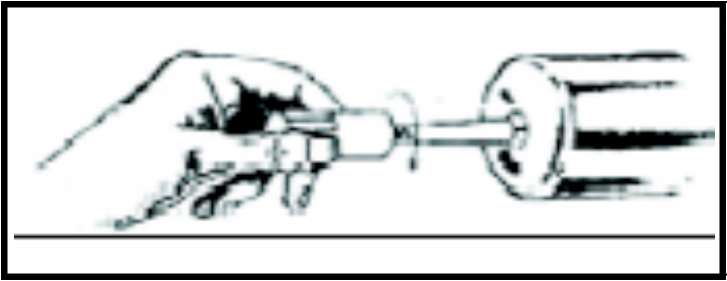
Şırıngayı tabladan çıkarın ve uç kapağının altındaki alanla pistonun dışını sızıntı izlerine karşı kontrol edin. Sızıntı görürseniz kullanmayın. Şırıngayı basınç silindirinin içine doğru yükleyin.
|
Mavi uç kapağının şırıngadan çıkarmak için bastırın ve çevirerek çıkartın, sonra da atın. Kapağın altındaki alan sterildir. Temas ederken artık dikkatli olunmalıdır.
|
|
|
Toz kapağını tutup sonuna kadar çevirip sıkıştırarak, luer kilit somununu şırıngaya takın. Steril bağlantı tübünü takmaya hazır olunca toz kapağını çıkartıp atın.
|
|
7.RUHSAT SAHİBİ
Covidien Sağlık A.Ş
Maslak Mah. Bilim Sok. Sun Plaza No:5 34398 Şişli-İSTANBUL TÜRKİYE
8.RUHSAT NUMARASI
126/83
9.İLK RUHSAT TARİHİ/RUHSAT YENİLEME TARİHİ
İlk ruhsatlandırma tarihi: 13 Şubat 2009
10.KÜB'ÜN YENİLENME TARİHİ
KÜB onay tarihi:
|
İlaç Bilgileri
Optiray 320 steril enjektabl solüsyon içeren kullanıma hazır şırıngaEtken Maddesi: İoversol Atc Kodu: V08AB07
Pdf olarak göster
|